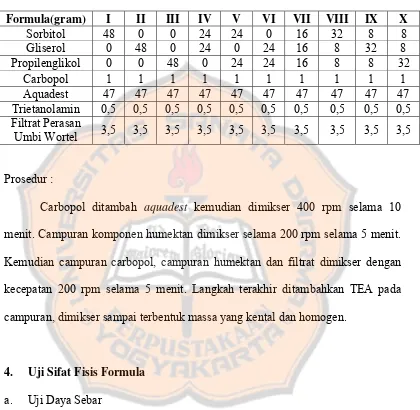
Optimasi formula sediaan gel uv protection filtrat perasan umbi wortel [Daucus carota, Linn.] : tinjauan terhadap sorbitol, gliserol, dan propilenglikol - USD Repository
Teks penuh
Gambar



Dokumen terkait
Teori pengambilan keputusan yang umum seperti itu dimulai dengan pemikiran mengenai tindakan (aksi) yang terbuka bagi individu-individu; hasil
Sampel yang telah digiling di analisa menggunakan analisis proksimat meliputi kuantifikasi nutrisi seperti air, abu, serat kasar, protein kasar, lemak, dan bahan ekstrak
kolaborasi dengan tim kesehatan lain, merencanakan asuhan, melaksanakan asuhan yang telah direncanakan, mengevaluasi asuhan dan mendokumentasikan dengan metode SOAP
Dari hasil tabel temuan studi diatas dapat diketahui penyebab ketidakefektifan Dinas Tata Kota (DTK) Kota Cimahi didalam melakukan pengendalian pemanfaatan ruang yaitu
Caput nyamuk Anopheles betina (kiri) memperlihatkan antena tipe pilose (A) dan sepasang palpus maksilaris (C) yang hampir sama panjang dengan probosis, dan Anopheles jantan
RTH privat adalah RTH milik institusi tertentu atau orang perseorangan yang pemanfaatannya untuk kalangan terbatas antara lain berupa kebun atau halaman
Di lain hal, pemasaran ikan teri nasi kering untuk dalam provinsi masih sangat sulit karena harga jual produk yang cukup tinggi sehingga dapat menjadi ancaman bagi
Beberapa pokok kebijakan ekonomi makro yang akan dilaksanakan dalam tahun 2005 mencakup; ( i ) memaksimalkan implementasi Instruksi Presiden Nomor 5 Tahun 2003 tentang Paket