Laporan Praktikum Kimia Organik Identifikasi Senyawa
Hidrokarbon
LAPORAN PRAKTIKUM KIMIA ORGANIK
PERCOBAAN IV
IDENTIFIKASI SENYAWA HIDROKARBON DAN
SENYAWA ORGANIK JENUH DAN TIDAK JENUH
A. Judul
Identifikasi senyawa hidrokarbon senyawa organic jenuh dan tidak jenuh B. Tujuan
1. Mengetahui kelarutan dari hidrokarbon alifatis dan aromatis 2. Mengamati dengan seksama perubahan reaksi yang terjadi C. Dasar Teori
Senyawa hidrokarbon merupakan senyawa karbon yang paling sederhana. Dari namanya, senyawa hidrokarbon adalah senyawa karbon yang hanya tersusun dari atom hidrogen dan atom karbon. Dalam kehidupan sehari-hari banyak kita temui senyawa hidrokarbon, misalnya minyak tanah, bensin, gas alam, plastik dan lain-lain.
Sampai saat ini telah dikenal lebih dari 2 juta senyawa hidrokarbon. Untuk mempermudah mempelajari senyawa hidrokarbon yang begitu banyak, para ahli mengolongkan hidrokarbon berdasarkan susunan atom-atom karbon dalam molekulnya. Berdasarkan susunan atom karbon dalam molekulnya, senyawa karbon terbagi dalam 2 golongan besar, yaitu senyawa alifatik dan senyawa siklik. Senyawa hidrokarbon alifatik adalah senyawa karbon yang rantai C nya terbuka dan rantai C itu memungkinkan bercabang. Berdasarkan jumlah ikatannya, senyawa hidrokarbon alifatik terbagi menjadi senyawa alifatik jenuh dan tidak jenuh.
- Senyawa alifatik jenuh adalah senyawa alifatik yang rantai C nya hanya berisi ikatan-ikatan tunggal saja. Golongan ini dinamakan alkana.
Contoh senyawa hidrokarbon alifatik jenuh:
- Senyawa alifatik tak jenuh adalah senyawa alifatik yang rantai C nya terdapat ikatan rangkap dua atau rangkap tiga. Jika memiliki rangkap dua dinamakan alkena dan memiliki rangkap tiga dinamakan alkuna. Contoh senyawa hidrokarbon alifatik tak jenuh:
- Senyawa hidrokarbon siklik adalah senyawa karbon yang rantai C nya melingkar dan lingkaran itu mungkin juga mengikat rantai samping. Golongan ini terbagi lagi menjadi senyawa alisiklik dan aromatik.
• Senyawa aromatik yaitu senyawa karbon yang terdiri dari 6 atom C yang membentuk rantai benzena.
http://sahri.ohlog.com/senyawa-hidrokarbon.oh84970.html
Dalam bidang kimia, hidrokarbon adalah sebuah senyawa yang terdiri dari unsur karbon (C) dan hidrogen (H). Seluruh hidrokarbon memiliki rantai karbon dan atom-atom hidrogen yang berikatan dengan rantai tersebut. Istilah tersebut digunakan juga sebagai pengertian dari hidrokarbon alifatik.
Sebagai contoh, metana (gas rawa) adalah hidrokarbon dengan satu atom karbon dan empat atom hidrogen: CH4. Etana adalah hidrokarbon (lebih terperinci,
sebuah alkana) yang terdiri dari dua atom karbon bersatu dengan sebuah ikatan tunggal, masing-masing mengikat tiga atom karbon: C2H6. Propanamemiliki tiga atom
C (C3H8) dan seterusnya (CnH2·n+2).
http://id.wikipedia.org/wiki/Hidrokarbon
Klasifikasi / Penggolongan Hidrokarbon (terdiri dari atom C dan H)
a. Berdasarkan jenis ikatan antar atom
karbonnya :rokarbon jenuh = senyawa hidrokarbon yang ikatan antar atom
karbonnya merupakanikatan tunggal.
hidrokarbon tak jenuh = senyawa hidrokarbon yang memiliki 1 ikatan rangkap dua (alkena) atau lebih dari 1 ikatan
rangkap dua (alkadiena), atau ikatan rangkap tiga
(alkuna). b. Berdasarkan bentuk rantai karbonnya :
Hidrokarbon alifatik = senyawa hidrokarbon dengan rantai terbuka jenuh (ikatan tunggal)maupun tidak jenuh (ikatan
rangkap).
Hidrokarbon alisiklik = senyawa hidrokarbon dengan rantai melingkar /
tertutup (cincin). Hidrokarbon aromatik = senyawa hidrokarbon dengan rantai melingkar
(cincin) yang mempunyai ikatan antar atom C
tunggal danrangkap secara selang-seling /
Skema Klasifikasi Hidrokarbon
Uraian hidrokarbon alifatik jenuh dan tak jenuh : ALKANA
o Adalah hidrokarbon alifatik jenuh yaitu hidrokarbon dengan rantai terbuka dan semua ikatan antar atom karbonnya merupakan ikatan tunggal.
o Rumus umum alkana yaitu : CnH2n+2 ; n = jumlah atom C
ALKENA
o Adalah hidrokarbon alifatik tak jenuh yaitu hidrokarbon dengan satu ikatan rangkap dua (–C=C–). Senyawa yang mempunyai 2 ikatan rangkap 2 disebutalkadiena, yang mempunyai 3 ikatan rangkap 2 disebut alkatriena dst.
o Rumus umum alkena yaitu : CnH2n ; n = jumlah atom C
ALKUNA
o Adalah hidrokarbon alifatik tak jenuh yaitu hidrokarbon dengan satu ikatan rangkap tiga (–C≡C–). Senyawa yang mempunyai 2 ikatan rangkap 3 disebutalkadiuna, yang mempunyai 1 ikatan rangkap 2 dan 1 ikatan rangkap 3 disebut alkenuna.
o Rumus umum alkuna yaitu : CnH2n-2 ; n = jumlah atom C
Benzena merupakan sikloheksena yaitu senyawa siklik yang memiliki ikatan rangkap dua aromatik dengan rumus struktur C6H12. Benzena dilambangkan dalam
dua bentuk, yang pertama adalah struktur Kekulé dan yang lainnya adalah heksagon dengan lingkaran di dalamnya untuk menggambarkan adanya resonansi ikatan ʋ atau distribusi elektron yang tersebar merata didalam cincin benzena. Kedua struktur ini disederhanakan pada Gambar 12.70.
Gambar 12.70. Struktur Kekulé dan heksagonal benzena
Adanya ikatan rangkap dua pada senyawa sikloheksena ini menunjukkan bahwa benzena termasuk hidrokarbon tidak jenuh, namun pada umumnya benzena tidak berperilaku seperti senyawa tak jenuh.
http://www.chem-is-try.org/materi_kimia/kimia-kesehatan/senyawahidrokarbon/benzena/
D. Alat dan Bahan
a. Alat : 1. Tabung reaksi 2. Erlen meyer 3. Pipet tetes 4. Kapas
5. Gelas ukur 6. Pipet gondok b. Bahan : 1. Asam nitrat pekat HNO3
2. Benzena C6H6
4. Aquadest 5. Kristal iodium 6. Asam sulfat H2SO4 7. Parafin 8. Minyak kelapa E. Prosedur
Reaksi
Hasil
Hidrokarbon alifatis
1 ml asam sulfat + 1 ml paraffin cair
Larutan bening berpisah
Hidrokarbon alimatis
1 ml aquadest + 1 ml etanol + 1 ml benzena
Larutan kuning berawan diatas dan
bening dibawah
Sifat benzene sebagai pelarut
1 ml aquadest + 1 ml paraffin cair
1 ml aquadest + 1 ml minyak kelapa
1 ml aquadest + 1 ml kristal iodium
1 ml benzena + 1 ml paraffin cair
Tidak tercampur
2 lapisan kuning + bening
Larutan coklat
Bening bercampur
1 ml benzena + 1 ml minyak kelapa
1 ml benzena + 1 ml kristal iodium
Larutan ungu
Nitrasi Benzen
1 ml asam sulfat + 3 ml asam nitrat pekat
+ 1 ml benzoat, amati + kan air 25 ml
Larutan bening tidak tercampur seperti
gumpalan minyak
Identifikasi
Prosedur
Hasil
Hidrokarbon
alifatis
(alkana)
H
2SO
4dan Parafin
2 lapisan, bening dan kuning
Hidrokarbon alimatis (benzene)
H
20 + Etanol + C
6H
62 lapisan, kuning dan bening
Sifat benzene sebagai
pelarut
- Aquadest + paraffin
- Aquadest + minyak kelapa
- Aquadest + kristal iodium
- Benzena + paraffin
- Benzena + minyak kelapa
- Benzena + kristal iodium
- 2 lapisan bening dan kuning
- 2 lapisan kuning dan bening
- Larutan kuning tak larut
- Bening tercampur
- Larutan kuning keruh
- Larutan ungu
Nitrasi
benzena
H
2SO
4+ HNO
3+ C
6H
6+ H
2O
Larutan tidak tercampur
G. Pembahasan
Pada percobaan praktikum ini mengidentifikasi senyawa hidrokarbon dan senyawa oragnik jenuh dan tak jenuh yang meliputi beberapa percobaan, diantaranya adalah :
1. Identifikasi hidrokarbon alifatis (alkana)
Percobaan ini mereaksikan antara 1 ml asam sulfat pekat dengan 1 ml paraffin cair, kemudian didapat larutan bening tidak tercampur dengan memisah 2 lapisan, dikarenakan kekentalan paraffin yang cukup tinggi dan bereaksi dengan asam.
2. Identifikasi hidrokarbon alimatis (benzene)
Percobaan ini mereaksikan 1 ml aquadest dengan 1 ml etanol kemudian direakiskan dengan 1 ml benzene, kemudian akan didapat hasil campuran reaksi yang terpisah dengan larutan kekuningan diatas dan terlapisi seperti bentuk awan dibawahnya dengan warna larutan bening.
3. Identifikasi senyawa benzene sebagai pelarut
a. 1 ml aquadest direaksikan dengan 1 ml paraffin cair dan menghasilkan warna larutan yang bening terpisah.
b. 1 ml aquadest direaksikan dengan 1 ml minyak kelapa dan menghasilkan larutan yang terpisah antara minyak dan air. Posisi minyak berada diatas dikarenakan kekentalan minyak yang sangat tinggi.
c. 1 ml aquadest direakiskan dengan kristal iodium dan akan menghasilkan warna lrutan coklat, itu dikarenakan warna iodium yang berwarna coklat.
d. 1 ml benzene direaksikan dengan 1 ml paraffin dan menghasilkan warna lrutan bening yang tercampur.
e. 1 ml benzene direaksikan dengan 1 ml minyak wijen dan akan menghasilkan larutan kuning keruh.
f. 1 ml benzene direakiskan dengan 1 ml kristal iodium dan akan menghasilkan warna larutan yang ungu.
4. Nitrasi benzene
Pada percobaan nitrasi ini, mereaksikan 1 ml asam sulfat dengan 3 ml asam nitrat pekat, kemudian diteteskan 1 ml benzene melalui dinding tabung reaksi, dan diamati perubahan warnanya, tetapi tidak terjadi perubahan warna, hanya ada sedikit gumpalan seperti minyak. Kemudian ditambahkan 25 ml aquadest dan menghasilkan larutan yang tetap berwarna bening dengan sedikit ada butiran minyak. Reaksi yang terjadi pada percobaan ini adalah sebagai berikut :
Percobaan diatas sama halnya seperti pada proses esterifikasi dengan menggunakan katalis asam, yaitu asam sulfat.
H. Simpulan
a. Hidrokarbon adalah sebuah senyawa yang terdiri dari unsur karbon (C) dan
hidrogen (H).
b. Hidrokarbon berdasarkan jenis ikatan antar atom karbonnya : Hidrokarbon jenuh
Hidrokarbon tak jenuh
c. Hidrokarbon berdasarkan bentuk rantai karbonnya : Hidrokarbon alifatik
Hidrokarbon alisiklik
Hidrokarbon aromatik d. Alkana termasuk hidrokarbon jenuh Alkena termasuk hidrokarbon tak jenuh Alkuna termasuk hidrokarbon tak jenuh
e. Benzena merupakan sikloheksena yaitu senyawa siklik yang memiliki ikatan
I. Daftar Pustaka http://sahri.ohlog.com/senyawa-hidrokarbon.oh84970.html Akses 12/04/11 21:15 WIB http://id.wikipedia.org/wiki/Hidrokarbon Akses 12/04/11 21:22 WIB http://www.chemistry.org/materi_kimia/kimiakesehatan/senyawahidrokarbon/benzena/ Akses 12/04/11 21:24 WIB
IDENTIFIKASI SENYAWA HIDROKARBON DAN SENYAWA ORGANIK
JENUH DAN TIDAK JENUH
PENDAHULUAN
1.1. Latar Belakang
Perbedaan antara senyawa karbon dan hidrokarbon yaitu, untuk senyawa karbon yaitu senyawa yang tidak hanya mengandung unsur C dan H, tetapi juga unsur lain seperti O, N, S, P atau halogen contohnya pada senyawa karbon yaitu alkanol, alkoksi alkana, alkanal, alkanon, alkanoat dan alkil alkanoat. sedangkan senyawa hidrokarbon yaitu senyawa yang mengandung hanya C dan H saja contohnya alkana, alkena dan alkuna.(April, 2002)
Sumber hidrokarbon utama di alam adalah minyak bumi. Minyak bumi digunakan secara luas sebagai bahan bakar dan sebagai bahan baku industri petrokimia. Minyak bumi terbentuk dari penguraian senyawa-senyawa organic yang berasal dari jasad organisme yang hidup jutaan tahun yang lalu, yang tertimbun di tanah baik di daratan ataupun di daerah lepas pantai. Pengaruh besarnya tekanan dan suhu tinggi menyebabkan terjadinya penguraian endapan fosil hewan/tumbuhan menjadi endapan minyak bumi dan gas. Pada umumnya minyak bumi terperangkap dalam bebatuan tidak berpori. Oleh karena itu minyak bumi disebut bahan bakar fosil dan disebut juga petroleum (dari bahasa Latin ‘petrus’ yang berarti batu dan ‘oleum’ yang berarti minyak). Minyak bumi merupakan sumber daya alam yang tidak dapat diperbarui. Minyak bumi mengandung bermacam-macam alkana yang berbeda jumlah atom C-nya. Minyak bumi ditemukan bersama-sama dengan gas alam. Gas alam merupakan campuran alkana. Komposisi gas alam tergantung sumbernya, umumnya mengandung 80% metana, 7% etana, 6% propane, 4% butane dan isobutana serta 3% pentane. Propana dan
butane dicairkan dengan tekanan tertentu dan dikenal sebagai Liquefied Petroleum Gas
(LPG). Minyak bumi yang telah dipisahkan dari gas alam disebut minyak mentah (crude
oil). Minyak bumi biasanya berada 3 – 4 km di bawah permukaan, untuk memperolehnya
dilakukan pengeboran, di darat dan di lepas pantai. Pengeboran lepas pantai dapat dilakukan dengan cara menanam pipa di dasar laut dan memompa ke daratan jika jarak
ladang minyak ke darat cukup dekat, atau dengan membuat anjungan di lepas pantai, selanjutnya minyak dibawa oleh kapal tanker ke kilang minyak (refinery) di daratan. Minyak mentah berbentuk cairan kental hitam. Minyak mentah belum dapat digunakan sebagai bahan bakar, tetapi harus diolah terlebih dahulu. Melalui distilasi bertingkat itulah minyak mentah dipisahkan berdasarkan titik didih yang mirip, menjadi fraksi-fraksi. (Andi, 2007).
Manfaat hidrokarbon dalam kehidupan sehari-hari misalnya BBM seperti bensin, LPG, aptur, minyak pelumas non BBM antara lain poly propylen (biji plastik), aspal untuk jalan.selain itu manfaat senyawa Hidrokarbon di Berbagai Bidang Kehidupan di antaranya dalam bidang pangan maka yang dimanfaatkan bukan merupakan senyawa hidrokarbon murni, tetapi sedikit lebih luas yaitu karbohidrat. Karbohidrat merupakan senyawa karbon, hidrogen dan oksigen yang terdapat dalam alam. Banyak karbohidrat mempunyai rumus empiris CH2O Banyak karbohidrat yang merupakan polimer yang tersusun dari molekul gula yang terangkai menjadi rantai yang panjang serta bercabang-cabang karbohidrat merupakan bahan makanan penting dan sumber tenaga yang terdapat dalam tumbuhan dan daging hewan. Selain itu, karbohidrat juga menjadi komponen struktur penting pada makhluk hidup dalam bentuk serat (fiber), seperti selulosa, pektin, serta lignin. Karbohidrat menyediakan kebutuhan dasar yang diperlukan tubuh. Selain itu juga manfaat hidrokarbon dalam bidang sandang dari bahan hidrokarbon yang bisa dimanfaatkan untuk sandang adalah PTA (Purified Terephthalic Acid) yang dibuat dari para-xylene dimana bahan dasarnya adalah kerosin (minyak tanah). Dari Kerosin ini semua bahannya dibentuk menjadi senyawa aromatik, yaitu para-xylene Para-para-xylene ini kemudian dioksidasi menggunakan udara menjadi PTA. Dari PTA yang berbentuk seperti tepung detergen ini kemudian direaksikan dengan metanol menjadi serat poliester. Serat poliester inilah yang menjadi benang sintetis yang bentuknya seperti benang (Fadholi, 2009).
1.2. Tujuan
Adapun tujuan dari praktikum tentang identifikasi senyawa hidrokarbon dan senyawa organik jenuh dan tidak jenuh yaitu :
a. Mengetahui kelarutan dari hidrokarbon alifatis dan aromatis
b. Mengetahui perubahan reaksi yang terjadi
2.1. Senyawa Hidrokarbon
Hidrokarbon adalah sebuah senyawa yang terdiri dari unsur atom karbon (C) dan atom hidrogen (H). Seluruh hidrokarbon memiliki rantai karbon dan atom-atom hidrogen yang berikatan dengan rantai tersebut. Istilah tersebut digunakan juga sebagai pengertian dari hidrokarbon alifatik. Sebagai contoh, metana (gas rawa) adalah hidrokarbon dengan satu atom karbon dan empat atom hidrogen: CH4. Etana adalah
hidrokarbon (lebih terperinci, sebuah alkana) yang terdiri dari dua atom karbon bersatu dengan sebuah ikatan tunggal, masing-masing mengikat tiga atom karbon: C2H6. Propana memiliki tiga atom C (C3H8) dan seterusnya (CnH2·n+2). ( Nurul, 2009)
2.2. Penggolongan Senyawa Hidrokarbon
Hidrokarbon terdiri dari hidrogen dan karbon. Hidrokarbon ini dapat diklasifikasi atau digolongkan untuk mempermudah dalam pengenalannya. Penggolongan pertama berdasarkan jenis ikatan antar atom karbonnya yaitu , Hidrokarbon jenuh yaitu senyawa hidrokarbon yang ikatan antar atom karbonnya merupakan ikatan tunggal. dan hidrokarbon tak jenuh, ini yaitu senyawa hidrokarbon yang memiliki 1 ikatan rangkap dua (alkena) atau lebih dari 1 ikatan rangkap dua atau ikatan rangkap tiga (alkuna). Sedangkan Penggolongan kedua berdasarkan bentuk rantai karbonnya yaitu hidrokarbon alifatik (senyawa hidrokarbon dengan rantai terbuka jenuh /ikatan tunggal maupun tidak jenuh / ikatan rangkap), hidrokarbon alisiklik (senyawa hidrokarbon dengan rantai melingkar atau tertutup /cincin ), dan hidrokarbon aromatik (senyawa hidrokarbon dengan rantai melingkar /cincin yang mempunyai ikatan antar atom C tunggal dan rangkap secara selang-seling / bergantian ). ( Miranda, 2002)
2.3. Sifat Senyawa Hidrokarbon
Adapun sifat-sifat senyawa hidrokarbon dalam alkana yaitu Pada suhu C1–C4 berwujud gas, C5–C17 berwujud cair, dan di atas 17 berwujud padat, Semakin bertambah jumlah atom C maka Mr ikut bertambah akibatnya titik didih dan titik leleh semakin tinggi. Alkana rantai lurus mempunyai titik didih lebih tinggi dibanding alkana rantai bercabang dengan jumlah atom C sama. Semakin banyak cabang, titik didih makin rendah, alkana mudah larut dalam pelarut organik tetapi sukar larut dalam air dan senyawa alkana mumpunyai rantai panjang dapat mengalami reaksi eliminasi an alkana juga dapat bereaksi subsitusi dengan halogen. dan sifa-sifat alkena yaitu Titik didih alkena mirip dengan alkana, makin bertambah jumlah atom C, harga Mr makin besar maka titik didihnya makin tinggi. Alkena mudah larut dalam pelarut organik tetapi sukar larut dalam air. Alkena dapat bereaksi adisi dengan H2 dan halogen (X2 = F2, Cl2, Br2, I2). Adisi alkena dengan H2. contoh: CH2=CH2 + H2 → CH3–CH3. Sedangkan untuk sifat-sifat alkuna yaitu titik didih alkuna mirip dengan alkuna dan alkena semakin bertambah jumlah atom C harga M, makin besar maka titik didihnya makin tinggi.alkuna juga dapat beraksi adisi dengan H2, halogen dan asam halida. (Nurul, 2009).
III. BAHAN DAN METODE
3.1. Waktu dan Tempat
Praktikum kimia dasar ini dilaksanakan pada hari Senin Tanggal 22 April 2013, pukul 15.00 – 16.40 WIB dan kegiatan ini dilaksanakan di Laboratorium Jurusan Budidaya Pertanian, Fakultas Pertanian, Universitas Palangka Raya.
3.2. Alat dan Bahan
Adapun alat yang digunakan pada praktikum identifikasi senyawa hidrokarbon dan senyawa organik jenuh dan tidak jenuh yaitu tabung reaksi, erlenmayer, pipet tetes, pipet volume, gelas ukur, dan pipet gondok sedangkan bahan yang digunakan yaitu benzena, asam nitrat, etanol, aquades, kristal iosium, asam sulfat parafin dan minyak kelapa.
3.3. Cara Kerja
Adapun cara kerja pada praktikum ini tentang identifikasi senyawa hidrokarbon dan senyawa organik jenuh dan tidak jenuh yaitu :
3.3.1. Hidrokarbon Alifatis (alkana)
- Memasukan 1 ml asam sulfat pekat kedalam tabung reaksi
- Menambahkan 1 ml alkana (parafin cair)
- Mengocok hingga berubah warna
- Mengulangi percobaan sekali lagi
- Mencatat hasil akhir yang di dapatkan
3.3.2. Hidrokarbon Aromatis (Benzena)
- Menyediakan 2 tabung reaksi dan masing-masing tabung mengisi dengan 1
ml aquades.
- Menambahkan 1 ml etanol pada tiap-tiap tabung kemudian menetesi dengan benzena
pada masing-masing tabung sebanyak 1 ml secara perlahan-lahan. - Mengamati perubahan yang terjadi
- Mengulangi percobaan sekali lagi
3.3.3. Sifat Benzena Sebagai Pelarut
- Menyediakan 6 tabung reaksi, 3 tabung masing-masing diisi dengan 1 ml aquades dan 3
tabung yang lain yakni 4, 5 dan 6 masing-masing mengisi dengan 1 ml benzena.
- Pada tabung 1, 2 dan 3 yang berisi aquades menambahkan 1 ml parafin pada tabung 1, 1
ml minyak kelapa pada tabung 2 dan 1 gram kristal iodium pada tabung 3 - Mengulangi perlakuan di atas terhadap tabung 4, 5 dan 6 yang berisi benzena
- Mengamati semua perubahan yang terjadi
- Mencatat semua perubahan yang terjadi
3.3.4. Nutrisi Benzena
- Menyediakan 1 tabung reaksi kemudian mengisi dengan 1 ml asam sulfat pekat
- Kemudian menambahakan dengan 3 ml asam nitrat pekat secara perlahan-lahan
(melakukan prosedur ini pada ruang asam)
- Menetesi dengan 1 ml benzena (mengamati perubahan yang terjadi)
- Lalu menuangkan 25 ml aquades secara perlahan-lahan (melakukan di ruang asam),
mengamati perubahan yang terjadi - Mengulangi percobaan sekali lagi
- Mencatat semua perubahan yang terjadi.
IV. HASIL DAN PEMBAHASAN
4.1. Hasil Pengamatan
Dari hasil pengamatan kami dilaboratorium tentang identifikasi senyawa hidrokarbon dan senyawa organik jenuh dan tidak jenuh dilaboratorium Jurusan Budidaya Pertanian, Fakultas Pertanian, Unuiversitas Palangka Raya di sajikan pada tabel 1, 2, 3 dan 4 di bawah ini.
Tabel 1. Hasil pengamatan hidrokarbon alifatis (alkana)
No
Bahan mula-mula Bahan yang ditambahkan
Hasil Perlakuan
Nama Warna jumlah Nama Warna Jumlah
1 Asam sulfat Bening 1 ml Parafin Bening 1 ml Bening dan
kental
Digojok
Tabel 2. Hasil pengamatan aromatik
No
Bahan mula-mula Bahan yang ditambahkan
Hasil perlakuan
Nama Warna jumlah Nama Warna Jumlah
1 Aquades Bening 1 ml Etanol
benzena Bening Bening 1 ml 1 ml Terjadi 2 lapisan Tidak ada perlakuan
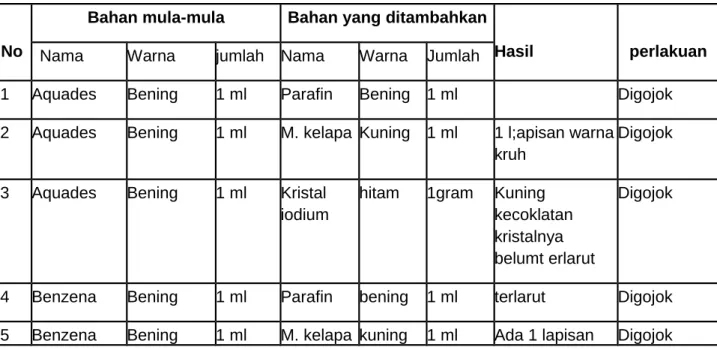
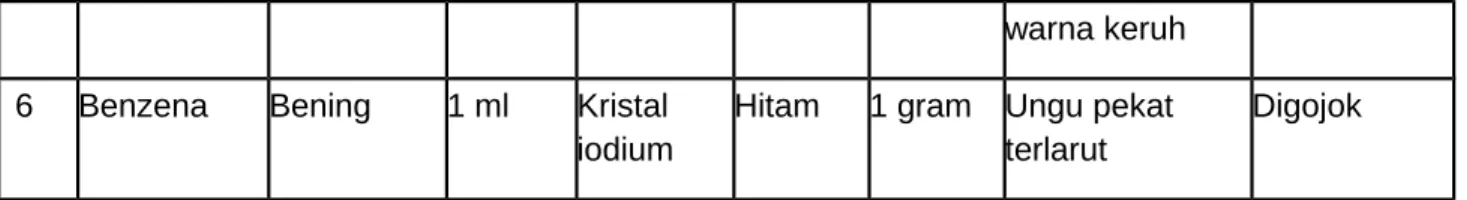
Tabel 3. Hasil pengamatan sifat benzena sebagai pelarut
No
Bahan mula-mula Bahan yang ditambahkan
Hasil perlakuan
Nama Warna jumlah Nama Warna Jumlah
1 Aquades Bening 1 ml Parafin Bening 1 ml Digojok
2 Aquades Bening 1 ml M. kelapa Kuning 1 ml 1 l;apisan warna
kruh
Digojok
3 Aquades Bening 1 ml Kristal
iodium
hitam 1gram Kuning
kecoklatan kristalnya belumt erlarut
Digojok
4 Benzena Bening 1 ml Parafin bening 1 ml terlarut Digojok
warna keruh
6 Benzena Bening 1 ml Kristal
iodium
Hitam 1 gram Ungu pekat
terlarut
Digojok
Tabel 4. Hasil pengamatan nitrasi benzena
No
Bahan mula-mula Bahan yang ditambahkan
Hasil perlakuan
Nama Warna jumlah Nama Warna Jumlah
1 H2SO4 pekat Bening 1 ml Asam nitrat
benzena + aquades Bening 3 ml 2 ml 2 lapisan. kedua lapisan itu bening Tidak ada perlakuan
2 H2SO4 pekat bening 1 ml Asam nitrat
benzena + aquades
bening25 l
4.2. Pembahasan
Dari Pada percobaan kali ini yang akan dilakukan adalah percobaan tentang
pengamatan hidrokarbon alifatis (alkana) menggunakan asam sulfat (H2SO4). Pada reaksi
ini melibatkan campuran parafin. Berikut adalah penjelasan lebih lanjut tentang percobaan ini yaitu percobaan pertama bahan mula-mula menggunakan asam sulfat dan di campurkan parafin yang berwarna bening dengan jumlah 1 ml, kemudian dimasukkan ke dalam tabung reaksi. Adapun Tingkat keberhasilan yang didapatkan pada percobaan ini dapat dilihat pada hasil pengamatan yaitu sebelum di gojok campuran tersebut berwarna putih bening setelah digojok beberapa menit ternyata campuran tersebut mengalami perubahan warna yaitu bening dan kental.
Pada percobaan selanjutnya tentang pengamatan hidrokarbon aromatis (benzena) dengan menggunakan bahan utama aquades. Berikut akan dijelaskan lebih lanjut tentang percobaan ini yaitu percobaan pertama bahan mula-mula menggunakan aquades
sebanyak 1 ml, kemudian dimasukan kedalam gelas ukur dan ditambahkan etanol (C2H5OH) dan benzena (C6H6) kedalam gelas ukur tersebut. Adapun tingkat keberhasilan
yang didapatkan pada percobaan ini tentang hidrokarbon aromatis (benzena) dapat dilihat pada hasil pengamatan bahwa terjadi 2 lapisan berwarna keruh dalam beberapa menit setelah direaksikan dengan bahan-bahan tersebut tanpa ada perlakuan.
Pada percobaan ketiga ini yaitu tentang sifat benzena sebagai pelarut menggunakan bahan utama aquades dan benzena pada reaksi ini melibatkan campuran parafin, minyak kelapa dan kristal iodium. Berikut akan dijelaskan lebih lanjut tentang percobaan ini yaitu percobaan pertama bahan mula-mula menggunakan aquades berwarna bening sebanyak 1 ml dan campurkan dengan parafin berwarna bening sebanyak 1 ml yang dimasukan kedalam gelas ukur. Adapun tingkat keberhasilan yang didapatkan adalah keruh terdapat 2 lapisansetelah digojok. Pada perlakuan kedua menggunakan bahan utama aqudes sebanyk 1 ml dan campurkan dengan minyak kelapa berwarna kuning sebanyak 1 dan tingkat keberhasilan yang didapatkan adalah 1 lapisan berwarna keruh setelah digojok. Pada perlakuan ketiga menggunakan bahan utama aquades sebanyak 1 ml dan campurkan kristala iodium berwarna hitam sebanyak 1 gram dan tingkat keberhasilan yang didapatkan yaitu larutan berwarna kuning kecoklatan dan kristalnya belum terlarut setelah di gojok. Pada perlakuan keempat menggunakan bahan utama benzena berwarna bening sebanyak 1 ml dan campurkan dengan menggunakan parafin yang berwarna bening sebanyak 1 ml. Adapun tingkat keberhasilan yang dapatkan adalah larutannya terlarut seletalah digojok. Pada perlakuan kelima menggunakan bahan utama benzena yang dicampurkan dengan menggunakan minyak kelapa sebanyak 1 ml dan tingkat keberhasilan yang didapatkan adalah ada 1 lapisan berwarna keruh setelah digojok dan pada perlakuan keenam menggunakan bahan utama benzena yang dicampurkan dengan menggunakan bahan kristal iodium sebanyak 1 gram dengan tingkat keberhasilan yaitu terjadi perubahan warna yaitu warna ungu pekat terlarut setelah digojok.
Pada percobaan terakhir ini yaitu tentang nitrasi benzena menggunakan bahan
dasar asam sulfat (H2SO4) yang di reaksikan dengan menggunakan bahan asam nitrat
benzena dan ditambah aquades. Berikut akan dijelaskan lebih lanjut tentang percobaan ini tentang hasil pengamatan nitrasi benzena. Percobaan pertama bahan mula – mula menggunakan asam sulfat berwarna bening sebanyak 1 ml dan campurkan atau ditambahkan asam nitrat benzena sebanyak 3 ml dan aquades 2 ml ke dalam gelas ukur. Adapun tingkat keberhasilan yang didaptkan yaitu terdapat 2 lapisan, kedua lapisan tersebut berwarna bening tanpa ada perlakuan. Adapuan pada percobaan kedua menggunakan bahan utama asal sulfat sebanyak 1 ml dan campurkan asam nitrat benzena sebanyak 3 ml dan aquades 25 ml dan tingkat keberhasilan yang di dapatkan adalah lapisan atas berwarna putih kentl, dan lapisan bawah putih bening tanpa ada perlakuan.
KESIMPULAN
Hidrokarbon adalah sebuah senyawa yang terdiri dari unsur karbon (C) dan hidrogen ( H ). Alkana tergolong zat yang sukar bereaksi sehingga disebut parafin. Adapun Sifat Benzena yang tidak larut membentuk lapisan ke dua dengan cincin
berbentuk awan berwarna putih.Benzena juga sebagai pelarut hanya dapat melarutan
senyawa-senyawa polar. Dalam nitrasi benzena diketahui jika Benzena, asam sulfat dan
asam nitrat yang masing-masing tidak saling melarutkan, dapat larut pada pelarut polar (air).
DAFTAR PUSTAKA
April, 2002. Senyawa karbon dan hidrogen. http://senyawa-karbon-dan-hidrogen .wordpress.com.
Diakses padatanggal 25/04/2013/
Andi, 2007. Hidrokarbon di alam. http://hidrokarbon-di-alam-blogspot.com. Diakses pada tanggal
25/04/2013.
Fadholi,2009. Manfaat hidrokarbon. Erlangga.jakarta.
http://manfaat-hidrokarbon-dalam-kehidupan-sehari-hari.blogspot.com. Diakses pada tanggal 26/04/2013
Miranda, 2002. Definisi senyawa hidrokarbon. http://pengertian
-senyawa-hidrokarbon. wordprees.com . Diakses pada tanggal 25/04/2013
Nurul, 2009. Makalah senyawa. http://makalah-senyawa-hidrokarbon -blogspot.com. Diakses