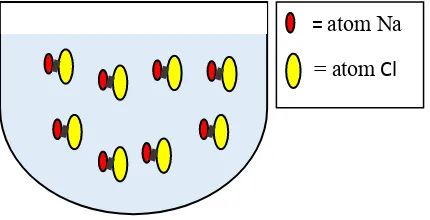
A. Yasthophi P. S.Ritonga - MISKONSEPSI MAHASISWA MENGENAI IKATAN ION DALAM SENYAWA NaCl
Teks penuh
Gambar

Dokumen terkait
Penelitian ini bertujuan untuk mengetahui pengaruh e-WOM, city branding terhadap keputusan kunjungan yang dimediasi oleh citra kota dalam mewujudkan kota pintar
Oleh karena itu dapat dilakukan upaya-upaya pengendalian zat organik dalam air seperti memperbaiki sanitasi pembuangan tinja dan limbah rumah tangga sehingga tidak mencemari sumber
Apabila tanah hak yang diterlantarkan kurang dari atau sama dengan 25 (dua puluh lima) persen sebagaimana dimaksud pada ayat (1) huruf c, maka Keputusan Penetapan
Pada bab kedua menjelaskan teori-teori yang berkaitan dengan penelitian yang akan dilakukan yaitu mengenai Teori Kebijakan Program UPK MP, Syarat Penerima SPP,
Pengambilan data lapangan yang dilakukan di Tambang PT Bukit Asam, Sumatera Selatan adalah sebagai berikut: (1) mengukur gaya tarik yang diperlukan untuk
Pementasan SZAVTP merupakan tahap akhir dari proses kreatif penciptaan tata busana dengan bahan material dari sampah plastik dan kain perca Semua bahan yang telah
Penggunaan variabel budaya inovasi mengacu pendapat (Robbins, 1996), yang mengatakan bahwa organisasi mampu melaksanakan inovasi jika ditunjang oleh budaya organisasi,
Pemekaran perumahan formal oleh pengembang properti swasta di wilayah Kabupaten Tangerang berpotensi menghasilkan “urban void” akibat degradasi kualitas permukiman