BAB 2
TINJAUAN PUSTAKA
2.1 Sistematika Tumbuhan Bawang Hutan (Scorodocarpus borneensis Becc) Tumbuhan bawang hutan (Scorodocarpus borneensis Becc) termasuk tumbuhan Olacaceae, tumbuhan ini mempunyai nama lokal antara lain :
Sumatera : Bawang, Kulim, Rengom.
Kalimantan : Ansam, Bawang, Bawang hutan, Cepeluk, Jauhi, Kudur, Marsindu, Madudu, Sedau, Selaru, Seluru, Teradu, Sindu dan Kayu bawang. Sistematika tumbuhan kayu bawang menurut Abe dan Yamauchi (1993) adalah :
Divisi : Spermatophyta
Sub divisi : Angiospermae
Kelas : Dicotyledoneae
Bangsa : Santalales
Famili : Olacaceae
Marga : Scorodocarpus
Jenis : Scorodocarpus borneensis Becc
Pohon ini merupakan tumbuhan yang sangat tinggi ( 36 m), seperti pada Gambar 2.1. Banyak tumbuh di Sumatera dan hutan primer Kalimantan pada ketinggian 300 m di atas permukaan laut, terutama pada tanah kering, tidak tumbuh di rawa–rawa, tidak membentuk hutan murni, di hutan rimba tumbuh secara berkelompok dan hanya di tempat–tempat tertentu tumbuh secara umum (Heyne, 1987).
Gambar 2.1 Tumbuhan bawang hutan (Scorodocarpus borneensis Becc)
2.1.1 Kandungan Kimia Aktif Biologis Tumbuhan Bawang Hutan
Tumbuhan bawang hutan mengandung senyawa polisulfida yang mirip dengan jalur pembentukan senyawa polisulfida pada spesies Allium lainnya sehingga mempunyai aktivitas sebagai anti mikroba, yaitu 2,4,5,7–tetrathiaoctane-4,4-dioksida dan 5-thioxo-2,4,6trithiaheptane-2,2-dioksida. Tumbuhan ini juga diduga memiliki senyawa O-etil S-metiltiometil tiosulfit (CH3SCH2SS(O)OCH2CH3) (3). Ekstrak
kasar kulit batang bawang hutan mengandung sesquiterpen saponin, steroid, flavonoid, dan senyawa metiltiometil yang menyebabkan bau seperti bawang putih dan mempunyai aktivitas anti mikroba (Kubota et al., 1999; Lim et al., 1998).
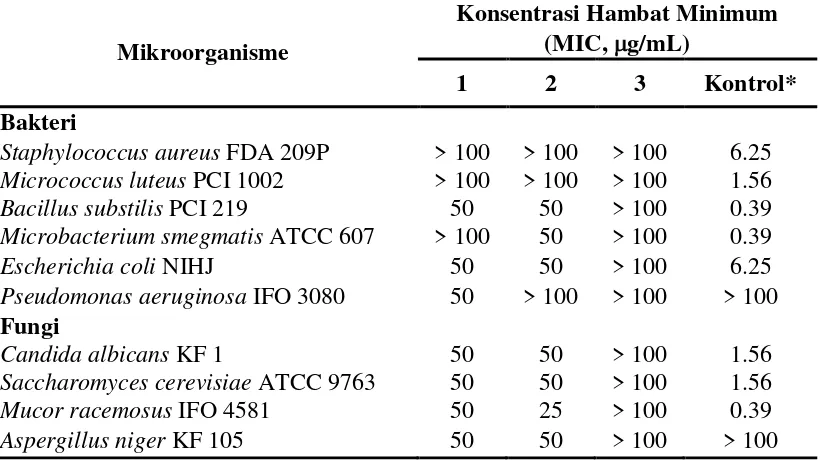
Tumbuhan bawang hutan sering dipergunakan sebagai bumbu untuk memasak oleh penduduk lokal Kalimantan. Bau dan kegunaan dari kayu bawang sangat mirip dengan bawang, sehingga dapat diperkirakan bahwa bawang hutan memiliki aktivitas fisiologis yang sama dengan bawang. Aktivitas antimikroba dari ketiga senyawa yang terkandung di dalam tumbuhan bawang hutan ditunjukkan pada Tabel 2.1
Tabel 2.1 Aktivitas antimikroba dari senyawa yang terdapat dalam tumbuhan bawang hutan (Lim, et al, 1998)
Senyawa kontrol : untuk bakteri adalah penisilin, untuk fungi adalah nistatin.
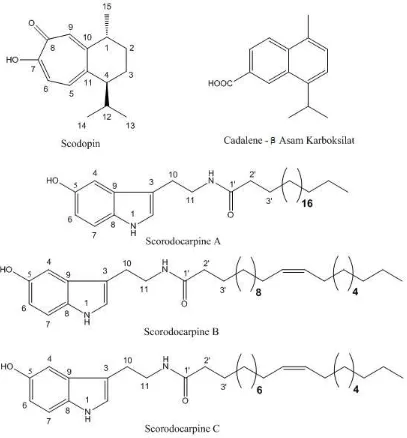
Wiart (2001) telah meneliti tentang tanaman Scorodarpus borneensis (Baill.) Becc (Olacaceae) yang diperoleh dari negara Malaysia, dan dari hasil isolasi tanaman tersebut diperoleh senyawa sesquiterpen, scodopin dan tiga senyawa alkaloid tipe triptamin yaitu Scorodocarpine A-C. Berdasarkan hasil elusidasinya diperoleh struktur kimia dari senyawa-senyawa tersebut seperti pada Gambar 2.3.
2.1.2 Ekstrak Bahan Alam Yang Memiliki Aktivitas Antikanker
Beberapa ekstrak bahan alam yang berpotensi sebagai anti kanker terdapat dalam beberapa tumbuhan antara lain yaitu :
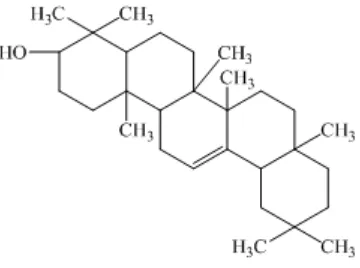
1. Benalu (Macrosolen cochinchinesis), ekstrak tumbuhan ini mengandung beberapa senyawa metabolit sekunder seperti alkaloid (β-amyrin), glukosida, flavanoid, saponin, asam oleanolat, lupeol, dan avicularin. Alkaloid jenis ini dapat menghambat S180 dan sel kanker JTC-26.
Gambar 2.4 Struktur kimia β-amyrin
2. Buah makasar (Bruea javanica (L.) Merr.), ekstrak tumbuhan ini mengandung beberapa senyawa metabolit sekunder seperti alkaloid (brucamarine, yatamine), glukosida (Brucea javani, brucealiue, yatanosida), bruceosida A dan B, fenol (brucenol dan asam bruceolat), dan brucetol. Alkaloid jenis brucamarine dan yatamine ini dapat mengobati kanker saluran pencernaan (esophagus, lambung, usus, dan rektum), kanker paru-paru, payudara, dan leher rahim (servik).
menghambat sel kanker linisel L1210 , P1534, HKR, EAC, S180 dan sel kanker
payudara. Sedangkan efektifitas antikanker dari vincristine lebih besar dari vinblastine yang dapat menghambat ridge way osteosarcoma, mecca limfosarcoma, dan kanker X563 sarcoma. Ekstrak air dan alkohol tumbuhan tapak dara dapat menghambat sarcoma 180 dengan tingkat keberhasilan 95,7% dan sudah tersedia dalam bentuk obat paten injeksi (Fowler, 1983).
Gambar 2.5 Struktur kimia Vinblastine dan Vincristine
2.1.3 Aktivitas Biologis Penghambatan Sel Kanker
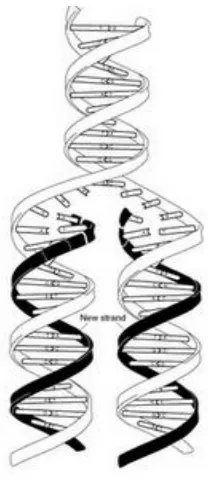
Aktivitas biologis untuk penghambatan sel kanker dapat dilakukan dengan mekanisme penghambatan sintesa DNA. Replikasi DNA dapat terjadi dengan adanya sintesis rantai nukleotida baru dimana rantai nukleotida lama berfungsi sebagai patron (cetakan ). Prosesnya dengan menggunakan komplementasi pasangan basa untuk menghasilkan suatu molekul yang berfungsi sebagai cetakan (template) DNA baru yang sama dengan molekul DNA lama. Proses yang terjadi tersebut dipengaruhi oleh enzim helikase, enzim polimerase, ligase dan dNTP - dNTP. Adapun tahapan – tahapan yang terjadi adalah sebagai berikut :
1. Denaturasi mol DNA utas rangkap (double helix) menjadi DNA utas tunggal dilakukan oleh enzim unwindase.
3. Agar point 2 dapat berlangsung harus tersedia dNTP2, enzim DNA polimerase. 4. Setelah rantai DNA baru sempurna disintesis maka oleh enzim ligase dibentuk
DNA utas rangkap yang dapat terjadi melalui 2 metode yaitu :
a. Metode konservatif apabila DNA utas rangkap yang terbentuk hasil penggabungan rantai DNA lama dengan rantai DNA lama.
b. Metode semi konservatif apabila DNA utas rangkap yang terbentuk merupakan hasil penggabungan dari DNA lama dengan DNA baru.
5. Untuk sel kanker diperlukan unsur tambahan selain dari pada komponen –
Ada tiga kemungkinan terjadinya replikasi DNA, yaitu konservatif, semikonservatif, dan dispersif.
1. Model konservatif, yaitu dua rantai DNA lama tetap tidak berubah, berfungsi sebagai cetakan untuk dua rantai DNA baru. Replikasi ini mempertahankan molekul dari DNA lama dan membuat molekul DNA baru.
3. Model dispersif, yaitu beberapa bagian dari kedua rantai DNA lama digunakan sebagai cetakan untuk sintesis rantai DNA baru. Oleh karena itu, hasil akhirnya diperoleh rantai DNA lama dan baru yang tersebar pada rantai DNA lama dan baru. Replikasi ini menghasilkan dua molekul DNA lama dan DNA baru yang saling berselang-seling pada setiap untai (Reggy, 2012).
Limus (2007) telah meneliti tentang mencegah kanker melalui mekanisme DNA. Metilasi DNA dan penekanan produksi Histon Deacetylase (HDAC) akibat rangsangan sulforaphane yang bekerja sama untuk mempertahankan fungsi sel normal, makin tinggi kadar sulforaphane maka semakin efektif untuk melawan kanker. Hal ini telah dibuktikan melalui penelitian terhadap kanker payudara pada tikus-tikus percobaan serta mencegah perkembangan sel-sel yang baru tumbuh (Munchberg, 2007).
Apabila gugus metil dari senyawa organo sulfida mensubstitusi gugus –OH posisi C no 3 dari DNA, maka sintesa DNA pada sel kanker akan terhambat karena tidak terjadi perpanjangan rantai DNA seperti pada Gambar 2.6. Akibatnya masuknya metil pada Citosin, maka perpanjangan DNA berikutnya akan terhambat karena pospat tidak dapat berikatan lagi pada atom C no. 3 sehingga sintesa DNA akan terhenti (Munchberg, 2007).
2.2 Mekanisme Pembentukan Kanker
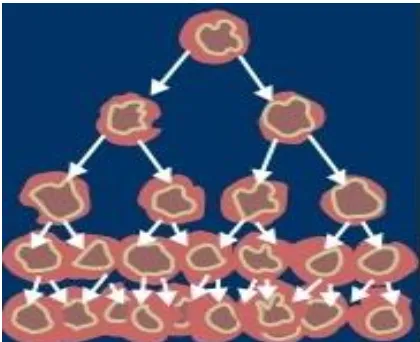
Pada dasarnya, pembelahan sel dibedakan menjadi 2 macam, yaitu pembelahan sel secara langsung dan secara tak langsung. Pembelahan sel secara langsung jika proses pembelahan tidak didahului dengan pembentukan gelondong pembelahan dan penampakan kromosom disebut dengan amitosis.
Adapun pembelahan sel secara tak langsung jika proses pembelahan didahului dengan pembentukan gelondong pembelahan dan penampakan kromosom. pembelahan secara tidak langsung ini meliputi pembelahan mitosis dan pembelahan meiosis.
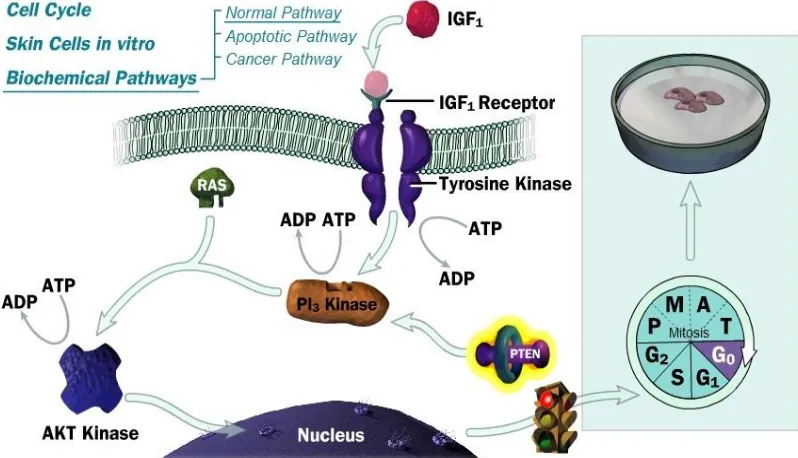
Dari mekanisme pada Gambar 2.7 terlihat bahwa pembelahan sel diawali dari terbentuk nya kompleks antara IGF1 dengan reseptor nya (IGF1 reseptor) lalu
mengaktifkan Tyrosin Kinase dengan bantuan ATP lalu PI3 akan aktif dengan
bantuan ATP untuk membentuk kompleks dengan RAS , kemudian kompleks PI3
Kinase – RAS akan mengaktifkan AKT Kinase dengan bantuan ATP selanjut nya akan memberi sinyal kepada Nukleus untuk memulai melakukan pembelahan sel sesuai dengan kebutuhan nya. Setelah keperluan sel yang dibutuhkan tercukupi maka PTEN akan merebut ATP yang akan dipergunakan PI3 Kinase sehingga kompleksnya
dengan RAS tidak berlangsung dan sinyal selanjutnya juga akan terhenti maka pembelahan sel berikutnya akan terhenti juga.
Proses terbentuknya sel kanker diawali terganggunya PTEN oleh faktor inflamasi maupun paparan benda asing mengakibatkan PI3 Kinase akan mengikat ATP secara tidak terkendali sehangga respon untuk pembelahan sel juga tidak terkendali yang menghasilkan sel yang tidak dewasa dan tidak memiliki hubungan antar sel sehingga sel tidak memiliki fungsi biologis sebagaimana mestinya yang disebut sel kanker
Setiap makhluk hidup dibentuk oleh berjuta-juta sel dan setiap sel dibentuk oleh organ-organ sel yang lebih dikenal dengan istilah organel sub selular. Salah satu organel selular yang penting yang terlibat di dalam pembelahan sel (perkembangbiakan sel) adalah inti sel. Inti sel terdiri dari 3 komponen yaitu :
a. Deoxyribonucleic Acid (DNA) b. Ribonucleic Acid (RNA) c. Nukleoprotein (Protein Inti)
nukleutida dalam jumlah tertentu yang berfungsi untuk mensintesis komponen sel di dalam perkembangannya.
Penggambaran struktur DNA berdasarkan pernyataan diatas dapat digambarkan sebagai berikut : komponen intron. X, Y, dan Z ketiganya disebut dengan gen struktural yaitu gen yang mensintesis komponen yang dibutuhkan oleh sel di dalam perkembangannya misalnya gen pembentuk/mensintesis enzim atau komponen lain yang dibutuhkan oleh sel. Di dalam proses pembelahan sel baik intron maupun exon semuanya mengalami pembelahan/denaturasi sehingga DNA yang tadinya merupakan utas rangkap (berbentuk untai ganda) terdenaturasi menjadi DNA utas tunggal. DNA utas tunggal yang terbentuk ini akan menjadi cetakan pateron didalam sintesis DNA baru dimana DNA baru dengan adanya dNTP2 serta enzim DNA polimerase. Baik intron
maupun exon mempunyai ciri dan jumlah nukleotida yang spesifik untuk setiap gen. Jumlah nukleotida pada intron jauh lebih besar (banyak) dari jumlah nukleotida pada
exon.
kanker, yang sel-selnya terus menerus tumbuh dan membelah sehingga mendesak dan merusak jaringan yang ada di sekitarnya (Plain, 2008).
Gambar 2.8 Pembelahan sel normal dengan metode semi konservatif
Kromosom organisme eukariotik memiliki struktur yang linier. Ujung kromosom ini memiliki struktur yang dikenal sebagai Telomer. Telomer dari semua
kromosom eukariotik terdiri atas rangkaian nukelotida pendek yang cenderung berulang pada ujung-ujung kromosomal DNA. Sebagai contoh, telomer dari manusia (sperma dan sel telur) mengandung antara 100-1700 perulangan heksanukleotida TTAGGG.
Namun, sebagian besar sel somatik mengunci telomerase. Akibatnya, pada setiap siklus pembelahan sel ketika sel mereplikasi DNA nya, sekitar 50 porsi nukleotida hilang dari ujung tiap telomer. Sehingga semakin lama telomer sel somatik pada hewan semakin pendek, dan akhirnya berujung pada ketidakstabilan dan
kematian sel. Fenomena ini membuat beberapa ilmuan mendukung suatu “teori
penuaan telomer” yang mengimplikasi pada pemendekan telomer sebagai faktor
utama dalam sel, jaringan, dan bahkan pada penuaan organisme. Menariknya, sel
kanker tampak “kekal” karena dapat terus berproduksi secara tidak terbatas. Sebuah
survey dari 20 jenis tumor yang berbeda oleh Geron Corporation dari Meuto Pask, California mengungkapkan bahwa semua tumor tersebut memiliki aktivitas Telomer.
Telomer pada kromosom manusia mengandung rangkaian heksanukleotida TTAGGG yang berulang antara 100 hingga 1700 kali. Perulangan rangkaian-rangkaian TTAGGG ini tersambung pada ujung-ujung 3’ dari untaian DNA dan
dipasangkan dengan rangkaian komplemen 3’-AATCCC-5’ pada untaian DNA yang
lain. Sehingga daerah kaya-G terbentuk pada ujung 3’ dari tiap untaian DNA, dan daerah kaya-C terbentuk pada ujung 5’ dari tiap untaian DNA. Secara khusus pada tiap ujung kromosom dengan daerah kaya-G protucedes 12 hingga 16 nukleotida diluar komplemen untaian kaya-C nya.
Seperti halnya telomerase lain, telomerase manusia adalah suatu ribonukleoprotein. Asam ribonukleik pada telomerase manusia adalah suatu molekul RNA dengan panjang 962 nukleotida. RNA ini berfungsi sebagai template untuk aktivitas DNA polimerase dari enzim telomerase. Nukleotida ke 56 dari RNA ini adalah CUAACCCUAAC dan menyediakan fungsi template (cetakan) untuk reaksi adisi terkatalisasi-telomerase dari unit-unit TTAGGG pada ujung 3’ dari untaian DNA (Watson, 1988).
Replikasi DNA bersifat semi diskontinyu. Penggabungan timin yang dilabeli dengan unsur radio aktif kedalam DNA selama replikasi, diikuti oleh autorediografi replikasi DNA mengungkapkan bahwa kedua untaian dari dupleks DNA tereplikasi pada tiap replikasi lanjutan oleh DNA polimerase. DNA polimerase menggunakan satu untaian DNA (single-stranded DNA/ssDNA) sebagai template dan membuat suatu untaian komplemennya (pelengkapnya) dengan mempolimerisasi deoksinukleotida yang sesuai dengan basa yang ada pada template. DNA polimerase
mensintesis DNA hanya pada arah 5’→3’, pembacaan untaian template antiparalel pada 3’→5’. Pertanyaan muncul pada bagaimana DNA polimerase mengkopi untaian induk yang terjadi pada arah 5’→3’ pada proses replikasi. Ini menunjukkan bahwa
replikasi bersifat semidiskontinue saat heliks DNA yang terbuka selama proses
replikasi dengan model 3’→5’.
Dengan demikian satu untaian induk dikopi secara kontinyu untuk membentuk suatu kopian baru yang tersintesis yang disebut untaian utama pada tiap percabangan replikasi. Untaian induk yang lain terkopi secara intermiten, atau dengan model diskontinyu untuk menghasilkan seperangkat fragmen-fragmen. Fragmen-fragmen ini tergabung untuk membentuk untaian pelapis utuh. Secara keseluruhan masing-masing dari dua dupleks DNA menghasilkan satu DNA lama dan satu DNA baru dalam suatu proses replikasi DNA (Watson, 1988).
verifikasi biokimia dari pola semidiskontinyu pada replikasi DNA yang baru saja diubah. Okazaki memaparkan suatu biakan E. coli yang membelah dengan cepat dengan thymidine yang dilabeli-3H selama 30 detik, dengan cepat mengumpulkan sel-sel, dan menemukan bahwa setengah dari bahan terlabel tersebut telah bergabung kedalam asam nukleat yang muncul dalam single strain DNA rantai pendek dengan panjang 1000 hingga 2000 nukleotida (setengah radioaktif lainnya telah tertutup dalam molekul DNA yang sangat besar). Fragmen Okazaki kemudian bergabung secara kovalen membentuk rantai polinukleotida yang lebih panjang, sesuai dengan replikasi model mikroskopik. Kebenaran dari model replikasi ini telah dikuatkan dengan mikrografik elektron dari DNA yang sedang mengalami replikasi pada sel eukariotik (902-904).
Umumnya sel kanker mempunyai sifat pertumbuhan yang berlebihan, gangguan diferensiasi sel dan jaringan, bersifat invasif terhadap jaringan di sekitarnya, dan menyebar ke jaringan lain (metastatis) yang menyebabkan pertumbuhan baru, dan terjadi perubahan metabolisme ke arah pembentukan makromolekul dari nukleosida serta asam amino juga peningkatan katabolisme karbohidrat untuk energi sel, seperti pada Gambar 2.9 (Watson, 1987).
Kanker merupakan salah satu isu yang penting dalam bidang kimia medis. Saiz-Urra (2005) melaporkan bahwa 7,6 juta kematian dari 58 juta kematian yang tercatat disebabkan oleh kanker. Lebih dari 70% kematian yang disebabkan oleh kanker ini terjadi di negara berkembang dengan pendapatan yang rendah serta kurangnya atau bahkan tidak adanya akses untuk diagnosis dan pengobatan .
Kanker diklasifikasikan sesuai dengan jaringan atau tipe sel dari mana ia timbul. Kanker yang timbul pada sel–sel epitelial (sel–sel permukaan) dinamakan karsinoma (carcinoma), misalnya kanker payudara, kanker kulit, dan kanker lambung. Kanker yang timbul pada jaringan konektif (penyambung) atau sel–sel otot disebut sarkoma, misalnya fibrosarkoma (kanker jaringan ikat) dan kanker yang tidak memenuhi salah satu dari dua kategori di atas adalah termasuk dalam berbagai jenis leukimia yaitu kanker yang berasal dari sel–sel hemopoietik (sel darah) dan kanker yang berasal dari sistem syaraf (Alberts, 1994).
Di alam banyak terdapat faktor-faktor penyebab kanker (karsinogen). Karsinogen adalah zat atau bahan yang dapat merangsang pembentukan kanker. Beberapa macam karsinogen dapat berbentuk senyawa kimia (karsinogen kimiawi), faktor fisika seperti radiasi sinar X atau sinar UV, virus atau juga disebut virus onkogenik serta ketidak setimbangan hormonal (Bulan, 2002).
Siklus sel merupakan urutan kejadian di dalam sel sejak sel muncul hingga membelah menjadi dua (mengalami duplikasi atau replikasi) sedangkan reproduksi sel merupakan bagian dari siklus sel, bagaimana sel tersebut membelah menjadi dua sel anak dan mendistribusikan seluruh DNA (genom) dari sel induk ke sel anak. Fungsi dasar dari siklus sel adalah menduplikasi secara akurat jumlah DNA dalam kromosom yang kemudian dipisahkan ke dalam dua sel anak yang identik secara genetik. Sel dari organisme eukariot mempunyai sistem pengendali siklus sel yang sangat kompleks, yang dipengaruhi oleh faktor-faktor baik dari dalam maupun luar sel. Sistem ini dapat mengendalikan perubahan biokimiawi, termasuk replikasi DNA, segregasi pada duplikasi kromosom, dan duplikasi organel maupun makromolekul. Bila sistem mengalami malfungsi antara lain dapat mengalami pertumbuhan berlebihan yang menyebabkan kanker.
Transformasi keganasan sel terjadi akibat akumulasi mutasi pada sejumlah gen tertentu, dan hal ini yang merupakan kunci terjadinya kanker pada manusia. Gen terdapat dalam kromosom pada inti sel. Sebuah gen akan menentukan untaian asam amino yang harus dirangkaikan antara satu dengan lainnya untuk membentuk suatu protein, dan protein ini kemudian akan melaksanakan fungsi gen tersebut. Bila gen diaktifkan, maka sel akan bereaksi dengan jalan mensintesis protein yang telah disandinya. Sehingga mutasi gen dapat mengubah jumlah atau aktivitas produk proteinnya (Soeng S dkk, 2009).
Gambar 2.10 Pembelahan sel normal Keterangan : 1 – Apoptosis
2 – Sel yang rusak (National Cancer Institute, 2008).
Sementara pada pembelahan sel yang terjadi secara tidak normal (sel kanker) seperti pada Gambar 2.11 untuk daur hidup sel-sel kanker juga melakukan siklus yang hampir sama dengan siklus sel normal tetapi mereka memotong salah satu kontrol yang membuat dirinya ber-replikasi terlalu banyak sehingga menyebabkan kematian dari sel kanker itu sendiri. Sel kanker ini tidak berhenti membelah diri secara normal. Dan pada pembelahan sel kanker tidak membutuhkan faktor eksternal untuk membelah dirinya dalam siklus sehingga proses pertumbuhannya sangat cepat (Hendri, 2011).
Beberapa ciri spesifik sel kanker dibandingkan dengan sel normal antara lain: sel kanker tidak mempunyai kontrol pertumbuhan; daya lekat sel kanker berkurang atau bahkan sudah tidak ada. Inhibisi kontak sel kanker sudah tidak ada sehingga jika ditanam pada media kultur jaringan akan diperoleh pertumbutan yang berlapis-lapis dan tidak teratur.
Sel kanker mempunyai sistem enzim yang berbeda yaitu jumlah macam enzim pada sel kanker lebih sedikit jika dibandingkan dengan sel normal, sebagai contoh sel kanker tidak mempunyai enzim asparagin sintetase, sehingga tidak dapat mensintesis asparagin. Enzim-enzim untuk pertumbuhan pada sel kanker lebih besar jika dibandingkan dengan sel normal (Mulyadi, 1997)
Tabel 2.2 Perbedaan antara sel normal dengan sel kanker
Sel Kanker Sel Normal
a Kontrol pertumbuhan sudah hilang kendali Masih ada kontrol pertumbuhan b Daya melekat sel satu dengan yang lain
berkurang atau hilang
Masih ada daya lekat sel c Inhibisi kontak sudah tidak ada*) Masih ada inhibisi kontak d Sistem enzimnya lebih sedikit
jumlahnya/macamnya, sebagai contoh sel kanker tidak mempunyai asparagin sintetase
Sistem enzim masih normal
e Enzim-enzim untuk pertumbuhan lebih besar Sistem enzim masih normal
*) Inhibisi kontak dapat diketahui dengan menumbuhkan sel normal dan sel kanker pada media yang cocok, kemudian pertumbuhan diamati.
2.3 Kanker Darah/Leukimia dan Jenis-Jenisnya
Leukemia merupakan kanker di dalam sel darah. Darah normal terdiri dari cairan yang disebut plasma serta memiliki tiga jenis sel yaitu sel darah putih, sel darah merah, dan keping darah (Platelets.) Sel darah putih atau leukosit, membantu tubuh melawan infeksi dari penyakit.
Sel darah merah atau eritrosit berfungsi membawa oksigen dari paru-paru menuju jaringan tubuh. Juga mengambil karbon dioksida dari jaringan tubuh untuk dibawa ke paru-paru . Sel darah merah ini yang membuat darah berwarna merah. Keping darah disebut juga trombosit berfungsi untuk membantu penggumpalan darah ketika seseorang terluka. Dengan penggumpalan trombosit, pendarahan bisa terkendali dan orang yang terluka tidak terlalu banyak kekurangan darah. Sel-sel darah dibentuk di dalam spon yang lembut di dalam tulang yang disebut sumsum tulang. Sedangkan sel-sel darah yang tidak terbentuk disebut blasts.
Beberapa blasts berada dalam sumsum hingga masak, sementara beberapa yang lain menuju bagian tubuh yang lain hingga masak. Secara normal, sel darah diproduksi secara terkendali, sebagaimana kebutuhan tubuh. Proses ini menjaga tubuh agar tetap sehat. Ketika leukemia terbentuk, tubuh memproduksi sejumlah sel darah putih secara abnormal. Sel-sel leukemia biasanya tampak berbeda dengan sel darah putih normal dan tidak dapat berfungsi dengan baik.
Penyakit leukimia dikelompokkan atas penyakit leukimia akut dan leukimia kronis, yaitu :
a. Leukemia akut, penyakit leukimia yang kondisinya akan semakin memburuk secara cepat.
b. Leukemia kronis, penyakit leukimia yang kondisinya akan semakin memburuk secara bertahap.
2.3.1 Leukimia Akut
Leukimia akut menunjukkan gejala klinik suhu badan naik, ada tanda–tanda infeksi, pendarahan karena trombositopenia, pucat, lesu, karena anemia dan nyeri pada tulang. Pemeriksaan laboratorium menunjukkan kesamaan, kecuali jenis sel leukemianya, yaitu kadar haemoglobin turun, jumlah leukosit naik, jumlah eritrosit turun, ditemukan banyak sel muda (immature), jumlah trombosit turun dan waktu pendarahan lama. Ada dua jenis leukimia akut yaitu Leukimia Mielositik Akut (LMA) dan Leukimia Limfositik Akut (LLA).
Leukimia Mielositik Akut (LMA) adalah penyakit yang bisa berakibat fatal, dimana mielosit (yang dalam keadaan normal berkembang menjadi granulosit) berubah menjadi ganas dan dengan segera akan menggantikan sel-sel normal di sumsum tulang. Sel-sel leukemik tertimbun di dalam sumsum tulang, menghancurkan dan menggantikan sel-sel yang menghasilkan sel darah yang normal. Sel kanker ini kemudian dilepaskan ke dalam aliran darah dan berpindah ke organ lainnya, selanjutnya tumbuh dan membelah diri. Mereka bisa membentuk tumor kecil (kloroma) di dalam atau tepat dibawah kulit dan bisa menyebabkan meningitis,
anemia, gagal hati, gagal ginjal, dan kerusakan organ lainnya.
Pada kemoterapi awal biasanya diberikan sitarabin (selama 7 hari) dan daunorubisin (selama 3 hari). Kadang diberikan obat tambahan (misalnya tioguanin atau vinkristin) dan prednison. Dengan kemoterapi yang intensif harapan hidup pasien LMA lebih dari satu tahun dan beberapa pasien ada yang bertahan sampai tiga tahun dan sekitar 20% kemungkinan dapat sembuh. Obat tunggal yang paling aktif bagi pasien LMA adalah sitarabin, tetapi lebih baik bila digunakan kombinasi dengan obat lain. Kombinasi yang baik yaitu sitarabin dengan tioguanin atau sitaraban dengan daunorubisin.
Leukimia Limfositik Akut (LLA) adalah suatu penyakit yang berakibat fatal, dimana sel-sel yang dalam keadaan normal berkembang menjadi limfosit berubah menjadi ganas dan dengan segera akan menggantikan sel-sel normal di dalam sumsum tulang. Leukemia jenis ini merupakan 25% dari semua jenis kanker yang mengenai anak-anak di bawah umur 15 tahun. LLA ini paling sering terjadi pada anak usia antara 3-5 tahun, tetapi kadang dapat juga terjadi pada usia remaja dan usia dewasa.
Sel-sel yang belum matang, yang dalam keadaan normal berkembang menjadi limfosit, berubah menjadi ganas. Sel leukemik ini tertimbun di sumsum tulang, lalu menghancurkan dan menggantikan sel-sel yang menghasilkan sel darah yang normal. Sel kanker ini kemudian dilepaskan ke dalam aliran darah dan berpindah ke hati, limpa, kelenjar getah bening, otak, ginjal dan organ reproduksi; dimana mereka melanjutkan pertumbuhannya dan membelah diri. Sel kanker bisa mengiritasi se. laput otak, menyebabkan meningitis dan bisa menyebabkan anemia, gagal hati, gagal ginjal dan kerusakan organ lainnya.
2.3.2 Leukimia Kronis
Leukimia kronis mempunyai ciri–ciri utama seperti timbulnya pada usia yang agak lanjut, jumlah leukosit tinggi, penurunan kadar haemoglobin ringan atau sedang dan sering berubah menjadi leukimia akut. Ada dua jenis leukimia kronis yaitu Leukimia Mielositik Kronis (LMK) dan Leukimia Limfositik Kronis (LLK).
Pada penyakit Leukimia Mielositik Kronis (LMK) perbandingan sel yang belum matang (immature) dengan sel yang sudah matang (mature) berbeda pada satu penderita dengan penderita yang lain. Pada tahap awal jumlah sel yang belum matang relatif sedikit, jumlah trombosit meningkat dan penurunan kadar haemoglobin ringan. Perubahan penyakit Leukimia Mielositik Kronis (LMK) menjadi stadium akut (stadium akhir) yang disebut blastic transformation atau blast crisis, terjadi perubahan sebagai berikut: jumlah mieloblas dan sel yang belum matang lain meningkat, jumlah basofil meningkat, trombosit menurun, leukosit meningkat dan kadar haemoglobin menurun drastis. Transformasi blastik ini umumnya timbul setelah tiga sampai empat tahun setelah diagnosis dan penyakit ini berubah menjadi leukimia akut. Dengan proses penghambatan dapat dilakukan menggunakan proses kemoterapi menggunakan busulfan.
Leukimia Limfositik Kronis (LLK) merupakan penyakit yang timbul akibat akumulasi sel limfosit dalam sumsum tulang, darah, kelenjar getah bening, limfa dan hati sehingga sel pembentuk darah lainnya di dalam sumsum tulang berkurang. Penyakit Leukimia Limfositik Kronis (LLK) ini sering timbul pada pasien-pasien yang berusia lanjut (usia 45 tahun keatas) dan sangat jarang terjadi pada pasien sebelum umur 45 tahun.
2.3.3 Mekanisme Penghambatan Sel Leukimia
Menurut teori Dogmasentral bahwa DNA akan mengalami transkripsi dan translasi untuk mensintesa protein, dan keadaan ini dapat terhenti apabila atom C no 3 dari deoksiribosa di metilasi sehingga sintesa proein secara otomatis juga terhenti. Kemudian secara alami pula sel dapat mereperasi diri sehingga proses sintesa protein dapat berlangsung kembali. Hal ini yang menyebabkan pemakaian obat kanker harus dikombinasi agar kinerjanya dapat maksimal. Sebagai contoh obat untuk leukimia akut yang digunakan selama ini adalah kombinasi dari 6-Merkaptopurin, Metotraksat, Prednison dan L-Asparaginase. Dimana fungsi masing- masing obat adalah sebagai berikut :
a) 6-Merkaptopurin merupakan analog basah adenin dan hiposantin. Bila difosporilasi dengan 5-fosfo-α-D-ribosilposfat menghasilkan 6-Merkaptopurin ribosit merupakan inhibitor perubahan 1MP menjadi AMP.
b) Metotraksat analog asam folat merupakan inhibitor enzim dehidrofolat reduktase sehingga reaksi berikut tidak dapat berlangsung.
Gambar 2.13 Mekanisme reaksi Folat menjadi Tetrahidrofolat (THF)
Enzim ini sangat peka terhadap senyawa-senyawa analog asam folat (anti metabolit) sehingga digunakan pada kemoterapi untuk sel kanker. Beberapa senyawa analog seperti metotraksat, aminopterin. Fungsi folat terutama di dalam mensintesis prekursor asam nukleat dimana analog-analog senyawa tersebut akan menghambat sintesis DNA sel-sel kanker.
Gambar 2.14 Reaksi dalam bentuk ion asam amino
Gambar 2.15 Reaksi dalam bentuk asam amino
d) Predmison seperti pada Gambar 2.16 merupakan senyawa anti inflamasi (peradangan) menghambat sintesis DNA/RNA limfosit.
Mekanisme kerja predmison belum begitu jelas tetapi aktivitas penyembuhan leukimia dihubungkan dengan penghambatan sintesis DNA dan RNA limfosit. Predmison adalah suatu ortikosteroid golongan glukokartikoid yang berfungsi untuk menghambat pengambilan glukosa oleh sel-sel kanker sehingga membatasi energi yang sangat dibutuhkan untuk biosintesis asam nukleat dan beberapa kasus sintesis DNA dan RNA mungkin langsung dipengaruhi (Montgomery, 1993).
2.4 Lini Sel L1210
Salah satu komponen sel digunakan untuk menguji sifat anti kanker suatu zat adalah inti sel L1210, di samping sel yang lainnya seperti sel hela (sel kanker yang
berasal dari kanker leher rahim manusia), sel P388, sel KB (nasopharynx carcinoma), sel sarkoma 180 A, sel V 79, sel walker 256 dan lain–lain (Itokawa dan Takeya, 1993; Bulan, 2002). Lini sel L1210 atau limfoid leukimia L1210 adalah sel tumor yang
diisolasi dari limfa tikus. Sifat–sifat yang spesifik dari lini sel L1210 adalah terjadinya
perkembangbiakan yang tersebar luas ke organ lainnya dan dapat menyebabkan kematian dalam kurun 8-11 hari, merupakan sel tumor yang tumbuh cepat dengan persentase sel cukup tinggi dan memiliki tingkat pertumbuhan 100% (Bauguess, dkk., 1981). Beberapa penelitian sebelumnya telah menunjukkan bahwa lini sel L1210
memiliki resistensi terhadap obat antikanker metotraksat (White dan Goldman, 1981; Wallerstein dkk, 1971).
Metrotraksat (MTX) memiliki indikasi sebagai antikanker, dan terdiri atas 3 kelas yaitu :
1. L-4-amino-N10- metil pteroil asam glutamat, atau L-Ametopterin Hidrat 98% (133073-73-1), dengan FW = 454,45, mp. 195 oC,
25D = + 17o
C, C = 1,00 M Na2CO3, Index merck 13,5908, safety 2.129C, FT-IR 1(2) 898D, dan teratogen
yang toksik. Senyawa ini potensial untuk menghambat dehidrofolatreduktase dan untuk antitumor.
2. DL-4-amino-N10- metil pteroil asam glutamat 96% (60338-53-6), dengan FW = 454,45, mp. 195 oC, FT-IR 1(2) 898B, safety 2.129B dan teratogen yang toksik. 3. D-4-amino-N10- metil pteroil asam glutamat, 95% (133073-73-1), dengan FW =
454,45, mp. 195 oC,
20D = - 19,4 oC, C = 2,01 M NaOH, Index merck 13,6015, FT-IR 1(2) 898C, safety 2.129D, dan teratogen yang toksik (Aldrich, 2003).Gambar 2.17 Struktur kimia D-4-amino-N10- metil pteroil asam glutamat (Bushan dkk, 1999)
Evaluasi sitoksitas suatu senyawa terhadap lini sel L1210 dilakukan dalam tiga
tahapan yaitu :
1. Tahap isolasi lini sel, 2. Tahap penggandaan sel
2.5 Peran Antioksidan Dalam Memutus Reaksi Berantai Radikal Bebas Serta Jenis-Jenisnya
Antioksidan adalah senyawa yang mempunyai struktur molekul yang dapat memberikan elektronnya dengan cuma-cuma kepada molekul radikal bebas tanpa terganggu sama sekali fungsinya dan dapat memutus reaksi berantai dari radikal bebas. Terdapat tiga macam antioksidan yaitu :
3. Antioksidan yang dibuat oleh tubuh kita sendiri yang berupa enzim antara lain superoksida dismutase, glutathione peroxidase dan katalase.
4. Antioksidan alami yang diperoleh dari tanaman atau hewan, yaitu tokoferol, vitamin C, betakaroten, flavonoid dan senyawa fenolik.
5. Antioksidan sintetik, yang dibuat dari bahan-bahan kimia yaitu butylated hydroxy anisole (BHA), butylated hydroxy toluen (BHT), tetra butil hidroquinon (TBHQ) dan propil galat (PG), yang ditambahkan dalam makanan untuk mencegah kerusakan lemak.
Atas dasar fungsinya antioksidan dapat dibedakan menjadi lima bagian yaitu : 8. Antioksidan Primer
Antioksidan ini berfungsi untuk mencegah terbentuknya radikal bebas baru karena ia dapat merubah radikal bebas yang ada menjadi molekul yang berkurang dampak negatifnya, yaitu sebelum sempat bereaksi. Antioksidan primer yang ada dalam tubuh yang sangat terkenal adalah enzim superoksida dismutase.
9. Antioksidan Sekunder
Antioksidan sekunder merupakan senyawa yang berfungsi menangkap radikal bebas serta mencegah terjadinya reaksi berantai sehingga tidak terjadi kerusakan yang lebih besar. Contoh yang populer, antioksidan sekunder adalah vitamin E, vitamin C dan beta karoten yang dapat diperoleh dari buah-buahan.
10. Antioksidan Tersier
memperbaiki DNA dalam inti sel. Enzim tersebut bermanfaat untuk perbaikan DNA pada penderita kanker.
4. Chelator atau Sequestrants
Senyawa Chelator atau Sequestrants dapat mengikat logam sehingga logam tersebut tidak dapat mengkatalisis reaksi oksidasi dan kerusakan dapat dicegah. Misalnya asam sitrat dan asam amino.
5. Oxygen Scavanger
Antioksidan yang termasuk oxygen scavanger yang mampu mengikat oksigen sehingga tidak mendukung reaksi oksidasi, misalnya vitamin C. (Kumalaningsih, 2006).
Antioksidan adalah senyawa yang dapat menghambat laju oksidasi atau menetralisir radikal bebas, sehingga dianggap sebagai “cancer prenetive agent”, karena radikal bebas yang berlebihan dapat memicu terjadinya kanker (Yen dan Chen, 1995). Berbagai macam metode telah digunakan untuk mengukur kekuatan dari suatu antioksidan. Metode tersebut adalah 1,1-diphenyl-2-picryhydrazyl (DPPH) free radical scavenging), 2,2'-azino-bis(3-ethylbenzthiazoline-6-sulphonic acid)
(ABTS) radical scavenging, superoxide anion radical scavenging serta ferric reducing antioxidant power (FRAP).
Gambar 2.18 Struktur kimia a) Diphenylpicrylhydrazyl (radikal bebas)
b) Diphenylpicrylhydrazyl (tereduksi) (Molyneux, 2004) Ketika larutan DPPH dicampur dengan bahan yang dapat memberikan sebuah atom hidrogen, molekul ini akan mereduksi DPPH sehingga intensitas warna ungu akan menjadi berkurang (Molyneux, 2004). Dengan ringkasan reaksinya yaitu :
Z
*
+ AH
ZH + A
*
Dimana :
Z* = Radikal DPPH AH = Molekul donor
ZH = Bentuk tereduksi dari DPPH A* = Radikal bebas yang terbentuk Penapisan (screening) obat antikanker biasanya didahului dengan penapisan aktivitas antioksidan dari suatu senyawa. Hirota dkk (2000) telah menggunakan aktivitas DPPH radical-scavenging untuk uji pendahuluan senyawa yang berasal dari miso sebelum diuji aktivitas antiproliferatif-nya (Hirota dkk, 2000).
2.6 Obat Antikanker
kematian pada tahun 2030. Oleh karena itu, obat-obatan kanker baru yang lebih efektif sangat diperlukan (Saiz-Urra, 2009). Penggunaan obat anti kanker dimulai tahun 1946 dengan ditemukannya mustar nitrogen untuk mengobati leukimia. Jenis pengobatan kanker salah satunya dengan memberikan obat–obat pembunuh sel kanker/sitostatika (kemoterapi). Tujuan utama kemoterapi kanker adalah merusak secara selektif sel tumor yang berbahaya tanpa mengganggu sel normal.
Obat antikanker dapat digolongkan menjadi beberapa jenis. Untuk lebih jelas tentang penggolongan obat antikanker dapat dilihat pada Tabel 2.3.
Tabel 2.3 Obat antikanker dan penggolongannya (Mulyadi, 1997)
Golongan Sub golongan Obat Ester asam sulfonat Busulfan, Mileran, Dimetilmileran. Epoksid Diepoksibutan, Epodil, Eponate. 2. Anti Sejenis purin 6-Merkaptopurin, 6-Tioguanin.
metabolit Sejenis pirimidin Sitaribin, 5-Fluorourasil, 6-Azauridin. Sejenis folat Metotraksat.
Antagonis asam amino
Alanin, Selenilalanin, Fenilselenilalanin. Antagonis vitamin Isoriboflavin, Deoksipiridoksin.
3. Antibiotik Daktinomisin, Mitomisin,Daunorubisin, Daksorubisin, Mitramisin, Bleomisin. 4. Hormon Estrogen Dietilstilbestrol, Etinilestradiol.
Kelompok obat CCS adalah vinkristin, vinblastin, sitarabin, fluorourasil, azositidin, bleomisin, merkaptopurin, tioguanin, hidroksiurea dan metotreksat. Kelompok kedua adalah kelompok cell cycle-nonspecific (CCNS). Kelompok obat CCNS adalah mekloroetamin, siklofosfamid, melfalan, busulfan, tiotepa, karmustin, lomustin, semustin, mitomisin, daktomisin, deoksorubisin, daunorubisin.
Dan Tabel 2.4 berikut merupakan beberapa merk obat antikanker yang sudah dijual dipasaran secara komersil beserta fungsinya (National Cancer Institute, 2003).
Tabel 2.4 Beberapa obat antikanker yang dijual secara komersial (NCI, 2003)
No Obat Merk obat Fungsi
1 Asparaginase Erwinia Chrysanthemi
Erwinaze LMA
2 Chlorambucil Ambochlorin, Amboclorin, Leukeran, dan Linfolizin
LLK
3 Clofarabine Clofarex, dan Clolar LLA
4 Cytarabine Cytosar-U, dan Tarabine PFS LLA, LMA, dan LMK
5 Cyclophosphamide Clafen, Cytoxan, Neosar, dan Chlorambucil Clafen
LLA, LMA, dan LLA, LMK 6 Daunorubicin
Hydrochloride
Cerubidine, dan Rubidomycin LLA, dan LMA 7 Doxorubicin
Hydrochloride
Adriamycin PFS, dan Adriamycin RDF,
LLA, dan LMA 8 Methotrexate Abitrexate , Folex, Folex PFS,
Mexate, dan Mexate-AQ
LLA 9 Vincristine Sulfate Vincasar PFS, dan Vincasar
PFS
LLA, dan LMA 10 Ponatinib
Hydrochloride
Iclusig LMK
Sitotoksik adalah toksik terhadap sel dalam jaringan. Sifat ini dapat dibedakan menjadi sitostatik dan sitosidal. Sitotoksik yaitu menghentikan pertumbuhan sel yang sering sekali reversible dan sitosidal yaitu pembunuhan terhadap sel.
Antitumor yaitu efektif terhadap suatu model sistem tumor secara in vivo.
Antikanker yaitu efektif dalam suatu percobaan terhadap suatu penyakit pada manusia.
Sedangkan untuk menetapkan suatu senyawa bersifat antikanker dilakukan beberapa tahap penelitian yaitu uji sifat farmakologi dan aktivitas terhadap berbagai sel (penapisan awal) adalah untuk menentukan tosisitas suatu senyawa. Uji toksikologi pra klinis dan farmakologi pada hewan percobaan untuk menentukan sifat anti tumor suatu senyawa, dan uji coba klinik pada manusia untuk menetapkan suatu senyawa sebagai obat antikanker.
Penentuan sifat toksisitas suatu senyawa dilakukan dengan uji sifat farmakologi dan aktivitasnya terhadap berbagai sel secara in vitro atau in vivo. Sel– sel yang digunakan antara lain sel P388 (sel limfositis yang berasal dari kanker pada tikus), lini sel L1210 (sel yang diisolasi dari limfa tikus), sel hela (sel yang berasal dari
kanker leher rahim manusia), sel KB (nasopharynx carsinoma), sel sarcoma 180 A, sel walker 256 (Itokawa dan Takeya, 1993; Bulan, 2002).
Bagaimanapun juga, berbagai macam lini sel leukimia lebih sering digunakan untuk mengelusidasi mekanisme apoptosis. Hal ini terjadi karena obat-obatan antikanker maupun reagen sitotoksik lebih efektif terhadap kanker leukemia daripada penyakit kanker lainnya. Contoh lini sel leukemia lainnya yang sering digunakan adalah lini sel promyelocytic HL-60 serta lini sel Jurkat T (Zhang dkk, 2008).
anti tumor sebanyak 17.000 jenis senyawa hasil fermentasi. Sel yang digunakan dalam kultur jaringan tersebut adalah sel hela.
Hasil pengujian yang diperoleh dibandingkan dengan pengujian secara in vivo
pada tikus yang telah diinokulasi dengan tumor. Ada korelasi sebesar 70% antara aktivitas anti tumor pada kultur jaringan dengan aktivitas pada tikus yang diinokulasi dengan tumor. Namun ada beberapa pengecualian yaitu ada zat yang sangat aktif pada kultur jaringan tetapi tidak aktif pada tikus percobaan dan sebaliknya ada zat yang aktif pada tikus percobaan tetapi tidak aktif pada kultur jaringan dengan tingkat konsentrasi yang sama. Maka dari kedua sistem tersebut dapat disimpulkan bahwa in vitro dan in vivo bersifat saling melengkapi.
Sejak tahun 1955–1975 lembaga kanker nasional Amerika (NCI, National Cancer Institute) menggunakan lini sel L1210 untuk penapisan awal zat anti kanker,
zat–zat yang aktif terhadap lini sel L1210 kemudian di uji secara in vivo pada tikus
yang diinokulasi dengan tumor. Program penapisan yang dilakukan NCI berhasil menguji aktivitas 40.000 senyawa. Senyawa yang menunjukkan aktivitas terhadap lini sel L1210 diuji lebih lanjut terhadap suatu panel uji sel tumor tikus sebelum
dilakukan uji klinik. Selanjutnya NCI menggunakan suatu desain dalam penapisan awal untuk mendeteksi aktivitas suatu zat anti tumor berdasarkan model seleksi dari beberapa tumor padat pada tikus.
Hasil seleksi yang dilakukan menghasilkan sel P388 digunakan sebagai uji penapisan awal, karena sel ini sangat sensitif terhadap bermacam golongan senyawa dan banyak sekali senyawa–senyawa yang menunjukkan aktivitas terhadap sel P388. setelah diketahui bahwa suatu zat aktif pada penapisan awal maka diuji lebih lanjut terhadap sel kanker yang lebih spesifik yaitu suatu panel uji sel tumor tikus baik secara invitro maupun secara in vivo dan selanjutnya di uji lagi dengan sel xenograft tumor manusia. Sel tumor tikus yang biasa digunakan untuk panel uji tersebut adalah lini sel L1210, sel Melanoma B16, sel tumor payudara CDFI, sel kanker paru–paru, dan
besar CX-1, sel tumor paru–paru LX-1, sel tumor payudara MX-1 (Suffnes dan Pezzuto, 1991).
Penentuan dapat atau tidaknya suatu zat dikembangkan sebagai obat anti kanker didasarkan pada sifat toksisitasnya. NCI telah menetapkan kriteria aktivitas berdasarkan nilai Inhibisy Concentartion 50 (IC50) yaitu konsentrasi yang dibutuhkan
untuk menghambat pertumbuhan sel sebesar 50%. Suatu zat disebut bersifat sitotoksik bila aktivitas terhadap sel uji mempunyai nilai IC50 < 20 g/mL untuk
suatu ekstrak, dan nilai IC50 < 4 g/mL untuk senyawa murni (Suffnes dan Pezzuto,
1991).
Selain IC50 untuk menentukan sifat sitotoksik suatu zat digunakan juga ukuran
lain yaitu ED50 yaitu dosis yang efektif untuk menghambat pertumbuhan sel sebesar
50%. Setelah lolos dari uji penapisan awal selanjutnya dilakukan uji toksikologi pra klinis dan farmakologis melalui pengujian secara in vivo dengan beberapa sistem tumor hewan yang dapat di transplantasikan dan telah ditentukan sifat–sifatnya pada hewan percobaan.
Kriteria yang ditetapkan pada hewan percobaan adalah berdasarkan nilai LD50
(mg/Kg) yaitu dosis yang dapat menyebabkan kematian hewan percobaan sebesar 50%. Senyawa yang memberikan harapan yaitu senyawa yang tidak mempunyai toksisitas berlebihan dilanjutkan ke uji coba klinik fase I yaitu penelitian jaringan tempat efek toksik dan farmakologinya pada pasien kanker stadium lanjut. Konsentrasi awal yang dianggap aman untuk digunakan pada manusia adalah konsentrasi dengan nilai LD10 pada hewan percobaan. Seterusnya dilakukan uji coba
2.7 Metode Penentuan Struktur Kimia
Spektrofotometri adalah pengukuran serapan/emisi radiasi elektromagnetik pada panjang gelombang tertentu yang monokromatis dari suatu zat baik dalam bentuk molekul atau atom. Spektrum biasanya diperoleh dengan melewatkan cahaya dengan panjang gelombang tertentu melalui larutan encer suatu senyawa dalam pelarut yang sesuai serta tidak menggangu penyerapan, misalnya air atau etanol (Silverstein, et al., 1981).
Untuk menentukan struktur kimia suatu senyawa dapat digunakan metode spektroskopi seperti Spektrofotometri UV-Vis, Spektrofotometri Fourier-Transform Infra Red (FT-IR), Spektrometri Resonansi Magnetik Inti (RMI), dan Spektrometri Massa.
2.7.1 Spektrofotometri UV-Vis
Pengukuran serapan dapat dilakukan pada daerah ultraviolet dengan panjang gelombang 190 nm - 380 nm atau daerah cahaya tampak dengan panjang gelombang 380 nm - 780 nm. Semua molekul dapat mengabsorbsi radiasi dalam daerah UV-Vis karena mengandung elektron yang dapat dieksitasi ke tingkat energi yang lebih tinggi.
Senyawa yang hanya mengandung ikatan sigma (σ) seperti pada ikatan tunggal C-C akan tereksitasi pada panjang gelombang sangat pendek dibawah 150 nm berada di luar daerah ukur spektrofotometer sehingga tidak akan menimbulkan
serapan. Senyawa memiliki elektron phi (π) (mempunyai ikatan rangkap) dan
mempunyai pasangan elektron bebas lebih mudah tereksitasi dan menyerap pada panjang gelombang yang lebih tinggi sehingga menimbulkan serapan pada spektrofotometer.
2.7.2 Spektrofotometri Inframerah
Daerah radiasi spektrofotometri inframerah berada pada bilangan panjang gelombang 12800-10 cm-1. Umumnya daerah radiasi IR terbagi dalam IR dekat (12800-4000 cm-1; 3,8-12 x 1014 Hz; 0,78-2,5 mikrometer), daerah IR tengah (4000-200 cm-1; 0,012-6 x 104 Hz; 2,5-50 mikrometer), daerah IR jauh (200-10 cm-1; 60-3 x 1011 Hz;50-1000 mikrometer). Daerah yang paling banyak digunakan untuk berbagai keperluan praktis adalah 4000-690 cm-1 yang biasa disebut sebagai daerah IR tengah (Silverstein, et al., 1981).
Spektrofotometri inframerah mempunyai dua macam instrumen yaitu:
a. Spektrofotometer infra merah dispersif, adalah spektrofotometri yang menggunakan monokromator untuk memisahkan frekuensi individu yang melewati sampel sehingga absorbsi dari masing-masing frekuensi dapat diukur. b. Spektrofotometer Fourier-transform, adalah spektrofotometri yang dalam
instrumennya tidak dipisahkan radiasinya, tetapi hampir semua panjang gelombang mencapai detektor secara bersamaan yang disebut Fourier-transform, yang digunakan untuk mengubah hasil spektrum infra merah menjadi khas. Yang digunakan sebagai pengganti monokromator adalah interferometer yang dapat memisahkan radiasi menjadi dua bagian dan menghubungkannya kembali sehingga variasi intensitas yang keluar dapat diukur sekali. Beberapa keuntungan spektrofotometer Fourier-transform dibandingkan dengan spektrofotometer dispersif adalah menghasilkan spektrum yang lebih cepat, resolusi yang lebih baik, dapat mengukur sampel dalam jumlah yang sangat sedikit (Silverstein, et al., 1981).
2.7.3 Spektrometri Resonansi Magnetik Inti (RMI)
momen magnet tidak sama dengan nol. Diantara inti-inti atom tersebut adalah proton (1H), inti fluor (19F), isotop nitrogen, dan banyak yang lain. Inti karbon (12C) yang sangat penting dalam kimia organik tidak memiliki momen magnet sehingga studi RMI dengan karbon hanya terbatas pada isotop 13C. Pelarut yang biasa dipakai adalah deuterokloroform (CDCl3), karbon tetraklorida (CCl4), dan deuterium oksida (D2O)
(Silverstein, et al., 1981).
RMI yang memberikan informasi yang berguna dalam penentuan struktur yaitu RMI 1 dimensi terdiri dari RMI proton (1H), RMI karbon (13C), DEPT (Distortionless Enhancement by Polarization Transfer).
a. RMI Proton
Prinsip RMI proton adalah inti atom hidrogen mempunyai sifat-sifat magnet, bila suatu senyawa mengandung hidrogen diletakkan dalam bidang magnet yang sangat kuat dan diradiasi menggunakan radiasi elektromagnetik maka inti atom hidrogen dari senyawa tersebut akan menyerap energi melalui suatu proses absorpsi yang dikenal dengan resonansi magnet. Tidak semua proton menyerap energi pada kekuatan medan magnet yang sama, karena proton-proton dilindungi dari medan magnet oleh elektron yang mengelilinginya. Makin besar densitas elektron yang mengelilingi proton maka makin besar medan magnet yang dihasilkan. Densitas elektron dipengaruhi oleh ada atau tidaknya atom yang mempunyai elektronegatifitas tinggi (Silverstein, et al., 1981).
b. RMI Karbon dan DEPT
Spektrum RMI karbon dan DEPT memberikan informasi jenis atom karbon primer (CH3), sekunder (CH2), tersier (CH), dan kuartener (C). DEPT (Distortionless
Enhancement by Polarization Transfer) merupakan salah satu tipe spektra RMI karbon yang memberikan informasi jumlah karbon dari CH3, CH2, CH dan C yang
diukur berdasarkan sudut pengukuran RMI karbon. Hasil penelitian DEPT pada sudut 135° menunjukkan bahwa sinyal karbon CH3 dan CH mengarah ke atas, sedangkan
CH2 mengarah ke bawah. Untuk mengetahui perbedaan CH3 dan CH dilakukan
c. RMI 2 Dimensi (COSY, HMQC, dan HMBC)
Spektrum RMI 2 dimensi seperti spektra dari COSY (Correlation Sepectroscopy); HMQC (Hetero Multiple Quantum Connetivity) dan HMBC (Hetero Multiple Bond Connetivity) adalah spektra turunan dari RMI 1 dimensio (proton dan karbon). COSY dapat diturunkan dari spektra RMI proton saja, sedangkan HMQC dan HMBC diturunkan dari spektra RMI proton dan karbon. COSY berguna untuk melihat korelasi antara proton dengan proton; HMQC untuk melihat korelasi antara proton dengan karbon pada ikatan geminal saja, sedangkan HMBC adalah korelasi di antara proton dengan karbon sampai 2 – 3 ikatan (Schraml, 1990).
2.7.4 Kromatografi Cair - Spektrometri Massa (KC-SM)