i BAB III DASAR TEORI
3.1 Jamur Kerak (Lichenes)
Jamur Kerak atau lichenes merupakan organisme komposit yang terdiri dari ganggang atau sianobakterium dan jamur (fungi) yang tumbuh bersama dalam simbiosis (hidup bersama antara dua atau lebih organisme). Biasanya disepakati bahwa asosiasi ini adalah mutualisme, yakni setiap pihak mendapat keuntungan. Ganggang menyediakan makanan bagi jamur (fungi) terutama karbohidrat yang dihasilkan dari fotosintesis. Jamur menyerap, menyimpan, menyediakan air dan mineral yang diperlukan oleh rekan fotosintetiknya, juga menyediakan suatu kerangka yang protektif dan menunjang. Jamur mampu memperoleh makanan dari ganggang dengan bantuan tonjolan-tonjolan renik seperti akar yang dinamakan houstarium yang menembus sel fotosintetiknya (Michael, 2007). Bagian–bagian penyusun Lichenes dapat dilihat pada Gambar 3.
ii
Jamur Kerak (Lichenes) tersebar luas di alam, tumbuh pada batu (Gambar 4), pohon dan substrat yang biasanya kurang baik bagi pertumbuhan tanaman. Banyak Jamur Kerak (lichenes) resisten terhadap temperatur yang ekstrim dan karena itu mampu hidup pada suhu rendah ke suhu yang tinggi seperti di lingkungan kutub. Akibatnya lichenes misalnya lumut rusa kutub, merupakan sumber makanan di daerah Arktrik. Lichenes tahan masa kekeringan yang lama (Michael, 2007).
Gambar 4. Lichenes pada batu candi
3.1.1 Klasifikasi Jamur Kerak (Lichenes)
Ada dua jenis Jamur Kerak (Lichenes), foliose (seperti daun) dan fruktikose (seperti rumpun). Lichenes foliase tumbuh sangat rapat pada substratum atau bahkan di dalam permukaannya. Lichenes fruktikose berbentuk rumpun yang tegak dan dapat mencapai ketinggian 10 cm (Michael, 2007).
iii
Lichenes sangat sulit untuk diklasifikasikan karena merupakan gabungan dari ganggang (algae) dan jamur (fungi) serta sejarah perkembangan yang berbeda. Lichenes diletakkan dalam ordo Leocanorales dari Ascomycetes (Bessey, 1979). Lichenes terkelompokkan dalam kelompok yang terpisah yang berbeda dari ganggang (algae) dan jamur (fungi) (Smith,1955). Lichenes memiliki klasifikasi yang bervariasi dan dasar dasar klasifikasinya secara umum adalah sebagai berikut :
1. Klasifikasi berdasarkan komponen jamur yang menyusunnya
A. Ascolichens
Jamur penyusunnya tergolong Pyrenomycetales, maka tubuh buah yang dihasilkan berupa peritesium, contoh: Dermatocarpon dan verrucaria jamur penyusunnya tergolong discomycetes. Lichenes membentuk tubuh buah berupa apothecium yang berumur panjang. Contoh: Usnea dan Parmelia alam klas Ascolichens ini dibangun juga oleh komponen ganggang dari famili: Mycophyceae dan Chlorophyceae yang bentuknya berupa gelatin. Genus dari Mycophyceae
adalah: Scytonema, Nostoc, Rivularia, Gleocapsa dan lain-lain. Dari
Cholophyceae adalah Protococcus, Trentopohlia, Cladophora. B. Basidiolichenes
Jamur yang berasal dari jamur Basidiomycetes dan ganggang
Mycophyceae. Basidiomycetes yaitu dari famili: Thelephoraceae, dengan tiga genus Cora, Corella dan Dyctionema. Mycophyceae berupa filamen yaitu: Scytonema dan tidak berbentuk filamen yaitu Chrococcus.
iv
Deutromycetes fungi, steril. Contoh: Cystocoleus, Lepraria, Leprocanlon, Normandia.
2. Klasifikasi berdasarkan ganggang yang menyusun thalus A. Homoimerus
Sel ganggang dan hifa jamur tersebar merata pada thallus. Komponen ganggang mendominasi dengan bentuk seperti gelatin, termasuk dalam Mycophyceae. Contoh: Ephebe, Collema Collema coccophorum.
B. Heteromerous
Sel ganggang terbentuk terbatas pada bagian atas thallus dan komponen
jamur menyebabkan terbentuknya thallus, ganggang tidak berupa gelatin
Chlorophyceae. Contoh: Parmelia.
3. Klasifikasi berdasarkan type thallus dan kejadiannya A. Crustose atau Crustaceous
Merupakan lapisan kerak atau kulit yang tipis di atas batu, tanah atau kulit pohon, seperti Rhizocarponpada batu, Lecanora dan Gaphis pada kulit kayu. Mereka terlihat sedikit berbeda antara bagian permukaan atas dan bawah. Rhizocarpon geogaphicum, Lecanora argopholis.
B. Fruticose atau filamentous
Lichenes semak, seperti silinder rata atau seperti pita dengan beberapa bagian menempel pada bagian dasar atau permukaan. Thallus bervariasi, ada yang pendek dan panjang, rata, silindris, seperti janggut, benang yang menggantung atau berdiri tegak. Bentuk yang seperti telinga tipis yaitu Ramalina. Panjang
v
menggantung seperti Usneadan alectoria. Cladonia adalah tipe antara kedua bentuk itu.
3.1.2 Morfologi Lichenes a. Morfologi luar
Tubuh Lichenes dinamakan thallus yang secara vegetatif mempunyai kemiripan dengan ganggang dan jamur. Thallus ini berwarna abu atau abu-abu kehijauan. Beberapa spesies ada yang berwarna kuning, oranye, coklat atau merah dengan habitat yang bervariasi. Bagian tubuh yang memanjang secara selluler dinamakan hifa. Hifa merupakan organ vegetatif dari thallus atau miselium yang biasanya tidak dikenal pada jamur yang bukan lichenes. Ganggang selalu berada pada bagian permukaan dari thallus. Berdasarkan bentuknya lichenes dibedakan atas empat bentuk:
a. Crustose
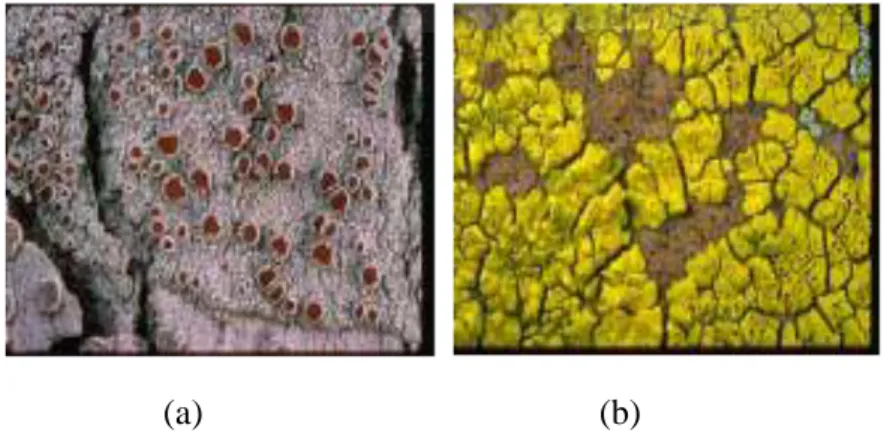
Lichenes yang memiliki thallus yang berukuran kecil, datar, tipis dan selalu melekat ke permukaan batu, kulit pohon atau di tanah. Jenis ini susah untuk mencabutnya tanpa merusak substratnya. Contoh: Gaphis scipta, Haematomma puniceum, Acarospora atau Pleopsidium, yang ditunjukkan pada Gambar 5.
(a) (b)
vi
LichenesCrustose yang ditunjukkan pada Gambar 6, tumbuh terbenam di dalam batu hanya bagian tubuh buahnya yang berada di permukaan disebut endolitik, dan yang tumbuh terbenam pada jaringan tumbuhan disebut endoploidik atau endoploidal. Lichenes yang longgar dan bertepung yang tidak memiliki struktur berlapis, disebut leprose.
Gambar 6. Caloplaca luteominea subspesies bolanderi (Lichenes endolitik)
b. Foliose
Lichenes foliose memiliki struktur seperti daun yang tersusun oleh lobuslobus. Lichenes ini relatif lebih longgar melekat pada substratnya. Thallusnya datar, lebar, banyak lekukan seperti daun yang mengkerut berputar. Bagian permukaan atas dan bawah berbeda. Lichenes ini melekat pada batu, ranting dengan rhizines. Rhizines ini juga berfungsi sebagai alat untuk
mengabsorbsi makanan. Contoh: Xantoria, Physcia, Peltigera, Parmelia,
vii
.
(a) (b)
.
(c) (d)
Gambar7. Lichenes jenis foliose. a). Xantoria elegans, b). Physcia aipolia, c). Peltigera malacea d). Parmelia sulcata
c. Fruticose
Thallusnya berupa semak dan memiliki banyak cabang dengan bentuk seperti pita. Thallus tumbuh tegak atau menggantung pada batu, daun-daunan atau cabang pohon. Tidak terdapat perbedaan antara permukaan atas dan bawah. Contoh : Usnea, Ramalina dan Cladonia.
(a) (b) (c) Gambar 8. Lichenes jenis Fruticose
viii
Lichenes ini memiliki lobus-lobus seperti sisik, lobus ini disebut squamulus yang biasanya berukuran kecil dan saling bertindih dan sering memiliki struktur tubuh buah yang disebut podetia (Yurnaliza,2002).
(a) (b)
Gambar 9. a). Psora pseudorusselli, b). Cladonia carneola
b. Morfologi dalam (Anatomi)
Struktur morfologi dalam diwakili oleh jenis foliose, karena jenis ini mempunyai empat bagian tubuh yang dapat diamati secara jelas yaitu :
a). Korteks atas
Korteks atas berupa jalinan yang padat disebut pseudoparenchyma dari hifa jamurnya. Sel ini saling mengisi dengan material yang berupa gelatin. Bagian ini tebal dan berguna untuk perlindungan.
b). Daerah ganggang
Daerah ganggang merupakan lapisan biru atau biru hijau yang terletak di bawah korteks atas. Bagian ini terdiri dari jalinan hifa yang longgar. Diantara hifa-hifa itu terdapat sel-sel hijau, yaitu Gleocapsa, Nostoc, Rivularia dan Chrorella. Lapisan thallus untuk tempat fotosintesa disebut lapisan gonidial sebagai organ reproduksi.
ix c). Medulla
Medulla terdiri dari lapisan hifa yang berjalinan membentuk suatu bagian tengah yang luas dan longgar. Hifa jamur pada bagian ini tersebar kesegala arah dan biasanya mempunyai dinding yang tebal. Hifa pada bagian yang lebih dalam lagi tersebar di sepanjang sumbu yang tebal pada bagian atas dan tipis pada bagian ujungnya. Dengan demikian lapisan tadi membentuk suatu untaian hubungan antara dua pembuluh.
d). Korteks bawah
Korteks bawah lapisan ini terdiri dari struktur hifa yang sangat padat dan membentang secara vertikal terhadap permukaan thallus atau sejajar dengan kulit bagian luar. Korteks bawah ini sering berupa sebuah akar (rhizines). Ada beberapa jenis lichenes tidak mempunyai korteks bawah. Bagian ini digantikan oleh lembaran tipis yang terdiri dari hypothallus yang fungsinya sebagai proteksi. Dari potongan melintang Physcia sp, terlihat lapisan hijau sel-sel ganggang dan rhizines coklat bercabang pada bagian bawah. Bagian tengah yang berwarna putih terdiri dari sel-sel jaringan jamur yang disebut medulla. Struktur pipih pada bagian atas dan kanan disebut apothecia dan lapisan coklat di atasnya disusun oleh asci, yaitu bagian dari ascomycete yang megandung spora jamur.
3.1.3 Ganggang Pada Lichenes
Sel-sel ganggang (algae) yang terjalin di dalam miselium jamur saling berinteraksi membentuk kehidupan simbiosis mutualisme dimana. Ganggang (algae) mampu menyediakan makanan untuk jamur. Ganggang biru (algae) dapat memfiksasi nitrogen bebas, kemudian menyediakan nitrogen organik untuk jamur.
x
Sementara itu, jamur dapat memberikan lingkungan dan perlindungan untuk kehidupan ganggang. Susunan hifa jamur memungkinkan terjadinya pertukaran udara menahan air dan garam-garam mineral, serta melindungi ganggang dari sengatan cahaya matahari.
Ganggang (algae) merupakan tumbuhan bertalus, yang belum dapat
dibedakan antara batang, akar, dan daun, serta selalu menempati habitat yang lembab dan basah (Tjitrosoepomo, 2005). Kelembaban sedikit saja akan memacu pertumbuhannya. Ganggang (algae) merupakan jenis jasad renik fotosintesis dimana adanya sinar matahari baik secara langsung maupun tidak (sinar difus) sangat diperlukan dalam proses metabolismenya. Proses fotosintesis akan terbentuk sejumlah besar bahan organik dimana sebagian dari mineral-mineral yang diperlukan diambil dari batuan tempatnya melekat. Ganggang(algae) cukup menduduki suatu bagian penting dan berpengaruh sebagai salah satu agensia pelapuk batuan secara biotis. Organisme photoautotroph mempunyai peranan di alam. Ganggang (algae) termasuk jasad tingkat rendah yang belum mempunyai diferensiasi jaringan sehingga dapat menggunakan energi cahaya matahari dalam sintesa bahan-bahan organik. Dilihat dari segi taxonomi, ganggang (algae) dapat digolongkan ganggang eukariotik dan ganggang prokariotik (Sadirin, 1998).
Beberapa ganggang (algae) teradaptasi pada tanah lembab, pepagan pohon, dan bahkan permukaan batuan, yang didegadasikan oleh ganggang (algae), sehingga menjadikan produk-produk dekomposisinya tersedia untuk
membangun dan memperkaya tanah. Ganggang (algae) adalah organime aerobik
fotosintetik, dijumpai dimana saja yang tersedia cukup cahaya, kelembapan, dan nutrient sederhana untuk memperpanjang hidupnya (Michael, 2007).
xi 3.2 Minyak Atsiri
3.2.1 Deskripsi minyak atsiri
Gambar 10. Minyak atsiri daun sereh
Secara umum sereh dibagi menjadi 2 jenis, yaitu sereh dapur (lemongass) dan sereh wangi (sitronela). Keduanya memiliki aroma yang berbeda. Minyak atsiri daun sereh yang selama ini dikenal di Indonesia merupakan minyak atsiri daun sereh wangi (citronella oil) yang biasanya terdapat dalam komposisi minyak tawon dan minyak gandapura. Minyak atsiri daun sereh wangi telah dikembangkan di Indonesia dan minyak atsirinya sudah diproduksi secara komersial dan termasuk komoditas ekspor. Sedangkan minyak atsiri daun sereh dapur (lemongass oil) belum pernah diusahakan secara komersial. Dari segi komposisi kimianya, keduanya memiliki komponen utama yang berbeda. Sereh wangi kandungan utamanya adalah citronella, sedangkan sereh dapur adalah sitral. Sereh dapur terbagi menjadi 2 varitas, yaitu sereh flexuosus (Cymbopogon flexuosus) dan sereh dapur (Cymbopogon citratus). Dalam dunia perdagangan minyak atsiri, minyak atsiri daun sereh flexuosus disebut sebagai East Indian lemongass oil (minyak atsiri daun sereh dapur India Timur). Sedangkan sereh
xii
dapur dikenal dengan West Indian lemongass oil (minyak atsiri daun sereh dapur India Barat). Keduanya dapat tumbuh subur di Indonesia meskipun yang terbanyak adalah jenis West Indian. Perbedaan yang sangat jelas dari keduanya terletak pada sifat-sifat minyak atsiri yang dihasilkan. Minyak atsiri daun sereh India Timur lebih berharga dari pada India Barat, terutama karena kandungan sitronelanya yang lebih tinggi.
Klasifikasi tanaman sereh :
Kingdom : Plantae Divisi : Anthophyta Filum : Angiospermae Kelas : Monocotyledonae Famili : Gaminae Genus : Cymbopogon
Species : Cymbopogon nardus
(Nukete, 2008).
3.2.2 Cara memperoleh minyak atsiri
Perlakuan pendahuluan terhadap bahan yang mengandung minyak atsiri umumnya dapat dilakukan dengan beberapa cara, yaitu dengan cara pengecilan ukuran bahan, pengeringan atau fermentasi oleh mikroorganisme. Adapun cara memperoleh minyak atsiri bisa dengan melalui proses destilasi. Menurut Guanther (1987) metode destilasi minyak atsiri ada tiga macam, yaitu :
xiii 1). Destilasi dengan air (Water Distillation)
Metode destilasi dengan air (hidrodestilasi), bahan yang akan didestilasi dikontak langsung dengan air mendidih. Bahan tersebut mengapung di atas air atau terendam secara sempurna, tergantung dari berat jenis dan jumlah bahan yang didestilasi. Peristiwa pokok yang terjadi pada proses hidrodestilasi yaitu : difusi minyak atsiri dan air panas melalui membran tanaman, hidrolisa terhadap beberapa komponen minyak atsiri dan dekomposisi yang disebabkan oleh panas. Kecepatan penguapan minyak atsiri dalam proses hidrodestilasi bahan tidak dipengaruhi oleh sifat mudah menguapnya komponen-kompenen minyak atsiri, melainkan lebih banyak oleh derajat kelarutannya dalam air.
2). Destilasi dengan air dan uap (Water and Steam Distillation)
Pada metode destilasi air dan uap, bahan diletakkan di atas saringan berlubang. Ketel suling diisi dengan air sampai permukaan air berada tidak jauh di bawah saringan. Air dapat dipanaskan dengan berbagai cara yaitu dengan uap jenuh yang basah dan bertekanan rendah. Ciri khas metode ini adalah uap selalu dalam keadaan basah, jenuh dan tidak terlalu panas.
3). Destilasi dengan uap (Steam Distillation)
Metode ini pada prinsipnya sama dengan destilasi dengan air dan uap kecuali air tidak diisikan dalam labu. Uap yang digunakan uap jenuh atau kelewat panas pada tekanan lebih dari pada 1 atmosfir. Uap dialihkan melalui pipa uap berlingkar yang berpori yang terletak dibawah bahan dan uap bergerak ke atas melalui bahan yang terletak di atas saringan. Peralatan pada metode destilasi dengan air (hidrodestilasi) pada umumnya terdiri dari 3 bagian utama. Tiga bagian utama tersebut adalah alat penyulingan, pendingin dan penampung kondensat.
xiv
Alat penyulingan berfungsi sebagai tempat bahan tanaman yang akan diproses. Dalam alat ini terdapat air yang berhubungan langsung dengan bahan tanaman dan menguapkan minyak atsiri yang dikandungnya. Pendingin berfungsi mengubah uap uap air yang mengandung uap minyak atsiri menjadi cairan. Penampung kondensat berfungsi untuk memisahkan minyak atsiri dari air yang terkondensasi secara sempurna. Kondensat mengalir dari pendingin ke penampung kondensat dan akan terlihat minyak atsiri yang dihasilkan akan terpisah dari air dengan sendirinya, karena berat jenis minyak atsiri lebih ringan dari pada air (Sastrohamidjojo, 2004). Prinsip kerja destilasi Stahl sama dengan destilasi dengan air (hidrodestilasi). Namun destilasi Stahl memiliki beberapa kelebihan. Kelebihan penggunaan destilasi Stahl antara lain:
a). Minyak atsiri yang dihasilkan tidak berhubungan langsung dengan udara luar sehingga tidak mudah menguap.
b). Volume minyak atsiri yang dihasilkan dapat langsung diketahui jumlahnya karena alatnya dilengkapi dengan skala.
xv 3.2.3 Kandungan minyak atsiri
Minyak atsiri mengandung dua golongan, yaitu oleopeptana dan
tearoptena. Oleoptena adalah bagian hidrokarbon di dalam minyak atsiri dan berwujud cairan. Sedangkan stearoptena umumnya terdiri atas senyawa turunan oksigen dari terpena. Secara kimiawi, minyak atiri tersusun dari campuran yang rumit berbagai senyawa dan senyawa tertentu biasanya menentukan aroma minyak atsiri. Sebagian besar komponen minyak atsiri termasuk dalam golongan senyawa organik terpenoid yang bersifat larut dalam minyak.
Beragamnya senyawa yang menyusun komponen minyak atsiri sehingga menghasilkan bau, aroma dan dapat digunakan sebagai obat. Klasifikasi minyak atsiri harus berdasarkan pada komponen yang paling dominan dalam menentukan sifat minyak tersebut. Jika minyak atsiri memiliki kandungan oleoptena dalam jumlah besar dan stearoptena dalam porsi kecil, maka kegunaannya lebih diutamakan sebagai pemberi bau yang spesifik atau peracah (flavoring). Sedangkan jika minyak atsiri mengandung lebih banyak senyawa golongan hidrokarbon, alkohol, keton, fenol, ester dari fenol, oksida dan ester, lebih memungkinkan untuk digunakan sebagai obat, karena secara teori diketahui bahwa semua senyawa itu memiliki gugus aktif yang berfungsi melawan suatu jenis penyakit (Sastrohamidjojo, 2004).
3.2.4 Manfaat minyak atsiri
Umumnya minyak atsiri memiliki bau yang khas sehingga dimanfaatkan pada industri parfum dan makanan (flavoring agent). Senyawa yang berperan pada industri tersebut diantaranya sitronela, geraniol dan eugenol. Selain itu ada
xvi
beberapa tumbuhan penghasil minyak atsiri yang bersifat aktif biologis sebagai antibakteri dan antijamur sehingga dapat dipergunakan sebagai bahan pengawet pada makanan dan sebagai antibiotik alami. Senyawa yang bersifat antibakteri diantaranya eugenol, linalool dan sitral (Knobloch et al.,1989).
3.2.5 Minyak atsiri daun sereh
a. Deskripsi minyak atsiri daun sereh
Dalam perdagangan dikenal dua tipe minyak atsiri daun sereh yaitu, tipe Ceylon dan tipe jawa. Tipe yang pertama diperoleh dengan cara mendestilasi daun dari Cymbopogon nardus Rendle di Ceylon atau disebut lenabatu, sedangkan tipe yang kedua diperoleh dari Cymbopogon winterianus Jowitt di Jawa disebut mahapengiri. Sesuai dengan Indian Standar Institute (I.S. 512-1954), minyak atsiri daun sereh tipe Ceylon mengandung 55-5% total alkohol, dihitung sebagai sitronela. Sedangkan minyak tipe Jawa mengandung 35-97% total alkohol, dihitung sebagai geraniol dan 34-45% total aldehide, dihitung sebagai sitronela (Sastrohamidjojo, 2004).
Minyak atsiri daun sereh diperoleh dengan cara menyuling daun sereh sehingga dihasilkan minyak atsiri daun sereh, dimana diperlukan beberapa perlakuan antara lain perajangan menjadi potongan–potongan kecil. Proses perajangan ini bertujuan agar kelenjar minyak dapat keluar sebanyak mungkin yang terkandung dalam tanaman tersebut dapat dibebaskan atau untuk memudahkan penguapan minyak atsiri dari bahan. Minyak yang sudah dibebaskan tersebut dapat segera dipisahkan dari tanaman dengan cara penguapan. Selain perajangan, akan terjadi penguapan komponen minyak bertitik didih rendah. Oleh
xvii
karena itu jika diinginkan rendemen mutu minyak yang baik, maka perajangan harus segera dimasukkan ke dalam alat penyulingan (Hapsari, 2008).
Adapun proses penyulingan menggunakan cara destilasi uap air. Bagian tanaman yang akan diproses secara penyulingan air dan uap ditempatkan dalam suatu tempat yang bagian bawah dan tengah berlubang-lubang yang ditompang diatas dasar alat penyulingan. Bagian bawah alat penyulingan diisi air sedikit dibawah dimana bahan ditempatkan, kemudian air dipanaskan dengan api. Pada proses ini penulis menggunakan pemanasan dengan kompor minyak tanah yang ditekan. Bahan tanaman yang akan disuling hanya terkena uap, dan tidak terkena air yang mendidih (Sastrohamidjojo, 2004).
(a) (b) Gambar 12. a). Tanaman sereh wangi, b). Minyak atsiri daun sereh
b. Standar mutu minyak atsiri daun sereh wangi.
Tabel 1. Karakteristik minyak atsiri daun sereh wangi dan syarat mutu SNI 06-3953-1995 N o Parameter SNI 06-3953-1995 1 Berat jenis 20 oC (g/cm3) 0.880-0.922 2 Viskositas (cP) - 3 Indeks bias (20 oC) 1,466-1,475 4 Bilangan ester -
5 Total geraniol (%) Min 85
xviii 3.3 Kromatogafi Gas
Kromatogafi gas adalah suatu metode pemisahan campuran yang terdiri dari dua macam komponen atau lebih, yang didasarkan pada distribusi diferensiall diantara dua fasa yaitu fasa diam yang berupa padatan atau cairan dan fasa gerak yang berupa gas (Sastrohamidjojo, 1985).
3.3.1 Bagian-Bagian Kromatogafi Gas 1. Gas pengangkut
Gas pengangkut (carrier gas) ditempatkan dalam silinder bertekanan tinggi. Biasanya tekanan dari silinder sebesar 150 atm. Tetapi tekanan ini sangat besar untuk digunakan secara langsung. Gas pengangkut harus memenuhi persyaratan-persyaratan:
a. Harus inert, tidak bereaksi dengan cuplikan cuplikan-pelarut dan material dalam kolom.
b. Murni dan mudah diperoleh serta murah.
c. Sesuai atau cocok untuk detektor.
Gas-gas yang sering dipakai adalah Helium atau Argon. Gas tersebut sangat baik tidak mudah terbakar, tetapi sangat mahal. Konduktivitas panas gas-gas tersebut tinggi dan molekulnya kecil. Berdasarkan faktor ekonomi H2 dan N2
digunakan sebagai gas pengangkut. H2 mudah terbakar sehingga dalam
xix 2. Pengatur aliran dan pengatur tekanan
Pengatur aliran dan pengatur tekanan disebut dengan Drager. Drager bekerja baik pada 2,5 atm dan mengalirkan massa aliran dengan tetap. Tekanan lebih baik pada tempat masuk dari kolom diperlukan untuk mengairkan cuplikan masuk ke dalam kolom. Ini disebabkan kenyataan lubang akhir dari kolom biasanya mempunyai tekanan atmosfir biasa, dimana suhu kolom yang diatur oleh thermostat akan tetap, maka aliran gas yang masuk kolom akan tetap juga. Komponen-komponen akan dielusikan pada waktu yang tetap yang disebut waktu penahanan (the retention time/tR). Kecepatan gas yang tetap, maka komponen juga
mempunyai volume karakteristik terhadap gas pengangkut=volume penahanan (the retention volume/VR)
3.Tempat Injeksi (The Injection Port)
Dalam pemisahan dengan GLC, cuplikan harus dalam bentuk fasa uap. Gas dan uap dapat dimasukkan secara langsung. Tetapi kebanyakan senyawa organik berbentuk cairan dan padatan. Senyawa yang berbentuk cairan dan padatan pertama-tama harus diuapkan terlebih dahulu. Ini membutuhkan pemanasan sebelum masuk dalam kolom. Panas itu terdapat pada tempat injeksi.
Tempat injeksi dari alat GLC selalu dipanaskan. Dalam kebanyakan alat suhu dari tempat injeksi dapat diatur. Aturan pertama untuk mengatur suhu ini adalah bahwa suhu tempat injeksi sekitar 50 oC lebih tingi dari tittik didih campuran dari cuplikan yang mempunyai titik didih yang paling tinggi. Bila kita tidak mengetahui titik didih komponen dari cuplikan maka kita harus mencoba-coba. Sebagai tindak lanjut suhu dari tempat injeksi dinaikkan. Jika
puncak-xx
puncak yang diperoleh lebih baik. Namun demikian suhu tempat injeksi tidak boleh terlalu tinggi, sebab kemungkinan akan terjadi perubahan karena panas atau peruraian dari senyawa yang akan dianalisis.
1. Kolom
Kolom merupakan jantung dari kromatogafi gas. Bentuk dari kolom dapat diluruskan, dibengkokkan, misal berbentuk V atau W dan kumparan atau spiral. Biasanya bentuk dari kolom adalah kumparan. Kolom selalu merupakan bentuk tabung. Tabung ini dapat terbuat dari tembaga, plastik (teflon), baja (stainless steel), aluminium dan gelas.
Isi kolom dapat berupa padatan pendukung yang berfungsi mengikat fasa diam, kebanyakan berupa zat diatomik yang telah dipanaskan atau dikeringkan. Diatomite terdiri dari satuan ganggang bersel satu atau diatom yang poti-porinya sangat kecil. Luas permukaan daris truktur berpori sekitar 20m/g. Luas permukaan yang besar ini dibutuhkan untuk mendistribusi fasa diam yang bersifat cairan dalam GLC. Syarat padatan pendukung yang baik adalah inert, kuat, stabil dalam suhu yang tinggi, permukaan yang terarur dan harus mempunyai tahanan yang rendah terhadap gas pengangkut.
Fasa diam dalam GLC berupa cairan. Pada fasa cairan inilah pemisahan komponen-komponen dari cuplikan terjadi. Dasar kerja adalah partisipasi antara cairan dan fasa gerak (gas) (Sastrohamidjojo, 2007).
2. Detektor
Pada detektor komponen-komponen cuplikan yang telah terpisah diddeteksi, ini menunjukkan bahwa karakteristik dari senyawa-senyawa organik diukur. Saat
xxi
ini telah ada 3 jenis detektor yang dapat digunakan untuk mendeteksi senyawa-senyawa organik yang diukur berdasarkan perbedaan sifat-sifat molekul, meskipun demikian hanya hanya ada dua detektor yang dijelaskan:
a. Detektor hantaran panas (The Thermal Conductivity Detector=TCD)
b. Detektor ionisasi nyala (The flame ionisation detector= FID)
Detektor mengubah sejumlah sifat-sifat molekul dari senyawa organik menjadi arus listrik, arus ini akan diteruskan ke pencatat untuk menghasikan kromatogam (Sastrohamidjojo, 2007).
3.4. Kromatogafi Gas-Spektofotometri Massa
Kromatogafi Gas-Spektofotometri Massa (KG-MS) merupakan gabungan antara alat kromatogafi gas dan spektroskopi mass. Alat kromatogafi gas memiliki fungsi untuk memisahkan komponen-komponen senyawa kimia yang dianalisis sedangkan spektroskopi massa digunakan untuk mendeteksi dari masing-masing senyawa kimia yang telah dipisahkan oleh alat kromatogafi gas. Jadi pada prinsipnya alat spektroskopi massa berperan sebagai detektor. Setiap molekul yang dideteksi dengan spektroskopi massa dapat ditentukan pola fragmentasinya. Salah satu aplikasi dari penggunaan alat KG-MS adalah untuk menentukan komponen-komponen senyawa kimia yang terdapat didalam minyak atsiri.
Kromatogafi gas berfungsi sebagai alat pemisah berbagai komponen campuran dalam sampel sedangkan spektrofotometer massa berfungsi untuk mendeteksi masing-masing komponen yang telah dipisahkan pada sistem kromatogai gas. Spektrofotometer massa merupakan alat analisis yang mempunyai kemampuan aplikasi yang paling luas yang dapat dipergunakan untuk
xxii
memperoleh informasi mengenai komposisi sampel dasar dari suatu bahan, struktur dari molekul anorganik, organik dan biologi, komposisi kuantitatif dan kualitatif dari kompleks, struktur dan komposisi dari permukaan padat dan perbandingan isotropik atom atom di dalam sampel (Skoog et al., 1997).
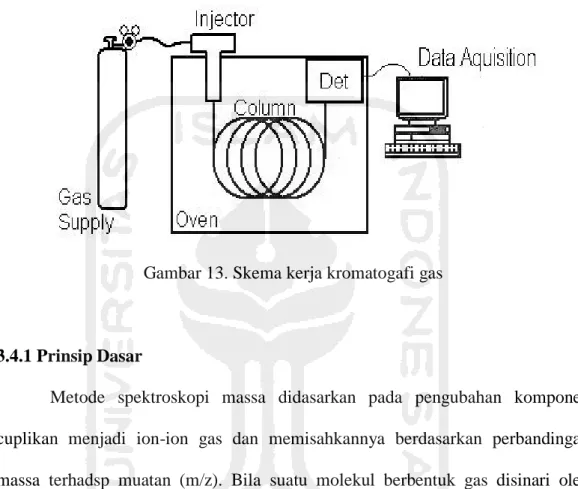
Gambar 13. Skema kerja kromatogafi gas
3.4.1 Prinsip Dasar
Metode spektroskopi massa didasarkan pada pengubahan komponen cuplikan menjadi ion-ion gas dan memisahkannya berdasarkan perbandingan massa terhadsp muatan (m/z). Bila suatu molekul berbentuk gas disinari oleh elektron berenergi tinggi di dalam sistem hampa akan terjadi ionisasi. Ion molekul akan terbentuk dan ion molekul yang tidak stabil pecah menjadi ion-ion yang lebih kecil. Lepasnya elektron dari molekul menghasilkan radikal kation dan proses ini dinyatakan sebagai berikut :
M→M+
Ion molekul M+ biasanya terurai lagi menjadi sepasang pecahan atau fragmen yang dapat berupa radikal dan ion atau molekul yang lebih kecil dan radikal kation.
xxiii
M→M1+ + M2 atau M1+ + M2
Dari kromatogam KG-MS akan diperoleh informasi jumlah senyawa yang terdeteksi dan dari spektra KG-MS akan diperoleh informasi struktur senyawa yang terdeteksi. Dalam kromatogafi gas, fasa gerak adalah gas pembawa, biasanya suatu gas inert seperti helium atau gas yang tidak reaktif seperti nitrogen. Fasa gerak membawa sampel melalui fasa diam yang ditempatkan dalam suatu kolom. Sampel dalama fasa gerak berinteraksi dengan fasa diam dengan kecepatan yang berbeda-beda. Saat terjadi interaksi, yang tercepat berinteraksi akan keluar dari kolom lebih dahulu sedangkan yang lambat akan keluar paling akhir. Detektor akan memberikan sinyal yang kemudian ditampilkan dalam komputer sebagai kromatogam (Howe dan Williams, 1981).
Pada kromatogam sumbu x menunjukkan waktu retensi, Rt (Retention time, waktu saat sampel diinjeksikan sampai elusi berakhir), sedangkan sumbu y menunjukkan intensitas sinyal. Dalam detektor selain memberikan sinyal sebagai kromatogam, kompnen yang telah terpisah akan ditembak oleh elektron sehingga akan terpecah menjadi fragmen-fragmen dengan m/z ditampilkan dalam komputer sebagai spektra massa, dimana sumbu x menunjukkan perbandingan m/z sedangkan sumbu y menunjukkan intensitas. Dari spektra tersebut dapat diketahui struktur senyawa dengan cara membandingkan dengan spektra massa senyawa standar dari literatur. Pendekatan pustaka terhadap spektra massa dapat digunakan untuk identifikasi bila indeks kemiripan atau similirity indeks (SI) ≥ 80% (Howe dan Williams, 1981).
xxiv 3.5 Scanning electron microscope (SEM)
Scanning Electron Microscope (SEM) adalah alat yang digunakan untuk mempelajari morfologi permukaan/ukuran butiran. Pengamatan morfologi permukaan dalam 3 Dimensi, resolusi tinggi dan analisa kimia.
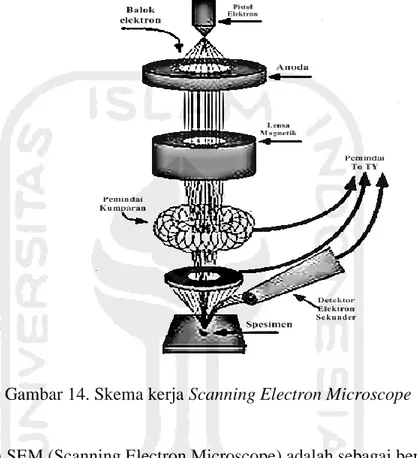
Gambar 14. Skema kerja Scanning Electron Microscope
Prinsip kerja SEM (Scanning Electron Microscope) adalah sebagai berikut: 1. Sumber Elektron / Penembak electron (Electron Gun).
Penembak elektron terdiri dari filamen Tungsten, penembak elektron ini digunakan untuk menghasilkan elektron dalam suatu volum tertentu dengan energi yang dapat ditentukan dengan mengatur arus listrik ke filamen sehingga terjadi pelepasan elektron.
xxv
Perangkat Demagnetisasi terdiri dari gabungan lensa-lensa lektromagnetik yang digunakan untuk menfokuskan E-Beam menjadi sangat kecil pada saat mencapai sampel.
3. Scan unit (sistem pelarikan).
Pembentukan Gambar dengan menggunakan prinsip scanning, dimana elektron diarahkan ke objek, gerakan berkas tersebut mirip dengan “Gerakan Membaca”. Scan unit dibangkitkan oleh scanning coil, sedangkan hasil interaksi berkas elektron dengan sampel menghasilkan Secondary Electron (SE) dan elektron Backs Scattered (BSc), diterima detektor SE/BSc, di ubah menjadi sinyal, data sinyal diperkuat oleh Video Amplifier kemudian disinkronkan oleh scanning circuit terbentuklah Gambar pada Tabung Sinar Katoda (CRT) (Sinuhaji dan marlianto, 2012).
Gambar 15 menunjukkan bentuk instrumen SEM dalam pengujian morfologi permukaan atau ukuran butiran.
xxvi 3.6 Spektrofotometri Serapan Atom (SSA)
Spektrofotometri serapan atom (SSA) adalah salah satu alat yang pengukurannya didasarkan pada penyerapan cahaya oleh atom-atom bebas. Atom adalah keadaan gas yang menyerap sejumlah energi sinar tertentu. Sinar yang diserap biasanya masih berada dalam spektra sinar tampak dan ultra lembayung. Dengan demikian molekul-molekul akan mengalami disosiasi dan direduksi menjadi atom-atom bebas. Spektrofotometer serapan atom ini sangat penting untuk analisis logam-logam renik karena memiliki kepekaan yang cukup tinggi.
Metode Spektrofotometri serapan atom (SSA) sangat tepat untuk analisis zat pada konsentrasi yang rendah. Teknik ini mempunyai beberapa kelebihan
dibandingkan metode spektroskopi emisi konvensional. Pada metode
konvensional, emisi tergantung pada sumber eksitasi.
Bila eksitasi dilakukan secara termal, maka ia bergantung pada temperatur sumber. Selain itu, eksitasi termal tidak selalu spesifik dan eksitasi secara serempak pada berbagai spesies dalam berbagai campuran dalam suatu spesies dapat saja terjadi. Sedangkan dengan nyala, eksitasi unsur-unsur dengan tingkat energi eksitasi yang sangat rendah dapat dimungkinkan. Tentu saja perbandingan banyaknya atom-atom yang tereksitasi terhadap atom yang berada pada tingkat dasar harus cukup besar, karena metode serapan atom, hanya bergantung pada temperatur. Metode serapan atom sangatlah spesifik logam-logam yang membentuk campuran kompleks dapat dianalisis dan selain itu tidak selalu diperlukan sumber energi yang besar (Khopkar, 1990).
Jika atom dianalisis dengan cahaya, atom tersebut akan menyerap cahaya yang mempunyai panjang gelombang spesifik untuk logam tersebut dan atom
xxvii
akan mengalami oksidasi, penyerapan cahaya ini sebanding dengan konsentrasi atom-atom nyala maka konsentrasi logam dalam contoh pada panjang gelombang
tertentu dinyatakan oleh hukum Lambert-Beer. Hukum Lambert-Beer merupakan
gabungan dari hukum lambert dan hukum beer.
Bunyi hukum lambert: “Bila suatu cahaya monokromatis atau
polikromatis melalui suatu media yang transparan, maka bertambah turunnya intensitas cahaya sebanding dengan tebalnya media.”
Bunyi hukum beer: “Bila suatu cahaya monokromatis atau polikromatis melalui suatu bidang atau media yang transparan maka bertambah turunnya intensitas cahaya yang dipancarkan sebanding dengan bertambahnya kepekatan.”
Bunyi hukum lambert-beer: “Bila suatu cahaya monokromatis atau
polikromatis melalui suatu media yang transparan maka bertambah turunnya intensitas cahaya yang dipancarkan sebanding dengan bertambahnya kepekatan dari media.’’
Bentuk matematika hukum Lambert-beer:
Keterangan: A=absorban
ɛ
= koefisienc=kepekatan media (mol/L) t=tebal media (cm)
Skema dari alat spektrofotometer serapan atom dapat dilihat pada Gambar berikut:
xxviii
Gambar 16. Skema kerja spektrofotometer serapan atom
3.6.1 Bagian-bagian spektrofotometer serapan atom
Bagian-bagian penyusun instrumen spektrofotometer serapan atom antara lain:
a). Sumber cahaya
Sumber cahaya ini dapat memancarkan spektrum garis yang sempit dan karakteristik dari unsur yang akan dianalisis, dimana sumber cahaya ini berasal dari lampu katoda yang berongga yang memiliki anoda dan katoda yang cekung dan silinder dalam suatu atmosfer gas inert pada tekanan yang rendah.
b). Sumber atom
Cuplikan yang dianalisis harus diuraikan terlebih dahulu menjadi atom-atom netral yang masih dalam keadaan dasarnya. Atom-atom-atom tersebut dihasilkan dengan cara disosiasi termal dan bias nyala. Pada nyala akan terjadi proses pengkabutan (nebulasi), penguapan pelarut (desolvasi), penguapan zat-zat (volatilasi) dan atomisasi.c). Monokromator
xxix
Berfungsi untuk mendispersi cahaya menjadi cahaya-cahaya yang mempunyai panjang gelombang yang berbeda dan setelah melalui celah yang lebarnya dapat diatur sehingga memungkinkan pemilihan panjang gelombang. d). Detektor
Untuk mengubah foton-foton cahaya menjadi sinyal-sinyal listrik. e). Amplifier
Berfungsi memperkuat sinyal listrik yang berasal dari detektor. f). Instrumen Pembaca
Dapat berupa galvanometer sederhana, voltameter sederhana, voltameter digital, potensiometer perekam pena tinta, dan komputer.
Gambar 17. Instrumen spektrofotometer serapan atom
3.6.2 Gangguan-gangguan pada spektrofotometer serapan atom a). Arus atau voltase yang tidak stabil.