xviii INTISARI
Buah cabai rawit hijau (Capsicum frutescens L.) mengandung senyawa kimia yaitu kapsaisin. Kapsaisin memiliki atom hidrogen yang bertanggungjawab terhadap aktivitas antioksidan. Penelitian ini bertujuan untuk menetapkan aktivitas antioksidan yang terdapat pada ekstrak etanol buah cabai rawit hijau dan menetapkan kadar kapsaisin dalam ekstrak etanol buah cabai rawit hijau.
Penelitian ini merupakan penelitian eksperimental. Penetapan aktivitas antioksidan dilakukan dengan metode DPPH. Pengukuran absorbansi
menggunakan spektrofotometer visibel pada maks 517,5 nm. Penetapan kadar
kapsaisin digunakan metode KLT – densitometri dengan fase diam silika gel 60 F254 dan fase gerak toluen : kloroform: aseton (45:25:30).
Hasil penelitian menunjukkan aktivitas antioksidan (IC50) kapsaisin
sebesar 15,9961±4,2 µg/mL dan ekstrak etanol buah cabai rawit hijau sebesar 115,2074±5,8 µg/mL. Hasil penetapan kadar kapsaisin ekstrak etanol buah cabai rawit hijau sebesar (0,066±0,003) % (b/b).
xix ABSTRACT
Fruit green chili pepper (Capsicum frutescens L.) contains a chemical compound called capsaicin. Capsaicin has a hydrogen atom are responsible for antioxidant activity. This research aims to assign antioxidant activity which is found in extract ethanol fruit green chili and set levels capsaisin in extract ethanol fruit green chili.
This is an experimental research study. The determination of antioxidant activity performed with a method of DPPH. The measurement of absorbansi use of the spectrophotometer visible in max 517,5 nm. The determination of the level of capsaisin used method of TLC – densitometry with silica gel 60 F254 as
stasionary phase and toluene : chloroform : acetone (45:25:30) as mobile phase. The result of examination showed that antioxidant activity (IC50) in
capsaisin is 15,9961±4,2 µg/mL and extract ethanol fruit green chili is 115,2074±5,8 µg/mL. The level of capsaisin in extract ethanol fruit green chili is (0,066±0,003) % (b/b).
i
UJI AKTIVITAS ANTIOKSIDAN EKSTRAK ETANOL BUAH CABAI RAWIT HIJAU (Capsicum frutescens L.) DENGAN METODE DPPH (1,1-difenil-2-pikrilhidrazil) DAN PENETAPAN KADAR KAPSAISIN SECARA
KROMATOGRAFI LAPIS TIPIS (KLT) – DENSITOMETRI
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm)
Program Studi Farmasi
Oleh:
Yenny
NIM : 098114063
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
iv
HALAMAN PERSEMBAHAN
Kupersembahkan karya ini untuk : Papa, Mama, Kakak dan Adik ku terkasih, Sahabat-sahabat ku dan Almamaterku
Sebab Aku ini mengetahui rancangan-rancangan apa yang ada pada-Ku mengenai kamu, demikianlah firman TUHAN, yaitu rancangan damai sejahtera dan bukan rancangan kecelakaan, untuk memberikan kepadamu hari depan yang penuh harapan. (Yeremia 29:11)
Masa depan adalah milik mereka yang
percaya tentang keindahan mimpi-mimpi mereka. (Eleanor Roosevelt)
Karena itu Aku berkata kepadamu : apa saja yang
kamu minta dan doakan, percayalah bahwa kamu
telah menerimanya, maka hal itu akan diberikan
kepadamu. (Markus 11:24)
Sebab Aku ini mengetahui rancangan-rancangan apa yang ada pada-Ku mengenai kamu, demikianlah firman TUHAN, yaitu rancangan damai sejahtera dan bukan rancangan kecelakaan, untuk memberikan kepadamu hari depan yang penuh harapan. (Yeremia 29:11)
Masa depan adalah milik mereka yang percaya tentang keindahan mimpi-mimpi mereka. (Eleanor Roosevelt)
Karena itu Aku berkata kepadamu : apa saja yang
kamu minta dan doakan, percayalah bahwa kamu
telah menerimanya, maka hal itu akan diberikan
vii PRAKATA
Puji Syukur kepada Tuhan atas semua berkat dan penyertaan-Nya kepada
penulis sehingga penulis dapat menyelesaikan skripsi yang berjudul “UJI
AKTIVITAS ANTIOKSIDAN EKSTRAK ETANOL BUAH CABAI RAWIT HIJAU (Capsicum frutescens L.) DENGAN METODE DPPH (1,1-difenil-2-pikrilhidrazil) DAN PENETAPAN KADAR KAPSAISIN SECARA KROMATOGRAFI LAPIS TIPIS (KLT) – DENSITOMETRI” ini dengan baik. Laporan akhir ini disusun untuk memenuhi salah satu persyaratan untuk
memperoleh gelar Sarjana Strata 1 Program Studi Ilmu Farmasi (S.Farm).
Dalam proses penyelesaian skripsi ini, penulis tidak lepas dari bimbingan
serta bantuan yang diberikan oleh semua pihak. Maka pada kesempatan ini
dengan segala kerendahan hati penulis mengucapkan terima kasih yang
sebesar-besarnya kepada:
1. Ipang Djunarko, M.Sc., Apt. selaku Dekan Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta yang telah memberikan kesempatan kepada
penulis untuk melakukan penelitian ini.
2. Prof.Dr.C.J. Soegihardjo, Apt., selaku Dosen Pembimbing yang telah
memberikan bantuan dan bimbingan selama rancangan, pengusulan skripsi,
saat dilakukan penelitian dan selama penulisan naskah skripsi dengan
kesabaran dan penuh perhatian.
3. Yohanes Dwiatmaka, M.Si., selaku Dosen Penguji yang telah memberikan
viii
4. Dra. M.M. Yetty Tjandrawati, M.Si., selaku Dosen Penguji yang telah
memberikan bimbingan dan saran sehingga skripsi ini dapat terselesaikan.
5. Agustina Setiawati, M.Sc., Apt., selaku Dosen Pembimbing Akademik yang
telah memberikan bimbingan dan saran.
6. Rini Dwiastuti, M.Sc., Apt. selaku Kepala Laboratorium Fakultas Farmasi
Universitas Sanata Dharma.
7. Seluruh staff laboratorium Universitas Sanata Dharma Yogyakarta terutama
Mas Bimo, Mas Wagiran, Mas Parlan dan Mas Kayat atas segala bantuan
selama penelitian skripsi.
8. Teman seperjuangan, Vanny Christy Silviani dan Christina atas semua
dukungan, semangat, persahabatan, doa dan kerjasamanya selama pengerjaan
skripsi.
9. Edy Trilaksono yang selalu memberi semangat, dukungan, dan doa selama
proses pengerjaan skripsi dari awal hingga selesai.
10.Sahabat terkasih, Agustina Erni Purnamasari, Marsela Lotjita, Christina Yessy
Jessica, Evy Fenny Veronica, Fitri Apriliyani Tiran dan Melisa Silvia yang
selalu memberikan dukungan, semangat dan doa yang tak terlupakan.
11.Teman-teman terkasih, Adel, Riza, Wisnu, Oni, dan Prita yang selalu
memberikan dukungan dan semangat.
12.Komsel Spirit of Angel, Yusita Halim, Lulu Margathe, Hana Eirene Tawe,
Rini Novianti, Rina Novianti, Cynthia Chrisdiananda Happy Anastasia Putri,
ix
13.Teman-teman FST 2009 dan FSM B 2009, atas kerjasama, doa, semangat,
canda tawa, saran dan kritik.
14.Semua pihak yang tidak dapat penulis sebutkan satu per satu dalam proses
kuliah dan pengerjakan skripsi ini.
Akhir kata penulis menyadari bahwa skripsi ini masih banyak memiliki
kekurangan. Oleh karena itu, penulis mengharapkan saran dan kritik yang
membangun demi kesempurnaan skripsi ini. Penulis juga berharap semoga
laporan ini dapat bermanfaat bagi teman-teman dan orang lain yang
membutuhkannya.
Yogyakarta,12 Maret 2013
x DAFTAR ISI
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN KEASLIAN KARYA ... v
LEMBAR PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS ... vi
PRAKATA ... vii
DAFTAR ISI ... x
DAFTAR TABEL ... xv
DAFTAR GAMBAR ... xvi
DAFTAR LAMPIRAN ... xvii
INTISARI ... xviii
ABSTRACT ... xix
BAB I PENGANTAR ... 1
A. Latar Belakang ... 1
1. Permasalahan ... 3
2. Keaslian Penelitian ... 3
3. Manfaat Penelitian ... 4
a. Manfaat teoritis ... 4
xi
B. Tujuan Penelitian ... 4
1. Tujuan umum ... 4
2. Tujuan khusus ... 4
BAB II PENELAAHAN PUSTAKA ... 5
A. Cabai ... 5
1. Klasifikasi Tanaman ... 5
2. Gambaran Umum ... 5
3. Kandungan Kimia dan Manfaat Tanaman Cabai Rawit Hijau ... 6
B. Kapsaisin ... 6
C. Radikal Bebas ... 7
D. Antioksidan ... 8
E. Metode DPPH (1,1-difenil-2-pikrilhidrazil) ... 9
F. Ekstraksi ... 9
G. Validasi Metode Analisis ... 10
H. Spektrofotometri Visibel ... 13
I. Metode Kromatografi Lapis Tipis (KLT) – Densitometri ... 14
J. Landasan Teori ... 15
K. Hipotesis ... 16
BAB III METODOLOGI PENELITIAN ... 17
A. Jenis dan Rancangan Penelitian ... 17
B. Variabel ... 17
1. Variabel Bebas ... 17
xii
3. Variabel pengacau ... 17
a. Terkendali ... 17
b. Tak terkendali ... 17
C. Definisi Operasional ... 17
D. Alat dan Bahan Penelitian ... 18
1. Alat penelitian ... 18
2. Bahan penelitian ... 18
E. Tatacara Penelitian ... 18
1. Determinasi tanaman ... 18
2. Pengumpulan bahan ... 19
3. Pembuatan ekstrak etanol buah cabai rawit hijau ... 19
4. Penentuan aktivitas antioksidan ekstrak etanol buah cabai rawit hijau dengan metode DPPH ... 19
a. Pembuatan larutan DPPH ... 19
b. Pembuatan larutan stok kapsaisin ... 19
c. Pembuatan larutan seri baku kapsaisin ... 20
d. Pembuatan larutan uji ... 20
e. Uji pendahuluan aktivitas antioksidan ... 20
f. Penentuan operating time (OT) ... 20
g. Penentuan panjang gelombang maksimum ( maks) ... 21
h. Penentuan aktivitas antioksidan ... 21
i. Validasi metode uji aktivitas antioksidan ... 22
xiii
5. Penetapan kadar kapsaisin ... 22
a. Pembuatan fase gerak ... 22
b. Pembuatan larutan stok kapsaisin ... 22
c. Pembuatan larutan seri baku kapsaisin ... 22
d. Pembuatan larutan uji ... 23
e. Penetapan kadar kapsaisin ekstrak etanol buah cabai rawit hijau ... 23
F. Analisis Hasil ... 24
1. Penentuan aktivitas antioksidan ekstrak etanol buah cabai rawit hijau dengan metode DPPH ... 24
2. Penetapan kadar kapsaisin ... 24
BAB IV HASIL DAN PEMBAHASAN ... 25
A. Hasil Determinasi Tanaman ... 25
B. Hasil Pengumpulan Bahan ... 25
C. Hasil Preparasi Sampel ... 26
D. Hasil Uji Pendahuluan ... 27
E. Hasil Optimasi Metode Uji Aktivitas Antioksidan ... 28
1. Penentuan operating time (OT) ... 28
2. Penentuan panjang gelombang maksimum ( maks) ... 29
F. Hasil Validasi Metode Uji Aktivitas Antioksidan ... 30
1. Linieritas ... 33
2. Akurasi ... 33
xiv
4. Spesifisitas ... 36
G. Hasil Estimasi Aktivitas Antioksidan dengan Radikal DPPH ... 36
H. Penetapan Kadar Kapsaisin ... 39
I. Analsis Statistik ... 43
BAB V KESIMPULAN DAN SARAN ... 44
A. Kesimpulan ... 44
B. Saran ... 44
DAFTAR PUSTAKA ... 45
LAMPIRAN ... 48
xv
DAFTAR TABEL
Tabel I. Kriteria Akurasi yang Dapat Diterima Menurut
Harmita (2004) ... 12
Tabel II. Kriteria Presisi yang Dapat Diterima Menurut APVMA
(cit., Angela, 2012) ... 12
Tabel III. Hasil Scanning Panjang Gelombang Maksimum
DPPH ... 30
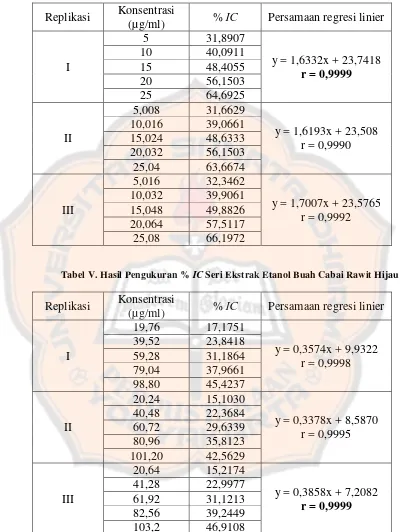
Tabel IV. Hasil Pengukuran % IC Seri Baku Kapsaisin ... 31
Tabel V. Hasil Pengukuran % IC Seri Ekstrak Etanol Buah Cabai
Rawit Hijau ... 31
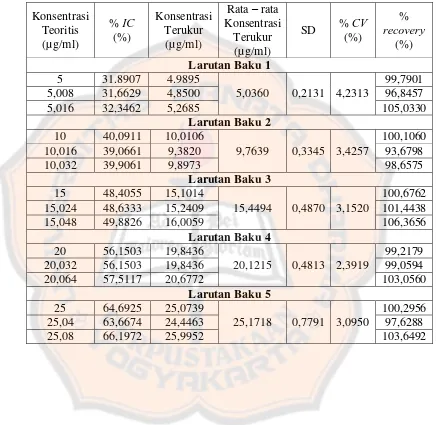
Tabel VI. Hasil % recovery dan % CV Uji Aktivitas Antioksidan
Baku Kapsaisin ... 34
Tabel VII. Hasil % recovery dan % CV Uji Aktivitas Antioksidan
Ekstrak Etanol Buah Cabai Rawit Hijau ... 35
Tabel VIII. Hasil IC50 Baku Kapsaisin dan Ekstrak Etanol Buah Cabai
Rawit Hijau ... 38
Tabel IX. Nilai Rf Baku Kapsaisin dan Ekstrak Etanol Buah Cabai
Rawit Hijau ... 40
Tabel X. Penetapan Kadar Kapsaisin dalam Ekstrak Etanol Buah
xvi
DAFTAR GAMBAR
Gambar 1. Struktur Senyawa Kapsaisin (Bickler, J.R., 2000) ... 7
Gambar 2. Soxhlet (Burge, D.M., James M. Reilly, and Douglas
W. Nishimura, 2002) ... 10
Gambar 3. Hasil Uji Pendahuluan ... 27
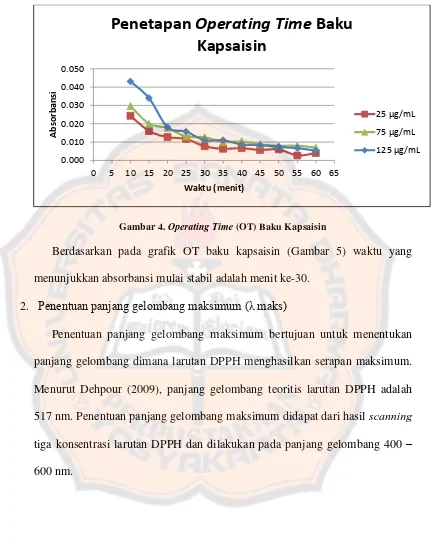
Gambar 4. Operating Time (OT) Baku Kapsaisin ... 29
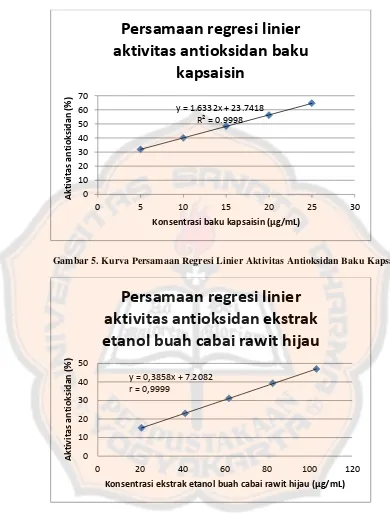
Gambar 5. Kurva Persamaan Regresi Linier Aktivitas Antioksidan
Baku Kapsaisin ... 32
Gambar 6. Kurva Persamaan Regresi Linier Aktivitas Antioksidan
Ekstrak Etanol Buah Cabai Rawit Hijau ... 32
Gambar 7. Penangkapan DPPH oleh Senyawa Antioksidan (Windono,
Soediman, Yudawati, Ermawati, Srielita dan
Erowati, 2001) ... 37
Gambar 8. Mekanisme Penghambatan Radikal Bebas oleh Senyawa
Kapsaisin ... 38
Gambar 9. Interaksi Kapsaisin dengan Fase Diam Silika Gel 60
F254 ... 40
xvii
DAFTAR LAMPIRAN
Lampiran 1. Sertifikat Kapsisin ... 48
Lampiran 2. Gambar Buah Cabai Rawit Hijau ... 49
Lampiran 3. Perhitungan Rendemen Ekstrak Etanol Buah Cabai Rawit Hijau ... 50
Lampiran 4. Data Penimbangan Pengujian Aktivitas Antioksidan ... 50
Lampiran 5. Perhitungan Konsentrasi Bahan Pengujian Aktivitas Antiokidan ... 51
Lampiran 6. Optimasi Metode Uji Aktivitas Antioksidan ... 52
Lampiran 7. Uji Aktivitas Antioksidan Menggunakan DDPH ... 55
Lampiran 8. Perhitungan % recovery, CV Uji Aktivitas Antioksidan Menggunakan DPPH ... 57
Lampiran 9. Perhitungan IC50 Kapsaisin dan Ekstrak Etanol Buah Cabai Rawit Hijau ... 59
Lampiran 10. Data Persamaan Kurva Baku Kapsaisin ... 59
Lampiran 11. Data dan Perhitungan Kadar Kapsaisin dalam Ekstrak Etanol Buah Cabai Rawit Hijau ... 60
Lampiran 12. Kromatogram Baku Kapsaisin ... 61
Lampiran 13. Kromatogram Ekstrak Etanol Buah Cabai Rawit Hijau ... 62
xviii INTISARI
Buah cabai rawit hijau (Capsicum frutescens L.) mengandung senyawa kimia yaitu kapsaisin. Kapsaisin memiliki atom hidrogen yang bertanggungjawab terhadap aktivitas antioksidan. Penelitian ini bertujuan untuk menetapkan aktivitas antioksidan yang terdapat pada ekstrak etanol buah cabai rawit hijau dan menetapkan kadar kapsaisin dalam ekstrak etanol buah cabai rawit hijau.
Penelitian ini merupakan penelitian eksperimental. Penetapan aktivitas antioksidan dilakukan dengan metode DPPH. Pengukuran absorbansi
menggunakan spektrofotometer visibel pada maks 517,5 nm. Penetapan kadar
kapsaisin digunakan metode KLT – densitometri dengan fase diam silika gel 60 F254 dan fase gerak toluen : kloroform: aseton (45:25:30).
Hasil penelitian menunjukkan aktivitas antioksidan (IC50) kapsaisin
sebesar 15,9961±4,2 µg/mL dan ekstrak etanol buah cabai rawit hijau sebesar 115,2074±5,8 µg/mL. Hasil penetapan kadar kapsaisin ekstrak etanol buah cabai rawit hijau sebesar (0,066±0,003) % (b/b).
xix ABSTRACT
Fruit green chili pepper (Capsicum frutescens L.) contains a chemical compound called capsaicin. Capsaicin has a hydrogen atom are responsible for antioxidant activity. This research aims to assign antioxidant activity which is found in extract ethanol fruit green chili and set levels capsaisin in extract ethanol fruit green chili.
This is an experimental research study. The determination of antioxidant activity performed with a method of DPPH. The measurement of absorbansi use of the spectrophotometer visible in max 517,5 nm. The determination of the level of capsaisin used method of TLC – densitometry with silica gel 60 F254 as
stasionary phase and toluene : chloroform : acetone (45:25:30) as mobile phase. The result of examination showed that antioxidant activity (IC50) in
capsaisin is 15,9961±4,2 µg/mL and extract ethanol fruit green chili is 115,2074±5,8 µg/mL. The level of capsaisin in extract ethanol fruit green chili is (0,066±0,003) % (b/b).
1 BAB I PENGANTAR
A. Latar Belakang
Radikal bebas adalah suatu atom atau molekul yang memiliki satu atau
lebih elektron bebas yang memilki sifat reaktif di dalam tubuh. Di dalam tubuh,
apabila jumlah elektron bebas sedikit maka dapat distabilkan oleh sistem enzim
yang ada di dalam tubuh namun jika berada dalam jumlah banyak maka dapat
bermasalah bagi kesehatan. Radikal bebas adalah suatu agen pengoksidasi yang
dapat menyebabkan beberapa penyakit seperti kerusakan protein dan DNA,
kanker, penuaan dini, dan penyakit degeneratif lainnya (Metris, 2012). Oleh
karena itu, tubuh memerlukan suatu senyawa antioksidan yang dapat berikatan
dengan radikal bebas supaya tidak menyebabkan munculnya penyakit di dalam
tubuh. Senyawa antioksidan biasanya terdapat pada tumbuh-tumbuhan dan
buah-buahan.
Antioksidan adalah suatu senyawa yang mampu memberikan satu atau
lebih elektron pada radikal bebas sehingga efek radikal bebas dapat dihindari
(Suhartono, 2002). Dalam tubuh manusia memiliki cadangan antioksidan yang
terbatas, sehingga ketika jumlah radikal bebas berlebih maka tubuh kita
memerlukan tambahan antioksidan eksogen. Antioksidan eksogen dapat berasal
dari makanan atau minuman yang mengandung vitamin C, vitamin E, beta karoten
dan asam amino. Antioksidan terdiri dari dua macam, yaitu antioksidan alami dan
Cabai merupakan salah satu tanaman yang sangat penting dalam industri
makanan dan industri farmasi karena biasa digunakan untuk bumbu masak dan
mulai banyak peneliti yang menganalisis kandungan dari cabai. Khasiat ekstrak
cabai adalah sebagai obat sariawan, tonik, stimulan kuat untuk jantung dan aliran
darah, antireumatik, antikoagulan, stomakik, karminatif, diaforetik dan diuretik
(Sentra Informasi Ilmu Pengetahuan dan Teknologi, 2005).
Pada cabai terkandung senyawa kimia yaitu kapsaisin
(8-methyl-N-vanillyl-6-nonenamide) yang dapat menimbulkan rasa pedas (Wellyan, 2000).
Menurut Henderson dan Slickman (1999), kapsaisin memiliki aktivitas
antioksidan dengan cara mendonorkan atom hidrogen sehingga radikal bebas
dapat bersifat netral. Oleh karena itu, perlu ditetapkan daya antioksidan pada
cabai.
Pengujian aktivitas antioksidan dapat dilakukan dengan beberapa metode.
Pada penelitian ini digunakan metode DPPH (1,1-difenil-2-pikrilhidrazil) untuk
mengetahui aktivitas antioksidan pada cabai rawit hijau. Metode DPPH
(1,1-difenil-2-pikrilhidrazil) dapat memberikan informasi mengenai penangkapan
radikal bebas yang menyebabkan elektron menjadi berpasangan. Nilai aktivitas
antioksidan dinyatakan dengan IC50 yang merupakan konsentrasi antioksidan yang
mampu menghambat 50% radikal. (Sunarni, 2005). Dalam penetapan kadar
kapsaisin digunakan metode kromatografi lapis tipis (KLT) – densitometri karena
1. Permasalahan
a. Berapa nilai aktivitas antioksidan ekstrak etanol buah cabai rawit hijau
dengan metode DPPH yang dinyatakan dengan IC50?
b. Berapa kadar kapsaisin yanag terkandung di dalam ekatrak etanol buah
cabai rawit hijau dengan metode kromatografi lapis tipis (KLT) –
densitometri?
2. Keaslian penelitian
Sejauh penelusuran penulis, uji aktivitas antioksidan pada buah cabai
rawit hijau dan penetapan kadar kapsaisin pernah dilakukan:
a. Penelitian Henderson dan Slickman (1999) tentang Quantitative HPLC
Determination of the Antioxidant Activity of Capsaicin on the Formation
of Lipid Hydroperoxides of Linoleic Acid: A Comparative Study against
BHT and Melatonin
b. Penelitian yang dilakukan Talcott, Brenes, dan Villalon (2000) mengenai
aktivitas antioksidan pada berbagai spesies Capsicum dengan metode β -karoten – linoleat.
c. Penelitian dari Sukrasno dan Kusmardiyani (1997) meneliti kandungan
kapsaisin pada berbagai buah Capsicum menggunakan metode KCKT.
Perbedaan dengan penelitian ini adalah pengujian antioksidan dengan
metode DPPH pada ekstrak etanol buah cabai rawit hijau dan penetapan kadar
3. Manfaat penelitian
a. Manfaat teoritis. Penelitian ini diharapkan dapat memberikan pengetahuan
mengenai aktivitas antioksidan ekstrak etanol buah cabai rawit hijau
dengan metode DPPH yang dinyatakan dengan IC50.
b. Manfaat praktis. Penelitian ini diharapkan dapat memberikan informasi
mengenai aktivitas antioksidan ekstrak etanol buah cabai rawit hijau
supaya dapat bermanfaat bagi kesehatan masyarakat dan perkembangan
pada sediaan farmasi.
B. Tujuan Penelitian 1. Tujuan umum
Menguji aktivitas antioksidan ekstrak etanol buah cabai rawit hijau dengan
metode DPPH.
2. Tujuan khusus
a. Mengetahui nilai aktivitas antioksidan ekstrak etanol buah cabai rawit
hijau dengan metode DPPH yang dinyatakan dengan IC50.
b. Mengetahui kadar kapsaisin yang terkandung di dalam ekstrak etanol buah
5 BAB II
PENELAAHAN PUSTAKA A. Cabai
1. Klasifikasi tanaman
Klasifikasi tanaman cabai rawit hijau menurut Plantmor, 2008 seperti
berikut:
Kingdom : Plantae
Subkingdom : Tracheobionta
Super Divisi : Spermatophyta
Divisi : Magnoliophyta
Kelas : Magnoliopsida
Sub Kelas : Asteridae
Ordo : Solanales
Famili : Solanaceae
Genus : Capsicum
Spesies : Capsicum frutescens L.
2. Gambaran umum
Secara morfologi, cabai rawit memiliki bagian-bagian penting yang
dapat dideskripsikan sebagai berikut: buah cabai rawit akan terbentuk setelah
penyerbukan. Buah cabai rawit memiliki bentuk bulat pendek dengan ujung
runcing atau kerucut. Warna buah cabai rawit bermacam-macam yaitu putih,
bulat pipih. Akar cabai rawit terdiri dari akar tunggang yang tumbuh lurus ke
pusat bumi dan akar serabut yang menyebar ke samping (Cahyono, 2003).
3. Kandungan kimia dan manfaat tanaman cabai rawit hijau
Kandungan kimia cabai rawit antara lain kapsaisin, kapsantin,
kapsarubin, karoten, karotenoid, minyak lemak, vitamin A, B dan C (Guntur,
2010). Manfaat cabai rawit hijau antara lain dapat menjaga kesehatan mata,
menambah nafsu makan, menormalkan kembali kaki dan tangan yang lemas,
batuk berdahak, melegakan hidung tersumbat pada sinusitis, migrain. Cabai
rawit yang memiliki rasa pedas apabila masuk ke dalam meridian jantung dan
pankreas dapat menimbulkan sensasi panas. Ekstrak buah cabai rawit
mempunyai daya hambat terhadap pertumbuhan Candida albicans. Daya
hambat ekstrak cabal rawit 1 mg/mL setara dengan 6,20 mcg/mL nistatin
dalam formamid (Sentra Informasi Ilmu Pengetahuan dan Teknologi, 2005).
B. Kapsaisin
Kapsaisin (8-metil-N-vanilil-6-nonenamida) merupakan suatu zat aktif
cabai yang dapat memberikan efek panas dalam cabai. Kapsaisin dapat
menimbulkan iritasi pada mammalian termasuk manusia dan menimbulkan rasa
terbakar dan panas pada jaringan yang tersentuh. Kapsaisin disebut juga
kapsaisinoid dan merupakan suatu metabolit sekunder dari cabai. Kapsaisin
memiliki sifat hidrofobik, tidak berwarna, tidak berbau, dan bentuk kristalnya
Kapsaisin mempunyai aktivitas antioksidan dengan menangkap radikal
bebas. Gugus fenol pada kapsaisin yang akan bertanggungjawab atas aktivitas
antioksidan dalam mendonorkan elektron kepada radikal bebas (Henderson and
Slickman, 1999).
Gambar 1. Struktur Senyawa Kapsaisin (Bickler, 2000)
C. Radikal Bebas
Radikal bebas adalah atom atau kelompok atom dengan nomor
(berpasangan) elektron ganjil dan dapat terbentuk ketika oksigen berinteraksi
dengan molekul tertentu (Sportmedweb, 2005).
Radikal bebas merupakan suatu atom atau gugus atom yang memiliki satu
elektron tidak berpasangan. Radikal bebas bersifat sangat reaktif dan memiliki
energi yang tinggi karena memiliki elektron tidak berpasangan (Fessenden dan
Fessenden, 1982).
Penangkap radikal bebas menyebabkan elektron menjadi berpasangan
yang kemudian menyebabkan penghilangan warna yang sebanding dengan jumlah
D. Antioksidan
Antioksidan merupakan senyawa yang dapat menghambat oksidasi yang
diperantarai oleh oksigen. Oksidasi memegang peranan penting dalam pertahanan
tubuh terhadap penyakit. Hal tersebut disebabkan senyawa antioksidan dapat
mencegah pengaruh buruk yang disebabkan oleh senyawa-senyawa radikal bebas.
Radikal bebas tersebut beberapa di antaranya toksik (beracun) dan sangat reaktif
sehingga dapat mempercepat proses penuaan dan kematian (Niki, 1987;
Goodman, 1999).
Menurut Halliwel (2000), antioksidan memiliki aktivitas sebagai berikut:
1. Menurunkan konsentrasi oksigen.
2. Mencegah inisiasi rantai pertama dengan menangkap radikal penginisiasi
seperti radikal hidroksil.
3. Mengikat ion logam dalam bentuk yang tidak akan menurunkan spesies
penginisiasi seperti radikal hidroksil dan tidak mendekomposisi peroksida
lipid menjadi radikal peroksi atau alkoksi.
4. Mendekomposisi peroksida dengan mengubah menjadi produk non radikal
seperti alkohol.
5. Memecah rantai pada radikal intermediet seperti radikal peroksi dan alkoksi
E. Metode DPPH (1,1-difenil-2-pikrilhidrazil)
Salah satu uji untuk menentukan aktivitas antioksidan penangkap radikal
adalah metode DPPH (1,1 Diphenyl-2-picrylhidrazyl). Metode DPPH
memberikan informasi reaktivitas senyawa yang diuji dengan suatu radikal stabil.
DPPH memberikan serapan kuat pada panjang gelombang 517 nm dengan warna
violet gelap. Penangkap radikal bebas menyebabkan elektron menjadi
berpasangan yang kemudian menyebabkan penghilangan warna yang sebanding
dengan jumlah elektron yang diambil (Sunarni, 2005).
F. Ekstraksi
Ekstraksi adalah kegiatan penarikan zat aktif dari simplisia nabati dan
hewani menggunakan pelarut yang sesuai kemudian pelarut diuapkan. Simplisia
yang diekstrak mengandung senyawa aktif yang dapat larut dan senyawa yang
tidak dapat larut dalam cairan penyari. Ekstrak adalah sediaan kental yang
diperoleh dengan mengekstraksi senyawa aktif dari simplisia nabati atau hewani
menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut
diuapkan dan massa yang tersisa diperlakukan sedemikian sehingga memenuhi
baku yang telah ditetapkan. Ekstrak cair adalah sediaan dari simplisia nabati yang
mengandung etanol sebagai pelarut atau sebagai pengawet. Faktor yang
mempengaruhi kecepatan penyarian adalah kecepatan difusi zat yang larut melalui
lapisan-lapisan batas antara cairan penyari dengan bahan yang mengandung zat
Soxhletasi merupakan metode ekstraksi dengan cara mengalirkan bahan
yang akan diekstraksi dengan pelarut yang sesuai dan selalu baru. Bahan yang
akan diekstrak dibungkus dengan menggunakan kantung ekstraksi, kemudian
dimasukkan ke dalam alat soxhlet. Soxhlet diletakkan di antara labu penampung
hasil ekstraksi dan suatu pendingin balik yang terhubung dengan pipa-pipa.
Dalam labu penampung hasil ekstraksi, pelarut akan diuapkan. Pelarut tersebut
akan bertambah sampai batas maksimal dan akan masuk ke dalam labu
penampung sehingga zat yang terekstraksi akan selalu terendam oleh pelarut yang
selalu baru (Voigt, 1994).
Gambar 2. Soxhlet (Burge, Jame and Douglas, 2002)
G. Validasi Metode Analisis
Validasi adalah suatu cara untuk mengetahui bahwa metode yang akan
digunakan sesuai dengan tujuan yang diinginkan (Rohman, 2009). Validasi
penelitian laboratorium untuk membuktikan bahwa parameter tersebut memenuhi
syarat untuk digunakan (Harmita, 2004).
Suatu metode analisis harus divalidasi untuk melakukan verifikasi bahwa
parameter-parameter kinerjanya cukup mampu mengatasi problem analisis,
karenanya suatu metode harus divalidasi ketika:
a. Metode baru dikembangkan untuk mengatasi problem analisis tertentu.
b. Metode yang sudah baku direvisi untuk menyesuaikan perkembangan, atau
karena munculnya suatu masalah yang mengarahkan bahwa metode baku
tersebut harus direvisi.
c. Penjaminan mutu yang mengindikasikan bahwa metode baku telah berubah
seiring dengan berjalannya waktu.
d. Metode baku digunakan di laboratorium yang berbeda dikerjakan oleh analis
berbeda, atau dikerjakan dengan alat yang berbeda. (Rohman, 2009).
Parameter validasi metode analisis antara lain adalah akurasi, presisi, dan
linieritas. Akurasi merupakan keterdekatan nilai pengukuran dengan nilai
sebenarnya dari analit dalam sampel (Mulja dan Suharman, 1995).
Akurasi merupakan ketelitian suatu metode analisis atau kedekatan antara
nilai terukur dengan nilai yang diterima baik nilai konvensi, nilai sebenarnya atau
nilai rujukan. Akurasi diukur sebagai banyaknya analit yang diperoleh kembali
pada suatu pengukuran (Gandjar dan Rohman, 2007). Akurasi dinyatakan dalam
Tabel I. Kriteria Akurasi yang Dapat Diterima Menurut Harmita (2004)
Analit pada matrik sampel (%)
Presisi merupakan ukuran kedekatan hasil yang diperoleh dari analisis
yang dilakukan berulangkali pada suatu sampel homogen dan kondisi yang
sama. Presisi dinyatakan dalam standar deviasi atau koefisien variasi (Mulja dan
Suharman, 1995).
Presisi merupakan ukuran keterulangan metode analisis dan biasanya
dinyatakan dengan simpangan baku relatif dari sejumlah sampel yang berbeda
signifikan secara statistik (Gandjar dan Rohman, 2007).
Tabel II. Kriteria Presisi yang Dapat Diterima
Menurut APVMA (cit., Angela, 2012)
Spesifisitas adalah kemampuan untuk mengukur analit yang dituju secara
tepat dan spesifik dengan adanya komponen-komponen lain dalam matriks sampel
seperti ketidakmurnian, produk degradasi dan komponen matriks (Gandjar dan
Rohman, 2007).
Linieritas merupakan kemampuan suatu metode untuk memperoleh
hasil-hasil uji yang secara langsung proposional dengan konsentrasi analit pada kisaran
yang diberikan. Linieritas suatu metode merupakan ukuran seberapa baik kurva
kalibrasi yang menghubungkan antara respon (y) dengan konsentrasi (x).
Linieritas dapat diukur dengan melakukan pengukuran tunggal pada konsentrasi
yang berbeda-beda. Data yang diperoleh selanjutnya diproses dengan metode
kuadrat terkecil, untuk selanjutnya dapat ditentukan nilai kemiringan (slope),
intersep dan koefisien korelasinya (Gandjar, dan Rohman, 2007).
H. Spektrofotometri Visibel
Spektrofotometri UV-VIS adalah salah satu teknik analisis fisika kimia
yang mengamati tentang interaksi atom/molekul dengan radiasi elektromagnetik
pada panjang gelombang 190-380 nm (UV) dan 380-780 nm (VIS) dengan
memakai instrumen spektrofotometer (Mulja dan Suharman, 1995).
Prinsip kerja spektrofotometri adalah berdasarkan atas interaksi antara
radiasi elektromagnetik (salah satu jenis energi yang ditransmisikan dalam ruang
dengan kecepatan tinggi) dengan materi (atom, ion/molekul) (Khopkar, 1990).
elektron-elektron dari orbital keadaan dasar berenergi rendah ke orbital tereksitasi
bernergi lebih besar (Fessenden dan Fessenden, 1982).
I. Metode Kromatografi Lapis Tipis (KLT) – Densitometri
Kromatografi lapis tipis (KLT) dan kromatografi kertas (KKt) adalah
metode kromatografi cair yang paling sederhana dalam penyajian data. Dengan
memakai KLT, pemisahan senyawa yang berbeda seperti senyawa organik alam
dan senyawa sintetik, kompleks organik-nonorganik, dan bahkan ion anorganik,
dapat dilakukan dalam beberapa menit dengan alat yang harganya tidak terlalu
mahal. Jumlah cuplikan serendah beberapa mikrogram atau setinggi 5 gram dapat
ditangani, bergantung pada alat dan gejala kromaografi yang terlibat. Kelebihan
KLT yang lain adalah pemakaian pelarut dan cuplikan yang jumlahnya sedikit,
kemungkinan penotolan cuplikan berganda (Gritter, 1991).
Kromatografi dapat dibedakan atas berbagai macam tergantung pada
pengelompokannya. Berdasarkan pada mekanisme pemisahannya, kromatografi
dibedakan menjadi kromatografi adsorbsi, kromatografi partisi, kromatografi
pasangan ion, kromatografi penukar ion, kromatografi eksklusi ukuran, dan
kromatografi afinitas (Gandjar dan Rohman, 2007).
KLT biasanya merupakan metode pilihan pertama dalam memisahkan
suatu campuran. Pada kromatografi lapis tipis, fase diam berada pada pelat gelas,
plastik atau logam dan sampel akan ditotolkan di atas pelat fase diam. Sampel
Volume sampel yang dapat digunakan pada kromatografi lapis tipis adalah 1
sampai 5 L (Dean, 1995).
Densitometri merupakan suatu analisis kuantitatif yang berdasarkan pada
interaksi radiasi elektromagnetik dengan analit yang merupakan bercak KLT.
(Gandjar dan Rohman, 2007).
J. Landasan Teori
Radikal bebas merupakan suatu senyawa yang memiliki satu atau lebih
elektron tidak berpasangan, hal ini yang menyebabkan radikal bebas bersifat tidak
stabil dan reaktif di dalam tubuh. Di dalam tubuh, radikal bebas akan menjadi
stabil dengan cara menyerang elektron disekitarnya sehingga dapat menimbulkan
kerusakan sel dan dapat menimbulkan penyakit degeneratif.
Cabai rawit hijau mengandung senyawa aktif, yaitu kapsaisin. Kapsaisin
memiliki gugus fenol yang dapat mendonorkan atom hidrogen pada radikal bebas
sehingga radikal dapat bersifat stabil.
Pengujian aktivitas antioksidan dapat dilakukan dengan metode DPPH.
DPPH merupakan suatu metode yang mampu menunjukkan terjadinya perubahan
warna larutan karena radikal bebas berikatan atom hidrogen dari senyawa
antioksidan.
Kadar kapsaisin ditetapkan dengan metode KLT – densitometri karena
dapat memisahkan senyawa-senyawa alam, sintetik, organik maupun nonorganik
dan dapat menganalisis secara kuantitatif dengan adanya interaksi radiasi
K. Hipotesis
1. Ekstrak etanol buah cabai rawit hijau memiliki daya aktivitas antioksidan yang
dinyatakan dengan IC50 menggunakan metode DPPH.
2. Ekstrak etanol buah cabai rawit hijau mengandung kapsaisin yang dapat
17 BAB III
METODOLOGI PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian yang berjudul uji aktivitas antioksidan ekstrak etanol buah
cabai rawit hijau (Capsicum frutescens L.) dengan metode DPPH dan penetapan
kadar kapsaisin secara kromatografi lapis tipis (KLT) – densitometri merupakan jenis penelitian eksperimental.
B. Variabel
1. Variabel bebas : konsentrasi ekstrak etanol buah cabai rawit hijau.
2. Variabel tergantung : persen inhibition concentration (%IC).
3. Variabel pengacau
a. Terkendali : lokasi pengambilan sampel, umur tanaman, cara pemanenan, waktu pemanenan dan bobot sampel.
b. Tak terkendali : cuaca, curah hujan dan kelembaban ruangan.
C. Definisi Operasional
1. Buah cabai rawit hijau adalah buah yang diperoleh dari pasar Beringharjo,
Yogyakarta, tidak dilakukan pemilihan ukuran.
2. Ekstrak etanol buah cabai rawit hijau adalah ekstrak yang diperoleh dari hasil
3. Inhibition concentration 50 (IC50) adalah nilai konsentrasi ekstrak etanol buah
cabai rawit hijau yang mampu menangkap 50% radikal DPPH.
D. Alat dan Bahan Penelitian 1. Alat penetitian
Alat-alat yang digunakan dalam penelitian ini adalah vortex,
spektrofotometer UV-VIS, alat soxhlet, densitometer, blender, corong
Buchner, oven, mikropipet 10-1000 µl; 1-10 mL, neraca analitik, vaccum
rotary evaporator, waterbath, tabung reaksi tertutup, bejana kromatografi dan
alat-alat gelas yang lazim digunakan di laboratorium analisis.
2. Bahan penelitian
Bahan-bahan yang digunakan dalam penelitian ini adalah buah cabai
rawit hijau (Capsicum frutescens L.) yang tidak ditentukan ukurannya dan di
dapat dari pasar Beringharjo, Yogyakarta. Bahan kimia kualitas farmasetis
berupa akuades. Bahan kimia kualitas pro analitik meliputi etanol 96%, silika
gel 60 F254 DPPH dan aluminium foil.
E. Tatacara Penelitian 1. Determinasi tanaman
Determinasi sampel buah cabai rawit hijau yang digunakan
berdasarkan ciri morfologinya dilakukan dengan membandingkan literatur
2. Pengumpulan bahan
Buah cabai rawit hijau diperoleh dari seorang pedagang di Pasar
Beringharjo, Yogyakarta.
3. Pembuatan ekstrak etanol buah cabai rawit hijau
Buah cabai rawit hijau sebanyak 1 kg yang masih segar dibersihkan
dan dicuci kemudian dibuang tangkainya, buah cabai rawit hijau dikeringkan
pada oven dengan suhu 50°C kemudian dihaluskan menggunakan blender.
Serbuk yang diperoleh ditimbang sebanyak 25 g dan dibungkus dengan kertas
saring. Simplisia yang telah dibungkus, dimasukkan ke dalam labu alas bulat
berisi 350 mL etanol p.a. Soxhletasi dilakukan pada suhu 70°C selama 8 jam
sampai diperoleh hasil ekstrasi jernih. Filtrat hasil ekstraksi diuapkan dengan
menggunakan vacuum rotary evaporator.
4. Penentuan aktivitas antioksidan ekstrak etanol buah cabai rawit hijau dengan metode DPPH
a. Pembuatan larutan DPPH, sebanyak 15,8 mg DPPH dilarutkan ke dalam
etanol p.a 100,0 mL sehingga diperoleh larutan DPPH dengan konsentrasi
0,4 mM. Larutan tersebut ditutup dengan aluminium foil dan harus selalu
dibuat baru.
b. Pembuatan larutan stok kapsaisin, sebanyak 2,5 mg kapsaisin dimasukkan
c. Pembuatan larutan seri baku kapsaisin, diambil sebanyak 1,0; 2,0; 3,0; 4,0
dan 5,0 mL larutan stok kapsaisin, kemudian ditambahkan etanol p.a
sampai 10,0 mL, sehingga diperoleh konsentrasi larutan baku kapsaisin
sebesar 25,0; 50,0; 75,0; 100,0 dan 125,0 µg/mL.
d. Pembuatan larutan uji, ditimbang sebanyak 25 mg ekstrak etanol buah
cabai rawit hijau dan ditambahkan etanol p.a sampai 25,0 mL. Diambil
sebanyak 1,0; 2,0; 3,0; 4,0 dan 5,0 mL larutan tersebut, kemudian
ditambahkan etanol p.a sampai 10,0 mL, sehingga diperoleh konsentrasi
larutan uji sebesar 100,0; 200,0; 300,0; 400,0 dan 500,0 µg/mL.
e. Uji pendahuluan aktivitas antioksidan, sebanyak 1 mL larutan DPPH
dimasukkan ke dalam tiga tabung reaksi. Ditambahkan masing-masing
dengan 1 mL etanol p.a, larutan baku kapsaisin 75,0 µg/mL, dan larutan
uji 300 µg/mL. selanjutnya, larutan tersebut ditambahkan dengan 3,0 mL
etanol p.a. Larutan tersebut kemudian divortex selama 30 detik. Setelah itu
di diamkan selama 30 menit dan amati warna pada larutan tersebut.
f. Penentuan operating time (OT), sebanyak 1,0 mL larutan DPPH
dimasukkan ke dalam tiga labu ukur 5,0 mL, ditambahkan masing-masing
dengan 1 mL larutan baku kapsaisin 25,0; 75,0 dan 125,0 µg/mL.
Selanjutnya, larutan tersebut ditambahkan dengan etanol p.a hingga tanda
batas. Larutan tersebut kemudian divortex selama 30 detik. Setelah itu
dibaca absorbansinya dengan spektrofotometer visibel pada panjang
g. Penentuan panjang gelombang maksimum (λmaks), pada tiga labu ukur 10
mL, dimasukkan masing-masing 0,5; 1,0 dan 1,5 mL larutan DPPH.
Ditambahkan ke dalam larutan tersebut dengan etanol p.a hingga tanda
batas sehingga konsentrasi DPPH menjadi 0,020; 0,040 dan 0,080 mM.
Larutan tersebut kemudian divortex selama 30 detik. Didiamkan selama
OT. Lalu dilakukan scanning panjang gelombang serapan maksimum
dengan spektrofotometer visibel pada panjang gelombang 400-600 nm.
h. Penentuan aktivitas antioksidan
1) Pengukuran absorbansi larutan DPPH (kontrol), pada labu ukur 5 mL,
dimasukkan sebanyak 1,0 mL larutan DPPH. Ditambahkan larutan
tersebut dengan etanol p.a hingga tanda batas. Kemudian larutan
tersebut dibaca absorbansinya pada saat OT dan panjang gelombang
maksimum. Pengerjaan dilakukan sebanyak tiga kali. Larutan ini
digunakan sebagai kontrol untuk menguji larutan baku dan uji.
2) Pengukuran absorbansi larutan baku dan uji, sebanyak 1 mL larutan
DPPH dimasukkan ke dalam labu ukur 5 mL kemudian ditambah
dengan 1 mL larutan baku dan uji pada berbagai seri konsentrasi telah
dibuat. Selanjutnya, larutan tersebut ditambah dengan etanol p.a
hingga tanda batas. Larutan tersebut kemudian divortex selama 30
detik dan didiamkan selama OT. Larutan dibaca absorbansinya dengan
spektrofotometer visibel pada panjang gelombang maksimum.
i. Validasi metode uji aktivitas antioksidan, hasil dari prosedur 4h 1) dan 2)
divalidasi akurasi (% recovery), presisi (% CV), spesifisitas (spectra
kontrol) dan linieritas (nilai r).
% recovery = jumlah analit terukur
jumlah analit teoritis x 100% (1) (Harmita, 2004).
% CV = s
rata-ratax 100% (2) (Harmita, 2004).
j. Estimasi aktivitas antioksidan, hasil dari prosedur 4h 1) dan 2) dihitung
nilai % IC dan IC50 untuk kapsaisin dan ekstrak etanol buah cabai rawit
hijau.
5. Penetapan kadar kapsaisin
a. Pembuatan fase gerak, fase gerak yang digunakan pada penelitian ini yaitu
campuran toluen - kloroform - aseton (45:25:30) v/v . Fase gerak dituang
dalam bejana kromatografi kemudian kertas saring dimasukkan dalam
bejana yang berisi fase gerak. Bejana ditutup rapat dan dibiarkan hingga
seluruh kertas saring terbasahi oleh fase gerak.
b. Pembuatan larutan stok kapsaisin, baku kapsaisin ditimbang seksama
sebanyak 1,0 mg dan dimasukkan dalam labu takar 10 mL, kemudian
dilarutkan dengan metanol sampai tanda batas sehingga diperoleh larutan
stok kapsaisin 0,1 mg/mL.
c. Pembuatan larutan seri baku kapsaisin, larutan stok kapsaisin ditotolkan
dengan volume 1,25; 2,5; 5; dan 10 µl pada lempeng silika gel 60 F254
d. Pembuatan larutan uji, sejumlah 50,0 mg ekstrak etanol buah cabai rawit
hijau ditimbang seksama kemudian dilarutkan dengan metanol sebanyak
500 µl. Larutan tersebut divortex selama 10 menit dengan pemanasan
diatas waterbath pada suhu 60ºC. kemudian larutan disentrifugasi selama
2 menit dan disaring dengan ayakan mesh 60. Larutan uji dibuat replikasi
sebanyak 3 kali.
e. Penetapan kadar kapsaisin ekstrak etanol buah cabai rawit hijau, sebanyak
10 L larutan uji ditotolkan pada lempeng silika gel F254, kemudian
dikembangkan dalam bejana kromatografi yang telah dijenuhkan dengan
fase gerak toluene - kloroform - aseton (45:25:30) v/v. Pengembangan
dilakukan setinggi 10 cm, lempeng silika kemudian dikeluarkan dan
ditunggu hingga kering. Bercak diamati di bawah lampu UV 254 nm
kemudian dianalisis dengan densitometer pada panjang gelombang
maksimum. Bercak seri baku kapsaisin diukur AUC-nya dengan
densitometer pada panjang gelombang yang telah diperoleh. Puncak
kromatogram dan nilai AUC yang muncul diamati. Dengan metode regresi
linier, nilai seri kadar (µg/mL) diplotkan terhadap nilai AUC
masing-masing seri larutan baku sehingga diperoleh persamaan y = bx + a dimana
y merupakan nilai respon (AUC), x merupakan konsentrasi senyawa baku,
a adalah intersep dan b adalah slope. Kadar kapsaisin dalam sampel
F. Analisis hasil
1. Penentuan aktivitas antioksidan ekstrak etanol buah cabai rawit hijau
dengan metode DPPH
Aktivitas penangkapan radikal DPPH (%) dihitung dengan rumus:
bsorbansilarutan kontrol – bsorbansilarutan baku uji
bsorbansilarutan kontrol
x 100%
Data aktivitas tersebut dianalisis dan dihitung nilai IC50
menggunakan persamaan regresi linier dengan sumbu x adalah konsentrasi
larutan uji maupun baku sedangkan sumbu y adalah % IC. Lalu dianalisis
secara statistik Mann-Whitney.
2. Penetapan kadar kapsaisin
Uji kadar kapsaisin dilakukan secara kromatografi lapis tipis. Nilai
kadar tersebut diperoleh dari analisis data kromatogram dengan menggunakan
densitometer. Analisis kualitatif dilakukan dengan membandingkan nilai Rf
sampel dengan nilai Rf baku. Analisis kuantitatif dilakukan berdasarkan data
AUC dari baku sehingga diperoleh persamaan regresi linier y = bx + a yang
merupakan hubungan antara kadar dengan luas area yang dihasilkan. Data
AUC sampel kemudian dimasukkan dalam persamaan regresi masing-masing
25 BAB IV
HASIL DAN PEMBAHASAN
A. Hasil Determinasi Tanaman
Determinasi tanaman bertujuan untuk memastikan kebenaran identitas
tanaman yang akan digunakan serta menghindari terjadinya kesalahan dalam
pengambilan sampel. Determinasi buah cabai rawit hijau dilakukan dengan
membandingkan beberapa spesies dari Capsicum yang mengacu pada Bosland,
Bailey, Iglesias-Olivas (1996).
Pembuktian determinasi buah cabai rawit hijau dilakukan dengan
membandingkan pengamatan morfologi dari buah dengan karakteristik spesies
Capsicum sesuai dengan literatur, yaitu panjang buah 3 – 4 cm, lebar buah kurang dari 1 cm, tegak lurus dan warna buah hijau. Dari hasil determinasi buah cabai
rawit hijau, telah dibuktikan bahwa buah yang digunakan pada penelitian ini
adalah buah cabai rawit hijau (Capsicum frutescens L.)
B. Hasil Pengumpulan Bahan
Buah cabai rawit hijau diperoleh dari Pasar Beringharjo, Yogyakarta pada
bulan September 2012. Pengumpulan bahan diambil dari seorang pedagang, hal
ini bertujuan untuk mengurangi variasi waktu panen yang dapat berpengaruh
C. Hasil Preparasi Sampel
Tujuan dari ekstraksi adalah untuk menarik kandungan kimia/zat aktif
yang dapat larut sehingga terpisah dari bahan yang tidak larut dalam pelarut cair
yang sesuai. Dalam ekstraksi ini yang diharapkan adalah menarik senyawa
kapsaisin yang ada dalam serbuk cabai rawit hijau. Hasil dari ekstraksi berupa
ekstrak cair.
Dalam penelitian ini metode ekstraksi yang digunakan adalah metode
soxhletasi. Prinsip dari soxhletasi adalah ekstraksi menggunakan pelarut yang
selalu baru secara kontinyu dengan adanya pendingin balik menghasilkan jumlah
pelarut yang konstan. Digunakan metode soxhletasi karena menurut Kristanti (cit.,
Kurniawan, 2008), metode yang digunakan untuk mengekstraksi kapsaisin adalah
menggunakan metode ekstraksi berulang secara otomatis selama delapan jam
pada suhu 60ºC. Pelarut yang digunakan dalam proses ekstraksi adalah etanol
96% karena kapsaisin memiliki kelarutan yang baik dalam etanol. Sebelum
diekstraksi, sampel dikeringkan menggunakan oven pada suhu 50ºC, setelah
kering, sampel dihaluskan menggunakan blender dan diayak untuk memperkecil
ukuran partikel dan memperoleh derajat kehalusan yang sama. Proses ekstraksi
dilakukan dengan memasukkan serbuk yang telah dibungkus ke dalam alat
soxhlet, kemudian pelarut etanol dituang ke dalamnya, kemudian dipanaskan.
Tujuan adanya pemanasan ini adalah untuk menguapkan pelarut dan dengan
adanya pendingin balik maka akan terbentuk embun, sehingga proses ekstraksi
Hasil dari ekstraksi adalah larutan berwarna hijau lumut. Larutan tersebut
kemudian dipekatkan menggunakan vacuum rotary evaporator pada suhu 60ºC
supaya didapatkan ekstrak kental. Prinsip dari alat vacuum rotary evaporator
adalah dengan adanya penurunan tekanan udara maka titik didih larutan akan
semakin menurun. Penurunan titik didih akan mempercepat penguapan pelarut
etanol. Bobot ekstrak kental yang diperoleh sebanyak 2,43 g, sehingga diperoleh
rendemen sebesar 8,1%.
D. Hasil Uji Pendahuluan
Uji pendahuluan bertujuan untuk mengetahui aktivitas antioksidan secara
kualitatif. Uji pendahuluan ini dilakukan dengan mereaksikan radikal bebas
berupa senyawa DPPH dengan senyawa kapsaisin. Adanya perubahan warna
ungu, yang merupakan warna senyawa DPPH menunjukkan bahwa senyawa
kapsaisin memiliki aktivitas antioksidan.
Uji pendahuluan dilakukan dengan menggunakan 3 larutan, yaitu larutan
A yang berisi baku kapsaisin dan DPPH, larutan B yang berisi larutan DPPH dan
larutan C yang berisi ekstrak etanol buah cabai rawit hijau dan DPPH.
Hasil pengujian menunjukkan hasil positif karena terjadi perubahan warna
ungu jika dibandingkan dengan larutan DPPH, sehingga ekstrak etanol buah cabai
rawit hijau memiliki aktivitas antioksidan.
E. Hasil Optimasi Metode Uji Aktivitas Antioksidan
1. Penentuan Operating Time (OT)
Operating Time (OT) adalah waktu dimana reaksi antara senyawa yang
memiliki aktivitas antioksidan dan larutan DPPH sudah berjalan sempurna
yang ditunjukkan dengan absorbansi yang stabil. Pengukuran OT dilakukan
dengan mengukur absorbansi larutan DPPH yang sudah direaksikan dengan
larutan baku kapsaisin konsentrasi 25, 75 dan 125 µg/mL. Pengukuran
dilakukan setiap 5 menit selama 60 menit dengan menggunakan
spektrofotometer visibel dan dilakukan pada panjang gelombang maksimal
yang telah ditentukan, yaitu 517,5 nm. Karena absorbansi terus mengalami
penurunan, maka penentuan OT dilakukan dengan menghitung selisih
penurunan absorbansi yang mendekati stabil setiap 5 menit sampai 60 menit
dan kemudian dibuat grafik supaya dapat diketahui waktu dimana absorabansi
Gambar 4. Operating Time (OT) Baku Kapsaisin
Berdasarkan pada grafik OT baku kapsaisin (Gambar 5) waktu yang
menunjukkan absorbansi mulai stabil adalah menit ke-30.
2. Penentuan panjang gelombang maksimum ( maks)
Penentuan panjang gelombang maksimum bertujuan untuk menentukan
panjang gelombang dimana larutan DPPH menghasilkan serapan maksimum.
Menurut Dehpour (2009), panjang gelombang teoritis larutan DPPH adalah
517 nm. Penentuan panjang gelombang maksimum didapat dari hasil scanning
tiga konsentrasi larutan DPPH dan dilakukan pada panjang gelombang 400 –
600 nm.
Penetapan
Operating Time
Baku
Kapsaisin
25 µg/mL
75 µg/mL
Tabel III. Hasil Scanning Panjang Gelombang Maksimum DPPH
Konsentrasi DPPH (mM)
maksimum hasil scanning
(nm) Rata-rata maksimum 0,02 517,5
517,5 nm 0,04 517,0
0,08 518,0
Hasil scanning tiga konsentrasi larutan DPPH didapatkan hasil panjang
gelombang maksimum rata-rata adalah 517,5 nm (Tabel III). Panjang
gelombang ini berbeda dengan panjang gelombang maksimum teoritis DPPH,
yaitu 517 nm. Hal ini diperbolehkan sesuai dengan ketentuan yang tercantum
dalam Farmakope Indonesia IV (1995), dimana batas pergeseran yang
diperkenankan adalah maksimum sebesar 2 nm. Oleh karena itu, panjang
gelombang maksimum yang digunakan pada penelitian ini adalah 517,5 nm.
F. Hasil Validasi Metode Uji Aktivitas Antioksidan
Pengujian validasi metode dilakukan dengan menggunakan baku kapsaisin
dan ekstrak etanol buah cabai rawit hijau masing-masing sebanyak 3 replikasi.
Hasil pengujian akan diperoleh 3 persamaan regresi linier antara konsentrasi
Tabel IV. Hasil Pengukuran % IC Seri Baku Kapsaisin
Replikasi Konsentrasi
(µg/ml) % IC Persamaan regresi linier
I
Tabel V. Hasil Pengukuran % IC Seri Ekstrak Etanol Buah Cabai Rawit Hijau
Replikasi Konsentrasi
(µg/ml) % IC Persamaan regresi linier
Gambar 5. Kurva Persamaan Regresi Linier Aktivitas Antioksidan Baku Kapsaisin
Gambar 6. Kurva Persamaan Regresi Linier Aktivitas Antioksidan Ekstrak Etanol Buah Cabai Rawit Hijau
Gambar 5 dan 6 menunjukkan korelasi yang baik antara konsentrasi baku
kapsaisin dan ekstrak etanol buah cabai rawit hijau dengan %IC. Hal ini
ditunjukkan dengan nilai r mendekati 1 yang berarti semakin besar konsentrasi
y = 1.6332x + 23.7418
Konsentrasi baku kapsaisin (µg/mL)
Persamaan regresi linier
Konsentrasi ekstrak etanol buah cabai rawit hijau (µg/mL)
Persamaan regresi linier
aktivitas antioksidan ekstrak
etanol buah cabai rawit hijau
baku kapsaisin maupun ekstrak etanol buah cabai rawit hijau maka semakin besar
pula % IC yang dihasilkan.
Analisis presisi (nilai Coefficient of Variation) dan akurasi (nilai
Recovery) seri baku kapsaisin menggunakan persamaan regresi linier dari
replikasi I, yaitu y = 1,6332x + 23,7418 (Tabel IV) sedangkan untuk ekstrak
etanol buah cabai rawit hijau menggunakan persamaan regresi linier dari replikasi
III, yaitu y = 0,3858x + 7,2082 (Tabel V) karena nilai r yang dihasilkan
merupakan yang paling baik (1 atau -1) dari ketiga replikasi yang telah dilakukan.
1. Linieritas
Hasil dari tiga replikasi yang dilakukan pada baku kapsaisin dan ekstrak
etanol buah cabai rawit hijau menunjukkan bahwa koefisien korelasi yang
paling baik pada baku kapsaisin sebesar r = 0,9999 (replikasi I), sedangkan
pada ekstrak etanol buah cabai rawit hijau sebesar r = 0,9999 (replikasi III).
Nilai r yang memenuhi persyaratan linieritas yang baik menurut Mulja dan
Hanwar (2003) adalah lebih besar 0,999, sehingga nilai r yang diperoleh
dalam penelitian ini masih dapat diterima karena masih berada diatas nilai r
yang dipersyaratkan. Hal ini menunjukkan bahwa metode yang digunakan
dalam penelitian ini mempunyai linieritas yang baik untuk analisis baku
kapsaisin dan ekstrak etanol buah cabai rawit hijau.
2. Akurasi
Akurasi dinyatakan dengan nilai % recovery. Nilai % recovery diperoleh
dari data hubungan antara seri konsentrasi baku kapsaisin dan ekstrak etanol
berikut menunjukkan % recovery baku kapsaisin dan ekstrak etanol buah
cabai rawit hijau.
Tabel VI. Hasil % recovery dan % CV Uji Aktivitas Antioksidan Baku Kapsaisin
Konsentrasi 15,024 48,6333 15,2409 101,4438 15,048 49,8826 16,0059 106,3656
Larutan Baku 4
20 56,1503 19,8436
20,1215 0,4813 2,3919
99,2179 20,032 56,1503 19,8436 99,0594 20,064 57,5117 20,6772 103,0560
Tabel VII. Hasil % recovery dan % CV Uji Aktivitas Antioksidan Ekstrak Etanol Buah
Persyaratan rentang % recovery yang baik menurut Harmita (2004) untuk
analit dengan kadar 0,01% sebesar 90% - 107%. Dari data yang ditunjukkan
pada Tabel VI rentang % recovery baku kapsaisin adalah 93,68% - 106,37%
yang telah memenuhi syarat % recovery yang dapat diterima. Hal ini
menunjukkan bahwa metode yang digunakan telah memberikan akurasi yang
baik.
Persyaratan rentang % recovery yang baik menurut APVMA (cit., Angela,
2012) untuk analit sebesar 0,1% - 1% yaitu 80% - 120%. Dari data yang
dapat diterima, walaupun pada konsentrasi 19,76 µg/ml tidak memenuhi %
recovery, namun pada konsentrasi lainnya memenuhi syarat % recovery,
sehingga dapat disimpulkan bahwa metode yang digunakan memiliki akurasi
yang baik.
3. Presisi
Presisi dinyatakan dengan nilai CV (Coevicient of Variation). Semakin
kecil nilai CV maka presisi suatu metode tersebut akan semakin baik.
Persyaratan rentang CV yang baik menurut APVMA (cit., Angela, 2012)
untuk analit dengan kadar < 0,01% sebesar ≤ 20%. Dari data yang ditunjukkan pada Tabel VI dan VII menunjukkan nilai CV memenuhi syarat. Hal ini
menunjukkan bahwa metode yang digunakan memiliki presisi yang baik.
4. Spesifisitas
Uji spesifisitas dilakukan dengan mengukur absorbansi larutan etanol yang
digunakan sebagai pelarut, kapsaisin, larutan ekstrak etanol buah cabai rawit
hijau pada panjang gelombang 517,5 nm yang merupakan panjang gelombang
maksimum DPPH. Hasil pengukuran dari ketiga larutan tersebut tidak terdapat
serapan. Hal ini menunjukkan bahwa metode yang digunakan spesifik
terhadap DPPH.
G. Hasil Estimasi Aktivitas Antioksidan dengan Radikal DPPH
Pengujian terhadap daya antioksidan ekstrak etanol buah cabai rawit hijau
dilakukan dengan metode DPPH (1,1-difenil-2-pikrilhidrazil). DPPH merupakan
hidrogen yang akan mengubah warna ungu menjadi kuning. Senyawa yang
mampu memberikan efek ini dipertimbangkan memiliki daya antioksidan
(Halliwell and Gutteridge, 2000).
Reaksi umum yang terjadi saat penangkapan DPPH oleh senyawa
antioksidan, yaitu sebagai berikut
Gambar 7. Penangkapan DPPH oleh Senyawa Antioksidan (Windono, Soediman, Yudawati, Ermawati, Srielita dan Erowati, 2001)
Salah satu senyawa yang terkandung di dalam buah cabai rawit hijau
adalah kapsaisin. Senyawa kapsaisin memiliki gugus OH yang dapat
mendonorkan atom hidrogennya untuk radikal bebas DPPH sehingga dapat
diketahui daya antioksidannya. Mekanisme penghambatan radikal bebas oleh
kapsaisin ditunjukkan Gambar 8, DPPH dilambangkan sebagai R•. danya
senyawa kapsaisin yang memiliki gugus OH akan mendonorkan atom hidrogen
pada elektron bebas DPPH sehingga senyawa radikal DPPH dapat bersifat netral.
Penangkapan atom H ini akan menimbulkan perubahan warna pada DPPH yang
O
Gambar 8. Mekanisme Penghambatan Radikal Bebas DPPH oleh Senyawa Kapsaisin
Untuk mengetahui aktivitas antioksidan suatu senyawa dengan metode
DPPH, parameter yang digunakan adalah IC50. Parameter yang dipakai untuk
menunjukan aktivitas antioksidan adalah harga konsentrasi efisien atau efficient
concentration (EC50) atau Inhibition Concentration (IC50) yaitu konsentrasi suatu
zat antioksidan yang memberikan penghambatan 50%. Zat yang mempunyai
aktivitas antioksidan tinggi, akan mempunyai harga EC50 atau IC50 yang rendah
(Brand-Williams, 1995).
Hasil pengukuran IC50 untuk baku kapsaisin dan ekstrak etanol buah cabai
rawit hijau adalah sebagai berikut
Tabel VIII. Hasil IC50 Baku Kapsaisin dan Ekstrak Etanol Buah Cabai Rawit Hijau
Larutan
Kapsaisin 16,0778 16,3601 15,5368 15,9961 4,1837 2,6162 Ekstrak
etanol buah cabai rawit
hijau
Dari Tabel VIII, CV yang dihasilkan untuk baku kapsaisin adalah 2,6162%
dan ekstrak etanol buah cabai rawit hijau adalah 5,5783% sehingga CV memenuhi
persyaratan yaitu ≤ 20%. Hasil IC50 untuk baku kapsaisin 15,9916±4,1827 µg/mL
dan ekstrak etanol buah cabai rawit hijau 115,2074±5,5783 µg/mL. Penggolongan
kekuatan aktivitas antioksidan berdasarkan nilai IC50, yaitu lemah (151 – 200
µg/mL), sedang (100 – 150 µg/mL), kuat (50 – 100 µg/mL) dan sangat kuat (< 50 µg/mL) (Ariyanto cit Angela, 2012). Berdasarkan penggolongan tersebut,
aktivitas antioksidan baku kapsaisin termasuk golongan sangat kuat dan aktivitas
antioksidan ekstrak etanol buah cabai rawit hijau termasuk golongan sedang.
H. Penetapan Kadar Kapsaisin
Penetapan kadar kapsaisin dilakukan dengan metode kromatografi lapis
tipis (KLT) – densitometri. Prinsip metode KLT adalah berdasarkan adanya
perbedaan interaksi senyawa yang diuji dengan fase diam dan fase gerak.
Sedangkan prinsip densitometri adalah suatu analisis kuantitatif yang berdasarkan
pada interaksi radiasi elektromagnetik dengan analit yang merupakan bercak KLT
(Rohman, 2009). Digunakan metode KLT – densitometri karena mudah dilakukan dan dapat dilakukan analisis kualitatif dan kuantitatif secara bersamaan.
Sistem kromatografi yang digunakan adalah sistem dengan fase normal
dimana fase diam yang digunakan bersifat polar sedangkan fase geraknya bersifat
non polar. Fase diam yang digunakan adalah silika gel 60 F254 dan fase gerak yang
digunakan adalah campuran antara toluen - kloroform - aseton (45:25:30) v/v yang
dengan senyawa lain yan terkandung dalam ekstrak etanol cabai rawit hijau dapat
terjadi karena adanya perbedaan interaksi masing-masing senyawa dengan fase
diam maupun fase gerak. Kapsaisin yang bersifar non polar akan lebih
berinteraksi dengan fase gerak yang juga bersifat non polar sehingga kapsaisin
akan terelusi. Interaksi antara kapsaisin dengan fase diam adalah interaksi
hidrogen (Gambar 9).
Gambar 9. Interaksi Kapsaisin dengan Fase Diam Silika Gel 60 F254
Pertama-tama dilakukan analisis kualitatif dengan membandingkan nilai
Rf baku dan Rf sampel. Nilai Rf baku dan sampel adalah sebagai berikut
Tabel IX. Nilai Rf Baku Kapsaisin dan Ekstrak Etanol Buah Cabai Rawit Hijau
Sampel Rf Baku kapsaisin 0,61 Ekstrak etanol buah cabai rawit
Dari Tabel IX, didapatkan bahwa nilai Rf baku kapsaisin dan Rf ekstrak
etanol buah cabai rawit hijau sama, yaitu 0,61 maka dapat dikatakan bahwa kedua
senyawa tersebut memiliki kesamaan polaritas dan sama-sama mengandung
kapsaisin.
Kurva baku merupakan hubugan linier antara konsentrasi analit dengan
AUC (Area Under Curve). Pada penelitian ini digunakan empat seri baku, yaitu
knsentrasi 0,125; 0,250; 0,500 dan 1,000 µg. Persamaan kurva baku yang
diperoleh digunakan untuk menetapkan kadar kapsaisin dalam ekstrak etanol buah
cabai rawit hijau.
Gambar 10. Kurva Persamaan Regresi Linier Baku Kapsaisin
Persamaan kurva baku kapsaisin yang diperoleh adalah y = 51136,273x – 174,5978 dengan r = 0,9992. Maka dapat disimpulkan bahwa koefisien korelasi
(r) memenuhi parameter linieritas yang baik, yaitu mendekati 1 sehingga
persamaan kurva baku dapat digunakan untuk menetapkan kadar kapsaisin dalam
ekstrak etanol buah cabai rawit hijau.
0
Persamaan Regresi Linier Baku
Kapsaisin
Y = 51136,2727x – 174,5978
Analisis kuantitatif kapsaisin dilakukan sebanyak tiga kali replikasi
dengan menggunakan densitometer pada panjang gelombang maksimum 228 nm.
Hasil pengukuran yang diperoleh adalah sebagai berikut
Tabel X. Penetapan Kadar Kapsaisin Ekstrak Etanol Buah Cabai Rawit Hijau
Replikasi
I. Analisis Statistik
Hasil dari uji aktivitas antioksidan yang diperoleh, dilakukan analisis hasil
uji secara statistik dengan SPSS 16.0. Pengujian yang pertama kali dilakukan
adalah uji normalitas dengan menggunakan data % IC untuk mengetahui apakah
data yang diperoleh terdistribusi normal atau tidak. Uji normalitas dilakukan
menggunakan uji Shapiro-Wilk dan menghasilkan nilai signifikansi pada baku
kapsaisin sebesar 0,209 dan ekstrak etanol buah cabai rawit hijau sebesar 0,559.
Berdasarkan data pada Lampiran 15a, nilai signifikansi yang diperoleh lebih besar
dari yang ditentukan yaitu 0,05 (taraf kepercayan 95%) sehingga hipotesis H0
diterima dan dapat disimpulkan bahwa data % IC baku kapsaisin dan ekstrak
etanol buah cabai rawit hijau terdistribusi normal.
Karena terbukti data tersebut terdistribusi normal maka dilakukan uji
selanjutnya yaitu uji T tidak berpasangan yang merupakan uji parametrik. Tujuan
dari uji T tidak berpasangan adalah untuk melihat signifikansi nilai IC50 baku
kapsaisin dan IC50 ekstrak etanol buah cabai rawit hijau sama atau berbeda. Pada
uji ini H0 yang digunakan adalah nilai IC50 baku kapsaisin tidak sama dengan nilai
IC50 ekstrak etanol buah cabai rawit hijau. Berdasarkan data pada Lampiran 15b,
hasil signifikansi yang diperoleh antara baku kapsaisin dengan ektrak etanol cabai
rawit hijau adalah 0,000. Karena nilai signifikansi yang diperoleh berbeda dengan
yang ditentukan yaitu 0,05, maka H0 ditolak. Sehingga dapat disimpulkan bahwa
nilai IC50 baku kapsaisin tidak sama dengan IC50 ekstrak etanol buah cabai rawit
hijau dimana nilai IC50 baku kapsaisin lebih kecil daripada nilai IC50 ekstrak
44 BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
1. Aktivitas antioksidan pada ekstrak etanol buah cabai rawit hijau menggunakan
metode DPPH yang dinyatakan dengan nilai IC50 sebesar 115,2±5,8 µg/mL,
didapatkan dengan ekstrapolasi.
2. Kandungan kapsaisin pada ekstrak etanol buah cabai rawit hijau menggunakan
metode KLT – densitometri sebesar (0,066±0,003) % (b/b).
B. Saran
1. Perlu dilakukan fraksinasi dengan metode yang sesuai untuk memisahkan
senyawa-senyawa yang terkandung dalam ekstrak etanol buah cabai rawit
hijau.
2. Perlu dilakukan validasi dalam melakukan penetapan kadar kapsaisin dengan