PENENTUAN KADAR FENOLIK TOTAL DAN STANDARDISASI EKSTRAK KULIT KAYU SECANG (CAESALPINIA SAPPAN L)
SKRIPSI
Diajukan kepada Fakultas Matematika dan Ilmu Pengetahuan Alam
Universitas Negeri Yogyakarta
Untuk Memenuhi Sebagian Persyaratan Guna
Memperoleh Gelar Sarjana Sains Kimia
Oleh :
Zainab Muthi’ah
12307144035
PROGRAM STUDI KIMIA
JURUSAN PENDIDIKAN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS NEGERI YOGYAKARTA
MOTTO
“Sesungguhnya beserta kesulitan itu ada kemudahan. Maka apabila engkau telah
selesai, maka tegaklah. Dan hanya kepada Tuhanmu, hendaknya engkau
berharap.”
(QS. Al-Insyiraa (94): 5-8)
“... Cukuplah Allah (menjadi penolong) bagi kami dan Dia sebaik-baik
pelindung.”
vi
PERSEMBAHAN
Dengan menyebut nama Allah Yang Maha Pengasih lagi Maha Penyayang
vii
PENENTUAN KADAR FENOLIK TOTAL DAN STANDARDISASI EKSTRAK KULIT KAYU SECANG (CAESALPINIA SAPPAN L)
Oleh : Zainab Muthiah NIM. 12307144035
Pembimbing: Dra., C. Budimarwanti, M.Si dan Idah Rosidah, M.Farm.Apt ABSTRAK
Penelitian ini bertujuan untuk mengetahui kadar fenolik total dalam ekstrak kental dan ekstrak kering, kandungan senyawa metabolit sekunder ekstrak kulit kayu secang (Caesalpinia Sappan L.) berdasarkan uji fitokimia kualitatif, dan standardisasi ekstrak kental dan ekstrak kering kulit kayu secang.
Proses pembuatan ekstrak dilakukan dengan metode maserasi-perkolasi menggunakan pelarut etanol 30%, 50%, dan 70%, dilanjutkan dengan penapisan fitokimia kualitatif terhadap alkaloid, flavanoid, tanin, steroid, dan saponin. Hasil ekstraksi dibuat ekstrak kental dan ekstrak kering kemudian ditentukan kadar fenolik totalnya menggunakan metode Folin-Cioulciateu dengan standar ekivalen asam galat (EAG) dan standardisasi ekstrak terhadap parameter spesifik dan parameter non-spesifik.
Hasil penapisan fitokimia menunjukkan ekstrak kulit kayu secang mengandung senyawa metabolit sekunder flavanoid, tanin/polifenol, steroid, dan saponin. Hasil penentuan kadar fenolik total dari ekstrak kulit kayu secang menggunakan pelarut etanol 30%, 50%, dan 70% bertrut-turut adalah 396,29 ± 10,85 mg EAG/g Ekstrak, 409,46 ± 14,16 mg EAG/g Ekstrak, dan 608,23 ± 28,13 mg EAG/g Ekstrak. Kadar fenolik total pada ekstrak kering terbaik adalah ekstrak kering (laktosa) sebesar 513,70 ± 44,52 mg EAG/g Ekstrak. Ekstrak kental dan ekstrak kering kulit kayu tanaman secang yang dibuat memenuhi standar yang telah ditentukan dalam FHI (Farmakope Herbal Indonesia).
viii
DETERMINATION OF TOTAL PHENOLIC CONTENT AND STANDARDIZATION OF SECANG (CAESALPINIA SAPPAN L.)
WOOD EXTRACT By :
Zainab Muthiah
Number of Student: 12307144035
Supervisor: Dra., C. Budimarwanti, M.Si and Idah Rosidah, M.Farm.Apt ABSTRACT
The aim of this research were to determine total phenolic content in secang (Caesalpinia sappan L) wood extract, to know it’s secondary metabolites content based on qualitative phytochemical screening, and it’s standardization of the thick and dried extract.
The production process of secang wood extract was carried out by maceration-percolation extraction method using ethanol 30%,50%,and 70% solvent, and then the qualitative phytochemical screening. The determination total phenolic content of thick and dried extract using Folin-Cioulciateu Assay method with gallic acid equivalent (EAG) standard and extracts standardization against specific and non-specific parameters.
Based on screening phytochemical, secang wood extract contains flavonoids, tannin/polyphenol, steroids, and sapponins. The total phenolic content of the extracts respectively from ethanol 30%, 50%, and 70% solvent was 396.29 ± 10.85 mg GAE/g Extract, 409.46 ± 14.16 mg GAE/g Extract, dan 608.23 ± 28.13 mg GAE/g Extract. Total phenolic content of the best dried extract (lactose) was 513.70 ± 44.52 mg GAE/g Extract. These Results were in accordance with FHI (Farmakope Herbal Indonesia) standard.
ix
KATA PENGANTAR
Assalamu’alaikum Warahmatullahi Wabarakatuh
Puji syukur saya panjatkan kehadirat Allah SWT atas limpahan rahmat, karunia, dan hidayah-Nya sehingga laporan tugas akhir skripsi ini mampu penulis selesaikan. Sholawat serta salam semoga terlimpah kepada Nabi Muhammad SAW beserta keluarga, sahabat, dan para pengikutnya sampai hari kiamat.
Pada kesempatan ini perkenankanlah penulis mengucapkan terima kasih kepada:
1. Bapak Dr. Hartono selaku Dekan FMIPA Universitas Negeri Yogyakarta yang telah memberikan izin dalam penulisan tugas akhir ini.
2. Bapak Drs. Jaslin Ikhsan, M.App.Sc., Ph.D selaku Ketua Program Studi dan Koordinator Tugas Akhir Skripsi Program Studi Kimia, Jurusan Pendidikan Kimia, Universitas Negeri Yogyakarta yang telah memberikan kelancaran pelayanan dan urusan akademik.
3. Ibu Dra. C. Budimarwanti, M.Si selaku ketua penguji dan dosen pembimbing utama yang telah memberikan bimbingan, pengarahan, dan saran.
4. Dr. Amanatie, M.Pd., M.Si. selaku sekretaris penguji, atas pertanyaan, kritik, dan saran yang diberikan.
5. Prof. Dr. Indyah Sulistyo Arty, M.S. selaku penguji utama dan Drs. Karim Theresih, SU selaku penguji pendamping, atas pertanyaan, kritik, dan saran yang diberikan.
6. Ibu Dra. Eddy Sulistyowati, M. Apt., MS. selaku Dosen Penasehat Akademik yang telah memberikan dorongan dalam penulisan tugas akhir ini.
x
disebutkan satu per satu yang telah memberikan, bimbingan, pengarahan, dan saran.
8. Semua pihak yang tidak dapat penulis sebutkan satu per satu yang telah membantu terselesaikannya penyusunan Tugas Akhir Skripsi ini.
Semoga laporan ini dapat bermanfaat.
Wassalamu’alaikum Warahmatullahi Wabarakatuh
xi
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN ... ii
HALAMAN PERNYATAAN ... iii
HALAMAN PENGESAHAN ... iv
HALAMAN MOTTO ... v
HALAMAN PERSEMBAHAN ... vi
ABSTRAK ... vii
ABSTRACT ... viii
KATA PENGANTAR ... ix
DAFTAR ISI ... Xi DAFTAR TABEL ... Xv DAFTAR GAMBAR ... xviii
DAFTAR LAMPIRAN ... xxi
BAB I PENDAHULUAN ... 1
A. Latar Belakang ... 1
B. Identifikasi Masalah ... 4
C. Pembatasan Masalah ... 5
D. Rumusan Masalah ... 6
E. Tujuan Penelitian ... 6
F. Manfaat Penelitian ... 7
BAB II KAJIAN PUSTAKA ... 8
A. KAJIAN PUSTAKA ... 8
1. Secang (Caesalpinia sappan L) ... 8
2. Ekstraksi ... 14
a. Metode Ekstraksi ... 14
b. Jenis Ekstrak ... 19
3. Uji Fitokimia ( Penapisan Fitokimia) ... 23
xii
5. Spektroskopi UV-Visibel ... 30
a. Absorpsi cahaya ... 30
b. Hukum Dasar Spektroskopi Absorpsi ... 31
c. Instrumen Spektroskopi UV-Vis ... 33
6. Standardisasi Ekstrak ... 35
a. Parameter Non-Spesifik ... 36
b. Parameter Spesifik ... 37
B. Penelitian yang Relevan ... 38
C. Kerangka Berfikir Teoritis ... 40
BAB III METODE PENELITIAN ... 42
A. Subjek dan Objek Penelitian ... 42
1. Subjek Penelitian ... 42
2. Objek Penelitian ... 42
B. Alat dan Bahan ... 42
1. Alat utama penelitian ... 42
2. Bahan utama penelitian ... 43
C. Prosedur Penelitian ... 44
1. Penyiapan Simplisia ... 44
2. Ekstraksi ... 44
3. Uji Fitokimia Pada ekstrak cair ... 46
a. Alkaloid ... 46
b. Uji Flavonoid ... 47
c. Uji Tanin ... 48
d. Uji Saponin ... 48
e. Uji Steroid ... 49
4. Standardisasi Ekstrak Kental Kayu Secang ... 49
a. Susut Pengeringan ... 49
b. Kadar Abu Total ... 50
c. Kadar Abu yang Larut Dalam Asam ... 51
d. Sisa Pelarut ... 51
xiii
5. Analisa Kandungan Total Fenolik ... 54
a. Mencari λ maksimal ... 54
b. Membuat Kurva Standar Asam Galat ... 54
c. Mengukur Absorbansi Sampel ... 54
6. Standardisasi Ekstrak Kering ... 55
a. Organoleptik ... 55
b. Kadar Air ... 55
c. Laju Alir ... 55
BAB IV HASIL PENELITIAN DAN PEMBAHASAN... 56
A. Hasil ... 56
1. Pembuatan Ekstrak Secang ... 56
2. Penapisan Fitokimia Kualitatif ... 57
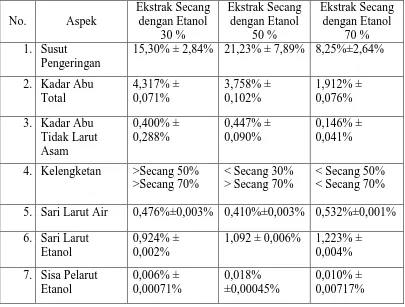
3. Standardisasi Ekstrak Kental ... 60
4. Kandungan Fenolik Total Ekstrak Kental... 60
5. Standardisasi Ekstrak Kering ... 61
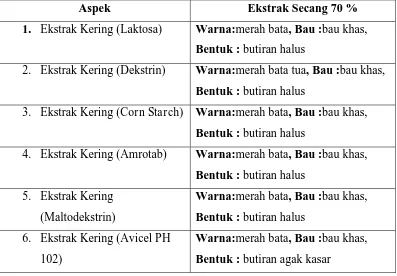
a. Organoleptik ... 61
b. Kadar Air ... 62
c. Sifat Alir ... 62
6. Kandungan Fenolik Total Ekstrak Kering ... 63
B. Pembahasan ... 63
1. Pembuatan Ekstrak Secang ... 63
2. Penapisan Fitokimia Kualitatif ... 64
a. Alkaloid ... 65
b. Tanin & Polifenol ... 67
c. Saponin ... 68
d. Flavanoid ... 68
e. Steroid ... 69
f. Pembandingan Sampel Ekstrak Secang Dengan Standar Asam Galat Menggunakan KLT ... 70
3. Standardisasi Ekstrak Kental ... 71
xiv
a. Mencari λ Maksimal untuk pengukuran dengan cara scaning dari
panjang Membuat Kurva Standar... 74
b. Membuat Kurva Standar ... 75
c. Mengukur Absorbansi Sampel ... 76
5. Standardisasi Ekstrak Kering ... 78
6. Kandungan Fenolik Total Ekstrak Kering ... 81
a. Membuat Kurva Standar ... 81
b. Mengukur Absorbansi Sampel ... 83
BAB V KESIMPULAN DAN SARAN... 85
A. Kesimpulan ... 85
B. Saran ... 86
DAFTAR PUSTAKA ... 87
xv
DAFTAR TABEL
Halaman
Tabel 1. Spektrum Tampak dan Warna-warna Komplementer ... 30
Tabel 2. Parameter Standar Ektrak Tanaman Obat ... 35
Tabel 3. Hasil Ekstrak Cair dan Ekstrak kental ... 56
Tabel 4. Hasil Skrining Fitokimia ekstrak etanol 30%, 50%, 70% kayu secang.. 58
Tabel 5. Hasil perhitungan Rf KLT... 59
Tabel 6. Standardisasi ekstrak kental ... 60
Tabel 7. Kadar Total Fenolik Ekstrak Kental ... 60
Tabel 8. Hasil Pengamatan Organoleptik ... 61
Tabel 9. Hasil Perhitungan Kadar Air ... 61
Tabel 10. Hasil Perhitungan Sifat Alir ... 62
Tabel 11. Kandungan Total Fenolik Ekstrak Kering 70% ... 63
Tabel 12. Absorbansi Standar Asam Galat Untuk Ekstrak Kental ... 75
Tabel 13. Absorbansi Standar Asam Galat Untuk Ekstrak Kering ... 82
Tabel 14. Perhitungan Parameter Susut Pengeringan ... 92
Tabel 15. Perhitungan Parameter Kadar Abu Total ... 93
Tabel 16. Perhitungan Parameter Kadar Abu Tak Larut Asam ... 94
Tabel 17. Perhitungan Parameter Sari Larut Air ... 95
Tabel 18. Perhitungan Parameter Sari Larut Etanol ... 96
Tabel 19. Data Kromatogram GC 1µl Standar A ulangan 1 ( etanol 1% n-propanol 0,5% ) ... 97
n-xvi
propanol 0,5% ) ... 99 Tabel 22. Data Kromatogram GC 1µl Standar A ulangan 4 ( etanol 1%
n-propanol 0,5% ) ... 100 Tabel 23. Data Kromatogram GC 1µl Standar B ulangan 1 ( etanol 0,75%
n-propanol 0,5% ) ... 101 Tabel 24. Data Kromatogram GC 1µl Standar B ulangan 2 ( etanol 0,75%
n-propanol 0,5% ) ... 102 Tabel 25. Data Kromatogram GC 1µl Standar B ulangan 3 ( etanol 0,75%
n-propanol 0,5% ) ... 103 Tabel 26. Data Kromatogram GC 1µl Standar C ulangan 1 ( etanol 0,5%
n-propanol 0,5% ) ... 104 Tabel 27. Data Kromatogram GC 1µl Standar C ulangan 2 ( etanol 0,5%
n-propanol 0,5% ) ... 105 Tabel 28. Data Kromatogram GC 1µl Standar D ulangan 1 ( etanol 0,25%
n-propanol 0,5% ) ... 106 Tabel 29. Data Kromatogram GC 1µl Standar D ulangan 2 ( etanol 0,25%
n-propanol 0,5% ) ... 107 Tabel 30. Data Kromatogram GC 1µl Standar D ulangan 3 ( etanol 0,25%
n-propanol 0,5% ) ... 108 Tabel 31. Data Kromatogram GC 1µl Standar D ulangan 4 ( etanol 0,25%
n-propanol 0,5% ) ... 109 Tabel 32. Data Kromatogram GC 1µl Standar E ulangan 1 ( etanol 0,1%
n-propanol 0,5% ) ... 110 Tabel 33. Data Kromatogram GC 1µl Standar E ulangan 2 ( etanol 0,1%
n-propanol 0,5% ) ... 111 Tabel 34. Data Kromatogram GC 1µl Standar E ulangan 3 ( etanol 0,1%
n-propanol 0,5% ) ... 112 Tabel 35. Data Kromatogram GC 1µl Standar E ulangan 4 ( etanol 0,1%
n-propanol 0,5% ) ... 113 Tabel 36. Data Kromatogram GC 1µl Standar E ulangan 5 ( etanol 0,1%
n-propanol 0,5% ) ... 114 Tabel 37. Data Kromatogram GC 1µl Standar F ulangan 1 ( etanol 0,05%
n-propanol 0,5% ) ... 115 Tabel 38. Data Kromatogram GC 1µl Standar F ulangan 2 ( etanol 0,05%
n-propanol 0,5% ) ... 116 Tabel 39. Data Kromatogram GC 1µl Standar F ulangan 3 ( etanol 0,05%
xvii
Tabel 42. Perhitungan Persamaan Regresi ... 120 Tabel 43. Data Kromatogram GC 1µl Ekstrak Secang Etanol 30% ulangan 1 ... 121 Tabel 44. Data Kromatogram GC 1µl Ekstrak Secang Etanol 30% ulangan 2 ... 122 Tabel 45. Data Kromatogram GC 1µl Ekstrak Secang Etanol 30% ulangan 3 ... 123 Tabel 46. Data Kromatogram GC 1µl Ekstrak Secang Etanol 50% ulangan 1 ... 124 Tabel 47. Data Kromatogram GC 1µl Ekstrak Secang Etanol 50% ulangan 2 ... 125 Tabel 48. Data Kromatogram GC 1µl Ekstrak Secang Etanol 50% ulangan 3 ... 126 Tabel 49. Data Kromatogram GC 1µl Ekstrak Secang Etanol 70% ulangan 1 ... 127 Tabel 50. Data Kromatogram GC 1µl Ekstrak Secang Etanol 70% ulangan 2 ... 128 Tabel 51. Data Kromatogram GC 1µl Ekstrak Secang Etanol 70% ulangan 3 ... 129 Tabel 52. Data Kromatogram GC 1µl Ekstrak Secang Etanol 70% ulangan 4.... 130 Tabel 53. Kadar Sisa Pelarut Etanol ekstrak Kental Secang ... 131 Tabel 54. Absorbansi Standar Asam Galat Untuk Ekstrak Kental ... 132 Tabel 55. Perhitungan Persamaan Garis Regresi Linier Asam Galat untuk
Ekstrak Kental ... 134
Tabel 56. Perhitungan Kadar Fenolik Total Ekstrak Kental Secang ... 135 Tabel 57. Perhitungan Kadar Air ... 137 Tabel 58. Perhitungan Sifat alir/ Sudut diam ... 138 Tabel 59. Perhitungan Persamaan Garis Regresi Linier Asam Galat untuk
xviii
DAFTAR GAMBAR
Halaman
Gambar 1. Struktur Asam Galat ... 10
Gambar 2. Struktur Kimia Tanin ... 12
Gambar 3. Struktur Asam Urat ... 13
Gambar 4. Persamaan perubahan warna folin (kuning) menjadi kompleks molybdenum (biru) ... 28
Gambar 5. Mekanisme metode folin-ciocalteu ... 29
Gambar 6. Landasan Hukum Lambert-Beer ... 31
Gambar 7. Skema Spektroskopi UV-Vis Single Beam ... 33
Gambar 8. Skema Spektroskopi UV-Vis Double-Beam ... 34
Gambar 9. Skema alat perkolator ... 45
Gambar 10. Ekstrak cair secang hasil ekstraksi maserasi-perkolasi ... 56
Gambar 11. Hasil Kromatografi Lapis Tipis Ekstrak Secang Berbagai variasi (a) Sinar Visibel, (b) UV 366 ... 59
Gambar 12. Reaksi uji Mayer ... 66
Gambar 13. Reaksi Uji Wagner ... 66
Gambar 14. Persamaan reaksi salah satu gugus hidroksil pada senyawa tanin berekasi dengan reagen FeCl3 menghasilkan kompleks warna dan endapan ... 67
Gambar 15. Reaksi hidrolisis saponin dalam air ... 68
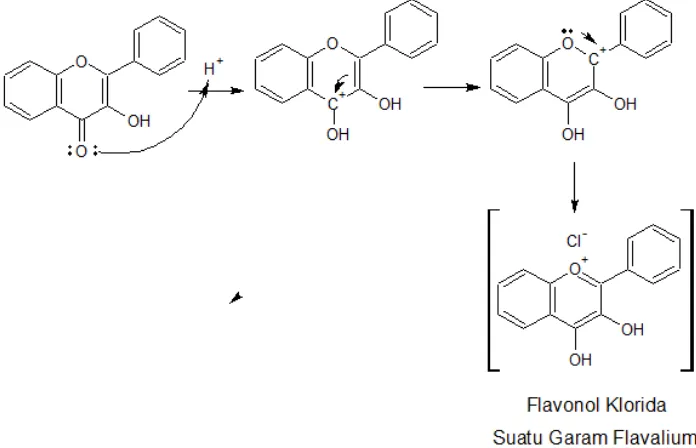
Gambar 16. Persamaan reaksi pembentukan garam flavilium ... 69
Gambar 17. Persamaan reaksi terpenoid/steroid dengan H2SO4 yang menyebabkan perubahan warna ... 70
Gambar 18. Kurva Standar Asam Galat Untuk Ekstrak Kental ... 75
Gambar 19. Grafik Perbandingan Kadar Fenolik Total Sampel ... 77
Gambar 20. Kurva Standar Asam Galat Untuk Ekstrak Kering ... 82
Gambar 21. Desain penelitian ... 91
xix
Gambar 22. Kromatogram GC 1µl Standar A ulangan 2 ( etanol 1% n-propanol 0,5% ) ... 97 Gambar 23. Kromatogram GC 1µl Standar A ulangan 3 ( etanol 1% n-propanol
0,5% ) ... 98 Gambar 24. Kromatogram GC 1µl Standar A ulangan 4 ( etanol 1% n-propanol
0,5% ) ... 99 Gambar 25. Kromatogram GC 1µl Standar B ulangan 1 ( etanol 0,75%
n-propanol 0,5% ) ... 100 Gambar 26. Kromatogram GC 1µl Standar B ulangan 2 ( etanol 0,75%
n-propanol 0,5% ) ... 101 Gambar 27. Kromatogram GC 1µl Standar B ulangan 3 ( etanol 0,75%
n-propanol 0,5% ) ... 102 Gambar 28. Kromatogram GC 1µl Standar C ulangan 1 ( etanol 0,5%
n-propanol 0,5% ) ... 103 Gambar 29. Kromatogram GC 1µl Standar C ulangan 2 ( etanol 0,5%
n-propanol 0,5% ) ... 104 Gambar 30. Kromatogram GC 1µl Standar D ulangan 1 ( etanol 0,25%
n-propanol 0,5% ) ... 105 Gambar 31. Kromatogram GC 1µl Standar D ulangan 2 ( etanol 0,25%
n-propanol 0,5% ) ... 106 Gambar 32. Kromatogram GC 1µl Standar D ulangan 3 ( etanol 0,25%
n-propanol 0,5% ) ... 107 Gambar 33. Kromatogram GC 1µl Standar D ulangan 4 ( etanol 0,25%
n-propanol 0,5% ) ... 108 Gambar 34. Kromatogram GC 1µl Standar E ulangan 1 ( etanol 0,1%
n-propanol 0,5% ) ... 109 Gambar 35. Kromatogram GC 1µl Standar E ulangan 2 ( etanol 0,1%
n-propanol 0,5% ) ... 110 Gambar 36. Kromatogram GC 1µl Standar E ulangan 3 ( etanol 0,1%
xx
propanol 0,5% ) ... 112
Gambar 38. Kromatogram GC 1µl Standar E ulangan 5 ( etanol 0,1% n-propanol 0,5% ) ... 113
Gambar 39. Kromatogram GC 1µl Standar F ulangan 1 ( etanol 0,05% n-propanol 0,5% ) ... 114
Gambar 40. Kromatogram GC 1µl Standar F ulangan 2 ( etanol 0,05% n-propanol 0,5% ) ... 115
Gambar 41. Kromatogram GC 1µl Standar F ulangan 3 ( etanol 0,05% n-propanol 0,5% ) ... 116
Gambar 42. Kurva Standar Sisa Pelarut Etanol ... 117
Gambar 43. Kromatogram GC 1µl Ekstrak Secang Etanol 30% ulangan 1... 121
Gambar 44. Kromatogram GC 1µl Ekstrak Secang Etanol 30% ulangan 2 ... 122
Gambar 45. Kromatogram GC 1µl Ekstrak Secang Etanol 30% ulangan 3... 123
Gambar 46. Kromatogram GC 1µl Ekstrak Secang Etanol 50% ulangan 1... 124
Gambar 47. Kromatogram GC 1µl Ekstrak Secang Etanol 50% ulangan 2... 125
Gambar 48. Kromatogram GC 1µl Ekstrak Secang Etanol 50% ulangan 3... 126
Gambar 49. Kromatogram GC 1µl Ekstrak Secang Etanol 70% ulangan 1... 127
Gambar 50. Kromatogram GC 1µl Ekstrak Secang Etanol 70% ulangan 2... 128
Gambar 51. Kromatogram GC 1µl Ekstrak Secang Etanol 70% ulangan 3... 129
Gambar 52. Kromatogram GC 1µl Ekstrak Secang Etanol 70% ulangan 4 ... 130
xxi
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Desain Penelitian ... 91
Lampiran 2. Perhitungan Standardisasi Ekstrak Kental (Susut Pengeringan) ... 92
Lampiran 3. Perhitungan Standardisasi Ekstrak Kental (Kadar Abu Total)... 93
Lampiran 4. Perhitungan Standardisasi Ekstrak Kental (Kadar Abu Tidak Larut Asam) ... 94 Lampiran 5. Perhitungan Standardisasi Ekstrak Kental (Sari Larut Air) ... 95
Lampiran 6. Perhitungan Standardisasi Ekstrak Kental (Sari Larut Etanol)... 96
Lampiran 7. Data Kromatogram Standar Etanol dalam penentuan Sisa Pelarut Etanol (Standardisasi Ekstrak Kental) ... 97 Lampiran 8. Perhitungan Kurva Standar Etanol dalam penentuan Sisa Pelarut Etanol (Standardisasi Ekstrak Kental)... 117 Lampiran 9. Data Kromatogram Pengukuran Sampel dalam penentuan Sisa Pelarut Etanol (Standardisasi Ekstrak Kental) ... 121 Lampiran 10. Perhitungan Sisa Pelarut Etanol dalam sampel (Standardisasi Ekstrak Kental) ... 131 Lampiran 11. Kandungan Fenolik Total dalam Ekstrak Kental ... 132
Lampiran 12. Standardisasi Ekstrak Kering Organoleptik ... 136
Lampiran 13. Perhitungan Kadar Air Ekstrak Kering ... 137
Lampiran 14. Perhitungan Sifat Alir Ekstrak Kering ... 138
1
BAB I PENDAHULUAN
A. Latar Belakang Masalah
Hasil alam yakni yang berasal dari tanaman maupun hewan sudah sejak lama dimanfaatkan manusia dalam berbagai aspek kehidupan. Salah satu penggunaan hasil alam yang paling sering digunakan adalah sebagai obat. Penggunaan tanaman sebagai obat sudah tercatat sejak 5000 tahun yang lalu, selain itu pengobatan herbal juga sudah dikenal di China selama lebih dari 2000 tahun, dalam litelatur kuno China tercatat lebih dari 100.000 resep pengobatan herbal tradisional China yang menggunakan tanaman sebagai bahan utamanya (Tri Joko Raharjo,2013,1-3). Hasil alam juga memegang peranan penting dalam pencarian obat-obatan modern, seperti sitesis aspirin, taxol, efedrin, dan kuinin serta masih banyak lagi, dimana merupakan senyawa alam yang memiliki kegunaan farmakologis tertentu.
Pengembangan obat baru dari hasil alam memerlukan waktu yang lama, serta sangat dimungkinkan dari sekian ribu senyawa yang ditemukan hanya beberapa yang sampai digunakan menjadi obat, tahap-tahap dalam pengembangan senyawa hasil alam menjadi obat dengan cara sebagai berikut : pencarian senyawa aktif secara farmakologis yang struktur senyawanya dijadikan dasar untuk pengembangan obat, uji praklinik (uji farmakologi terhadap hewan), uji klinis (tes efek obat terhadap manusia), pendaftaran obat, dan terakhir persetujuan dari FDA (Food and Drug Administration). Tahap-tahap seperti diatas memerlukan waktu
7-2
9). Proses pengembangan obat tidak selalu berjalan mulus, suatu tanaman maupun ekstrak tanaman yang sudah digunakan dalam pengobatan dalam waktu yang lama dan terbukti efektif, setelah diisolasi senyawa-senyawanya belum tentu menghasilkan senyawa yang aktif, serta tidak selalu senyawa aktif diperoleh dari tanaman obat atau ekstrak aktif. Penjelasan yang masuk akal yang mungkin dari fenomena tersebut adalah kemungkinan bahwa aktivitas yang terbaca dalam ekstrak tanaman dimungkinkan merupakan hasil sinergi dari berbagai senyawa, yang mana senyawa – senyawa tersebut apabila dipisahkan tidak mempunyai aktifias seperti yang diharapkan (Tri Joko Raharjo, 2003,9).
3
Akan tetapi allopurinol memiliki beberapa efek samping yaitu kemerahan pada kulit, leukopenia, kadang–kadang terjadi toksisitas pada gastrointestinal dan meningkatkan serangan akut gout pada awal terapi (Dipiro dkk., 2005). Oleh karena itu, sekarang masyarakat banyak yang menggunakan tanaman obat sebagai obat tradisional dalam mengatasi penyakit hiperurisemia karena memiliki efek samping yang relatif aman, mudah didapatkan, dan harganya relatif murah dibandingkan dengan obat sintesis.
Berdasarkan penelitian yang telah dilakukan secang mampu menghambat aktivitas enzim xantin oksidase sampai 56,47%, yang memiliki 2/3 dari aktivitas penghambat enzim xantin oksidase dari obat sintesis allopurinol yakni sebesar 87,47% (Pertamawati dan Mutia, 2015, 12-15). Menurut literatur penghambatan kerja enzim xantin oksidase disebabkan olehkandungan gugus fenolik yang tinggi dalam tanaman secang. Selain dapat mengahambat kerja xantin oksidase gugus fenolik juga dapat dijadikan antioksidan, yakni sumber antioksidan alami.
4
lingkungan seperti infeksi oleh mikroba patogen, mekanik, dan sinar UV atau tingkat cahaya tampak yang berlebihan (Farah dan Donangelo, 2006).
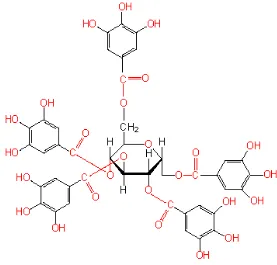
Kulit kayu secang (Caesalpinia sappan L.) secara empiris dimanfaatkan sebagai bahan untuk pengobatan penyakit asam urat. Berbagai macam zat yang terkandung dalam kulit kayu secang antara lain brazilin, alkaloid, flvonoid, saponin, tanin, fenilpropana dan terpenoid. Selain itu juga mengandung asam galat, delta-aphellandrene, oscimene, resin dan resorin (Xu dkk, 1994. )
Penelitian mengenai efek secang sebagai agen antihiperurisemia, anti bakteri, obat kanker dan masih banyak lagi telah banyak dikembangkan, sedangkan penelitian mengenai standardisasi ekstrak secang terhadap berbagai konsentrasi pelarut belum banyak dilakukan, maka dilakukan penelitian terhadap standardisasi ekstrak herbal secang terstandar dengan berbagai pelarut, sehingga diperoleh ekstrak herbal secang terstandar.
B. Identifikasi Masalah
Berdasarkan latar belakang penelitian ini maka dapat diidentifikasi beberapa masalah seperti berikut:
1. Tanaman yang akan dibuat ekstrak
2. Jenis metode yang digunakan untuk ekstraksi 3. Pelarut yang digunakan untuk mengekstraki
4. Metode identifikasi yang digunakan untuk mengetahui kandungan senyawa metabolit sekunder yang terdapat dalam ekstrak
5. Senyawa penanda (senyawa marker) yang akan dianalisa
5
7. Aspek Standardisasi obat herbal (berasal dari bahan alami) yang digunakan untuk ekstrak kering maupun kental
C. Pembatasan Masalah
Batasan masalah dalam penelitian “Penentuan Kadar Fenolik Total Dan
Standardisasi Ekstrak Kulit Kayu Secang (Caesalpinia Sappan L) “ ini adalah:
1. Tanaman yang akan dibuat ekstrak adalah kulit kayu tanaman secang (Caesalpina Sappan L).
2. Pembuatan ekstrak dilakukan dengan metode ekstraksi maserasi-perkolasi. 3. Pelarut yang digunakan untuk mengekstraksi adalah etanol 30%, 50%, dan
70%.
4. Metode yang digunakan untuk identifikasi kandungan senyawa metabolit sekunder yang terdapat dalam ekstrak kulit kyu secang aadalah penapisan fitokimia secara kualitatif.
5. Senyawa penanda (senyawa marker) yang akan dianalisa adalah senyawa fenolik total.
6. Penentuan kadar fenolik total dilakukan dengan instrumen spektroskopi UV-Visible.
6
D. Rumusan Masalah
Rumusan masalah dari penelitian “Penentuan Kadar Fenolik Total Dan
Standardisasi Ekstrak Kulit Kayu Secang (Caesalpinia Sappan L) “ yaitu:
1. Berapa kadar fenolik total dalam ekstrak kental dan ekstrak kering kayu secang (Caesalpinia Sappan L.) yang dibuat?
2. Apa saja kandungan senyawa metabolit sekunder yang terdapat dalam ekstrak kayu secang (Caesalpinia Sappan L.) berdasarkan uji fitokimia kualitatif? 3. Apakah ekstrak kayu kulit secang yang telah dibuat memenuhi standar yang
telah ditetapkan dalam FHI (Farmakope Herbal Indonesia? E. Tujuan Penelitian
Tujuan dari penelitian “Penentuan Kadar Fenolik Total Dan Standardisasi Ekstrak Kulit Kayu Secang (Caesalpinia Sappan L)“ yaitu:
1. Mengetahui kadar fenolik total yang terdapat dalam ekstrak kental dan ekstrak kering kulit kayu secang (Caesalpinia Sappan L.).
2. Mengetahui kandungan metabolit sekunder yang terdapat dalam ekstrak kayu secang (Caesalpinia Sappan L.) berdasarkan uji fitokimia kualitatif.
7
F. Manfaat Penelitian
Manfaat dari penelitian “Penentuan Kadar Fenolik Total Dan Standardisasi Ekstrak Kulit Kayu Secang (Caesalpinia Sappan L) “ yaitu:
1. Memberikan pengetahuan tentang kadar fenolik total yang terdapat dalam ekstrak kental dan ekstrak kering kayu secang (Caesalpinia Sappan L.). 2. Memberikan pengetahuan tentang kandungan senyawa metabolit sekunder
yang terdapat dalam ekstrak kayu secang (Caesalpinia Sappan L.).
8
BAB II
KAJIAN PUSTAKA
A. KAJIAN PUSTAKA
1. Secang (Caesalpinia sappan L) a. Deskripsi
Secang atau sepang (Caesalpinia sappan L.) adalah pohon anggota suku polong-polongan (Fabaceae) yang dimanfaatkan kulit kayu dan kayunya sebagai komoditi perdagangan rempah-rempah. Secang merupakan semak atau pohon kecil dengan tinggi sampai 10 meter. Ranting-ranting secang berlentisel dan berduri dengan bentuk duri bengkok dan tersebar. Secang memiliki daun majemuk dengan panjang 25 sampai 30 cm, bersirip, setiap sirip mempunyai 10 sampai 20 pasang anak daun yang berhadapan. Anak daun tersebut tidak bertangkai, berbentuk lonjong, pangkal hampir rompang ujung bundar dan sisinya agak sejajar (BPOM RI , 2004: 15).
9
hiniaga, sinyiang, singiang (Halmahera Utara), sunyiang (Ternate), roro (Tidore), sappanwood (Inggris), dan suou (Jepang). Kerabat dekatnya yang berasal dari Amerika Selatan, kayu brazil atau brezel (C. echinata), juga dimanfaatkan untuk hal yang sama (BPOM RI, 2008: 18).
b. Klasifikasi Tanaman Secang
Kerajaan :Plantae (Tumbuhan)
Divisi :Magnoliophyta (Tumbuhan berbunga) Kelas :Magnoliopsida (Berkeping dua / dikotil)
Ordo :Fabales
Famili :Fabaceae(Polong-polongan)
Genus :Caesalpinia
Spesies :C. Sappan L
Nama binomial :Caesalpinia sappan L.(Depkes, 2008:19)
c. Kandungan kimia
10
taninyang kebanyakan terdapat dalam batang pohonnya, berikut penjelasan mengenai kedua senyawa tersebut.
1) Asam Galat (Asam 3,4,5-trihidroksibenzoat)
Asam galat adalah senyawa golongan asam fenolik C6-C1 atau hidroksibenzoat, yaitu asam 3,4,5-trihidroksibenzoat. Asal kata galat adalah kata galle dalam bahasa Prancis yang berarti pembengkakan pada jaringan tanaman setelah terserang serangga parasit. Senyawa ini dapat ditemukan pada daun ek dan anggur dan memiliki aktivitas sebagai antioksidan (penangkal radikal bebas). Asam galat adalah subunit dari galotanin, yaitu polimer heterogen yang mengandung beberapa asam galat yang saling terikat dengan glukosa (monosakarida). galotanin dapat menghambat pertumbuhan tanaman karena dapat merombak enzim sitoplasma dengan cara mendenaturasi protein (dimana enzim terdiri dari protein). Struktur senyawa asam galat tertera pada Gambar 1.
Gambar 1. Struktur Asam Galat / Asam 3,4,5-trihidroksibenzoat (Mujica.,dkk, 2009, 652)
2) Asam Tanat (Tanin)
11
tanaman. Tanin merupakan polifenol yang larut dalam air dengan berat molekul biasanya berkisar 1000-3000 (Waterman dan Mole tahun 1994, Kraus dkk., 2003). Menurut definisi, tanin mampu menjadi pengompleks dan kemudian mempercepat pengendapan protein serta dapat mengikat makromolekul lainnya (Zucker, 1983). Tanin merupakan campuran senyawa polifenol yang jika semakin banyak jumlah gugus fenolik maka semakin besar ukuran molekulnya. Apabila dilihat dengan mikroskop, tanin tampak sebagai butir berwarna kuning, merah, atau cokelat.
Tanin dapat ditemukan di daun, tunas, biji, akar, dan batang jaringan. Sebagai contoh dalam jaringan batang yakni di daerah pertumbuhan pohon, seperti floem sekunder dan xylem dan lapisan antara korteks dan epidermis. Tanin dapat membantu mengatur pertumbuhan jaringan ini.
Tanin dapat bereaksi dengan protein membentuk kopolimer mantap yang tak larut dalam air. Dalam industri, tanin adalah senyawa yang berasal dari tumbuhan, yang mampu mengubah kulit hewan yang mentah menjadi kulit siap pakai karena kemampuannya menyambung silang protein.
12
[image:33.595.189.466.232.497.2]Secara kimiawi, taninmemiliki sifat-sifat diantaranya: merupakan senyawa kompleks dalam bentuk campuran polifenol yang sukar dipisahkan sehingga sukar mengkristal, tanin dapat diidentifikasi dengan kromotografi, dan senyawa fenol dari tanin mempunyai aksi astrigensia (zat yang dapat meringkas pori), antiseptik dan pemberi warna
Gambar 2. Struktur Kimia Tanin (1,2,3,4,6-pentagalat-β-D-glukopiranosa) (Mujica.,dkk, 2009, 652)
d. Efek farmakologis
13
malaria, tetanus, tumor, asam urat, kanker, anti bakteri dan radang selaput lendir mata (Kusmiati, 2014).
Kandungan yang terdapat dalam batang pohon secang dapat bekerja sebagai penghenti pendarahan, pembersih darah, penawar racun, dan obat antiseptik . Karena tanaman ini mengandung senyawa anti bakteri dan bersifat anti koagulasi atau anti penggumpalan, maka secang dapat digumakan sebagai obat diare, batuk dan dapat menyembuhkan luka. Menurut penelitian lain secang juga memiliki aktivitas anti mikroba (Candra dan Saravakumar,2013,172-174)
Pertamawati dan Mutia(2015) menyatakan bahwasecang mampu menghambat aktivitas enzim xantin oksidase sampai 56,47%, 2/3 dari aktivitas penghambat enzim xantin oksidase dari allopurinol (87,47%). Enzim xantin oksidase dalam tubuh merupakan enzim yang bekerja dalam pembentuk asam purin yang apabila menumpuk akan menjadi penyakit asam urat (hiperurisemia). Berikut ini penjelasan mengenai penyakit asam urat.
14
[image:35.595.251.403.139.242.2]menjadi xantin yang selanjutnya diubah menjadi asam urat, struktur asam urat seperti pada Gambar 3.
Gambar 3. Struktur Asam Urat 2. Ekstraksi
Ekstraksi adalah metode pemisahan bahan dari suatu zat padat maupun cair berdasarkan kelarutan bahan yang akan dipisahkan. Ekstrak merupakan sediaan pekat yang diperoleh dari proses ekstraksi simplisia nabati atau simplisia hewani menggunakan pelarut yang sesuai,kemudian pelarut diuapkan menggunakan alat evaporator.
a. Metode Ekstraksi
Berdasarkan suhuekstraksi, metode ekstraksi dibagi menjadi dua, yakni metode dingin dan metode panas.
1) Metode Dingin
Merupakan metode ekstraksi tanpa penaikan atau penambahan temperatur awal (ekstraksi dilakukan pada temperatur ruang), berikut ini merupakan ekstraksi yang termasuk metode dingin:
a) Maserasi
15
suhu ruang kemudian simplisia direndam beberapa lama, biasanya selama 24 jam. Remaserasi dilakukann dengan menambahkan pelarut pada residu setelah dilakukan penyaringan ekstrak hasil maserasi yang pertama dan seterusnya.
b) Perkolasi
Perkolasi merupakan cara ekstraksi sederhana seperti halnya maserasi. Pada perkolasi, pelarut yang digunakan selalu baru,karena pelarut dialirkan melalui serbuk simplisia dan kemudian ditampung kedalam sebuah wadah yang ada selang menuju pompa, sehingga pelarut dipompa kembali ke tabung perkolasi.
Prinsip perkolasi adalah sebagai berikut: serbuk simplisia ditempatkan dalam suatu bejana silinder, yang bagian bawahnya diberi sekat berpori. Cairan penyari dialirkan dari atas ke bawah melalui serbuk tersebut, cairan penyari akan melarutkan zat aktif sel-sel yang dilalui sampai mencapai keadaan jenuh. Gerak kebawah disebabkan oleh kekuatan gaya beratnya sendiri dan cairan diatasnya, dikurangi dengan daya kapiler yang cenderung untuk menahan. Kekuatan berperan pada perkolasi antara lain: gaya berat, kekentalan, daya larut, tegangan permukaan, difusi, osmosa, adesi, daya kapiler dan daya geseran.
16
pada ekstraksi bahan alam terlihat pada tetesan perkolat yang sudah tidak berwarna.
Cara perkolasi lebih baik dibandingkan dengan cara maserasi karena: (1) Sirkulasi pelarut menyebabkan adanya pergantian larutan yang
terjadi dengan larutan yang konsentrasinya lebih rendah, sehingga meningkatkan derajat perbedaan konsentrasi larutan.
(2) Ruangan diantara serbuk-serbuk simplisia membentuk saluran tempat mengalir cairan penyari.karena kecilnya saluran kapiler tersebut,maka kecepatan pelarut cukup untuk mengurangi lapisan batas,sehingga dapat meningkatkan perbedaan konsentrasi larutan. c) Maserasi-perkolasi
Maserasi-perkolasi merupakan penggabungan metode maserasi dan perkolasi, dimana proses maserasi adalah perendaman, sedangkan proses perkolasi adalah proses sirkulasi pelarut, metode maserasi-perkolasi ini juga tidak menggunakan pemanasan, pada metode ini lamanya perendaman serbuk simplisia adalah 30 menit serta lamanya sirkulasi pelarut sekitar 90 menit.
2) Metode Panas
17
a) Refluks
Refluks merupakan ekstraksi menggunakan pelarut pada suhu titik didihnya selama waktu tertentu dan jumlah pelarutnya terbatas yang relatif konstan, menggunakan labu refluks leher tiga dengan rangkaian pendingin balik untuk mencegah pelarut menguap ke luar sistem refluks. b) Soxhlet
Soxhlet merupakan ekstraksi menggunakan pelarut yang disirkulasi, pada umumnya dilakukan menggunakan alat khusus soxhlet sehingga terjadi ekstraksi secara terus menerus. Proses ekstraksi ini dilakukan pada suhu titik didih pelarut dengan pelarut yang relatif konstan dengan adanya pendingin balik. Perbedaan soxhletasi dengan metode maserasi dan perkolasi adalah pada soxhletasi dilakukan pada suhu tertentu (suhu titik didih pelarut) sedangkan pada maserasi dilakukan pada suhu ruangan.
c) Digesti
Digesti adalah metode ekstraksi dengan cara maserasi kinetik (pengadukan kontinyu) menggunakan pemanasan lemah, yaitu pada suhu 40° – 50°C. Cara maserasi ini hanya dapat dilakukan untuk simplisia yang zat aktifnya tahan terhadap pemanasan. Dengan pemanasan diperoleh keuntungan antara lain:
18
(2) Daya melarutkan cairan penyari akan meningkat, sehingga pemanasan tersebut mempunyai pengaruh yang sama dengan pengadukan.
(3) Koefisien difusi berbanding lurus dengan suhu dan berbanding terbalik dengan kekentalan, sehingga kenaikan suhu akan berpengaruhpada kecepatan difusi. Umumnya kelarutan zat aktif akan meningkat bila suhu dinaikkan.
Jika cairan penyari mudah menguap pada suhu yang digunakan, maka perlu dilengkapi dengan pendingin balik, sehingga cairan akan menguap kembali ke dalam bejana.
d) Infus
Infus adalah ekstraksi dengan pelarut air pada temperatur pemanasan air (bejana infus tercelup dalam air penangas yang mendidih), temperatur terukur (96-98 °C) selama waktu tertentu antara 15 hingga 20 menit.
b. Jenis Ekstrak 1) Ekstrak Cair
19
2) Ekstrak Kental
Ekstrak kental merupakan ekstrak kering yang telah melalui tahapan evaporasi (penguapan pelarut) sehingga ekstrak berbentuk pasta dengan sisa sedikit pelarut.
3) Ekstrak Kering
Ekstrak kering merupakan hasil olahan dari ekstrak kental yang telah melalui tahapan penambahan filler dan pengeringan di dalam oven vakum, penambahan filler juga dilakukan untuk mendapatkan tekstur ekstrak kering yang baik, berikut ini penjelasan mengenai filler.
a) Pengertian Filler
Bahan pengisi juga disebut bahan pengencer / Filler / Diluents. Penambahan filler bertujuan untuk menyesuaikan bobot dan ukuran tablet sesuai yang dipersyaratkan, untuk membantu kemudahan dalam pembuatan, dan meningkatkan mutu sediaan tablet.
20
dibandingkan daya tarik zat pada lembab atau jumlah lembab yang ada.Berdasarkan kelarutan filler dalam air dibagi menjadi 2 macam yaitu: (1) Filler yang larut air: laktosa sukrosa, glukosa, manitol, sorbitol (2) Filler tidak larut air: dikalsium fosfat, kalsium fosfat, amilum
termodifikasi, mikrokristalin selulosa.
Kriteria yang harus dimiliki oleh filler antara lain, sebagai berikut: harus non toksik, tidak kontraindikasi antar bahan, stabil secara fisik dan kimia, Bebas mikroba, netral secara fisiologis, tidak mengganggu metabolisme obat
Jenis filler untuk tablet kempa sangat banyak, tetapi yang paling sering adalah laktosa. Banyak jenis laktosa dan semua laktosa tersebut tidak sama baiknya secara kimia, fisikokimia atau fungsional. Oleh karena itu dalam memilih filler beberapa faktor harus dipertimbangkan. b) Jenis-Jenis Filler
Berikut ini beberapa jenisfiller yang sering digunakan dalam pembuatan ekstrak kering:
(1) Laktosa
21
basah atau metode kempa langsung. Laktosa merupakan filler yang baik sekali, digunakan dalam tablet yang mengandung zat aktif berkonsentrasi rendah karena mudah campur homogen. Selain itu harga laktosa lebih murah daripadafiller lainnya.
(2) Pati (Amilum)
Tablet yang menggunakan pati dalam konsentrasi tinggi sering lunak dan sulit dikeringkan. Secara komersial pati dapat mengandung lembab yang beragam antara 11-14%. Pati pada umumnya digunakan sebagai filler dan pengikat dalam tablet yang dibuat dengan metode granulasi basah dan kering. Satu-satunya pati modifikasi yang telah diterima sebagai filler dalam kempa langsung adalah Starch 1500
(3) Starch 1500 / Corn Starch
Starch 1500 secara fisik dibuat dari pati jagung. Apabila
dikempa sendirian, zat ini mudah melubrikasi dan hancur. Sehingga pada starch 1500 harus dikombinasikan dengan 5-10% komponen yang tidak
bersifat lubrikan. Starch 1500 memiliki kemampuan mengalir yang lebih baik daripada pati biasa dan memenuhi spesifikasi untuk pati pragelatinasi. Starch 1500 memiliki kandungan lembab yang cukup tinggi yaitu 12-13% ( Siregar, C.J.P dan Wikarsa, S : 2010).
(4) Mikrokristalin Selulosa / Avicel PH 102
22
kekerasan dan friabilitas yang baik. Avicel PH 103 juga baik digunakan untuk tablet kempa langsung.
Avicel filler yang relatif mahal dibandingkan dengan laktosa atau amilum. Avicel memiliki fungsi kemampuan yang baik sebagai pengikat maupun desintegran dalam beberapa formula tablet sehingga sangat berguna dalam tablet yang memerlukan peningkatan kekuatan kohesif, tetapi tidak boleh memperpanjang waktu hancur yang dipersyaratkan. Menghasilkan tablet yang keras dengan tekanan kecil) kompresibilitas baik) dan friabilitas tablet rendah, waktu stabilitas panjang. (Lachman, L., dkk : 1994).
(5) Maltodekstrin
Maltodekstrin adalah suatu polisakarida yang digunakan sebagai bahan tambahan pangan. Senyawa ini dibuat dari amilum dengan cara hidrolisis parsial, dan biasanya dijumpai dalam bentuk serbuk putih yang dikeringkan dengan cara spray-drying dan bersifat higroskopis. Maltodekstrin mudah dicerna, diserap dengan cepat sebagai glukosa, dan berasa sedikit manis atau hampir tak berasa. Umum digunakan dalam produksi soda dan kembang gula. Dapat pula dijumpai sebagai bahan campuran berbagai makanan olahan.
23
binaragawan dan atlet lainnya dalam bentuk serbuk, karena ini adalah karbohidrat yang mudah dicerna sehingga dapat mensupai energi yang cukup ke seluruh tubuh untuk memicu sintesis protein.
Maltodekstrin digunakan sebagai bahan tambahan yang murah untuk menebalkan makanan seperti pada formula bayi. Ini digunakan juga sebagai filler pada pengganti gula dan produk lainnya. Maltodekstrin mempunya indeks glikemik antara 85 hingga 103.
(6) Dekstrin
Dekstrin merupakan sejenis oligosakarida yang dihasilkan dari aktivitas pemecahan polisakarida (pati atau glikogen). Dekstrin dapat
berupa α-1,6 dan α-1,4. Dekstrin dapat digunakan untuk berbagai pelapis
untuk produk farmaseutikal, lem yang dapat dimakan, dan sealant.
Filler yang lain antara lain seperti Sorbitol, Emdex, Dekstrosa,
Sugartab, Trikalsium Fosfat, Kalsium Sulfat Dihidrat. 3. Uji Fitokimia ( Penapisan Fitokimia)
Penapisan fitokimia atau sering disebut skrining fitokimia adalah tahapan awal untuk mengidentifikasi kandungan kimia yang terkandung dalam tumbuhan, karena pada tahap ini kita bisa mengetahdapat diketahui golongan senyawa kimia yang dikandung tumbuhan yang sedang diuji.
24
pereaksi yang spesifik karena dirasakan lebih sederhana, dalam penelitian ini akan dilakukan uji fitokimia serta uji KLT, seperti pada uji-uji berikut ini:
a. Uji alkaloid.
25
Uji tanin dan polifenol dilakukan dengan mengekstrak sampel menggunakan akuades panas, kemudian didinginkan. Setelah itu ditambahkan NaCl 10% dan disaring. Filtrat dibagi 3 bagian A, B, dan C. Filtrat A digunakan sebagai blangko, ke dalam filtrat B ditambahkan reagen FeCl3, dan ke dalam filtrat C ditambah garam gelatin. Kemudian diamati perubahan yang terjadi. Apabila pada filtrat B terjadi perubahan warna hal tersebut menunjukkan adanya tanin ataupun polifenol dikarenakan apabila tanin atau polifenol bereaksi dengan FeCl3 akan terbentuk sebuah kompleks warna. Apabila pada filtrat C terjadi pengendapan hal tersebut menunjukkan adanya tanin maupun polifenol dikarenakan tanin dapat mengendapkan protein dalam gelatin yang berupa kopolimer mantap yang tidak larut dalam air c. Uji saponin.
Uji Saponin dilakukan dengan metode Forth yaitu dengan cara memasukkan sampel kedalam tabung reaksi, kemudian ditambahkan 10 mL akuades lalu dikocok selama 30 detik, diamati perubahan yang terjadi. Apabila terbentuk busa yang mantap (tidak hilang selama 30 detik) maka identifikasi menunjukkan adanya saponin.
d. Uji flavonoid.
26
etanol kemudian disaring. Filtrat dibagi 4 bagian A, B, dan C. Filtrat A sebagai blangko, filtrat B ditambahkan HCl pekat kemudian dipanaskan pada penangas air, jika terjadi perubahan warna merah tua sampai ungu menunjukkan hasil yang positif (metode Bate Smith-Metchalf). Filtrat C ditambahkan HCl dan logam Mg kemudian diamati perubahan warna yang terjadi (metode Wilstater). Warna merah sampai jingga diberikan oleh senyawa flavon, warna merah tua diberikan oleh flavonol atau flavonon, warna hijau sampai biru diberikan oleh aglikon atau glikosida.
e. Uji Steroid.
Uji steroid dilakukan dengan cara menguapkan pelarut dalam larutan uji di atas cawan, kemudian residu yang tersisa ditambahkan asam asetat anhidrat dan H2SO4 pekat, lalu diamati perubahan warna yang terjadi pada residu tersebut, dimana menunjukkan positif steroid bila terjadi perubahan warna menjadi merah setelah penambahan H2SO4 pekat dalam suasana asam.
f. Uji Kromatografi Lapis Tipis 1) Deskripsi.
27
didasarkan pada adsorpsi, partisi, atau kombinasi keduanya, yang tergantung dari jenis lempeng, cara pembuatan, dan jenis pelarut yang digunakan. Perkiraan identifikasi diperoleh dengan pengamatan bercak dengan harga rf yang identik dan ukuran yang hampir sama, dengan cara menotolkan bahan uji dan pembanding pada plat yang sama (Depkes, 2008, 163-164).
2) Penggunaan pembanding dalam uji fitokimia
Penggunaan KLT pada uji fitokimia ini dilakukan hanya untuk uji penegasan bahwa dalam ekstrak yang dibuat mengandung senyawa fenolik. Uji penegasan dilakukan dengan larutan pembanding asam galat dan larutan uji berupa ekstrak secang dengan pelarut etanol 30%, ekstrak secang dengan pelarut etanol 50%, dan ekstrak secang dengan pelarut etanol 70% yang ditotolkan pada lempeng silika gel, dengan jarak penotolan tertentu. Uji ini menggunakan fasa gerak (pelarutan pemisah) berupa campuran antara n-heksan dengan etil asetat dengan perbandingan tertentu.
4. Uji Fenolik Total
28
29
mereduksi asam heteropoli sehingga warna biru yang dihasilkan semakin pekat (Singleton dan Rossi, 1965).
Gambar 4.Persamaan reaksi dalam perubahan warna folin (kuning) menjadi kompleks molybdenum (biru)
30
Gambar 5. Mekanisme metode Folin-Ciocalteu
5. Spektroskopi UV-Visibel
Daerah UV sekitar 10 nm – 380 nm, tetapi paling banyak penggunaannya secara analitik dari 200 – 380 nm dan disebut sebagai UV pendek (dekat). Di bawah 200 nm, udara dapat mengabsorpsi sehingga instrumen harus dioperasikan kondisi vakum, daerah ini disebut dengan daerah UV Vakum. Daerah tampak (visibel) sangat kecil panjang gelombang yang dikaitkan dengan cahaya tampak itu mampu mempengaruhi selaput pelangi pada manusia, dan karenanya menimbulkan
kesan subyektif akan ketampakan (vision). λ daerah tampak dari 380 nm –
sekitar 780 nm.
a. Absorpsi cahaya
31
Apabila cahaya polikromatis (cahaya putih) yang berisi seluruh spektrum panjang gelombang melewati medium tertentu, akan menyerap panjang gelombang lain, sehingga medium itu akan tampak berwarna. Oleh karena hanya panjang gelombang yang diteruskan yang sampai ke mata maka panjang gelombang inilah yang menentukan warna medium. Warna ini disebut warna komplementer terhadap warna yang diabsorpsi. Spektrum tampak dan warna-warna komplementer ditunjukkan dalam Tabel 1 berikut ini
Tabel 1. Spektrum tampak dan warna-warna komplementer
Panjang Gelombang (Nm)
Warna yang Diabsorpsi
Warna yang Dipantulkan (Komplementer)
340 –450 Lembayung Kuning – hijau
450 – 495 Biru Kuning
495 – 570 Hijau Violet
570 – 590 Kuning Biru
590 – 620 Jingga Hijau – biru
620 - 750 Merah Biru - hijau
b. Hukum Dasar Spektroskopi Absorpsi
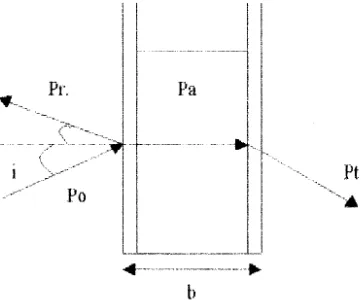
Jika suatu berkas cahaya melewati suatu medium homogen, sebagian dari cahaya datang (Po) diabsorpsi sebanyak (Pa), sebagian dapat diabaikan dipantulkan (Pr), sedangkan sisanya ditransmisikan (Pt) dengan efek intensitas murni sebesar :
32
Dengan Po = intensitas cahaya masuk, Pa = intensitas cahaya diabsorpsi, Pr = intensitas cahaya dipantulkan, Pt = intensitas cahaya ditransmisikan. Pada prakteknya, nilai Pr adalah kecil ( - 4 %), sehingga untuk tujuan praktis :
Po = Pa + Pt
[image:53.595.240.422.264.414.2]Lambert (1760), Beer (1852) dan Bouger menunjukkan hubungan berikut :
Gambar 6. Landasan Hukum Lambert-Beer
T =
= 10
-abc
dengan b = jarak tempuh optik, c = konsentrasi.
Log (T) = Log
= - abc dengan a = tetapan absorptivitas, T = transmitansi.
Log
= Log
= abc = A dengan A = absorbansi.
33
1) Jika suatu berkas cahaya monokromatis yang sejajar jatuh pada medium pengabsorpsi pada sudut tegak lurus setiap lapisan yang sangat kecil akan menurunkan intensitas berkas.
2) Jika suatu cahaya monokromatis mengenai suatu medium yang transparan, laju pengurangan intensitas dengan ketebalan medium tertentu sebanding dengan intensitas cahaya.
3) Intensitas berkas cahaya monokromatis berkurang secara eksponensial bila konsentrasi zat pengabsorpsi bertambah. Hal diatas menunjukkan persamaan mendasar untuk spektroskopi absorpsi, dan dikenal sebagai hukum Lambert Beer. atau hukum Beer Bouger. Satuan untuk b (cm), c (mol/ L), a = absorptivitas molar adalah absorpsi larutan yang diukur dengan ketebalan 1 cm dan konsentrasi 1 mol/ L.
A = abc
4) Jika konsentrasi (c) diekspresikan sebagai molaritas (mol/L) dan ketebalan sel (b) dinyatakan dalam centimeter (cm), koefisien
absorptivitas molekuler (a) disebut koefisien ekstingsi molar (ε) dan
memiliki satuan [L/(mol.cm)].
A =Ɛbc
c. Instrumen Spektroskopi UV-Vis
Menurut konfigurasinya instrumen spektroskopi UV-Vis , dibagi dalam:
34
Single-beam instrument dapat digunakan untuk kuantitatif
dengan mengukur absorbansi pada panjang gelombang tunggal. Single-beam instrument mempunyai beberapa keuntungan yaitu sederhana, harganya murah, dan mengurangi biaya yang ada merupakan keuntungan yang nyata. Beberapa instrumen menghasilkan single-beam instrument untuk pengukuran sinar ultra violet dan sinar tampak. Panjang gelombang paling rendah adalah 190 sampai 210 nm dan paling tinggi adalah 800 sampai 1000 nm (Skoog, DA, 1996, 572-574).
Gambar 7. Skema Spektroskopi UV-Vis Single Beam 2) Double-beam instrument
35
secara elektronik dan ditunjukkan oleh alat pembaca (Skoog, DA, 1996, 572-574).
Gambar 8. Skema Spektroskopi UV-Vis Double-Beam 6. Standardisasi Ekstrak
Standardisasi ekstrak dilakukan untuk mengetahui apakah ekstrak dari bahan alam yang dibuat dapat memenuhi standar yang telah ditentukan, sehingga diharapkan obat-obatan herbal yang berasal dari bahan alam memiliki konsitensi mutu seperti standar berikut pada tabel 1.
Tabel 2. Parameter Standar Ektrak Tanaman Obat
No. Parameter Standar Standar FHI /
Quality Standard (%)
1. Kadar air/ Moisture content ≤10,00 2. Kadar sari air/ Water extractable ≤18,00 3. Kadar sari alkohol/ Alcohol
extractable
≤9,70
4. Kadar abu/Ash content ≤ 1,40
5. Kadar abu tak larut asam/ Insoluble in HCl
≤ 0,6
36
a. Parameter Non-Spesifik
3) Parameter susut pengeringan
Susut pengeringan merupakan pengukuran sisa zat setelah pengeringan pada temperatur 105°C selama 30 menit atau sampai berat konstan, yang dinyatakan dalam nilai persen . tujuan dari dilakukan parameter standar susut pengeringan ini adalah untuk memberikan batasan maksimal (rentan) tentang besarnya senyawa yang hilang pada proses pengeringan ( Depkes RI, 2000, 13.)
4) Parameter kadar air
Pengukuran kandungan air yang berada di dalam bahan, biasanya dapat dilakukan dengan cara titrasi, destilasi, atau gravimetri. namun yang sering dilakukan adalah metode titrasi dengan pereaksi Karl Fischer, dalam penelitian ini digunakan alat Karl-Fischer Moisture Titrator MKS-520 untuk memudahkan pengukuran (Depkes RI, 2000, 14-16.)
5) Parameter kadar abu total
37
6) Parameter Kadar abu tidak larut asam
pengukuran kadar abu tidak larut asam dilakukan setelah bahan awal diabukan, abu yang tersisa dilarutkan dalam asam sulfat encer dan dipanaskan pada temperatur dimana larutan asam yang melarutkan mineral terdestruksi dan menguap sehingga tinggal unsur mineral dan anorganik yang tidak larut asam (Depkes RI, 2000, 17.)
7) Sisa pelarut
Menentukan kandungan sisa pelarut tertentu yang secara umum ditentukan dengan kromatografi gas, untuk ekstrak cair berati kandungan pelarutnya, misalnya dalam penelitian ini digunakan pelarut etanol untuk mengekstraksi sehingga kadar yang diukur adalah sisa pelarut etanolnya. tujuan daridilakukan penentuan kadar pelarut adalah untuk memberikan jaminan bahwa selama proses tidak meninggalkan sisa pelarut, terutama pelarut yang berbahaya seperti pelarut kloroform harus bernilai negatif sesuai batas deteksi instrumen. sedangkan ekstrak kental boleh terdapat sisa pelarut dengan batas maksimal tertentu (Depkes RI, 2000, 17-18.)
b.Parameter Spesifik 1) Organoleptik
Merupakan pengamatan terhadap ekstrak menggunakan pancaindra untuk mendeskripsikan bentuk, warna, bau, rasa sebagai berikut:
1. bentuk : padat, cair, serbuk-kering, kental 2. warna : kuning, coklat, merah, dll
38
4. Rasa : pahit, manis, kelat, dll
dengan pengenalan awal yang sederhana dan seobjektif mungkin (Depkes RI, 2000, 31.)
2) Terlarut dalam air
Melarutkan ekstrak dengan pelarut air untuk ditentukan jumlah solut yang identik dengan jumlah senyawa kandungan secara gravimetri. tujuan dari parameter senyawa terlarut dalam pelarut air ini adalah untuk mengetahui gambaran awal senyawa yang terlarut dalam pelarut air (Depkes RI, 2000, 31.)
3) Terlarut dalam etanol
Melarutkan ekstrak dengan pelarut etanol untuk ditentukan jumlah solut yang identik dengan jumlah senyawa kandungan secara gravimetri. tujuan dari parameter senyawa terlarut dalam pelarut etanol ini adalah untuk mengetahui gambaran awal senyawa yang terlarut dalam pelarut air (Depkes RI, 2000, 31.)
B. Penelitian yang Relevan
Penelitian mengenai“Penentuan Kadar Fenolik Total Dan Standardisasi Ekstrak Kulit Kayu Secang (Caesalpinia Sappan L)“ yang dilakukan didasarkan pada penelitian-penelitia yang telah dilakukan sebelumnya.
Penelitian yang dilakukan oleh Wahyu Widowati pada tahun 2011 berjudul “Uji Fitokimia dan Potensi Antioksidan Ekstrak Etanol Kulit kayu
39
secang dengan etanol 96% menggunakan metode maserasi selama 24 jam, kemudian ekstrak yang dihasilkan diuji fitokimianya Ekstrak kulit kayu secang mengandung senyawa terpenoid, fenol sangat tinggi, mengandung flavonoid tinggi, tidak namun steroid dan tanin. Ekstrak kulit kayu secang diukur kandungan fenolik totalnya dengan standar epigalokatekin (EGC) dan epikatekin galat (ECG) dimana penentuan kandungan fenolik totalnya menggunakan metode Folin-Ciousalteu, didapatkan informasi bahwa ekstrak kulit kayu secang mengandung kadar fenolik total ekivalen EGC 849,11
g/mg dan ekivalen ECG 825,11 g/mg.
Penelitian mengenai kandungan senyawa metabolit sekunder ekstrak dilakukan dengan metode penapisan fitokimia dan standardisasi ekstrak seperti yang dilakukan oleh Pandey, Gangrale, Upadhyay dan Priyanka, pada tahun 2014 yang berjudul“Physiochemical Analysis Of Pterocarpus Santalinus L. Extracts” dalam penelitian ini dilakukan pengujian fitokimia dan menstandardisasi tanaman Raktachandan (Pterocarpus santalinus L.)tersebut.Uji fitokimia kualitatif yang dilakukan adalah terhadap
keberadaan alkaloid, saponin, flavonoid and glikosida dalam ekstrak Pterocarpus santalinus L.Dilakukan pula penstandardisasi parameter fisik
40
C. Kerangka Berfikir Teoritis
Kulit kayu secang (Caesalpinia sappan L.) secara empiris dimanfaatkan sebagai bahan untuk pengobatan penyakit asam urat. Berbagai macam zat yang terkandung dalam kulit kayu secang antara lain brazilin, alkaloid, flavonoid, saponin, tanin, fenil propana dan terpenoid. Selain itu juga mengandung asam galat, brasilein, delta-aphellandrene, oscimene, resin dan resorin (Xu dkk, 1994. )
Penelitian mengenai efek secang (Caesalpinia sappan L.) sebagai agen antihiperurisemia, anti bakteri, obat kanker dan masih banyak lagi telah banyak dikembangkan, sedangkan penelitian mengenai standardisasi ekstrak secang terhadap berbagai konsentrasi pelarut belum banyak dilakukan, maka dilakukan penelitian terhadap standardisasi ekstrak herbal secang terstandar dengan berbagai pelarut, sehingga diperolehekstrak herbal secang terstandar.
41
ekstrak kental, kemudian ekstrak kental yang dibuat digunakan untuk analisis kandungan fenolik total dan dilakukan standardisasi ekstrak kental.
Penentuan kadar fenolik total dalam penelitian ini menggunakan standar asam galat dan regen folin Ciolte 1:10 dan Na2CO3 6%, dimana untuk menentukan kadar fenolik totalnya dilakukan dengan membaca absorbansi ekstrak kulit kayu secang yang telah diberi folin dan Na2CO3 menggunakan spektroskopi UV-Vis. standardisasi ekstrak kental yang dilakukan pada aspek spesifik dan aspek non-spesifik seperti kadar air, susut pengeringan, kadar abu total, kadar abu tidak larut asam, kadar sari larut air, kadar sari larut etanol, serta kadar sisa etanol yang terdapat dalam ekstrak.
42
BAB III
METODE PENELITIAN
A. Subjek dan Objek Penelitian 1. Subjek Penelitian
Subjek dalam Penelitian Ini adalah kayu dari tanaman secang (Caesalpinia Sappan L. )
2. Objek Penelitian
Objek penelitian ini adalah penentuan kadar fenolik total dan standardisasi ekstrak kental dan ekstak kering dari kayu secang (Caesalpinia Sappan L.) B. Alat dan Bahan
1. Alat penelitian
a. Spektroskopi UV-Vis
b. Karl Fischer Titrator (Karl-Fischer Moisture Titrator MKS-520) c. Hot Plate and Stirer (Hidolph RZR 2051, Jerman)
d. Sonication Bath (Elmasonic S15)
e. Timbangan Analitik (Precisa XT 220, Swiss dan KERN ALJ 220-4NM)
f. Shaker (GFL 3017) g. Grinder (Retsch)
h. Mousture Balance (Precisa HA60, Swiss) i. MikroPipet (Ependolph)
43
k. Desikator l. Kuvet kotak m. Stopwatch
n. Vacum Rotavapor (Heidolph, Jerman) o. Krus
p. Kertas Saring Bebas Abu q. Furnace (Thermolyne 1400)
r. Kromatografi Gas (GC DANI 1000) s. Pompa Vakum (Buchi V-700) t. Kromatografi Lapis Tipis 2. Bahan penelitian
a. Kayu Secang b. Etanol 96%
c. HgCl (Merck, Jerman) d. KI (Merck, Jerman)
e. Bi(NO3).H2O (Merck, Jerman) f. HNO3 (Scharlau, Spayol) g. NaCl (Merck, Jerman)
h. Kloroform 10 (Sigma-Aldrich, USA) i. H2SO4
j. n-Heksan (Scharlau, Spayol) k. Mg Powder (Sigma-Aldrich, USA)
44
m. Na2CO3 (Sigma-Aldrich, USA) n. Standar Asam Galat (Merck, Jerman) o. HCL (Scharlau, Spayol)
p. Dekstrin (Brataco Chemika, indonesia) q. Corn Starch (Brataco Chemika, indonesia) r. Laktosa (Brataco Chemika, indonesia) s. Maltodekstrin (Brataco Chemika, indonesia) t. Avicel ph 102 (Brataco Chemika, indonesia) u. Amprotab (Brataco Chemika, indonesia) C. Prosedur Penelitian
1. Penyiapan Simplisia
Kayu secang (Caesalpinia Sappan L) sebanyak 10 Kg dibersihkan, kemudian kayu secang yang telah bersih dipotong-potong dan dikeringkan di dalam oven dengan suhu 40°C, setelah kering kayu diserut menjadi potongan lebih kecil. Kemudian hasil simplisia kering kayu secang disimpan dalam wadah penampung untuk menunggu tindakan selanjutnya.
2. Ekstraksi
45
46
Gambar 9. Skema alat perkolator 3. Uji Fitokimia Pada ekstrak cair
Penapisan Fitokimia
a. Alkaloid (Depkes, 1995 dan Sirait, 2007)
1) Ekstrak ditambahkan dengan 1 ml HCl 2N dan 9 ml akuades, kemudian dipanaskan di penangas air selama 2 menit, dinginkan. Kemudian filtrat disaring dan ditampung. Filtrat digunakan sebagai larutan percobaan selanjutnya (larutan uji).
47
3) Larutan uji diambil 1 ml dan dituang ke dalam kaca arloji, kemudian ditambahkan 2 tetes Reagen Wagner, jika terbentuk endapan coklat muda sampai kuning menunjukkan adanya alkaloid
4) Larutan uji diambil 1 ml dan dituang ke dalam kaca arloji, kemudian ditambahkan 2 tetes Reagen Mayer, jika terbentuk endapan menggumpal putih atau kuning yang larut dalam metanol menunjukkan adanya alkaloid.
5) Larutan uji diambil 1 ml dan dituang ke dalam kaca arloji, kemudian ditambahkan 2 tetes Reagen Dragendorf, jika terbentuk endapan jingga coklat menunjukkan adanya alkaloid.
b. Uji Flavonoid (Depkes, 1995 dan Farnsworth, 1966)
Ekstrak ditambahkan dengan 5 ml etil asetat hingga ekstrak larut (larutan uji).
1) 1 ml larutan uji diuapkan dan ditambahkan 2 ml etanol 95% dan 0,5 gram serbuk seng, kemudian ditambahkan 2 ml HCl 2N, diamkan 1 menit.Setelah itu, ditambahkan 10 tetes HCl pekat. Kocok perlahan, kemudian didiamkan 2 sampai 5 menit. Terbentuk warna merah intensif (flavonoid positif).
48
3) 1 ml larutan diuapkan dan ditambahkan dengan 2 ml aseton, kemudian dilarutkan. Setelah itu, ditambahkan sedikit serbuk asam borat dan asam oksalat, panaskan hati-hati. Lalu, ditambahkan 10 ml eter. Amati dengan sinar ultraviolet 366 nm. Larutan akan berfluoresensi kuning intensif (flavonoid positif).
c. Uji Tanin (Farnsworth, 1966 dan Trease, 1961)
Ekstrak kental ditambahkan dengan 50 ml air panas. Kemudian dipanaskan hingga mendidih selama 5 menit. Filtrat disaring (larutan uji).
1) Sejumlah 5 ml larutan uji dimasukkan ke dalam tabung reaksi, kemudian ditambahkan beberapa tetes FeCl3
2) Sejumlah 5 ml larutan uji dimasukkan ke dalam tabung reaksi, kemudian ditambahkan beberapa tetes larutan gelatin 10%, terbentuk endapan putih (tanin positif). terbentuk warna hijau violet (tanin positif).
3) Sejumlah 5 ml larutan uji dimasukkan ke dalam tabung reaksi, kemudian ditambahkan beberapa tetes larutan NaCl-gelatin (larutan gelatin 1% dalam larutan NaCl 10%), terbentuk endapan putih (tanin positif).
d. Uji Saponin (Depkes, 1995b & Farnsworth, 1966)
49
diamkan selama 10 menit. Terbentuk buih setinggi 1 hingga 10 cm. Pada penambahan 1 tetes HCl 2N buih tidak hilang.
e. Uji Steroid
Ekstrak ditambahkan asam asetat anhidrat dan H2SO4 pekat jika terjadi perubahan warna menjadi merah darah pekat menunjukkan adanya steroid .
f. Pembandingan Sampel Ekstrak Secang Dengan Standar Asam Galat Menggunakan KLT
1) Menyiapkan plat KLT sebesar 12 x 7 cm sebagai fasa diam, dan menyiapkan fasa gerak yang terdiri dari campuran larutan n-heksan : etil asetat dengan perbandingan 1: 3
2) Menotolkan standar dan sampel pada plat KLT dengan masing masing berjarak 1 cm, kemudian KLT tersebut dielusikan sepanjang 10 cm. 3) Menandai pemisahan noda dan menngukur nilai Rf dibawah lampu
UV 366
4. Standardisasi Ekstrak Kental Kayu Secang a. Susut Pengeringan
50
Ekstrak kental sebanyak satu gram ditimbang dan dimasukkan ke dalam wadah yang kemudian diratakan dengan cara menggoyangkan wadah. Setelah itu dimasukkan ke dalam oven dengan suhu 105°C hingga berat konstan. Biarkan wadah yang berisi ekstrak mendingin dalam eksikator hingga suhu ruang kemudian ditimbang kembali. Massa simplisia yang hilang setelah dioven dinyatakan sebagai besarnya senyawa yang hilang pada proses pengeringan (susut pengeringan) Persentase susut pengeringan ekstrak dapat diketahui dengan perhitungan menggunakan rumus berikut:
% Susut Pengeringan =
x 100% Keterangan:
A = Massa Krus dan tutup kosong (gram) B = Massa Wadah + Simplisia Awal (gram) C = Massa Wadah + Simplisia Akhir (gram) b. Kadar Abu Total
51
selama 30 menit. Setelah itu krus didinginkan dalam desikator dan ditimbang massanya.
Sebanyak setengah gram ekstrak ditimbang dan dimasukkan kedalam krus yang sebelumnya telah ditimbang. Setelah itu dibakar di dalam furnace dengan temperatur 450°C selama satu jam. Kemudian didinginkan dan ditimbang, setelah ditimbang krus dimasukkan kembali ke dalam furnace selama tiga puluh menit. setelah itu krus didinginkan dan ditimbang, apabila massanya telah konstan maka tidak perlu dilakukan pembakaran ulang. Rumus untuk menghitung % kadar abu total adalah sebagai berikut:
% Kadar Abu total = ( 1 -
) X 100% Keterangan :
A : Massa Krus dan tutup kosong (gram)
B : Massa Krus dan tutup + ekstrak awal (gram) C : Massa krus dan tutup + ekstrak akhir (gram) c. Kadar Abu yang Larut Dalam Asam
52
hingga bobot tetap. Rumus untuk menghitung % kadar abu yang tidak larut dalam asam adalah:
% Kadar abu tak larut asam =
X 100 X % Abu Total Keterangan :
A : Massa Krus dan tutup kosong (gram)
B : Massa Krus dan tutup + ekstrak awal (gram)
D : Massa krus dan tutup + abu yang tidak larut asam(gram) d. Sisa Pelarut
Penentuan sisa pelarut etanol dalam penelitian ini menggunakan instrumen kromatografi Gas (GC DANI 1000) berikut prosedur pengukuran sisa pelarut menggunakan kromatografi gas. 1) Pembuatan Standar
Larutan standar etanol dibuat dengan konsentrasi 0,005 % ; 0,0075% ; 0,01 % ; 0,025 % ; 0,05 % ; dan 0,1 % v/v. Dipipet sejumlah tertentu etanol sesuai dengan konsentrasi kemudian ditambahkan 25 µl n-propanol dan dilarutkan dengan akuades sehingga volume berjumlah 5 ml.
53
konsentrasi dan luas area. Dihitung persamaan regresinya (y = a +bx) dengan konsentrasi sebagai x dan rasio perbandingan luas area sebagai y.
2) Penentuan Kadar etaol dalam ekstrak kayu secang
Dipipet sejumlah tertentu ekstrak sampel sesuai dengan konsentrastertentu ditambahkan 25 µl n-propanol dan dilarutkan dengan akuades sehingga volume berjumlah 5 ml. Larutan sampel masing-masing disuntikkan ke dalam kromatografi gas sebanyak 1 µl dengan kondisi suhu kolom 235 °C, detektor FID, suhu detektor 260 °C, suhu oven 205 °C, jenis gas H2/O2/N2, tekanan gas masing masing 0,4 Bar (400 mBar). Luas area yang diperoleh pada masing – masing konsentrasi kemudian digunakan untuk menghitung sisa pelarut den