BAB II
TINJAUAN PUSTAKA
2.1 DURIAN
2.1.1 Sejarah Singkat
Durian (Durio zibethinus) merupakan tanaman buah berupa pohon. Sebutan durian diduga berasal dari istilah Melayu yaitu dari kata duri yang diberi akhiran -an sehingga menjadi duri-an. Kata ini terutama dipergunak-an untuk menyebut buah yang kulitnya berduri tajam. Tanaman durian berasal dari hutan Malaysia, Sumatra, dan Kalimantan yang berupa tanaman liar. Penyebaran durian ke arah Barat adalah ke Thailand, Birma, India dan Pakistan. Buah durian sudah dikenal di Asia Tenggara sejak abad 7 M. Nama lain durian adalah duren (Jawa, Gayo), duriang (Manado), dulian (Toraja), rulen (Seram Timur) [23].
2.1.2 Jenis Tanaman
Tanaman durian termasuk famili Bombaceae sebangsa pohon kapuk-kapukan. Yang lazim disebut durian adalah tumbuhan dari marga (genus) Durio, Nesia, Lahia, Boschia dan Coelostegia. Ada puluhan durian yang diakui keunggulannya oleh Menteri Pertanian dan disebarluaskan kepada masyarakat untuk dikembangkan. Macam varietas durian tersebut adalah: durian sukun (Jawa Tengah), petruk (Jawa Tengah), sitokong (Betawi), simas (Bogor), sunan (Jepara), otong (Thailand), kani (Thailand), sidodol (Kalimantan Selatan), sijapang (Betawi) dan sihijau (Kalimantan Selatan) [23].
2.1.3 Manfaat Tanaman
Manfaat durian selain sebagai makanan buah segar dan olahan lainnya, terdapat manfaat dari bagian lainnya, yaitu:
1) Tanamannya sebagai pencegah erosi di lahan-lahan yang miring.
2) Batangnya untuk bahan bangunan/perkakas rumah tangga. Kayu durian setara dengan kayu sengon sebab kayunya cenderung lurus.
4) Kulit dipakai sebagai bahan abu gosok yang bagus, dengan. cara dijemur sampai kering dan dibakar sampai hancur [23].
2.1.4 Karakteristik Biji Durian
Tanaman durian adalah tanaman tahunan. Bila ditanam melalui biji, tanaman ini akan mulai berbunga untuk pertama kali sepuluh tahun setelah tanam. Namun, tanaman ini akan menghasilkan buah yang lezat dan memiliki banyak manfaat. Selain buahnya, biji durian dapat dimanfaatkan sebagai bioetanol. Biji merupakan alat perkembangbiakan yang utama karena di dalam biji terdapat calon tumbuhan baru. Biji durian terdiri dari beberapa bagian yaitu kulit biji, tali biji, dan inti biji [23].
Biji durian berbentuk bulat telur, dan berkeping dua. Selain itu, biji durian berwarna putih kekuningan hingga. Biji durian (pongge) memiliki kandungan pati yang cukup tinggi sehingga dapat digunakan sebagai pengganti bahan makanan. [23].
Apabila dipotong atau dikupas kulitnya, biji durian biasanya mengeluarkan lendir. Lendirnya tidak berbau dan berasa serta larut dalam air dingin ataupun panas. Lendirnya dapat membentuk suatu larutan kental yang disebut gum. Berikut adalah tabel komposisi biji durian dalam buku Michael J. Brown (1997:157) [23].
Tabel 2.1 Komposisi Biji Durian [23]
Zat Per 100 gram biji segar
(mentah) tanpa
kulitnya
Per 100 gram biji telah
dimasak tanpa kulitnya
Kadar air 51,5 gram 51,5 gram
Lemak 0,4 gram 0,2-0,23 gram
Protein 2,6 gram 1,5 gram
Karbohidrat total 47,6 gram 48,2 gram
Tabel 2.1 Komposisi Biji Durian (lanjutan)[23]
Kalsium 17 miligram 3,9-88,8 miligram
Fosfor 68 miligram 86,65-87 miligram
Besi 1,0 miligram 0,6-0,64 gram
Natrium 3 miligram -
Kalium 962 miligram -
Beta karoten 250 �gram -
Riboflavin 0,05 miligram 0,05-0,052 miligram
Thiamin - 0,03-0,032 miligram
Niacin 0,9 miligram 0,89-0,9 miligram
Dari tabel dapat dilihat bahwa kandungan karbohidrat pada biji durian sangat tinggi yaitu 47,6 gram per 100 gram biji segar, sedangkan bila dimasak menjadi 48,2 gram. Amilum (karbohidrat) berbentuk polisakarida yang dapat dipecah menjadi glukosa. Kemudian glukosa akan difermentasi menjadi etanol.
2.2 KARBOHIDRAT
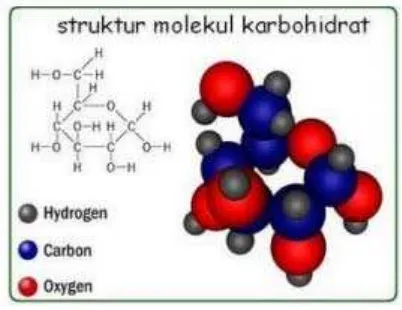
Karbohidrat atau sakarida adalah segolongan besar senyawa organik yang tersusun hanya dari atom karbon, hidrogen dan oksigen. Bentuk molekul karbohidrat paling sederhana tersusun dari satu molekul gula sederhana. Pada umumnya karbohidrat yang terdapat di alam merupakan polimer yang tersusun dari molekul gula yang terangkai menjadi rantai yang panjang serta bercabang.
diperoleh dari bahan makanan yang dimakan sehari- hari, terutama bahan makanan yang berasal dari tumbuh – tumbuhan.
\
Gambar 2.1 Rumus Bangun Karbohidrat
Karbohidrat menyediakan kebutuhan dasar yang diperlukan tubuh. Tubuh menggunakan karbohidrat seperti layaknya mesin mobil menggunakan bensin. Karbohidrat juga merupakan bahan yang penting dan sumber tenaga yang terdapat dalam tumbuhan dan daging hewan. Selain itu, karbohidrat juga menjadi komponen struktur penting pada makhluk hidup dalam bentuk serat (fiber), seperti selulosa, pektin, serta lignin.
Ada beberapa cara analisis yang digunakan untuk memperkirakan kandungan karbohidrat dalam bahan makanan . Yang paling mudah adalah dengan cara perhitungan kasar (aproximate analysis),yaitu suatu analisis dimana kandungan karbohidrat termasuk serat kasar diketahui bukan melalui analisis tetapi melalui perhitungan sebagai berikut:
% karbohidrat = 100% - % ( protein + lemak + abu + air )
Molekol karbohidrat terdiri atas atom – atom karbon,hidrogen dan oksigen. Jumlah atom hidrogen dan oksigen merupakan perbandingan 2 : 1 seperti pada molekol air. Sebagai contoh molekol gluko sa mempunyai rumus kimia C6H12O6.
Glukosa adalah salah satu aldoheksosa yang sering disebut dekstrosa karena mempunyai sifat dapat memutar cahaya terpolarisasi kearah kanan. Di alam, glukosa terdapat didalam buah – buahan dan madu lebah. Darah manusia normal mengandung glukosa dalam jumlah atau konsentrasi yang tetap, yaitu antara 70-100 mg tiap 100 ml darah. Glukosa darah dapat bertambah setelah kita makan makanan sumber karbohidrat, namun 2 jam setelah itu, jumlah glukosa darah akan kembali pada keadaan semula. Pada orang yang menderita diabetes mellitus atau kencing manis, jumlah glukosa darah lebih besar dari 130 mg per 100 ml darah.
Dalam alam, glukosa dihasilkan dari reaksi antara karbondioksida dan air dengan bantuan sinar matahari dan klorofil dalam daun. Proses ini disebut fotosintesis dan glukosa yang terbentuk terus digunakan untuk pembentukan amilum atau selulosa. Amilum terbentuk dari glukosa dengan jalan penggabungan molekul – molekul glukosa yang membentuk rantai lurus maupun bercabang dengan melepaskan air [26].
Karbohidrat menurut ukuran molekulnya dapat dikelompokkan menjadi tiga kelompok, yaitu monosakarida, disakarida, dan polisakarida [15].
2.2.1 Monosakarida
Monosakarida merupakan karbohidrat yang mempunyai molekul paling sederhana dibandingkan dengan molekul karbohidrat lain. Molekul karbohidrat ini tidak dapat dihidrolisis dan merupakan suatu persenyawaan netral dan mudahlarut dalam air, sukar larut dalam alkohol dan tidak larut dalam eter [39]. Gula monosakarida yang umumnya terdapat dalam pangan mengandung 6 atom karbon yang mempunyai rumus atom C6H12O6. Tiga senyawa gula yang paling penting dalam monosakarida ialah :
1. Glukosa
dapat memutar cahaya terpolarisasi ke arah kanan [15]. Glukosa terdapat dalam jumlah yang bervariasi dalam sayurandan buah-buahan [39]. Struktur molekul glukosa dapat dilihat dalamgambar berikut :
Gambar 2.2 Struktur Glukosa 2. Fruktosa
Fruktosa merupakan suatu karbon heksosa yang mempunyai sifat memutar cahaya terpolarisasi ke kiri Fruktosa ini didapatkan bersamasama dengan glukosa dalam berbagai bentuk buah-buahan dan madu [39].
3. Galaktosa
Galaktosa jarang terdapat di alam bebas. Pada umumnya berikatan dengan glukosa dalam bentuk laktosa, yaitu gula yang terdapat dalam susu [15]. Gula ini secara kimiawi mirip glukosa. Didalam makanan senyawa ini tidak terdapat seperti apa adanya tetapi dapat menghasilkan laktosa jika sebuah sakarida dipecah dalam pencernaan [39].
2.2.2 Disakarida
Gula disakarida mempunyai rumus umum C12H22O11. Senyawa-senyawa ini terbentuk jika dua molekul monosakarida bergabung dengan melepas satu molekul air.
1. Sukrosa
Senyawa ini adalah senyawa yang dikenal sehari-haridalam rumah tangga sebagai gula dan dihasilkan dalam tanaman dengan jalan mengkondensasikan glukosa dan fruktosa. Sukrosa didapatkan dalam tumbuhan, sayuran dan buah-buahan, seperti tebu yang mengandung sukrosa dalam jumlah yang relatif besar.
2. Laktosa
3. Maltosa
Molekul maltosa dibentuk dari hasil kondensasi dua molekul glukosa.
2.2.3 Polisakarida
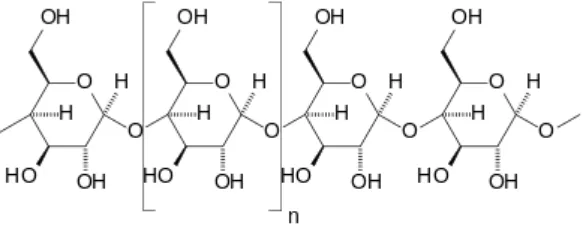
Polisakarida adalah polimer hasil kondensasi monosakarida dan tersusun dari banyak molekul monosakarida yang berikatan satu sama lain, dengan melepaskan sebuah molekul air untuk setiap ikatan yang terbentuk. Senyawa ini mempunyai rumus umum (C6H10O5)n, dimana n adalah bilangan yang besar. Polisakarida terpenting sebagai sumber karbohidrat yang tersebarluas di alam dan banyak terdapat pada tanaman adalah pati. Pati penting dalam industri-industri pangan, tekstil, lem, kertas, permen, dan lain-lain. Pati tersusun oleh dua macam polimer, yaitu : polimer rantai lurus (amilosa) dan polimer bercabang (amilopektin).
Amilosa adalah polisakarida berantai lurus (tidak bercabang) dan larut dalamair, dengan berat molekul berkisar antara sekitar 250-300 unit glukosa yang satu sama lainnya dihubungkanoleh ikatan 1 alpha glikosida melalui atom C
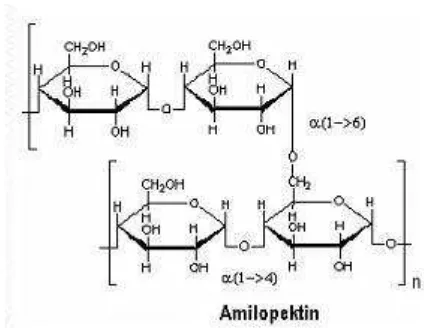
Amilopektin adalah ikatan alpha glikosida. Disamping sebagian besar adalah ikatan 1ikatan 1-6, secara kimia terbukti bahwa amilopektin merupakan rantai yang bercabang. Rantai utama memiliki rantai samping dan begitu pula dengan rantai selanjutnya.
Dalam biji atau umbi tumbuh-tumbuhan, pati (C6H10O5)n merupakan makanan cadangan, terdapat dalam bentuk butir-butir atau granula yang berwarna putih mengkilat, tidak berbau dan berasa.
2.2.4 Analisis kadar karbohidrat (glukosa)
Metode luff Schoorl adalah merupakan suatu metode atau cara penentuan monosakarida dengan cara kimiawi. Pada penentuan metode ini, yang ditentukan bukannya kuprooksida yang mengendaptapi dengan menentukan kuprioksida dalam larutan sebelum direaksikan dengan gula reduksi ( titrasi blanko) dan sesudah direaksikan dengan sampel gula reduksi ( titrasi sampel). Penentuan titrasi dengan menggunakan Na-tiosulfat. Selisih titrasi blanko dengan titrasi sampel ekuivalen dengan kuprooksida yang terbentuk dan juga ekuivalen dengan jumlah gula reduksi yang ada dalam bahan / larutan.
Reaksi yang terjadi selama penentuan karbohidrat cara ini mula- mula kuprooksida yang ada dalam reagen akan membebaskan iod dari garam K-iodida. Banyaknya iod yang dibebaskan ekuivalen dengan banyaknya kuprioksida. Banyaknya iod dapat diketahui dengan titrasi dengan menggunakan Na-tiosulfat. Untuk mengetahui bahwa titrasi sudah cukup maka diperlukan indikator amilum. Apabila larutan berubah warnanya dari biru menjadi putih, adalah menunjukkan bahwa titrasi sudah selesai.
Reaksi yang terjadi dalam penentuan gula cara Luff dapat dituliskan sebagai berikut :
R – COH + 2CuO Cu2O + R-COOH H2SO4 + CuO CuSO4 + H2O
CuSO4 + 2 KI Cu2I2
I2 + Na2S2O3 Na2S4O6 + NaI [33].
2.3 PATI
Pati merupakan homopolimer glukosa dengan ikatan -glikosidik. Berbagai macam pati tidak sama sifatnya bergantung dari panjang rantai karbonnya serta apakah lurus atau bercabang rantai molekulnya. Pati terdiri dari dua fraksi yang dapat dipisahkan dengan air panas. Fraksi terlarut disebut amilosa dan fraksi tidak terlarut disebut amilopektin [38].
bentuk, ukuran, keseragaman dan letak hilum (ditengah atau ditepi) berbeda-beda untuk setiap jenis tanaman penghasil pati. Ukuran granula pati yang berasal dari biji-bijian lebih kecil dari tanaman sumber pati lainnya, yaitu berkisar antara 3-20 m dan yang berasal dari umbi-umbian 10-100 m sedangkan yang berasal dari batang 50 m. Kondisi tersebut salah satunya menyebabkan pati yang berasal dari biji-bijian cenderung mempunyai suhu gelatinasi yang rendah dan lebih mudah untuk dihidrolisis oleh katalisator asam maupun enzim [25].
Dalam air dingin pati tidak dapat larut, akan tetapi dalam air panas akan membentuk larutan yang lebih kental. Butir-butir pati akan mengembang dan mengabsorbsi air dalam jumlah besar apabila campuran antara pati dan air dipanaskan. Air yang berdifusi dalam jumlah cukup besar akan mengakibatkan gelatinasi membentuk gel sehingga akan lebih mudah dihidrolisis [12].
Amilosa terdiri dari 250300 unit Dglukosa yang terikat dengan ikatan -1,4 glikosidik, jadi molekulnya merupakan rantai terbuka. Amilopektin juga terdiri atas molekul D-glukosa yang sebagian besar mempunyai ikatan 1,4 gikosidik dan sebagian lagi ikatan 1,6 glikosidik. Adanya ikatan glikosidik ini menyebabkan terjadinya percabangan sehingga molekul amilopektin berbentuk rantai terbuka dan bercabang. Molekul-molekul amilopektin lebih besar daripada molekul amilosa karena terdiri dari 1000 unit glukosa. Pati dapat dihidrolisis sempurna menjadi glukosa dengan menggunakan asam dan juga enzim [26].
Hidrolisis sempurna amilosa hanya menghasilkan D-glukosa sedangkan hidrolisis parsial amilosa menghasilkan maltose sebagai satu-satunya diskarida. Pada hidrolisis sempurna amilopektin hanya akan menghasilkan suatu campuran disakarida maltose dan isomaltosa [15].
Gambar 2.4 Struktur Amilopektin
Proprosi pati relatif dari amilosa dan amilopektin berbeda-beda dari satu jenis pati dengan pati lainnya. Pati alami biasanya mengandung amilopektin lebih banyak daripada amilosa. Butiran pati mengandung amilopektin lebih banyak daripada amilosa berkisar antara 15-30% sedangkan amilopektin berkisar antara 70-80% [12].
2.4 HIDROLISIS
Gula merupakan kebutuhan pokok bagi manusia, selama ini kebutuhan gula dipenuhi oleh industri gula (penggiling tebu). Industri kecil seperti gula merah, gula aren. Gula dapat berupa glukosa, sukrosa, fruktosa dan sakrosa. Glukosa dapat digunakan sebagai pemanis dalam makanan, minuman, dan es krim.
Hidrolisis pati terjadi antara suatu reaktan pati dengan air. Reaksi ini adalah orde satu karena reaktan air yang dibuat berlebih, sehingga perubahan reaktan dapat diabaikan. Reaksi hidrolisis pati dapat menggunakan katalisator ion H+ yang dapat diambil dari asam. Reaksi yang terjadi pada hidrolisis pati adalah sebagai berikut:
(C6H10O5)x + x H2O x C6H12O6 Variabel-variabel yang berpengaruh terhadap reaksi hidrolisa: 1. Katalisator
Hampir semua reaksi hidrolisa memerlukan katalisator untuk mempercepat jalannya reaksi. Katalisator yang dipakai dapat berupa enzim atau asam sebagai katalisator, karena kerjannya lebih cepat. Asam yang dipakai beraneka ragam mulai dari asam klorida, asam sulfat sampai asam nitrat. Yang berpengaruh terhadap kecepatan reaksi adalah konsentrasi ion H bukan jenis asamnya. Meskipun demikian di dalam industri umumnya dipakai asam klorida. Pemiliham ini didasarkan atas sifat garam yang terbentuk pada penetralan jika konsentrasinya tinggi. Karena itu konsentrasi asam dalam air penghidrolisa ditekan sekecil mungkin. Umumnya dipergunakan larutan asam yang mempunyai konsentrasi asam lebih tinggi daripada pembuatan sirup. Hidrolisa pada tekanan 1 atm memerlukan asam yang lebih pekat.
2. Suhu dan Tekanan
3. Pencampuran (Pengadukan)
Supaya zat pereaksi dapat saling bertumbukan dengan sebaik-baiknya, maka perlu adanya pencampuran. Untuk proses batch, hal ini dapat dicapai dengan bantuan pengadukan atau alat pengadukan. Apabila prosesnya berupa proses alir (kontiniu), maka pencampuran dilakukan dengan cara mengatur aliran di dalam reactor supaya berbentuk olakan.
4. Perbandingan zat pereaksi
Kalau salah satu zat pereaksi berlebihan jumlahnya maka keseimbangan dapat menggeser ke sebelah kanan dengan baik. Oleh karena itu suspensi pati yang kadarnya rendah memberi hasil yang lebih baik dibandingkan kadar patinya tinggi. Bila kadar suspensinya diturunkan dari 40% menjadi 20% atau 1%, maka konversi akan bertambah dari 80% menjadi 87% atau 99% . Pada permukaan kadar suspense pati yang tinggi sehingga molekul-molekul zat pereaksi akan sulit bergerak. Untuk menghasilkan pati sekitar 20%.
2.5 KLASIFIKASI HIDROLISIS
Klasifikasi proses hidrolisa dapat dibagi menjadi:
1. Hidrolisis fase gas : sebagai penghidrolisa adalah air dan reaksi berjalan pada fase uap
2. Hidrolisis fase cair : pada hidrolisa ini, ada 4 tipe hidrolisa, yaitu: a. Hidrolisis murni : Efek dekomposisinya jarang terjadi, tidak semua
bahan terhidrolisa. Efektif digunakan pada; Reaksi Grigrad dimana air digunakan sebagai penghidrolisa
c. Hidrolisis dengan alkali berair: penggunaan konsentrasi alkali yang rendah dalam proses hidrolisa diharapkan ion H+ bertindak sebagai katalisator sedangkan pada konsentrasi tinggi diharapkan dapat bereaksi dengan asam yang terbentuk.
d. Hidrolisis dengan enzim : Senyawa dapat digunakan untuk mengubah suatu bahan menjadi bahan hidrolisa lain.
Aplikasi hidrolisa pati banyak digunakan dalam industri makanan dan minuman yang menggunakan sirup glukosa hasil hidrolisis pati sebagai pemanis. Produk akhir hidrolisa pati adalah glukosa yang dapat dijadikan bahan baku untuk produksi fruktosa dan sorbitol. Hasil hidrolisis pati juga banyak digunakan dalam industry obat-obatan. Dan juga glukosa yang dihasilkan dapat digunakan sebagai bahan baku pembuatan bioetanol. Penggunaan asam sebagai penghidrolisa menghasilkan biaya produksi yang sedikit, namun produk yang dihasilkan tidak seragam dan banyak senyawa pati yang rusak oleh asam tersebut, sedangkan penggunaan enzim sebagai penghidrolisa menghasilkan produk yang seragam, lebih terkontrol, namun biaya produksi lebih tinggi karena harga dari enzim sendiri lebih mahal jika dibandingkan dengan asam.
2.5.1 Hidrolisis Enzim
Enzim adalah biomolekul berupa protein yang berfungsi sebagai katalis (senyawa yang mempercepat proses reaksi tanpa habis bereaksi) dalam suatu reaksi kimia organik. Molekul awal yang disebut substrat akan dipercepat perubahannya menjadi molekul lain yang disebut produk. Jenis produk yang akan dihasilkan bergantung pada suatu kondisi/zat, yang disebut promoter. Semua proses biologis sel memerlukan enzim agar dapat berlangsung dengan cukup cepat dalam suatu arah lintasan metabolism yang ditentukan oleh hormone sebagai promoter.
X + C XC (1) Y + XC XYC (2)
XYC CZ (3)
CZ C + Z (4) [4].
Meskipun senyawa katalis dapat berubah pada reaksi awal, pada reaksi akhir molekul katalis akan kembali ke bentuk semula. Sebagian besar enzim bekerja secara khas, yang artinya setiap jenis enzim hanya dapat bekerja pada satu macam senyawa atau reaksi kimia. Hal ini disebabkan perbedaan struktur kimia tiap enzim yang bersifat tetap. Sebagai contoh enzim alfa amylase hanya dapat digunakan pada proses perombakan pati menjadi glukosa.
2.5.2 Hidrolisis Asam
Pati dapat dikonversi dengan cara menghidrolisis suspensi pati secara terkendali dengan menggunakan asam dan pemanasan. Beberapa bagian dari ikatan glikosidik pati akan mengalami pemutusan dengan perlakuan asam sehingga dapat dihasilkan molekul pati menurun, dimana akan dihasilkan pati dengan perlakuan asam sehingga dapat dihasilkan molekul pati yang lebih pendek. Hal ini mengakibatkan sifat kemempuan gelatinasi pati menurun, dimana akan dihasilkan pati dengan viskositas yang lebih rendah pada saat pemasakan. Dengan demikian konsentrasi pati yang dapat digunakan dalam proses pengolahan dapat lebih besar. Pati akan lebih larut dengan viskositas yang lebih rendah tetapi dapat menghasilkan struktur gel yang lebih kuat.
2.5.3 Hidrolisis Karbohidrat
Hidrolisis karbohidrat dapat dilakukan dengan cara hidrolisis dengan katalis asam, kombinasi asam dengan enzim serta kombinasi enzim dengan enzim. Hidrolisis pati dengan asam memerlukan suhu tinggi yaitu 120-160oC . Asam akan memecah molekul pati secara acak dan gula yang dihasilkan sebagian besar adalah gula pereduksi. Pada tahap pertama hidrolisis dilakukan dengan katalis asam sampai mencapi nilai derajat konversi sekitar 40-50%. Hidrolisis dengan kombinasi asam dan enzim akan mencapai nilai dekstrosa yang dikehendaki sebesar 62% setelah dinetralkan, dijernihkan dan dihidrolisis dengan enzim dengan memanfaatkan mikroorganisme [19].
Pada proses hidrolisis untuk pembuatan sirup glukosa terdiri dari 2 tahap yaitu dengan likuifikasi dan sakarifikasi. Likuifikasi adalah proses pencairan gel pati dengan menggunakan enzim -amilase untuk menghidrolisis pati. Penggunaan asam dalam hidrolisis memiliki kelebihan yaitu lebih mudah dalam proses karena tidak dipengaruhi oleh beberapa faktor, hidrolisis terjadi secara acak dan waktu lebih cepat. Kelebihan hidrolisis dengan menggunakan enzim yaitu reaksi hidrolisis yang terjadi dapat beragam, kondisi proses yang digunakan tidak ekstrim, seperti suhu sedang dan pH mendekati netral, tingkat konversi lebih tinggi, polutan lebih rendah dan reaksi yang spesifik [19].
Hasil hidrolisis enzim pemecah pati dipengaruhi oleh beberapa faktor, diantaranya jenis pati, kandungan amilosa dan amilopektin pati, kondisi lingkungan enzim meliputi suhu, pH dan konsentrasi substrat maupun enzim dan perlakuan pendahuluan enzim sebelum hidrolisis [25].
Mekanisme reaksi hidrolisis karbohidrat dapat dilihat pada gambar berikut:
2.5.4 Hidrolisis Pati
Hidrolisis pati terjadi antar suatu reaktan pati dengan reaktan air. Reaksi hidrolisis pati bertujuan untuk memotong suatu ikatan polimer sakarida dalam pati dengan bantuan suatu senyawa tertentu sebagai katalis, dalam hal ini adalah enzim α-amylase. Hidrolisis bisa jadi merupakan reaksi yang reversible. Namun jika kondisi operasinya di atur, reaksi hidrolisis bisa berlangsung secara Irreversibel
(C5H10O5)x + xH2O (x-1)C6H12O6 pati air gula
Suhu dan waktu hidrolisis serta konsentrasi katalis adalah beberapa variabel yang berpengaruh dalam reaksi hidrolisis. Makin tinggi suhu makin cepat jalannya reaksi makin tinggi harga DEnya. Namun harus diperhatikan jika katalisator yang dipakai adalah enzim, karena enzim sensitif terhadap suhu tinggi. Jika suhu terlalu tinggi aktifitas enzim akan menurun bahkan enzim dapat rusak. Perbedaan waktu hidrolisis akan menyebabkan jumlah pati yang termodifikasi juga berbeda. Makin lama waktu hidrolisis makin besar persentase pati yang berubah menjadi gula pereduksi. Hal ini dapat dilihat dari harga DE yang semakin tinggi.
Konsentrasi katalis juga dapat berpengaruh pada harga DE dari produk yang dihasilkan. Makin tinggi konsentrasi katalis, dalam hal ini adalah enzim, makin banyak gula pereduksi yang terbentuk. Hal ini berarti harga DE akan semakin tinggi. Meskipun demikian, penentuan konsentrasi katalis memiliki batas optimum. Jika melebihi batas tersebut, hidrolisis akan terhambat [9].
2.6 SIRUP GLUKOSA
Sirup glukosa yang mempunyai nama lain dectrose adalah salah satu produk bahan pemanis makanan dan minuman yang berbentuk cairan, tidak berbau dan tidak berwarna tetapi memiliki rasa manis yang tinggi. Sirup glukosa atau sering juga disebut gula cair dibuat melalui proses hidrolisis pati. Perbedaannya dengan gula pasir yaitu, gula pasir (sukrosa) merupakan gula disakarida, sedangkan sirup glukosa adalah monosakarida, terdiri atas satu monomer yaitu glukosa. Sirup glukosa dapat dibuat dengan cara hidrolisis asam atau dengan cara enzimatis. Dari kedua cara tersebut, pembuatan sirup glukosa secara enzimatis dapat dikembangkan di pedesaan karena tidak banyak menggunakan bahan kimia sehingga aman dan tidak mencemarilingkungan. Bahan lain yang diperlukan adalah enzim amilase [32].
Proses pembuatan Sirup glukosa dapat dilakukan dengan dua cara yaitu: 1.Hidrolisis secara enzimatis
2.Hidrolisis secara asam
2.6.1 Hidrolisis Secara Enzimatis
Hidrolisis secara enzimatis memutus rantai pati secara spesifik pada percabangan tertentu. Hidrolisis enzimatis memiliki beberapa keuntungan, yaitu prosesnya lebih spesifik, kondisi prosesnya dapat dikontrol, biaya pemurnian lebih murah, dihasilkan lebih sedikit abu dan produk samping, dan kerusakan warna dapat diminimalkan. Pada hidrolisis pati secara enzimatis untuk menghasilkan sirup glukosa, enzim yang dapat digunakan adalah α-amilase, β-amilase, amiloglukosidase, glukosa isomerase, pullulanase, dan isoamilase.
Hidrolisa enzim dilakukan menggunakan bantuan enzim α-amilase dan enzim glukoamilase (amiloglukosidase). Enzim α-amilase digunakan pada proses likuifikasi, sedangkan glukoamilase digunakan pada proses sakarifikasi. Hidrolisa enzim lebih banyak memberikan keuntungan dibandingkan dengan hidrolisa asam. Hidrolisa enzim menghasilkan konversi yang lebih besar jika dibandingkan dengan hidrolisa asam. Hidrolisa enzim juga dapat mencegah adanya reaksi efek samping karena sifat katalis enzim sangat spesifik, sehingga dapat mempertahankan flavor dan aroma bahan dasar [40].
Adapun kelebihan dan kekurangan hidrolisis pati dengan enzim adalah : Kelebihan :
1. Bahan baku mudah didapat.
2. Proses lebih sederhana dibandingkan dengan menggunakan asam 3. Peralatan tidak rumit sehingga operasi tidak butuh tenaga banyak 4. Akan di dapat hasil sirup glukosa yang lebih jernih dan bersih Kekurangan :
1. Pemakaian enzim banyak
2. Enzim yang dipakai masih import dan harganya relatif mahal
2.6.2 Hidrolisis Secara Asam
Hidrolisis pati dengan menggunakan katalis asam, molekul pati akan dipecah secara acak oleh asam dan gula yang dihasilkan sebagian besar merupakan gula pereduksi. Pada hidrolisis pati menggunakan katalis enzim, molekul pati akan dipecah atau diputus oleh enzim secara spesifik pada percabangan tertentu. Hidrolisis pati secara asam hanya akan mendapatkan sirup glukosa dengan dektrosa equivalen (DE) sebesar 55. Sedangkan hidrolisis pati secara enzimatis akan mendapatkan sirup glukosa dengan DE lebih dari 95% [34].
terjadinya reaksi sampingan karena sifat enzim yang sangat spesifik sehingga dapat mempertahankan flavor dan aroma bahan dasar.
Adapun kelebihan dan kekurangannya adalah : Kelebihan :
1. Bahan baku mudah didapat
2. Tidak menggunakan enzim sehingga menghemat biaya.
3. Peralatan tidak rumit sehingga operasi tidak butuh tenaga banyak.
4. Cocok untuk kondisi kritis saat ini karena seluruh bahan tersedia di dalam negeri.
Kekurangan :
Pemakaian asam menyebabkan korosi peralatan [32].
2.7 POTENSI EKONOMI SIRUP GLUKOSA DARI BIJI DURIAN
Biji durian merupakan salah satu komoditi yang menarik untuk dikembangkan penggunaannya. Selain menarik, komoditi ini memiliki kecenderungan peningkatan produksi setiap tahunnya, khususnya di Indonesia. Peningkatan biji durian ini dapat dilihat dari peningkatan hasil produksi buah durian. Data produksi durian di Indonesia dapat dilihat pada tabel 2.2 di bawah ini.
Tabel 2.2 Data Produksi Durian Indonesia [43] Tahun Produksi Durian(ton)
2010 492.139
2011 883.969
2012 888.127
Salah satu produk dari pengolahan biji durian adalah sirup glukosa. Produksi sirup glukosa nasional juga mengalami peningkatan yang cukup signifikan. Hal ini dapat dilihat pada tabel 2.3 berikut ini.
Tabel 2.3 Data Produksi dan Impor Sirup Glukosa (kg) [44]
No. Uraian 2010 2011 2012 2013
1 Total produksi 3.504.883 5.847.827 3.850.698 2.266.179 2 Impor 21.572.474 21.743.106 41.303.296 73.099.849
Dari data tabel 2.2 di atas dapat dilihat bahwa produksi durian semakin meningkat setiap tahunnya dan hal ini juga seiring dengan peningkatan jumlah biji durian. Seiring dengan peningkatan ini maka diharapkan dapat menunjang kebutuhan sirup glukosa yang semakin meningkat juga setiap tahunnya.
Sejalan dengan hal tersebut, perlu adanya pengembangan teknologi yang berkaitan dengan produksi sirup glukosa, termasuk di dalamnya adalah variasi bahan baku yang digunakan. Salah satu bahan baku yang dapat diproses menjadi sirup glukosa adalah biji durian yang mengandung karbohidrat yang cukup tinggi yang berpotensi dijadikan menjadi sirup glukosa melalui proses hidrolisis.
Ditinjau berdasarkan bahan baku biji durian yang tersedia di indonesia cukup banyak, dimana indonesia merupakan salah satu negara penghasil durian. Karena memiliki potensi yang cukup baik, perlu dilakukan kajian ekonomi terhadap hal ini. Namun, dalam tulisan ini hanya akan dilakukan kajian ekonomi secara sederhana yaitu dengan menghitung selisih antara harga biaya produksi dengan harga produk yang dijual.
Berikut ini adalah biaya produksi dan harga produk :
Biaya produksi = Rp 5.000/ liter
![Tabel 2.1 Komposisi Biji Durian (lanjutan)[23]](https://thumb-ap.123doks.com/thumbv2/123dok/1938472.1178680/3.595.109.516.104.384/tabel-komposisi-biji-durian-lanjutan.webp)
![Gambar 2.5 Mekanisme Reaksi Hidrolisis Karbohidrat [24]](https://thumb-ap.123doks.com/thumbv2/123dok/1938472.1178680/15.595.123.490.596.700/gambar-mekanisme-reaksi-hidrolisis-karbohidrat.webp)
![Tabel 2.2 Data Produksi Durian Indonesia [43]](https://thumb-ap.123doks.com/thumbv2/123dok/1938472.1178680/19.595.203.422.534.673/tabel-data-produksi-durian-indonesia.webp)