PEMBUATAN MEMBRAN KITOSAN POLIVINIL ALKOHOL SEBAGAI ADSORBEN UNTUK MENURUNKAN KADAR LOGAM NIKEL (Ni) DAN
KROM (Cr)
SKRIPSI
MUHAMMAD MARDUANSYAH 140822038
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
MEDAN
2017
PEMBUATAN MEMBRAN KITOSAN POLIVINIL ALKOHOL SEBAGAI ADSORBEN UNTUK MENURUNKAN KADAR
LOGAM NIKEL (Ni) DAN KROM (Cr)
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
MUHAMMAD MARDUANSYAH 140822038
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SUMATERA UTARA
MEDAN
2017
PERSETUJUAN
Judul: Pembuatan Membran KitosanPolivinilAlkohol Sebagai Adsorben Untuk Menurunkan Kadar Logam Nikel (Ni)danKrom (Cr)
Kategori : Skripsi
Nama : Muhammad Marduansyah
Nomor Induk Mahasiswa : 140822038
Program Studi : Sarjana (S1) Kimia
Departemen : Kimia
Fakultas : Matematika Dan IlmuPengetahuanAlam (FMIPA)Universitas Sumatera Utara
Disetujui di Medan,Januari2017 KomisiPembimbing :
Pembimbing 2, Pembimbing 1,
Prof.Dr.ZulAlfian,MSc Prof.Dr.Harry Agusnar,MSc.,M.Phill NIP. 195504051983031002 NIP. 195308171983031002
Departemen Kimia FMIPA USU Ketua,
Dr. Rumondang Bulan, MS.
NIP. 195408301985032001
PERNYATAAN
PEMBUATAN MEMBRAN KITOSAN POLIVINIL ALKOHOL SEBAGAI ADSORBEN UNTUK MENURUNKAN KADAR
LOGAM NIKEL (Ni)DAN KROM (Cr)
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil karya saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing-masing disebutkan sumbernya.
Medan,Januari 2017
MUHAMMAD MARDUANSYAH
140822038
PENGHARGAAN
Bismillaahhirrohmaanirrohiim.
Alhamdulillaahi Robbil aalamiin Penulis ucapkan sebagai suatu ungkapan rasa syukur kepada Allah SWT yang Maha Esa atas kuasanya yang tetap mencurahkan berkah, rahmat, nikmat kesehatan jasmani dan rohani, sehingga Penulis dapat menyelesaikan penelitiandanskripsi ini sebagai salah satu persyaratan yangharusdipenuhiuntuk mendapatkan gelar SarjanaSainsdi Fakultas Matematika Dan Ilmu Pengetahuan Alam (FMIPA) Universitas Sumatera Utara.
Penulis mengucapkan penghargaan dan cinta kasih yang terdalam dan tulus kepada ayahanda Ponidi dan Ibunda Ida Warsih atas segala do’a, binbingan, semangat, pengorbanan waktu dan materi serta kasih sayang yang diberikan kepada penulis sehingga dapat menyelesaikan kuliah dengan baik. Kepada abang dana dik- adik tercinta Ramdiansyah, Tri Kusnandri A.Md, Siti Fatimah Azzahra dan Djopi Bhimatara yang telah memberikan bantuan dan dukungan kepada Penulis baik dalam suka maupun duka.
Ucapan terima kasih juga penulis sampaikan kepada Prof.Dr.Harry Agusnar,MSc.,M.Phill sebagai pembimbing 1 yang telahmem berikan topic dan tunjuk ajar hingga terselesaikannya penulisan skripsi ini dan Prof.Dr.ZulAlfian,MSc sebagai pembimbing 2 yang pada penyelesaian skripsi ini telah memberikan panduan dan penuh kepercayaan kepada penulis untuk menyempurnakannya.Terimakasih kepada Dr. Rumondang Bulan, MS dan Drs. Albert Pasaribu, M.Sc selaku Ketua Departemen dan Sekertaris Departemen Kimia FMIPA USU. Terima kasih juga Penulis ucapkan kepada M.Dimas Ekananda S.Si danjuga Ayu Manja S.Si yang telah memberikan pengetahuan mengenai preparasi membrane kitosan kepada Penulis sehingga dapat membantu dalam menyelesaikan skripsi ini. Dan tak lupa Penulis ucapkan terima kasih kepada teman-teman seperjuangan windri, aisyah, Adrian,nizar, ikhsan dan seluruh teman-teman kimia ekstensi dan semua pihak yang telah membantu, memberi dukungan, semangat dan motivasi selama masa perkuliahan ini.
Semoga Allah memberikan rahmat dan berkah-Nya serta membalas segala kebaikan yang telah diberikan kepada Penulis. Amin Ya Rabbal’alamin
Penulis
PEMBUATAN MEMBRAN KITOSAN POLIVINIL ALKOHOL SEBAGAI ADSORBEN UNTUK MENURUNKAN KADAR
LOGAM NIKEL (Ni) DAN KROM (Cr)
ABSTRAK
Telah dilakukan penelitian pembuatan membran kitosan polivinil alkohol sebagai adsorben untuk menurunkan kadar logam nikel (Ni) dan krom (Cr). Polivinil Alkohol (PVA) merupakan salah satu jenis bahan polimer yang mempunyai sifat permeabilitas mampu membentuk film dan mampu berikatan dengan kitosan. Pada penelitian ini, didahului dengan pembuatan membran kitosan dengan melarutkan kitosan dan asam laktat 3% dan ditambahkan larutan polivinil alkohol yang kemudian direfluks pada suhu 85
0C selama 30 menit. Selanjutnya campuran kitosan- PVA dimasukan kedalam plat kaca kemudian sampel kitosan-PVA dipanaskan dalam oven pada suhu 40
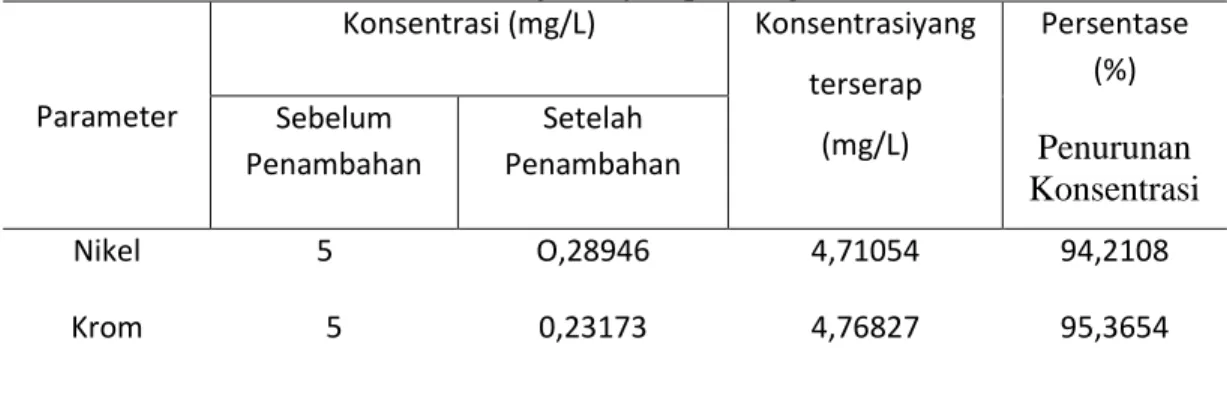
0C selama 24 jam. Setelah membran kitosan mengering dan dilepaskan dari plat kaca. 0,5 gram membran kitosan-PVA dimasukkan ke dalam beaker glass, lalu masing-masing ditambahkan dengan 50 mL larutan standar nikel dan krom 5mg/L, didiamkan selama 30 menit. Hasil penelitian menunjukkan bahwa proses adsorpsi logam Nikel (Ni) diperoleh persentase penyerapan 94,2108%. Dan logam krom (Cr) diperoleh persentase penyerapan 95,3654%.
Katakunci:Kitosan, PVA, Adsorben, Logam Ni, Logam Cr
PRODUCT OF MEMBRANE CHITOSAN POLYVINYL ALCOHOL AS ADSORBENT TO REDUCE OF
NICKEL METAL AND CHROM METAL
ABSTRACT
Has been done the research product of chitosan polyvinyl alcohol as absorbent to reduce of Ni metal and Cr metal. PVA is one type of polymer material that has a permeability able to form of film and able of binding of chitosan. In this research, preceded by making of membrane chitosan by dissolving chitosan and lactic acid 3%
and added a solution of PVA and then refluxed at a temperature of 85
oC for 30 minutes. The next mixture chitosan-PVA Inserted into glass plate and then sample chitosan-PVA heated in an oven at a temperature 40
oC for 24 hours. After chitosan- PVA dry out and removed from glass plate. 0,5 gram chitosan membrane is inserted into the glass beaker. Then each added with 50 mL standard solution Ni metal and Cr metal 5 mg/L. allowed to stand for 30 minutes. The results showed that the adsorption Ni metal process was gained 94,2108% in the percentage and adsorption Cr metal process was gained 95,3654% In the percentage.
Keywords: Chitosan, Adsorbent, Ni Metal, Cr metal
DAFTAR ISI
Halaman
Persetujuan ii
Pernyataan iii
Penghargaan iv
Abstrak v
Abstract vi
Daftar Isi vii
Daftar Tabel ix
Daftar Gambar x
Daftar Lampiran xi
BAB 1 PENDAHULUAN 1.1. Latar Belakang 1
1.2. Permasalahan 3
1.3. Pembatasan Masalah 3
1.4. Tujuan Penelitian 3
1.5. Manfaat Penelitian 3
1.6. Lokasi Penelitian 4
1.7. Metodologi Penelitian 4
BAB 2 TINJAUAN PUSTAKA 2.1. Kitin dan Kitosan 5
2.2. Metode Penyediaan Kitosan 7
2.2.1. Metode Harowitz 8
2.2.2. Metode Rigby dan Wolfrom 8
2.2.3. Metode Fujita 8
2.2.4. Metode Alimuniar dan Zainuddin 9
2.3. Derajat Deasetilasi 9
2.4. Sifat- Sifat Kitosan 10
2.5. Aplikasi dan Kegunaan Kitosan 13
2.6. Keterkaitan Sifat Fisik-Kimia pada Kitosan 15
2.7. Polivinil Alkohol 16
2.8. Penanganan Limbah 18
2.9. Logam Berat dan Pengaruhnya Pada Kesehatan 18
2.9.1. Logam Krom 19
2.9.2. Logam Nikel 19
2.9.3. Logam Timbal 20
2.9.4. Tembaga Cu 20
2.9.5. Logam Kadmium 20
2.10. Kemampuan Kitosan Untuk Menyerap Logam 21
2.11. Adsorpsi 22
2.12. Membran 24
2.12.1. Klasifikasi Membran 25
2.12.2. Membran Polimer Alam 27
2.13. Spekstroskopi Fourier Transform Infra Red (FTIR) 27
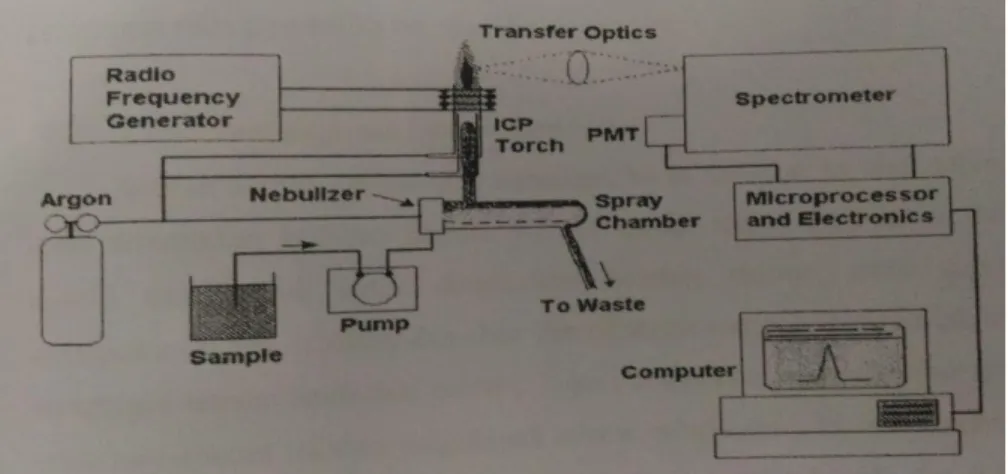
2.14. Bagian-bagian alat ICP (Inductively Coupled Plasma) 29
BAB 3 METODE PENELITIAN 3.1. Alat 33
3.2. Bahan 33
3.3. Prosedur Penelitian 34
3.3.1. Pembuatan Larutan Pereaksi 34
3.3.1.1. Penyediaan Larutan Asam Laktat 3% 34
3.3.2. Pembuatan Larutan Standart Nikel 34
3.3.2.1. Pembuatan Larutan Induk 1000ppm dari NiCl
234
3.3.2.2 Pembuatan Larutan Sandart Nikel 100ppm 34
3.3.2.3. Pembuatan Larutan Sandart Nikel 10ppm 34
3.3.2.4. Pembuatan Larutan Sandart Nikel 5ppm 34 3.3.3. Pembuatan Larutan Standart Krom 35
3.3.2.1. Pembuatan Larutan Induk 1000ppm dari K
2Cr
2O
735
3.3.2.2 Pembuatan Larutan Sandart Krom 100ppm 35
3.3.2.3. Pembuatan Larutan Sandart Krom 10ppm 35
3.3.2.4. Pembuatan Larutan Sandart Krom 5ppm 35 3.3.4. Pembuatan Membran Kitosan Polivinil Alkohol 35
3.3.5. Penerapan Logam Nikel dengan Membran Kitosan-PVA 36 3.4. Bagan Penelitian 36
3.4.1. Preparasi Sampel Kitosan 3% 36
3.4.2. Pembuatan Kitosan Sampel-PVA 36
3.4.3. Penerapan Logam Nikel dengan Membran Kitosan PVA 37 3.4.4. Penerapan Logam Krom dengan Membran Kitosan PVA 37 BAB 4 HASIL DAN PEMBAHASAN 4.1. Data dan Pembahasan Spekstroskopi Fourier Transform Infra Red (FTIR) 38
4.2. Data Inductively Coupled Plasma (ICP) 41
4.3. Perhitungan Persentase Penurunan Kadar Logam Nikel dan
Krom dalam Laruan (penurunan % adsorpsi) 42
BAB 5 KESIMPULAN DAN SARAN
5.1. Kesimpulan 43
5.2. Saran 43
Daftar Pustaka 44
Lampiran 47
DAFTAR TABEL
Nomor Judul Halaman
Tabel
2.1. Kelarutan Kitosan pada berbagai Pelarut Asam Organik 10 2.2. Karakteristik Kitosan
13 2.3. Aplikasi dan Fungsi Kitosan di berbagai Bidang 15
2.4. Spesifikasi Kitosan 16
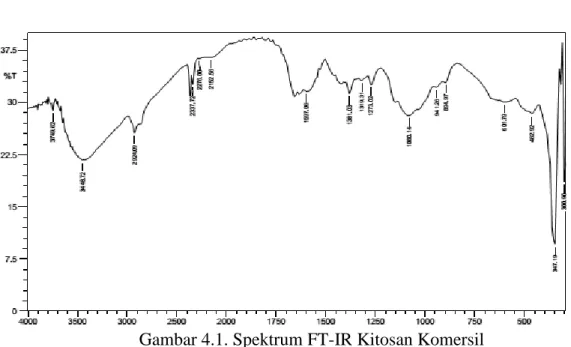
4.1. Data FT-IR Kitosan Komersil 38
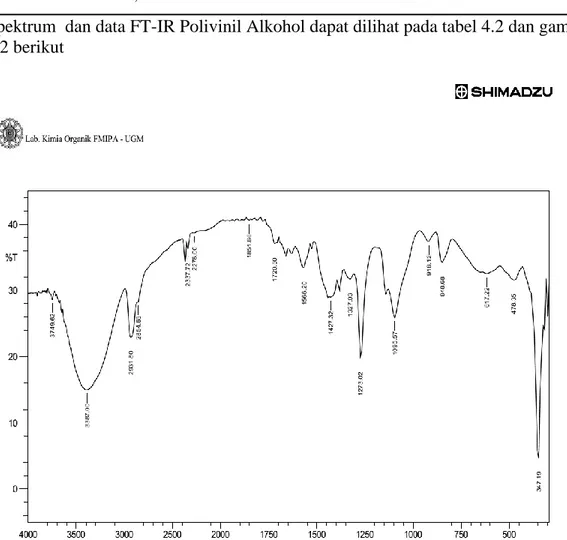
4.2. Data FT-IR Polivinil Alkohol 39
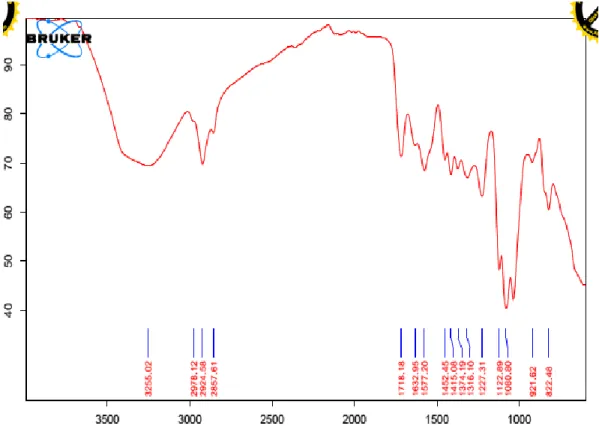
4.3. Data FT-IR Kitosan-Polivinil Alkohol 40
4.4. Data Hasil Uji Penyerapan Logam Metode ICP 43
DAFTAR GAMBAR
Nomor Judul Halaman
Gambar
2.1. Struktur Kitin 5
2.2. Struktur Kitosan 6
2.3. Kitosan sebagai Polielektrolit Kationik 16
2.4. Reaksi Pembentukan PVA dari Metanolisis Polivinil Asetat 18
2.5. Komponen dari Alat ICP 29
4.1. Spektrum FT-IR Kitosan Komersil 38
4.2. Spektrum FT-IR Polivinil Alkohol 39
4.3. Spektrum FT-IR Kitosan-Polivinil Alkohol 40
DAFTAR LAMPIRAN
Nomor
Lampiran Judul Halaman
1. Foto Membran Kitosan-Polivinil Alkohol 47
2. Foto Data Hasil Uji Analisa Penyerapan Logam Nikel
Menggunakan Alat ICP 48
3. Foto Data Hasil Uji Analisa Penyerapan Logam Krom
Menggunakan Alat ICP 49
4. Spektrum FT-IR Kitosan Komersil 50
5. Spektrum FT-IR Polivinil Alkohol 51
6. Spektrum FT-IR Kitosan-Polivinil Alkohol 52
BAB 1
PENDAHULUAN
1.1. Latar Belakang
Dewasa ini aplikasi kitin dan kitosan sangat banyak dan meluas. Dibidang industri kitin dan kitosan berperan antara lain sebagai koagulan polielektrolit pengolahan limbah cair, pengikat dan penyerap ion logam, mikroorganisme, mikroalga, pewarna residu pestisida, lemak, tanin, dan lain sebagainya, sementara dibidang pertanian dan pangan kitin dan kitosan digunakan antara lain untuk pencampuran ransum pakan ternak, antimikroba, anti jamur serat bahan pangan, penstabilisasi pembentuk gel, pembentuk tekstur, pengental, pengemulsi produk olahan pangan, pembawa zat aditif makanan. Sedangkan dalam bidang farmasi dan kedokteran kitosan dapat digunakan sebagai bahan pembuat obat-obatan, anti tumor, anti virus, pembuluh darah kulit dan ginjal sintetik, aditif kosmetik, anti infeksi, pembalut luka dan benang bedah yang mudah diserap (Sugita, 2009).
Modifikasi kitosan sebagai adsorben dapat berada dalam berbagai bentuk, antara lain bentuk butir, serpih, hidrogel, membran (film). Kitosan sebagai adsorben sering dimanfaatkan untuk proses adsorpsi ion logam berat. Kemampuan kitin dan kitosan dalam mengadsorpsi logam berat dipengaruhi oleh jumlah gugus –NH
2yang ditunjukkan oleh derajat deasetilasi. (Rao et al, 1993).
Membran kitosan /polivinil alkohol merupakan salah satu modifikasi kimia
yang bisa dilakukan untuk menghasilkan suatu material baru yang memiliki
karakteristik yang lebih baik. Seperti yang diketahui kitosan yang berasal dari cangkang blangkas memiliki berat molekul yang lebih tinggi sehingga membran (film) yang terbentuk darinya akan memiliki sifat mekanik yang lebih baik dari pada kitosan yang berbobot molekul sedang dan rendah. Selain itu polivinil alkohol (PVA) merupakan polimer sintetik yang bersifat biokompatibel, tidak toksik dan tidak karsinogenik. PVA memiliki gaya adhesi yang tinggi sehingga sangat baik dalam meningkatkan sifat mekanik, elastisitas dan kekompakan dari material dalam penelitian ini.
Menurut Peraturan Pemerintah Republik Indonesia Nomor 82 tahun 2001, air limbah adalah sisa dari suatu usaha dan atau kegiatan yang berwujud cair. Air limbah dapat berasal dari rumah tangga maupun industri. Limbah cair industri adalah buangan hasil proses/sisa dari suatu kegiatan/usaha yang berwujud cair dimana kehadirannya pada suatu saat dan tempat tidak dikehendaki lingkungannya karena tidak mempunyai nilai ekonomis sehingga cenderung untuk dibuang ( Asmadi,2012 ).
Logam berat didefinisikan sebagai logam yang memiliki densitas atau
kerapatan tinggi dan merupakan pencemar yang banyak dijumpai baik di lingkungan
darat maupun di perairan. Keberadaan logam berat akan membawa pengaruh pada
kehidupan organisme di lingkungan (termasuk manusia), karena sifatnya yang
meracun dan dapat menyebabkan kematian apabila jumlahnya melewati ambang
batas yang ditetapkan. Kandungan logam berat di lingkungan dapat dikurangi dengan
cara menyerapnya, salah satunya dengan menggunakan kitosan. Beberapa contoh
logam berat adalah Hg,Zn,Cd,Cu,Ni,Pb dan Cr. Proses penyerapan logam berat pada
kitosan dan modifikasinya berlangsung spontan (Karthikeyan et al, 2004).
Meriatna (2008) dalam Tesisnya “Penggunaan Membran Kitosan Unuk Menurunkan Kadar Logam Krom (Cr) dan Nickel (Ni) dalam Limbah Cair Pelapis Logam” diketahui membran kitosan yang hasil cukup baik yaitu memiliki persentase daya serap yang tinggi dengan waktu kontak 30 menit dan konsentrasi 3% dan memiliki sifat mekanik yang cukup baik jika dibandingkan dengan konsetrasi yang lebih rendah.
Nikel dan krom sebagai bahan paduan logam banyak digunakan diberbagai bidang industri logam, berbagai macam baja, serta elektroplating karena bersifat kuat, tahan tempa, anti karat, tahan suhu tinggi. Logam/senyawa nikel dan krom merupakan bahan karsinogenik. Terutama bagi pekerja di industri pemurnian logam.
Pekerja yang terpapar nickel atau krom ditempat kerja selama 40 tahun bisa mengalami kanker paru-paru dan kanker nasal (Widowati, 2008)
Karena dampak sifat logam Nikel (Ni) dan Krom (Cr) yang berbahaya dan merupakan bahan dasar pada industri elektroplating, Limbah hasil proses kemungkinan besar mengandung sisa nikel dan krom yang dapat terpapar langsung pada pekerja industri, maka penulis tertarik untuk membuat membran kitosan dengan PVA sebagai adsorben untuk meningkatkan proses penyerapan logam-logam berbahaya seperti Nikel dan Krom.
1.2 Permasalahan
1. Bagaimana cara preparasi pembuatan membran kitosan PVA?
2. Bagaimana pengaruh daya serap kitosan terhadap logam Ni dan Cr?
1.3 Pembatasan Masalah
1. Sampel yang digunakan adalah kitosan dari cangkang blangkas 2. PVA diperoleh secara komersil
3. Campuran kitosan dan PVA dibuat menjadi bentuk membran
1.4 Tujuan Penelitian
1. Untuk mengetahui cara preparasi pembuatan membran kitosan PVA.
2. Untuk mengetahui pengaruh daya serap kitosan PVA terhadap logam Ni dan Cr.
1.5 Manfaat Penelitian
Hasil yang diperoleh dari penelitian ini diharapkan dapat menjadi salah satu informasi ilmiah bahwa membran kitosan PVA dapat digunakan sebagai penanggulangan pencemaran logam berat seperti logam Ni dan Cr.
1.6 Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Kimia Analitik dan Laboratorium Kimia Polimer, Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara. Analisa gugus fungsi menggunakan Spektrofotometer Fourier Transform Infra Red (FTIR) di Laboratorium Kimia Organik, Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Gajah Mada. Analisa logam Nikel dan Krom dilakukan di Balai Teknik Kesehatan Linkungan dan Pengendalian Penyakit (BTKLPP).
1.7 Metodologi Penelitian
1. Penelitian ini dilakukan secara eksperimen laboratorium
2. Pembuatan membran kitosan dengan cara menimbang dan dilarutkan dengan asam laktat 3% campuran kitosan dan asam laktat selanjutnya ditambahkan dengan polivinil alkohol 10% hingga homogen dengan ratio perbandingan 1:1 kemudian direfluks selanjutnya dipanaskan di dalam oven pada suhu 40ºC selama 24 jam. Hasil di karakterisasi dengan spektrofotometer FTIR
3. Analisa logam Ni dan Cr sebelum dan sesudah penyerapan dengan kitosan
dianalisa dengan menggunakan Inductively Coupled Plasma (ICP)
BAB 2
TINJAUAN PUSTAKA
2.1 Kitin dan Kitosan
Kitin pertama kali ditemukan pada tahun 1811 oleh Henry Broconnot sebagai hasil isolasi dari jamur, sedangkan kitin dari serangga diisolasi pertama kali pada tahun 1820-an. Kitosan ditemukan oleh Rouget pada tahun 1859 dengan merefluks kitin dan alkali pada suhu 180
oC. Disini proses deasetilasi kitin dapat berlaku tanpa pemutusan rantai polimer (Brine, 1984)
Senyawa kitin banyak terdapat pada kulit luar hewan seperti Antropoda, Molusca, Annelida dan juga terdapat pada dinding sel tumbuhan tingkat rendah seperti Fungi. Setelah selulosa, kitin diperhitungkan sebagai polisakarida yang terdapat melimpah di alam (Sirait, 2002).
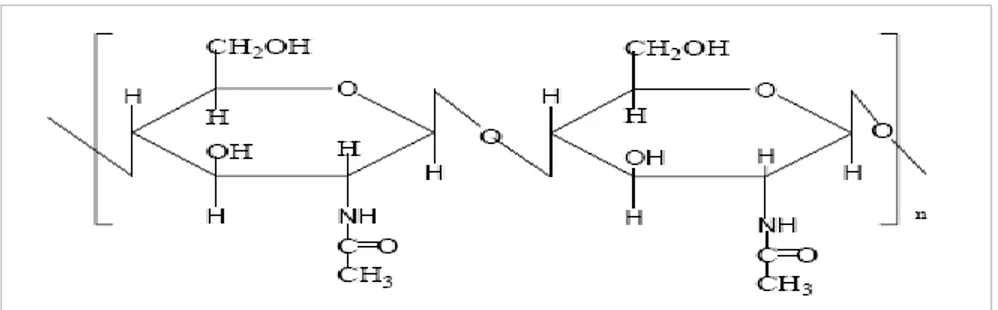
Pada Gambar 1 dan 2 terlihat bahwa kitin murni mengandung gugus Asetamida (NH-COCH
3), dan kitosan murni mengadung gugus amino (NH
2).
Perbedaan gugus ini akan mempengaruhi sifat-sifat kimia senyawa tersebut.
Perbedaan antara kitin dan kitosan adalah berdasarkan kandungan nitrogennya,
bila nitrogen kurang dari 7% maka polimer disebut kitin dan apabila kandungan
total nitrogennya ggg lebih dari 7% maka disebut kitosan (Roberts, 1992).
Gambar 2.1. Struktur Kitin
Rumus umum kitosan adalah (C
6H
11NO
4)
natau disebut sebagai (1,4)-2-Amino-2- Deoksi-β-D-Glukosa, dimana strukturnya dapat dilihat sebagai berikut:
Gambar 2.2. Struktur Kitosan
Sebenarnya kitin dan kitosan yang diproduksi secara komersial memiliki kedua gugus asetamido dan gugus amido pada rantai polimernya, dengan beragam komposisi gugus tersebut.
Kitosan ditemukan pertama kali oleh C. Rouget pada tahun 1859 dengan cara
merefluks kitin dengan kalium hidroksida pekat. Dalam tahun 1934, dua paten
didapatkan oleh Rigby yaitu penemuan mengenai pengubahan kitin menjadi kitosan
dan pembuatan film dari serat kitosan. Perkembangan penggunaan kitin dan kitosan
meningkat pada tahun 1940-an, dan semakin berkembang pada tahun 1970-an seiring
dengan diperlukannya bahan alami dalam berbagai bidang industri (Kaban, 2009).
Kitosan adalah poli-(2-amino-2-deoksi-β-(1 4)-D-glukopiranosa) dengan rumus molekul (C
6H
11NO
4)
n(Gambar 2.2) yang dapat diperoleh dari deasetilasi kitin (Gambar 2.1) Kitosan juga dijumpai secara alamiah dibeberapa organisme (Sugia,2009).
Kitosan merupakan senyawa yang tidak larut dalam air, larutan basa kuat, sedikit larut dalam HCl dan HNO3, 0.5% H3PO4 sedangkan dalam H2SO4 tidak larut. Kitosan tidak beracun dan mudah terbiodegradasi (Muzzarelli, 1978).
Kitosan mempunyai kemampuan untuk mengadsorpsi logam dengan membentuk komplek kitosan dengan logam dan dapat digunakan untuk mengolah limbah. Dalam penggunaannya kitosan tidak beracun dan mampu untuk menurunkan kadar kolesterol dalam darah. (Simangunsong, 1997)
Proses deasetilasi kitosan dapat dilakukan dengan cara kimiawi maupun
enzimatik. Proses kimiawi menggunakan basa, misalnya NaOH, dan dapat
menghasilkan kitosan dengan derajat deasetilasi yang tinggi, yaitu mencapai 85-93 %
(Tsigos et al., 2000). Namun proses kimiawi menghasilkan kitosan dengan bobot
molekul yang beragam dan deasetilasinya juga sangat acak sehingga sifat fisik dan
kimia kitosan tidak seragam (Martinou et al.,2000). Selain itu proses kimiawi juga
dapat menimbulkan pencemaran lingkungan, sulit dikendalikan, dan melibatkan
banyak reaksi samping yang dapat menurunkan rendemen. Proses enzimatik dapat
menutupi kekurangan proses kimiawi. Pada dasarnya deasetilasi secara enzimatik
bersifat selektif dan tidak merusak struktur rantai kitosan, sehingga menghasilkan
kitosan dengan karakteristik yang lebih seragam agar dapat memperluas bidang
aplikasinya (Sugita.2009).
2.2 Metode Penyediaan Kitosan
Metode penyediaan kitosan pertama kali dilakukan oleh Hope-Seyler (1894) yaitu dengan merefluks kitin dalam kalium hidroksida pada suhu 180
oC. Dimana proses deasetilasi kitin dapat dilakukan tanpa pemutusan rantai polimernya.
Terdapat beberapa metode penyediaan kitosan antara lain: (Muzzarelli, 1977).
2.2.1. Metode Harowitz
Kitin dilarutkan dengan kalium hidroksida dan campuran logam nikel di bawah aliran gas nitrogen. Campuran dipanaskan pada suhu 180
oC selama 30 menit, setelah itu di masukkan ke dalam etanol dan akan mengendap kemudian hasil yang diperoleh dicuci dengan air suling.
Hal yang sama dilakukan dengan pelarut pertama di dalam 5% asam asetat dimana NaOH yang berlebih akan mengendap. Metode ini dapat menghasilkan 95% dari pada asetil dalam rantai kitin
2.2.2. Metode Rigby dan Wolfrom
Kitin dicampur dengan 40% NaOH pada suhu 115
oC selama 6 jam di
bawah keadaan yang mengandung nitrogen. Kemudian didinginkan dan seterusnya
dicuci dengan air untuk menetralkan campuran tadi. Metode ini dapat
menghasilkan 82% dari pada asetil pada rantai kitin.
2.2.3. Metode Fujita
Kitin dicampur dengan NaOH 50% dan larutan parafin selama 2 jam pada suhu 120
oC, campuran tersebut dituangkan dalam air dan seterusnya disaring dan dibilas dengan air suling. Metode ini lebih bagus dibandingkan dengan metode lain karena hanya memerlukan sedikit alkali dibandingkan dengan metode lain.
2.2.4. Metode Alimuniar dan Zainuddin
Pada metode ini kiti 10 gr dicampurkan dengan NaOH 50% sebanyak 140 ml dalam beaker glass 500 ml pada temperatur 30
oC dan dibiarkan selama 6 hari, setiap harinya dilakukan pengadukan kemudian dicuci dengan air hingga pH air cucian menjadi netral. kemudian dikeringkan dan dianalisa Metode ini lebih ekonomis dibandingkan metode lain karena proses deasetilasi kitin terjadi tanpa pemanasan pada temperatur 30
oC. Pada umumnya metode lain menggunakan vessel khusus dengan kontrol atmosfir selama waktu tertentu, sedangkan pada metode ini hanya menggunakan vessel sederhana. Metode lain untuk mengontrol reaksi pembentukan produk dibutuhkan sejumlah bahan aditif, sedangkan pada metode ini tidak menggunakan konsumsi bahan aditif lainnya.
2.3 Derajat Deasetilasi (DD)
Kurita (1986) melaporkan bahwa kitin yang direaksikan dengan alkali dapat
mengalami hidrolisis dari gugus asetamida kepada gugus amino. Proses hidrolisis
ini selalu menggunakan NaOH dan KOH pada suhu tinggi. Dalam proses hidrolisis
alkali dapat mengalami penurunan berat molekul, jika waktu reaksi berlangsung
lama. Oleh karena itu di dalam penyediaan kitosan, hidrolisis dapat terjadi jika
pemanasan dilakukan, dan ini tergantung kepada konsentrasi alkali yang digunakan.
Kitosan dengan 45-55% derajat deasetilasi dapat larut dalam air, jika lebih dari 60% atau kurang 40% derajat deasetilasinya, tidak larut dalam air. Sifat kelarutan ini adalah disebabkan oleh deastilasi dalam larutan NaOH pekat. Dan untuk mengukur derajat deasetilasi ini dapat dilakukan dengan cara analisis elemental, infra merah dan titrasi.
2.4 Sifat - sifat Kitosan
Kitosan merupakan padatan amorf yang berwarna putih dengan rotasi spesifik [α]
D11-3 hingga -10
o(padatan konsentrasi asam asetat 2%). Kitosan larut pada kebanyakan larutan asam organik, pada pH sekitar 4,0 tetapi tidak larut pada pH lebih besar dari 6,5, juga tidak larut dalam pelarut air, alkohol dan aseton. Dalam asam mineral HCl dan HNO
3, kitosan larut pada konsentrasi 0,15-1,1%, tetapi tidak larut pada konsentrasi 10%. Kitosan tidak larut dalam H
2SO
4pada berbagai konsentrasi, sedangkan dalam H
3PO
4tidak larut pada konsentrasi 1% sementara pada konsentrasi 0,1% sedikit larut. Perlu kita ketahui, bahwa kelarutan kitosan dipengaruhi oleh bobot molekul, derajat deasetilasi dan rotasi spesifiknya yang beragam tergantung pada sumber dan metode isolasi serta transformasinya (Sugita, 2009).
Tabel 2.1. Kelarutan kitosan pada berbagai pelarut asam organik Konsentrasi asam organik Konsentrasi asam organik (%)
10 50 >50
Asam asetat + ± -
Asam adipat - - -
Asam sitrat + - -
Asam format + + +
Asam laktat + - -
Asam maleat + - -
Asam malonat + - -
Asam oksalat + - -
(Sugita, 2009)
Keterangan : + larut; -tidak larut; ±larut sebagian
Kitosan tidak larut dalam air, pelarut-pelarut organik, juga tidak larut dalam alkali dan asam-asam mineral pada pH di atas 6,5. Dengan adanya sejumlah asam, maka dapat larut dalam air - metanol, air - etanol, dan campuran lainnya. Kitosan larut dalam asam formiat dan asam asetat dan menurut Peniston dalam 20% asam sitrat juga dapat larut. Asam organik lainnya juga tidak dapat melarutkan kitosan, asam-asam anorganik lainnya pada pH tertentu setelah distirer dan dipanaskan dan asam sitrat juga dapat melarutkan kitosan (Sugita, 2009).
Kitosan bersifat polikationik yang dapat mengikat lemak dan logam berat pencemar. Kitosan yang mempunyai gugus amina yaitu adanya unsur N bersifat sangat reaktif dan bersifat basa (Inoue. 1994 ).
Kitosan mempunyai sifat spesifik yaitu adanya sifat bioaktif, biokompatibel, pengkelat, anti bakteri dan dapat terbiodegradasi. Kualitas kitosan dapat dilihat dari sifat intrinsiknya, yaitu kemurniannya, massa molekul, dan derajat deasetilasi.
Umumnya kitosan mempunyai derajat deasetilasi 75-100%. Massa molekul kitosan
dan distribusinya berpengaruh terhadap sifat-sifat fisiko-kimia polisakarida, seperti
sifat reologi kitosan, fleksibilitas rantai. Derajat deasetilasi dan massa molekul
kitosan hasil deasetilasi kitin pada dasarnya dipengaruhi oleh konsentrasi alkali/basa,
rasio larutan terhadap padatan, suhu dan waktu reaksi, lingkungan/kondisi reaksi
selama deasetilasi. Konsentrasi alkali, rasio padatan dan larutan yang tinggi dapat
memfasiltasi proses deasetilsi menghasilkan kitosan yang memiliki sifat fisika-kimia
yang memenuhi syarat untuk berbagai aplikasi (Ramadhan, 2010).
Menurut Robert, (1992), kitosan mudah mengalami degradasi secara biologis, tidak beracun dan baik sebagai flokulan dan koagulan serta mudah membentuk membran atau film. Kitosan merupakan suatu biopolimer alam yang reaktif yang dapat melakukan perubahan - perubahan kimia. Karena ini banyak turunan kitosan dapat dibuat dengan mudah. Beberapa turunan kitosan yang telah dihasilkan dan juga telah diketahui kegunaannya antara lain :
a. N-karboksialkil kitosan, digunakan sebagai pengumpul ion logam b. Asetil kitosan, digunakan dalam industri tekstil dan membran
c. Kitosan glukan, digunakan sebagai pengkelat ion logam dan agen penggumpal
Sama seperti kitin, kitosan juga dapat digunakan dalam berbagai bidang, misalnya : a. Untuk industri kertas, kaca, kain dan pewarna
b. Dalam industri kosmetik
c. Dalam bidang pertanian dan makanan d. Dalam industri semen
e. Dalam bidang kesehatan f. Untuk penyerapan ion logam
Sandford dan Hutchins (1987) menyatakan sifat kationik, biologi dan sifat larutan kitosan adalah sebagai berikut:
1. Sifat kationik:
a. Jumlah muatan positif tinggi: satu muatan per unit gugus glukosamin, jika banyak material bermuatan negatif (seperti protein) maka muatan positif kitosan berinteraksi kuat dengan permukaan negatif.
b. Flokulan yang baik: gugus NH
3+berinteraksi dengan muatan negatif darikoloid.
c. Mengikat ion-ion logam ( Fe, Cu, Cd, Hg, Pb, Cr, Ni, Pu, dan U).
2. Sifat biologi:
a. Dapat terdegradasi secara alami b. Polimer alami
c. Nontoksik
3. Sifat Kimia:
a. Linear poliamin (poli D-glukosamin) yang memiliki gugus amino yang baik untuk reaksi kimia dan pembentukan garam dengan asam.
b. Gugus amino yang reaktif
c. Gugus hidroksil yang reaktif (C3-OH, C6-OH) yang dapat membentuk senyawa turunannya.
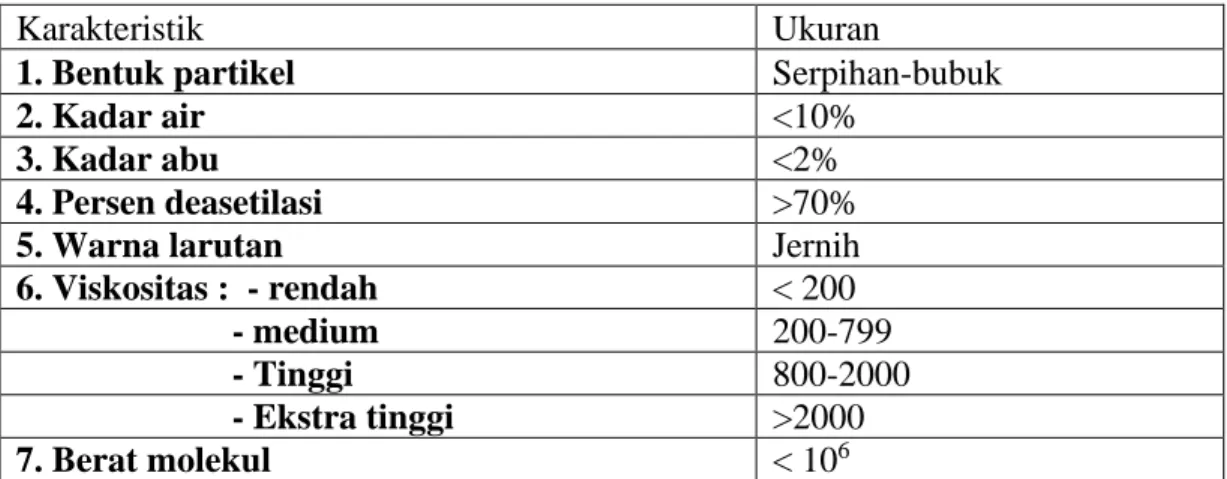
Tabel 2.2 Karakteristik Kitosan
Karakteristik Ukuran
1. Bentuk partikel Serpihan-bubuk
2. Kadar air <10%
3. Kadar abu <2%
4. Persen deasetilasi >70%
5. Warna larutan Jernih
6. Viskositas : - rendah < 200
- medium 200-799
- Tinggi 800-2000
- Ekstra tinggi >2000
7. Berat molekul < 10
6Sumber: Robert (1992)
4. Sifat larutan kitosan (Kationik amin, NH
3+):
a. Larut dalam larutan asam b. Berbentuk larutan kental c. Berbentuk gel
d. Larut dalam campuran alkohol-air.
2.5. Aplikasi dan Kegunaan Kitosan
Kitosan banyak digunakan oleh berbagai industri antara lain industri farmasi, kesehatan, biokimia, bioteknologi, pangan, pengolahan limbah, kosmetik, agroindustri, industri tekstil, industri perkayuan, industri kertas dan industri elektronika. Aplikasi khusus berdasarkan sifat yang dipunyainya antara lain untuk pengolahan limbah cair terutama bahan sebagai bersifat resin penukar ion untuk minimalisasi logam - logam berat, mengkoagulasi minyak/lemak, serta mengurangi kekeruhan, penstabil minyak, rasa dan lemak dalam produk industri pangan (Rismana, 2004).
Sedangkan menurut Wirdaniati, (2006).Kitosan dapat dimaanfaatkan di berbagai bidang biokimia, obat-obatan dan farmakologi, pangan dan gizi, pertanian, mikrobiologi, penanganan air limbah, industri-industri kertas, tekstil membran atau film, kosmetik dan lain sebagainya
Dalam penggunaannya kitosan tidak beracun dan mampu menurunkan kadar kolesterol dalam darah. Kitosan juga dapat digunakan dalam penjernihan atau pengolahan air minum. Pemakaian kitosan pada pengolahan air minum lebih baik dari pada memakai alum atau tawas dan Poli Aluminium Klorida (PAC), karena tawas dan PAC dapat mengakibatkan efek racun bagi kesehatan manusia (Roberts, 1991).
Karena adanya gugus amino, kitosan merupakan polielektrolit kationik (pKa
≈ 6,5) hal yang sangat jarang terjadi secara alami. Sifat yang basa ini menjadikan
kitosan memiliki sifat, yaitu (Meriaty, 2002):
a. Dapat larut dalam media asam encer membentuk larutan yang kental sehingga dapat digunakan dalam pembuatan gel. Dalam beberapa variasi konfigurasi seperti butiran, membran, pelapis kapsul, serat dan spons.
b. Membentuk kompleks yang tidak larut dengan air dengan polianion yang dapat juga digunakan untuk pembuatan butiran gel, kapsul dan membran.
c. Dapat digunakan sebagai pengkelat ion logam berat dimana gelnya menyediakan system produksi terhadap efek dekstruksi dari ion.
Beberapa aplikasi dan fungsi kitosan diberbagai bidang dapat ditunjukkan pada tabel 2.3 berikut ini.
Tabel 2.3 Aplikasi dan fungsi kitosan di berbagai bidang
Bidang Aplikasi Fungsi
I. Pengolahan limbah - Bahan Koagulasi/Flokulasi untuk limbah cair - Penghilangan ion-ion metal dari limbah cair II. Pertanian - Dapat menurunkan kadar asam sayur, buah dan ekstrak kopi
- Sebagai pupuk - Bahan antimicrobial III. Industri tekstil - Serat tekstil
- Meningkatkan ketahanan warna IV. Bioteknologi - Bahan-bahan immobilisasi enzim V.Klarifikasi/penjernihan:
-Limbah industri pangan - Koagulasi/flokulasi -Industri sari buah - Flokulan pektin/protein -Pengolahan minuman beralkohol - Flokulan protein/mikroba -Penjernihan air minum - Koagulasi
-Penjernihan kolam renang - Flokulan mikroba -Penjernihan zat warna - Pembentuk komplek -Penjernihan Tanin - Pembentuk komplek
VI. Kosmetik - Bahan untuk rambut dan kulit
VII. Biomedis - Mempercepat penyembuhan luka
- Menurunkan kadar kolesterol
VIII. Fotografi - Melindungi film dari kerusakan
Sumber: Robert (1992)
Kitosan mempunyai kemampuan untuk mengadsorpsi logam dan membentuk kompleks kitosan dengan logam. Kitosan juga dapat digunakan untuk mengolah limbah, seperti pengolahan limbah dari industri koagulasi karet dan untuk memisahkan protein dari limbah dan padatan dimanfaatkan sebagai sumber protein dalam makanan ternak.
2.6. Keterkaitan Sifat Fisik –Kimia pada Kitosan
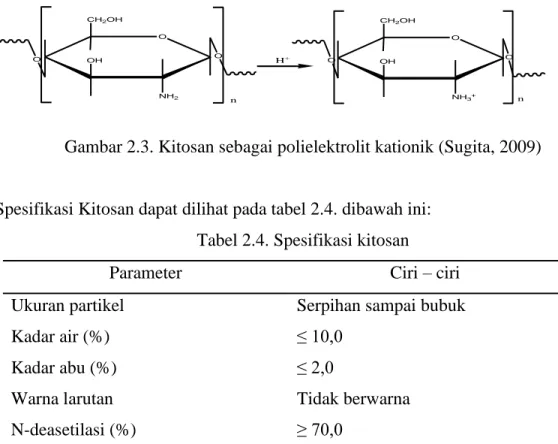
Kitosan dalam bentuk terprotonasi menunjukkan kerapatan muatan yang tinggi dan bersifat sebagai polielektrolit kationik, seperti yang dapat dilihat pada Gambar 2.3 dan sangat efektif berinteraksi dengan biomolekul bermuatan negatif dan biomolekul permukaan. Sedangkan dalam bentuk netralnya, kitosan mampu mengkompleks ion logam berat berbahaya seperti Cu, Cr, Cd, Mn, Co, Ph, Hg, Zn, dan Pd.
O
NH2 OH
CH2OH
O O
n
O
NH3+ OH
CH2OH
O O
n H+
Gambar 2.3. Kitosan sebagai polielektrolit kationik (Sugita, 2009)
Spesifikasi Kitosan dapat dilihat pada tabel 2.4. dibawah ini:
Tabel 2.4. Spesifikasi kitosan
Parameter Ciri – ciri
Ukuran partikel Serpihan sampai bubuk
Kadar air (%) ≤ 10,0
Kadar abu (%) ≤ 2,0
Warna larutan Tidak berwarna
N-deasetilasi (%) ≥ 70,0
Kelas viskositas (cps) :
- Rendah < 200
- Medium 200799
- Tinggi pelarut organik 8002000 (Sugita, 2009)
2.7. Polivinil Alkohol
Polivinil alkohol (PVA) dengan rumus kimia [(C
2H
4OH)
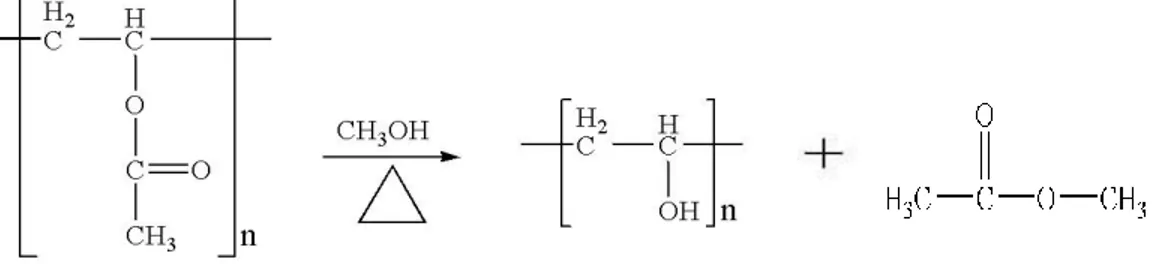
x] adalah polimer sintetik yang diproduksi oleh hidrolisis dari polivinil asetat seperti yang ditunjukkan pada Gambar 2.7. PVA bersifat nontoksik dan larut dalam air, sehingga banyak digunakan di berbagai bidang, antara lain bidang medis dan farmasi (Theresia, 2011) . Produk ini sangat sesuai untuk digunakan secara komersial dalam skala besar sebagai eksipien dalam berbagai produk farmasi seperti tablet salut, tetes mata, biofermentasi dan topikal. PVA bersifat kompatibel secara hayati dan sesuai untuk simulasi jaringan alami. Selain itu, PVA mempunyai permeabilitas oksigen yang baik, tidak bersifat imunogenik, dan memiliki sifat yang sangat baik dalam pembentukan film, pengemulsi dan dapat dilembabkan (Gessner dan Hawley, 1981). PVA berwarna putih, bentuk seperti serbuk, rasa hambar,tembus cahaya, tidak berbau dan larut dalam air. PVA salah satu polimer yang mempunyai sifat hidrofolik dan sebagai perekat. PVA dapat digunakan sebagai lapisan tipis yang sensitif (Gessner dan Hawley, 1981).
Polivinil alkohol (PVA) merupakan salah satu jenis bahan polimer yang
relatif murah dan tidak toksik. PVA dapat digunakan sebagai bahan dasar pembuatan
hidrogel sebagai matriks untuk mengekang obat dan kemudian obat tersebut
dilepaskan kembali (Zainuddin, 1994). Menurut Binh (2001), hidrogel yang
transparan, kuat secara mekanik dapat dihasilkan dari campuran PVA dan kitosan
yang diiradiasi sehingga dapat digunakan untuk antibakteri, mencegah infeksi dan menstimulasi repitelisasi.
Polivinil alkohol dapat membentuk film yang sangat baik, pengemulsi dan sifat perekat. PVA juga tahan terhadap minyak, lemak dan pelarut. Memiliki kekuatan tarik tinggi dan fleksibilitas , serta tinggi oksigen. Namun sifat ini tergantung pada kelembaban, dengan kata lain , dengan kelembaban yang lebih tinggi lebih banyak air diserap. Air , yang bertindak sebagai plasticizer, maka akan mengurangi kekuatan tarik , tetapi meningkatkan elongasi dan kekuatan sobek . PVA memiliki titik leleh 230°C dan 180-190°C ( 356-374 derajat Fahrenheit ) untuk nilai sepenuhnya dihidrolisis dan sebagian dihidrolisis masing-masing . Ini terurai dengan cepat di atas 200° C karena dapat menjalani pirolisis pada suhu tinggi (Fromageau et
al.,2003).Gambar 2.4. Reaksi pembentukan polivinil alkohol dari metanolisis polivinil asetat
2.8. Penanganan Limbah
Karena sifat polikationiknya, kitosan dapat dimanfaatkan sebagai agensia
penggumpal dalam penanganan limbah terutama limbah berprotein yang kemudian
dapat dimanfaatkan sebagai pakan ternak. Pada penanganan limbah cair, kitosan
dapat menyerap logam beracun seperti mercuri, timah, tembaga,pluranium dan
uranium dalam perairan dan untuk mengikat zat warna tekstil dalam air limbah (Krissetiana, 2004).
2.9. Logam Berat dan Pengaruhnya Pada Kesehatan
Logam berat merupakan polutan yang sangat toksik dan sangat berpengaruh terhadap kesehatan manusia, beberapa logam berat yang berpengaruh bagi kesehatan tersebut antara lain (Darwono, 1995):
2.9.1. Logam Krom (Cr)
Logam krom merupakan logam berat yang berbahaya dan beracun dengan konsentrasi yang tinggi akan membahayakan lingkungan. Sumber utama limbah krom adalag industri pelapisan logam, penyamakan kulit dan industri kimia.
Adapun sifat-sifat yang dimiliki oleh logam krom adalah (Darwono,1995):
1. Sifat kimia krom
a. Logam yang mengkilap dan titik cairnya tinggi yang banyak dipergunkan di indusri baja.
b. Dapat larut dalam asam kecuali nitrit, tidak larut dalam air
c. Pada tingkat konsentrasi 10 ppm dalam air, krom diperkirakan toksik bagi beberapa alga
2. Sifat fisik krom
a. Titik lebur 1903
oC pada tekanan 1 atm b. Titik didih 2642
oC pada 1 atm
c. Massa jenis 650 gr/cm
3Krom valensi tiga dalam jumlah tertentu merupakan unsur yang esensial bagi manusia dan hewan untuk mempertahankan proses metabolisme glukosa.
Pemasukan krom secara oral dalam jumlah berlebih dapat menimbulkan kerusakan hati dan ginjal (Darwono, 1995).
2.9.2. Logam Nikel (Ni)
Nikel merupakan salah satu Iogam berat yang sering dipergunakan di dalam proses industri. Biasanya logam nikel digunakan untuk proses pelapisan logam.
Limbah industri elektroplating yang tidak diolah dapat mencemari lingkungan.
Keracunan dapat terjadi lewat pernafasan atau terserap lewat kulit dan yang diserang adalah syaraf. Akumulasi Ni dalam tubuh dalam jumlah berlebih dapat menimbulkan kerusakan hati dan ginjal dan anemia atau gangguan kecerdasan pada keturunan (Darwono, 1995).
2.9.3. Logam Timbal (Pb)
Timbal dalam dosis tertentu dapat digunakan untuk campuran bahan bakar
bensin yang berfungsi untuk menaikan nilai oktan dan ini memnyebabkan
pencemaran Pb dalam lingkungan udara. Keracunan dapat tejadi lewat
pernafasanatau terserap lewat kulit dan yang diserang adalah syaraf. Akumulasi
Pb dalam tubuh dapat menyebabkan anemia atau gangguan kecerdasan pada
keturunan (Darwono, 1995).
2.9.4. Tembaga (Cu)
Air minuman seperti air buah-buahan yang telah masak pada pH lebih kecil dari 5,5 dapat melarutkan Cu bila ditempatkan dalam alat-alat yang mengandung logam Cu sehingga dapat memcemari minuman tersebut.
Keracunan tembaga dalam tubuh manusia dapat menyebabkan kerusakan hati, ginjal, penyakit kuning, radang paru-paru dan gangguan pernafasan yang berakibat kematian (Darwono, 1995).
2.9.5. Logam Kadmium (Cd)
Pada umumnya gelas-gelas berwarna dan logam-logam alat rumah tangga bila dilapisi dengan kadmium akan menjadi masalah karena lapisan kadmium ini dapat larut dalam makanan asam dan cuka.
Masuknya kadmim dalam batas yang tidak dizinkan sangat berbahaya karena dapat menyebabkan penyakit jantung, efek lain yaitu dapat meracuni pernafasan yang mengakibatkan kerusakan pada paru-paru, usus, hati, ginjal dan akhirnya dapat menyebabkan kematian. Pada umumnya keracunan kadmium dapat merusak semua sel tubuh (Darwono, 1995).
2.10. Kemampuan Kitosan Untuk Menyerap Logam
Kemampuan kitosan untuk mengikat logam dengan cara pengkhelat adalah
dihubungkan dengan kadar nitrogen yang tinggi pada rantai polimernya. Kitosan
mempunyai satu kumpulan amino linier bagi setiap unit glukosa. Kumpulan amino
ini mempunyai sepasang elektron yang dapat berkoordinat atau membentuk
ikatan -ikatan aktif dengan kation - kation logam. Unsur nitrogen pada setiap
monomer kitosan dikatakan sebagai gugus yang aktif berkoordinat dengan kation logam (Hutahahean, 2001).
Interaksi kitosan dengan ion logam terjadi karena proses pengkompleksan dimana penukaran ion, penyerapan dan pengkhelatan terjadi selama proses berlangsung. Ketiga proses tersebut tergantung dari ion logam masing - masing seperti penukaran ion logam masing - masing seperti penukaran ion pada logam Ca. Kitosan menunjukkan affinitas yang tinggi pada logam transisi golongan 3, begitu pula pada logam yang bukan golongan alkali dengan konsentrasi rendah (Muzzarelli, 1973).
Menurut Mc Kay (1987), kitosan mempunyai kemampuan untuk mengikat logam dan membentuk kompleks kitosan dengan logam. Contoh mekanismenya adalah sebagai berikut :
2R-NH
3+ Cu
2++ 2Cl
-(RNH
2)CuCl
2Pengaruh pH yang rendah akan mengurangi penyerapan ion logam kedalam kitosan karena bersaing dengan ion H
+untuk menyerap gugus amino bebas.
2.11. Adsorpsi
Adsorpsi adalah proses akumulasi substansi dipermukaan antara dua fasa yang
terjadi secara fisika dan atau kimia, atau proses terserapnya molekul-molekul pada
permukaan eksternal atau internal suatu padatan. Akumulasi yang terjadi dapat
berlangsung pada proses cair-cair, cair-padat dan padat-padat. Sedangkan
komponen-komponen yang diserap disebut adsorbat contoh bahan yang bisa
digunakan sebagai adsorbat antara lain : aluminium, karbon aktif, silika gel, dan lain-lain (Mc. Cabe, 1999)
Adsorpsi yang terjadi karena adanya gaya tarik dari permukaan adsorban dan energi kinetik molekul adsorbat, dapat berupa adsorpsi fisika, adsorpsi kimia dan adsorpsi isoterm. Pada adsorpsi fisika terjadi gaya van der Waals antara molekul adsorbat dan adsorban untuk berikatan. Hal ini terjadi akibat perbedaan energi gaya tarik elektrostatik oleh karena itu adsorpsi fisika merupakan reaksi reversibel. Sedangkan adsorpsi kimia adalah merupakan interaksi antara elektron-elektron pada permukaan adsorben dengan molekul-molekul adsorbat membentuk ikatan yang lebih kuat dibandingkan dengan adsorpsi fisika dan proses ini merupakan irreversibel (Bernasconi, 1995)
Proses adsorpsi berlangsung dalam tiga tahap yaitu : pergerakan molekul- molekul adsorbat menuju permukaan adsorben, penyebaran molekul-molekul adsorbat kedalam rongga-rongga adsorben dan penarikan molekul-molekul adsorbat oleh permukaan aktif membentuk ikatan yang berlangsung sangat cepat (Sorpsi) (Metcalf and Eddy, 1979).
Pada adsosrpi di dalam permukaan tetap konsentrasi fase fluida dan fase zat padat berubah menutut waktu dan menurut posisinya di dalam permukaan.
Kinetika adsorpsi dapat dianggap sebagai laju reaksi yang merupakan perbedaan waktu. Pengambilan logam (q) adalah adsorben dihitung dengan menggunakan persamaan :
Ci −Cf
q = V W ………. (2.1)
1000
dimana : V = Volume larutan (ml)
Ci = Konsenrasi awal logam (mg/l) Cf = Konsentrasi akhir logam (mg/l) W = Berat adsorben (gh)
q = Banyaknya logam yang teradsorpsi dalam adsorben (mg/l) Model isoterm Langmuir diterapkan dengan asumsi bahwa seluruh permukaan adsorben mempunyai afinitas yang relatif sama atau perbeda yang tidak signifikan terhadap logam. Persamaanya dalam bentuk umum adalah :
𝑞 = 𝑞𝑚𝑎𝑥
𝑏𝐶𝑓1+𝑏𝐶𝑓
……… (2.2)
dimana: q = jumlah adsorbat per unit berat adsorben (g)
Cf = konsentrasi kesetimbangan adsorbat dalam larutan (mg/l) q
max= konstanta kapasitas adsorsi langmui (mg/l)
b = konstanta energi adsorpsi Langmuir
Persamaan diatas dapat dituliskan dalam bentuk persamaan linier sebagai berikut:
Cf/q = 1/q
maxb + Cf/q
max…….………... (2.3)
Dengan memplotkan harga Cf terhadap Cf/q sehingga dapat ditentukan nilai konstata q
maxdan b untuk setiap kondisi percobaan.
Dalam persamaan isoterm Freundlich adsorpsi terjadi pada lebih dari satu
lapisan tunggal dengan permukaan yang homogen sehingga ikatan di masing-
masing tempat pelekatan berbeda. Persamaan empiris untuk isoterm Freundlich
dapat ditulis dalam bentuk :
x/m = K
fC
f1/n………... (2.4) dimana : x/m = Jumlah adsorbat yang teradsorpsi per unit berat
adsorben(mg/L)
Cf = Konsentrasi kesetimbangan adsorbat dalam larutan setelah adsorpsi
berlangsung(mg/L).
Kf,n = Konstanta empiris
Konstanta dalam isoterm Freunflich dapat ditentukan dengan memplotkan x/m terhadap Cf sehingga dihasilkan persamaan sebagai berikut:
log(x/m) = log K
f+ 1/n log C ………... (2.5)
2.12. Membran
Kata membran berasal dari bahasa latin membrana yang berarti potongan kain. Membran adalah suatu lapisan yang memisahkan dua fasa dimana perpindahan massanya dapat diatur dan hanya dapat dilewati oleh ion-ion tertentu.
Komponen aktif membran adalah suatu senyawa bermuatan atau netral yang mampu membentuk senyawa kompleks dengan ion-ion secara reversibel dan membawanya melalui membran organik. Senyawa seperti ini disebut ionofor atau pembawa ion (ion carrier). Membran disebut juga selaput dan bersifat semipermeabel yang memungkinkan lewatnya jenis molekul tertentu.
Membran dapat berupa padatan ataupun campuran dan berfungsi sebagai media
pemisah yang selektif berdasarkan perbedaan kofesien difusivitas, muatan listrik
maupun perbedaan kelarutan.
Membran banyak digunakan dalam proses pemisahan, pemurnian, dan pemekatan suatu larutan. Keunggulan pemisahan dengan menggunakan membran antar lain hemat energi, serta mampu memisahkan larutan - larutan yang peka terhadap suhu.
Membran kitosan lebih mudah diperoleh dibandingkan dengan membran kitin. Karena kelarutannya yang tinggi terhadap asam asetat 1% sehingga mudah untuk mendapatkan membrannya setelah pelarutnya diuapkan. Namun karena ketahanan sobeknya rendah untuk kegunanan tertentu sering ditambahkan polimer penguat seperti polivinil klorida (PVC), PVA, poliester dan N-metilon nilon.
Membran kitosan adalah membran pengkompleks pertama dari polimer alam dan telah digunakan untuk menarik unsur-unsur logam transisi dalam jumlah renik dari larutan garamnya.
2.12.1 Klasifikasi Membran
Banyak jenis membran yang kita kenal sehingga dapat diklasifikasikan memnjadi beberapa golangan. Misalnya ada membran berukuran tipis atau tebal, strukturnya bisa homogen atau heterogen, membran alami atau buatan, dan lain sebagainya. Secara makro membran merupakan pembatas antara dua fasa yang berjalan secara selektif sedangkan proses pemisahannya merupakan skala mikro yang meliputi difusi, pelarutan, osmosis, ultrafiltrasi, dialisis, pertukaran ion, dan elektrodialisa (Stephenson, 2000).
Membran dapat dibagi berdasarkan beberapa hal (Mulder, 1991) yaitu :
1. Jenis membran berdasarkan bahan dasar pembuatannya
a. Membran biologis, yaitu membran yang terdapat dalam sel mahluk hidup
b. Membran sintetis, dapat dibedakan menjadi membran organik (bahan penyusun utamanya adalah polimer atau cairan), membran anorganik (bahan penyusun utamanya logam atau non logam, kaca), atau campuran keduanya
(keramik).
2. Jenis membran Berdasarkan fungsi
Membran dapat diklasifikasikan dalam beberapa golongan yang secara tidak langsung berhubungan dengan ukuran diameter yang akan dipisahkan, membran mikrofiltrasi memiliki ukuran pori 0,02 - 10 μm dan tebal antara 10 - 150 μm.
Mikrofiltrasi digunakan pada berbagai macam aplikasi di Industri terutama untuk pemisahan partikel ukuran 0,1 μm dari larutannya, membran mikrofiltrasi dapat dibedakan dari membran reverse osmosis (RO) dan ultrafiltrasi (UL) berdasarkan ukuran partikel yang dapat dipisahkan. Membran ultrafiltrasi ukuran porinya berkisar antara 0,05 - 1 μm terutama untuk pemisahan partikel ukuran 0,001 μm dari larutannya. Sedangkan proses reverse osmosis menggunakan membran dengan ukuran pori 0,0001 - 0,001 μm. Membran reverse osmosis digunakan untuk memisahkan zat terlarut yang memiliki berat molekul rendah seperti garam anorganik atau molekul organik kecil seperti glukosa dan sukrosa dari larutannya. 3. Jenis membran berdasarkan prinsip pemisahan akibat ukuran pori
Berdasarkan ukuran porinya untuk proses pemisahan, membran dapat diklsasifikasikan sebagai berikut :
a. Membran berpori, prinsip pemisahannya bersadarkan ukuran partikel zat yang akan dipisahkan dengan ukuran pori-pori membran. Membran jenis ini biasa digunakan dalam proses pemisahan mikrofiltrasi dan ultrafiltrasi
b. Membran tak berpori, prinsip pemisahannya berdasarkan perbedaan kelarutan
dan kemampuan berdifusi suatu zat terhadap membran tersebut. Membran ini
digunakan untuk pemisahan gas dan pervaporasi
c. Membran cair (berbentuk emulsi), dimana di dalam membran terdapatzat pembawa yang menentukan selektivitas terhadap komponen tertentu yang akan dipisahkan. Pemisahan menggunakan membran cair sering dilakukan dengan teknik difusi berfasilitas dengan memilih jenis emulsi dan zat pembawa yang spesifik untuk zat tertentu. (Mulder, 1991)
2.12.2. Membran Polimer Alam
Polimer alam yang sudah banyak digunakan sebagai membran adalah turunan selulosa seperti selulosa asetat, selulosa triasetat, etil selulosa. Selulosa nitrat dan sejumpah polimer lain yang telah banyak dikenal dipasaran. Polimer dari turunan selulosa dapat digunakan sebagai membran ultrafiltrasi maupun mikrofiltrasi bahkan untuk membran revese osmosis,
Bahan dasar sari selulosa asetat adalah selulosa. Selulosa adalah merupakan polimer alam yang mempunyai struktur rantai yang linier seperti batang dan molekul infleksibel, bersifat hidrofilik namun tidak larut dalam air, hal ini disebabkan sifat kristalin dai ikatan hidrogen antara gugus hidroksilnya (Mulder, 1991).
2.13. Spekstroskopi Fourier Transform Infra Red (FTIR)
Spektroskopi adalah ilmu yang mempelajari segala sesuatu tentang interaksi antara
materi dengan radiasi elektromagnetik (REM). Interaksi yang terjadi dalam
spektroskopi inframerah ini merupakan inteaksi dengan REM melalui absorbsi
radiasi. Pancaran inframerah pada umumnya mengacu pada bagian spektrum
elektromagnetik yang terletak di antara daerah tampak dan glombang mikro. Molekul
menyerap radiasi elektromagnetik dengan panjang gelombang yang khusus.
Absorbansi cahaya ultraviolet mengakibatkan pindahnya sebuah electron ke orbital dengan energi yang lebih tinggi. Radiasi inframerah tidak cukup mengandung energi untuk melakukan eksitasi tersebut, absorbsinya hanya mengakibatkan membesarnya amplitude getaran atom-atom yang terikat satu sama lain (Julianti, 2012)
Konsep radiasi infra merah diajukan pertama kali dikemukakan oleh Sir William Herschel (1800) melalui percobaannya mendispersikan radiasi matahari dengan prisma. Ternyata pada daerah sesudah sinar merah menunjukkan adanya kenaikan temperatur tertinggi yang berarti pada daerah panjang gelombang radiasi tersebut banyak kalori (energi tinggi). Daerah spektrum tersebut selanjutnya disebut infrared. Spektroskopi inframerah ditujukan untuk maksud penentuan gugus-gugus fungsi molekul pada analisa kualitatif, disamping untuk tujuan analisis kuantitatif (Mulja, 1995).
Pengukuran pada spectrum inframerah dilakukan pada cahaya inframerah tengah (mid-infrared) yaitu pada panjang gelombang 2,5 – 50 µm atau bilangan gelombang 4000-200 cm
-1. Energy yang dihasilkan oleh radiasi ini akan enebakan vibrasi atau getaran pada molekul. Pita absorsi inframerah sangatkhas dan spesifik ntuk setiap tipe ikatan kimia atau gugus fungsi. Spektrum yang dihasilan berupa grafik yang menunjukkan persentase transmitan yang bervariasi pada setiap frekuensi radiasi inframerah (Dachriyanus, 2004).
Jumlah energy yang diserap juga bervariasi untuk setiap ikatan. Hal ini
disebabkan karena terjadinya perubahan momen ikatan suatu absorbsi. Ikatan non
polar (C-H atau C-C) pada umumnya akan memberikan absorbansi lemah, sedangkan
ikatan polar (C-O) akan terlihat sebagai absorbansi yang kuat. Spektroskopi FTIR
dapat digunakan untuk analisa kualitatif maupun kuantitatif. Analisa kualitatif
spektroskopi FTIR secara umum dipergunakan untuk identifikasi gugus-gugus fungsional yag terdapat dalam suatu senyawa yang dianalisa (Silverstein, 1986).
Analisa kuantitatif dari spektroskopi FTIR dapat dilakukan berdasarkan spectra inframerah yang dihasilkan, salah satu contohnya adalah penentuan derajat deasetilasi dari kitin dan kitosan menggunakan Persamaan Domszy dan Roberts (2) (Sugita,2009).
%D = 1 - [
𝐴1665𝐴3450
𝑥
11,33