UDAYANA UNIVERSITY PRESS
2015
SEMINAR NASIONAL
DAN TEKNOLOGI
Kuta, 29 - 30 Oktober 2015
LEMBAGA PENELITIAN DAN PENGABDIAN
KEPADA MASYARAKAT
xxvi | Kuta, 29-30 Oktober 2015
SOSIALISASI TEKNOLOGI TEPAT GUNA BIDANG TANAMAN PRODUKTIF DI DESA ANTAP KECAMATAN SELEMADEG KABUPATEN TABANAN
Ni Made Wiasti1, I Nyoman Dhana2, A.A Bags Wiraw3, Putu Sukardja ...1070
ANALISIS KERUSAKAN SAYURAN SEGAR DALAM STYROFOAM BOX DENGAN TEKNIK TOP ICE COOLING
Ida Ayu Rina Pratiwi Pudja1), Pande Ketut Diah Kencana ...1074
PEMANFAATAN UBI JALAR UNGU SEBAGAI BAHAN DASAR PRODUK PIA
I. G .N . Agung*), A.A.G.N. Jambe*) dan A.S. Duniaji ...1081
KESEHATAN DAN OBAT-OBATAN
TERAPI AUTO URINE PADA PENGOBATAN PENYAKIT MANUSIA (Studi Analisis Kimia dan Tinjauan Islam)
Panji Hidayat ...1089
PERHITUNGAN NILAI BESARAN FISIS FILM HASIL PHOTO SINAR-X MAMMOGRAFI JENIS LESI GANAS DAN LESI JINAK KANKER PAYUDARA
1Anak Agung Ngurah Gunawan,MT,2I Nyoman Widana ...1097
PANJANG SIKLUS ESTRUS DAN JUMLAH ANAK TIKUS BETINA (RATTUS RATTUS) YANG DIINJEKSI WHITE VITAMIN C DOSIS TINGGI DALAM JANGKA WAKTU LAMA Ni Wayan Sudatri1), Dwi Ariani Yulihastuti,2) Iriani Setyawati ...1101
KONSUMSI ENERGI DAN PROTEIN SERTA STATUS GIZI RUMAH TANGGA MISKIN PROVINSI BALI
Kadek Tresna Adhi1), Ni Wayan Arya Utami ...1106
APOPTOSIS SEL SPERMATOGENIK PADA TIKUS PUTIH (RATTUS NORVEGICUS) YANG TERPAPAR ASAP ROKOK SETELAH PEMBERIAN EKSTRAK BUAH JUWET (SYZYGIUM CUMINI)
A.A. Sg A. Sukmaningsih1, N Made Rai Suarni1, N.Wayan Sudatri1
Triwahyu Pangestiningsih2, Sitarina Widyarini ...1113
PENGARUH MAKANAN ATEROGENIK TERHADAP STRES OKSIDATIF DAN INFLAMASI PADA TIKUS WISTAR
Ni Wayan Bogoriani1), I Wayan Sudiarta ...1120
DETEKSI MOLEKULER KEBERADAANTOXOPLASMA GONDII
PADA SUMBER AIR DI BALI
Made Pasek Kardiwinata1*), Kadek Karang Agustina 2**), I Made Subrata ...1130
ULTIMATEANALISIS DAN IDENTIFIKASI KANDUNGAN EKSTRAK ETANOL KULIT BUAH MANGGIS (GARCINIA MANGOSTANA L.)
AKTIVITAS HIPOGLIKEMIA EKSTRAK DAUN KELOR (MORINGA OLEIFERA) MENURUNKAN EKSPRESI MALONDIALDEHIDA PADA SEL PULAU LANGERHAN PANKREAS TIKUS WISTAR DIABETES MELITUS
Ni Luh Eka Setiasih ...1139
PERILAKU KESEHATAN REPRODUKSI PADA REMAJA SEKAA TERUNA TERUNI DI DESA BENGKALA, KECAMATAN KUBUTAMBAHAN, BULELENG, BALI Ni Luh Putu Suariyani1), Desak Putu Yuli Kurniati1), , Rina Listyowati1),
Frieda Mangunsong2), Hadi Pratomo, Mitha Harahap ...1147
PERILAKU KESEHATAN REPRODUKSI PADA REMAJA SEKAA TERUNA TERUNI DI DESA BENGKALA, KECAMATAN KUBUTAMBAHAN, BULELENG, BALI Ni Luh Putu Suariyani1), Desak Putu Yuli Kurniati1), , Rina Listyowati1),
Frieda Mangunsong2), Hadi Pratomo, Mitha Harahap ...1152
AKTIVITAS ANTITUBERKULOSIS EKSTRAK ETANOL KULIT BATANG
CEMPAKA KUNING TERHADAPMYCOBACTERIUM TUBERCULOSIS MDR SECARAIN VITRO Ni Putu Ariantari1), Ida Bagus Nyoman Putra Dwija2)Made Ari Puji Astuti2) Ni Luh Rustini ...1157
PERBANDINGAN ISOLASI SEL MONONUKLEAR DARAH TEPI MENGGUNAKAN FICOLL 20% DAN FICOLL-PAQUE PLUS
Inna Narayani1, Rasmaya Niruri1, Nyoman Mantik Astawa ...1167
ZOONOSIS PARASIT POTENSIAL PADA ANJING DI BALI
Nyoman Sadra Dharmawan1), I Made Sukada2) I Made Damriyasa ...1170
PRODUKSI DAN KARAKTERISASI ANTIBODI MONOKLONAL ANTI-GLIKOPROTEIN VIRUS RABIES
Nyoman mantik Astawa1, Gusti Ayu Yuniati Kencana1, Ida Bagus Suardana ...1177
IDENTIFIKASI DAN UJI AKTIVITAS SENYAWA FLAVONOID DARI EKSTRAK DAUN TREMBESI (ALBIZIA SAMAN(JACQ.) MERR) SEBAGAI ANTIBAKTERIESCHERICHIA COLI Wiwik Susanah Rita1), I Kadek Pater Suteja2 I A Raka Astiti Asih2),
I Made Dira Swantara1) -, I Wayan Gede Gunawan ...1184
PENETAPAN KADAR ALFA MANGOSTIN DAN UJI AKTIVITAS ANTIBAKTERI S. aureus PADA EKSTRAK ETANOL KULIT BUAH MANGGIS (Garcinia mangostana L.)
Ketut Widyani Astuti1), Ni Putu Ayu Dewi Wijayanti ...1191
EFEKTIFITAS EKSTRAK TOKSIK SPONSHYRTIOS ERECTA SEBAGAI ANTIKANKER TERHADAP SEL HELA
I Made Dira Swantara1), Wieik Susanah Rita ...1197
PROTEKSI RADIASI MATAHARI TERHADAP RESIKO KANKER KULIT BAGI WISATAWAN YANG BEJEMUR DI PANTAI KUTA BALI
Kuta, 29-30 Oktober 2015 | 1177
PRODUKSI DAN KARAKTERISASI ANTIBODI MONOKLONAL
ANTI-GLIKOPROTEIN VIRUS RABIES
Nyoman mantik Astawa1, Gusti Ayu Yuniati Kencana1, Ida Bagus Suardana1
1).Laboratorium Virologi, Fakultas Kedokteran Hewan. Universitas Udayana Jln. PB Sudirman Denpasar
Bali Indonesia. Email:nyaomanmantikastawa@yahoo.com, Telpon: 031223791
ABSTRAK
Rabies merupakan penyakit zoonosis tertua di dunia dan sampai sekarang belum dapat diatasi secara tuntas. Produksi dan karakterisasi antibodi monoklonal (AbMo) anti-glikoprotein virus rabies diperlukan dalam pengembangan metode diagnosis yang akurat untuk virus rabies isolat Bali. Antibodi monoklonal diproduksi dengan cara fusi limfosit mencit yang kebal terhadap virus rabies dengan sel mieloma. Karakterisasi meliputi penentuan spesi sitasnya dengan uji enzym-linked immunosorbent assay (ELISA) dan Western Blotting (WB) dan kemampuannya untuk melacak virus pada otak anjing yang terinfeksi dengan uji imunoperoksidase dan indirect imuno ourescence. Hasil penelitian menunjukkan bahwa telah diproduksi sebanyak 8 klon sel hibridoma (CH9, AE7, BB5, EE9, DB9, AE11 dan AF6) yang menghasilkan antibodi monoklonal terhadap virus rabies. Tiga (BB5, AF6 dan AE11) dari 8 AbMo yang diproduksi bereaksi dengan protein 66 Kda (glikoprotein) virus rabies. Pada uji imunoperoksidase, ketiga AbMo anti-glikoprotein tersebut dapat melacak antigen virus rabies pada jaringan otak anjing terinfeksi yang sebelumnya telah di ksasi dengan formalin. Sementara itu, dengan uji indirect imuno ourescence antigen virus rabies terlacak pada jaringan segar. Hasil ini menunjukkan bahwa AbMo anti-glikoprotein virus rabies sangat berpotensi untuk dikembangkan sebagai reagen diagnosis yang akurat untuk virus rabies isolat bali.
Kata kunci: antibodi, monoklonal, virus, rabies, glikoprotein
1. PENDAHULUAN
Rabies merupakan penyakit zoonosis tertua di dunia dan sampai sekarang belum dapat diatasi secara tuntas. Penyakit ini diperkirakan membunuh sekitar 37 000- 86 000 manusia di sekitar 85 negara yang masih endemik rabies (WHO, 2010). Berbagai upaya telah dilakukan untuk memberantas penyakit rabies di dunia, tetapi sampai sekarang penyakit ini belum dapat diberantas secara tuntas. Upaya pemberantasan penyakit ini masih terus dilakukan seperti dengan vaksinasi, pengendalian populasi hewan penular rabies, dan tindakan lainnya. Namun, pada kenyataannya rabies masih tetap ada dan bahkan di beberapa negara berkembang, penyebarannya cenderung makin meluas.
Di Indonesia, penyakit rabies telah ada sejak 1889 dan penyebarannya cenderung meluas. Beberapa daerah yang dulunya bebas historis kini menjadi daerah tertular seperti Flores tahun 1997, Pulau Bali (2008), dan Pulau Nias (2010) yang kini menjadi daerah endemis. Selain itu, pada akhir tahun 2011 rabies muncul di Kabupaten Morotai, Provinsi Maluku Utara dan Pulau Babar, Kabupaten Maluku Barat Daya, Provinsi Maluku. Dengan demikian, wilayah Indonesia yang masih bebas rabies secara historis tinggal 5 yaitu, Papua, Papua Barat, Nusa Tenggara Barat, Kepulauan Riau dan Kepulauan Bangka Belitung. Di beberapa daerah rabies berhasil diberantas seperti Jawa Timur, Jawa Tengah dan DI Yogyakarta pada tahun 1997 serta DKI Jakarta yang dibebaskan pada tahun 2004, sehingga saat ini tercatat ada 9 (sembilan) provinsi di Indonesia yang berstatus bebas rabies (Dirjennakkeswan, 2012)
dan 2). Penentuan adanya virus rabies pada hewan terinfeksi sehingga tindakan yang perlu dilakukan dapat diputuskan dengan cepat.
Glikoprotein (G) yang merupakan protein perlekatan (atachment) berfungsi menginisiasi infeksi dengan cara melekatkan virus pada permukaan sel target. Jika glikoprotein virus rabies ini melekat pada permukaan sel target (umumnya sel syaraf), maka virus dapat menginfeksi sel tersebut (Kuzminaet al, 2013, Mori dan Marimoto, 2014). Keberadaan antibodi yang mengikat protein G (antibodi anti-glikoprotein virus rabies) dapat mencegah virus untuk melekat pada permukaan sel target sehingga dapat mencegah infeksi (mentralisasi virus). Karena itu, protein inilah yang mengandung antigen pemicu antibodi netralisasi virus yang dapat melindungi tubuh dari infeksi virus rabies. Banyak vaksin rabies yang dibuat hanya dengan hanya menggunakan protein G virus rabies.
Diagnosis rabies berbasis glikoprotein dapat dilakukan untuk melacak virus pada hewn terinfeksi menggunakan antibodi monoklonal anti-glikoprotein virus rabies seperti ourescene antibody technique
(FAT). Penggunaan antibodi monoklonal anti- glikopeotein diharapkan dapat meningkatkan spesivisitas dan sensitivitas uji, serta memudahkan penyediaan reagen diagnostik. Selain itu, tersedianya antibodi monoklonal terhadap protein G virus rabies dapat dipakai untuk memurnikan protein dari jaringan atau sel terinfeksi yang nantinya dapat dipakai sebagai antigen untuk melacak antibodi rabies pada hewan pasca vaksinasi. Hal ini juga akan memudahkan pemantauan respons imun hewan pasca vaksinasi yang sangat bermanfaat dalam mengevaluasi keberhasilan vaksinasi. Dalam paper ini dipaparkan produksi dan karakterisasi antibodi monoklonal rabies yang diharapkan nantinya dapat dipakai untuk mengembangkan metode diagnosis yang lebih akurat.
2. BAHAN DAN METODE
2.1. Pembuatan dan Pemurnian AbMO Anti-glikoprotein Virus Rabies
AbMo anti glikoprotein virus rabies dibuat dengan mengimunisasi mencit Balb/c dengan vaksin rabies yang tersedia secara komersial dan virus rabies isolate Bali. Skema imunisasi dilakukan sesuai dengan prosedur yang dijabarkan oleh Astawaet al, 2012. Dalam hal ini, mencit diimunisasi 4 kali dengan interval waktu 10 hari. Satu minggu setelah imunisasi terakhir, mencit diimunisai setiap hari selama 3 hari secara berturut-turut. Mencit kemudian siap dipakai untuk pembuatan sel hibridoma.
Hibridoma dibuat dengan cara memfusikan sel mieloma dengan limfosit asal limpa mencit yang telah kebal terhadap virus rabies. Sebanyak 108sel limfosit asal mencit yang kebal (menghasilkan antibodi) terhadap virus rabies difusikan dengan 2 x 107 sel mieloma (NS1) menggunakan polyethylene glycol (PEG)45 %. Sel hasil fusi kemudian disuspensikan dengan medium selektif DMEM-HAT (dulbecomodi ed
essential medium-hypxanthine amainopterin thymine) yang mengandung 106 sel per sumuran dalam sel-96 sumuran pada suhu 37oC. Media selektif membunuh sel mieloma, tetapi tidak membunuh sel hibridoma yang merupakan fusi sel myeloma dan limfosit. Tujuh hari setelah fusi, sel hibridoma dibiakan dalam media HTsampai muncul klon hibridoma yang menghasilkan antibodi terhadap antigen virus rabies. Skrining klon hibridoma yang menghasilkan AbMo terhadap glikoprotein virus rabies dilakukan dengan uji ELISA menggunakan virus rabies isolat Bali sebagai antigen. Hibridoma yang terbukti menghasilkan AbMo terhadap glikprotein kemudian diisolasi dan dipakai untuk menyiapkan AbMo dalam jumlah besar. AbMo stok ini dibuat dengan cara menumbuhkan hibridoma dalam media HT sampai terlihat tanda-tanda kematian sel. Cairan supernatannya kemudian ditampung, disimpan dalam -20oC dan dipakai sebagai AbMo stok. Selain itu, AbMo stok juga dibuat dengan penyuntikan sel hibridoma pada mencit Balb/c. Pertama, mencit jantan dewasa disuntik dengan dengan 0,5 ml pristane. Dua minggu setelah penyuntikan pristane, sebanyak 1 juta sel hibridoma penghasil antibodi disuntikkan ke dalam rongga abdomen mencit. Cairan ascites dipanen setelah perut mencit mengalami pembengkakan.
2.2. Penentuan Protein Virus Rabies yang Bereaksi dengan AbMo
Kuta, 29-30 Oktober 2015 | 1179 Tris-HCl 0,0625 M. pH. 6,0, gliserol 10%, bromophenolblue 0,001%) dan dianalisis dengan SDS-PAGE (sodium dedocylsulphate- polyacrylamidegel electropjoresis). Protein virus rabies yang telah dipisahkan dalam gel kemudian ditransfer ke membran nitroselulosa. Membran nitroselulosa dipotong kecil-kecil dan direaksikan dengan AbMo. Adanya ikatan antara AbMo dengan protein virus rabies divisualisasikan dengan penambahan anti-mouse IgG-alkaline phosphatase dan substrat BCIP/NBT.
2.3. Pelacakan Antigen Virus pada Otak Anjing Terinfeksi
Pelacakan antigen virus pada otak anjing yang terinfeksi dilakukan dengan uji imunohistokimia dan
uji imuno ouresen indirek. Untuk uji imunohistokimia, jaringan otak yang sebelumnya telah di ksasi
dengan formalin dan pemerosesan jaringan, dipotong setebal 4 mikron. Potongan jaringan tersebut kemudian dibuat di atas glas obyek yang telah dilapisi dengan poly-L-lysine dan jaringan selanjutnya diwarnai dengan teknik immunoperoxidase mengikuti teknik yang dijabarkan oleh Ohnishi et al (2005).
Pertama potongan jaringan di atas glas obyek dideparaf nisai 2 kali dalam xylol dan dibersihkan 2 kali
dengan ettanol absolut. Potongan jaringan kemudian dicuci 3 kali dengan PBS dan dicelupkan kedalam buffer sitrat yang mengandung 0.05% Tween-20 pada suhu 90oC selama 20 menit untuk membuka kembali
epitop yang tertutup akibat ksasi dengan formalin. Enzim peroksidase endogen kemudian diinaktifkan
dengan mencelupkan potongan jaringan ke dalam 3% H2O2 dalam PBS for 20 menit pada suhu ruangan. Setelah jaringan diblok dengan susu skim 5% dalam PBS, AbMo antiglikoprotein virus rabies ditambahkan ke atas potongan jaringan dan diinkubasikan selama 18 suhu 4oC dalam ruangan yang lembab. Setelah pencucian 3 kali dengan PBS.biotinylated goat anti-mouse IgG (Biocare, USA).Streptavidin-horse radish peroxidase (Biocare, USA). Sel yang terinfeksi virus rabies kemudian divisualisasikan dengan penambahan substat diazinobenzidine (DAB) (Biocare, USA).
Uji imuno ouresen indirek dilakukan dengan membuat preparat sentuh otak anjng terinfeksi pada objek gelas yang telah dilapisi dengan poly- L-lysin. Setelah di ksasi dengan aseton selama 15 menit,
sediaan jaringan sentuh kemudian dicuci dengan PBS, ditambahkan antibodi monoklonal anti-glikoprotein virus rabies, dan diikubasi selama 1 jam pada suhu kamar. Jaringan di atas gelas objek kemudian dicuci kembali seperti di atas dan digenangi kembali dengan antimouse IgG- ourescence Isotiocyanate(FITC) selama 30 menit. Setelah dicuci dengan PBS sebanyak 3 kali, jaringan ditutup dengan gliserol dan coverglass. Adanya sel terinfeksi virus rabies dilihat di bawah mikroskop ouresen.
3. HASIL
3.1. Sel Hibridoma Penghasil AbMo
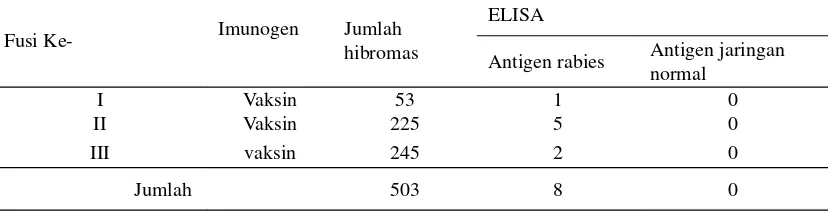
Dari 3 kali percobaan fusi diperoleh 503 klon sel hibridoma yang terdiri atas 53 klon dari fusi-1, 225 klon dari fusi ke-2 dan 245 dari fusi ke-3. Skrining dengan uji ELISA menunjukkan bahwa 8 klon sel hibroma yang menghasilkan antibodi monoklonal terhadap virus rabies yang terdiri atas, 1 klon sel hibridoma dari fusi pertama (klon CH9), 5 klon hibridoma dari fusi ke-2 (AE7, BB5, DB8, EE9 dan AG9), dan 2 klon dari fusi ke 3 (AF6, dan AC11) (Tabel 1) .
Tabel 1. Jumlah Hibridoma Penghasil Antibodi Monoklonal Anti-virus Rabies dari Percobaan Fusi
3.2. Karakteristik Antibodi Monoklonal
Tiga (BB5, AF6 dan AE11) dari 8 antibodi monoklonal tersebut bereaksi dengan protein 66 kDa (glikoprotein) seperti yang terlihat pada hasil uji Western blotting (Gambar 1). Penentuan isotipe menunjukkan bahwa ke 8 AbMo berturut-turut mepunyai isotipe berikut yaitu, 5 AbMo mempunyai isotipe IgG1 (AG9, EE9, AF6, BB5 dan AC11, dan 3 AbMo mempunyai Isotype IgG2a ( AE7, DB8 dan CH 9 ) (Tabel 2).
Gambar 1. Reaktivitas antibodi monoclonal terhadap protein virus rabies isolate Bali. Protein standar (1), AbMo CH9, AC7, AG9, DB8, EE9, BB5, AE11, AF6 (2-9).
Tabel 2. Karakteristik Antibodi Monoklonal Anti-virus Rabies
AbMo Isotipe Titer ELISA Protein reaktif IHK FAT
CH9 IgG2a 25 ---- ++ ±
AC7 IgG2a 26 --- ++ +
DB8 IgG2a 28 --- +++ ++
EE9 IgG1 25 --- + +
AG9 IgG1 25 --- + +
BB5 IgM 26 66 KDa ++ ++
AF6 IgG1 25 66 KDa ++ ++
AC11 IgG1 24 66 Kda ++ ++
Keteranagan : AbMo: antibodi monoklonal, ELISA : enzyme-linked immunosorbent assay, IHK: imunohistokimia, FAT: ourescence antibody technique
3.3. Reaktivitas AbMo dengan Antigen Virus Rabies pada Sel Otak Terinfeksi
Semua AbMo yang diproduksi dalam penelitian ini dapat melacak virus rabies dalam jaringan otak anjing yang terinfeksi. Dengan uji imunohistokimia 3 AbMo (BB5, AF6 dan AE11) yang mengenali
glikoprotein virus rabies dapat melacak antigen virus pada jaringan otak ajing terinfeksi dan telah di ksasi
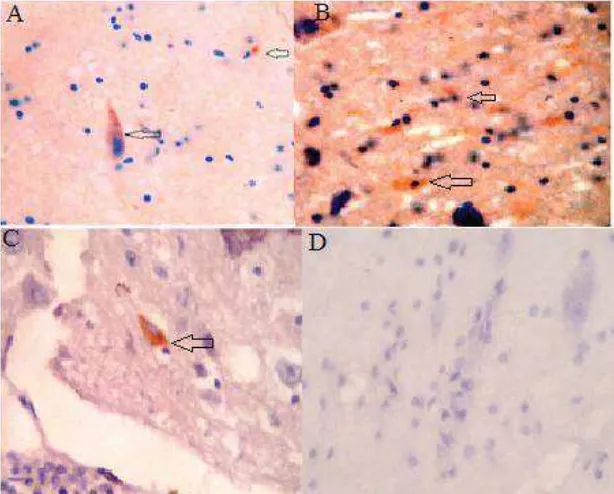
dengan formalin. Hasil potitif ditandai dengan adanya negri bodi pada sel neuron.. Sel yang terinfeksi ditandai dengan adanya warna coklat kemerahan pada sitoplasma dari sel otak yang meliputi sekitar 10-20 % sel otak. Virus rabies tidak terlacak pada jaringan otak anjing yang tidak terinfeksi (Gambar 2).
Jika dibandingkan dengan 5 AbMo lainnya, ketiga AbMo antiglikoprotein bereaksi lebih spesi k ditandai
Kuta, 29-30 Oktober 2015 | 1181 Gambar 2. Antigen virus Rabies yang terlacak dengan teknik imunohistokimia antibodi monoklonal pada sel otak anjing menggunakan antibodi monoklonal antiglikoprotein (A). AbMo AF (B). AbMo BB5 (C). AbMo. (D) . Jaringan normal
dengan AbMo , (Tanda panah): Sel terinfeksi virus rabies
Sementara itu, Uji imuno oureecen indirek digunakan untuk melacak virus rabies pada sediaan sentuh otak segar pada gelas obyek yang di ksai dengan aseton. Pewarnaan dengan AbMo BB5 , AF6 dan
AE11 menghasilkan gambaran yang serupa yaitu adanya titik berwarna hijau kekuningan yang berbendar pada sel yang terinfeksi tetapi tidak pada sel yang tidak terinfeksi. Ukuran titik berwarna yang ditemukan bervariasi dari yang kecil sampai yang relative besar (Gambar 3).
Gambar 3. Antigen virus rabies yang terlacak dengan antibodi monoklonal antiglikopotein pada sedian sentuh otak segar terinfeksi. (A). AbMo BB5, (B) AbMo AE11, (C). AbMo (AF6). (D).
4. PEMBAHASAN
Dalam penelitian ini sejumlah antibodi monoklonal yang mengenalai antigen virus rabies telah berhasil dibuat dan beberapa di antaranya berekasi dengan glikoprotein virus rabies isolate Bali. Adanya AbMo yang berekasi dengan glikoprotein virus rabies isolat bali dapat digunakan digunakaannya untuk melacak virus rabies pada jaringan otak anjing atau hewan lainnya yang terinfeksi virus. Glikoprotein virus rabies mempunyai berat molekul antara 64-68 kDA (Yonedaet al, 2008) dan protein yang dikenali oleh beberapa AbMo yang diproduksi dalam penelitian ini dengan berat molekul sekitar 66 Kda (Gambar 1) adalah glikoprotein virus rabies isolate bali. Penggunaan AbMo terhadap glikoprotein virus rabies diharapkan dapat meningkatkan spesivisitas dan sensitivitas uji diagnostik rabies. Hal ini dimungkinkan mengingat glikoprotein merupakan protein permukaan virus dan merupakan protein yang tersisa dalam negri bodi sel yang terinfeksi. Karena itu , pelacakan menggunakan AbMo glikoprotein diharapkan menghasilkan gambaran yang lebih jelas dibanding mengunakan AbMo terhadap protein lainnya.
Tersedianya AbMo terhadap glikpprotein virus rabies juga memungkinkan pemurnian glikoprotein virus tersebut dari jaringan atau sel terinfeksi virus rabies. Glikoprotein virus rabies yang murni dan berasal dari sel atau jaringan terinfeksi sangat berpotensi untuk dipakai sebagai antigen untuk melacak antibodi pada hewan. Glikoprotein murni yang berasal dari sel maupun jaringan otak terinfeksi merupakan glikoprotein alami yang bila digunakan dalam uji serologi sangat meungkin memberikan hasil yang lebih baik daripada protein lainnya. Glikoprotein merupakan protein virus yang sangat berperan dalam menginisiasi infeksi virus ke dalam sel. Infeksi virus rabies hanya terjadi jika glikoprotein virus tersebut berikatan dengan reseptornya pada permukaan sel inang (Consales dan Bolzan, 2007). Karena perannya dalam infeksi, glikoprotein penggunaannya sebagai antigen untuk melacak antibody pada hewan dapat mencermikan tingkat kekebalan hewan, terutama tingkat kekebalan pascavaksinasi. Ini dimungkinkan karena hanya antibodi yang berikatan dengan glikoprotein yang mempu menetralisasi virus.
5. SIMPULAN
Tiga dari delapan antibody monoclonal yang diproduksi dalam penelitian ini bereaksi dengan glikoprotein virus rabies (66 KDa). Dengan uji imunohistokimia, ketiga AbMo tersebut dapat melacak
antigen virus rabies pada jaringan otak yang telah di ksasi dengan formali. Dengan uji imuno ouresen
indirek, ketiga Abmo juga dapat melacak antigen virus rabies pada sedian sentuh dari jaringan otak segar anjing terinfeksi virus rabies.
Ucapan Terima Kasih
Penelitian ini di danai oleh didanai oleh Program Penelitian Desentralisasi Hibah Bersaing 2014/2015 dan karena itu penulis mengucapkan banyak terima kasih.
DAFTAR PUSTAKA
Astawa, N.M., Suardana, I.B.K. dan Kencana. G.A.Y. (2012). Production and use of monoclonal antibodies for detection of avian influenza virus infection in duck.Jurnal Veteriner 13 (11), pp. 284-292 Aurélie, A., Albertini, V., Eduard, B. E., Anna, F. dan Gaudin, Y. ( 2012). Molecular and Cellular Aspects
of Rhabdovirus Entry.Viruses 4, pp. 117-139
Baloul, L. dan Lafon, M. (2003). Apoptosis and rabies virus neuroinvasion.Biochemistry 85 (8) pp. 777-788.
Consales, C.A. dan Bolzan, V.L. (2007). Rabies review: immunopathology, clinical aspects and treatment. Jornal of Venomous and Animal Toxins including Tropical Disiease, 13 (1) p. 5-38
Dirjennakkeswan. (2012). Rakornas Rabies. Arahan Direktur Jenderal Peternakan dan Kesehatan Hewan. Pertemuan Koordinasi Pengendalian Rabies Nasional Bali, 28 Maret 2012
Kuta, 29-30 Oktober 2015 | 1183 Mori,T. dan Morimoto, K. (2004). Rabies virus glycoprotein variants display different patterns. Frontier in Neurology 7: Available at: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3877770/pdf/fnana-07-00047. pdf [Diakses 26 September 2015].
Ohnishi, K., Sakaguchi, M., Kaji, T., Akagawa, K., Taniyama, T., Kasai, M., Tsunetsugu-Yokota, Y., Oshima, M., Yamamoto, K., Takasuka, N., Hashimoto, S., Ato, M., Fujii, H., Takahashi, Y., Morikawa, S., Ishii, K., Sata, T., Takagi, H., Itamura, S., Odagiri, T., Miyamura, T., Kurane, I., Tashiro, M., Kurata, T., Yoshikura, H. dan Takemori, T. (2005). .Immunological detection of severe acute respiratory syndrome coronavirus by monoclonal antibodies. Japan Journal of Infectious Disease 58(2) pp.88-94.
World Health Organization (WHO). (2015).’ WHO Expert Consultation on Rabies’. Available at. http:// apps.who.int/iris/bitstream/10665/85346/1/9789240690943_eng.pdf [Diakses 26 September 2015] Yoneda, A., Tuciya, K., Takasima, Y., Arakawa, T., Tsuji, N., hayashi, Y. dan Matsumoto, Y. (2008).