Tabel Periodik Unsur Keperiodikan=keteraturan
Kemiripan di antara sifat unsur secara teratur & periodik jika unsur diatur menurut bobot atom (ba).
Perkembangan Tabel Periodik
Lavosier (1769)
Dalton
Bobot atom (ba): sifat yang digunakan untuk membedakan atom unsur dengan atom unsur lain.
Johan W. Dobereiner (1817)
Ada hub. antara sifat unsur dan ba nya.
Kelompok 3 unsur yang sifatnya mirip. Klor, brom, dan yod. Ba brom 80, sebagai rata-rata ba klor 35 dan ba yod 127.
J. A. K. Newland (1863-1865)
Menyusun unsur menurut kenaikan ba nya.
Ada pengulangan sifat setiap unsur ke-8.
Unsur 1, unsur ke-8, ke-15 dst merupakan awalan suatu kelompok (hukum oktaf).
Begeyer De Chancourtois (1863)
Penyusun unsur pertama periodik.
Fakta, unsur disusun menurut penyusunan ba, diperoleh secara periodik unsur sifatnya mirip.
Lothar Meyer (1869)
Hub lebih jelas antara sifat unsur dan ba.
Mengukur volume atom setiap unsur dalam keadaan padat.
Volume atom setiap unsur = ba unsur dibagi dengan kerapatannya.
Dimitri Mendeleev (1869)
Meyer menyusun daftar unsur berdasarkan sifat fisika.
Mendeleev : sifat kimia unsur.
Memperhitungkan unsur yang belum ditemukan.
Ada hub. antara sifat - ba unsur.
Menyusun daftar unsur berdasarkan kenaikan ba & unsur memiliki sifat hampir sama = 1 golongan.
Sifat unsur = fungsi berkala dari ba (daftar periodik Mendeleev).
Ada 2 penyimpangan: unsur telurium & yod, kalium & argon penempatannya tidak sesuai dengan kenaikan ba. Diperbaiki daftarnya menjadi urutan unsur dalam periodik berdasar nomor atom (na).
Sistem Periodik Panjang
Penyusunan berdasar kenaikan na unsur (aturan Aufbau & Hund).
Unsur dikelompokan : perioda & golongan. Horizontal = 7 perioda
Vertikal = gol A & B
Gol A: unsur representatif (unsur utama), 8 golongan: (I-8A).
- Konfigurasi elektron terluar ns1-2 np0-6 :
Pangkat = jumlah kulit elektron kulit terluar.
n = periode
jumlah elektron kulit terluar = golongan
Ex: 11Na = 1s2 2s2 2p6 3s1 = golongan 1A, periode 3
Golongan B: unsur transisi (8 golongan 1-8B).
konfigurasi elektron terluar (n-1)d1-10 ns1-2
•Jk jumlah elektron 11 = gol 1B, 12 = gol 2B. Untuk jumlah lainnya = penentuan gol A.
25Mn = 1S2 2S2 SP6 3S2 3P6 4S2 3d5 = 7B, periode 4 29Cu = 1S2 2S2 2P6 3S2 3P6 4S1 3d10 = 1B, periode 4
Blok s = unsur yang elektron terluar mengisi orbital s (1A & 2A).
Blok p = unsur yang elektron terluar mengisi orbital p (3A - 8A).
Blok d = unsur yang elektron terluar mengisi orbital d (1B & 8B).
Blok f = unsur yang elektron terluar mengisi orbital f (lantanida & aktinida).
Sifat Periodik Unsur a. Sifat Logam
unsur dibagi:
Logam = zat dapat menghantar listrik & panas.
Non logam = zat tidak dapat menghantar listrik.
Semi logam (metaloid) = zat bersifat logam sekaligus non logam.
1 golongan: ke atas letak unsur sifat logamnya makin berkurang.
1 perioda: ke kanan letak unsur sifat logamnya makin berkurang.
b. Jari-jari atom
1 perioda: ke kanan letak unsur, jari atom makin kecil (jumlah proton dalam inti & jumlah elektron dalam orbital bertambah, sehingga tarikan elektrostatik antara pertikel berlawanan muatannya bertambah).
Elektron yang berada pada kulit terluar akan tertarik ke inti sehingga ukuran atom bertambah kecil.
1 golongan makin ke bawah, jari atom semakin besar. (bertambahnya kulit elektron sesuai dengan bertambahnya bilangan kuantum utama).
c. Jari-jari Ion
Jika atom melepaskan elektron jari ionnya
< dibanding dengan jari-jari atom netralnya. Disebabkan tarikan inti lebih kuat dibanding tarikan inti pada atom netral.
Jika atom menangkap elektron , maka jari-jari ionnya > dibanding dengan jari-jari atom netralnya.
d. Energi ionisasi (Potensial Ionisasi)
Energi ionisasi: energi diperlukan untuk melepas 1 elektron dari suatu atom yang berdiri sendiri.
1 gol energi ionisasi makin berkurang jika na ber+ (semakin ber + nya kulit elektron, maka elektron kulit terluar berada semakin jauh dari inti). Menyebabkan gaya tarikan ke inti semakin kecil & elektron dengan mudah dapat dilepaskan.
1 periode, energi ionisasi cenderung bertambah dari kiri ke kanan.
Afinitas Elektron
Energi dilepaskan jika atom dalam bentuk gas menerima elektron dengan membentuk ion negatif.
1 gol: makin ke bawah letak suatu unsur afinitas elektron makin berkurang.
1 periode: makin ke kanan letak suatu unsur afinitas elektron makin bertambah. Disebabkan makin kecil jari atom, afinitas elektron makin besar.
Keelektronegatifan
Kemampuan atom menarik elektron. Berkaitan dengan energi ionisasi & afinitas elektron.
Sifat keelektronegatifan = energi ionisasi = afinitas elektron: makin kecil jari2 atom maka harga kelektronegatifan makin besar.
Sifat-sifat Magnetik
Atom menunjukan sifat magnetik jika ditempatkan dalam medan magnet.
Atom digolongkan 2 kelompok berdasar sifat magnetik:
Gejala diamagnetisme jika interaksi elektron yang berpasangan dengan medan magnetik tolak-menolak.
Paramagnetik: gejala yang disebabkan jika atom mempunyai elektron yang tidak berpasangan. Makin banyak elektron tidak berpasangan makin kuat gaya tarik medan magnetnya.
Tata Nama
Nama senyawa kimia memberikan informasi kualitatif & kuantitatif mengenai susunan senyawanya.
1. Bilangan Oksidasi
Banyaknya elektron atom terlibat pembentukan ikatan.
Muatan ion dalam senyawa.
Aturan penetapan biloks unsur sebagai komponen senyawa:
1. Biloks sebuah atom sebuah unsur bebas (tidak terikat) = 0
2. Jumlah biloks semua atom dalam sebuah molekul /satuan rumus=0
Untuk sebuah ion, jumlah biloks sama dengan muatan ion tsb, baik besar maupun tandanya, tanpa memperdulikan apakah ion tersebut terdiri dari atom tunggal atau terdiri dari 2 atom/lebih.
3. Logam alkali (1A) memiliki biloks +1 dan logam alkali tanah (2A) biloks = +2.
4. Biloks Hidrogen = +1, Fl = -1 5. Biloks Oksigen = -2
6. Senyawa biner dengan logam, unsur gol 7A, biloks = -1, 6A = -2, 5A = -3.
Bila ada 2 aturan berlawanan dengan yang lain, ikuti aturan yang muncul lebih dulu.
1. Senyawa S8 = sebuah atom dari unsur bebas , biloks = 0.
2. Al2O3
semua atom dalam sebuah satuan rumus = 0 (aturan 2). Biloks O = -2 (aturan 5). Jumlah biloks 3 atom O = -6. biloks 2 atom Al = +6. biloks 1 atom Al = +3.
3. Ion CrO4-2
jumlah biloks semua atom dalam ion -2. biloks 4 atom O = -8. Biloks Cr = +6.
4. Fe3O4
Jumlah biloks 4 atom O = -8. Biloks tiap atom Fe +1/3 = +22/
Penamaan Senyawa Biner
Senyawa yang dibentuk oleh 2 unsur. Penamaan Senyawa Biner Ionik
Dibentuk 1 unsur logam & 1 bukan logam, dituliskan nama logam tanpa modifikasi & diikuti dengan penamaan unsur bukan logam melalui pemberian akhiran ‘ida’.
KCL = Kalium klorida, MgF2 = Magnesium klorida, Kalium oksida = K2O.
Menentukan perbedaan rumus & nama senyawa, harus menentukan biloks unsur tersebut. 2 sistem penulisan yang umum digunakan:
1. Penamaan penulisan biloks menggunakan angka romawi.
2. Penamaan dengan sistem akhiran “o” untuk kation dengan biloks yang lebih rendah, akhiran ‘i’ untuk kation dengan biloks yang lebih tinggi.
Rumus
molekul Sistem stock
Sistem akhiran
CrCl2 Kromium (II) klorida Kromo klorida CrCl3 Kromium (III) klorida Kromi klorida Pb2O Plumbum (I) oksida Plumbo oksida PbO Plumbum (II) oksida Plumbi oksida
Penamaan Senyawa Biner Kovalen
Terdiri unsur non logam & unsur non logam. Pertama dituliskan unsur dengan biloks positif.
Ex: HCl bukan ClH.
Penamaan dilakukan berdasar pemberian awal menyatakan jumlah relatif tiap jenis atom dalam sebuah molekul .
Mono = 1 hepta = 7
di (bis) = 1 okta = 8
Tri (tris) = 3 nona = 9 Tetra (tetrakis) = 4 deka = 10 Penta (pentakis) = 5 undeka = 11 Heksa (heksakis) = 6 dodeka = 12
SO2 = belerang dioksida / berdasarkan sistem stock : belerang (IV) oksida
SO3 = belerang trioksida / berdasarkan sistem stock : belerang (VI) oksida
B2Br4 = diborontetrabromida , system stock = Boron (II) bromide
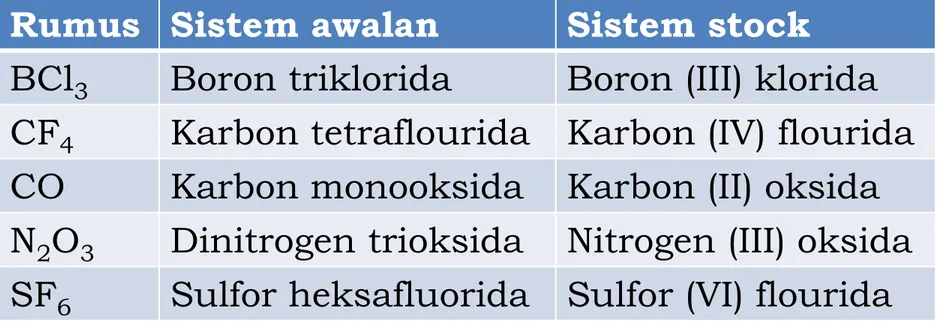
Tabel Penamaan Senyawa Biner Kovalen
Rumus Sistem awalan Sistem stock
BCl3 Boron triklorida Boron (III) klorida CF4 Karbon tetraflourida Karbon (IV) flourida CO Karbon monooksida Karbon (II) oksida N2O3 Dinitrogen trioksida Nitrogen (III) oksida SF6 Sulfor heksafluorida Sulfor (VI) flourida
Penamaan Asam Biner
Segolongan senyawa biner kovalen dalam keadaan tertentu dapat melepaskan ion hidrogen (H+) = senyawa asam.
Asam biner terbatas jumlahnya.
Penamaannya berdasarkan gabungan dari awalan ‘hidro’ dengan nama bukan logam yang diberi akhiran ‘at’.
Ex: HF = asam hidrofluorat (asam flourida) HBr = asam hidrobromat (asam bromat) H2S = asam hidrosulforat (asam sulfida)
Penamaan Senyawa Poliatomik
Senyawa mengandung ion poliatomik.
Ion poliatomik: 2 atom/lebih terikat secara bersama.
Jenis Anion poliatomik
>
kation poliatomik. Unsur dominan anion poliatomik: oksigen (O-2).
O2 terikat dengan atom non logam lain : oksoanion.
Sejumlah unsur membentuk deret oksoanion mengandung jumlah atom O berbeda.
Penamaanya sesuai dengan peningkatan biloks atom non logam yang mengikat atom O.
Peningkatan biloks
Hipo…it …it …at per…at Peningkatan jumlah atom O
Senyawa oksoanion mempunyai atom H berbeda & diberi nama berdasar jumlah atom H.
Ex: HPO4-2 = ion hidrogen fosfat. H2PO4- = ion dihidrogen fosfat.
1 Atom belerang mengantikan 1 atom O (ion sulfat =
1 atom S, 4 atom O-2, pada reaksi dapat terbentuk ion yang mempunyai 2 atom S, 3 atom O-2
)= penambahan awalan ‘+10’ pada penulisan nama belerang.
Sedikit asam biner yang penting.
Kebanyakan senyawa asam memiliki 3 unsur berbeda (senyawa terner) : terdiri atas H+, O-2, dan unsur bukan logam lainnya (asam okso) = hasil penggabungan ion H+ dan oksoanion.
Sistem penamaan asam okso = sistem penamaan deret oksoanion.
Penamaan senyawa-senyawa kompleks
Senyawa garam = hasil netralisasi asam + basa, unsur penyusunnya gabungan seny. asam + basa bereaksi & terdiri atas atom unsur berderet panjang. 1. Garam Asam
Penamaan garam dalam senyawanya masih mengandung atom H dari asam (garam terbentuk dari asam polivalen, hanya sebagian atom H asam digantikan oleh atom logam), diberi sisipan ‘hidrogen’:
NaHSO4 = Natrium hidrogen sulfat NaH2PO4 = Natrium dihidrogen fosfat
2. Garam basa
Penamaan garam dalam molekulnya masih mengandung gugus OH-, diberi sisipan hidroksi:
Ba (OH) Cl : barium hidroksiklorida
Al (OH)2 Cl : Aluminium dihidroksiklorida 3. Garam Rangkap
Penamaan garam mengandung 2 jenis anion/kation.
K2SO4. Al2 (SO4)3. 24 H2O : Kalium Aluminium Sulfat hidrat
4. Garam Kompleks
Penamaan senyawa kovalen koordinasi berdasarkan beberapa aturan tertentu:
a. Penamaan Ligan
jika menjadi penyusun senyawa kompleks koordinasi, ligan memiliki nama khusus
NH3 : amina H2O : aqua No : nitrosil CO : karbonil
Ligan anionic dituliskan dalam nama umum yang biasa dipakai tapi dengan pemberian akhiran ‘O’:
CH3COO- : aseto OH- : hidrokso CN- : siano H- : hidrido
F- : fluoro NO
2- : nitro O2- : okso ONO- : nitrito O2-2 : perokso
b. Penamaan Radikal
Radikal organik meskipun dianggap sebagai anion di dalam penentuan bilangan oksidasi normal suatu logam, tetap menggunakan nama umum radikalnya,: CH3 : metil
C6H5 : fenil
Ligan yang saling berkaitan memiliki nama umum penggabungan dengan sistem penulisan digabungkan (tanpa jarak) antar nama keduanya.
Contoh penamaan senyawa kompleks koordinasi, dalam penulisan rumus, atom logam dituliskan dahulu baru diikuti oleh ligan.
[Cr (H2O)4 Cl2] Cl : tetraquadiklorokromium (III) klorida
[Ag (NH3)2 Cl] : diaminaargentoklorida [Cu (NH3)4] SO4 : tetraminakuprisulfat K4[Fe (CN)6 : kaliumheksasianoferat