5 BAB II
TINJAUAN PUSTAKA 2.1Uraian Bahan
2.1.1 Metampiron
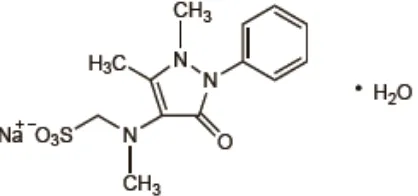
Menurut Ditjen, BKAK., (2014), uraian tentang metampiron sebagai berikut: Rumus struktur:
Gambar 2.1 Struktur Metampiron
Nama Kimia : Natrium 2,3-dimetil-1-fenil-5-pirazolon-4 metil amino metana sulfonat
Rumus Molekul : C13H16N3NaO4S.H2O Berat Molekul : 351,37
Pemerian : serbuk hablur, putih atau putih kekuningan
Kelarutan : Larut dalam 1,5 bagian air, 30 bagian etanol, tidak larut dalam eter, CHCl3 dan Aseton
Metampiron adalah derivat sulfonat dari aminofenazon yang larut dalam air. Derivat aminofenazon berkhasiat analgetis, antipiretis,dan antiradang. Obat ini dapat secara mendadak dan tak terduga menimbulkan kelainan darah yang adakalanya fatal (Tan dan Rahardja, 2013).
6
penggunaannya dianggap dibenarkan hanya dalam rasa sakit berat atau demam di mana tidak ada alternatif yang tersedia atau sesuai. metampiron telah diberikan secara oral dalam dosis 0,5-4 g sehari dalam dosis terbagi. Hal ini juga telah diberikan secara intramuscular atau intravena injeksi dan rektal sebagai supositoria (Sweetman, 2009).
2.1.2 Fenilbutazon
Menurut Ditjen, BKAK., (2014), uraian tentang fenilbutazon sebagai berikut: Rumus Struktur:
Gambar 2.2 Struktur Fenilbutazon Nama Kimia : 4-Butil-1,2-difenil-3,5-pirazolidinadion Rumus Molekul : C19H20N2O2
Berat Molekul : 308,38
Pemerian : Serbuk hablur, putih atau agak putih; tidak berbau
Kelarutan : Sangat sukar larut dalam air; mudah larut dalam aseton dan dalam eter; larut dalam etanol
7
Beberapa jenis antiinflamasi antara lain fenilbutazon, sulfinpirazon, oksifenbutazon dan asam mefenamat, dapat menggeser antikoagulan oral dari ikatannya dengan albumin plasma. Penggeseran ini menyebabkan peningkatan sementara kadar antikoagulan oral bebas dalam darah; biotransformasi dan eksresi juga meningkat sehingga masa paruh diperpendek, selanjutnya akan tercapai taraf-mantap baru dengan nilai kadar antikoagulan bebas di dalam darah dan masa protrombin seperti belum terjadi interaksi obat. Meskipun hanya bersifat sementara, peningkatan kadar antikoagulan oral bebas dalam darah ini dapat menyebabkan perdarahan berat (Dewoto, 2011).
8 2.2 Spektrofotometri
Spektrofotometer adalah alat untuk mengukur transmitan atau serapan suatu sampel sebagai fungsi panjang gelombang. Spektrofotometer merupakan penggabungan dari dua fungsi alat yang terdiri dari spektrometer yang menghasilkan sinar dari spektrum dengan panjang gelombang tertentu dan fotometer sebagai alat pengukur intensitas cahaya yang ditransmisikan atau yang diabsorpsi. Ketika cahaya (monokromatik atau heterogen) mengenai medium homogen, suatu bagian dari cahaya yang ada akan dipantulkan, sebagian diserap medium, dan sisanya ditransmisikan atau diteruskan (Day dan Underwood, 1998).
Jika suatu molekul bergerak dari suatu tingkat energi ke tingkat energi yang lebih rendah maka beberapa energi akan dilepaskan. Energi ini dapat hilang sebagai radiasi dan dapat dikatakan telah terjasi emisi radiasi. Jika suatu molekul dikenai suatu radiasi elektromagnetik pada frekuensi yang sesuai sehingga energi molekul tersebut ditingkatkan ke level yang lebih tinggi, maka terjadi peristiwa penyerapan (absorpsi) energi oleh molekul (Rohman, 2007).
9 2.2.1. Hukum Lambert-Beer
Menurut Hukum Lambert, serapan berbanding lurus terhadap ketebalan sel yang disinari. Sedangkan menurut Beer, serapan berbanding lurus dengan konsentrasi. Kedua pernyataan ini dapat dijadikan satu dalam Hukum Lambert-Beer, sehingga diperoleh bahwa serapan berbanding lurus terhadap konsentrasi dan ketebalan sel, hukum Lambert-Beer menyatakan bahwa intensitas yang diteruskan oleh larutan zat penyerap berbanding lurus dengan tebal dan konsentrasi larutan (Rohman, 2007). Hukum Lambert-Beer umumnya dikenal dengan persamaan sebagai berikut:
A = a.b.c Dimana: A = absorbansi
a = absorptivitas b = tebal kuvet (cm) c = konsentrasi
Absorptivitas (a) merupakan suatu konstanta yang tidak tergantung pada konsentrasi, tebal kuvet dan intensitas radiasi yang mengenai larutan sampel. Absorptivitas tergantung pada suhu, pelarut, struktur molekul dan panjang gelombang radiasi (Rohman, 2007).
2.2.2. Komponen Spektrofotometer
Menurut Day dan Underwood (1998), unsur - unsur terpenting suatu spektrofotometer adalah sebagai berikut:
10
lampu tungsten digunakan untuk daerah visibel pada panjang gelombang antara 350- 900 nm.
2. Monokromotor: digunakan untuk memperoleh sumber sinar yang monokromatis. Alatnya berupa prisma untuk mengarahkan sinar monokromatis yang diinginkan dari hasil penguraian.
3. Kuvet (sel): digunakan sebagai wadah sampel untuk menaruh cairan ke dalam berkas cahaya spektrofotometer. Kuvet itu haruslah meneruskan energi radiasi dalam daerah spektrum yang diinginkan. Pada pengukuran di daerah sinar tampak, kuvet dapat digunakan, tetapi untuk pengukuran pada daerah ultraviolet kita harus menggunakan sel kuarsa karena gelas tidak tembus cahaya pada daerah ini. Kuvet tampak dan ultraviolet yang khas mempunyai ketebalan 1 cm.
4. Detektor: Peranan detektor penerima adalah memberikan respon terhadap cahaya pada berbagai panjang gelombang.
2.3. Spektrofotometri Derivatif
Konsep derivatif telah diperkenalkan pertama kali pada tahun 1950, dimana terlihat memberikan banyak keuntungan. Aplikasi utama spektrofotometri derivatif ultraviolet–visibel adalah untuk identifikasi kualitatif dan analisis senyawa dalam sampel. Metode spektrofotometri derivatif sangat cocok untuk analisis pita absorpsi yang overlapping atau tumpang tindih (Owen, 1995).
11
pada kemiringan. Spektrum derivatif pertama diperoleh dengan memplot spectrum yang kemiringannya nol pada puncak maksimum dan kemiringannya maksimum pada sekitar separuh dari tinggi puncak. Pada spectrum derivatif kedua, kemiringan segmen 2 nm yang berdekatan dibandingkan dan ini memberikan titik-titik bagian kurva maksimum pada spectrum tersebut (Watson, 2009).
Spektrofotometri derivatif berkaitan dengan transformasi spektrum serapan menjadi spektrum derivatif pertama, kedua atau spektrum derivatif dengan order yang lebih tinggi. Spektrum derivat pertama dibuat dengan memplotkan dA / dλ
dengan panjang gelombang, derivat kedua dibuat dengan memplotkan d2A / d λ2 dengan panjang gelombang dan seterusnya (Ditjen, POM., 1995).
12 c = Konsentrasi Sampel
Untuk komponen kuantifikasi tunggal pemilihan gelombang untuk spektrum derivatif ini tidak sederhana seperti untuk spektrum absorbansi karena ada baik puncak positif dan puncak negatif. Untuk orde mantap yang derivatif ada puncaknya maksimum atau minimum pada saat yang sama panjang gelombang maksimum sebagai spektrum absorbansi (Owen,1995).
Ada empat aplikasi spektrofotometri derivatif yang sering digunakan dalam analisa kuantitatif, antara lain metode peak to zero (zero crossing), metode peak to peak, metode peak to tangent dan metode peak to peak ratio (Talsky, 1994).
Panjang gelombang zero crossing adalah panjang gelombang dimana senyawa tersebut mempunyai serapan nol dan menjadi panjang gelombang analisis untuk zat lain dalam campurannya. Metode zero crossing memisahkan campuran dari spektrum derivatifnya pada saat panjang gelombang komponen pertama tidak ada sinyal. Pengukuran pada zero crossing tiap komponen dalam campuran merupakan fungsi tunggal konsentrasi dari yang lainnya (Nurhidayati, 2007).
Panjang gelombang serapan maksimum suatu senyawa pada spektrum normal akan menjadi panjang gelombang zero crossing pada spektrum derivatif pertama, panjang gelombang tersebut tidak mempunyai serapan atau dA / dλ = 0 (Nurhidayati, 2007).
13
paling besar, serapannya lebih stabil sehingga kesalahan analisis dapat diperkecil (Nurhidayati, 2007).
2.4. Validasi Metode Analisis
Validasi metode analisis adalah suatu tindakan penilaian terhadap parameter tertentu pada prosedur penetapan yang dipakai, untuk membuktikan bahwa parameter tersebut memenuhi persyaratan untuk penggunaannya (Harmita, 2004).
Proses validasi dimulai dengan perangkat lunak yang tervalidasi dan system yang terjamin, lalu metode yang divalidasi menggunakan system yang terjamin dikembangkan. Akhirnya, validasi total diperoleh dengan melakukan kesesuaian system. Masing-masing tahap dalam proses validasi ini merupakan suatu proses yang secara keseluruhan bertujuan untuk mencapai kesuksesan validasi (Rohman, 2007).
Pada tahap validasi, suatu usaha harus dikerahkan untuk mendemonstrasikan bahwa metode bekerja dengan sampel yang mengandung analit tertentu, pada suatu kosentrasi yang diharapkan dalam suatu matriks sampel, dengan tingkat presisi dan akurasi yang tinggi. Validasi metode yang sempurna hanya dapat terjadi jika metode tersebut sudah dikembangkan dan dioptimasi (Rohman, 2007).
2.4.1. Akurasi
Kecermatan adalah ukuran yang menunjukkan derajat kedekatan hasil analis
dengan kadar analit yang sebenarnya. Kecermatan dinyatakan sebagai persen
perolehan kembali (recovery) analit yang ditambahkan. Kecermatan hasil analis
sangat tergantung kepada sebaran galat sistematik di dalam keseluruhan tahapan
analisis. Oleh karena itu untuk mencapai kecermatan yang tinggi hanya dapat
14
peralatan yang telah dikalibrasi, menggunakan pereaksi dan pelarut yang baik,
pengontrolan suhu, dan pelaksanaannya yang cermat, taat asas sesuai prosedur
(Harmita, 2004).
Untuk mendokumentasikan akurasi dilakukan pengumpulan data dari 9 kali
penetapan kadar dengan 3 konsentrasi yang berbeda (missal 3 konsentrasi dengan 3
kali replikasi). Data harus dilaporkan sebagai persentase perolehan kembali
(Rohman, 2007).
Menurut Harmita (2004), Perhitungan perolehan kembali dapat juga ditetapkan dengan rumus sebagai berikut:
% Perolehan kembali = CFC−CA
A
∗ x 100 %
Keterangan:
CF = konsentrasi total sampel yang diperoleh dari pengukuran
CA = konsentrasi sampel sebenarnya
C*A = konsentrasi analit yang ditambahkan
2.4.2. Presisi
Presisi merupakan ukuran keterulangan metode analisis dan biasanya
diekspresikan sebagai simpangan baku relatif dari sejumlah sampel yang berbeda
signifikan secara statistik. Dokumentasi presisi seharusnya mencakup simpangan
baku, simpangan baku relative (RSD) atau koefisien variasi (CV), dan kisaran
kepercayaan (Rohman, 2007).
Keseksamaan adalah ukuran yang menunjukkan derajat kesesuaian antara
hasil uji individual, diukur melalui penyebaran hasil individual dari rata-rata jika
15
campuran yang homogen (Harmita, 2004).
2.4.3. Batas Deteksi (Limit Of Detection, LOD)
Batas deteksi didefinisikan sebagai konsentrasi analit terendah dalam sampel
yang masih dapat dideteksi, meskipun tidak selalu dapat dikuantifikasi. LOD
merupakan batas uji yang secara spesifik menyatakan apakah analit di atas atau di
bawah nilai tertentu. Defenisi batas deteksi yang paling umum digunakan dalam
kimia analisis adalah bahwa batas deteksi merupakan kadar analit yang memberikan
respon blanko (Rohman, 2007).
Penentuan batas deteksi suatu metode berbeda-beda tergantung pada metode
analisis itu menggunakan instrumen atau tidak. Pada analisis yang tidak
menggunakan instrumen batas tersebut ditentukan dengan mendeteksi analit dalam
sampel pada pengenceran bertingkat. Pada analisis instrumen batas deteksi dapat
dihitung dengan mengukur respon blangko beberapa kali lalu dihitung simpangan
baku respon blangko (Harmita, 2004).
2.4.4 Batas Kuantitasi (Limit Of Quantification, LOQ)