TINJAUAN PUSTAKA
Destilat Asam Lemak Minyak Sawit (DALMS)
Destilat asam lemak minyak sawit (DALMS) atau Palm Fatty Acid Destilate (PFAD) merupakan produk samping proses pemurnian minyak sawit dalam industri minyak goreng. Tahapan proses pemurnian minyak adalah pemisahan gum (degumming), pemisahan asam lemak bebas (deasifikasi/ netralisasi), pemucatan (bleaching) dan penghilangan bau (deodorasi).
Proses degumming perlu dilakukan sebelum proses netralisasi, sebab sabun yang terbentuk dari hasil reaksi antara asam lemak bebas dan alkali pada proses netralisasi akan menyerap gum (getah dan lendir) sehingga menghambat proses pemisahan sabun dari minyak (Ketaren 2005).
Deasifikasi atau netralisasi merupakan proses pemisahan asam lemak bebas dalam minyak, yang dapat dilakukan dengan metode kimia, fisik, biologis, reesterifikasi, ekstraksi pelarut, supercritical fluid extraction dan teknologi membran. Deasifikasi secara kimia dilakukan dengan cara mereaksikan asam lemak bebas dengan basa sehingga membentuk sabun. Basa yang biasa digunakan adalah NaOH, proses ini dikenal dengan istilah caustic deacidification (Bhosle 2004).
Bleaching merupakan salah satu tahapan proses pemurnian minyak yang bertujuan untuk menghilangkan zat warna, dilakukan dengan mencampur minyak dengan sejumlah kecil adsorben seperti tanah serap (fuller earth), lempung aktif (activated clay) dan arang aktif (Ketaren 2005).
Deodorasi dilakukan untuk memisahkan rasa dan bau dari minyak, prinsip dari proses deodorasi yaitu destilasi minyak oleh uap dalam keadaan hampa udara. Pada suhu tinggi, komponen-komponen yang menimbulkan bau mudah diuapkan kemudian melalui aliran uap komponen tersebut dipisahkan dari minyak. Komponen-komponen yang dapat menimbulkan rasa dan bau dari minyak antara lain asam lemak bebas, aldehida, keton, hidrokarbon dan minyak essensia (Djadmiko dan Widjaja 1985). Deodorisasi dilakukan dengan cara menguapkan komponen-komponen volatil, proses ini dilakukan secara kontinu pada suhu 245-265oC dalam keadaan vakum 1-2 tor (Siswanto 2000). Pada proses deodorasi ini destilat asam lemak minyak sawit dihasilkan. Pemisahan asam lemak bebas
penting dilakukan di industri minyak goreng karena kandungan asam lemak bebas yang tinggi pada minyak akan menyebabkan minyak mudah teroksidasi dan menyebabkan rendahnya titik asap. Titik asap yang rendah mengakibatkan minyak tidak dapat dipergunakan pada suhu tinggi, sehingga fungsi minyak sebagai media penghantar panas tidak tercapai.
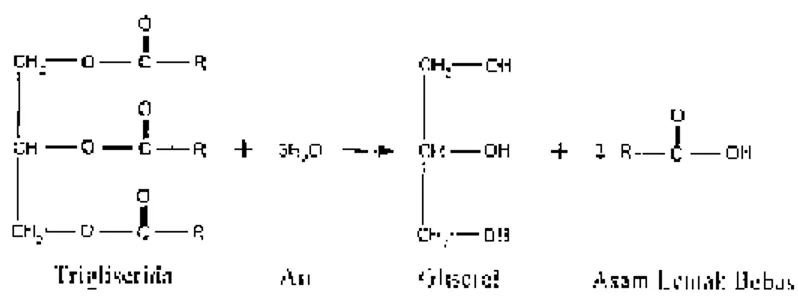
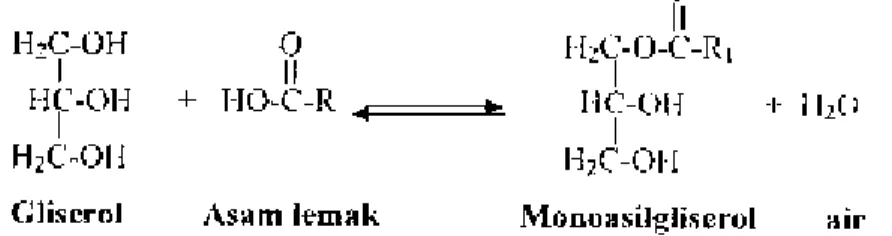
Menurut Gapor et al. (1992) pada produksi minyak kelapa sawit akan menghasilkan produk samping destilat asam lemak sawit sebesar 3-3,7 % w/w dari minyak sawit kasar. Pembentukan asam lemak bebas pada minyak sawit kasar merupakan suatu kerusakan yang disebabkan oleh reaksi hidrolisis, mekanisme reaksi hidrolisis dapat dilihat pada Gambar 1.
Pada saat ini sebagian besar DALMS baru dimanfaatkan untuk bahan pembuatan sabun yang bernilai ekonomi rendah. Produksi minyak sawit kasar Indonesia pada tahun 2005-2010a dan perkiraan jumlah DALMS yang dihasilkan dapat dilihat pada Tabel 1.
Gambar 1 Mekanisme reaksi hidrolisis (Ketaren 2005)
Tabel 1 Produksi minyak sawit kasar dan DALMS tahun 2005-2010a Tahuna Total produksi minyak sawit
kasar (ton)a Perkiraan jumlah DALMS (ton)c 2005 2006 2007b 2008b 2009b 2010b 19.300.000 21.700.000 23.300.000 25.300.000 27.500.000 29.700.000 579.000 651.000 699.000 759.000 825.000 891.000 a Sumber : Ditjen Perkebunan (2007)
b Perkiraan oleh Ditjen Perkebunan
DALMS mengandung asam lemak bebas sekitar 80% terutama dari jenis asam lemak palmitat dan oleat, 14.5% asilgliserol (campuran mono, di, dan triasilgliserol), 0.4% sterol (β-sitosterol, stigmasterol dan kolesterol) serta 1.5% hidrokarbon (squalen). Asam lemak bebas merupakan salah satu faktor penentu mutu minyak sawit dan juga merupakan salah satu indikator dalam kerusakan minyak. Asam lemak bebas dalam minyak tidak dikehendaki karena degradasi asam lemak bebas tersebut menghasilkan rasa dan bau yang tidak disukai, oleh karena itu dalam pengolahan minyak diupayakan kandungan asam lemak bebas serendah mungkin (Ketaren 2005).
Asam lemak bebas yang terdapat pada DALMS dapat diolah lebih lanjut melalui reaksi esterifikasi dengan gliserol dan katalis lipase untuk menghasilkan monoasilgliserol dan diasilgliserol, selanjutnya monoasilgliserol dan diasilgliserol dapat dipergunakan sebagai emulsifier pada produk pangan atau non pangan seperti kosmetik dan obat-obatan (Elizabeth dan Boyle 1997). Komposisi asam lemak DALMS hasil penelitian terdahulu dapat dilihat pada Tabel 2.
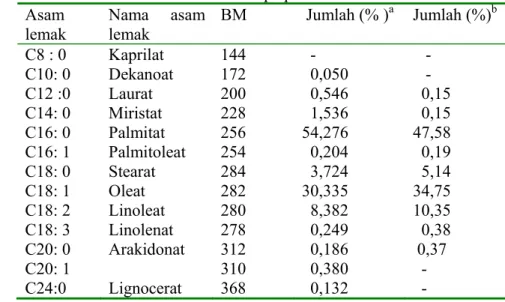
Tabel 2 Komposisi asam lemak DALMS yang digunakan sebagai substrat esterifikasi enzimatis dari beberapa peneliti
Asam
lemak Nama asam lemak BM Jumlah (% )
a Jumlah (%)b C8 : 0 C10: 0 C12 :0 C14: 0 C16: 0 C16: 1 C18: 0 C18: 1 C18: 2 C18: 3 C20: 0 C20: 1 C24:0 Kaprilat Dekanoat Laurat Miristat Palmitat Palmitoleat Stearat Oleat Linoleat Linolenat Arakidonat Lignocerat 144 172 200 228 256 254 284 282 280 278 312 310 368 - 0,050 0,546 1,536 54,276 0,204 3,724 30,335 8,382 0,249 0,186 0,380 0,132 - - 0,15 0,15 47,58 0,19 5,14 34,75 10,35 0,38 0,37 - - a Sumber : Christina (2000) b Sumber :Atmaja (2000)
Enzim Lipase
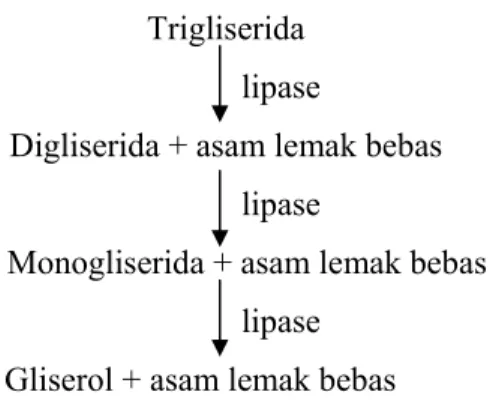
Lipase (EC 3.1.1.3; triasil gliserol hidrolase) merupakan enzim yang sangat fleksibel karena lipase tidak hanya dapat mengkatalisis reaksi hidrolisis trigliserida menjadi asam lemak bebas dan gliserol seperti dapat dilihat pada Gambar 2 tetapi juga dapat mengkatalisis reaksi transesterifikasi maupun esterifikasi. Substrat alami enzim lipase adalah trigliserida dari asam lemak rantai panjang. Trigliserida tersebut tidak larut di dalam air dan enzim lipase dikarakterisasi dengan melihat kemampuannya dalam mengkatalisis hidrolisis ikatan ester pada interfase. Kemampuan menghidrolisis ester asam lemak rantai panjang yang tidak larut membedakan lipase dari esterase yang selama ini sering dikacaukan karena daya kerjanya yang sangat mirip yaitu mengkatalisis hidrolisis ester karboksilat. Esterase cenderung bekerja pada ester karboksilat yang bersifat larut dibandingkan yang tidak larut (Winarno 1999).
Trigliserida lipase
Digliserida + asam lemak bebas lipase
Monogliserida + asam lemak bebas lipase
Gliserol + asam lemak bebas
Gambar 2 Reaksi lipase dengan substrat trigliserida ( Muchtadi D et al.1992)
Substrat lipase dapat berupa trigliserida atau ester asam karboksilat dan amida dalam bentuk larut maupun tak larut. Enzim lipase dapat dihasilkan dari sejumlah mikroorganisme (bakteri, kapang, khamir), hewan dan tumbuhan. Produksi enzim dari hewan dan tumbuhan memiliki kelemahan sehingga industri umumnya menggunakan pembiakan mikroorganisme. Mikroorganisme penghasil lipase dari bakteri antara lain Pseudomonas fluorescens, Staphylococcus carnosus, Bacillus stearothermophillus dan Chromobacterium viscosum. Lipase yang berasal dari kapang adalah Aspergillus niger, Mucor miehei dan Rhizophus delemar. Lipase dari khamir dapat diperoleh dari Candida cylindriceae, Candida
auriculariae, Candida curvata, Hansenula aromala dan jenis khamir lainnya (Brockman 1984).
Penggunaan lipase akhir-akhir ini berkembang pesat terutama setelah diketahui kemampuan enzim ini bereaksi dalam medium organik dan ketersediaannya secara komersial dari berbagai merk dipasaran. Berbagai produk yang dikatalisis oleh lipase telah dieksplorasi oleh para peneliti dan dilaporkan sangat berpotensi diaplikasikan di industri (Bastida 1998).
Enzim lipase dapat mengkatalisa reaksi esterifikasi antara asam lemak bebas dengan gliserol dan menghasilkan monoasilgliserol. Hasil yang didapatkan lebih spesifik pada posisi sn-1,3 ; yaitu transfer gugus asil terjadi pada posisi 1 dan atau 3 menghasilkan monoasilgliserol dengan gugus asil di posisi 1 atau 3 (1(3)- MAG) dan DAG dengan gugus asil pada posisi 1 dan 3 (1,3- DAG) (Elizabeth dan Boyle 1997). Jensen et al. (1990) menyatakan bahwa spesifisitas enzim dipengaruhi oleh sifat fisikokimia enzim dan substrat seperti pH, suhu, jenis pelarut, modifikasi fisik atau kimia dan sumber enzim. Sedangkan (Van camp et al. 1998) menyatakan bahwa selektifitas dan spesifisitas lipase sangat tergantung pada kondisi yang diterapkan selama proses seperti aw, pH, suhu, tipe pelarut, pilihan kosubstrat dan imobilisasi. Peningkatan suhu pada enzim tertentu dapat meningkatkan kecepatan reaksi sebaliknya sampai batas tertentu peningkatan suhu reaksi dapat menurunkan kecepatan reaksi bahkan dapat menginaktifkan enzim.
Menurut Elizabeth dan Boyle (1997), produksi monoasilgliserol menggunakan katalis lipase memiliki beberapa kelebihan antara lain; kondisi reaksi lebih ramah, khususnya suhu reaksi lebih rendah yaitu sekitar 22-70 oC; lemak atau minyak yang dapat digunakan lebih bervariasi karena berbagai lipozyme® 1M dapat menunjukkan aktivitas pada berbagai asam lemak, lebih banyak pilihan lipase dengan spesifisitas tertentu untuk menghasilkan produk yang spesifik; energi yang dipergunakan lebih rendah dan proses produksi lebih bersifat ramah lingkungan.
Aplikasi lipase telah dilakukan oleh beberapa peneliti untuk menghasilkan berbagai produk turunan atau produk modifikasi lemak/minyak. Produk-produk hasil reaksi menggunakan lipase tersebut antara lain MAG yang bersifat
antibakteri dari minyak kelapa (Mappiratu 1999) MAG fungsional (Watanabe 2002), ester asam lemak untuk flavor (Babali et al. 2001), surfaktan sorbitan oleat (Xu et al. 2003), lemak coklat dari minyak sawit (Satiawiharja et al.1999), produk makanan bayi yang kaya kandungan asam palmitat pada posisi 2 (Quinlan dan Moore 1993), trigliserida kaya DHA (Irimescu et al. 2001), butyl oleat untuk aditif biodiesel (Linko et al. 1995) dan lain-lain.
Gliserol
Nama lain gliserol adalah gliserin yaitu suatu larutan kental yang memiliki rasa manis, tidak berwarna, tidak berbau dan bersifat higroskopis. Rumus kimia dari gliserol adalah C3H8O3 dengan nama kimia propane-1,2,3-triol. Berat
molekul gliserol 92,10, masa jenis 1,261 g/cm3, titik didih 290oC dan viskositas 1,5 Pa.s. Gliserol merupakan gula alkohol dan mempunyai tiga gugus hidroksil yang bersifat hidrofilik sehingga dapat larut dalam air (Anonim 2006).
Gliserol banyak terdapat dalam bentuk gliserida pada lemak atau minyak dalam jaringan hewan atau tumbuhan. Gliserol juga dapat sebagai produk samping hidrolisis lemak dan minyak, selain asam lemak bebas dan garam logam (sabun). Gliserol sering digunakan sebagai pelarut, pemanis, humektan, bahan tambahan pada industri peledak, kosmetik, sabun cair, permen dan pelumas. Gliserol juga dipakai sebagai komponen antibeku (cryoprotectant) suatu campuran dan sebagai sumber nutrisi pada kultur fermentasi dalam produksi antibiotik (Anonim 2006).
Gliserol dapat digunakan sebagai bahan dasar untuk pembuatan monogliserida, digliserida dan trigliserida melalui proses reaksi esterifikasi atau interesterifikasi secara kimia atau enzimatis. Bila suatu radikal asam lemak berikatan dengan gliserol akan terbentuk suatu monogliserida. Trigliserida akan terbentuk bila tiga asam lemak beresterifikasi dengan satu molekul gliserol (Winarno 2002). Penggunaan gliserol akan menyebabkan reaksi keseimbangan menuju ke arah kanan reaksi esterifikasi sehingga menghasilkan produk monodiasilgliserol yang cukup tinggi (Fischer 1998).
Emulsifier Mono-diasilgliserol (M-DAG)
Sistem emulsi pangan maupun non pangan bersifat jauh lebih kompleks dibandingkan definisi emulsi, yaitu dispersi koloidal suatu droplet cairan pada fase cairan lain; karena fase terdispersi dapat berupa padatan atau fase kontinyu mungkin mengandung bahan yang terdiri dari kristal padatan, seperti pada es krim (Bos et al. 1997). Persamaan karakter pada hampir semua sistem emulsi adalah ketidakstabilan emulsi. Ketidakstabilan atau rusaknya sistem emulsi dapat dicegah dengan cara menggunakan alat mekanik untuk mengatur ukuran droplet terdispersi atau dengan menambahkan bahan penstabil seperti emulsifier. Tujuan utama penambahan emulsifier adalah mencegah coalesen atau penggabungan irreversibel dua atau lebih droplet atau partikel menjadi unit yang lebih besar (Kamel 1991).
Emulsifier adalah salah satu ingredien unik dalam industri pangan, yang biasanya digunakan dalam bakeri, mayonnaise, margarin, minuman yang diformulasi, industri coklat, modifikasi adonan dan beberapa aplikasi yang lain. Emulsifier yang umum dihasilkan dari suatu industri pengolahan minyak tumbuhan adalah monogliserida, digliserida dan ester propilen glikol (Hui 1996).
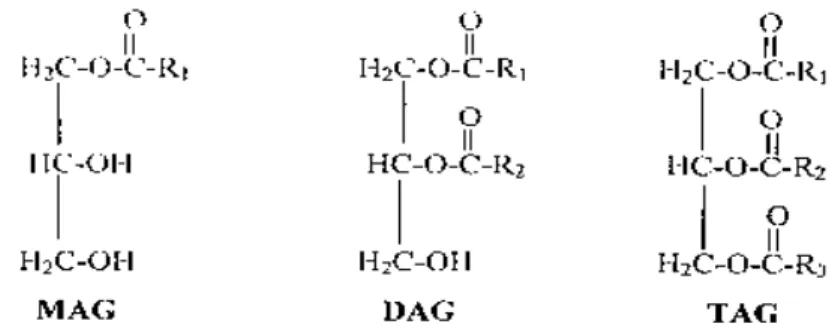
Emulsifier campuran M-DAG didefinisikan sebagai emulsifier lipofilik yang mengandung monogliserida dan digliserida, yang dibuat dengan mereaksikan gliserol dan lemak atau minyak yang spesifik (Igoe dan Hui 1996). M-DAG dapat berupa ester yang padat dan mempunyai titik leleh tinggi, ester yang berbentuk cair pada suhu ruang, maupun ester berbentuk plastis yang bersifat antara padat dan cair (Zielinski 1997; O’Brien 1998). M-DAG memiliki struktur molekul yang terdiri dari bagian hidrofilik pada gugus OH dan bagian lipofilik pada gugus ester asam lemak, struktur MAG, DAG dan TAG dapat dilihat pada Gambar 5.
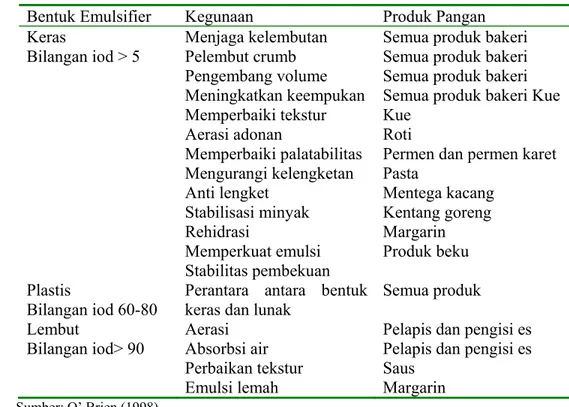
Bentuk emulsifier M-DAG dipengaruhi asam lemak penyusunnya, semakin banyak asam lemak mengandung ikatan rangkap maka bentuk emulsifier akan semakin lunak. Hubungan antara besarnya bilangan iod suatu emulsifier dengan bentuk serta kegunaannya pada produk pangan dapat dilihat pada Tabel 4.
Gambar 5 Struktur molekul Monodiasilgliserol (MAG), Diasilgliserol (DAG) dan Triasilgliserol (TAG)(Hassenhuettl 1997)
Emulsifier adalah bahan yang mampu mengurangi tegangan permukaan pada interfasial dua fase yang pada keadaan normal tidak bercampur, menyebabkan keduanya bercampur dan membentuk emulsi (Dziezak 1988). Emulsifier termasuk bahan dalam formulasi untuk meningkatkan formasi dan stabilisasi emulsi seperti aerasi busa dan suspensi. Emulsifaier memiliki gugus hidrofilik dan terikat pada fase akueus dan rantai lipofilik yang cenderung berada pada fase minyak (Hassenhuettl 1997).
Menurut Krog (1990), emulsifier memiliki berbagai fungsi, terutama untuk meningkatkan stabilitas emulsi, menstabilkan sistem aerasi, mengatur aglomerasi dari globula lemak; memodifikasi tekstur, umur simpan dan sifat reologi dengan mengkompleks molekul pati dan protein, mengembangkan tekstur pangan yang berbasis lemak dengan mengatur polimorfisme dari lemak.
Emulsifier sintetik mulai digunakan pada pertengahan abad 20 dan pemakaiannya berkembang seiring dengan berkembangnya industri pangan olahan yang memerlukan teknologi untuk memproduksi dan mempertahankan kualitas produk Emulsifier digunakan untuk memperpanjang umur simpan produk emulsi seperti salad dressing yang dapat disimpan lebih dari setahun tanpa terpisah fase air dan minyaknya (Hassenhuettl 1997).
Campuran mono dan diasilgliserol (M-DAG) adalah emulsifier komersial pertama di Amerika yang pada tahun 1929 diaplikasikan pada produk margarin dan sejak saat itu emulsifier telah menjadi produk yang dibutuhkan dalam jumlah besar pada sektor industri. Pemakaian emulsifier pada tahun 1982 adalah sebesar 120 juta kg dengan konsumsi pemakaian M-DAG sebesar 96 juta kg (Dziezak 1988).
Tabel 4 Kegunaan emulsifier M-DAG pada produk pangan
Bentuk Emulsifier Kegunaan Produk Pangan Keras Bilangan iod > 5 Menjaga kelembutan Pelembut crumb Pengembang volume Meningkatkan keempukan Memperbaiki tekstur Aerasi adonan Memperbaiki palatabilitas Mengurangi kelengketan Anti lengket Stabilisasi minyak Rehidrasi Memperkuat emulsi Stabilitas pembekuan
Semua produk bakeri Semua produk bakeri Semua produk bakeri Semua produk bakeri Kue Kue
Roti
Permen dan permen karet Pasta Mentega kacang Kentang goreng Margarin Produk beku Plastis Bilangan iod 60-80
Perantara antara bentuk keras dan lunak
Semua produk Lembut Bilangan iod> 90 Aerasi Absorbsi air Perbaikan tekstur Emulsi lemah
Pelapis dan pengisi es Pelapis dan pengisi es Saus
Margarin
Sumber: O’ Brien (1998)
Campuran mono dan diasilgliserol (M-DAG) termasuk ke dalam golongan polimorfik seperti trigliserida. Kristal M-DAG yang berasal dari proses pendinginan masih dalam bentuk kristal α. Kristal α termasuk kristal yang bersifat intermediat dan akan berubah menjadi kristal β yang lebih stabil dan memiliki titik leleh yang lebih tinggi dibanding kristal α. Monogliserida dapat larut dengan sempurna dalam lemak dan minyak dan terdispersi dalam air pada kondisi tertentu (Gunstone et al. 1994).
Reaksi Esterifikasi
Reaksi esterifikasi seperti pada Gambar 3 dan Gambar 4 merupakan reaksi yang menghasilkan senyawa ester dari asam karboksilat dan alkohol. Proses esterifikasi memerlukan katalis berupa katalis logam atau biokatalis (enzim). Reaksi esterifikasi dengan katalis logam berlangsung pada suhu dan tekanan tinggi, sedangkan dengan biokatalis banyak dilaporkan dapat berlangsung pada suhu yang relatif rendah (Harnanik 2005). Linko et al. (1995) menyimpulkan bahwa kandungan air awal sistem reaksi, jumlah enzim dan rasio mol substrat
merupakan faktor-faktor yang sangat penting dalam mempengaruhi hasil esterifikasi.
R1OH + R2COOH R2COOR1 + H2O
Keterangan : R1OH adalah alkohol
R2COOR1 adalah ester
R2COOH adalah asam karboksilat
H2O adalah air
Gambar 3 Skema reaksi esterifikasi (Harnanik 2005)
Gambar 4 Reaksi esterifikasi satu molekul asam lemak dengan satu molekul gliserol (Winarno 2002)
Esterifikasi langsung dari gliserol dan asam lemak menghasilkan monogliserida, digliserida dan trigliserida pada berbagai tingkatan. Komposisi dari produk akhir tergantung pada rasio gliserol : asam lemak, tipe asam lemak dan kondisi proses yang diterapkan. Esterifikasi dapat dilakukan dengan atau tanpa katalis, proses reaksi tanpa menggunakan katalis memerlukan suhu reaksi yang tinggi dan waktu yang lama serta menghasilkan produk yang cenderung berwarna gelap (Hui 1996).
Penelitian yang dilakukan sebelumnya Oleh Pujiastuti (1998) adalah menggunakan DALMS sebagai sumber asam lemak bebas dan gliserol sebagai kosubtratnya untuk menghasilkan M-DAG dengan enzim lipase komersial Rhizomucor miehei. Sintesis M-DAG mencapai optimum pada kondisi reaksi sebagai berikut : rasio DALMS dengan gliserol 2:3, enzim lipase 400 mg, suhu 60oC, waktu 4 jam, waktu pengendapan 24 jam.
Christina (2000) telah berhasil mengoptimasi proses produksi M-DAG dari DALMS dengan memodifikasi metode Pujiastuti yaitu enzim dipisahkan baru direfrigerasi dan enzim yang digunakan 1 g sedangkan kondisi yang lain sama. Selain itu Christina juga telah mengkarakterisasi sebagian sifat fisiko-kimia dan sifat fungsionalnya serta mengaplikasikannya pada beberapa produk pangan. Namun demikian produk yang dihasilkan masih cukup banyak mengandung asam lemak bebas dan memiliki bau kurang disukai.
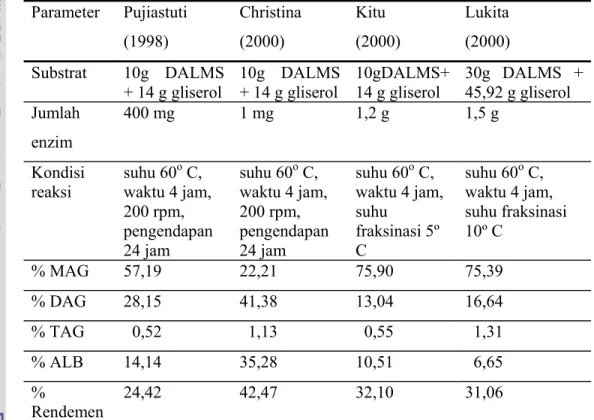
Tabel 3 Perbandingan hasil reaksi sintesis M-DAG secara enzimatik berbahan dasar DALMS beberapa peneliti.
Parameter Pujiastuti (1998) Christina (2000) Kitu (2000) Lukita (2000) Substrat 10g DALMS + 14 g gliserol 10g DALMS + 14 g gliserol 10gDALMS+ 14 g gliserol 30g DALMS + 45,92 g gliserol Jumlah enzim 400 mg 1 mg 1,2 g 1,5 g Kondisi reaksi suhu 60 o C, waktu 4 jam, 200 rpm, pengendapan 24 jam suhu 60o C, waktu 4 jam, 200 rpm, pengendapan 24 jam suhu 60o C, waktu 4 jam, suhu fraksinasi 5º C suhu 60o C, waktu 4 jam, suhu fraksinasi 10º C % MAG 57,19 22,21 75,90 75,39 % DAG 28,15 41,38 13,04 16,64 % TAG 0,52 1,13 0,55 1,31 % ALB 14,14 35,28 10,51 6,65 % Rendemen 24,42 42,47 32,10 31,06
Kitu (2000) juga menggunakan enzim komersial Lipozim dari Rhizomucor miehei dan substrat DALMS untuk menghasilkan M-DAG dengan kondisi reaksi sebagai berikut rasio substrat 10 g DALMS berbanding 14 g gliserol, lipase 5% dari total substrat, waktu 4 jam dan suhu fraksinasi 5o C. Lukita (2000)
mensintesis M-DAG menurut metode Kitu dengan skala yang ditingkatkan yaitu 30 g DALMS, 45,92 gliserol suhu 50o C, waktu 4 jam, enzim 2% dan suhu fraksinasi 10oC.
Perbandingan hasil reaksi esterifikasi dari beberapa peneliti tersebut disajikan dalam Tabel 3. Dari Tabel 3 dapat dilihat bahwa ke empat peneliti sebelumnya mereaksikan substrat DALMS dan gliserol dengan kondisi reaksi (suhu dan waktu) yang sama yaitu suhu 60o C dan waktu reaksi 4 jam tetapi enzim yang digunakan bervariasi yaitu berkisar 400 mg sampai 1,2 g untuk berat substrat yang sama yaitu 10 g DALMS dan 14 g gliserol. Hasil reaksi yang diperoleh bervariasi dari 22,21% sampai 75,90% untuk fraksi MAG, 13,04% sampai 41,38% untuk fraksi DAG, 0,52% sampai 1,13% untuk fraksi TAG dan 24,42% sampai 42,47% untuk rendemen dengan kadar asam lemak bebas berkisar antara 6,65% sampai 35,28 %. Untuk jumlah substrat yang ditingkatkan menjadi 30 g DALMS dan 45,92 g gliserol, enzim ditingkatkan menjadi 1,5 g dan kondisi reaksi tetap yaitu suhu 60o C dan waktu reaksi 4 jam diperoleh fraksi MAG 75,39%, fraksi DAG 16,64%, fraksi TAG 1,31% dan rendemen 31,06% dengan kadar asam lemak bebas 6,65%.
Peranan Pelarut Dalam Sintesis Mono-diasilgliserol (M-DAG) a. Heksan
Faktor- faktor yang mempengaruhi rendemen dalam biosintesis M-DAG antara lain kadar air sistem reaksi, jenis pelarut organik (polaritas pelarut) dan sifat kespesifikan lipase serta faktor lain yang berpengaruh terhadap aktivitas lipase seperti pH, suhu dan konsentrasi substrat (Mappiratu 1999).
Pengaruh jenis pelarut (sifat polaritas pelarut) terhadap rendemen M-DAG dilaporkan oleh Li dan Ward (1993) di dalam Mappiratu (1999) pada reaksi gliserolisis konsentrat asam lemak omega-3 minyak ikan menggunakan lipase PS-30 dan lipase IM-60. Derajat sintesis dalam satuan persen yang sebanding dengan rendemen M-DAG relatif lebih rendah dalam pelarut organik yang bersifat lebih polar (benzena, aseton dan kloroform) dibandingkan dalam pelarut yang bersifat lebih non polar (hidrokarbon).
Fraksi massa M-DAG untuk semua kadar air medium reaksi yang diterapkan meningkat sejalan dengan meningkatnya sifat ketidak polaran pelarut. Pelarut petroleum eter menempati urutan tertinggi dalam hal biosintesis M-DAG
yaitu mencapai rendemen 29,40% diikuti berturut-turut pelarut heksan dengan rendemen 28,35%, campuran heksan /dietil eter dan terakhir pelarut dieter etil (Mappiratu 1999).
Heksan adalah suatu hidrokarbon alkana dengan rumus kimia CH3(CH2)4CH3, berupa cairan tidak berwarna dengan massa molar 86,18 g/ mol,
densitas 0,6548 g/ml, titik leleh -95º C dan titik didih 69º C serta viskositas 0,294 cP pada 25º C. Heksan memiliki 5 isomer yaitu heksan dengan 6 atom C (CH3CH2CH2CH2CH2CH3), isoheksan CH3CH(CH3)CH2CH2CH3, 3- Metil
pentana CH3CH2CH(CH3)CH2CH3, 2,3- Dimetilbutana
CH3CH(CH3)CH(CH3)CH3, 2,2- Dimetilbutana CH3C(CH3)2CH2CH3.
Heksan pada umumnya diproduksi pada proses pemurnian minyak bumi kasar, dimana pada industri 50 % berupa isomer dengan rantai lurus yaitu fraksi yang mendidih pada 65-70º C. Isomer dari heksan sebagian besar tidak reaktif dan sering digunakan sebagai pelarut inert dalam reaksi organik, karena heksan bersifat sangat tidak polar.
b. Butanol
Yang dan Parkin (1994) didalam Mappiratu (1999) melaporkan bahwa fraksi massa M-DAG yang dihasilkan dari gliserolisis minyak mentega dalam pelarut tertier-butanol dengan lipase PS-30 dalam gel ENT-3400 mencapai maksimum pada kadar air 0,4% sedangkan dengan lipase PS-30 dalam gel ENTP- 4000 mencapai maksimum pada kadar air 0,8%
Menurut Rendon et al. (2001) reaksi tanpa menggunakan pelarut transfer massa yang terjadi akan lebih kecil akibat tingginya viskositas, sedangkan pada reaksi yang menggunakan pelarut viskositas akan lebih rendah dan transfer massa lebih tinggi sehingga rendemen yang dihasilkan juga lebih tinggi.
Butanol atau butil alkohol atau kadang-kadang disebut sebagai biobutanol jika diproduksi secara biologi, adalah suatu alkohol primer dengan 4 atom Carbon dan rumus molekulnya C4H10O. Butanol merupakan suatu cairan bening, massa
molar 74,1216 g/ mol, densitas 0,8098 g/ cm3 pada 20º C, titik leleh – 89,5º C, titik didih 117,73º C, kelarutan dalam air 9,1 ml/ 100 ml H2O pada 25º C dan
viscositas 3 cP pada 25º C. Pada umumnya butanol digunakan sebagai pelarut, sebagai intermediat dalam sintesis kimia dan sebagai bahan bakar.
Butanol memiliki 4 isomer, n- butanol atau 1- butanol adalah isomer rantai lurus dengan gugus –OH pada C ujung, isomer berantai lurus dengan gugus –OH pada atom C yang ditengah disebut sec- butanol atau 2- butanol sedangkan isomer dengan rantai bercabang dan gugus –OH pada C ujung disebut isobutanol; 2- metil -1- propanol, isomer ke empat adalah isomer bercabang dengan gugus – OH pada atom C yang ditengah disebut tertier - butanol atau 2- metil-2- propanol. Isomer butanol dengan struktur yang berbeda akan memiliki titik didih dan titik leleh yang berbeda.