BAHAN DAN METODE Tempat dan Waktu Penelitian
Penelitian ini dilaksanakan di Laboratorium Penyakit Tumbuhan Fakultas Pertanian Universitas Sumatera Utara, Medan dengan ketinggian tempat + 25 meter di atas permukaan laut pada bulan juli 2016 sampai dengan selesai.
Bahan dan Alat
Adapun bahan yang digunakan adalah isolat murni F. oxysporum, isolat murni bakteri kitinolitik, alkohol 96%, kloroks 5%, kapas, spirtus, cling wrap, aquades, Media Kitin, Media nutrient agar (Na), Media nutrient broth (NB), Media Potato Dextrose Agar (PDA), kertas stensil, aluminium foil, methyl blue, label nama dan bahan yang mendukung lainnya.
Adapun alat yang digunakan dalam penelitian ini adalah mikroskop compound, micropipet, batang kaca, cawan petri, pinset, tabung reaksi, inkubator, timbangan analitik, erlenmeyer, oven, beaker glass, objek glass, autoclave, bunsen, laminar air flow, coke borer, kulkas, jarum ose, gunting, pisau, handsprayer, kamera, alat tulis dan alat yang mendukung lainnya.
Metode Penelitian
Penelitian ini menggunakan Rancangan Acak Lengkap (RAL)non Faktorial dengan perlakuan sebagai berikut:
BK0 = F. oxysporum (Kontrol)
Jumlah ulangan sebanyak 3, yang diperoleh dari: t(r-1) ≥ 15
49 (r-1)≥ 15
49r - 49 ≥ 15
49r ≥64
r ≥ 1,3
r ≥ 2 Pelaksaan Penelitian Isolasi Bakteri Kitinolitik
Eksplorasi bakteri dimulai dengan mencari tanah Tanaman sehat ini dapat dianggap telah mendapat stimulus dari mikroorganisme dilingkungan akar yang melindungi akar tanaman dari infeksi patogen. Tanah-tanah dengan fenomena suppressivitas ini diambil dari perakaran rumpun tanaman bawang merah secukupnya untuk isolasi mikroorganisme bakalan di laboratorium Penyakit Tumbuhan Fakultas Pertanian USU.
20 menit, kemudian umbi bawang secara aseptik disayat dengan ketebalan 3-4 mm menggunakan pisau steril, sayatan umbi bawang ini diletakkan dalam cawan petri steril yang telah dialas dengan kertas saring steril yang dilembabkan dengan air suling steril. Bagian tanaman terinfeksi yang telah mendapat perlakuan sterilisasi permukaan dengan larutan 1% NaOCl selama 3 menit dan dicuci dengan air suling steril sebanyak 3 kali, diletakkan di atas kaca slaid mikroskop. Perlakuan ini diinkubasi tanpa cahaya selama lebih kurang 5 hari pada temperatur 25 – 26ºC dalam media PDA.
Uji Aktifitas Antibiosis Bakteri Kitinolitik di Laboratorium
a. Uji aktififitas antibiosis Bakteri kitinolitik
b. Antibiosis filtrat kultur bebas sel
Filtrat kultur bakteri kitinolitik di panen dari kultur masing-masing setelah 5 hari dalam biakan media cair kaldu nutrien. Filtrat di panen dan dan disentrifugasi pada 8.000 rpm pada suhu 4°C selama 10 menit, untuk mendapatkan bebas sel, filtrat kultur disaring menggunakan membran 0,45 Millipore filter. Antibiosis filtrat diuji dalam medium PDA menggunakan cawan petri 9 cm dengan cara mencampurkan filtrat kedalam medium PDA dengan perlakuan 10%, 20%, 30%, 40%, 50%. Cakram miselium F. oxysporum diambil dari tepi koloni kultur aktif dan diinokulasikan tepat di tengah cawan petri. Perlakuan ini diinkubasi selama 5 hari.
Peubah Amatan
1. Daerah Hambatan (%)
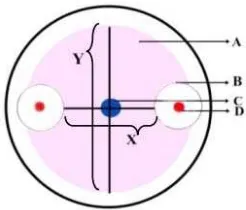
Gambar 1. Metode pengukuran zona hambat bakteri kitinolitik terhadap koloni jamur; A. Koloni jamur, B. Zona hambat bakteri kitinolitik terhadap koloni jamur, C. Titik tengah jamur diletakkan, D. Koloni bakteri kitinolitik, X. Diameter koloni jamur yang terhambat pertumbuhannya, Y. Diameter koloni jamur normal (Suryanto, 2010)
(Suryanto et al., 2011).
2. Pengamatan Struktur Hifa Abnormal
Pengamatan struktur hifa secara mikroskopis dilakukan dengan cara mengamati ujung miselium pada daerah zona hambat fungi patogen. Abnormalitas pada pertumbuhan miselium fungi pathogen seperti, pembengkokan ujung miselium, miselium pecah, miselium berbelah, miselium bercabang, miselium lisis, dan miselium tumbuh kerdil yang diamati dibawah mikroskop dan dilakukan dokumentasi (Lorito et al., 1992).
3. Kecepatan Tumbuh
Laju pertumbuhan cendawan diketahui dengan cara mengukur pertambahan diameter koloni cendawan setiap hari setelah inokulasi (hsi) sampai hari ke-5 (hsi).
Analisis Data