BAB 2
TINJAUAN PUSTAKA
2.1. Daun Nenas (Ananas comosus (L) Merr)
Tanaman nenas (Ananas cosmosus (L) Merr)yang termasuk family Bromeliaceae merupakan tumbuhan tropis dan subtropis yang banyak terdapat diIndonesia.Bentuk daun nenas menyerupai pedang yang meruncing diujungnyadengan warna hijau kehitaman dan pada tepi daun terdapat duri yang tajam seperti pada Gambar 2.1. Tergantung dari spesies atau varietas tanaman, panjang daun nenas berkisar antara 55 sampai 75 cm dengan lebar 3,1 sampai 5,3 cm dan tebal daun antara 0,18sampai 0,27 cm.Serat nenas terdiri atas selulosa dan non selulosa yang diperolehmelalui penghilangan lapisan luar daun secara mekanik. Lapisan luar daun berupapelepah yang terdiri atas sel kambium, zat pewarna yaitu klorofil, xantofill dankaroten yang merupakan komponen kompleks dari jenis tanin, serta lignin yangterdapat di bagian tengah daun.Selain itu lignin juga terdapat pada lamela dariserat dan dinding sel serat (Hidayat, 2008).
Adapun klasifikasi tanaman nenas menurut Anonim, 2010 sebagai berikut :
Kingdom : Plantae
Sub kingdom : Spermatophyta
Superdivisio : Magnoliophyta
Divisio : Magnoliophyta
Kelas : Angiospermae
Sub-kelas : Asteridae
Ordo : Farinosae
Familia : Bromiliaceae
Genus : Ananas
Spesies : Ananas comosus (L) Merr.
Berdasarkan pengamatan dengan mikroskop, sel-sel dalam serat daun nanas mempunyai ukuran diameter rata-rata berkisar 10 μm dan panjang rata-rata 4,5 mm dengan ratio perbandingan antara panjang dan diameter adalah 450. Rata-rata ketebalan dinding sel dari serat daun nanas adalah 8,3 μm.Komposisi kimia dari serat daun nenas ditunjukkan pada Tabel 2.1.
Tabel 2.1 Komposisi Kimia Serat Daun Nenas (Rahmat, 2007)
NO Komposisi kimia Kadar (%)
1 Alpha Selulosa 69,5 – 71,5
2 Pentosan 17,0 – 17,8
3 Lignin 4,4 – 4,7
4 Pektin 1,0 – 1,2
5 Lemak dan wax 3,0 – 3,3
6 Abu 0,7 – 0,87
Serat yang diperoleh dari daun nenas muda kekuatannya relatif rendah dan seratnya lebih pendek dibanding serat dari daun yang sudah tua.Sama halnya dengan serat-serat alam lainnya yang berasal dari daun (leaf fibres), secara morfologi jumlah serat dalam daun nanas terdiri dari beberapa ikatan serat (bundleof fibres) dan masing-masing ikatan terdiri dari beberapa serat (multi-cellulerfibre) (Onggo, 2005).
2.2. Selulosa
Selulosa merupakan biopolimer yang berlimpah dialam yang bersifat dapat diperbaharui, mudah terurai, tidak beracun, dan juga merupakan polimer karbohidrat yang tersusun atas β-D glukopiranosa dan terdiri dari tiga gugus hidroksi per anhidro glukosa menjadikan selulosa memiliki derajat fungsionalitas yang tinggi.Sebagai materi yang diperbaharui, selulosa dan turunannya dapat dipelajari dengan baik.Bahan dasar selulosa telah digunakan lebih dari 150 tahun dalam berbagai macam aplikasi, seperti makanan, produksi kertas, biomaterial, dan dalam bidang kesehatan(Coffey et al, 1995).
Selulosa merupakan konstituen utama kayu kira-kira 40-50% bahan kering dalam kebanyakan spesies kayu adalah selulosa, terutama terdapat dalam dinding sel sekunder. Selulosa merupakan homo-polisakarida yang tersusun atas unit-unit β -D-Glukopiranosa yang terikat satu sama lain dengan ikatan-ikatan glikosida (Hardjono, 1995).
Secara alamiah molekul-molekul selulosa tersusun dalam bentuk fibril- fibrilyang terdiri dari beberapa molekul selulosa yang dihubungkan dengan ikatan glikosidik. Fibril-fibril ini membentuk struktur kristal yang dibungkus oleh lignin. Komposisi kimia dan struktur yang demikian membuat kebanyakan bahan yang mengandung selulosa bersifat kuat dan keras.Sifat kuat dan keras yang dimiliki oleh sebagian besar bahan berselulosa membuat bahan tersebut tahan terhadap peruraian secara enzimatik.Secara alamiah peruraian selulosa berlangsung sangat lambat (Fan et al., 1982).
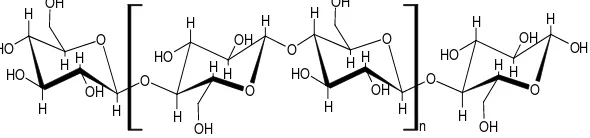
Selulosaadalahsenyawaseperti serabut, liat, tidak larut dalam air dan ditemukan didalam dinding sel pelindung tumbuhan, terutama pada tangkai, batang, dahan dan semua bagian berkayu dari jaringan tumbuhan. Kayu terutama mengandung selulosa dan senyawa polimer lain. Selulosa tidak hanya merupakan polisakarida struktural ekstraselular yang paling banyak dijumpai pada dunia tumbuhan, tetapi juga merupakan senyawa yang paling banyak diantara semua biomolekul pada tumbuhan atau hewan. Karena selulosa merupakan homopolisakarida linear tidak bercabang, terdiri dari 10.000 atau lebih unit D-glukosa yang dihubungkan oleh ikatan β 1,4 glikosida senyawa ini akan kelihatan seperti amilosa, dan rantai utama glikogen (Lehninger, 1988).
O
Gambar 2.2 Struktur Selulosa (Setiyawan, 2010)
Menurut Clark, berdasarkan panjang rantainya membagi selulosa menjadi tiga bagian yaitu :
1. Alpha selulosa merupakan selulosa rantai panjang, tidak larut dalam larutan 17,5 % NaOH dengan DP sekitar 600 – 1500
2. Beta selulosa merupakan selulosa rantai pendek, larut dalam larutan 17,5 % NaOH, memiliki DP sekitar 15 – 90
3.Gamma selulosa merupakan selulosa rantai pendek, larut dalam larutan 17,5 % NaOH dan larutan asam, dan memiliki DP kurang dari 15 (Smook, 1987).
Selulosa membentuk komponen serat dari dindng sel tumbuhan.Ketegaran selulosa disebabkan oleh struktur keseluruhannya. Molekul selulosa merupakan rantai-rantai, atau mikrofibril, dari D-glukosa sampai sebanyak 14.000 satuan yang terdapat sebagai berkas-berkas terpuntir mirip tali, yang terikat satu sama lain oleh ikatan hidrogen. Hidrolisis lengkap dalam HCl 40% dalam air, hanya menghasilkan D-glukosa.Disakarida yang terisolasi dari selulosa yang terhidrolisis sebagian adalah selobiosa, yang dapat dihidrolisis lebih lanjut menjadi D-glukosa dengan suatu katalis asam atau dengan emulsion enzim (Fesenden, 1994).
ikatan hidrogen yang kuat, selulosa mempunyai kekuatan tarik yang tinggi dan tidak larut dalam kebanyakan pelarut (Atalla, 1987).
Setiap unit β-D-glikopiranosa didalam rantai selulosa mempunyai tiga gugus hidroksil reaktif, dua sekunder (HO-2 dan HO-3) dan satu primer (HO-6).Untuk eterifikasi, gugus hidroksil sekunder (HO-2) biasanya paling mudah bereterifikasi sedangkan untuk esterifikasi, gugus hidroksil primer (HO-6) memiliki reaktifitas yang lebih tinggi. Aksesbilitas berarti kemudahan relatif gugus-gugus hidroksil untuk dicapai oleh pereaksi-pereaksi gugus (HO-6) reaktifitasnya lebih tinggi terhadap substituen-substituen yang besar dari pada gugus-gugus hidroksil yang lain karena paling sedikit halangan steriknya (Fengel, 1995).
2.3. AsamSitrat
Asam sitrat terdapat pada jeruk nipis sebanyak kira-kira 6%.Asam sitrat selalu ditambahkan kepada minuman-minuman ringan dan gula-gula sebagai penyedap.Asam ini juga merupakan perantara yang penting pada metabolisme karbohidrat dan merupakan komponen dalam darah dan urin (Siregar, 1988).Asam sitrat memiliki karakteristik seperti asam hidrosikarboksilat lainnya dalam bentuk garam, esterifikasi, anhidrida, amida dan reaksi kimia lainnya (Grimaux, 1880). Rumus kimia asam sitrat adalah C6H8O7atauCH2
(COOH)-COH(COOH)-CH2(COOH), rumus struktur asam sitrat ini tercermin pada nama IUPAC-nya, asam
pemanasan di atas 740C.(id.wikipedia.org). Struktur asam sitrat dapat dilihat pada gambar 2.3.
H2C
C
COOH
HO COOH
H2C COOH
Gambar 2.3. Struktur Asam Sitrat (Apelblat, 2014)
Sifat-sifat asam sitrat adalah sebagai berikut : a. Rumus molekul : C6H8O7
b. Berat Molekul : 192.12 g/mol c. Titik lebur : 1530 C d. Titik didih : 1750 C
e. Densitas : 1.665 g/cm3 (Anonim, 1952)
Konversi dari asam sitrat anhidrat ditunjukkan melalui interaksi asam padat dengan asetat anhidrat berlebih dalam asam asetat glasial pada suhu 360C – 380C. Titik lebur dari kristal anhidrat putih yaitu 1210 – 1230C. Identifikasi dari senyawa ini dapat dilihat melalui analisis dasar, titrasi potensiometri,cryoscopic dan pengukuran NMR. Sintesis alkil sitrat (gugus alkil rantai pendek) merupakan cairan berminyak. Namun dengan meningkatnya rantai, maka akan berubah menjadi seperti lilin dan bubuk padatan dengan variasi kelarutan dalam air dan pelarut organik (Apelblat,2014).
2.4. Esterifikasi
dan air akan terjadi. Proses ini disebut esterifikasi Fischer, yang ditemukan oleh Emil Fischer Seorang ahli kimia yang menonjol pada abad ke-19. Walaupun reaksi berada dalam kesetimbangan, reaksi ini dapat digunakan untuk membuat ester dengan hasil yang memuaskan dengan jalan mendorong kesetimbangan ke kanan (Siregar, 1988).
Esterifikasi juga dapat didefenisikan sebagai reaksi antara asam karboksilat dan alkohol (Gandhi, 1997).Esterifikasi dapat dilakukan dengan menggunakan katalis enzim (lipase) dan asam anorganik (asam sulfat dan asam klorida), dengan berbagai variasi alkohol biasanya metanol, etanol, 1-propanol, 1-butanol, amyl alkohol, dan lain-lain (Ozgulsun, 2000).
Asam anorganik yang digunakan sebagai katalis akan menyebabkan asam karboksilat mengalami konjugasi sehingga asam konjugat dari asam karboksilat tersebutlah yang akan berperan sebagai substrat. Cara lain dalam pembentukan ester adalah dengan melewatkan HCl ke dalam campuran reaksi tersebut dan direfluks. Cara ini dikenal dengan nama metode Fischer-Spieser. Esterifikasi tanpa katalis dapat juga dilakukan dengan satu molekul asam karboksilat dan satu pereaksi secara berlebih.Pertambahan hasil juga dipengaruhi oleh dehidrasi yang artinya menarik air terbentuk sebagai hasil samping reaksi. Air dapat dipisahkan dengan cara menambahkan pelarut yang bersifat non polar seperti misalnya benzene dan kloroform sehingga air yang terbentuk akan segera terikat pada pelarut yang digunakan atau dengan menambahkan molekular sieves (Yan, 2001).
2.5. Esterifikasi Selulosa
Untuk mendapatkan sifat fisik dan kimia yang lebih baik dan memperluas aplikasinya, selulosa dibuat dalam berbagai turunannya diantaranya turunan ester dan eter. Ester selulosa banyak digunakan sebagai serat dan plastik, sedangkan eter sebagai pengikat dan bahan tambahan untuk mortar khusus atau kimia khusus untuk bangunan dan konstruksi juga stabilisator viskositas pada cat, makanan, produk farmasetik, dan lain-lain (Zugenmaier, 2008).
Pembentukan ester selulosa menggunakan asam organik melalui proses esterifikasi terhadap gugus hidroksi alkohol, yang umum menggunakan asam klorida atau asam anhidrat lainnya sebagai agen yang meningkatkan derajat esterifikasi secara signifikan. Esterifikasi gugus hidroksi alkohol umumnya berlangsung dalam reaksi setimbang, di mana ikatan ester yang dibentuk dipengaruhi dan diputus dalam suasana asam encer, dan penggunaan alkali pekat secukupnya membentuk ester penyabunan yang bersifat irreversible.
2.5.1. Selulosa Xantate
Cell OH CS2 NaOH Cell O C S
S- Na+ Selulosa Xantate
Larutan dari selulosa xantate ini dilewatkan melalui suatu lubang kecil atau celah ke dalam larutan yang bersifat asam. Regenerasi gugus –OH dari selulosa ini menyebabkan lapisan endapan seperti jaringan atau lembaran :
Cell O C S
S- Na+ H3O +
Cell OH
Rayon atau kertas kaca(Solomons, 2014)
2.5.2. Selulosa Nitrat
Modifikasi ester selulosa dengan asam organik dan asam anorganik membentuk turunan selulosa bersifat kovalen yang pertama kali disintesis dalam laboratorium.Selulosa nitrat, selulosa asetat dan selulosa xantogenat telah diproduksi dalam skala industri pada pertengahan abad yang lalu dan saat ini telah mencakup lebih dari 90 % total produksi selulosa.Diawali dengan ester selulosa dari asam anorganik, hingga asam organik telah dipersiapkan dalam esterifikasi konvensional, demikian juga reaksi yang dirancang secara khusus.Selulosa nitrat merupakan turunan selulosa pertama yang diproduksi dalam skala industri untuk pembuatan kain sutera sintetik. Ini dapat dibentuk melalui reaksi antara polimer dengan HNO3
berdasarkan reaksi :
Cell OH HNO3 Cell O NO2 H 2O
2.5.3. Selulosa Asetat
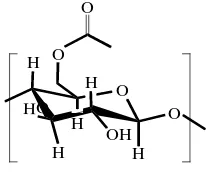
pada Gambar 2.4.Seiring perkembangan zaman, Franchimont (1879) menemukan penggunan katalis yang efisien yakni H2SO4 dan HClO4. Kedua percobaan ini
menjadi dasar pembuatan selulosa asetat dengan asetat anhidrat sebagai agen dalam proses esterifikasi dan asam sulfat atau asam perklorat sebagai katalis.
O
Gambar 2.4. Ester Selulosa-asetat (Ganstrom, 2009)
2.5.3. Selulosa Sulfat
Sebagian besar asam sulfat, asam sulfit, atau asam klorosulfonat dapat digunakan sebagai agen sulfonasi, yang juga dapat dikombinasikan dengan pelarut inert seperti alkohol. Secara umum reaksi pembentukan selulosa sulfat dapat ditunjukkan oleh reaksi berikut :
Cell-OH + SO3 Cell-OSO3H
Cell-OH + XSO3H Cell-OSO3H + HX (X = NH2, OH, Cl)
Selulosa sulfat secara detail dapat dibentuk melalui beberapa tahap berikut: (i) Sulfonasi gugus hidroksi biasanya dimulai dalam sebuah sistem heterogen.
(ii)Sulfonasi gugus hidroksi yang bebas sebagian membentuk ester selulosa atau eter selulosa di mana subtituent primer bertindak sebagai gugus pelindung.
(iii)Sulfonasi oleh pertukaran tempat gugus ester atau eter dengan makromolekul yang datang.
2.2.5. Selulosa Fenil Karbamat
trikarbanilat dengan penggunaan reagen berlebih dalam 10 jam reaksi pada suhu 70-1000 C. Reaksi secara perlahan akan berubah dari heterogen menjadi homogen dan disertai karbanilasi melalui degradasi cincin yang dapat diabaikan. Jalur ini cocok untuk mengubah selulosa polimer analog menjadi turunan selulosa yang memiliki kelarutan dalam larutan. Reaksi pembentukan selulosa fenil karbamat ditunjukkan pada Gambar 2.5 berikut :
Cell OH N C O Cell O OC HN
Gambar 2.5. Reaksi Pembentukan Selulosa Fenil Karbamat (Klem, 1998)
2.6. Adsorpsi
Adsorpsi atau penyerapan adalah proses pemisahan komponen tertentu dari suatu fluida berpindah ke permukaan zat padat yang menyerap (adsorben). Biasanya partikel-partikel kecil adsorben ditempatkan dalam suatu hamparan tetap dan fluida dialirkan melalui hamparan itu sampai adsorben mendekati jenuh dan pemisahan yang dikehendaki tidak dapat berlangsung lagi. Pemisahan adsorpsi banyak digunakan pada industry kimia, misalnya pada pemisahan gas, mengurangi kelembaban udara, penghilangan bau, dan penyerapan gas yang tidak diinginkan dari suatu hasil proses (Maron, 1984).
Jenis adsorpsi yang umum dikenal adalah adsorpsi kimia (Kemisorpsi) dan adsorpsi fisika (Fisisorpsi).
1. Adsorpsi Kimia (Kemisorpsi)
adsorpsi kimia hanya satu lapisan gaya yang terjadi. Besarnya energi adsorpsi kimia sekitar 100 kj/mol.
2. Adsorpsi Fisika (Fisisorpsi)
Molekul-molekul yang diadsorpsi secara fisika tidak terikat kuat pada permukaan, dan biasanya terjadi proses balik cepat, sehingga mudah diganti dengan molekul yang lain. Adsorpsi fisika didasarkan pada gaya Van Der Waals dan dapat terjadi pada permukaan yang polar dan non polar. Adsorpsi juga mungkin terjadi dengan mekanisme pertukaran ion.Oleh karena itu ion pada gugus senyawa permukaan padatan adsorbennya dapat bertukar dengan ion-ion adsorbat.Mekanisme pertukaran ini merupakan penggabungan dari kemisorpsi dan fisisorpsi, karena mengikat ion-ion dengan ikatan secara kimia tetapi ikatan mudah dilepas kembali untuk terjadinya pertukaran ion.Besarnya energi adsorpsi fisika sekitar 10 kj/mol (Barrow, 1979).
1.7. Logam Kadmium (Cd)
Kadmium adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Cd dan nomor atom 48.Kadmium merupakan salah satu jenis berbahaya karena elemen ini beresiko tinggi terhadap berpengaruh terhadap manusia dalam jangka waktu panjang dan dapat terakumulasi pada tubuh khususnya berefek terhadap gangguan pa yang kronis.Jumlah normal kadmium di tertinggi (1.700 ppm) dijumpai pada permukaan sampel tanah yang diambil di dekat pertambangan biji seng (Zn) (https:id.wikipedia.org/wiki/Kadmium).
kadmium dapat masuk ke dalam tubuh melalui berbagai cara, diantaranya dari udara yang tercemar, kontaminasi perairan, jalur rantai makanan dan wadah makanan/minuman yang berlapis kadmium. Kadmium dalam tubuh dapat merusak sistem fisiologis tubuh antara lain sistem urinaria, sistem respirasi (paru-paru), sistem sirkulasi darah dan jantung, kerapuhan tulang dan sistem reproduksi (Widowati, 2008).
Kadmium dan bentuk garamnya banyak digunakan pada beberapa jenis pabrik untuk proses produksinya. Industri pelapisan logam adalah pabrikyang paling banyak menggunakan kadmium murni sebagai pelapis, begitu juga pabrik yang membuat Ni-Cd bateri.Kadmium lebih beracun bila terisap melalui saluran pernapasan daripada saluran pencernaan. Kasus keracunan akut kadmium kebanyakan dari mengisap debu dan asap cadmium, terutama kadmium oksida (CdO). Dalam beberapa jam setelah mengisap, korban akan mengeluh gangguan saluran pernapaan, muntah, kepala pusing, dan sakit pinggang ( Darmono, 2001).
Kadmium dengan tingkat oksidasi +2 mempunyai konfigurasi (36Kr) 4d10 5s0
5p0 5d0 sehingga pada orbital d elektron belum terisi penuh. Adanya peran d-orbital back donation dari logam ini dapat menjadi dasar konsep pembentukan khelat.Pearson (1963) mengklasifikasikan asam-basaLewis menurut sifat kuat dan lemahnya. Menurut Pearson, situs aktif pada permukaan padatan dapat dianggap sebagai ligan yang dapat mengikat logam secara selektif. Logam dan ligan dikelompokkanmenurut sifat kuat dan lemahnya berdasarkan pada polarisabilitas unsur.