SKRIPSI
KAJIAN KUALITAS AIR PADA TAMBAK TRADISIONAL PLUS YANG DIBERI BAKTERI ANAEROB DI DESA MANAKKU KECAMATAN
LABAKKANG KABUPATEN PANGKAJENE DAN KEPULAUAN
MUH. TASRIF 10594088814
JURUSAN BUDIDAYA PERAIRAN FAKULTAS PERTANIAN
UNIVERSITAS MUHAMMADIYAH MAKASSAR 2020
3HALAMAN PENGESAHAN
Judul Skripsi : Kajian Kualitas Air Pada Tambak Tradisional Plus Yang Diberi Bakteri Anaerob Di Desa Manakku Kecamatan Labakkang Kabupaten Pangkajene Dan Kepulauan
Nama : Muh. Tasrif
NIM : 10594088814
Program Studi : Budidaya Perairan Fakultas : Pertanian
Komisi Pembimbing :
Pembimbing I Pembimbing II,
Dr.Murni , S.Pi., M.Si. Asni Anwar, S.Pi., M.Si. NIDN : 090337306 NIDN: 0921067302 Diketahui :
KOMISI PENGUJI
Judul Proposal : Kajian Kualitas Air Pada Tambak Tradisional Plus Yang Diberi Bakteri Anaerob Di Desa Manakku Kecamatan Labakkang Kabupaten Pangkajene Dan Kepulauan.
Nama : Muh. Tasrif
NIM : 10594088814 Prodi : Budidaya Perairan
SUSUNAN KOMISI PENGUJI
Nama Tanda Tangan
1. Dr.Murni , S.Pi., M.Si. (...) Ketua Sidang
2. Asni Anwar, S.Pi., M.Si. (...) Sekretaris
3. Dr. Abdul Haris Sambu., S.Pi.,M.Si (...) Anggota
4. Dr. H. Burhanuddin, S.Pi., M.P (...) Anggota
KATA PENGANTAR
Puji Syukur kehadirat Allah swt., yang senantiasa melimpahkan rahmat dan hidayahn-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul Kajian Kualitas Air Pada Tambak Tradisional Plus yang Diberi Bakteri Anaerobdi Desa Manakku Kecamatan Labakkang Kabupaten Pangkajene dan Kepulauan ini.
Dalam penulisan ini penulis banyak memperoleh pengalaman berharga dan tidak lepas dari beberapa rintangan dan halangan. Namun, dengan adanya doa dan motivasi dari berbagai pihak sehingga skripsi ini dapat selesai dengan baik dan tepat waktu.
Skripsi ini disusun untuk memenuhi persyaratan akademik untuk memperoleh gelar sarjana dalam bidang Budidaya Perairan di Pertanian Universitas Muhammadiyah Makassar. Skripsi ini dapat penulis selesaikan atas bantuan dari beberapa pihak. Oleh karena itu, penulis ucapkan terima kasih kepada pihak-pihak yang telah membantu dalam menyelesaikan proposal ini.
Penulis mengucapkan terima kasih banyak kepada Ibu Dr. Ir. Andi Khaeriyah, M.Pd., dan Ibu Asni Anwar, S.Pi., M.Si., selaku pembimbing satu dan pembimbing dua yang telah memberi perhatian, kasih sayang, semangat, doa serta bantuan moril dan material kepada penulis. Terima kasih kepada kedua orang tua, keluarga, sahabat serta teman-teman yang telah memberikan semangat, dorongan dan doa dalam menyelesaikan proposal ini.
DAFTAR ISI
SAMPUL i
HALAMAN JUDUL ii
LEMBAR PENGESAHAN iii
KOMISI PENGUJI iv
LEMBAR KEASLIAN SKRIPSI v
KATA PENGATAR vi
DAFTAR ISI vii
DAFTAR TABEL ix
1. PENDAHULUAN 1
1.1. Latar Belakang 1
1.2. Tujuan dan Kegunaan Penelitian 3
2. TINJAUAN PUSTAKA 4
2.1. Kondisi Umum Tambak. 4
2.2. Tambak Marginal 4
2.3. Parameter Kualitas Air 5
2.3.1 Suhu 5
2.3.2 Salinitas 7
2.3.3 Tingkat Keasaman (pH) 8
2.3.4 Oksigen Terlarut (DO) 9
2.3.5 Aminiak Tingkat Keasaman (pH) 10
2.3.6 Nitrit 11
2.3.7 Ortofosfat (PO4) 12
2.3.8 Bahan Organik Total (BOT) 13
2.4. Tabel pengelompokkan tingkat kesesuaian tambak 13
3. METODE PENELITIAN 15
3.3. Pengambilan sampel air 15
3.4. Analisis Parameter Kualitas Air 16
3.4.1.Suhu 16
3.4.2.Salinitas 16
3.4.3.Pengukuran Ph 17
3.4.4.Pengukuran Oksigen terlarut (DO) 17
3.4.5.Amoniak (NH3) 17
3.4.6.Nitrit (NO2-N) 18
3.4.7.Ortisfat (PO4-P) 18
3.4.8.BOT ( Bahan Organik Total) 19
3.5. Rancangan Penelitian 21
3.6. Analisis Data 4. HASIL DAN PEMBAHASAN 23
4.1 Hasil 23 4.2 Pembahasan 23 5. PENUTUP 29 5.1 Kesimpulan 29 5.2 Saran 29 DAFTAR PUSTAKA 30
DAFTAR TABEL
Tabel 2.1 Tingkatan DO Perairan 8 Tabel 2.2 Klasifikasi kesuburan perairan berdasarkan
konsentrasi fosfat 12
Tabel 2.3. Matriks Kesesuaian Lahan untuk Budidaya Tambak 13 Tabel 3.1 Alat dan metode pengukuran parameter kualitas air 20 Tabel 4.1 Kisaran kualitas air fisika kimia air pada tambak traditionl plus
yang diberi bakteri probiotik anaerob di Desa Manakku Kecamatan Labakkang 22
1. PENDAHULUAN 1.1. Latar Belakang
Tambak pendidikan terletak di Desa Manakku Kec.Labakkang Kabupaten Pangkajenne dan Kepulauan. Tambak tersebut memiliki luas 7 Ha dan diapit oleh 2 sungai besar yaitu sungai Lompoa disebelah Utara dan Sungai Bontoala disebelah Selatan. Terdapat beberapa komoditas yang dibudidayakan di Tambak tersebut salah satunya yaitu udang windu.
Penggunaan obat obatan dan pupuk anorganik secara berlebihan untuk meningkatkan produksi tambak dapat mengakibatkan penumpukan bahan bahan organik pada tambak dan air pasang yang terbatas serta akumulasi dari kegiatan budidaya itu sendiri merupakan beberapa factor yang dapat membuat tambak menjadi kurang produktif (marginal).
Penumpukan bahan organik pada tambak tersebut dapat menurunkan kualitas air yang memicu bakteri perombak tumbuh dengan cepat. Yang mengakibatkan menurunnya daya tahan udang yang dibudidayakan karena menurunnya nafsu makan. Selain itu juga dapat mengakibatkan matinya jasad renik yang berperan penting dalam siklus hara dan rantai makanan di dalam tambak seperti bakteri Nitrosomonas dan Nitrobacter yang sangat berperan dalam proses nitrifikasi (Nurdjana, 2009).
Hal tersebut menyebabkan daya dukung tambak sangat rendah. Akibatnya tambak menjadi kehilangan potensi produktivitas (tambak marjinal).
Terganggunya keseimbangan oksigen yang terlarut di dalam perairan karena peningkatan bahan organik dapat menyebabkan meningkatnya komsumsi oksigen yang semakin besar dibandingkan dengan tingkat produksi oksigen terlarutnya. Hal ini dapat menjadikan lapisan anoksi menjadi semakin tebal dan mempengaruhi kebutuhan oksigen. Lebih lanjut, oksigen yang hilang diperairan dapat juga disebabkan oleh oksigen yang dimanfaatkan oleh mikroba agar dapat mengoksidasi bahan organik, (Jati : 2012).
pH, oksigen, suhu dan bahan organik pada proses daur ulang oleh bakteri pengurai dapat berjalan dengan maksimal. Bakteri Aerob dan bakteri Anaerobdapat dapat melakukan proses oksidasi ini, tetapi dalam memiliki keterbatasan dalam mengurai bahan-bahan tersebut. ketika jumlah yang melampai batas dari limbah bahan organik dan faktor lingkungan tidak mendukung, seperti suhu, oksigen, pH dan bahan organik yang sulit terurai sempurna dapat berdampak buruk bagi kondisi perairan
Peran bakteri yang sangat penting dalam merombak bahan-bahan organik supaya tidak racun bagi perairan terutama bagi biota yang dipelihara dalam tambak. Agar tidak akan menjadi racun maka perlu dilakukan perombakan yang baik.
Dekomposisi bahan organik sangat bermanfaat terutama untuk bahan pembuangan sampah dan sangat berguna untuk organisme yang lain. Pembuangan limbah ke lingkungan mesti didahului dengan pengolahan yang baik agar tidak merusak lingkungan. Pemanipulasian lingkungan untuk menuju
arah perbaikan produksi diperlukan pemahaman mengenai dasar proses fisika, kimia dan biologi perairan (Boyd, 1986 dalam Thakur and Lin., 2003).
Dalam pemanfaatan yang mulai menurun daya dukungnya maka perlu evaluasi kesesuaian lahan dan analisa lebih dalam untuk mendapatkan data dan informasi mengenai tingkat kesesuaian tambak pada kondisi sekarang dengan melakukan evaluasi kualitas air pada tambak tradisional plus yang diberi bakteri Anaerob.
1.2. Tujuan dan Kegunaan Penelitian
Tujuan penelitian ini agar dapat mengevaluasi kualitas air lahan tambak tradisional plus yang diberi bakteri anaerob di Desa Manakku, Kecamatan Labakkang, Kabupaten Pangkajene dan Kepulauan, Provinsi Sulawesi Selatan.
Kegunaan penelitian ini untuk memberikan informasi ilmiah kepada pembudidaya dan seluruh stakeholdermengenai kualitas air air tambak marginal.
II TINJAUAN PUSTAKA
2.1. Kondisi Umum Tambak.
Tambak di Desa Manakku Kec.Labakkang Kabupaten Pangkep berdiri sejak tahun 2017, terbentuknya tambak ini mulanya area persawahan yang dialih fungsikan menjadi tambak dengan luas 7 Ha lokasi tambak memiliki jarak dari bibir pantai sekitar 5 km di apit oleh 2 sungai yaitu diseblah selatan sungai Bontoala dan seblah Utara sungai Lompoa.
2.2. Tambak Marginal
Lahan kritis atau sering disebut juga lahan marginal merupakan lahan bermasalah yang dalam pemanfaatanya memerlukan teknologi khusus. Lahan kritis atau marginal menurut istilahnya adalah berhubungan dengan tepi (batas), tidak terlalu menguntungkan, dan berada di pinggir (Yuwono, 2009). Produktivitas lahan kritis sangat ditentukan oleh karakteristik fisik, iklim, tanah, hidrologi dan topografi.
Kualitas air ialah kondisi kalitatif air yang diukur dan atau di uji berdasarkan parameter-parameter tertentu serta metode tertentu berdasarkan peraturan perundang-undangan yang berlaku (Pasal 1 keputusan Menteri Negara Lingkungan Hidup Nomor 115 tahun 2003). Kualitas air dapat dinyatakan dengan parameter kualitas air. Parameter ini meliputi parameter fisik, kimia, dan mikrobiologis(Masduqi,2009).
Kualitas air diketahui dengan melakukan pengujian tertentu terhadap air tersebut. Pengujian yang dilakukan adalah uji kimia, fisik, biologi, atau uji
kenampakan (bau dan warna). Adapun ciri–ciri tambak marginal yaitu produktifitas tambak menjadi rendah, dan mudahnya organisme budidaya terserang penyakit.
2.3. Parameter Kualitas Air 2.3.1. Suhu
Pada umumnya dalam pemeliharaan udang diperlukan suhu pada air media pemeliharaan yang baik karena berkaitan dengan nafsu makan dan proses metabolisme udang. Kondisi tambak dengan mikrolimat yang berfluktuatif akan sangat dipengaruhi oleh air pada media yang ditempati untuk pemeliharaan. contohnya ketika terjadi musim kemarau pada bulan Juli hingga September suhu udara dan air media pemeliharaan udang menjadi sangat rendah (24oC).
Pengaruh angin selatan (musim dingin) mengakibatkan suhu menjadi rendah dan pada musim ini suhu air antara 22-26oC. bagi udang windu suhu di
vawah 26oC akan menjadikan nafsu makan berkurang sedangkan pada jenis udang
putih masih normal antara 24-31oC
faktor yang mempengaruhi temperatur ekosistem air adalah ketinggian geografi, pertukaran panas dengan udara, cahaya matahari, dan vegetasi pohon. faktor anthropogen juga dapat mempengaruhi suhi perairan (faktor yang di akibatkan oleh aktivitas manusia) seperti limbah panas yang berasal dari air pendingin pabrik, penggundulan DAS yang menyebabkan hilangnya perlindungan, sehingga badan air terkena cahaya matahari secara langsung (Efendi H 2003).
tubuh lemah, kurus, dan tingkah laku abnormal. Pada suhu rendah, akibat yang ditimbulkan antara lain ikan menjadi lebih rentan terhadap infeksi fungi dan bakteri patogen akibat melemahnya sistem imun.
Pada dasarnya suhu rendah memungkinkan air mengandung oksigen lebih tinggi, tapi suhu rendah menyebabkan menurunnya laju pernafasan dan denyut jantung sehingga dapat berlanjut dengan pingsannya ikan-ikan akibat kekurangan oksigen (Irianto, 2005).
2.3.2. Salinitas
Salinitas air terdiri dari garam-garam mineral. salinitas adalah tingkat kadar garam yang terlarut dalam air yang sangat bermanfaat bagi kehidupan organisme yang hidup dalam air. kandungan garam tersebut dapat dimanfaatkan oleh organisme tertentu misalnya pada kulit udang untuk mempercepat proses pembentukan kulit.
Salinitas juga dapat memberikan efek buruk bagi organisme tertentu jika melewati batas kemampuan organisme itu. Bagi udang windu batas salinitas yang diperlukan berada pada 5-25 ppt. ketika salinitas lebih tinggi dari kondisi tersebut maka akan sangat merugikan bagi udang windu. misalnya udang windu akan kesulitan untuk berganti kulit, akan mengurangi energi dan nutrisi udang windu hanya untuk beradaptasi, tingginya bakteri, udang windu menjadi lebih sensitif dan mudah stress juga sering mengalami lumutan atau disebut Penyakit seperti SEMBV (white spot)
2.3.3. Tingkat Keasaman (pH)
antara ion H+dan OH-. Semakin tingginya pH maka ion OH+ akan semakin rendah dan ion H+ akan menjadi semakin tinggi. Cairan tersebut ialah cairan alkalis. Sebaliknya, makin banyak H+makin rendah PH dan cairan tersebut bersifat masam. Dalam ekosistem kehidupan tambak Ph antara 7-9 sangat akan sangat ideal. terkadang pH air dapat turun sampai mencapai 4 itu dikarenakan karena keadaan tertentu tambak yang memiliki potensi keasaman air dasar.
Kehidupan jasad renik sangat dipengaruhi oleh kesuburan perairan. Perairan asam akan kurang produktif, malah bisa membunuh hewan budidaya. Jika selera makan berkurang dan aktivitas naik karena komsumsi oksigen yang menurun berarti kandungan oksigen terlarut berkurang biasanya terjadi pada keadaan keasaman yang tinggi dan pH rendah. Hal ini sebaliknya terjadi di suasana basa. Atas dasar ini, maka usaha budidaya perairan dapat berhasil baik dalam air dengan pH 6,5 – 9.0 dan kisaran optimal adalah ph 7,5 – 8,7 ( Kordi dan Andi,2009). Menurut Susana (2009) rendahnya nilai pH mengindikasikan menurunnya kualitas perairan yang pada akhirnya berdampak terhadap kehidupan biota di dalamnya.
2.3.4. Oksigen Terlarut (DO)
Oksigen terlarut dalam air merupakan faktor penting dalam budidaya karena sangat erat hubungannya dengan proses respirasi udang. Kelarutan oksigen dipengaruhi oleh beberapa faktor diantaranya temperatur, salinitas, pH dan bahan organik. Salinitas semakin tinggi, kelarutan oksigen semakin rendah. DO meter adalah alat yang digunakanuntuk mengukur kandungan oksigen terlarut dan suhu pada air kolam (satuan mg/L). (Taufiqull, H. 2016).
bergantung pada kerapatan tumbuhan, jangka waktu, dan intensitas cahaya efektif (Sahami, et al.,2014).
Tabel 2.1. Tingkatan DO Perairan
Range DO Keterangan
<1 ppm Dalam waktu lebih dari 3 jam udang bisa mati
2-4 ppm Pertumbuhan menurun
4-9 ppm Baik untuk pertumbuhan udang > 9 ppm Plankton blooming dan tumbuh pesat.
Sumber : Taufiqull, H. 2016
2.3.5. Amoniak
Ammonia pada air dapat berasal dari pemupukan, eksresi hewan dan hasil perombakan komponen nitrogen oleh mikroba. Beberapa jenis tanaman dapat menyerap ammonia. Bakteri pengurai (nitrobacter) bisa mengoksidasi ammonia menjadi nitrat. Oleh karena itu ammonia bisa menurun konsentrasinya dengan beragam cara. Akan tetapi dengan kepadatan ikan yang tinggi dikolam dan pemberian makanan buatan bisa meningkatkan konsentrasi ammonia.
Bentuk NH3 Ammonia sangat beracun, sedangkan dalam bentuk NH4+ yang sudah terionosasi relatif tidak beracun.
NH3 + H2O —> NH4+ + OH- Pengaruh Ammonia Pada Perairan adalah :
2. Keseimbangan total ammonia nitrogen ialah ammonia (NH3) akan bertambah konsentrasinya bila pH dan temperature nya tinggi. Efek yang paling tinggi adalah pengaruh pH dibandingkan pengaruh temperature. pH 6,8 dan suhu 26° C pada air dan jumlah ammonia nitrogen 2 mg/l akan mengandung ammonia (NH3) 0,12 mg/l yang terjadi karena perkalian antara 2 mg/l dengan 0,006, sedangkan ph 9 dengan suhu 26° C akan mengandung ammonia (NH3) 0,823 mg/l. maka dengan kenaikan pH dapat menyebabkan kenaikan ammonia (NH3).
3. Sifat ammonia (NH3) pada ikan i a l a h dapat meningkatkan konsumsi oksigen dalam jaringan, merusak insang serta mengurangi kemampuan darah untuk mentranportasi oksigen.
4. Konsentrasi ammonia yang bisa membunuh ikan dalam waktu singkat adalah 0,6 – 3,1 mg/l NH3-N untuk semua ikan.
5. Daya racun ammonia akan meningkat bila oksigen turun. Konsentrasi kalsium (Ca) yang tinggi bisa menurunkan daya racun ammonia.
6. Pertumbuhan ikan terhambat jika terjadi akumulasi ammonia pada media pemeliharaan,bahkan bisa menyebabkan keracunan pada ikan.
2.3.6. Nitrit
Nitrit adalah peralihan dari bentuk antara ammonia dan nitrat atau disebut juga nitrifikasi dan peralihan bentuk antara nitrat dengan gas nitrogen atau disebut sebagai denitrifikasi. sifat nitrit sangat tidak stabil jika bersama dengan oksigen. jumlah nitrit sekitar 0,001 mg/l pada perairan alami. jika suatu perairan mengandung nitrit dengan kadar 0,06 mg/L maka perairan tersebut akan bersifat toksik. ketika suatu perairan mengandung nitrit berarti pada perairan tersebut
terjadi proses biologis berupa perombakan bahan organik dengan kadar oksigen terlarut yang rendah (Madigan et al. 2003).
2.3.7. Ortofosfat (PO4)
ortofofat adalah ion poliatomik atau radikal tang terdiri dari satu atom fosforus dan empat oksigen. Dalam bentuk ionik, dia membawa -3 muatan formal, dan dinotasikan PO4. Dalam batuan beku atau sedimen terdapat unsur fosfat dengan beberapa unsur fosfor ekonomis. Ketika terjadi pembentukan magma terdapat mineral apatit, mineral apatit terkandung fosfat apatit.
fosfor merupakan bahan kimia yang sangat dibutuhkan oleh mahluk hidup. fosfor dapat dijumpai dalam dua bentuk yaitu fosfat organik dan fosfat anorganik. fosfat organik dapat ditemukan pada tumbuhan dan hewan sedangkan fosfat anorganik dari air dan tanah dimana fosfat anorganik terlarut pada air dan tanah yang terkikis dan menjadi sedimen karena pengendapan.
keberadaan ortofosfat dapat ditemukan pada air alam dan air limbah sebagai senyawa dalam unsur fosfat. ortofosfat yang ditemukan pada lokasi pertanian itu asalnya dari bahan pupuk yang terlarut ke sungai melalui pengairan. Bahan deterjen yang dipakai penduduk juga mengandung fosfat dan akibat pembuangan limbah bahan deterjen yang mengandung fosfat. ortofosfat yang terlarut dari bakteri ataupun tanaman terbentuk menjadi fosfat organis karena menyerap fosfat untuk proses kehidupan dan pertumbuhan mahluk hidup (Alaerts dan Santika, 1984). Klasifikasi kesuburan perairan berdasarkan konsentrasi fosfat yaitu:
Tabel 2.2. Klasifikasi kesuburan perairan atas dasar konsentrasi fosfat (Hakanson and Bryann, 2008).
2.3.8. Bahan Organik Total BOT)
Bahan organik total air menggambarkan kandungan bahan organik total suatu perairan yang terdiri dari bahan organik yang terdiri dari bahan organik terlarut, tersuspensi, dan koloid. Bahan organik perairan terdapat sebagai plankton, partikel-partikel tersuspensi dari bahan organik yang mengalami perombakan (detritus) dan bahan – bahan organik total yang berasal dari daratan dan terbawa oleh aliran sungai. kandungan bahan organik total dalam air laut biasanyanya rendah dan tidak melebihi 3 mg/L.
Menurut Reid (1961) dalam Pirzan dan Rani (2008) , perairan dengan kandungan bahan organik total diatas 26 mg/L adalah golongan perairan yang subur. Kandungan bahan organik diperairan akan mengalami fluktuasi yang disebabkan bervariasinya jumlah masukan dari organik, pertanian, maupun sumber lainya .kandungan bahan organik dalam perairan akan mengalami peningkatan yang disebabkan buangan dari rumah tangga pertanian, organik, hujan, dan aliran air permukaan .
Pada musim kemarau kandungan bahan organik akan meningkat sehingga akan meningkatkan pula kandungan unsur hara perairan dan sebaliknya pada musim hujan akan terjadi penurunan karena adanya proses pengenceran (wardoyo
NO3 (mg/L air) Tingkat kesuburan (trofik) perairan 0 – 0,11 Rendah (Oligotrofik)
0,11 – 0,29 Cukup (Mesotrofik) 0,29 – 0,94 Baik (Eutrofik)
2.4. Tabel Pengelompokan Tingkat Kesesuaian Tambak
Pengelompokkan tingkat kesesuaian tambak untuk budidaya tambak ditentukan atas nilai kesesuaian lahan yang disesuaikan dengan metode tradisional semiintensif, dan intensif dapat dikelompokkan sebagai berikut (Utojo et al, ,2004).
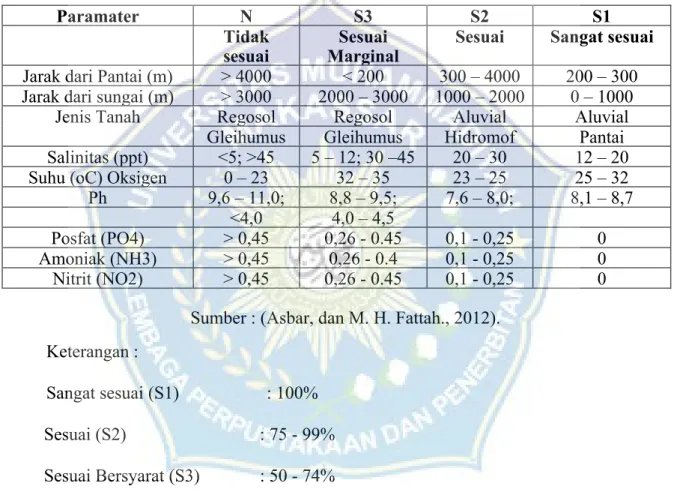
Tabel 2.3. Matriks Kesesuaian Lahan untuk Budidaya Tambak
Paramater N S3 S2 S1
Tidak
sesuai MarginalSesuai Sesuai Sangat sesuai Jarak dari Pantai (m) > 4000 < 200 300 – 4000 200 – 300 Jarak dari sungai (m) > 3000 2000 – 3000 1000 – 2000 0 – 1000
Jenis Tanah Regosol Regosol Aluvial Aluvial
Gleihumus Gleihumus Hidromof Pantai
Salinitas (ppt) <5; >45 5 – 12; 30 –45 20 – 30 12 – 20
Suhu (oC) Oksigen 0 – 23 32 – 35 23 – 25 25 – 32
Ph 9,6 – 11,0; 8,8 – 9,5; 7,6 – 8,0; 8,1 – 8,7
<4,0 4,0 – 4,5
Posfat (PO4) > 0,45 0,26 - 0.45 0,1 - 0,25 0
Amoniak (NH3) > 0,45 0,26 - 0.4 0,1 - 0,25 0
Nitrit (NO2) > 0,45 0,26 - 0.45 0,1 - 0,25 0
Sumber : (Asbar, dan M. H. Fattah., 2012). Keterangan :
Sangat sesuai (S1) : 100% Sesuai (S2) : 75 - 99% Sesuai Bersyarat (S3) : 50 - 74% Tidak Sesuai Permanen (N) : < 50%
III METODE PENELITIAN 3.1. Waktu dan Tempat
Penelitian dilaksanakan pada bulan Juli sampai Agustus 2020, bertempat di Desa Manakku, Kecamatan Labakkang,Kabupaten Pangkajenne dan kepulauan, Provinsi Sulawesi Selatan. Untuk analisis sampel parameter kimia dilakukan di Laboratorium Kualitas Air Balai Riset Perikanan Budidaya Air Payau (BRPBAP) Maros.
3.2.Alat dan Bahan.
Penelitian ini menggunakan alat yaitu buku dan pulpen berfungsi untuk menulis data, kamera untuk mengambil gambar sebagai dokumentasi, turbidimeter untuk mengukur kekeruhan, DO meter untuk mengukur oksigen terlarut, Thermometer untuk mengukur suhu, Salinometer untuk mengukur salinitas, pH meter digunakan untuk mengukur pH, botol sampel sebagai tempat sampel air, secchi diskuntuk mengukur kecerahan, tetra test amonia.
Bahan yang dipakai dalam penelitian ini yaitu alkohol, aquades untuk mensterilkan alat di laboratorium, kertas label untuk penanda sampel, kertas saring sebagai penyaring, dan tisu untuk mengeringkan alat.
3.3. Pengambilan Sampel Air
Data tentang nilai dan konsentrasi setiap parameter kualitas air yang diteliti,didapatkan melalui kegiatan pengambilan sample air dari 3 stasiun antara lain yaitu:
b. Stasiun 2 : Petakan tambak
c. Stasiun 3 : Pintu pengeluaran air (outlet)
Pelaksanaan pengambilan sample air dilakukan pada waktu kurang lebih 3 jam, yaitu dimulai dari pukul 10.00 WITA sampai dengan 12.00 WITA. Air contoh yang akan digunakan untuk menganalisis parameter kualitas air diambil pada bagian tengah kolom perairan. Untuk sampel air yang akan dipergunakan untuk analisis parameter kualitas air di laboratorium dimasukkan ke dalam wadah botol BOD, kemudian ditutup rapat dan dimasukkan ke dalam ice box.
3.4. Analisis Parameter Kualitas Air
Pada penelitian ini parameter kualitas air yang diteliti adalah suhu air, salinitas, pH air, oksigen terlarut, amoniak, nitrit, posfat dan BOT. Analisa dari seluruh parameter kualitas air di atas akan dijelaskan melalui uraian berikut ini
3.4.1 Suhu
Pengukuran nilai suhu air setiap stasiun dilakukan secara in situ dengan menggunakan YSI multiparameter. Alat tersebut dikalibrasi terlebih dahulu hingga kembali ke posisi awal (0) kemudian ukur konsentrasi DO dari sampel dengan mencelupkan batang probe YSI multiparameter kemudian liat skala yang terterah pada layar alat.
3.4.2 Salinitas
mencelupkan batang probe YSI multiparameter kemudian liat skala yang terterah pada layar alat.
3.4.3 Pengukuran pH
Setiap stasiun pH air dari diukur secara in situdengan menggunakan YSI multiparameter. Dilakukan melalui cara mencelupkan batang probe YSI multiparameter kemudian liat skala yang terterah pada layar alat.. Perangkat YSI multiparameter ialah perangkat digital yang dapat mengukur derajat keasaman dari suatu perairan secara otomatis melalui sensor (probe).
3.4.4 Pengukuran Oksigen terlarut (DO)
Pada penelitian ini, oksigen terlarut (DO) konsentrasi oksigen terlarut dari setiap stasiun diukur secara in situ dengan menggunakan alat YSI multiparameter. Dilakukan dengan cara mencelupkan batang probe YSI multiparameter kedalam sampel air. Lalu secara otomatis pada YSI multiparameter dapat terbaca konsentrasi oksigen terlarut pada kolom air tersebut.
3.4.5 Amoniak (NH3)
Menentukan banyaknya konsentrasi total ammonia nitrogen pada air contoh digunakan prinsip spektrofotomerik yang dilakukan di labortorium. Untuk mempermudah terbacanya hasil pada mesin spektrofotometer maka harus menyaring amonia dalam 10 ml air contoh dengan 0,5 ml senyawa fenol serta 0.5 ml sodium nitroprusid selanjutnya dihomogenkan,
kemudian di reaksikan dengan oxidizing reagent sebanyak 1 ml dan lalu homogenkan kembali.
Kemudian tabung reaksi yang digunakan untuk melakukan reaksi tersebut ditutup rapat lalu didiamkan selama satu jam. Setelah itu absorbansi warna air contoh (biru) diukur dengan spektrofotometer pada panjang gelombang 640 nm. Warna biru yang ditimbulkan merupakan akibat terbentuknya senyawa indofenol. Kemudian absorbansi air contoh disesuaikan dengan absorbansi akuades (blanko) serta konstanta perhitungan (Stirling et al., 1985).
3.4.6 Nitrit (NO2-N)
Metode Spektrofotometer dilakukan untuk menentukan kadar nitrit (SNI 06-6989.9-2004). Pada kisaran kadar 0,01 mg/l – 1,0 mg/l. dengan kondisi asam (pH 2-2,5), maka sulfanilamid (SA) dan N-(1-naphthyl) ethylene diamine dihydrochloride (NED dihydrochloride) akan bereaksi dengan nitrit membentuk senyawa azo yang berwarna merah keunguan yang dapat diukur pada panjang gelombang 543 nm.
3.4.7 Ortofosfat (PO4-P)
pengukuran konsentrasi ortofosfat dapat menggunakan prinsip spektrofotomerik yang dilakukan di labortorium. air contoh reaksikan dengan beberapa senyawa kimia yang harus berjalan dibawah pH 8,3 yang diberikan maksimal 2 tetes indikator phenolphthalein sebagai penunjuk pH.
encer sampai warnanya berubah menjadi bening yang menunjukkan bahwa pH < 8,3. kemudian direaksikan dengan 1.6 ml combine reagent yang terdiri atas H2SO4 5 N, potasium antimonil tartat, amonium molibdat, dan
asam askorbat.
Kemudian ditutup rapat lalu didiamkan selama 10 menit. Absorbansi warna air contoh (biru) diukur melalui spektrofotometer pada panjang gelombang 880 nm. Warna biru yang ditimbulkan merupakan akibat terbentuknya senyawa amonium fosfomolibdat tereduksi. Kemudian Absorbansi air contoh disesuaikan absorbansi akuades (blanko) dan konstanta perhitungan (Apha, 1989) .
3.4.8 BOT ( Bahan Organik Total)
Pengambilan sampel untuk mengukur BOT dilakukan dengan mengambil air tambak dimasukkan dalam botol kemudian diberi label dan disimpan ke dalam coolbox selanjutnya di lakukan di laboratorium dengan mengambil sampel air 50 ml yang dimasukkan kedalam tabung erlenmmayer dan dilarutkan 9.5 ml KMnO4 ditambah dengan
menggunakan buret. kemudian dengan menggunakan pipet tets ditambahkan larutan H2SO4 sebanyak 10 ml dan dipanaskan sampai
suhunya mencapai 70-80 0C lalu ditambahkan natrium oksalat 0.01 sampai
suhu menjadi 70 0C dengan perlahan sampai terlihat warna bening pada
Rumus yang digunakan dalam perhitungan BOT (bahan organic total) yaitu (SNI, 2016)
( / ) =(x−y)x 31,6 x 0,01 x 1000
Keterangan :
x = mL KmnO4 untuk sampel
y = mL KMnO4 untuk aquades (larutan blanko)
31,6 = seperlima dari BM KMnO4
mL = volume sampel 0,01 = normalitas KMnO4
1000 = konversi 1 liter air dari mL
Secara ringkas alat serta metode yang digunakan untuk menganalisis parameter kualitas air terkait dapat dilihat pada Tabel 3.1.
Tabel 3.1. Alat serta metode pengukuran parameter kualitas air
Parameter Satuan Alat/Metode Lokasi
Fisika
Suhu 0C YSI Multiparameter In situ
Salinitas Ppt YSI Multiparameter In situ
Kimia
Ph Unit SI YSI Multiparameter In situ
DO Mg/l YSI Multiparameter In situ
Amoniak Mg/l Spektrofotometer Ex situ
Nitrit Mg/l Spektrofotometer Ex situ
3.5. Rancangan Penelitian
Penelitian ini menggunakan metode deskriptif dengan cara mendeskrifsikan sejumlah variabel yang berkenaan dengan masalah yang diteliti antara fenomena yang di uji. Analisis dengan cara deskriptif dilakukan demi menjabarkan nilai atau konsentrasi rata-rata, kisaran serta kondisi-kondisi lain yang mempengaruhi parameter kualitas air.
3.6. Analisis Data
Data parameter fisika, kimia air dianalisis secara deskriptif dan hasil yang di dapatkan distabulasikan menggunakan microsoft excel 2010 dan ditampilkan dalam bentuk table dan grafik.
IV HASIL DAN PEMBAHASAN 4.1. HASIL
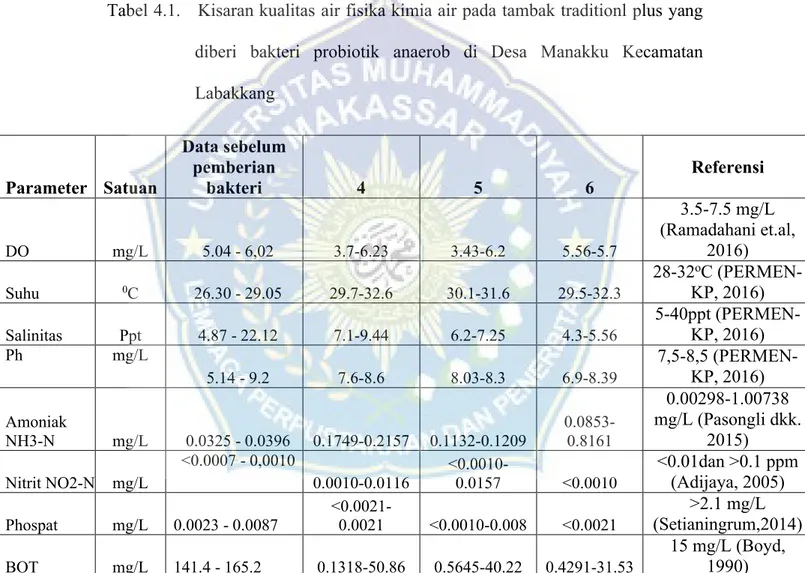
Hasil pengukuran kualitas air fisika kimia air pada tambak traditional plus yang diberi bakteri probiotik anaerob di Desa Manakku Kecamatan Labakkang Kabupaten Pangkajene dan Kepulauan dipaparkan pada Tabel 4.1
Tabel 4.1. Kisaran kualitas air fisika kimia air pada tambak traditionl plus yang diberi bakteri probiotik anaerob di Desa Manakku Kecamatan Labakkang Parameter Satuan Data sebelum pemberian bakteri 4 5 6 Referensi DO mg/L 5.04 - 6,02 3.7-6.23 3.43-6.2 5.56-5.7 3.5-7.5 mg/L (Ramadahani et.al, 2016) Suhu 0C 26.30 - 29.05 29.7-32.6 30.1-31.6 29.5-32.3 28-32oC (PERMEN-KP, 2016) Salinitas Ppt 4.87 - 22.12 7.1-9.44 6.2-7.25 4.3-5.56 5-40ppt (PERMEN-KP, 2016) Ph mg/L 5.14 - 9.2 7.6-8.6 8.03-8.3 6.9-8.39 7,5-8,5 (PERMEN-KP, 2016) Amoniak NH3-N mg/L 0.0325 - 0.0396 0.1749-0.2157 0.1132-0.1209 0.0853-0.8161 0.00298-1.00738 mg/L (Pasongli dkk. 2015) Nitrit NO2-N mg/L <0.0007 - 0,0010 0.0010-0.0116 <0.0010-0.0157 <0.0010 <0.01dan >0.1 ppm (Adijaya, 2005) Phospat mg/L 0.0023 - 0.0087 <0.0021-0.0021 <0.0010-0.008 <0.0021 >2.1 mg/L (Setianingrum,2014) BOT mg/L 141.4 - 165.2 0.1318-50.86 0.5645-40.22 0.4291-31.53 15 mg/L (Boyd, 1990)
4.2.PEMBAHASAN
Parameter Kualitas Air Fisika Kimia
Berdasarkan pengukuran data dilapangan maka diketahui suhu di lokasi penelitian kisaran 26,3 – 28,9 OC. hal tersebut masih berada dalam batas normal,
dimana menurut Perkins kisaran suhu yang dianggap layak bagi kehidupan organisme akuatik ialah 25 – 32 OC. Suhu pada suatu tambak juga dipengaruhi
oleh kondisi musim, diwilayah tambak pendidikan Unismuh dimana bulan juli merupakan musim kemarau. Sehingga suhu ditambak mengalami peningkatan. Peningkatan suhu tertinggi akan menyebabkan berkurangnya jumlah oksigen terlarut dalam air serta akan menimbulkan suasana anoksik di stasiun inlet,tambak dan outlet.
Salinitas mempunyai hubungan erat dengan tekanan osmotik air. Semakin tinggi salinitas air maka semakin tinggi tekanan osmotiknya. Tekanan osmotik inilah yang dapat mempengaruhi kehidupan organisme pada tambak, sebab tekanan osmotic lingkungan perairan akan mempengaruhi tekanan osmotik darah di dalam tubuh ikan (Amanda, 2016) 2007).
Berdasarkan hasil interpolasi titik pengambilan sampel (Inlet, Tambak, Outlet). Tingkat salinitas pada saluran pemasukan lebih tinggi dibandingkan dua stasiun yang lain hal tersebut diduga karena salinitas dipengaruhi oleh pasang surut dan musim dimana pada musim kemarau pada saat aliran air sungai dimuara berkurang air laut dapat masuk lebih jauh kearah darat sehingga salinitas muara akan meningkat dan air dari muara tersebut yang dimasukan kedalam saluran pemasukan.
Sementara nilai salinitas menurun pada stasiun tambak hal dipengaruhi oleh kedalaman dari suatu perairan dimana menurut Efendi (2003) nilai salinitas akan bertambah sesuai dengan makin dalam suatu perairan selain itu salinitas pada stasiun tambak rendah diduga karena blooming klekap pada stasiun tambak yang mengakibatkan intensitas cahaya matahari kurang sehingga tidak terjadi penguapan. Sedangkan pada stasiun pengeluaran salinitas kembali meningkat hal diperkirakan adanya proses penguapan dimana semakin besar penguapan maka salinitas semakin tinggi. Salinitas yang tinggi akan berpengaruh terhadap kinerja pertumbuhan dari organisme budidaya.salah satunya yaitu menghambat proses molting pada udang.
Derajat keasaman ( pH air ) mempengaruhi tingkat kesuburan perairan karena mempengaruhi kehidupan jasad renik. Perairan bersifat asam akan mempengaruhi kehidupan jasad renik. Perairan bersifat asam akan kurang produktif, sehingga dapat membunuh organisme budidaya. Pada pH rendah (asam) effendi (2003) menyatakan bahwa jamur lebih menyukai pH yang rendah (asam), kandungan oksigen terlarut akan kurang. Akibatnya konsumsi oksigen menurun dan aktifitas pernapasan naik, dan selera makan organisme budidaya akan berkurang. Hal sebaliknya terjadi pada suasana basa. (Amanda, 2016).
Berdasarkan data yang diperoleh di tiga stasiun pengambilan sampel di lapangan bisa diketahui pH air di lokasi penelitian berkisar 7,99 – 9,25. Dimana untuk saluran pengeluaran dan pemasukan masih sesuai untuk biota aquatic sedangkan untuk stasiun tambak sudah tidak sesuai untuk budidaya hal tersebut
yang sesuai untuk budidaya antara 6,5 sampai 8,5. Namun bila dilihat secara seksama kondisi pH di stasiun tambak sangat tinggi.
Hal tersebut disebabkan semakin minimnya pasokan air tawar yang masuk seiring semakin berkurangnya tingkat curah hujan dimana menurut Susana faktor yang mempengaruhi peningkatan nilai pH yaitu kurangnya curah hujan dan salinitas yang tinggi.
Oksigen yang larut (Dissolved oxygen) merupakan peubah kualitas air yang paling penting dalam budidaya perikanan. Kelarutan oksigen pada air dipengaruhi oleh peubah lain seperti suhu, salinitas, bahan organik dan kecerahan. Oksigen yang terlalu rendah dapat menghambat pertumbuhan, bahkan membunuh organisme yang dipelihara (Vivi, 2016). Berdasarkan pada pengukuran dilapangan`diketahui DO air pada lokasi penelitian berkisar 2,28 – 5,04 m/gl. Konsentrasi oksigen yang tinggi pada stasiun tambak juga dipengaruhi oleh fakor rendahnya suhu pada stasiun tersebut sehingga kandungan oksigen meningkat.
Rendahnya oksigen terlarut pada saluran pemasukan dan pengeluaran akibat banyaknya bahan organic yang terakumulasi di perairan. Hal tersebut juga diungkapkan melalui Savana dan Stino (2000) dimana kandungan oksigen rendah di perairan dipengaruhi oleh tingginya bahan organik dan laju dekomposisi. Nilai DO yang diperoleh masih mendukung kegiatan budidaya dimana menurut Salmin (2005) dalam keadaan normal dan tidak tercemar oleh senyawa beracun. Komposisi oksigen terlarut sebaiknya tidak bisa kurang dari 1,7 mg/l.
Amonia berasal dari penimbunan limbah kotoran dan sisa pakan yang tidak dikonsumsi. Sebagian besar pakan yang dimakan, selanjutnya dirombak untuk
proses metabolisme sedangkan sisanya dibuang berupa kotoran padat (faeces) dan terlarut (amonia). Konsentrasi ammonia yang tinggi pada stasiun inlet disebabkan oleh ion ammonium tidak bisa mengalami nitrifikasi menjadi nitrat karena tidak tersedianya oksigen yang cukup dimana pada saluran pemasukan nilai oksigen terlarut sebesar 2,28 mg/l. berkurangnya konsentrasi ammonia di stasiun tambak disebabkan oleh terpakainya sejumlah ion ammonium makrofita, pitoplankton serta alga bentik di stasiun tersebut.
Hal ini sesuai dengan pendapat Dodds et all (2002) dimana proses berkurangnya ammonia disuatu perairan dan pemamfaatanya secara langsung oleh biota. Bahkan volatilisasi ammonia bebas sebagai salahsatu senyawa penyusun TAN. Konsentrasi ammonia yang kembali meningkat pada stasiun outlet diduga karena penguraian bahan organik yang mengandung protein dan asam amino secara anaerobik. Bahan organik tersebut berasal dari sisa pakan dan sisa eksresi hewang budidaya yang ikut terbuang selama proses pembuangan lumpur tambak.
Fosfat di stasiun outlet terbentuk dengan proses hidrolisir dari seluruh senyawa fosfat yang terdapat dalam air buangan tambak. Kandungan fosfat pada air limbah tambak berasal dari penguraian bahan organik yang berasal dari sisa pakan yang tidak termakan dan ikut terbuang selama proses pembuangan air dan lumpur dari dalam tambak maupun pergantian air.
Sementara kandungan fosfat pada stasiun inlet cenderung mengalami penurunan disebabkan oleh fosfat tersebut dimanfaatkan oleh fitoplankton,
makrofita, serta bakteri selain itu fospat dapat tersuspensi untuk kemudian mengendap di dasar perairan.
Nitrit merupakan salah satu stressor bagi organisme bubidaya, sehingga keberadaanya yang cukup tinggi di tambak harus diperhatikan , kadar nitrit dalam tambak sebaiknya jangan melebihi 0,05 mg/l kadar nitrit lebih dari 0,05 mg/l bersifat toksit bagi beberapa organisme perairan, kadar nitrit yang tinggi dalam perairan menunjukan sedang terjadi proses perombakan bahan organik yang menggunakan oksigen, sehingga kandungan oksigen terlarut diperairan rendah..
Bahan organik total (BOT) yang diperoleh pada stasiun penelitian berkisar antara 43,13 – 67.57 mg/l. Hal tersebut dapat dijelaskan bahwa pada masa budidaya bahan organik yang terakumulasi berupa sedimen kemungkinan meningkat dengan bertambahbya umur pemeliharaan. Seiring dengan pertumbuhan organisme, maka jumlah pakan semakin bertambah sehingga sisa pakan hasil metabolisme organisme juga bertambah. Selain itu padat penebaran yang tinggi menyebabkan kandungan bahan organik seperti ammoniak yang berasal dari sisa pakan dan ekskresi organisme meningkat. BOT pada tambak dapat memberikan sumber kehidupan bagi jamur (Hariadi,2014).
Adanya BOT pada tambak akan mempengaruhi organisme budidaya sehingga menyebabkan kualitas air menjadi buruk (Suwoyo 2009). Tingginya BOT pada stasiun outlet diduga dari bahan-bahan organic total yang berasal dari daratan dan terbawa oleh aliran sungai. Dan dimasukkan kedalam saluran pemasukan sedangkan BOT pada tambak mengalami penurunan hal tersebut
diduga karena bahan organic diperairan yang berupa plankton dan partikal-partikal tersuspensi mengalami perombakan.
V KESIMPULAN DAN SARAN 5.1 Kesimpulan
Berdasarkan hasil penelitian menunjukkan bahwa sebelum pemberian bakteri, kualitas air tidak memenuhi syarat tapi setelah pemberian bakteri Anaerob, terdapat perubahan beberapa pamareter yang diamati mengalami perubahan kualitas air yang positif sesuai dengan kisaran budidaya pada organisme Udang vaname.
5.2 Saran
Peneltian ini diharapkan dapat memberikan rujukan baru dalam memahami pemberian bakteri Anaerob di tambak pendidikan Unismuh Makassar. Penelitian ini mestinya dilakukan secara mendalam lagi sebab, pemilik lahan marginal akan dapat merasakan secara nyata dari hasil penelitian ini yang telah melalui prosedur ilmiah.
DAFTAR PUSTAKA
Alaerts G, Sartika S 1987. Metode Penelitian Air. Usaha Nasional Surabaya APHA (American Public Health Association). 1989. Standard Methods for The Examination of Water and Wastewater 17th ed APHA, AWWA (American Water Work Association) and WPCF (Water Pollution Control Federation). Washington D.C.
Andayani, S. 2005. Manajemen Kualitas Air Untuk Budidaya Perairan . Universitas Brawijaya: Malang.
Amri, K., 2003. Budi Daya Udang Windu Secara Intensif. Kiat Mengatasi Permasalahan Praktis. Teknik Mempersiapkan Benur Membesarkan sampai Panen dengan Orientasi dengan Daya Dukung Lahan dan Kualitas Produksi:Agromedia Pustaka. Jakarta Selatan.
Amanda Lita. 2016. Evaluasi Kesesuaian Lahan Tambak Untuk Budidaya Asbar, dan M. H. Fattah., 2012. Model Pengembangan Teknologi Produksi Tambak Marjinal dan Terlantar pada Sentra Produksi Udang Windu (Penaeus monodon) di Sulawesi Selatan. Usul Penelitian. Penelitian Tim Pascasarjana. Universitas Muslim Indonesia. Makassar.
Boyd CE. 2004. Farm Level Issues in aquaculture certification: tilapia WWF-US. Auburn Alabama. Ditjenkanbud, 2006. Profil Rumput Laut Indonesia Direktorat Jenderal Perikanan Budidaya Departemen Perikanan dan Kelautan, Jakarta.
Effendi, H 2000. Telaah Kualitas Air. Manajemen Sumber Daya Perairan. Fakultas Perikanan dan Ilmu Kelautan. Institute Pertanian Bogor. Bogor Efendi, H. 2003. Telaah Kualitas Air. Kansius. Yogyakarta.
Feriningtyas, D. 2005. Perubahan Spasial dan Temporal Kualitas Air Waduk Cirata, Jawa Barat Selama Periode 2000-2004. Skripsi. Departemen Manajemen
Sumberdaya Perairan. Fakultas Perikanan dan Ilmu Kelautan. Institut Pertanian Bogor.
Hadinafta, R. 2009 Analisis Kebutuhan Oksigen untuk Dekomposisi Bahan Organik pada Lapisan Dasar Perairan Estuari Sungai Cisadane, Tangerang. Skripsi. Fakultas Perikanan dan Ilmu Kelautan, Institut Pertanian Bogor..
Hariadi, W. M. 2014. Ekspolarasi bakteri dan jamur tanah pada pertanian padi (Oryza sativa) organic dan konvensional pada inpectisol lawing. Skripsi Fakultas Pertanian, Universitas Brawijaya, Malang.
Hakanson. L & A.C. Bryhn, 2008. Eutrophication in the Baltic Sea Present
Situation, Nutrien Transport processes, Remedial Strategies. Springer – Verlag Berlin Heidelberg.. Harjiwigeno, S. 2010. Ilmu tanah . Akademika presindo. Jakarta.
Hutagalung H. P. dan A. Rozak, (1997) Penentuan Kadar Nitrat. Metode Analisis Air Laut, Sedimen dan Biota H. P. Hutagalung, D Setiapermana dan S. H Riyano (editor), pusat penelitian dan pengembangan Oceonologi. LIPI , Jakarta.
Kordi K Ghufron dan Andi Baso Tancung 2009. Pengelolaan kualitas air dalam Budidaya perairan:Rineka Cipta Jakarta.
Laili, A. N. 2004. Studi Kesesuaian Lahan Tambak dengan Memanfaatkan Teknologi Penginderaan Jauh dan Sistem Informasi Geografis di Kabupaten Lampung Timur. Skripsi. Program Studi Ilmu Kelautan. Departemen Ilmu dan Teknologi Kelautan. Fakultas Perikanan dan Ilmu Kelautan. Institut Pertanian Bogor..
Masduqi, A dan A. Slamet. 2009. Satuan Operasi Untuk Pengolahan Air Surabaya: Jurusan Tekni Lingkungan FTSPITS Maladi, Irham, dkk.(2013). Analisis Uji Fisik Amonia (NH3), Nitrit (NO2), penentuan kadar besi (FE) mangan (Mn) clorin (cl) dalam sampel air minum Nestle dan Cleo UIN Syrif Hidayatullah. Jakarta.
Pirzan AM, dan Rani P. 2008. Hubungan Keragaman Fitoplankton dengan Kualitas Air di Lokasi Pulau Bauluang, Kabupaten Takalar Sulawesi Selatan. Biodiversitas Vol 9 nomor 3 :
Poernomo, A. 1988. Pembuatan Tambak Udang di Indonesia. Seri Pengembangan No. 7, 1988. Departemen Pertanian. Badan Penelitian dan Pengembangan Pertanian.Purnamawati. 2002. Peranan Kualitas Air Terhadap Keberrhasilan Budidaya Ikan di Kolam. Warta Penelitian Perikanan Indonesia 8 (1)
R Duhari. dkk. 2004. Pengelolaan Sumber Daya Lautan dan Pesisir secara terpadu :PT perdaya Permata Jakarta
Reid, G.K. 1961. Ecology Inland Water Estuaria. New York: Reinhold Published Co.Sahami, F. M., Hamzah, S. N., Panigoro, C. dan Hasim. 2014. Lingkungan Perairan dan Perairan Produktivitasnya. Deepublish, Yogyakarta.
Standar Nasional Indonesia (SNI) 03-1990-2016. Bidang Pekerjaan Umum Mengenai Kualitas Air. Departemen Pekerjaan Umum , Bogor.
Susana, T. 2009. Tingkat Keasaman (pH) dan Oksigen Terlarut dan Indikator Kualitas Perairan Sekitar Muara Sungai Cisadane. Jurnal Teknologi Lingkungan. Vol.5 [2]
Suwoyo, Hidayat S. 2009. Tingkat Konsumsi Oksigen Sedimen pada Dasar Tambak Intensif Udang Vanname (lithopenaus vannamei). Sekolah Pascasarjana Institut Pertanian Bogor . Bogor.
Taufiqull, H. 2016. Kadar dan kelarutan oksigen. https://www.tneutron.nest/ blog/kadar-dan-kelarutan-oksigen/. [Diakses tanggal 25 September 2020].
Utojo, A. Mansyur, Rahmansyah, Hasnawi. 2004. Identifikasi Kelayakan budidaya rumput laut di kota baru, Kalimantan Selatan. Jurnal Riset Aquakultur ,1 (3) : 303 – 318
Vivi Dwi Lestari. 2016. Evaluasi kesesuaian Lahan untuk Budidaya Ikan Bandeng di Lahan Bonorowo Kecamatan Kalitengah, Kabupaten Lamongan. Jurnal Geografi : Swara Bhumi Volume 01 Nomor 01 Tahun 2016 Yuwono T.,2009, Biologi molecular mikrobiologi Fakultas Pertanian Universitas
RIWAYAT HIDUP
Penulis dilahirkan di Majene pada tanggal 14 April 1996, sebagai anak keetiga dari lima bersaudara dari pasangan Sugiono dan Hasriani. Penulis menyelesaikan pendidikan sekolah dasar (SD) pada tahun 2007 di SDN 3 Somba setelah tamat SD penulis melanjutkan ke sekolah MTS DDI Somba pada tahun 2007 diselesaikan pada tahun 2010, pada tahun yang sama penulis masuk ke sekolah manengah atas (SMA) di SMAN 1 Sendana pada tahun 2014 penulis diterima sebagai mahasiswa program studi Budidaya Perairan, Fakultas Pertanian, Universitas Muhammadiyah Makassar melalui jalur tes.
Selama kuliah penulis pernah magang di Balai Beni Ikan Poniang Kecamatan Sendana Kabupaten Majene. Penulis dapat menyelesaikan tugas akhir berupa skripsi yang berjudul “Kajian kualitas air pada tambak tradisional plus yang diberi bakteri Anaeerob di Desa Manakku Kecamatan Labakkang Kabupaten Pangkajene dan Kepulauan” dibawah bimbingan Dr. Murni, S.Pi., M.Si, dan Asni Anwar S.Pi.,M.Si.