ISOLASI DAN IDENTIFIKASI AGLIKON SAPONIN KECAMBAH KACANG HIJAU (Phaseolus radiatus L.)
SKRIPSI
Diajukan untuk Memenuhi Salah Satu Syarat Memperoleh Gelar Sarjana Farmasi (S.Farm.)
Program Studi Ilmu Farmasi
Oleh : Yohana Octaviani NIM : 038114013
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2009
ii
iii
HALAMAN PERSEMBAHAN
Aku memulai segalanya dengan pikiranku Mengerjakannya dengan tanganku
Hanya berhenti sejenak untuk melepas lelah Dan akhirnya…
Menyelesaikan segala sesuatunya dengan hasil yang sangat memuaskan
Aku melakukan pekerjaan-pekerjaan besar
Membuat aku begitu bangga menjadi diriku sendiri
Dengan demikian aku menjadi besar
Bahkan lebih besar dari apa yang selama ini aku mimpikan Dan tak sekalipun aku menahan hatiku dari sukacita apapun Sebab hatiku bersukacita karena segala jerih payahku
Dan ketika aku merenungkan segalanya Melihat kembali apa yang telah aku lakukan Sesungguhnya aku bertanya pada diriku sendiri Apa yang menjadi tujuan hidupku
Karena ternyata segala sesuatu adalah kesia-siaan dan usaha menjaring angin
Dan inilah yang bukan menjadi kesia-siaan
Mempersembahkan karya termegahku untukMu, BAPA Karena menyenangkanMu adalah kerinduan hatiku
(Pengkotbah 2:1-26)
Karya ini kupersembahkan untuk TUHAN YESUS, Bapa dan Rajaku
PAPA & MAMA, penyalur berkat terbesar dari Bapa ANGGI, ANGGA, ANGELIA, adik-adikku yang menjadi
penyemangat hidupku
BENNY, yang selalu mendampingiku dalam segala keadaanku dan ALMAMATERKU
GBU...GBU...GBU...GBU...GBU...GBU...GBU...GBU...GBU...GBU...GBU...GBU...GBU...GBU...GBU
iv
v
KATA PENGANTAR
Puji dan syukur penulis panjatkan kepada Tuhan Yang Maha Esa atas segala berkat dan pertolongan-Nya sehingga penulis dapat menyelesaikan skripsi yang berjudul Isolasi dan Identifikasi Aglikon Saponin Kecambah Kacang Hijau (Phaseolus radiatus L.). Skripsi ini disusun sebagai salah satu syarat untuk memperoleh gelar Sarjana Farmasi di Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
Dalam penelitian dan penyusunan skripsi ini tentunya tidak terlepas dari bantuan berbagai pihak. Oleh karena itu, dalam kesempatan ini penulis ingin mengucapkan terima kasih yang sebesar-besarnya kepada :
1. Ibu Rita Suhadi, M.Si., Apt. selaku Dekan Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta.
2. Bapak Yohanes Dwiatmaka, M. Si. selaku dosen pembimbing atas
kesediaannya membimbing, mengoreksi, dan memberi saran selama persiapan usulan penelitian, pelaksanaan penelitian, sampai selesainya penyusunan skripsi ini.
3. Ibu Erna Tri Wulandari, M. Si., Apt. selaku dosen penguji yang telah
memberikan masukan dan saran dalam penyusunan skripsi ini.
4. Ibu Lucia Wiwid Wijayanti, M. Si. selaku dosen penguji yang telah
memberikan masukan dan saran dalam penyusunan skripsi ini.
5. Bapak Ign. Kristio Budiasmoro, M. Si. yang telah membantu penulis dalam
mendeterminasi tanaman.
vi
6. Ibu Christine Patramurti, M. Si., Apt. yang telah memberikan saran dan bantuan sehingga penulis bisa menyelesaikan skripsi ini.
7. Papa dan mama serta adik-adikku Anggi, Angga, Angelia, untuk semua
dukungan dan doa, juga khususnya untuk bantuan dalam materi dan dalam memperoleh bahan-bahan penelitian. I love U.
8. Benny, terima kasih untuk doa dan semangat yang diberikan, kebersamaan
yang indah, kotbah-kotbah yang membangun kehidupan rohaniku, dan kasih yang nyata. Terima kasih karena mengajariku banyak hal dalam memaknai hidupku.
9. Mas Wagiran, Sigit, Andri, Sarwanto, Ottok, Parlan, Kunto, Iswanto, Bapak
Mukmin. Terima kasih atas bantuan yang diberikan.
10.Dita, teman seperjuanganku dalam menyelesikan skripsi ini. Terima kasih
untuk kerjasamanya.
11.Shyu dan Adhy. Terima kasih untuk persahabatan yang indah.
12.Teman-teman farmasi khususnya Nia, Nenes, Ci Prima, Mba Ayu, terima
kasih atas setiap bantuan dan semangatnya.
13.Pdt. Sarah Anthony selaku gembala GSJA Filipi Klaten dan Bapak Ev. Daniel Yohanes, terima kasih atas doanya.
14.Teman-teman kos Dewi, persekutuan Gospel, GSJA Filipi Klaten, GKM-IBS,
komsel ’Be-Bless’, dan komsel Rajawali. Terima kasih untuk setiap doa, bantuan, kepedulian, dan semangat yang diberikan kepada penulis.
15.Bapak Rudy Gunawan, DDD selaku dosen di GKM-IBS dan Ibu Renny.
Terima kasih atas semangat yang diberikan.
vii
16.Pihak lain yang tidak dapat disebutkan satu persatu oleh penulis.
Penulis menyadari sepenuhnya bahwa penyusunan skripsi ini masih jauh dari sempurna. Maka dari itu, penulis dengan senang hati menerima segala saran maupun kritik yang bersifat membangun, yang dapat membantu skripsi ini agar dapat menjadi lebih sempurna dan berguna. Akhir kata semoga skripsi ini dapat memberi manfaat bagi pembacanya dan bagi perkembangan ilmu pengetahuan terutama di bidang kefarmasian.
Yogyakarta, 4 Mei 2009 Penulis
viii
ix
INTISARI
Saponin merupakan salah satu senyawa kimia yang terkandung dalam
biji kacang hijau (Phaseolus radiatus L.) dan kadarnya meningkat ketika
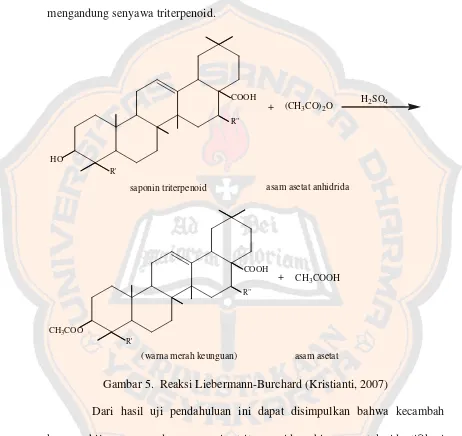
berkecambah. Bila dihidrolisis dengan asam, saponin akan menghasilkan aglikon (sapogenin). Berdasarkan aglikonnya, saponin dibedakan menjadi saponin steroid dan triterpenoid. Saponin steroid digunakan sebagai senyawa awal untuk sintesis beberapa bahan seperti hormon seks, kortison, vitamin D, dan glikosida jantung. Sedangkan saponin triterpenoid sering dimanfaatkan sebagai ekspektoran dan antiinflamasi. Penentuan tipe saponin berguna untuk pemanfaatan selanjutnya dari tanaman yang mengandung tipe saponin tersebut. Penelitian ini bertujuan mengetahui tipe aglikon saponin dalam kecambah kacang hijau beserta karakternya secara KLT dan spektrofotometri UV.
Jenis penelitian yang digunakan adalah penelitian noneksperimental dengan cara analisis deskriptif komparatif. Sebagai pembanding digunakan Succus Liquiritiae. Uji pendahuluan saponin dilakukan dengan uji buih dan reaksi warna Liebermann-Burchard. Saponin dihidrolisis menjadi aglikonnya dan diisolasi dengan metode KLT preparatif, kemudian dilakukan uji kemurnian secara KLT multi-eluen untuk mendapatkan karakter aglikon saponin berupa warna bercak dan harga Rf. Selanjutnya, dilakukan karakterisasi aglikon saponin dengan spektrofotometri UV.
Hasil penelitian menunjukkan bahwa kecambah kacang hijau mengandung saponin triterpenoid. Isolasi dengan KLT preparatif menghasilkan isolat yang murni secara KLT. Dengan analisis KLT, isolat tersebut tampak sebagai bercak ungu pada deteksi dengan sinar UV 254 nm dan biru dengan deteksi anisaldehid-asam sulfat. Hasil spektrofotometri UV menunjukkan puncak tunggal isolat aglikon saponin kecambah kacang hijau dengan λmax 280,4 nm.
Kata kunci : aglikon saponin, triterpenoid, kecambah, Phaseolus radiatus L., KLT, KLT preparatif, spektrofotometri UV
x
ABSTRACT
Saponin is one of the chemical substance in mungbean (Phaseolus
radiatus L.) and its concentration promotes up in the sprout-shape. Saponins are hydrolized by acids to give an aglycone (sapogenin). Saponin are divided into two types according to the aglycone, they are steroidal and triterpenoid types. Steroidal saponins are used as starting materials for the synthesis of such compounds as the sex hormones, cortisone, vitamin D, and the cardiac glycosides. Meanwhile the triterpenoid saponins are generally used for expectorant and antiinflamation. Knowing the type of saponin is very useful for the next preparation of the plants that include the type of the saponin. The purposes of this research are to knowing the type of saponin of mungbean sprouts and their characterization based on Thin Layer Chromatography and UV spectrophotometry.
This was a non-experimental research using comparative descriptive analysis. Succus Liquritiae is used as standard. Saponin was tested with foam test and Liebermann-Burchard reaction. Saponin was hydrolized to produce its aglycone. The isolation was done through preparative TLC method. Purity test was done using multi-eluen TLC to get characters of saponin aglycone, included spot colour and Rf value. Then, characterization was done through UV spectrophotometry.
Based on the research, indicate that mungbean sprout contained triterpenoid saponin. Isolation using TLC preparative gave pure triterpenoid saponin isolate by TLC multi-eluen. Using TLC analysis, the isolate seemed like a violet spot by UV 254 nm detection and blue spot by reaction with anisaldehide-sulphuric acid. The result of UV spectrophotometry showed only one peak of isolate saponin aglycone mungbean sprout with λmax 280,4 nm.
Key words : saponin aglycone, triterpenoid, sprout, Phaseolus radiatus L., TLC, PTLC, UV spectrophotometry
xi
DAFTAR ISI
Halaman
HALAMAN JUDUL... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN... iii
HALAMAN PERSEMBAHAN ... iv
PERNYATAAN PERSETUJUAN PUBLIKASI KARYA ILMIAH UNTUK KEPENTINGAN AKADEMIS ... v
KATA PENGANTAR ... vi
PERNYATAAN KEASLIAN KARYA ... ix
INTISARI . ... x
ABSTRACT... xi
DAFTAR ISI... xii
DAFTAR TABEL... xvi
DAFTAR GAMBAR ... xvii
DAFTAR LAMPIRAN... xviii
BAB I . PENGANTAR... 1
A. Latar Belakang... 1
1. Permasalahan ... 2
2. Keaslian penelitian... 3
3. Manfaat penelitian... 3
B. Tujuan Penelitian... 3
BAB II PENELAAHAN PUSTAKA... 4
A. Kacang hijau... 4
xii
1. Keterangan botani... 4
F. Kromatografi Lapis Tipis (KLT) dan Kromatografi Lapis Tipis Preparatif (KLTP)... 11
G. Spektrofotometri Ultraviolet... 12
H. Keterangan Empiris... 16
BAB III METODE PENELITIAN... 17
A. Jenis dan Rancangan Penelitian... 17
B. Definisi Operasional... 17
C. Bahan dan Alat penelitian... 18
D. Jalan Penelitian... 19
1. Determinasi tanaman... 19
2. Pengumpulan bahan dan proses perkecambahan... 19
3. Pemeriksaan organoleptik dan makroskopik... 19
4. Uji saponin... 19
5. Hidrolisis saponin kecambah kacang hijaudan
xiii
Succus Liquiritiae ……… 20
6. Ekstraksi aglikon saponin kecambah kacang hijau dan Succus Liquiritiae... 20
7. Pemeriksaan pendahuluan aglikon saponin dengan KLT... 21
8. Isolasi aglikon saponin dengan KLT preparatif... 21
9. Uji kemurnian dengan KLT multi-eluen... 22
10.Spektrofotometri Ultra Violet (UV)... 22
E. Tata Cara Analisis Hasil... 23
BAB IV. HASIL DAN PEMBAHASAN... 24
A. Determinasi Tanaman... 24
B. Pengumpulan Bahan dan Proses Perkecambahan... 24
C. Hasil Pemeriksaan Organoleptik dan Makroskopik... 25
D. Uji Saponin... 26
E. Hidrolisis Saponin Kecambah Kacang Hijau dan Succus Liquiritiae... 29
F. Ekstraksi Aglikon Saponin Kecambah Kacang Hijau dan Succus Liquiritiae... 30
G. Pemeriksaan Pendahuluan Aglikon Saponin dengan KLT... 31
H. Isolasi Aglikon Saponin dengan KLT Preparatif... 36
I. Uji Kemurnian dengan KLT multi-eluen... 37
J. Spektrofotometri Ultra Violet (UV)... 43
BAB V. KESIMPULAN DAN SARAN... 46
xiv
A. Kesimpulan... 46
B. Saran... 46
DAFTAR PUSTAKA... 47
LAMPIRAN... 49
BIOGRAFI PENULIS... 55
xv
DAFTAR TABEL
Tabel I. Hasil kromatogram KLT pendahuluan... 33
Tabel II. Hasil kromatogram uji kemurnian dengan
KLT multi-eluen ... 38
xvi
DAFTAR GAMBAR
Gambar 1. Struktur kimia dua macam golongan saponin... 8 Gambar 2. Diagram spektrofotometer ... 15 Gambar 3. Gugus hidrofilik dan lipofilik pada saponin... 26 Gambar 4. Adsorpsi molekul-molekul saponin pada antarmuka
air-udara ... 27 Gambar 5. Reaksi Liebermann-Burchard ... 28 Gambar 6. Mekanisme hidrolisis Succus Liquiritiae dalam
suasana asam ... 30 Gambar 7. Hasil kromatogram KLT pendahuluan... 32
Gambar 8. Reaksi antara saponin triterpenoid dengan deteksi
anisaldehida-asam sulfat ... 35 Gambar 9. Hasil kromatogram KLT multi-eluen dengan fase gerak
kloroform – metanol (95:5 v/v)... 39 Gambar 10. Hasil kromatogram KLT multi-eluen dengan fase gerak
kloroform – metanol – air (64:50:10 v/v) ... 40 Gambar 11. Hasil kromatogram KLT multi-eluen dengan fase gerak
n-butanol – etanol – air (7:2:5 v/v) ... 41
Gambar 12. Spektra aglikon saponin kecambah kacang hijau (sampel) 45
Gambar 13. Spektra saponin Succus Liquiritiae (pembanding) ... 45
xvii
DAFTAR LAMPIRAN
Lampiran 1. Surat pengesahan determinasi ... 49
Lampiran 2. Sertifikat analisis Succus Liquiritiae... 50
Lampiran 3. Foto biji dan kecambah kacang hijau... 51
Lampiran 4. Foto uji saponin... 52
Lampiran 5. Foto alat hidrolisis ... 53
Lampiran 6. Foto alat menyaring isolat... 54
xviii
BAB I PENGANTAR
A.Latar Belakang
Hampir semua tumbuhan memiliki khasiat dalam hubungannya dengan
kesehatan. Dasar inilah yang membuat penelitian tentang tumbuhan berkembang
pesat. Lebih jauh lagi, penelitian selanjutnya bukan hanya untuk mengetahui efek
kesehatan dari suatu tumbuhan, tetapi juga untuk mengetahui senyawa kimia apa
sajakah yang dapat memberikan efek kesehatan bagi manusia. Salah satu dari
senyawa kimia ini adalah saponin.
Pada dasarnya, pencarian saponin dalam tumbuhan didasari atas
kebutuhan akan sumber sapogenin (aglikon saponin). Saponin dengan aglikon
triterpenoid banyak dimanfaatkan sebagai ekspektoran dan antiinflamasi
(Bruneton, 1999), sedangkan saponin dengan aglikon steroid sangat penting
dalam sintesis bahan-bahan seperti hormon seks, kortison, vitamin D, dan
glikosida jantung (Evans, 2002).
Salah satu sumber saponin adalah biji kacang hijau. Bila biji kacang
hijau ini dikecambahkan, kadar saponinnya akan meningkat sekitar 450%. Selain
dapat membangkitkan sistem kekebalan tubuh, saponin dalam kecambah juga
dapat menurunkan kadar lemak LDL (Low Density Lipoprotein) tanpa
mengganggu kadar lemak HDL (High Density Lipoprotein) (Anonim, 2007). LDL
bersifat atherogenik (dapat memicu atherosklerosis atau pengerasan pembuluh
darah akibat penimbunan lemak) sedangkan HDL bersifat anti atherogenik
1
2
(mengangkut kolesterol kembali ke hati untuk dikatabolisme sehingga
mengurangi simpanan kolesterol). Kadar LDL normal adalah < 130 mg/dl,
sedangkan kadar HDL normal adalah > 40 mg/dl. Di Indonesia, kecambah
merupakan bahan pangan yang cukup dikenal dan memiliki harga yang
terjangkau. Kecambah atau tauge ini merupakan salah satu sayuran dalam
masakan soto dan rawon.
Penentuan tipe saponin berguna untuk pemanfaatan selanjutnya dari
tanaman yang mengandung saponin tersebut. Setelah diketahui tipe saponin dan
karakter aglikon saponin dari kecambah kacang hijau, diharapkan selanjutnya
dapat diketahui secara pasti struktur saponin pada kecambah kacang hijau dan
pemanfaatan selanjutnya saponin kecambah kacang hijau tersebut sebagai obat
untuk menurunkan kolesterol dan membangkitkan sistem kekebalan tubuh.
Untuk mengetahui dan lebih mendalami tentang saponin kecambah
kacang hijau maka dilakukan penelitian mengenai isolasi aglikon saponin
kecambah kacang hijau (Phaseolus radiatus L.) secara kromatografi lapis tipis
preparatif (KLTP) dan identifikasinya secara kromatografi lapis tipis (KLT) dan
spektrofotometri ultraviolet (UV).
1. Permasalahan
Berdasarkan latar belakang di atas, timbul permasalahan untuk
diteliti, yaitu :
1. Tipe saponin apakah yang terdapat dalam kecambah kacang hijau?
2. Bagaimana karakter aglikon saponin kecambah kacang hijau secara KLT
dan spektrofotometri UV?
3
2. Keaslian penelitian
Sejauh penelusuran pustaka yang dilakukan penulis, penelitian
mengenai isolasi dan identifikasi aglikon saponin kecambah kacang hijau serta
karakternya secara KLT dan spektrofotometri UV belum pernah dilakukan.
3. Manfaat penelitian
a. Manfaat teoritis
Penelitian ini diharapkan dapat bermanfaat dalam pengembangan
ilmu kefarmasian khususnya tentang tipe saponin kecambah kacang hijau.
b. Manfaat praktis
Penelitian ini diharapkan dapat melengkapi informasi mengenai
tipe saponin kecambah kacang hijau dan karakternya secara KLT dan
spektrofotometri UV serta memberikan informasi sumber saponin dari
bahan pangan.
B. Tujuan Penelitian 1. Tujuan umum
Penelitian ini secara umum bertujuan untuk lebih mendalami
pengetahuan tentang kecambah kacang hijau.
2. Tujuan khusus
Penelitian ini secara khusus bertujuan untuk mengetahui tipe saponin
kecambah kacang hijau dan karakter aglikon saponin pada kecambah kacang
hijau secara KLT dan spektrofotometri UV.
BAB II
PENELAAHAN PUSTAKA
A. Kacang Hijau 1. Keterangan botani
Kacang hijau memiliki nama ilmiah Phaseolus radiatus L. dan
termasuk suku Papilionaceae (Marzuki dan Soeprapto, 2005). 2. Nama daerah
Kacang hijau dikenal dengan berbagai macam nama, antara lain : Sumatera : kacang padi, retak – hijo, retik – ritak
Jawa : kacang ijo, kacang hejo, kacang herang
Sulawesi : tamul, tambul, bue kope, hue moidono, tibuang kopek
Maluku : bua, hue elo, temelo, tamelo, bora, tangun, kalebu, pue mepim (Anonim, 1995) 3. Deskripsi
Tanaman kacang hijau berbatang tegak dengan ketinggian sangat bervariasi, antara 30-60 cm, tergantung varietasnya. Cabangnya menyamping pada batang utama, berbentuk bulat, dan berbulu. Warna batang dan cabangnya ada yang hijau ada juga yang ungu.
Daunnya trifoliat (terdiri dari tiga helaian) dan letaknya berseling. Tangkai daunnya cukup panjang, lebih panjang dari helaian daunnya. Warna daunnya hijau muda sampai hijau tua.
4
5
Bunganya berwarna kuning, tersusun dalam tandan, keluar pada cabang serta batang dan dapat menyerbuk sendiri. Polong berbentuk silindris dengan panjang antara 6-15 cm dan biasanya berbulu pendek. Sewaktu muda polong berwarna hijau dan setelah tua berwarna hitam atau coklat.
Bijinya lebih kecil dibandingkan biji kacang-kacangan lain. Warna bijinya kebanyakan hijau kusam atau hijau mengkilap, beberapa ada yang berwarna kuning, coklat, dan hitam. Tanaman kacang hijau berakar tunggang dengan akar cabang pada permukaan (Marzuki dan Soeprapto, 2005).
4. Khasiat
Kacang hijau berkhasiat sebagai obat beri-beri, demam nifas, pelancar air seni dan buang air besar, jantung lemah, dan kurang darah (Anonim, 1995; Anonim, 2007)
5. Kandungan kimia
Biji kacang hijau mengandung sterol/ terpen, saponin, protein, lemak, karbohidrat, kalsium, fosfor, besi, vitamin A, vitamin B1, vitamin C (Anonim, 1995).
B. Kecambah
Kecambah merupakan tumbuhan kecil yang baru tumbuh dari biji dan
masih hidup dari persediaan makanan yang terdapat dalam biji (Tjitrosoepomo, 2003).
6
Menurut Sutopo (1985), ada 5 tahap proses perkecambahan, yaitu : 1. proses penyerapan air oleh biji, melunaknya kulit biji, dan hidrasi dari
protoplasma.
2. adanya kegiatan-kegiatan sel dan enzim-enzim serta naiknya tingkat respirasi biji.
3. penguraian bahan-bahan seperti karbohidrat, lemak, dan protein menjadi bentuk-bentuk yang melarut dan ditranslokasikan ke titik-titik tumbuh.
4. asimilasi bahan-bahan tadi di daerah meristematik untuk menghasilkan energi untuk kegiatan pembentukan komponen dan pertumbuhan sel-sel baru.
5. pertumbuhan kecambah melalui proses pembelahan, pembesaran, dan pembagian sel-sel pada titik-titik tumbuh.
Faktor-faktor yang mempengaruhi perkecambahan dibedakan menjadi 2, yaitu :
1. Faktor dalam, yang meliputi tingkat kemasakan biji, ukuran biji, dormansi, dan zat-zat penghambat perkecambahan
2. Faktor luar, yang meliputi air, temperatur, oksigen, cahaya, dan medium (Sutopo, 1985)
Ketika biji-bijian dan kacang-kacangan dikecambahkan, secara umum kadar saponinnya menanjak 450%. Saponin dalam kecambah akan menurunkan LDL tanpa mengganggu kandungan HDL. Setelah melalui sejumlah percobaan pada binatang, saponin kecambah diketahui dapat membangkitkan sistem kekebalan tubuh, dengan cara menaikkan aktivitas sel pembunuh alami (natural killer cells), khususnya sel T-limfosit dan interferon (Anonim, 2006).
7
Manfaat kecambah bagi kesehatan antara lain mencegah kanker, mencegah serangan jantung dan stroke, mencegah osteoporosis, membangkitkan sistem kekebalan tubuh, menjaga keasaman lambung dan memperlancar pencernaan, membantu meningkatkan kesuburan, dan juga baik untuk kecantikan (Anonim, 2005).
C. Succus Liquiritiae
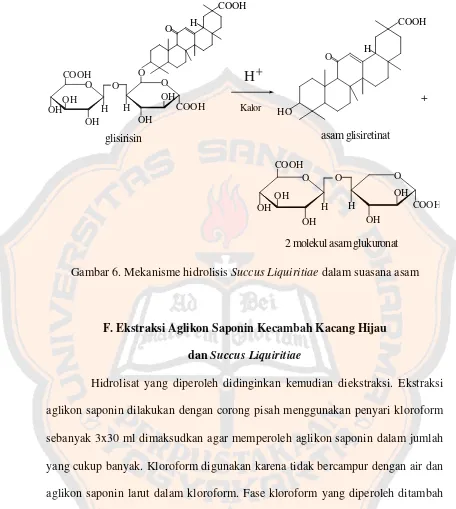
Succus Liquiritiae merupakan ekstrak dari Liquiritiae Radix. Liquiritiae Radix (Glycyrrhiza, Licorice root, akar kayu manis cina) berasal dari sari akar Glycyrrhiza glabra L. yang dikeringkan (Anonim, 1965). Liquiritiae Radix mengandung glikosida saponin, yaitu glisirisin (asam glisirizinat) yang berasa manis 50 kali lipat sukrosa. Bila dihidrolisis, glisirisin akan terurai menjadi asam glisiretinat dan 2 molekul asam glukuronat yang tidak berasa manis lagi. Asam
glisiretinat merupakan derivat triterpen pentasiklik tipe β-amyrin. Kandungan lainnya adalah glikosida flavonoid (antara lain likuiritin, isolikuiritin, liquiritosida, isolikuiritosida, ramnoli-kuiritin, dan ramnoisolikuiritin), derivat kumarin (herniarin dan umbeliferon), asparagine, 22,23-dihidrostigmasterol, glukosa, manitol, dan amilum 20% (Tyler, 1988).
D. Saponin
Saponin merupakan suatu glikosida yang memiliki berat molekul dan kepolaran yang tinggi. Sebagai glikosida, saponin dapat dihidrolisis dengan asam atau enzim untuk menghasilkan aglikon (sapogenin), gula, dan asam uronat.
8
Saponin merupakan surfaktan yang kuat yang menimbulkan busa bila dikocok dalam air dan pada konsentrasi yang rendah sering menyebabkan hemolisis sel darah merah. Saponin tersebar luas pada tanaman tingkat tinggi dan merupakan obat yang pahit menusuk. Saponin larut dalam air dan etanol tetapi tidak larut dalam eter (Brotosisworo, 1979; Robinson, 1995; Evans, 2002).
Hidrolisis saponin menghasilkan aglikon yang disebut sapogenin. Berdasarkan aglikonnya, saponin dibagi menjadi dua, yaitu saponin steroid dan saponin triterpenoid (gambar 1). Kedua macam senyawa tersebut mempunyai hubungan glikosidal pada C-3 dan mempunyai asal-usul biogenetika yang sama melalui asam mevalonat dan satuan isoprenoid (Brotosisworo, 1979; Bruneton, 1999; Evans, 2002).
1
Gambar 1. Struktur kimia dua macam golongan saponin(Robbers, 1996)
9
Saponin meningkatkan aktivitas epitel yang bersilia, suatu peristiwa yang memicu batuk untuk mengeluarkan dahak, sedangkan pengaruh iritasi lokal saponin dapat menimbulkan bersin. Selain itu, saponin juga dapat meningkatkan absorpsi zat diuretika dan merangsang ginjal supaya lebih aktif (Brotosisworo, 1979) dan menghambat pertumbuhan kanker kolon serta membantu kadar kolesterol menjadi normal (Arnelia, 2004). Beberapa saponin steroid digunakan sebagai senyawa awal untuk sintesis beberapa bahan seperti hormon seks, kortison, steroid diuretik, vitamin D, dan glikosida jantung (Evans, 2002). Sedangkan saponin triterpenoid banyak dimanfaatkan sebagai ekspektoran dan antiinflamasi (Bruneton, 1999).
E. Penyarian
Penyarian adalah kegiatan penarikan zat yang dapat larut dari bahan yang tidak dapat larut dengan pelarut cair. Untuk melakukan penyarian harus diketahui zat aktif yang dikandungnya sehingga mempermudah pemilihan cairan penyari serta cara penyarian yang tepat (Anonim, 1986). Metode ekstraksi menggunakan pelarut dapat dibedakan menjadi dua cara yaitu cara dingin dan panas.
1. Cara dingin a. Maserasi
Maserasi adalah proses pengekstraksian simplisia menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur.
10
b. Perkolasi
Perkolasi adalah ekstraksi dengan pelarut yang selalu baru sampai sempurna yang umumnya dilakukan pada temperatur kamar.
2. Cara panas
a. Refluks
Refluks adalah ekstraksi dengan pelarut pada temperatur titik didihnya, selama waktu tertentu dan jumlah pelarutnya terbatas yang relatif konstan dengan adanya pendingin balik.
b. Soxhlet
Soxhlet adalah ekstraksi menggunakan pelarut yang selalu baru yang umumnya dilakukan dengan alat khusus sehingga terjadi ekstraksi kontinu dengan jumlah pelarut yang relatif konstan dengan adanya pendingin balik.
c. Digesti
Digesti adalah maserasi kinetik pada temperatur yang lebih tinggi dari temperatur ruangan, secara umum dilakukan pada temperatur 40 - 50 °C. d. Infus
Infus adalah sediaan cair yang dibuat dengan menyari simplisia dengan air pada suhu 90 °C selama 15 menit.
e. Dekok
Dekok adalah infus pada waktu yang lebih lama (≥ 30 menit) dan
temperatur sampai titik didih air (Anonim, 2000).
11
F. Kromatografi Lapis Tipis (KLT) dan Kromatografi Lapis Tipis Preparatif (KLTP)
KLT merupakan metode pemisahan komponen-komponen atas dasar perbedaan adsorpsi atau partisi oleh fase diam di bawah pergerakan pelarut pengembang atau pelarut pengembang campur. Pemilihan pelarut pengembang atau pelarut pengembang campur sangat dipengaruhi oleh macam dan polaritas zat-zat kimia yang dipisahkan (Mulja dan Suharman, 1995). Penjerap yang umum ialah silika gel (paling banyak digunakan), aluminium oksida, selulosa dan turunannya, poliamida, dan lain-lain (Stahl, 1985).
Jarak pengembangan senyawa pada kromatogram dinyatakan dengan angka Rf atau hRf.
jarak titik pusat bercak dari titik awal Rf = ————————————————
jarak garis depan dari titik awal
Angka Rf berjangka 0,00 dan 1,00 dan hanya dapat ditentukan dengan dua desimal, sedangkan hRf adalah angka Rf dikalikan faktor 100 (h) menghasilkan nilai berjangka 0 sampai 100 (Stahl, 1985).
Salah satu metode pemisahan yang memerlukan pembiayaan paling murah dan memakai peralatan paling dasar adalah kromatografi lapis tipis preparatif (KLTP). Ketebalan penjerap yang paling sering dipakai ialah 0,5-2 mm. Ukuran pelat kromatografi biasanya 20x20 cm atau 20x40 cm (Hostettmann dan Marston, 1995).
Cuplikan dilarutkan dalam sedikit pelarut sebelum ditotolkan pada pelat KLTP. Pelarut yang baik adalah pelarut atsiri. Kebanyakan penjerap KLTP
12
mengandung indikator fluoresensi yang membantu mendeteksi kedudukan pita yang terpisah sepanjang senyawa yang dipisahkan menyerap UV (Hostettmann dan Marston, 1995).
Pita yang kedudukannya telah diketahui dikerok dari pelat dengan spatula atau pengerok berbentuk tabung yang disambungkan ke pengumpul vakum. Cara terakhir tidak dapat dilakukan untuk senyawa peka karena penjerap yang mengandung senyawa yang sudah murni terus menerus terkena aliran udara dan resiko otooksidasi selalu ada. Kemudian senyawa harus diekstraksi dari penjerap dengan pelarut sekitar 5 ml untuk 1 g penjerap. Harus diperhatikan bahwa makin lama senyawa berkontak dengan penjerap makin besar kemungkinan penguraian (Hostettmann dan Marston, 1995).
G. Spektrofotometri Ultraviolet
Teknik spektroskopik adalah salah satu teknik analisis fisiko-kimia yang mengamati tentang interaksi atom atau molekul dengan radiasi elektromagnetik (REM). Spektrofotometri ultraviolet merupakan teknik analisis spektroskopik yang memakai sumber radiasi elektromagnetik ultraviolet dekat (190-380 nm) dengan memakai instrumen spektrofotometer. Dasar dari metode ini adalah interaksi antara radiasi elektromegnetik dengan atom, molekul, atau ion. Interaksi ini akan menyebabkan eksitasi elektron ke tingkat energi yang lebih tinggi (Mulja dan Suharman, 1995). Proses eksitasi ini mengakibatkan terjadinya satu atau lebih transisi. Transisi-transisi tersebut diklasifikasikan sebagai berikut :
13
1. Transisi elektron n Æ π*, meliputi transisi elektron-elektron heteroatom tak berikatan ke orbital antibonding π* dan terjadi pada panjang gelombang yang panjang dan intensitasnya rendah. Transisi ini menunjukkan pergeseran hipsokromik dalam pelarut-pelarut yang lebih polar dan dengan substituen-substituen yang bersifat pemberi elektron.
2. Transisi elektron n Æ σ*, terjadi pada senyawa-senyawa jenuh yang
mengandung heteroatom seperti oksigen, nitrogen, belerang, atau halogen 3. Transisi elektron πÆ π*, terjadi pada elektron di orbital π, yaitu pada ikatan
rangkap dua dan rangkap tiga. Eksitasi ini paling mudah terbaca dan bertanggung jawab terhadap spektra elektronik dalam daerah UV dan tampak
4. Transisi elektron σ Æ σ*, terjadi pada elektron yang mempunyai ikatan
tunggal kovalen dan menduduki orbital σ. Tingkat energi yang dibutuhkan
untuk eksitasi ini sangat besar (Mulja dan Suharman, 1995; Sastrohamidjojo, 2001).
Spektrum ultraviolet adalah suatu gambar antara panjang gelombang atau frekuensi serapan lawan intensitas serapan (transmitasi atau absorbansi). Kromofor merupakan gugus tak jenuh kovalen yang dapat menyerap radiasi dalam daerah ultraviolet dan terlihat. Contoh kromofor adalah gugus karbonil (keton) pada aseton yang memberi serapan maksimum pada 188 nm (dengan
transisi elektronik πÆπ* dan 279 nm (dengan transisi elektron nÆπ*).
Sedangkan auksokrom merupakan gugus jenuh yang bila terikat pada kromofor akan mengubah panjang gelombang dan intensitas serapan maksimum. Ciri auksokrom adalah heteroatom yang langsung terikat pada kromofor, misal
14
–OCH3, –Cl, –OH dan NH2. Terikatnya gugus auksokrom oleh gugus kromofor
akan mengakibatkan pergeseran pita absorpsi menuju ke panjang gelombang yang lebih panjang. Pergeseran ini disebut pergeseran merah atau pergeseran batokromik, yang biasanya disertai dengan peningkatan intensitas serapan (efek hiperkromik). Substitusi atau pengaruh pelarut, selain menyebabkan pergeseran batokromik, juga dapat menyebabkan pergeseran hipsokromik (pergeseran biru), yaitu pergeseran serapan ke arah panjang gelombang yang lebih pendek. Sedangkan efek hipokromik adalah penurunan intensitas serapan (Pecsok, 1976; Mulja dan Suharman, 1995; Sastrohamidjojo, 2001).
Panjang gelombang dimana terjadi eksitasi elektronik yang memberikan absorban maksimum disebut panjang gelombang maksimum. Penentuan panjang gelombang maksimum dapat digunakan untuk mengidentifikasi molekul (Mulja dan Suharman, 1995).
Spektrum serapan kandungan tumbuhan dapat diukur dalam larutan yang sangat encer dengan pembanding blangko pelarut serta menggunakan spektrofotometer yang merekam otomatis. Senyawa tak berwarna diukur pada panjang gelombang 200-400 nm, senyawa berwarna pada panjang gelombang 200-700 nm. Panjang gelombang serapan maksimum dan minimum pada spektrum serapan yang diperoleh direkam (dalam nm), demikian juga kekuatan absorbansi. Bahan yang diperlukan hanya sedikit saja karena sel spektrofotometri baku (1x1 cm) hanya dapat diisi 3 ml larutan. Pengukuran spektrum yang demikian penting pada identifikasi kandungan tumbuhan, yaitu untuk memantau
15
eluat dari kolom kromatografi sewaktu pemurnian dan untuk mendeteksi golongan senyawa tertentu (Harborne, 1987).
Pelarut yang dipakai untuk melarutkan sampel dalam spektrofotometri UV harus memenuhi persyaratan sebagai berikut :
1. tidak mengandung sistem ikatan rangkap terkonjugasi pada struktur
molekulnya dan tidak berwarna
2. tidak terjadi interaksi dengan molekul senyawa yang dianalisis
3. kemurniannya harus tinggi atau derajat untuk analisis (Mulja dan Suharman, 1995).
Pelarut yang banyak digunakan untuk spektrofotometri UV adalah etanol 95% karena kebanyakan golongan senyawa larut dalam pelarut tersebut. Dan sebaiknya alkohol mutlak niaga harus dihindari karena mengandung benzena yang menyerap di daerah UV pendek (Harborne, 1987).
Komponen-komponen pokok dari spektrofotometer meliputi : (1) sumber tenaga radiasi yang stabil, (2) sistem yang terdiri atas lensa-lensa, cermin, celah-celah, dan lain-lain, (3) monokromator untuk mengubah radiasi menjadi komponen-komponen panjang gelombang tunggal, (4) tempat cuplikan yang transparan, dan (5) detektor radiasi yang dihubungkan dengan sistem meter atau pencatat. Diagram sederhana dari spektrofotometer adalah sebagai berikut:
sumber sel
penyerap
detektor pencatat
monokromator
Gambar 2. Diagram spektrofotometer
(Sastrohamidjojo, 2001)
16
H. Keterangan Empiris
Dari penelitian ini diharapkan dapat diketahui tipe saponin pada kecambah kacang hijau beserta karakter aglikon saponinnya secara KLT dan spektrofotometri UV.
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian ini termasuk dalam penelitian noneksperimental karena di dalam penelitian ini tidak dilakukan manipulasi atau intervensi terhadap subjek uji.
B. Definisi Operasional
1. Identifikasi organoleptik dan makroskopik adalah cara untuk menentukan ciri khas kecambah kacang hijau yang dilakukan berdasarkan pengamatan terhadap rasa, warna, bau, dan bentuk.
2. Uji buih adalah cara untuk mengetahui adanya saponin dengan menggojog ekstrak air dari kecambah kacang hijau dalam tabung reaksi sampai terbentuk buih yang tidak hilang selama 10 menit.
3. Isolasi aglikon saponin kecambah kacang hijau adalah proses pengambilan aglikon saponin dari kecambah kacang hijau dengan metode KLTP.
4. Karakter aglikon saponin kecambah kacang hijau secara KLT adalah hasil KLT yang didapatkan berupa warna bercak dan Rf aglikon saponin kecambah kacang hijau.
5. Karakter aglikon saponin kecambah kacang hijau secara spektrofotometri UV adalah hasil spekra isolat aglikon saponin kecambah kacang hijau berupa panjang gelombang maksimum (λmax)
17
18
C. Bahan dan Alat Penelitian 1. Bahan
a. Bahan utama : kacang hijau
b. Bahan pembanding yang digunakan adalah Succus Liquiritiae yang
diambil dari Laboratorium Farmasetika Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta (asal BRATACO/pharmaceutical grade).
c. Bahan kimia yang digunakan, kecuali disebut lain, berderajat pro analisis, antara lain : aquadestilata (diambil dari Laboratorium Farmakognosi Fitokimia Fakultas Farmasi Universitas Sanata Dharma Yogyakarta), asam asetat anhidrida, asam sulfat, asam klorida, natrium sulfat anhidrat, silika gel GF254, kloroform, metanol, anisaldehida, etanol, n-butanol.
2. Alat
Bakul bambu, neraca analitik (Metler Toledo), kompor, waterbath, seperangkat alat refluks, magnetic stirrer, sinterred glass, oven, alat penyemprot, pipet mikroliter, lampu UV 254 nm, bejana kromatografi, spektrofotometer UV-Vis Lambda 20 (Perkin Elmer) dan kuvet (Quartz), peralatan gelas (tabung reaksi, Erlenmeyer, corong pisah, gelas ukur, dan lain-lain).
19
D. Jalan Penelitian 1. Determinasi tanaman
Determinasi tanaman kacang hijau dilakukan dengan menggunakan buku acuan(Van Steenis, 1975).
2. Pengumpulan bahan dan proses perkecambahan
Biji kacang hijau diperoleh dari pedagang biji-bijian di Klaten. Kacang hijau yang digunakan adalah kacang hijau jenis lokal. Biji yang baik dipilih untuk dikecambahkan.
Biji kacang hijau direndam dalam air selama satu malam kemudian ditebarkan dalam bakul bambu, dan diberi daun untuk menjaga kelembaban.
Setiap hari disiram air sebanyak 4 kali (Gsianturi, 2003). Kecambah yang
digunakan adalah kecambah berumur 2 hari. 3. Pemeriksaan organoleptik dan makroskopik
Pemeriksaan organoleptik dan makroskopik dilakukan berdasarkan pengamatan terhadap rasa, warna, bau, dan bentuk kecambah kacang hijau, 4. Uji saponin
a. Uji buih
Sebanyak 500 mg kecambah kacang hijau dilumatkan dan dimasukkan dalam tabung reaksi, lalu ditambah 10 ml air panas, didinginkan kemudian dikocok kuat-kuat selama 10 detik. Terbentuknya buih selama tidak kurang dari 10 menit menunjukkan adanya saponin (Anonim, 1995).
20
b. Reaksi Liebermann – Burchard
Sebanyak 500 mg kecambah kacang hijau dilumatkan, dipanasi dengan 1 ml asam asetat anhidrida lalu ditetesi dengan asam sulfat pekat 2 tetes, akan terbentuk warna hijau sampai biru bila mengandung senyawa steroid atau warna merah muda sampai merah bila mengandung senyawa triterpen (Bruneton, 1999).
5. Hidrolisis saponin kecambah kacang hijau dan Succus Liquiritiae
Secara terpisah, 10 gram Succus Liquiritiae dihaluskan dan 10 gram kecambah kacang hijau dilumatkan kemudian dihidrolisis dengan 50 ml asam sulfat 1 N selama 2 jam dengan menggunakan refluks kemudian didinginkan (Harborne, 1987). Hasil hidrolisis ini dinamakan hidrolisat.
6. Ekstraksi aglikon saponin kecambah kacang hijau dan Succus Liquritiae Hidrolisat yang diperoleh dituang ke dalam Erlenmeyer bertutup,
ditambahkan kloroform 30 ml dan diaduk menggunakan magnetic stirrer
selama 30 menit. Fase kloroform yang terbentuk dipisahkan dengan corong pisah, larutan fase air-asam diekstraksi ulang dengan kloroform sebanyak 3 kali. Fase kloroform yang diperoleh ditambah dengan natrium sulfat anhidrat lalu disaring. Filtrat yang diperoleh diuapkan sampai volumenya sekitar 5 ml. Hasil yang diperoleh adalah ekstrak kloroform kecambah kacang hijau dan ekstrak kloroform Succus Liquiritiae (Stahl, 1985).
21
7. Pemeriksaan pendahuluan aglikon saponin dengan kromatografi lapis tipis (KLT)
Pemisahan dengan metode KLT ini menggunakan fase diam silika gel GF 254 dan fase gerak kloroform – metanol (95:5 v/v). Pada titik pertama
lempeng ditotolkan pembanding (ekstrak kloroform Succus Liquiritiae)
sebanyak 10 μl dan pada titik kedua ditotolkan sampel (ekstrak kloroform
kecambah kacang hijau) sebanyak 20 μl. Jarak penotolan 1,5 cm dari tepi
bawah lempeng dengan jarak pengembangan 10 cm, lalu diamati dengan sinar UV 254 nm. Selanjutnya disemprot dengan pereaksi anisaldehida-asam sulfat LP dan dipanaskan pada suhu 110 °C selama 10 menit lalu diamati dengan sinar tampak.
8. Isolasi aglikon saponin dengan KLT preparatif
Isolasi atau pemisahan aglikon saponin dari senyawa-senyawa lain dilakukan dengan metode KLT preparatif. Fase diam yang digunakan adalah silika gel GF254 pada lempeng berukuran 20 x 20 cm dengan ketebalan 0,5 mm
dengan fase gerak kloroform – metanol (95:5 v/v).
Pada lempeng dilakukan penotolan ekstrak kloroform berbentuk pita kemudian dikembangkan dengan fase gerak kloroform – metanol (95:5 v/v). Jarak penotolan 1,5 cm dari tepi bawah lempeng. Setelah jarak pengembangan mencapai 10 cm, pelat diambil dan dikeringkan kemudian dimasukkan lagi dalam bejana. Pengembangan berulang dilakukan sebanyak 2 kali.
Setelah pelat dikeringkan, pita yang berfluoresensi di bawah sinar UV 254 nm dan diduga merupakan aglikon saponin dikerok dan dikumpulkan.
22
Hasil kerokan ini dilarutkan dalam kloroform dan disaring dengan sinterred glass. Filtrat diuapkan di atas waterbath sampai volumenya sekitar 5 ml. Hasil yang diperoleh disebut isolat aglikon saponin Succus Liquiritiae dan isolat aglikon saponin kecambah kacang hijau. Isolat ini kemudian diuji kemurniannya dengan KLT multi-eluen dan diidentifikasi secara spektrofotometri ultra violet.
9. Uji kemurnian dengan KLT multi-eluen
Uji kemurnian dengan KLT multi-eluen ini menggunakan fase diam silika gel GF254 dan 3 fase gerak yang berbeda, yaitu kloroform – metanol
(95:5 v/v), kloroform – metanol – air (64:50:10 v/v), dan n-butanol – etanol – air (7:2:5 v/v) (Stahl, 1973; Gasparic, 1978; Wagner, 1999).
Pada titik pertama lempeng ditotolkan isolat pembanding sebanyak 10 µl dan pada titik kedua ditotolkan isolat aglikon saponin kecambah kacang hijau sebanyak 20 µl dengan jarak 1,5 cm dari tepi bawah lempeng. Selanjutnya ketiga lempeng dielusi dengan ketiga fase gerak tersebut dalam bejana yang sudah dijenuhkan. Setelah mencapai jarak pengembangan 10 cm, lempeng diangkat dan dikeringkan, lalu diamati dengan di bawah lampu UV 254 nm. Selanjutnya disemprot dengan pereaksi anisaldehida-asam sulfat LP,
dipanaskan pada suhu 1100 C selama 10 menit lalu diamati dengan sinar
tampak.
10. Spektrofotometri Ultra Violet (UV)
Isolat aglikon saponin pembanding dan isolat aglikon saponin kecambah kacang hijau diuapkan sampai kering kemudian dilarutkan dalam
23
etanol dan dibaca serapannya dengan spektrofotometer UV pada panjang gelombang 220-350 nm.
E. Tata Cara Analisis Hasil
Data yang telah diperoleh berupa data kualitatif dan dipaparkan secara deskriptif komparatif, yaitu dengan menggambarkan apa adanya hasil yang
diperoleh dan dibandingkan dengan pembanding yang sesuai, yaitu Succus
Liquiritiae.
Untuk mengetahui tipe aglikon saponin kecambah kacang hijau dilakukan uji pendahuluan yang meliputi uji buih dan reaksi warna Liebermann – Burchard. KLT pendahuluan digunakan untuk mengetahui bercak aglikon saponin sehingga dapat diketahui bercak mana yang akan diisolasi. Caranya adalah dengan membandingkan warna bercak dan Rf dari ekstrak kecambah kacang hijau dan ekstrak Succus Liquiritiae secara kualitatif.
Isolasi aglikon saponin kecambah kacang hijau dilakukan dengan metode KLT preparatif, sedangkan uji kemurnian isolat dilakukan dengan metode KLT multi-eluen. Analisis hasil KLT multi-eluen dilihat dari kromatogramnya yang hanya menghasilkan satu macam bercak. Setelah itu dilakukan juga analisis secara kualitatif dengan spektrofotometri UV untuk melihat karakter dari aglikon saponin yang berupa panjang gelombang maksimum (λmax).
BAB IV
HASIL DAN PEMBAHASAN
A. Determinasi Tanaman
Biji kacang hijau yang digunakan dalam penelitian ini diperoleh dari
pedagang biji-bijian. Oleh karena itu, biji yang digunakan untuk dikecambahkan
ditumbuhkan menjadi tanaman kemudian dideterminasi menggunakan buku acuan
determinasi menurut Van Steenis (1975).
Berdasarkan hasil determinasi dapat disimpulkan bahwa tanaman yang
ditumbuhkan dari biji tersebut benar adalah Phaseolus radiatus L. (lampiran 1).
B. Pengumpulan Bahan dan Proses Perkecambahan
Bahan yang digunakan adalah biji kacang hijau yang diperoleh dari
pedagang biji-bijian di Klaten. Proses pembuatan kecambah dilakukan dengan
menggunakan biji kacang hijau yang baik, artinya biji tidak busuk dan bentuk
masih baik. Biji kacang hijau kemudian dicuci bersih dan direndam dalam air
selama 1 malam. Proses perendaman ini bertujuan supaya biji menarik air dan
kulit bijinya melunak, sehingga dapat berkecambah. Setelah perendaman selama 1
malam, keesokan paginya biji disebar di atas daun yang dimasukkan dalam wadah
bambu dan ditutupi dengan daun. Biji disebar supaya semua biji mendapat udara
untuk proses respirasi. Biji disiram air 3 kali sehari dan ditutupi dengan daun
untuk menjaga supaya biji tetap dalam lingkungan yang lembab sehingga dapat
mendukung proses perkecambahannya. Keesokan harinya biji sudah berkecambah
24
25
dengan panjang sekitar 1,5 – 2 cm. Kecambah inilah yang digunakan sebagai
bahan percobaan. Kulit biji yang berwarna hijau dipisahkan dari kecambah.
Kecambah dilumatkan dalam mortir dengan stamper dan siap untuk digunakan
dalam percobaan.
C. Hasil Pemeriksaan Organoleptik dan Makroskopik
Pemeriksaan organoleptik dan makroskopik kecambah kacang hijau
dilakukan berdasarkan pengamatan terhadap bentuk, rasa, warna, dan baunya.
Dari hasil pemeriksaan didapatkan hasil sebagai berikut :
Rasa : tawar
Warna : kuning pucat
Bau : langu
Bentuk : radikel berwarna putih dengan panjang ± 1,5 cm; kotiledon
berwarna kekuningan dengan bentuk cembung pada satu sisi
dan rata pada sisi lain, jumlah dua, dan duduk berhadapan pada
sisi yang rata
Kecambah yang digunakan pada penelitian ini dipilih yang baik, artinya memiliki
kotiledon dan radikel yang tidak rusak, utuh, tidak lembek, dan tidak ada noda.
26
D. Uji Saponin 1. Uji buih
Hasil uji buih pada kecambah kacang hijau adalah positif, ditandai
dengan pembentukan buih yang mencapai tinggi lebih kurang 1,5 cm dan setelah
10 menit buih ini tidak hilang. Hal ini menunjukkan bahwa kecambah kacang
hijau mengandung saponin. Hasil uji tersebut sesuai dengan pustaka menurut
Anonim (1995), yaitu terbentuknya buih yang tidak hilang selama 10 menit.
Pembentukan buih ini dikarenakan sifat saponin yang dapat menurunkan
tegangan permukaan air. Molekul saponin mengandung gugus hidrofilik (bagian
polar) dan lipofilik (bagian nonpolar). Di dalam air, gugus hidrofilik akan
berikatan dengan air dan gugus hidrofilik menjauhi air (gambar 3).
HO
Gambar 3. Gugus hidrofilik dan lipofilik pada saponin
27
Gugus hidrofilik dapat bergabung dengan air namun gugus lipofilik
ditolak karena gaya adhesifnya dengan air lebih kecil dibandingkan dengan gaya
kohesif antar molekul air. Akibatnya zat tersebut diadsorpsi pada antarmuka
air-udara (Martin,1993).
lipofilik udara
hidrofilik air
Gambar 4. Adsorpsi molekul-molekul saponin pada antarmuka air-udara
(Martin, 1993)
Adsorpsi molekul saponin pada antarmuka air-udara dapat
mengakibatkan penurunan tegangan permukaan air yang dapat menimbulkan buih.
Dengan adanya alasan ini saponin diklasifikasikan sebagai zat aktif permukaan
(surfaktan) (Martin, 1993).
2. Reaksi Liebermann-Burchard
Uji reaksi ini dilakukan untuk membuktikan ada tidaknya senyawa
triterpenoid atau steroid dalam kecambah kacang hijau karena reaksi ini positif
dengan kebanyakan triterpenoid dan steroid. Uji ini sangat menentukan
pembanding apa yang akan digunakan dalam identifikasi aglikon saponin kacang
hijau secara KLT. Bila didapatkan hasil bahwa kecambah kacang hijau
mengandung saponin tipe triterpenoid maka akan digunakan asam glisiretinat
sebagai pembanding dan bila kecambah kacang hijau mengandung saponin tipe
steroid maka akan digunakan stigmasterol sebagai pembanding. Kacang hijau
28
yang sudah dilumatkan dipanasi dengan asam asetat anhidrat (sebagai pereaksi)
dan ditetesi dengan asam sulfat (sebagai katalis) menghasilkan warna merah
keunguan (gambar 5) yang menunjukkan bahwa kecambah kacang hijau
mengandung senyawa triterpenoid. saponin triterpenoid asam asetat anhidrida
asam asetat
Gambar 5. Reaksi Liebermann-Burchard (Kristianti, 2007)
Dari hasil uji pendahuluan ini dapat disimpulkan bahwa kecambah
kacang hijau mengandung saponin triterpenoid, sehingga untuk identifikasi
dengan KLT akan digunakan asam glisiretinat sebagai pembanding.
29
E. Hidrolisis Saponin Kecambah Kacang Hijau dan Succus Liquiritiae
Untuk mendapatkan aglikonnya, saponin harus dihidrolisis dengan asam.
Asam yang digunakan adalah asam klorida 0,1 M. Hidrolisis dilakukan selama 2
jam menggunakan alat pendingin balik (refluks). Pembanding yang digunakan
adalah asam glisiretinat. Karena tidak tersedianya asam glisiretinat atau glisirisin
dalam bentuk murni, digunakan Succus Liquiritiae sebagai pembanding karena
Succus Liquiritiae mengandung saponin tipe triterpenoid, yaitu glisirisin.
Sedangkan pada uji saponin sebelumnya didapatkan bahwa kecambah kacang
hijau juga mengandung saponin tipe triterpenoid. Glisirisin terhidrolisis dalam
suasana asam menghasilkan asam β-glisiretinat (aglikon) yang merupakan derivat
triterpen pentasiklik dengan tipe β-amirin dan 2 molekul asam glukuronat
(glikon). Succus Liquiritiae diperlakukan sama dengan sampel kecambah kacang
hijau. Untuk mengetahui bahwa hidrolisis sudah terjadi dapat diketahui dari
perubahan warna yang terjadi, yaitu kecambah kacang hijau yang semula
berwarna kekuningan, setelah dihidrolisis menjadi berwarna coklat.
30
2 molekul asam glukuronat
O H
Gambar 6. Mekanisme hidrolisis Succus Liquiritiae dalam suasana asam
F. Ekstraksi Aglikon Saponin Kecambah Kacang Hijau dan Succus Liquiritiae
Hidrolisat yang diperoleh didinginkan kemudian diekstraksi. Ekstraksi
aglikon saponin dilakukan dengan corong pisah menggunakan penyari kloroform
sebanyak 3x30 ml dimaksudkan agar memperoleh aglikon saponin dalam jumlah
yang cukup banyak. Kloroform digunakan karena tidak bercampur dengan air dan
aglikon saponin larut dalam kloroform. Fase kloroform yang diperoleh ditambah
natrium sulfat anhidrat untuk menarik sisa air yang kemungkinan masih ada di
dalam ekstrak lalu disaring. Filtrat yang diperoleh diuapkan sampai volumenya
kira-kira 5 ml. Hasil yang diperoleh berupa ekstrak kloroform kecambah kacang
hijau dan ekstrak kloroform Succus Liquiritiae.
31
G. Pemeriksaan Pendahuluan Aglikon Saponin dengan KLT
Pemeriksaan pendahuluan aglikon saponin dengan KLT dilakukan untuk
mengetahui aglikon saponin yang terdapat dalam ekstrak kloroform kecambah
kacang hijau. Caranya adalah dengan membandingkan ekstrak kloroform
kecambah kacang hijau sebagai sampel dan ekstrak kloroform Succus Liquiritiae
sebagai pembanding dalam satu pelat dan dikembangkan dalam fase gerak yang
sama dengan metode KLT. Perbandingan ini ditentukan berdasarkan harga Rf dan
warna bercak yang dihasilkan.
Fase diam yang digunakan adalah silika gel GF254, yang merupakan
silika gel dengan perekat CaSO4 dan indikator fluoresensi sehingga akan
berfluoresensi pada deteksi sinar UV 254 nm, sedangkan bercaknya akan terlihat
lebih gelap (peredaman) karena sinar UV yang seharusnya diteruskan sampai ke
fase diam (sehingga fase diam berfluoresensi) dihalangi oleh adanya senyawa
yang menyerap sinar UV tersebut dan tidak dipantulkan kembali. Fase gerak yang
digunakan adalah kloroform – metanol (95:5 v/v) yang bersifat nonpolar sehingga
sistem KLT ini merupakan kromatografi fase normal. Alasan digunakannya fase
gerak yang bersifat nonpolar ini adalah karena aglikon saponin (sapogenin)
cenderung bersifat nonpolar, sehingga dengan fase gerak yang bersifat nonpolar,
diharapkan aglikon saponin dapat terelusi dengan baik.
32
(1) (2)
Gambar 7. KLT pendahuluan
Keterangan :
A : ekstrak kloroform Succus Liquiritiae (pembanding) B : ekstrak kloroform kecambah kacang hijau (sampel)
Deteksi :
(1) Dilihat dibawah sinar UV 254 nm
(2) Pereaksi anisaldehid-asam sulfat, dipanaskan 110°C selama 5-10 menit, dilihat dengan sinar tampak
Fase diam : silika gel GF254
Fase gerak : kloroform – metanol (95:5 v/v)
Jarak pengembangan : 10 cm
33
Tabel I. Hasil kromatogram KLT pendahuluan dengan menggunakan fase diam silika gel GF254 dan fase gerak kloroform – metanol (95:5 v/v)
warna bercak nama bercak no
bercak Rf UV 254nm anisaldehid-asam sulfat
1 0,23 - kuning B : ekstrak kloroform kecambah kacang hijau (sampel)
Deteksi :
(1) Dilihat dibawah sinar UV 254 nm
(2) Pereaksi anisaldehid-asam sulfat, dipanaskan 110°C selama 5-10 menit, dilihat dengan sinar tampak
Jarak pengembangan : 10 cm
Dari hasil kromarogram (gambar 7 dan tabel I) dapat dilihat bahwa
terdapat 6 bercak yang berasal dari cuplikan pembanding (ekstrak Succus
Liquiritiae) dan 5 bercak dari cuplikan sampel (ekstrak kecambah kacang hijau).
Dari bercak tersebut terdapat 3 pasang bercak yang mempunyai Rf dan warna
bercak yang hampir sama, yaitu bercak A3 dan B2, bercak A5 dan B4, serta
bercak A6 dan B5. Bercak A3 dan B2 masing-masing mempunyai Rf 0,55 dan
0,54 dengan warna bercak pada deteksi sinar UV 254 nm adalah ungu dan setelah
disemprot dengan pereaksi anisaldehid-asam sulfat dan dipanaskan 1100C selama
34
5-10 menit, kedua bercak menghasilkan warna biru. Bercak A5 dan B4
masing-masing mempunyai Rf 0,85 dan 0,86 dengan bercak yang tidak tampak pada
deteksi sinar UV 254, namun setelah disemprot dengan pereaksi anisaldehid-asam
sulfat dan dipanaskan 1100C selama 5-10 menit, kedua bercak sama-sama
menghasilkan warna biru. Bercak A6 dan B5 sama-sama mempunyai Rf 1,00
dengan bercak yang tidak tampak pada deteksi sinar UV 254, namun setelah
disemprot dengan pereaksi anisaldehid-asam sulfat dan dipanaskan 1100C selama
5-10 menit, kedua bercak sama-sama menghasilkan warna coklat.
Sebenarnya tidak ada saponin yang dapat dideteksi atau diamati secara
spesifik dengan menggunakan sinar lampu UV 254 dan 365 nm, kecuali asam
glisiretinat (Wagner, 1984). Jadi untuk memperjelas identifikasi saponin perlu
menggunakan pereaksi semprot. Salah satu pereaksi semprot yang digunakan
untuk mengidentifikasi aglikon saponin triterpenoid adalah anisaldehid-asam
sulfat. Reaksi dengan anisaldehid-asam sulfat mengakibatkan penambahan
panjang gugus kromofor yang menyebabkan serapan bercak senyawa berada pada
panjang gelombang yang lebih panjang sehingga terjadi peningkatan intensitas
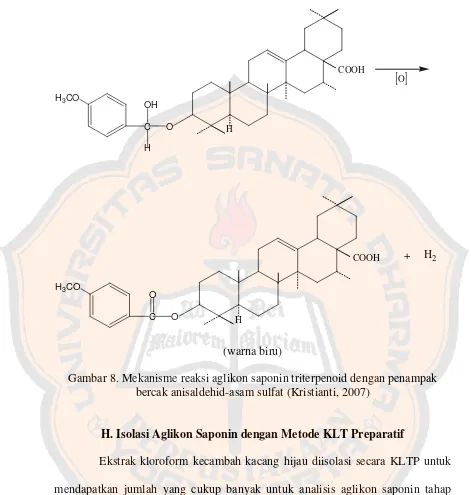
warna dan dapat dilihat pada sinar tampak (gambar 8).
Stahl (1985)menyatakan bahwa aglikon saponin dari Succus Liquiritiae
adalah asam glisiretinat yang memiliki harga hRf sekitar 20-30 dengan warna
bercak biru sampai ungu dengan deteksi anisaldehid-asam sulfat, pada fase diam
silika gel GF254 asam dan fase gerak kloroform – metanol (95:5 v/v). Dari hasil
penelitian yang dilakukan oleh Yanuarsih (2001) diperoleh bahwa aglikon saponin
triterpenoid golongan β-amirin memiliki hRf 55 dengan warna biru setelah
35
dideteksi dengan anisaldehid-asam sulfat. Dari dasar inilah dapat disimpulkan
bahwa aglikon saponin pembanding (asam glisiretinat) adalah bercak A3 dan
aglikon saponin dari sampel adalah bercak B2.
OCH3
36
Gambar 8. Mekanisme reaksi aglikon saponin triterpenoid dengan penampak bercak anisaldehid-asam sulfat (Kristianti, 2007)
H. Isolasi Aglikon Saponin dengan Metode KLT Preparatif
Ekstrak kloroform kecambah kacang hijau diisolasi secara KLTP untuk
mendapatkan jumlah yang cukup banyak untuk analisis aglikon saponin tahap
selanjutnya. Isolasi dilakukan dengan menggunakan fase diam silika gel GF254
pada pelat kaca 20x20 cm dan fase gerak kloroform – metanol (95:5 v/v) karena
pada literatur yang diperoleh, hanya didapatkan data karakteristik aglikon saponin
pembanding dengan fase diam dan fase gerak tersebut.
37
Cuplikan yang akan dipisahkan ditotolkan membentuk pita dan
dikembangkan 2x. Pengembangan berulang dimaksudkan supaya pemisahan
senyawa semakin baik. Dalam penelitian ini, 2x pengembangan sudah
menghasilkan pemisahan yang cukup baik. Hal ini dapat dilihat dari bercak yang
didapat yang terlihat cukup jelas dan tidak terlalu dekat satu sama lain, sehingga
lebih mudah dikerok. Bercak yang menunjukkan Rf dan warna yang hampir sama
dengan bercak yang diduga aglikon saponin pada KLT pendahuluan dikerok
dengan menggunakan spatula dan dikumpulkan. Hasil kerokan ini dilarutkan
dalam kloroform dan disaring dengan sinterred glass. Filtrat kemudian diuapkan
sampai volumenya kira – kira 5 ml. Fase diam yang digunakan pada isolasi ini
sejumlah 5 pelat untuk mendapatkan isolat yang lebih banyak. Jumlah kloroform
yang digunakan untuk satu kali penyarian adalah 20 ml supaya hasil kerokan
benar-benar terendam oleh pelarut, dan dilakukan 5x penyarian supaya
mendapatkan aglikon saponin dalam jumlah yang cukup banyak. Selanjutnya dari
hasil isolat ini dianalisis untuk uji kemurnian dengan menggunakan metode KLT
multi-eluen.
I. Uji Kemurnian dengan Metode KLT multi-eluen
Uji kemurnian ini dilakukan untuk memastikan apakah senyawa yang
telah dipisahkan benar-benar murni hasil dari isolasi senyawa yang diinginkan,
dan tidak tercampur dengan senyawa lain. Isolat yang diperoleh diuji
kemurniannya dengan 3 macam fase gerak yang berbeda, yaitu kloroform –
metanol (95:5 v/v), kloroform – metanol – air (64:50:10 v/v), dan n-butanol –
38
etanol – air (7:2:5 v/v). Jika isolat tersebut murni maka hanya akan menghasilkan
satu bercak. Fase gerak yang dipilih adalah fase gerak yang pernah digunakan
dalam identifikasi beberapa macam aglikon saponin dalam literatur (Stahl, 1973;
Gasparic, 1978; Wagner, 1999) sehingga diharapkan dapat mengelusi aglikon
saponin dalam sampel. Selain itu, fase gerak juga dipilih berdasarkan tingkat
kepolarannya sehingga dapat diketahui benar kemurniannya. Fase gerak
kloroform – metanol (95:5 v/v) bersifat relatif nonpolar dibandingkan dengan
kloroform – metanol – air (64:50:10 v/v) dan n-butanol – etanol – air (7:2:5 v/v).
Masing-masing isolat ditotolkan sejumlah 20 µl, karena jumlah tersebut
dapat menghasilkan intensitas warna bercak yang cukup jelas dilihat pada deteksi
dengan sinar UV sehingga mudah dalam identifikasinya.
Tabel II. Hasil uji kemurnian isolat aglikon saponin dengan KLT multi-eluen
warna bercak
fase gerak nama
bercak Rf UV 254 nm anisaldehid-asam sulfat
A 0,59 ungu biru
kloroform – metanol
(95:5 v/v) C 0,59 ungu biru
A 0,92 ungu biru
kloroform – metanol – air
(64 : 50 : 10 v/v) C 0,91 ungu biru
A 0,81 ungu biru
n-butanol – etanol – air
(7:2:5 v/v) C 0,79 ungu biru
Keterangan :
A = isolat kecambah kacang hijau (sampel) C = isolat Succus Liquiritiae (pembanding)
39
(1) (2)
Gambar 9. Uji kemurnian dengan KLT multi-eluen dengan fase gerak kloroform – metanol (95:5 v/v)
Keterangan :
A : isolat aglikon saponin kecambah kacang hijau (sampel)
B : isolat aglikon saponin gabungan (Succus Liquiritiae dan kecambah kacang hijau)
C : isolat aglikon saponin Succus Liquiritiae (pembanding)
Deteksi :
(1) Dilihat dibawah sinar UV 254 nm
(2) Pereaksi anisaldehid-asam sulfat, dipanaskan 110°C selama 5-10 menit, dilihat dengan sinar tampak
Fase diam : silika gel GF254
Jarak pengembangan : 10 cm
40
(1) (2)
Gambar 10. Uji kemurnian dengan KLT multi-eluen dengan fase gerak kloroform – metanol – air (64:50:10 v/v)
Keterangan :
A : isolat aglikon saponin kecambah kacang hijau (sampel)
B : isolat aglikon saponin gabungan (Succus Liquiritiae dan kecambah kacang hijau)
C : isolat aglikon saponin Succus Liquiritiae (pembanding)
Deteksi :
(1) Dilihat dibawah sinar UV 254 nm
(2) Pereaksi anisaldehid-asam sulfat, dipanaskan 110°C selama 5-10 menit, dilihat dengan sinar tampak
Fase diam : silika gel GF254
Jarak pengembangan : 10 cm
41
(1) (2)
Gambar 11. Uji kemurnian dengan KLT multi-eluen dengan fase gerak n-butanol – etanol – air (7:2:5 v/v)
Keterangan :
A : isolat aglikon saponin kecambah kacang hijau (sampel)
B : isolat aglikon saponin gabungan (Succus Liquiritiae dan kecambah kacang hijau)
C : isolat aglikon saponin Succus Liquiritiae (pembanding)
Deteksi :
(1) Dilihat dibawah sinar UV 254 nm
(2) Pereaksi anisaldehid-asam sulfat, dipanaskan 110°C selama 5-10 menit, dilihat dengan sinar tampak
Fase diam : silika gel GF254
Jarak pengembangan : 10 cm
42
Dari hasil deteksi menggunakan sinar UV 254 nm menunjukkan adanya
peredaman bercak yang berwarna ungu dengan latar belakang berfluoresensi
hijau. Hal ini dikarenakan aglikon saponin memiliki gugus kromofor yang
menyerap sinar UV dan tidak memantulkannya kembali, sehingga terjadi
peredaman. Bercak aglikon saponin kecambah kacang hijau dan Succus Liquritiae
setelah disemprot dengan pereaksi anisaldehid-asam sulfat tampak menimbulkan
bercak berwarna biru (gambar 8). Deteksi dengan pereaksi ini digunakan untuk
mengetahui bercak aglikon saponin dan kemungkinan adanya bercak-bercak lain.
Isolat dikatakan sudah murni bila hanya menghasilkan satu bercak saja pada
masing-masing komposisi fase gerak.
Pada KLT dengan fase gerak kloroform – metanol (95:5 v/v) didapatkan
bercak tunggal dengan Rf 0,59 baik pada isolat aglikon saponin pada kecambah
kacang hijau maupun Succus Liquiritiae. Dari KLT dengan fase gerak kloroform
– metanol – air (64:50:10 v/v) didapatkan bercak tunggal dengan Rf 0,92 pada
isolat aglikon saponin kecambah kacang hijau dan Rf 0,91 pada isolat aglikon
saponin Succus Liquiritiae. Untuk KLT dengan fase gerak n-butanol – etanol – air
(7:2:5 v/v) didapatkan bercak tunggal dengan Rf 0,81 pada isolat aglikon saponin
kecambah kacang hijau dan Rf 0,79 pada isolat aglikon saponin Succus
Liquiritiae. Semua bercak pada uji kemurnian ini berwarna ungu pada deteksi
dengan sinar UV 254 nm dan berwarna biru pada deteksi dengan sinar tampak
setelah disemprot dengan pereaksi anisaldehid-asam sulfat. Dari hasil
kromatogram yang diperoleh, dapat dilihat bahwa isolat aglikon saponin pada
sampel dan pembanding sudah murni dan selanjutnya dapat dilakukan identifikasi
43
dengan spektrofotometri UV. Berdasarkan data tersebut juga dapat disimpulkan
bahwa sampel kecambah kacang hijau mengandung senyawa yang sama dengan
yang dikandung pembanding Succus Liquiritiae, yaitu saponin golongan
triterpenoid. Selain harga Rf dan warna yang mirip, persamaan tersebut juga
didukung dengan hasil KLT pada totolan gabungan antara sampel dan
pembanding yang menghasilkan satu bercak saja dan sama dengan bercak sampel
dan pembanding ( gambar 9, 10, dan 11).
J. Spektrofotometri Ultra Violet (UV)
Pemeriksaan spektra dengan spektrofotometer UV ini dilakukan untuk
melihat karakterisitik dari aglikon saponin kecambah kacang hijau. Panjang
gelombang yang dipilih adalah 220-350 nm karena senyawa yang diukur tidak
berwarna. Pelarut yang juga digunakan sebagai blangko adalah etanol karena
saponin larut dalam etanol dan etanol memenuhi persyaratan pelarut untuk
spektrofotometri UV, yaitu tidak mengandung sistem ikatan rangkap terkonjugasi,
tidak terjadi interaksi dengan molekul senyawa yang dianalisis, dan kemurnian
atau derajat untuk analisisnya tinggi.
Dari spektra (gambar 12 dan 13) tampak bahwa aglikon saponin
kecambah kacang hijau memiliki puncak tunggal pada panjang gelombang 280,4
nm, sedangkan aglikon saponin dari Succus Liquiritiae juga memiliki puncak
tunggal pada panjang gelombang 280,5 nm. Hasil tersebut dapat dikatakan sama
karena hanya memiliki selisih 0,1 nm dan menurut Farmakope Indonesia edisi IV,
range perbedaan yang diperbolehkan adalah 2 nm. Selain itu, bentuk spektra dari
44
kedua isolat aglikon saponin tersebut mirip. Pada aglikon saponin kecambah
kacang hijau, terbentuk puncak tunggal mulai dari 244,0 nm kemudian naik
membentuk puncak pada 280,4 nm lalu menurun kembali. Demikian pula pada
aglikon saponin Succus Liquiritiae, terbentuk puncak tunggal mulai dari 242,9
nm kemudian naik membentuk puncak pada 280,5 nm lalu menurun kembali.
Adanya perbedaan tinggi puncak spektra dikarenakan perbedaan kadar saponin
dalam etanol tersebut. Suatu puncak pada spektra dengan menggunakan
spektrofotometri UV menunjukkan adanya gugus kromofor dengan serapan
maksimum pada panjang gelombang tersebut. Oleh karena itu, dapat disimpulkan
bahwa kecambah kacang hijau memiliki tipe saponin yang sama dengan Succus
Liquiritiae, yaitu saponin triterpenoid, dengan gugus kromofor yang sama pula.
45
Gambar 12. Spektra aglikon saponin kecambah kacang hijau (sampel)
Gambar 13. Spektra aglikon saponin Succus Liquiritiae (pembanding)
BAB V
KESIMPULAN DAN SARAN
A. KESIMPULAN
1. Saponin pada kecambah kacang hijau adalah saponin tipe triterpenoid
2. Karakter aglikon saponin kecambah kacang hijau secara KLT adalah bercak berwarna ungu pada deteksi dengan sinar UV 254 nm dan berwarna biru pada deteksi dengan anisaldehid-asam sulfat dilihat pada sinar tampak dengan : a. Rf 0,59 pada fase gerak kloroform – metanol (95:5 v/v)
b. Rf 0,92 pada fase gerak kloroform – metanol – air (64:50:10 v/v) c. Rf 0,81 pada fase gerak n-butanol – etanol – air (7:2:5 v/v)
Karakter aglikon saponin kecambah kacang hijau dengan spektrofotometri UV adalah puncak tunggal dengan λmax 280,4 nm.
B. SARAN
1. Perlu dilakukan uji KLT sebelum dan setelah hidrolisis untuk lebih
memastikan bahwa proses hidrolisis telah sempurna.
2. Perlu dilakukan penelitian saponin kecambah kacang hijau secara kuantitatif 3. Perlu dilakukan penelitian lebih lanjut untuk identifikasi senyawa dan
elusidasi struktur aglikon saponin kecambah kacang hijau dengan menggunakan spektroskopi IR dan NMR.
46
47
DAFTAR PUSTAKA
Anonim, 1965, Farmakope Indonesia, ed. II, 305, DepKes RI, Jakarta
Anonim, 1986, Sediaan Galenik, Ed I, 2-4,7, DepKes RI, Jakarta
Anonim, 1995a, Materia Medika Indonesia, vol.VI , 194, 336, DepKes RI, Jakarta
Anonim, 1995b, Farmakope Indonesia, ed. IV, 1062-1066, DepKes RI, Jakarta
Anonim, 2000, Parameter Standar Umum Ekstrak Tumbuhan Obat, 9-11, DepKes RI, Jakarta
Anonim, 2005, Taoge, Si Imut Kaya Khasiat, File :
http://www.abolhaq.web.ugm.ac.id
Anonim, 2006, Jangan Remehkan Taoge, File : http://www.freewebs.com
Anonim, 2007, Phaseolus radiatus L., File : http://micro.magnet.fsu.edu
Anonim, 2008, Taoge Vs Kanker dan Stroke, File : http://anik.blog.unair.ac.id
Arnelia, 2004, Fito-kimia Komponen Ajaib Cegah PJK, DM, dan Kanker, File :
http://www.kimianet.lipi.go.id
Brotosisworo, S., 1979, Obat Hayati Golongan Glikosida, 44, UGM Press, Yogyakarta
Bruneton, J., 1999, Pharmacognosy: Phytochemistry Medicinal Plants, 2nd edition, 680-683, Lavoisier Publishing Inc., Paris
Evans, W.C., 2002, Pharmacognosy, ed.XV, 289, W.B.Saunders, London
Gasparic, J., and Churacek, J., 1978, Laboratory Handbook of Paper and Thin Layer Chromatography, John Wiley & Sons, New York
Gsianturi, 2003, Mari, Ramai-Ramai Makan Tauge, File : http://www.gizi.net
Harborne, J.B., 1987, Metode Fitokimia, 21, 155, ITB, Bandung
Hostettmann, K, Hostettmann, M, Marston, A , 1995, Preparatif Chromatography Techniques, 9-11, ITB, Bandung