EFEKTIVITAS AMPAS TEH SEBAGAI ADSORBEN
ALTERNATIF LIMBAH CAIR INDUSTRI TEKSTIL
RETNOWATI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2005
ABSTRAK
RETNOWATI. Efektivitas Ampas Teh sebagai Adsorben Alternatif Limbah Cair
Industri Tekstil. Dibimbing oleh KOMAR SUTRIAH dan HENNY
PURWANINGSIH SUYUTI.
Penanganan limbah cair berwarna dari industri tekstil yang menggunakan karbon
aktif, membutuhkan biaya besar. Untuk mengatasi ha l ini perlu dihasilkan adsorben
alternatif berbaha n dasar murah, misalnya ampas teh yang digunakan dalam penelitian
ini.
Serbuk ampas teh dicuci dengan air deionisasi (biosorben TA), kemudian
pencucian dilanjutkan dengan HNO
30.6 M (AA), NaOH 0.6 M (AB), atau etanol
(AE). Adsor psi terbesar amaran dan biru metilina masing-masing diperoleh dari
biosorben AE dan TA, yaitu 90.51% dan 94.93%. Waktu yang dibutuhkan 0.1 g
biosorben AE untuk mengadsorpsi larutan amaran adalah 6 jam. Biosorben TA
sebanyak 0.2 g mengadsorpsi larutan biru metilena dengan waktu kontak 2 jam.
Perubahan kuat ion dan pH mempengaruhi daya adsorpsi ampas teh. Biosorben AA
0.10 M meningkat adsorpsinya terhadap amaran pada penambahan KNO
31.00 M.
Penambahan KNO
30.10 M pada larutan biru metilena meningkatkan kemampuan
adsorpsi seluruh biosorben. Pengkondisian pH 4 meningkatkan adsorpsi biosorben
AB terhadap larutan biru metilena dan pH 6 meningkatkan adsorpsi biosorben AA
terhadap larutan yang sama.
Berdasarkan pola isoterm adsorpsi, biosorben ampas teh lebih selektif terhadap
larutan bir u metilena dibandingkan amaran.
ABSTRACT
RETNOWATI. The Effectivness of Teawaste as Alternative Adsorbent for Textile
Industries Wastewater. Supervised by KOMAR SUTRIAH and HENNY
PURWANIN GSIH SUYUTI.
Colored wastewater from textile industries treated by activated carbons requires
relatively high costs. To overcome this disadvantages relatively cheap materials are
used as alternative adsorbent, such as teawaste that has been used in this study.
The teawaste powder was washed by deionized water (TA biosorbent), then
washed by HNO
30.6 M (AA), NaOH 0.6 M (AB), or ethanol (AE). The highest
adsorption for amaranth and methylene blue was obtained from AE and TA
biosorbent, i.e. 90.51% and 94.93%. The required time for 0.1 g AE biosorbent to
adsorp amaranth solution was 6 hours. The amount of 0.2 g TA biosorbent was the
best in adsorbing methylene blue solution at 2 hours contact time.
The change of ionic strength and pH influenced adsorption capac ity of teawaste.
The adsorption capacity of AA biosorbent to amaranth was increasing by adding
KNO
31.00 M. Addition of 0.10 KNO3 to methylene blue solution increased the
capacity of all biosorbent . Adjusting to pH 4 increased AB biosorbent capacity of
methylene blue solution and pH 6 increased AA biosorbent adsorption capacity to the
same solution.
According to the pattern of isotherm adsorption from teawaste, biosorbent was
selective to methylene blue rather than to amaranth.
EFEKTIVITAS AMPAS TEH SEBAGAI ADSORBEN
ALTERNATIF LIMBAH CAIR INDUSTRI TEKSTIL
RETNOWATI
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
BOGOR
2005
Judul skripsi : Efe ktivitas Ampas Teh sebagai Adsorben Alternatif Limbah Cair
Industri Tekstil
Nama
: Retnowati
NIM
: G01498070
Disetujui
Drs. Komar Sutriah, M.Si. Henny Purwaningsih suyuti, S.Si, M.Si
Ketua Anggota
Diketahui
Dekan fakultas Matematika dan Ilmu Pengetahuan Alam
Dr. Ir. Yonny Koesmaryono, M.S.
NIP. 131 473 999
PRAKATA
Puji syukur penulis panjatkan kepada Allah SWT atas segala rahmat dan
karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Penelitian ini dilakukan
dari bulan November 2004 sampai Juni 2005 dengan judul Efektifitas Ampas Teh
sebagai Adsorben Alternatif Limbah Cair Industri Tekstil. Penelitian ini dilakukan di
Laboratorium Kimia Fisik Departemen Kimia Fakultas Matematika dan Ilmu
Pengetahuan Alam Institut Pertanian Bogor.
Terima kasih penulis ucapkan kepada Bapak Drs. Komar Sutriah, M.Si dan
Ibu Henny Purwaningsih, S.Si, M.Si selaku pembimbing yang telah banyak
memberikan saran. Di samping itu, penghargaan penulis sampaikan kepada semua
pihak di Laboratorium Kimia Fisik Departemen Kimia FMIPA IPB yang telah banyak
memberikan bantuannya. Terima kasih untuk Lina, Dian, Nisa, Isye, Mila Citra, Erna,
Lia, Ika, dan mas Heri atas dukungan dan bantuannya. Ungkapan terima kasih juga
disampaikan kepada bapak, ibu, dan kakak atas segala do’a, dukungan, dan semua
sarana yang tak ternilai.
Semoga karya ilmiah ini bermanfaat.
Bogor, Oktober 2005
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 11 Agustus 1980 dari ayah Rakidi
dan ibu Juminem. Penulis merupakan putri bungsu dari sebelas bersaudara.
Tahun 1998 penulis lulus dari SMA Negeri 62 Jakarta dan pada tahun yang
sama lulus seleksi masuk ke IPB melalui jalur Ujian Masuk Perguruan Tinggi Negeri.
Penulis memilih Program Studi Kimia, Fakultas Matematika dan Ilmu Pengetahuan
Alam.
Selama mengikuti perkuliahan penulis pernah mengikuti praktek lapangan di
dinas Pengendalian Mutu Petrokimia (DPMP) Pertamina pada tahun 2000.
DAFTAR ISI
Halaman
DAFTAR GAMBAR ... ix
DAFTAR LAMPIRAN... x
PENDAHULUAN ... 1
TINJAUAN PUSTAKA
Teh ... 1
Adsorpsi... 2
Karbon Aktif ... 3
Kuat Ion... 3
pH... 3
Zat Warna ... 3
METODE PENELITIAN
Bahan dan Alat... 4
Metode ... 4
HASIL DAN PEMBAHASAN
Penentuan Bobot Optimum Adsorben dan Waktu Optimum Adsorpsi... 5
Pengaruh Kuat Ion terhadap Adsorpsi... 7
Pengaruh pH terhadap Adsorpsi... 8
Penentuan Isoterm Adsorpsi... 8
SIMPULAN DAN SARAN... 9
Simpulan ... 9
Saran... 9
DAFTAR PUSTAKA ... 9
DAFTAR GAMBAR
Halaman
1 Struktur senyawa amara n... 3
2 Struktur senyawa biru metilena ... 4
3 Adsorpsi larutan amaran 1.1249x10
-5M oleh biosorben TA ... 6
4 Adsorpsi larutan amaran 1.1249x10
-5M oleh biosorben AA ... 6
5 Adsorpsi larutan amaran 1.1249x10
-5M oleh biosorben AB ... 6
6 Adsorpsi larutan amaran 1.1249x10
-5M oleh biosorben AE ... 6
7 Adsorpsi larutan amaran 1.1249x10
-5M oleh arang aktif ... 7
8 Adsorpsi larutan biru metilen 1.1255x10
-5M oleh berbagai biosorben ... 7
9 Adsorpsi larutan amaran 1.1249x10
-5M dengan penambaha n kuat ion... 7
10 Adsorpsi larutan biru metilen 1.1255x10
-5M dengan penambahan kuat ion 8
11 Adsorpsi larutan amaran 1.1249x 10
-5M dengan perubahan pH ... 8
12 Adsorpsi larutan biru metilen 1.1255x 10
-5M dengan perubahan pH... 8
13 Isoterm adsorpsi larutan amaran oleh biosorben AA... 8
DAFTAR LAMPIRAN
Halaman
1 Bagan alir penelitian... 12
2 Kadar air ampas teh... 13
3 Kurva standar ... 13
4 Isoterm adsorpsi larutan amaran oleh biosorben TA... 19
5 Isoterm adsorpsi larutan amaran oleh berbagai biosorben... 20
6 Isoterm adsorpsi larutan amaran oleh arang aktif ... 20
7 Isoterm adsorpsi larutan biru metilen oleh biosorben TA ... 20
8 Isoterm adsorpsi larutan biru metilen oleh biosorben AA ... 20
9 Isoterm adsorpsi larutan biru metilen ole h biosorben AB ... 20
10 Isoterm adsorpsi larutan biru metilen oleh biosorben AE ... 20
1
PENDAHULUAN
Limbah cair merupakan masalah utama dalam pengendalian dampak lingkungan in-dustri tekstil. Masuknya zat warna dari limbah ke perairan mengakibatkan karakter fisika dan kimia dari sumber daya air berubah. Agar dapat memenuhi baku mutu, limbah cair harus diolah secara terpadu, baik yang dihasilkan selama proses produksi maupun setelah proses produksi.
Pengelolaan limbah cair di dalam proses produksi dimaksudkan untuk meminimalkan volume, konsentrasi, dan toksisitas limbah. Pengelolaan limbah cai r setelah proses produksi dimaksudkan untuk menghilangkan atau menurunkan kadar bahan pencemar yang terkandung di dalamnya, sampai limbah cair memenuhi syarat untuk dapat dibuang (memenuhi baku mutu yang ditetapkan).
Pengelolaan limbah cair yang paling banyak dilakukan oleh pabrik tekstil adalah koagulasi (penggumpalan) yang diikuti ad-sorpsi bahan pencemar dengan melewatkan air limbah melalui zeolit dan arang aktif (Forlink 2000).
Adsorpsi merupakan peristiwa penjerapan suatu zat pada permukaan zat lain yang terjadi karena adanya ketidakseimbangan gaya tarik pada permukaan zat tersebut (Siaka 2002). Zat yang menjerap disebut adsorben, sedangkan zat yang tejerap disebut adsorbat. Adsorben dapat berupa zat padat maupun zat cair. Adsorben padat diantaranya ad alah silika gel, alumina, platina halus, selulosa, dan arang atau arang aktif. Adsorbat dapat berupa gas dan zat cair. Penelitian ini menggunakan larutan zat warna sebagai adsorbat.
Adsorben dapat digunakan di bidang industri pangan maupun non pangan. Beberapa kegunaan adsorben diantaranya adalah untuk memurnikan udara dan gas, memurnikan pelarut, penghilangan bau dalam pemurnian minyak nabati dan gula, penghilangan warna produk -produk alam dan larutan (Lynch 1990), serta untuk penjerap zat warna dalam pengolahan limbah industri tekstil. Berkembangnya industri tersebut diikuti dengan makin tingginya kebutuhan terhadap adsorben. Demikian pula kebutuhan terhadap arang aktif sebagai salah satu jenis adsorben juga akan terus meningkat dan belum bisa terpenuhi secara maksimum. Untuk mengatasi hal tersebut perlu diupayakan
keragaman sumber bahan baku adsorben sehingga dapat mengimbangi kebutuhan industri-industri terhadap adsorben.
Teh merupakan sumber devisa bagi beberapa negara berkembang. Khususnya di
Srilanka, India dan Cina, Industri teh
merupakan penyumbang sangat penting dalam pendapatan nasional masing-masing negara tersebut. Indonesia sebagai salah satu negara berkembang menerima devisa dari ekspor teh sebesar 7.4% dari penerimaan total devisa dari ekspor.
Pemanfaatan teh masih sangat terbatas dan dalam ruang lingkup yang kecil. Bidang peternakan menggunakan teh sebagai tambahan dalam pembuatan kompos (Soilfoodweb 2001) dan tambahan dalam pakan ternak (Fiberti 2002). Sebagai bahan baku adsorben alternatif, ampas teh telah digunakan untuk menjerap ion logam dengan keefektifan sampai 100% (Mahvi 2005).
Penelitian ini bertujuan mengkaji kemam-puan ampas teh sebagai penjerap zat warna dengan menggunakan larutan amaran dan biru metilena sebagai model dan melihat pengaruh kuat ion serta pH terhadap daya adsorpsinya.
Dua manfaat yang akan diperoleh dari kegiatan ini adalah perolehan sumber adsorben alternatif baru dan penanganan limbah industri zat warna. Teh sebagai bahan alami aman bagi lingkungan, ampasnya mudah didapat sebagai limbah industri minuman teh.
TINJAUAN PUSTAKA Teh
Tanaman teh berasal dari spesies Camellia sinensis dan famili Tehaceae (Ullah 1991). Jenis teh pada dasarnya hanya terdiri atas tiga kelompok utama, yaitu teh hitam, teh oolong, dan teh hijau (Changjaya 2002).
Daun teh segar mengandung senyawaan seperti polisakarida, lemak, vitamin, mineral, purin, kafein, dan polifenol (katekin dan flavonoid). Proses pembuatan teh menjadi teh hitam, teh oolong, dan teh hijau menyebabkan perubahan komposisi senyawa dalam daun teh. Teh hijau memiliki kadar katekin tertinggi dibanding dua jenis teh lainnya. Proses fermentasi dalam pembuatan teh hitam merusak asam askorbat dan membuat kadar katekinnya terendah (Tourle 2003).
Ampas teh mengandung protein kasar 27.42% (persen dalam berat kering), lemak 3.26%, kobalt 1.14%, fosfor 0.25%, dan serat kasar 20.39% (Fiberti 2002). Tingginya kadar
2
serat dalam ampas teh ini dimanfaatkan sebagai pakan ternak.
Ampas teh juga dapat digunakan sebagai kompos. Adanya penambahan ampas teh ini menyebabkan terbangunnya struktur tanah, sehingga mengurangi erosi. Pengaruh positif lainnya terhadap tanaman, yaitu membantu tanaman mengambil zat -zat hara yang dibutuhkan, menekan penyakit, dan mengurangi hilangnya nutrisi yang terdapat dalam air yang akan diserap tanaman tersebut (Soilfoodweb 2001).
Mahvi (2005) menggunakan ampas te sebagai adsorben untuk logam berat timah, kadmium, dan nikel. Efektivitas ampas teh untuk ketiga logam ini, baik dalam bentuk tunggal maupun campuran, bervariasi dari 77.2% hingga mencapai 100%.
Umumnya adsorben dari bahan alam diaktivasi terlebih dahulu untuk meningkatkan kinerjanya. Aktivasi adsorben bertujuan untuk meningkatkan kapasitas dan efisiensi adsorpsi dari adsorben. Aktivasi dapat dilakukan dengan memberi perlakuan kimia seperti direaksikan dengan asam dan basa juga dengan perlakuan fisika seperi pemanasan dan pencucian. Biomassa seperti kulit singkong dapat dicuci dengan asam untuk mengaktivasi selulosanya (Horsfall 2003). Pencucian dengan alkohol bertujuan menghilangkan pengotor dari adsorben dan diharapkan meningkatkan kemampuan adsorpsi dari adsorben.
Adsorpsi
Adsorpsi merupakan peristiwa terakumulaisnya partikel pada permukaan (Atkins 1994). Partikel yang terakumulasi dan diserap oleh permukaan disebut adsorbat dan material tempat terjadinya adsorpsi disebut adsorben (Satake 1990). Adsorben yang terbuat dari material biomassa umum disebut sebagai biosorben.
Ukuran pori dan luas permukaan adsorben merupakan hal yang sangat penting dalam adsorpsi (Lynch 1990). Perbesaran luas permukaan adsorben dapat dilakukan dengan pengecilan partikelnya.
Adsorpsi molekul zat terlarut dari larutan oleh permukaan padatan biasanya hanya membentuk monolayer. Pembentukan multilayer pada adsorpsi semacam ini sangat jarang ditemukan. Adsorben polar cenderung mengadsorpsi adsorbat polar secara kuat, dan mengadsorpsi adsorbat non polar secara lemah. Sebaliknya, adsorben non polar cenderung untuk mengadsorpsi
secara kuat adsorbat non polar dan mengadsorpsi adsorbat polar secara lemah (Bird 1993).
Molekul dan atom dapat menempel pada permukaan dengan dua cara, yaitu fisisorpsi dan kimisorpsi. Tabel 1 memperlihatkan perbedaan keduanya.
Tabel 1 Perbedaan fisisorpsi dan kimisorpsi
Fisisorpsi Kimisorpsi - Ikatannya lemah dengan jarak pendek - Permukaan tidak selektif - H ads = 5-50 kJ mol-1 Adsorpsi multi -layer
- Ikatan kuat, jarak pendek - Permukaannya se-lektif - Hads = 50-500 kJ mol-1 - Adsorpsi monolayer
Isoterm Adsorpsi. Adsorpsi sering
dirangkaikan dengan istilah isoterm, yang menunjukkan hubungan antara aktivitas (konsentrasi) fase cair dari adsorbat dan jumlah adsorbat pada suhu konstan. Isoterm menggambarkan kesetimbangan yang tercapai setelah permukaan adsorben mengadakan kontak dengan adsorbat dia jangka waktu tertentu dan suhu tetap.
Isoterm adsorpsi Freundlich. Isoterm adsorpsi
Freundlich sering digunakan dalam pembahasan adsorpsi dari larutan cair (Atkins)1994.
Isoterm adsorpsi freundlich menggambarkan hubungan antar logaritmik dari sejumlah komponen yang teradsorpsi per unit adsorben dengan konsentrasi komponen tersebut pada kesetimbangan suhu konstan.
Freundlich memformulasikan persamaan isotermnya sebagai berikut
X /M = k c 1/n
X adalah jumlah zat terlarut yang diadsorpsi padatan bermassa M, c k onsentrasi larutan pada kesetimbangan dan n, k adalah konstanta (Bird 1993). Besarnya nilai n adalah kurang dari satu. Persamaan di atas dapat juga ditulis dalam bentuk:
Log (X / M) = 1/ n log c + log k
Konstanta n dan k menunjukkan ikatan antara adsorben dan adsorbat.
Isoterm adsorpsi digunakan untuk men-jelaskan hubungan zat warna yang terdasorpsi pada adsorben dengan konsentrasi dari molekul
3
zat warna bebas dalam larutan. Isoterm adsorpsi juga dapat menjelaskan kapasitas adsorpsi, yaitu seberapa besar ads orben mampu menjerap zat warna.
Karbon aktif
Struktur karbon aktif dapat digambarkan lebih tepat sebagai jaringan yang tumpang tindih dari dataran lapisan karbon dengan ikatan silang oleh gugus jembatan alifatik. Difraksi sinar x memperlihatkan bahwa kar bon aktif bersifat nongrafitik dan amorf. Hal ini memeberikan suatu sifat yang unik, disebut struktur pori internal yang mudah dipenetrasi. Mikropori merupakan jenis pori yang dianggap penting karena sebagian besar adsorpsi terjadi di dalamnya. Mikropori adalah ruang dua dimensi yang terbentuk dari dua dinding seperti grafit, bidang planar kristalit yang disusun oleh gugus aromatik atom-atom karbon. Karbon aktif memiliki struktur kristalit yang kurang teratur disebut struktur turbostatik. Mikropori ini merupakan salah satu kelebihan dari karbon aktif.
Keistimewaan lain dari karbon aktif adalah gugus fungsional pada permukaannya. Gugus kompleks oksigen yang terletak di permukaan membuat permukaan karbon aktif menjadi reaktif secara kimiawi dan menentukan sifat adsorpsinya seperti hidrofilik, keasaman dan potensial negatif (Setiadi 1999).
Kuat Ion
Jika suatu spesies ionik teradsorpsi pada suat permukaan, maka untuk mempertahanka kenetralan listriknya permukaan harus mengadsorpsi pasangan ionnya. Muatan permukaan dan pasangan ionnya ini membentuk lapisan listrik rangkap. Pasangan ion teradsorpsi melalui gaya tarik Coulomb atau elektrostatik pada permukaan karena melawan ion-ion penentu potensial.
Ionisasi permukaan pada proses adsorpsi menyebabkan permukaan menjadi bermuatan. Permukaan ini dinetralkan muatannya dan diamati sebagai fungsi pH dan kuta ion. Kuat ion dipengaruhi oleh konsentrasi dari seluruh spesies yang ada dan muatannya. Makin besar kuat ion, aktivitas ion makin berbeda.
Ion-ion H+ dan OH- memegang peranan penting sebagai reaktan dalam proses ionisasi pusat-pusat permukaan dan dalam
pelarut air. Besarnya muatan permukaan akan meningkatkan dan potensial permukaan menurun dengan meningkatnya kuat ion (Anggraningrum 1996).
pH
pH adalah istilah yang akan digunakan untuk menggambarkan aktivitas ion hidrogen dari suatu sistem. Nilai pH mempengaruhi keefektifan adsorpsi selain kuat ion, aktivasi adsorben, dan konsentrasi larutan (Wu 1998). Wu (1998) menemukan bahwa semakin tinggi pH maka adsorpsi ion tembaga oleh karbon aktif juga semakin besar. Citroreksoso (1994) menyimpulkan bahwa daya adsorpsi optimum terhadap anion kromat bergantung pada pH dan jenis adsorbennya.
Zat Warna
Zat warna tekstil merupakan senyawa organik (McGraw Hill 1993) yang keberada annya dalam perairan dapat mengganggu ekosistem di dalamnya. Sebelum dibuang ke perairan, limbah cair yang berwarna ini akan diproses terlebih dahulu sampai konsentrasinya cukup aman di perairan. Contoh, sebuah pabrik tekstil menurunkan kadar zat warna reaktif dalam limbahnya dari 225 ppm hingga 0.17 ppm setelah melalui proses koagulasi.
Amaran. Amaran adalah zat warna yang
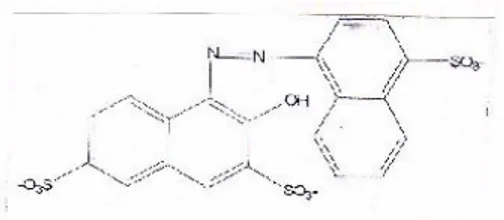
digunakan pada industri tekstil yang pada kadar tertentu masih aman digunakan untuk makanan. Nama kimia untuk amaran adalah trisodium 2-hidroksi-1-(4-sulfonat-1-naftilazo) naftalena 3,6-disulfonat dengan bobot molekul sebesar 604.48. Amaran juga dikenal dengan nama CI Food Red 9, FD & C Red 2, dan Acid Red 27 (Saujanya 2000).
Amaran tersedia secara komersil dengan kemurnian sekitar 85% (Saujanya 2000). Senyawa ini juga mengandung logam-logam berat seperti merkuri, arsenat, timah, serta kadmium dengan konsentrasi satu sampai sepuluh ppm.
Gambar 1 Struktur senyawa amaran (Saujanya 2000).
4
Interaksi amaran dan air menghasilkan ion yang bermuatan negatif. Anion dari amaran berinteraksi dengan adsorben dan menurunkan intensitas warna larutan tersebut.
Biru Metilena. Biru metlena digunakan
sebagai pewarna dalam bakteriologi, sebagai reagen analitis, indicator oksidasi -reduksi, antimetem oglobin, antidote sianida, dan sebagai antiseptik.
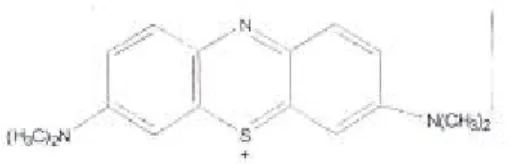
Biru metilena juga dikenal dengan nama fenotiazin -5-ium, 3,7-bis (dimetilamino)-klorida; C.I. Basic Blue 9 Sandocryl Blue BRL; tetrametiltionin klorida; dan Yamamoto Methylene Blue ZF C.I 52015.
Dosis tinggi dari biru metilena dapat menyebabkan mual, muntah, nyeri pada mulut dan dada, sakit kepala, keringat berlebihan, dan hipertensi (RSC 1992).
Interaksi biru metilena dengan air akan menghasilkan ion dari biru metilena yang bermuatan positif. Kation yang dihasilkan akan berinteraksi dengan adsorben. Adanya interaksi antara ion dan adsorben akan menurunkan intensitas warna larutan.
Gambar 2 Struktur kation biru metilena (RSC 1992).
BAHAN DAN METODE Bahan dan Alat
Bahan-bahan yang digunakan adalah ampas teh , H2SO4 85%, HCl 37%, HNO3
65%, etanol 97%, kristal kalium nitrat, kristal natrium hidroksida, serbuk amaran, serbuk biru metilena, air deionisasi, dan karbon aktif komersial.
Alat-alat yang dipakai adalah spektrofotometer UV-Vis, konduktometer, pH meter, neraca analitik, pengaduk magnet, oven, eksikator, blender, plat pemanas, dan alat-alat kaca.
Metode Penelitian Pembuatan Serbuk Ampas Teh
Ampas teh dari limbah minuman teh dicuci di air mengalir selama 24 jam.
Setelah dikeringudarakan, digiling hingga menjadi serbuk dan di ayak (Lampiran 1). Serbuk ampas teh ini selanjutnya disebut ampas teh tanpa pencucian.
Analisis kadar Air Ampas Teh
Ampas teh sebanyak 1 g yang sudah dibersihkan dan dikeringudarakan, ditempatkan dalam cawan petri yang tela h dikeringkan dalam oven dan telah diketahui bobot kosongnya. Cawan Petri berisi sampel dikeringkan dalam oven pada suhu 105 °C selama 3 jam dan didinginkan. Setelah dingin, disimpan dalam eksikator, lalu ditimbang. Analisis dilakukan tiga kali ulangan (Lampiran 2). Kadar air dihitung sebagai berikut:
Kadar air = a-b c Keterangan
a: bobot sample dan cawan petri sebelum dikeringkan
b: bobot sample dan cawan petri sesudah dikeringkan
c: bobot sampel
Pembuatan Larutan Zat Warna
Sebanyak 0.0068 g serbuk amaran dan 0.0036 g sebuk biru metilena dilarutkan dalam air destilata dan diencerkan hingga satu liter. Kemudian kedua larutan dibuat kurva standarnya (Lampiran 3).
Pencucian Adsorben
Tiga gelas piala 1 L masing-masing dimasukkan 100 g serbuk ampas teh dan ditambah air deionisasi 660 mL. Campuran dikocok selama 20 menit kemudian airnya dibuang. Pencucian diulang sebanyak dua kali, selanjutnya dikeringkan dalam oven pada suhu 50 °C selam 24 jam (Dewi 2005). Masing-masing sampel kemudian dicuci dengan asam nitrat 0.6 M, NaOH 0.6 M dan etanol. Caranya adalah sebagai berikut. Sampel yang telah dicuci dengan air deionisasi dimasukkan dalam gelas piakla 1 L dan ditambah 660 mL asam. Campuran dikocok selama 30 menit, dan disaring. Sampel dikeringkan dalam oven pada suhu 50 °C selama 24 jam, kemudian suhu dinaikkan 180 °C dan didinginkan. Sampel kemudian dicuci dengan air panas, disaring dan dikeringkan dalam oven pada suhu 50 °C selama 24 jam. Ketiga sampel yang dihasilkan selanjutnya disebut ampas teh dengan pencucian asam (AA). Ampas teh pencucian basa (AB), dan ampas teh pencucian etanol (AE).
5
Penentuan Bobot Optimum Adsorben dan Waktu Optimum Adsorpsi
Biosorben TA, AA, AB, dan AE masing-masing seberat 0.1, 0.2, dan 0.4 g dimasukan ke dalam erlenmeyer yang berisi 100 mL
larutan amaran 1.1249x10-5 M. Setelah
didiamkan selama 6 jam, larutan disaring kemudian diukur absorbansnya pada panjang gelombang (ë) maksimum. Hal yang sama dilakukan pada variasi waktu 12, 24, dan 30 jam (Lukito 1996).
Dua belas erlenmeyer 125 mL masing-masing dimasukkan 0.1, 0.2, dan 0.4 g biosorben TA, AA, AB, dan AE. Kemudian ditambahkan 100 mL larutan biru metilena 1.1255x10-5 M . Setelah itu campuran diaduk selama 2 jam (ASTM 1995), kemudian disaring. Filtrat yang didapat diukur absorbansnya pada ë maksimum.
Jumlah zat warna yang terjerap dihitung melalui persen (%) removal dengan rumus :
Removal (%) = Co - C x100% Co
Co = konsentrasi awal larutan (ppm)
C = konsentrasi akhir larutan (ppm)
Pengaruh Kuat Ion terhadap Adsorpsi
Tiga Erlenmeyer yang berisi masing-masing 100 mL, larutan amaran 1.1249x10-5 M dan 10 mL KNO3 0.01, 0.10 dan 1.00 M,
ditambahkan 0.4 g biosorben TA. Setelah didiamkan selama 24 jam, larutan disaring
dan diukur absorbansnya pada ë maksimum.
Untuk biosorben AA, biosorben yang ditambahkan 0.4 g dan waktu adsorpsi 6 jam. Biosorben AB dan AE ditambahkan masing-masing 0.1 g dengan waktu adsorpsi masing-masing 24 dan 6 jam.
Dua belas erlenmeyer yang berisi
masing-masing 100 mL, larutan biru
metilena 1.1255x10-5 M dan 10 mL KNO3
0.01, 0.10, dan 1.00 M, ditambahkan 0.2 g biosorben TA dan AB, dan 0.1 g untuk biosorben AA dan AE. Campuran dikocok selama 2 jam kemudian disaring dan diukur absorbansnya pada ë maksimum.
Pengaruh pH terhadap Adsorpsi
Sebanyak 0.4 g biosorben TA ditambahkan ke dalam erlenmeyer yang berisi 100 mL larutan amaran 1.1249x10-5 M dengan pH 4, 7, dan 10. Setelah 24 jam larutan disaring dan diukur absorbansnya
pada ë maksimum. Untuk biosorben AA
jumlah yang ditambahkan 0.4 g dan waktu adsorpsi 6 jam. Biosorben AB dan AE
ditambahkan masing-masing 0.1 g dengan waktu adsorpsi masing-masing 24 jam dan 6 jam.
Dua belas erlenmeyer yang masing-masing berisi 100 mL larutan biru metilena 1.1255x10-5 M dengan pH 4, 6, dan 8, ditambahkan masing-masing 0.2 g biosorben TA dan AB, dan 0.1 g untuk biosorben AA dan AE. Campuran dikocok selama 2 jam, kemudian disaring dan diukur absorbansnya.
Penentuan Isoterm Adsorpsi
Isoterm adsorpsi ditentukan sebagai berikut. Erlenmeyer yang berisi 0.4 g biosorben (untuk biosorben TA dan AA 0.1 g untuk biosorben AB dan AE) dimasukkan 100 mL larutan amaran dengan konsentrasi 1, 5, 10, 20, dan 25 ppm. Setelah waktu yang ditetapkan (24 jam untuk biosorben TA dan AB dan 6 jam untuk AA dan AE), larutan disaring dan diukur absorbansnya.
Untuk larutan biru metilena isoterm adsorpsi ditentukan sebagai berikut. Erlenmeyer yang masing-masing berisi 0.1 g adsorben TA dan AB, serta 0.1 g adsorben AA dan AE dimasukkan 100 mL larutan biru metilena dengan konsentrasi 0.5, 1, 5, dan 10 ppm. Setelah pengocokan selama 2 jam larutan
disaring dan diukur absorbansnya pada ë
maksimum.
Panjang gelombang maksimum untuk larutan amaran adalah 515 nm dan larutan biru metilena 665 nm.
Isoterm adsorpsi dilakukan pada p H adsorpsi maksimum. Arang aktif sebagai pembanding diperlakukan sama seperti halnya ampas teh sebagai biosorben.
HASIL DAN PEMBAHASAN Penentuan Bobot Optimum Adsorben dan
Waktu Optimum Adsorpsi
Ampas teh yang merupakan limbah industri minuman teh digunakan sebagai biosorben larutan amaran dan larutan biru metilena. Pencucian yang dilakukan terhadap ampas teh adalah pencucian asam, pencucian basa, dan pencucian alkohol.
Semakin banyak jumlah biosorben maka ketersediaan pori dan luas permukaan aktif dari biosorben juga meningkat. Bertambahnya pori dan sisi-sisi aktif dari permukaan memungkinkan adsorpsi terjadi di banyak tempat dari permukaan biosorben. Meningkatnya jumlah biosorben menyebabkan nilai persen (%) removal juga semakin besar.
6
Pengaruh waktu adsorpsi dapat dilihat dari nilai % removal yang meningkat dengan lamanya waktu adsorpsi. Nilai % removal akan mencapai titik optimum, namun nilainya kembali turun ketika melewati waktu kesetimbangannya. Turunnya nilai % removal dimungkinkan karena adanya proses desorpsi.
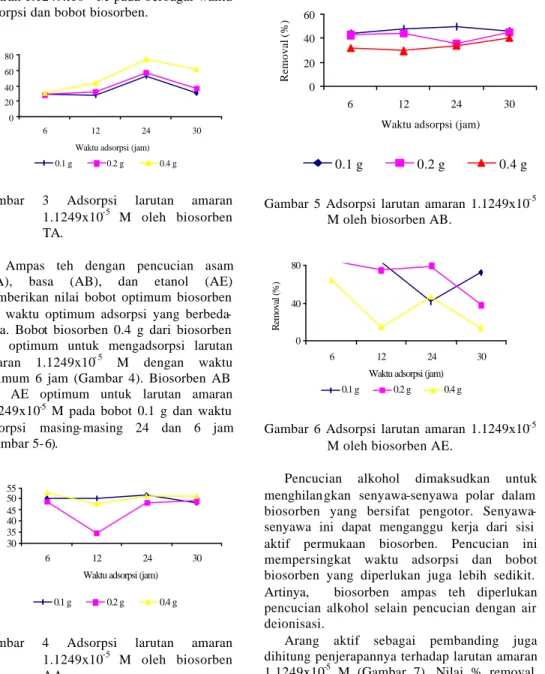
Bobot optimum biosorben ampas teh tanpa pencucian (TA) dan waktu optimum adsorpsi untuk larutan amaran adalah 0.4 g dan 24 jam. Gambar 3 memperlihatkan nilai % removal biosorben TA terhadap larutan amaran 1.1249x10-5 M pada berbagai waktu adsorpsi dan bobot biosorben.
0 20 40 60 80 6 12 24 30
Waktu adsorpsi (jam)
Removal (%)
0.1 g 0.2 g 0.4 g
Gambar 3 Adsorpsi larutan amaran
1.1249x10-5 M oleh biosorben
TA.
Ampas teh dengan pencucian asam (AA), basa (AB), dan etanol (AE) memberikan nilai bobot optimum biosorben dan waktu optimum adsorpsi yang berbeda-beda. Bobot biosorben 0.4 g dari biosorben AA optimum untuk mengadsorpsi larutan
amaran 1.1249x10- 5 M dengan waktu
optimum 6 jam (Gambar 4). Biosorben AB dan AE optimum untuk larutan amaran 1.1249x10-5 M pada bobot 0.1 g dan waktu adsorpsi masing-masing 24 dan 6 jam (Gambar 5-6). 30 35 40 45 50 55 6 12 24 30
Waktu adsorpsi (jam)
Removal (%)
0.1 g 0.2 g 0.4 g
Gambar 4 Adsorpsi larutan amaran
1.1249x10-5 M oleh biosorben
AA.
Pada waktu optimum, sisi aktif dari biosorben AA meningkat akibat pencucian. Sehinggga adsorbat larutan amaran yang terjerap lebih banyak. Adanya pengaruh pencucian asam terhadap kapasitas adsorpsi juga disampaikan oleh Wu (1998).
Pencucian basa meningkatkan kinetika adsorpsi (Wu 1998). Biosorben AB membutuhkan bobot yang lebih sedikit untuk mencapai % removal terbesarnya, yaitu 0.1 g. Adsorpsi oleh biosorben , meskipun bobot biosorben yang digunakan lebih sedikit.
0 20 40 60
6 12 24 30 Waktu adsorpsi (jam)
Removal (%)
0.1 g 0.2 g 0.4 g
Gambar 5 Adsorpsi larutan amaran 1.1249x10-5 M oleh biosorben AB.
0 40 80
6 12 24 30
Waktu adsorpsi (jam)
Removal (%)
0.1 g 0.2 g 0.4 g
Gambar 6 Adsorpsi larutan amaran 1.1249x10-5 M oleh biosorben AE.
Pencucian alkohol dimaksudkan untuk menghilan gkan senyawa-senyawa polar dalam biosorben yang bersifat pengotor. Senyawa-senyawa ini dapat menganggu kerja dari sisi aktif permukaan biosorben. Pencucian ini mempersingkat waktu adsorpsi dan bobot biosorben yang diperlukan juga lebih sedikit. Artinya, biosorben ampas teh diperlukan pencucian alkohol selain pencucian dengan air deionisasi.
Arang aktif sebagai pembanding juga dihitung penjerapannya terhadap larutan amaran
1.1249x10-5 M (Gambar 7). Nilai % removal
arang aktif terbesar adalah 93.90% pada waktu adsorpsi 24 jam dan bobot biosorben 0.1 g.
7
Biosorben AE dengan % remoal 90.51% cukup efisien sebagai adsorben allternatif untuk larutan amaran dengan konsentrasi
1.1249x10-5 M, meskipun keefektifannya
masih di bawah arang aktif.
8 5 9 0 9 5
6 1 2 2 4 3 0 waktu adsorpsi (jam)
Removal (%)
0.1 g 0.2 g 0.4 g
Gambar 7 Adsorpsi larutan amaran 1.1249x10-5 M oleh arang aktif. Metode yang berbeda diberikan terhadap larutan biru metilena. Adsorpsi dilakukan dengan waktu pengadukan 2 jam. Biosorben TA dan AB bekerja maksimum pada bobot 0.2 g dan biosorben TA serta AE di 0.1 g (Gambar 8). Meningkatnya kapasitas adsorpsi akibat pencucian asam dan alkohol mengakibatkan bobot biosorben yang diperlukan untuk mencapai kesetimbangan lebih sedikit. 0 30 60 90 TA AA AB AE Arang aktif Jenis biosorben Removal (%) 0.1 g 0.2 g 0.4 g
Gambar 8 Adsorpsi larutan biru metilena 1.1255x10-5 M oleh berbagai biosorben.
Secara umum jumlah adsorbat larutan biru metilena yang terjerap lebih banyak dibandingkan amaran. Hal ini menunjukkan biosorben ampas teh lebih baik digunakan sebagai penjerap larutan biru metilena dibandingkan larutan amaran. Artinya, biosorben ampas teh lebih selektif terhadap biru metilena.
Perlakuan pencucian asam dan basa terhadap biosorben ampas teh memberikan hasil yang kurang baik dibandingkan yang tanpa pencucian. Penambahan kuat ion dan perubahan pH dilakukan dalam upaya meningkatka n adsorpsi.
Pengaruh Kuat Ion terhadap Adsorpsi
Penambahan ion dapat meningkatkan jumlah larutan zat warna yang diadsorpsi. Peningkatan % removal akibat penambahan KNO3 0.10 M pada larutan amaran 1.1249x10-5
M terjadi pada biosorben AA dari 52.54% menjad i 54.33% (Lampiran 10). Pengaruh KNO3 ini tidak terlihat di biosorben lainnya
(Gambar 9). 0 20 40 60 80 100 TA AA AB AE Arang aktif Jenis biosorben Removal (%) 0.00 M 0.01 M 0.10 M 1.00 M
Gambar 9 Adsorpsi larutan amaran 1.1249x10-5 M dengan penambahan kuat ion. Berbeda dengan larutan amaran,
panambahan KNO3 meningkatkan % removal
larutan biru metilena oleh semua jenis biosorben (Gambar 10). Perubahan nilai % removal akibat penambahan KNO3 pada larutan
amaran dan biru metilena bisa disebabkan oleh dua hal. Pertama kompetisi ionik. Jason (2004) menuliskan bahwa karbon aktif menunjukkan pola adsorpsi yang berbeda, bergantung pada anion dan kationnya. Dalam penelitian ini, biosorben AA dapat meningkat adsorpsinya baik baik untuk larutan amaran maupun biru metilena, sedangkan biosorben lainnya hanya dapat meningkatkan adsorpsi larutan biru metilena. Hal ini menunjukkan biosorben ampas teh lebih selektif terhadap kation biru metilena. Turunnya % removal oleh biosorben TA, AB, dan AE pada larutan amaran disebabkan
biosorben cenderung menjerap ion NO3
karena anion amaran berikatan dengan ion K+.
75 80 85 90 95 100 TA AA AB AE Arang aktif Jenis biosorben Removal (%) 0.00 M 0.01 M 0.01 M 1.00 M
Gambar 10 Adsorpsi larutan biru metilena
1.1255x10-5 M dengan
8
Pengaruh pH terhadap Adsorpsi
pH mempengaruhi kapasitas adsorpsi (Jason 2004). pH memegang peranan penting dalam karakteristik adsorpsi karena pH yang rendah akan menyediakan jumlah
ion H+ yang disukai dalam jumlah yang
besar. Ion H+ dapat mengambil ruang pada sisi permukaan untuk ion lainnya. Keadaan ini menyebabkan menurunnya adsorpsi amaran oleh seluruh biosorben dan biru metilena oleh biosorben TA dan AE.
Variasi pH yang diujicobakan pada larutan amaran tidak dapat meningkatkan adsorpsinya (Gambar 11). Tapi variasi ini dapat meningkatkan adsorpsi larutan biru metilena oleh biosorben AA dan AB (Gambar 12). pH dapat meningkatkan adsorpsi jika kompetisi antara proton dan ion biru metilena pada sisi permukaan biosorben AA dan AB menurun.
0 20 40 60 80 1 0 0 T A A A A B A E Arang aktif Jenis biosorben Removal (%) pH awal pH 4 pH 7 pH 10
Gambar 11. Adsorpsi larutan amaran
1.1249x 10-5 M dengan perubahan pH. 75 80 85 90 95 100 TA AA AB AE Arang aktif Jenis biosorben Removal (%) pH awal pH 4 pH 6 pH 8
Gambar 12. Adsorpsi larutan biru metilena
1.1255x 10-5 M dengan
perubahan pH.
Penentuan Isoterm Adsorpsi
Kapasitas adsorpsi dipelajari melalui tipe isotermnya. Kurva regresi linier adsorpsi Freundlich dibuat berdasarkan data konsentrasi adsorbat (larutan zat warna) sebelum dan sesudah adsorpsi serta bobot biosorben.
Larutan amaran yang diadsorpsi oleh biosorben AA me mberikan kurva regresi dengan kelinieran sebesar 97.36% (Gambar 13). Tingginya nilai ini menunjukkan adsorpsi berlangsung secara fisisorpsi.
y = 3.1232x - 4.1845 R2 = 0.9736 -1.2 -0.8 -0.4 0 0.4 0 0.5 1 1.5 log C log X/M
Gambar 13 Isoterm adsorpsi larutan amaran oleh biosorben AA.
Freundlich mengasumsikan adsorpsi fase padat-cair berlangsung secara adsorpsi multilayer. Dalam fisisorpsi, ikatan antara adsorbat maupun ikatan antar adsorbat dengan adsorben bersifat lemah karena hanya melibatkan interaksi Van der Waals.
Biosorben lain, yaitu TA, AB, dan AE mengalami desorpsi. Hal ini terlihat dari bertambahnya konsentrasi zat warana amaran bebas dalam larutan. (Lampiran 4). Naiknya konsentrasi zat warna bebas pada larutan ditandai dengan bertambahnya kekeruhan pada warna larutan. Hal ini menunjukkan pencucian basa tidak cocok dilakukan untuk biosorben ampas teh. Perlakuan pencucian asam dan basa dapat merusak selulosa yang terdapat dalam ampas teh, komponen yang berperan dalam adsorpsi zat warna oleh biosorben. Akibatnya pencucian ini justru mendeaktivasi permukaan biosorben.
Biru metilena dapat diadsorpsi dengan baik oleh biosorben TA, AA, AB, dan AE Akan tetapi pola penjerapannya kurang baik. Hal ini terlihat dari kelinieran kurva yang rendah (Lampiran 7-11). Kurang baiknya pola penjerapan biru metilena ol eh biosorben dapat diakibatkan waktu kontak antara biru metilena dan biosorben belum maksimum. Artinya perlakuan dua jam belum memenuhi kesetimbangan adsorpsi antara biru metilena dan biosorben.
Bentuk logaritma dari persamaan Freundlich Log (X/M ) = 1/ n log C + log k
Persamaan di atas menunjukkan jumlah zat warna yang dijerap oleh ampas the (Log X/M ) berbanding terbalik dengan nilai konstanta n
9
dan berbanding lurus dengan konstanta k. Artinya jumlah zat warna yang dijerap akan semakin besar jika nilai konstanta n kecil dan nilai konstanta k besar.
Nilai konstanta n arang aktif pada larutan amaran kecil. Selain itu, nilai konstanta k arang aktif jauh lebih besar (Tabel 2). Oleh karena itu, larutan amaran dijerap lebih banyak oleh arang aktif dibandfing biosorben AA.
Larutan biru metilena juga dijerap dengan baik oleh arang aktif. Hal ini terlihat dengan besarnya nilai k pada arang aktif, meskipun harga n arang aktif juga besar. Biosorben AA menjerap larutan biru metilena paling sedikit dibanding biosorben lainnya. Hal ini terlihat dari nilai konstanta k biosorben AA yang sangat kecil. Dengan demikian arang aktif lebih efektif dalam menjerap kedua larutan dibandingkan dengan biosorben ampas teh.
Tabel 2 Nilai konstanta n dan k Bio-sorben n k R2 (%) Larutan amaran AA Arang aktif 0.3202 0.1923 6.5833x10-5 3.2900 97.36 58.86 Larutan biru metilena
TA AA AB AE Arang aktif -2.2873 -0.7501 0.1814 0.4666 0.4750 0.7898 0.0744 3.5571x104 4.0616x102 3.4770x104 0.42 17.97 82.78 65.30 88.22 Dapat terjerapnya biru metilena oleh semua biosorben menunjukkan ampas teh selektif terhadap zat warna ini dibandingkan dengan amaran. Keselektifan permukaan menunjukkan reaksi berlangsung secara kimisorpsi.
Selain tipe isoterm adsorpsi Freundlich, dikenal juga tipe isot erm adsorpsi Langmuir. Asumsi pada isoterm adsorpsi adalah adsorpsi berlangsung secara kimisorpsi monolayer. Pada adsorpsi jenis ini, ikatannya melibatkan tumpang tindih orbital dan transfer muatan. Permukaan adsorben pada kimisorpsi bersifat selektif. Adsorpsi dapat berlangsung menurut isoterm Freundlich dan isoterm Langmuir sekaligus.
Hal ini dapat diketahui jika linieritas kurva untuk kedua isoterm tinggi.
SIMPULAN DAN SARAN
Simpulan
Ampas teh, baik dengan pencucian maupun yang tidak, dapat digunakan sebagai adsorben larutan amaran dan biru metilena. Bobot terendah dan waktu adsorpsi tercepat dicapai oleh biosorben AE untuk larutan amaran dan biosorben AA untuk larutan biru metilena.
Perubahan kuat ion dan pH mempengaruhi daya adsorpsi ampas teh. Biosorben AA meningkat adsorpsinya tehadap larutan amaran
pada penambahan KNO3 1.00 M, sedangkan
penambahan KNO3 dengan konsentrasi dengan
konsentrasi yang berbeda-beda pada larutan biru metilena meningkatkan kemampuan adsorpsi seluruh biosorben. pH 4 meningkatkan adsorpsi biosorben AB terhadap larutan biru metilena dan pH 6 meningkatkan biosorben AA terhadap larutan yang sama.
Ampas teh lebih selektif terhadap larutan biru metilena. Adsorpsi larutan amaran oleh biosorben AA berlangsung secara fisisopsi dengan kelinieran sebesar 97.36%.
Saran
Penelitian ini dilakukan dengan menggunakan larutan tunggal. Penelitian selanjutnya dapat diujicobakan adsorpsi ampas teh pada larutan campuran. Selain itu dapat dilakukan uji coba kemampuan adsorpsi ampas teh terhadap zat warna tak bermuatan (netral).
DAFTAR PUSTAKA
Anggraningrum IT.1996. Model adsrpsi ion kompleks koordinasi nikel (II) pada permukaan alumina [tesis]. Jakarta: Magister Sains Ilmu Kimia. Universitas Indonesia.
[ASTM] American Society for Testing Materials. 1995. Standard practice for determination of adsorptive capacity of acyivated carbon of aqueous phase isotherm technique. Vol 15 (1). UK. Atkins PW. 1994. Physical Chemistry. Ed ke-5.
England: Oxford Univ Pr.
Bird T. 1993. Kimia Fisik untuk Universitas. Jakarta: Gramedia Pustaka Utama.
10
Changjaya. 2002. Teh berkhasiat obat. http//www.changjaya-abadi.com [13 Apr 2003].
Citroreksoso P, Yulianti PA, Muharini A, Sumekar H. 1994. Daya adsorpsi arang aktif terhadap anion kromium (VI) pada perubahan jenis dan bobot arang serta pH contoh. Prosiding Seminar Nasional III Kimia dalam Industri dan Lingkungan: 16-23.
Dewi IR. 2005. Modifikasi asam terhadap kulit singkong sebagai bioremoval logam Pb (II) dan Cd II). [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan, Institut Pertanian Bogor. Fiberti E. 2002. pengaruh benberapa tingkat
penggunaan ampas teh dalam ransum bentuk pellet terhadap performan kelinci persilangan lepas sapih [skripsi]. Bogor: Fakultas Peternakan, Institut Pertanian Bogor.
Forlink. 2000. Paket terapan produksi bersih pada industri tekstil. http://www.forlink. dml.or.id/pterapb/te. html 18k[22 Des 2004].
Jason PP. 2004. Activated carbon and some applications for the remediation soil and ground water pollution. http//www.cee.edu/program areas [8 Jun 2004].
Lukito L. 1996. Pembuatan adsorben
TiO2.Al2O3 dan pengujian daya
adsorpsinya terhadap ion CO (II) amoniakal [skripsi]. Jakarta: Fakultas Matematika dan Ilmu Pengetahuan Alam, Universitas Indonesia.
Lynch CT. 1990. Practical Handbook of Material science. Ed ke-2. New York: CRC Pr.
Mahvi AH, Naghipour D, Vaezi F, Nazmara S. 2005. Teawaste as an adsorben for heavy metal removal from industrial wastewaters. Am J App Sci 2(1):372-375. 21372-2(1):372-375.pdf [19 Jun 2005].
[McGraw-Hill]. 1993. McGraw-Hill Encyclop-edia of Chemistry. Ed ke-2. New York: McGraw-Hill.
[RSC] Royal Society of Chemistry. 1992. The Dictionary of substances and Their Effects . Vol Ke-1. England: Clays.
Satake M, Nagahiro T. 1990. Modern
Dictionary Physical Chemistry. New Delhi: Discovering.
Saujanya. 2000. Amaranth. http//www.sau-janya. com./gov/niosh/riecs/9j63. html -20k [13 April 2003].
Siaka M, Sukadana IM, Rahayu KS. 2002. Arang kulit kacang tanah sebagai adsorben alternatif untuk adsorpsi larutan nitrat. Chemical review: 67-73 Vol V. Universitas Udayana.
Setiadi, Sugiarso E. 1999. Pengaruh impregnan NaOH terhadap luasan permukaan karbon aktif dan kemampuan adsorpsi terhadap CO2. Di dalam: Fundamental dan Apl ikasi
Teknik Kimia. Prosiding seminar Nasional; Surabaya 24-25 Nov 1994. Depok: Universitas Indonesia A17: 1-7.
Soilfoodweb. 2001. Compost tea defined. http//www.soilfoodweb.com [4 mar 2003]. Tourle R. 2003. Camellia sinensis(Tea).
http//A:\Camellia%20sinensis%20(Tea). Htm [5 Nov 2003].
Ullah MR. 1991. Food Enzymologi . New York. Applied Sci.
Wu S, Paul C. 1998. Modification of commercial activated carbon for metal adsorption by several approaches. [Makalah Pribadi]. http//www.cee.vt.edu/journalshun-nianchen [20 Jan 2004].
11
12
Lampiran 1 Bagan alir penelitian
Ampas teh Analisis kadar air
Pencucian dengan air deionisasi
Pencucian asam Pencucian basa Pencucian etanol
Penentuan bobot optimum adsorben dan waktu optimum adsorpsi
Pengaruh kuat ion terhadap adsorpsi
Pengaruh pH terhadap adsorpsi
Penentuan isoterm adsorpsi Pembuatan serbuk
13
Lampiran 2 Kadar air ampas teh
ulangan a b c Kadar air
(%) 1 2 3 57.0427 59.4972 60.7192 56.8162 59.2578 60.4733 1.0093 1.0047 1.0082 22.44 23.83 24.39 Keterangan:
a: bobot sampel dan cawan petri sebelum dikeringkan b: bobot sampel dan cawan petri sesudah dikeringkan c: bobot sampel
Lampiran 3a Kurva standar larutan amaran (ë maksimum = 515 nm)
y = 0.0411x - 0.0270 R2 = 0.9826 -0.1 0.1 0.3 0.5 0.7 0 5 10 15 20 Konsentrasi (ppm) Absorbans
Lampiran 3b Kurva standar larutan metilen (ë maksimum = 665 nm) Konsentrasi (ppm) Absorbans 0.00 0.10 0.25 0.50 1.00 1.50 2.00 0.0000 0.0297 0.1158 0.2090 0.4365 0.6734 0.8239 y = 0.4254x + 0.0018 R2 = 0.9982 0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 0 0.5 1 1.5 2 2.5 Konsentrasi (ppm) Absorbans Konsentrasi (ppm) Absorbans 0.0 0.5 1.0 2.0 4.0 5.0 10.0 15.0 0.0000 0.0017 0.0315 0.0575 0.1013 0.1068 0.4485 0.5784
14
Lampiran 4 Isoterm adsorpsi larutan amaran oleh berbagai biosorben
TA AB AE Co (ppm) Absorbans akhir C (ppm) Co (ppm) Absorbans akhir C (ppm) Co (ppm) Absorbans akhir C (ppm) 1 5 10 20 25 0.0969 0.2034 0.3851 0.6345 0.5986 3.0150 5.6058 10.0268 16.0949 15.2214 1 5 10 20 25 0.1367 0.2708 0.4976 0.8013 0.7447 3.9830 7.2457 12.7640 20.1533 18.7762 1 5 10 20 25 0.0757 0.2034 0.4365 0.7594 0.8539 2.4988 5.6058 11.2774 19.1338 21.4331 Lampiran 5 Isoterm adsorpsi larutan amaran oleh biosorben AA
Co (ppm)
Absorbans
akhir C (ppm) Log C X (mg) X/M (mg/g) Log X/M
1 5 10 20 25 0.0799 0.1831 0.3706 0.7212 0.8297 2.6010 5.1119 9.6740 18.2044 20.8443 0.4151 0.7086 0.9856 1.2602 0.3190 0.0362 0.1796 0.4156 0.0815 0.4490 1.0390 -1.0888 -0.3477 0.0166 Lampiran 6 Isoterm adsorpsi larutan amaran oleh arang aktif
Co (ppm)
Absorbans
akhir C (ppm) Log C X (mg) X/M (mg/g) Log X/M
1 5 10 20 25 0.0070 0.0214 0.0168 0.0343 0.0114 0.8273 1.1776 1.0657 1.4915 0.9373 -0.0823 0.0710 0.0276 0.1736 -0.0295 0.0173 0.3822 0.8934 1.8509 2.4065 0.1730 3.8220 8.9340 18.5090 24.0650 -0.7619 0.5823 0.9510 1.2674 1.3814 Lampiran 7 Isoterm adsorpsi larutan biru metilen oleh biosorben TA
Co (ppm)
Absorbans
akhir C (ppm) Log C X (mg) X/M (mg/g) Log X/M
0.5 1 5 10 0.0958 0.1079 0.0726 0.0820 0.2210 0.2924 0.1664 0.1885 -0.6556 -0.3031 -0.7788 -0.7247 0.0279 0.0751 0.4834 0.9811 0.1395 0.6755 2.4170 4.9205 -0.8554 -0.4254 0.3833 0.3920 Lampiran 8 Isoterm adsorpsi larutan biru metilen oleh biosorben AA
Co (ppm)
Absorbans
akhir C (ppm) Log C X (mg) X/M (mg/g) Log X/M
0.5 1 5 10 0.0747 0.0241 0.0353 0.0381 -0.7660 -1.2807 -1.1051 -1.0691 0.0425 0.0948 0.4921 0.9915 0.0425 0.0948 0.4921 0.9915 0.4250 0.9480 4.9210 9.9150 -0.3716 -0.0232 0.6920 0.9963
15
Lampiran 9 Isoterm adsorpsi larutan biru metilen oleh biosorben AB
Co (ppm)
Absorbans
akhir C (ppm) Log C X (mg) X/M (mg/g) Log X/M
0.5 1 5 10 0.0585 0.0506 0.0799 0.0757 0.1333 0.1147 0.1360 0.1737 -0.8752 -0.9404 -0.7361 -0.7602 0.0367 0.0885 0.4816 0.9826 0.1835 0.4425 2.4080 4.9130 -0.7364 -0.3541 0.3816 0.6523 Lampiran 10 Isoterm adsorpsi larutan biru metilen oleh biosorben AE
Co (ppm) Absorbans
akhir C (ppm) Log C X (mg) X/M (mg/g) Log X/M
0.5 1 5 10 0.0195 0.0381 0.0655 0.0458 0.0416 0.0853 0.1497 0.1034 -1.3809 -1.0691 -0.8248 0.9897 0.0458 0.0915 0.4850 0.9897 0.4580 0.9150 4.8500 9.8970 -0.3391 -0.0386 0.6857 0.9955 Lampiran 11 Isoterm adsorpsi larutan biru metilen oleh biosorben AE
Co (ppm)
Absorbans
akhir C (ppm) Log C X (mg) X/M (mg/g) Log X/M
0.5 1 5 10 0.0035 0.0017 0.0079 0.0061 0.0040 -0.0002 0.0143 0.0101 -2.3979 -1.8447 -1.9957 0.0496 0.4986 0.9990 0.2480 2.4930 4.9950 -0.6050 0.3967 0.6985