BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
2.1.1 Habitat dan daerah tumbuh
Tumbuhan kubis (Brassica oleracea) bentuk capitata merupakan tumbuhan dari famili Brassicaceae atau Cruciferae (Majeed, 2004). Bentuk capitata menghasilkan kubis ungu maupun kubis putih. Kubis ungu dapat ditanam di dataran rendah maupun dataran tinggi dengan curah hujan rata-rata 850-900 mm dan umur panen berbeda-beda berkisar dari 90 hari sampai 150 hari. Kubis dapat diperbanyak dengan biji atau setek tunas (Dalimartha, 2000).
2.1.2 Morfologi
2.1.3 Taksonomi tumbuhan
Sistematika tumbuhan kubis ungu (Majeed, 2004) adalah sebagai berikut: Kingdom : Plantae
Divisi : Magnoliophyta Kelas : Magnoliopsida Bangsa : Capparales Suku : Brassicaceae Marga : Brassica
Spesies : Brassica oleracea L. var. capitata f. rubra
2.1.4 Nama lain
Tumbuhan kubis ungu mempunyai nama lain dari berbagai negara, diantaranya: Rode Kool (Belanda), Suitkool (Afrika), Chou Cobus (Prancis), Kopfkohl (Jerman), Purple / Red Cabbage (Inggris) (Heyne, 1987).
2.1.5 Khasiat dan penggunaan
Tumbuhan kubis ungu digunakan sebagai pewarna alami di berbagai produk, mempunyai serat diet yang cukup tinggi dalam membantu pencegahan kanker kolon, kolesterol, diabetes dan obesitas. Mengonsumsi jus kubis ungu juga dapat membantu memperbaiki lapisan lambung dan mengobati ulkus (Draghici, 2013). Jus kubis ungu dibuat dengan cara mencuci ¼ bagian kubis segar sampai bersih, bilas dengan air matang, lalu potong – potong seperlunya. Jus kubis tersebut, lalu sarinya diminum (Dalimartha, 2000).
metanol sebagai antioksidan dan antiinflamasi (Rokayya, et.al., 2013), ekstrak metanol sebagai antihiperglikemik dan analgesik (Daud, et.al., 2015).
2.1.6 Kandungan Kimia
Kubis ungu memiliki kandungan karbohidrat, protein, glikosida, flavonoid, fenol (Shama, et.al, 2012), air, lemak, karbohidrat, serat, kalsium, fosfor, besi, natrium, kalium, vitamin (A, C, E), beta karoten, antosianin (pemberi warna merah-ungu) (Dalimartha, 2000).
2.2 Ekstraksi
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut sehingga terpisah dari bahan yang tidak dapat larut dengan menggunakan suatu pelarut cair. Senyawa aktif yang terdapat dalam berbagai simplisia dapat digolongkan kedalam golongan minyak atsiri, alkaloida, flavonoida dan lain-lain. Dengan diketahuinya senyawa aktif yang dikandung simplisia akan mempermudah pemilihan pelarut dengan cara ekstraksi yang tepat (Ditjen POM., 2000).
Ekstrak adalah sediaan kering, kental atau cair dibuat dengan menyari simplisia nabati atau hewani menurut cara yang cocok, di luar pengaruh cahaya matahari langsung (Ditjen POM., 1979). Tujuan utama ekstraksi ini adalah untuk mendapatkan atau memisahkan sebanyak mungkin zat-zat yang memiliki khasiat pengobatan (Syamsuni, 2006). Beberapa metode ekstraksi yang sering digunakan dalam berbagai penelitian antara lain yaitu:
a. Cara dingin 1. Maserasi
beberapa kali pengocokan atau pengadukan pada temperatur ruangan, sedangkan remaserasi merupakan pengulangan penambahan pelarut setelah dilakukan penyaringan maserat pertama, dan seterusnya (Ditjen POM, 2000).
Maserasi dilakukan dengan cara masukkan 10 bagian simplisia atau campuran simplisia dengan derajat halus yang cocok ke dalam sebuah bejana, tuangi dengan 75 bagian cairan penyari, tutup, biarkan selama 5 hari terlindung dari cahaya sambil sering diaduk, serkai, peras, cuci ampas dengan cairan penyari secukupnya hingga diperoleh 100 bagian. Pindahkan ke dalam bejana tertutup, biarkan di tempat sejuk, terlindung dari cahaya selama 2 hari. Enap tuangkan dan saring (Ditjen POM, 1979).
2. Perkolasi
Perkolasi adalah suatu proses penyarian simplisia menggunakan alat yang disebut perkolator dimana simplisia terendam dalam cairan penyari, zat-zat akan terlarut dan larutan tersebut akan menetes secara beraturan. Prosesnya terdiri dari tahapan pengembangan bahan, tahap perendaman antara, tahap perkolasi sebenarnya (penetesan / penampungan perkolat) sampai diperoleh ekstrak (Ditjen POM., 2000).
lalu terdapat selapis cairan penyari di atas simplisia, hingga diperoleh 80 bagian perkolat. Peras massa, campurkan cairan perasan ke dalam perkolat, tambahkan cairan penyari secukupnya hingga diperoleh 100 bagian. Pindahkan ke dalam bejana, tutup, biarkan selama 2 hari di tempat yang sejuk, terlindung dari cahaya. Enap tuangkan atau saring (Ditjen POM., 1979).
b. Cara panas 1. Refluks
Refluks adalah proses penyarian simplisia dengan menggunakan alat pada temperatur titik didihnya dalam waktu tertentu dimana pelarut akan terkondensasi menuju pendingin dan kembali ke labu (Ditjen POM., 2000).
2. Sokletasi
Sokletasi adalah proses penyarian dengan menggunakan pelarut yang selalu baru, dilakukan dengan menggunakan alat soklet dimana pelarut akan terkondensasi dari labu menuju pendingin, kemudian jatuh membasahi sampel (Ditjen POM., 2000).
3. Digesti
Digesti adalah proses penyarian dengan pengadukan kontinu pada temperatur lebih tinggi dari temperatur kamar, yaitu secara umum dilakukan pada temperatur 40-50°C (Ditjen POM., 2000).
4. Infudasi
Infudasi adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90°C selama 15 menit (Ditjen POM., 2000).
5. Dekoktasi
2.3 Toksisitas
Uji toksisitas merupakan suatu uji untuk mendeteksi efek toksik suatu zat pada sistem biologi dan untuk memperoleh data dosis-respon yang khas dari sediaan uji. Data yang diperoleh dapat digunakan untuk memberi informasi mengenai derajat bahaya sediaan uji tersebut bila terjadi pemaparan pada manusia, sehingga dapat ditentukan dosis penggunaannya demi keamanan manusia.
Uji toksisitas menggunakan hewan uji sebagai model berguna untuk melihat adanya reaksi biokimia, fisiologik dan patologik pada manusia terhadap suatu sediaan uji. Hasil uji toksisitas tidak dapat digunakan secara mutlak untuk membuktikan keamanan suatu bahan/ sediaan pada manusia, namun dapat memberikan petunjuk adanya toksisitas relatif dan membantu identifikasi efek toksik bila terjadi pemaparan pada manusia (BPOM RI., 2014).
1. Uji toksisitas akut oral
digunakan untuk menetapkan tingkat dosis, merancang uji toksisitas selanjutnya, memperoleh nilai LD50 suatu bahan/sediaan, serta penentuan penggolongan bahan/ sediaan dan pelabelan (BPOM RI., 2014).
2. Uji toksisitas subkronis oral
Uji toksisitas subkronis oral adalah suatu pengujian untuk mendeteksi efek toksik yang muncul setelah pemberian sediaan uji dengan dosis berulang yang diberikan secara oral pada hewan uji selama sebagian umur hewan, tetapi tidak lebih dari 10% seluruh umur hewan. Prinsip dari uji toksisitas subkronis oral adalah sediaan uji dalam beberapa tingkat dosis diberikan setiap hari pada beberapa kelompok hewan uji dengan satu dosis per kelompok selama 28 atau 90 hari, bila diperlukan ditambahkan kelompok satelit untuk melihat adanya efek tertunda atau efek yang bersifat reversibel. Selama waktu pemberian sediaan uji, hewan harus diamati setiap hari untuk menentukan adanya toksisitas. Hewan yang mati selama periode pemberian sediaan uji, bila belum melewati periode rigor mortis (kaku) segera diotopsi, dan organ serta jaringan diamati secara makropatologi dan histopatologi.
dan mempelajari adanya efek kumulatif dan efek reversibilitas zat tersebut (BPOM RI., 2014).
3. Uji toksisitas kronis oral
Uji toksisitas kronis oral adalah suatu pengujian untuk mendeteksi efek toksik yang muncul setelah pemberian sediaan uji secara berulang sampai seluruh umur hewan. Uji toksisitas kronis pada prinsipnya sama dengan uji toksisitas subkronis, tetapi sediaan uji diberikan selama tidak kurang dari 12 bulan. Tujuan dari uji toksisitas kronis oral adalah untuk mengetahui profil efek toksik setelah pemberian sediaan uji secara berulang selama waktu yang panjang, untuk menetapkan tingkat dosis yang tidak menimbulkan efek toksik (NOAEL). Uji toksisitas kronis harus dirancang sedemikianrupa sehingga dapat diperoleh informasi toksisitas secara umum meliputi efek neurologi, fisiologi, hematologi, biokimia klinis dan histopatologi (BPOM RI., 2014).
2.4 Hati
Hati adalah salah satu organ pencernaan terbesar dan terletak di posisi sangat strategis. Semua nutrien dan cairan yang diserap dari usus masuk kehati melalui vena porta hepatis, kecuali produk lemak kompleks, yang masuk dan diangkut oleh pembuluh limfe (Eroschenko, 2013).
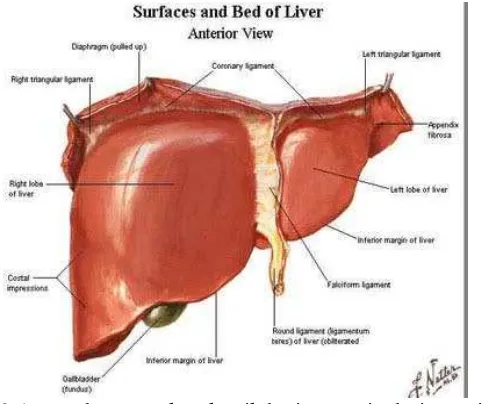
2.4.1 Anatomi hati
dalam keadaan segar merah kecoklatan, warna tersebut terutama disebabkan oleh adanya darah yang amat banyak (Lee, et al., 1997).
Gambar 2.1. Gambaran makroskopik hati manusia dari anterior
Setiap lobulus hati terdiri dari berbagai komponen, yaitu sel-sel hati (hepatosit), vena sentralis, sinusoid, cabang-cabang vena porta, cabang-cabang arteri hepatika, sel Kupffer dan kanalikuli biliaris (Junqueira and Carneiro, 2009). 2.4.2 Fisiologi hati
Selain merupakan organ parenkim yang paling besar, hati juga mempunyai beberapa fungsi. Fungsi utama hati yaitu (Irianto, 2000):
1. Memproduksi protein plasma (albumin, fibrinogen, protrombin; juga memproduksi heparin, yaitu suatu antikoagulan darah).
2. Fagositosis mikroorganisme dan eritrosit dan lekosit yang sudah tua dan rusak.
3. Pusat metabolisme protein, lemak, dan karbohidrat. Bergantung kepada keperluan tubuh, ketiganya dapat saling terbentuk.
beracun diubah menjadi urea yang relatif tidak beracun pada Daur Krebs – Urea di dalam sel hati.
5. Memproduksi cairan empedu
6. Merupakan gudang penyimpanan berbagai zat seperti mineral (Cu, Fe); vitamin A, D, E, K, B12, glikogen dan berbagai racun yang tidak dapat
dikeluarkan dari tubuh, misalnya pestisida DDT.
Hati mempunyai tiga kelompok penting: sintesis, ekskresi dan penyimpanan. Energi dan zat-zat gizi yang didapat dari makanan harus diproses dan kemudian disimpan, disebar atau diubah bentuknya oleh hati. Hati merombak, mendetoksikasi dan mengubah metabolit-metabolit primer dan pertengahan untuk ekskresi, penyimpanan atau untuk dipakai lagi (Widmann, 1989).
2.4.3 Histologi hati
kanalikuli yang bersatu membentuk saluran empedu yang makin lama makin besar hingga menjadi duktus koledokus (Price dan Wilson, 2003).
2.4.4 Patologi hati
Kerusakan pada hati dapat terjadi oleh beberapa faktor yaitu onset pemaparan yang terlalu lama, durasi pemaparan, dosis dan sel inang yang rentan (Jubb, 1993). Kerusakan yang terjadi pada sel hati dapat bersifat sementara (reversible) dan tetap (irreversible) (Wicaksono, 2002). Sel akan mengalami perubahan untuk beradaptasi mempertahankan hidupnya, perubahan ini biasa disebut degenerasi. Degenerasi sel dapat berupa degenerasi hidropis dan degenerasi lemak. Degenerasi terjadi karena adanya gangguan biokimiawi yang disebabkan oleh iskemia, anemia, metabolisme abnormal dan zat kimia yang bersifat toksik(Cheville, 1999).
Degenerasi hidropik merupakan peristiwa meningkatnya kadar air di intraseluler yang menyebabkan sitoplasma dan organel-organel membengkak dan membentuk vakuola-vakuola. Rusaknya permeabilitas membran sel menyebabkan terhambatnya aliran Na+ keluar dari sel sehingga menyebabkan ion-ion dan air masuk secara berlebihan kedalam sel. Degenerasi hidropik merupakan respon awal sel terhadap bahan-bahan yang bersifat toksik, serta merupakan proses awal dari kematian sel (Jones, et al., 1997; Cheville, 1999).
Kerusakan sel secara terus-menerus akan mencapai suatu titik sehingga terjadi kematian sel. Paparan zat toksik pada sel apabila cukup hebat atau berlangsung cukup lama, maka sel tidak dapat lagi mengkompensasi dan tidak dapat melanjutkan metabolisme. Inti sel yang mati dapat terlihat lebih kecil dan menjadi lebih padat (piknosis), hancur bersegmen-segmen (karioreksis) dan kemudian inti sel menghilang (kariolisis) (Underwood, 1994). Nekrosis hati adalah kematian hepatosit yang umumnya merupakan kerusakan akut (Lu, 1995). 2.4.5 Aminotransferase
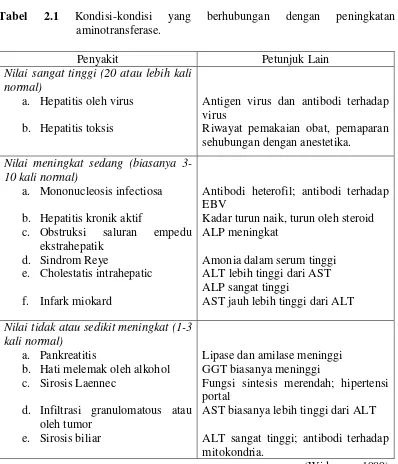
memiliki konsentrasi ALT yang tinggi, walaupun ginjal, jantung dan otot bergaris mengandung ALT dalam jumlah sedang. Kadar ALT menjadi petunjuk yang lebih sensitif ke arah kerusakan hati karena sangat sedikitnya kondisi bukan hati berpengaruh terhadap kadar ALT dalam serum (Widmann, 1989). Kadar ALT normal pada tikus yaitu 35-80 U/L (Research Animal Resource, 2009). Pemeriksaan enzim-enzim pada berbagai penyakit dapat dilihat pada Tabel 2.1. Tabel 2.1 Kondisi-kondisi yang berhubungan dengan peningkatan
aminotransferase.
Penyakit Petunjuk Lain
Nilai sangat tinggi (20 atau lebih kali normal)
a. Hepatitis oleh virus b. Hepatitis toksis
Antigen virus dan antibodi terhadap virus
Riwayat pemakaian obat, pemaparan sehubungan dengan anestetika.
Nilai meningkat sedang (biasanya 3-10 kali normal)
a. Mononucleosis infectiosa b. Hepatitis kronik aktif
c. Obstruksi saluran empedu ekstrahepatik
d. Sindrom Reye
e. Cholestatis intrahepatic f. Infark miokard
Antibodi heterofil; antibodi terhadap EBV
Kadar turun naik, turun oleh steroid ALP meningkat
Amonia dalam serum tinggi ALT lebih tinggi dari AST ALP sangat tinggi
AST jauh lebih tinggi dari ALT
Nilai tidak atau sedikit meningkat (1-3 kali normal)
a. Pankreatitis
b. Hati melemak oleh alkohol c. Sirosis Laennec
d. Infiltrasi granulomatous atau oleh tumor
e. Sirosis biliar
Lipase dan amilase meninggi GGT biasanya meninggi
Fungsi sintesis merendah; hipertensi portal
AST biasanya lebih tinggi dari ALT ALT sangat tinggi; antibodi terhadap mitokondria.