SKRIPSI– TK141581
SIMULASI DAN PEMODELAN ABSORPSI
CO
2& H
2S DALAM LARUTAN MDEA
DENGAN
PROMOTOR
POTASSIUM
METHIONINE (PM) MENGGUNAKAN TRAY
COLUMN
Oleh:
Alif Ramadhani Utomo NRP 2313100058 Veby Iqbal Hariadi NRP 2313100120 Dosen Pembimbing:
Prof. Dr. Ir. Ali Altway, M.S. NIP. 1951 08 04 1974 12 1001 Dr. Ir. Susianto, DEA. NIP. 1962 08 20 1989 03 1004 DEPARTEMEN TEKNIK KIMIA FAKULTAS TEKNOLOGI INDUSTRI
INSTITUT TEKNOLOGI SEPULUH NOPEMBER SURABAYA
FINAL PROJECT – TK141581
MODELING AND SIMULATION OF CO2
&
H
2S ABSORPTION IN ACTIVATED MDEA
SOLUTION
WITH
POTASSIUM
METHIONINE (PM) USING THE TRAY
COLUMN
Proposed by:
Alif Ramadhani Utomo NRP 2313100058 Veby Iqbal Hariadi NRP 2313100120 Advisor :
Prof. Dr. Ir. Ali Altway, M.S. NIP. 1951 08 04 1974 12 1001 Dr. Ir. Susianto, DEA. NIP. 1962 08 20 1989 03 1004 DEPARTEMEN TEKNIK KIMIA FAKULTAS TEKNOLOGI INDUSTRI
INSTITUT TEKNOLOGI SEPULUH NOPEMBER SURABAYA
iii
SIMULASI DAN PEMODELAN ABSORPSI
CO
2& H
2S DALAM LARUTAN MDEA
DENGAN PROMOTOR POTASSIUM
METHIONINE (PM) MENGGUNAKAN TRAY
COLUMN
Mahasiswa : Alif Ramadhani Utomo 2313100058 Veby Iqbal Hariadi 2313100120 Pembimbing I : Prof. Dr. Ir. Ali Altway, M.S.
Pembimbing II : Dr. Ir. Susianto, DEA
ABSTRAK
Pengambilan Hidrogen Sulfida (H2S) dan Karbon
Dioksida (CO2) dalam gas alam adalah merupakan proses yang
paling penting dalam pemanisan gas alam. H2S merupakan gas
korosif apabila bercampur dengan moisture dan CO2 yang lepas
dari sistem dan keluar ke atmosfer akan menyebabkan efek rumah kaca. CO2 dapat menurunkan nilai bakar gas alam,
sehingga harus diminimalisir kandungannya dalam gas alam. Salah satu proses pengambilan gas tersebut adalah dengan cara absorpsi reaktif menggunakan larutan MDEA dengan promotor Potassium Methionine (PM), karena pelarut ini mempunyai sifat selektif terhadap penyerapan H2S dan CO2. Proses absorbsi gas
CO2 dan H2S yang dilakukan dalam tray column merupakan
pilihan yang lebih baik dari pada packed column yaitu untuk menghindari masalah distribusi liquida di dalam kolom yang berdiameter besar dan untuk mengurangi ketidakpastian dalam pembesaran skala. Penelitian ini bertujuan untuk menggunakan model matematik dan simulasi untuk proses absorpsi CO2 dan
H2S dari gas alam dengan larutan MDEA dan promotor PM
menggunakan tray column. Pada kajian teoritis ini diperlukan data-data seperti konstanta kesetimbangan reaksi, laju reaksi, data kelarutan, koefisien perpindahan massa pada sisi gas dan liquid
iv
dikembangkan berdasarkan pada transfer massa pada teori film dengan asumsi reaksi pseudo first order. Penyelesaian numerik yang telah dilakukan menunjukan bahwa laju penyerapan meningkat seiring dengan peningkatan temperature karena terjadi peningkatan pada laju reaksinya. Peningkatkan tekanan dapat meningkatkan kelarutan gas sehingga meningkatkan laju absorpsi. Peningkatan konsentrasi akan mempengaruhi hukum aksi massa sehingga laju penyerapan akan semakin meningkat. Jumlah konsentrasi promotor yang digunakan dapat meningkatkan %removal secara signifikan, namun akan cenderung konstan ketika jumlahnya ditingkatkan
Kata kunci : absorpsi, MDEA, PM, tray, laju absorpsi, percent
v
MODELING AND SIMULATION OF CO
2&
H
2S ABSORPTION IN ACTIVATED MDEA
SOLUTION WITH POTASSIUM
METHIONINE (PM) USING THE TRAY
COLUMN
Compiled by : Alif Ramadhani Utomo 2313100058 Veby Iqbal Hariadi 2313100120 Advisor I : Prof. Dr. Ir. Ali Altway, M.S.
Advisor II : Dr. Ir. Susianto, DEA
ABSTRACT
Hydrogen Sulfide (H2S) and Carbon Dioxide (CO2)
removal in natural gas is the most important process in the natural gas plant. H2S is a corrosive gas when mixed with moisture and
release CO2 into the atmosphere will cause the greenhouse effect.
CO2 can reduce the heating value of natural gas, so it should be
minimized its content in natural gas. One of the gas removal method is reactive absorption using MDEA solution with promotor Potassium Methionine (PM) , because it has the properties as selective solvent for absorption of H2S and CO2. The
process of absorption of CO2 and H2S gas is conducted in a tray
column is a better choice than the packed column that is to avoid distribution problems Liquid in large diameter columns and to reduce uncertainties in an enlarged scale. In this theoretical study required data such as the equilibrium constant of the reaction, the reaction rate, the data solubility, mass transfer coefficient on the gas side and the liquid obtained from the literature. Developed a mathematical model based on mass transfer in film theory assuming a pseudo first order reaction. Numerical solution that has been done shows that the rate of absorption increases with increasing temperature due to an increase in the rate of reaction. Increasing the pressure can increase the solubility of the gas so as
vi
to increase the rate of absorption. Increased concentration will affect the law of mass action so that the rate of absorption will increase. Total concentration of promoter used can significantly increase the% removal, but will tend to be constant when the number has been increased
Keywords: absorption, MDEA, PM, tray, absorption rate, percent removal
vii
KATA PENGANTAR
Segala puji dan syukur kami ucapkan ke hadirat Allah Yang Maha Kuasa atas segala rahmat dan karunia-Nya sehingga kami dapat menyelesaikan skripsi yang berjudul:
“SIMULASI DAN PEMODELAN ABSORPSI CO2 DAN H2S
DALAM LARUTAN MDEA DENGAN PROMOTOR
POTASSIUM METHIONINE (PM) MENGGUNAKAN TRAY
COLUMN”.
Skripsi ini disusun untuk melengkapi persyaratan penelitian skripsi dalam memperoleh gelar Sarjana Teknik (ST) pada bidang Studi S1 Teknik Kimia di Institut Teknologi Sepuluh Nopember Surabaya. Pada kesempatan ini dengan kerendahan hati kami menyampaikan terima kasih kepada:
1. Allah SWT yang telah mempermudah segala urusan kami dan selalu mengaruniakan kesehatan kepada kami. 2. Kedua orang tua dan keluarga kami yang telah
memberikan segalanya yang tak mungkin tercantumkan dalam tulisan ini.
3. Bapak Juwari, S.T, M.Eng, Ph.D, selaku Ketua Jurusan Teknik Kimia FTI-ITS Surabaya.
4. Bapak Prof. Dr. Ir. Ali Altway, M.S, selaku Dosen Pembimbing 1 dan Kepala
Laboratorium Perpindahan Panas dan Massa atas bimbingan dan saran yang telah diberikan.
5. Bapak Dr. Ir. Susianto, DEA. selaku Dosen Pembimbing 2 atas bimbingan dan saran yang telah diberikan.
6. Bapak Prof. Ir. Dr. Nonot Soewarno, M.Eng, Bapak Fadlilatul Taufany, S.T, Ph.D, Ibu Dr. Yeni Rahmawati, S.T., M.T, dan Siti Nurkhamidah, ST., MSc., Ph.D selaku Dosen Laboratorium Perpindahan Panas dan Massa, atas bimbingan dan saran yang telah diberikan.
viii
7. Bapak dan Ibu Dosen Pengajar atas segala ilmu yang diberikan serta seluruh karyawan Jurusan Teknik Kimia FTI-ITS Surabaya.
8. Teman-teman di Laboratorium Perpindahan Panas dan Massa atas doa, semangat, perhatian dan kasih sayang selama ini.
9. Teman-teman K53 yang telah memberikan dukungan dan bantuan sehingga kami dapat menyelesaikan skripsi ini. 10. Seluruh pihak yang tidak dapat kami sebutkan satu
persatu, yang turut membantu kami.
Kami menyadari bahwa skripsi ini masih jauh dari sempurna. Oleh karena itu, kritik dan saran dari para pembaca sangat penulis harapkan sebagai upaya peningkatan kualitas dari skripsi ini.
Surabaya, Juli 2017
Penyusun
ix
DAFTAR ISI
LEMBAR PENGESAHAN
ABSTRAK...iii
ABSTRACT ...v
KATA PENGANTAR ...vii
DAFTAR ISI ...ix
DAFTAR GAMBAR ...xi
DAFTAR TABEL...xii
BAB I
PENDAHULUAN...1
1.1
Latar Belakang...1
1.2
Perumusan Masalah...4
1.3
Batasan Masalah...4
1.4
Tujuan Penelitian………...4
1.5
Manfaat Penelitian...5
BAB II
TINJAUAN PUSTAKA...6
2.1
Absorpsi Fisik...6
2.2
Absorpsi Disertai Reaksi Kimia………..13
2.3
Alkanolamine………..19
2.4
Jenis Promotor……….22
2.5
Kinetika Reaksi...23
2.6
Tipe Kolom...25
2.7
Penelitian yang Sudah Dilakukan……...28
BAB III
METODE PENELITIAN………....31
3.1
Sistem yang Ditinjau...33
3.2
Model Matematika...34
3.3
Penyelesaian Numerik……….42
3.4
Pembuatan Program………42
3.5
Validasi Data………...42
3.6
Analisa Model Matematis………...42
3.7
Variabel Penelitian………..43
x
4.1
Pengaruh Temperatur (K) Terhadap
Percent Recovery……...45
4.2
Pengaruh Tekanan (atm) Terhadap Percent
Recovery………...47
4.3
Pengaruh Konsentrasi MDEA (%wt)
Terhadap Percent Recovery…………....49
4.4
Pengaruh Konsentrasi Potassium
methionine (%wt) Terhadap Percent
Recovery………...51
4.5
Distribusi Konsentrasi Komponen Dalam
Gas………...52
4.6
Distribusi Konsentrasi Komponen Dalam
Liquid………..53
4.7
Validasi Data Simulasi MATLAB dengan
HYSYS dan Eksperimen……….56
4.8
Perbandingan Hasil Simulasi Matlab
Dengan Variasi Jenis Promotor………...57
BAB V
KESIMPULAN DAN SARAN………...59
5.1
Kesimpulan...59
5.2
Saran...60
DAFTAR PUSTAKA...xiii
DAFTAR NOTASI...xvi
LAMPIRAN A
LAMPIRAN B
LAMPIRAN C
xi
DAFTAR TABEL
Tabel 2.1 Perbandingan Karakteristik Pelarut
Alakanolamina...20
Tabel 2.2 Penelitian yang Sudah Dilakukan...29
Tabel 4.1 Validasi hasil simulasi MATLAB dan
HYSYS...56
Tabel 4.2Validasi hasil simulasi MATLAB dan
Eksperimen……….56
Tabel 4.3Perbandingan hasil simulasi MATLAB
xii
DAFTAR GAMBAR
Gambar 2.1 Konsep teori 2 film Whitman untuk
perpindahan massa fase gas - cair...8
Gambar 2.2 Surface Renewal Model...10
Gambar 2.3 Tranfer Massa Gas ke Dalam Liquida
Disertai Reaksi Kimia...15
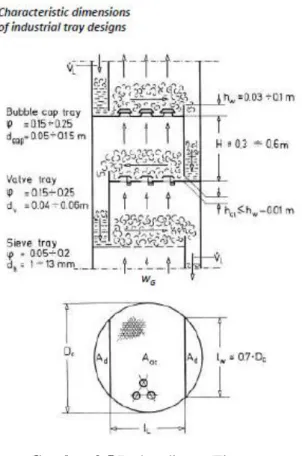
Gambar 2.4 Tipe tray...27
Gambar 2.5 Perbandingan Tipe Tray...28
Gambar 3.1 Langkah-langkah pembuatan model
matematik untuk proses absorpsi gas
CO2 dari gas alam ke dalam larutan
promotor MDEA dengan aktivator PM
di dalam tray column...32
Gambar 3.2 Sistem Absorpsi Gas CO
2dari Gas
Alam ke dalam Larutan MDEA
dengan Aktivator PM di dalam Tray
Column...33
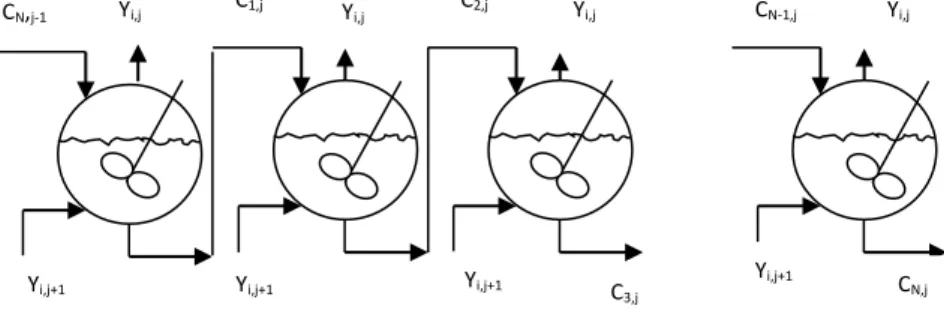
Gambar 3.3 Skema untuk Tray Absorber...39
Gambar 3.4 Model Satu Tray Dalam Bentuk
CSTR...40
Gambar 4.1 Grafik pengaruh temperatur larutan
MDEA terhadap percent removal
CO2...46
Gambar 4.2 Grafik pengaruh temperatur larutan
MDEA terhadap percent removal
H2S...46
Gambar 4.3 Grafik pengaruh tekanan larutan
MDEA terhadap percent removal
CO2...48
Gambar 4.4 Grafik pengaruh tekanan larutan
xiii
H2S...48
Gambar 4.5 Grafik pengaruh konsentrasi MDEA
(%wt) terhadap percent removal
CO2...50
Gambar 4.6 Grafik pengaruh konsentrasi MDEA
(%wt) terhadap percent removal
H2S...50
Gambar 4.7 Grafik pengaruh konsentrasi PM
(%wt) terhadap percent removal
CO
2...51
Gambar 4.8 Grafik pengaruh konsentrasi PM
(%wt) terhadap percent removal
H
2S...52
Gambar 4.9 Distribusi konsentrasi komponen gas
CO2 dan H2S di dalam tray column..53
Gambar 4.10 Distribusi konsentrasi komponen
liquid CO2 dan H2S di dalam tray
column...54
Gambar 4.11 Distribusi konsentrasi komponen
liquid CO
2dan H
2S di dalam tray
column...55
1
BAB I
PENDAHULUAN
1.1. Latar Belakang
Dalam beberapa tahun terakhir, minat pada pengembangan teknologi penghilangan karbon dioksida (CO2) dan Hidrogen
Sulfida (H2S) semakin meningkat karena dampaknya pada
pemanasan global dan perubahan iklim, yang terutama disebabkan oleh emisi CO2.Selain itu, CO2dan H2S biasanya
banyak terdapat pada eksplorasi gas alam. Gas alam (NG) merupakan sumber daya alternatif yang memiliki kandungan CO2
dan H2S yang tinggi yang membutuhkan proses pemisahan
sebelum diolah lebih lanjut. Sebagai pengotor, CO2 dan H2S bisa
menjadi zat yang bersifat korosif dengan adanya air dan menyebabkan kerusakan di jaringan pipa gas.
Kandungan CO2 yang tinggi dalam pipa dapat memberikan
efek negatif, antara lain menurunkan nilai bakar (heating value) gas alam, menyebabkan korosi pada peralatan proses dan berpotensi terjadinya pembekuan (freezing) dalam pipa. Freezing berkaitan dengan suhu gas alam yang dipasarkan pada suhu sangat rendah yaitu -161oC dalam bentuk LNG dimana pada suhu tersebut CO2 akan berada dalam keadaan beku. Sedangkan H2S
merupakan gas beracun yang sangat korosif terhadap peralatan diproses kilang. Berdasarkan informasi tentang pengaruh negatif tersebut, dapat disimpulkan bahwa proses penyisihan CO2dan H2S
merupakan tahapan penting dalam pengolahan gas alam keseluruhan.
Terdapat banyak proses penyisihan H2S dan CO2
diantaranya adalah adsorpsi, absorpsi, cryogenic dan teknologi membran. Diantara metode tersebut pemisahan dengan metode absorpsi baik dengan larutan alkali (larutan amina) atau pelarut fisik (larutan glikol) adalah metode yang paling banyak digunakan dan paling efektif, namun absorpsi dengan pelarut fisik tidak ekonomis (Kohl,1997).
2
Absorben adalah cairan yang dapat melarutkan bahan yang akan diabsorpsi pada permukaannya. Absorben berbasis amina, seperti monoethanolamine (MEA), diethanolamine (DEA), N-metildietanolamina (MDEA) dan di-2-propanolamine (DIPA) adalah absorben yang paling banyak digunakan karena reaktivitas tinggi dengan CO2 serta reaksi berlangsung secara reversible
sehingga proses removal menjadi lebih mudah. Dari beberapa larutan amina yang ada,MDEA dipilih karena mempunyai beberapa keuntungan yaitu, tekanan uap rendah, dapat digunakan hingga konsentrasi 60% berat tanpa adanya komponen yang hilang akibat adanya penguapan, stabil pada suhu tinggi, sedikit korosif, panas reaksi rendah, dan selektivitas terhadap H2S tinggi,
dimana reaksi antara MDEA dengan CO2 dan H2S adalah sebagai
berikut :
CO2 + (C2H4OH)2CH3N + H2O CH3N (C2H4OH)2H+ + HCO3─ (1.1)
(C2H4OH)2CH3N + H2S CH3N (C2H4OH)2H+ + HS─
(1.2) Larutan MDEA kemudian dicampurkan dengan aktivator
spesifik potassium methionine (PM) yang berfungsi
meningkatkan proses penyerapan. Penggunaan PM yang ditambahkan pada pelarut berfungsi untuk mengaktifkan pelarut MDEA.PM adalah pelarut yang stabildengan kapasitasnya sebagai penangkap CO2, memiliki tingkat penyerapan CO2 yang
tinggi, tidak mudah terdegradasidan oksidatif (Mazari, 2016). Absorber yang akan digunakan pada penelitian ini yaitu jenis absorber tray atau plate tower. Tray column adalah kolom pemisah berupa silinder tegak dimana bagian dalam dari kolom berisi sejumlah tray atau plate yang disusun pada jarak tertentu (tray/plate spacing) di sepanjang kolom. Cairan dimasukan dari puncak kolom dan dalam perjalanannya cairan akan mengalir dari
tray yang satu ke tray yang lain yang ada di bawahnya. Selama
proses berlangsung, di setiap tray akan terjadi kontak antara fase cair dengan fase uap yang dimasukkan dari dasar kolom.
Dalam beberapa tahun terakhir telah dilakukan penelitian mengenai optimasi penyisihan CO2 dan H2S dengan larutan
3
promotor MEA sebesar 2,5% mol ke dalam larutan MDEA mampu mengurangi kebutuhan jumlah tray dari 40 ke 25. Namun kelemahannya adalah promotor MEA hanya meningkatkan nilai
enhancement factor pada bagian atas kolom saja. Penelitian lebih
lanjut mengenai proses penyisihan CO2 dan H2S juga telah
dilakukan oleh Rozi .M (2009) dengan umpan gas alam yang telah divalidasikan pada industri migas dengan jenis valve tray dan diameter tray 2,2 m serta jumlah tray sebanyak 12 dimana penelitian ini menggunakan pelarut MDEA tanpa menggunakan tambahan aktivator PM.
Model yang digunakan adalah model film dengan pendekatan enhancement factor dalam kondisi isotermal. Dimana hasil penelitian tersebut menunjukan bahwa semakin tinggi suhu semakin besar nilai persen removal gas CO2 dan H2S, demikian
juga dengan konsentrasi dan tekanan dimana kenaikannya diiringi dengan bertambahnya nilai persen removal gas CO2 dan H2S
sehingga didapatkan kondisi optimum operasi yaitu tekanan 30 atm, suhu larutan MDEA 40oC dan konsentrasi MDEA 0,0043 gmol/cm3. Dimana persen removal yang didapatkan pada penelitian menunjukan penyimpangan 14,7% untuk gas CO2
sedangkan untuk gas H2S sebesar 0,16%. Kemudian, Baniadam
dkk.,(2009) menunjukan bahwa model matematis dengan
two-film theory akan memberikan fenomena distribusi suhu serta nilai enhancement factor pada tiap tray. Sedangkan menurut Ibrahim
dkk.,(2014),menjelaskan bahwa penggunaan promotor potassium methionine didalam penyisihan CO2 pada gas alam sebanyak 3%
menurunkan jumlah CO2 yang terkandung didalam umpan hingga
kurang dari 1% yang mana keadaan tersebut tidak dapat dicapai oleh larutan MDEA saja tanpa adanya penambahan promotor PM, selain itu kenaikan suhu sebesar 10oC akan meningkatkan
penyerapan CO2 sebesar 0,5% secara bertahap dengan
menambahkan konsentrasi dari PM dalam konsentrasi rendah. Sedangkan tekanan didalam kolom akan memberikan efisiensi tertinggi pada tekanan sekitar 20 bar.
4
Borhani dkk.,(2015) dalam studinya menjelaskan mengenai penggunaan rate-based model didalam absorpsi reaktif antara CO2 dan H2S dengan larutan MDEA di dalam packed column
eksperimen tersebut hasil yang didapatkan adalah model absorber menunjukan bahwa seiring bertambahnya konsentrasi acid gases didalam umpan maka akan diiringi dengan penurunan area spesifik permukaan packing dan koefisien neraca massa overall bertambah seiring dengan penambahan umpan absorben di dalam
packed column. Dengan mempertimbangkan penelitian-penelitian
tersebut, perlu dilakukannya penelitian absorpsi gas CO2 dan H2S
dengan larutan MDEA dan katalis PM di dalam kolom sieve tray untuk membuat simulasi absorpsinya dan hasilnya akan divalidasi dengan eksperimen.
1.2. Perumusan Masalah
Menggunakan model two-film theory dengan pendekatan
enhancement factor di dalam absorpsi reaktif CO2 dan H2S
dengan larutan MDEA berpromotor PM menggunakan tray
column dan mempelajari distribusi pengaruh variabel-variabel
proses terhadap % CO2 dan % H2S removal. 1.3. Batasan Masalah
Untuk membatasi masalah yang akan dibahas maka digunakan asumsi-asumsi :
1. Absorpsi CO2 dan H2S terjadi pada kondisi steady state.
2. Fase liquid mengandung komponen non-volatile sehingga tidak ada material atau energi yang hilang karena evaporasi.
3. Pola aliran liquid adalah Crossflow.
4. Reaksi pada fase liquid seluruhnya terjadi dalam film. 5. Properti-properti fisik dari fase gas bergantung pada suhu
dan mengasumsikan gas ideal.
6. Reaksi berlangsung dengan kondisi isothermal.
5
Tujuan dari penelitian ini adalah:
1. Menggunakan model matematika di dalam proses absorpsi gas
CO2 dan H2S dengan larutan MDEA berpromotor PM
menggunakan tray column.
2. Melakukan validasi model matematika dengan
membandingkan hasil prediksi dengan HYSYS dan data eksperimen.
3. Mengkaji secara teoritis pengaruh distribusi berbagai variabel proses seperti suhu, tekanan, konsentrasi larutan MDEA, dan konsentrasi promotor terhadap efisiensi absorpsi.
1.5. Manfaat Penelitian
Dari hasil penelitian diharapkan dapat dijadikan acuan pada industri untuk merancang unit pemisahan CO2 dan H2S dalam
6
BAB II
TINJAUAN PUSTAKA
Absorpsi adalah proses pemisahan bahan dari suatu campuran gas dengan cara pengikatan bahan tersebut pada permukaan absorben cair yang diikuti dengan pelarutan. Kelarutan gas yang akan diserap dapat disebabkan hanya oleh gaya-gaya fisik (pada absorpsi fisik) atau selain gaya tersebut juga oleh ikatan kimia (pada absorpsi kimia). Komponen gas yang dapat mengadakan ikatan kimia akan dilarutkan lebih dahulu dan juga dengan kecepatan yang lebih tinggi. Secara umum, absorpsi reaktif dikenal sebagai penyerapan gas dalam medium cair dengan reaksi kimia. Proses tersebut memiliki beberapa keuntungan dimana dalam proses tersebut dapat meningkatkan yield reaksi dan selectivity, mengatasi hambatan termodinamika seperti reduksi dalam konsumsi energi, air dan pelarut. Oleh karena adanya interaksi antara reaksi kimia dan perpindahan massa dan panas yang cukup kompleks (Gorak & Kenig, 2005).
2.1 Absorbsi Fisik
Absorbsi merupakan suatu teknik pemurnian gas paling penting. Teknik ini menyangkut perpindahan massa suatu material dari fase gas ke fase cair melalui batas fase. Material yang diserap dapat larut secara fisik dalam cairan, maka disebut absorbsi fisik, atau bereaksi secara kimia dengan cairan disebut absorbsi kimia. Absorbsi fisik adalah absorbsi dimana gas terlarut dalam cairan tanpa disertai reaksi kimia, misalnya absorbsi CO2
atau H2S dengan menggunakan pelarut-pelarut air,
n-methyl-2-pyrolidone, methanol, dan propylene carbonate (Kohl & Nielsen, 1997).
Ada bebrapa teori yang digunakan untuk menggambarkan fenomena perpindahan massa yang terjadi pada absorbsi fisik. (Astarita, 1967), yakni:
7 2. Teori penetrasi
3. Teori pembaharuan permukaan
2.1.1 Teori Lapisan Film (Film Model)
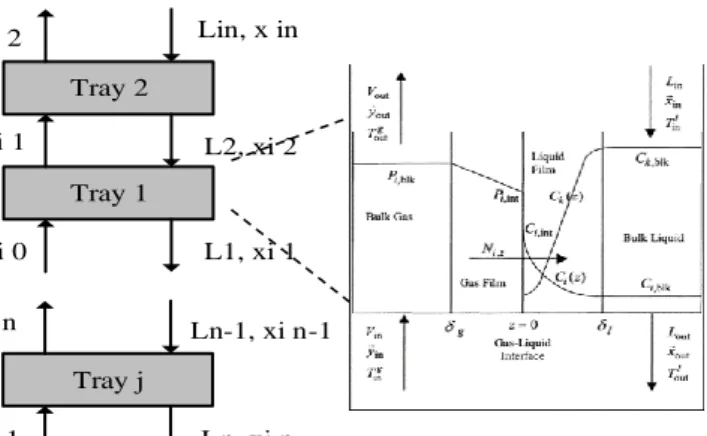
Teori dua film diajukan oleh Whitman pada tahun 1923 dan pada tahun 1928 Hatta menggunakan model ini untuk memodelkan absorbsi disertai reaksi kimia. Pada teori ini dianggap ada suatu lapisan stagnan dalam kedua fase sepanjang
interface. Di dalam fase gas perpindahan massa komponen A
kedalam interface mengalami tahanan dalam film gas dan tahanan perpindahan massa komponen A dari interface ke badan cairan film cair (Treybal, 1980). Bila diterapkan pada suatu proses absorpsi yang dikendalikan oleh sisi cair, model teori film mengevaluasi laju absorpsi per satu satuan luas permukaan R:
0 A A x C R D x (2.1) Secara skematis model film Whitman diberikan pada persamaan 2.1. Gradien konsentrasi A antara x = 0 sampai x = adalah konstan dalam film stagnan bila tidak terjadi generasi atau reaksi kimia. Gradien konsentrasi untuk model Whiteman diberikan pada persamaan berikut:
0 0 Ai A A x C C C x
(2.2) Koefisien perpindahan massa untuk sisi cair kL, untukabsorbsi fisik diberikan oleh persamaan
0 L Ai A R k C C (2.3) Sehingga apabila disubstitusikan antara persamaan (2.3) ke persamaan (2.2) maka didapatkan
0 A x L C R x k
(2.4)Apabila persamaan (2.4) disubstitusikan ke persamaan (2.1) maka didapatkan persamaan
8 A L D k (2.5)
Gambar 2.1 Konsep teori 2 film Whitman untuk
perpindahan massa fase gas-cair
Teori dua film merupakan teori untuk keadaan steady state. Diasumsikan bahwa gas dan cairan berada pada kesetimbangan pada interface dan bahwa film-film tipis memisahkan interface dari bagian kedua fase. Karena kuantitas material yang dipindahkan dari interface ke cairan maka dapat diambil hubungan seperti persamaan berikut ini.
0
A G A Ai L A Ai
N k p p k C C (2.6) 2.1.2 Teori Penetrasi
Pada teori penetrasi interface gas-cair dianggap terdiri dari banyak elemen-elemen cairan yang secara terus menerus dibawa hingga permukaan cairan dan sebaliknya oleh gerakan fase cair itu sendiri, Masing-masing elemen cairan selama berada di permukaan dapat dianggap stagnan, dan konsentrasi gas terlarut di dalam elemen dapat dianggap sama di semua bagian. Pada umumnya waktu kontak fluida sangat singkat sehingga selama elemen cairan berada di permukaan terjadi proses difusi molekular gas ke dalam fase cair dalam keadaan unsteady, dan gas hanya sempat menembus fase cair tidak jauh dari permukaan bidang batas. Model teori penetrasi menganggap bahwa semua elemen cairan berada pada permukaan dalam selang waktu yang sama (Astarita, (1967). Dalam teori penetrasi permukaan yang dikembangkan Danckwerts atau yang biasa disebut teori pembaharuan permukaan, permukaan gas cair, dianggap terdiri
9
dari banyak elemen-elemen permukaan dengan waktu kontak berbeda-beda. Elemen-elemen cairan ini pada waktunya digantikan dengan cairan segar yang mempunyai komposisi yang sama. Model pembaharuan ini mengganggap bahwa kesempatan elemen permukaan digantikan tidak tergantung waktu kontaknya (Danckwerts, 1970). x c D F (2.7)
2.1.3 Teori Pembaharuan permukaan (Surface Renewal)
Absorpsi gas digambarkan sebagai penggantian pada interval waktu tertentu elemen-elemen cair pada permukaan dengan cairan dari dalam yang mempunyai komposisi bulk rata-rata. Elemen cair pada permukaan tersebut berkontak dengan gas, sehingga elemen ini menyerap gas seolah-olah dalam keadaan stagnan dan mempunyai kedalaman yang tak berhingga. Gambar. 2.2 menunjukkan mekanisme model ini. Laju absorpsi R adalah fungsi waktu kontak elemen dengan gas.
Pada umumnya laju absorpsi cepat pada keadaan awal dan kemungkinan menurun dengan waktu. Penggantian elemen cair pada permukaan oleh cairan dari dalam dengan komposisi bulk bisa dilaksanakan karena adanya gerakan turbulen dari cairan.
10
Gambar 2.2 Surface Renewal Model
Model surface renewal pertama kali disarankan oleh Higbie. Model Higbie ini, menganggap waktu kontak elemen-elemen cair di permukaan dengan gas dianggap sama. Waktu kontak ditentukan oleh sifat-sifat hidrodinamika sistem. Makin turbulen cairnya, pergantian elemen-elemen cair makin sering, berarti harga θ makin kecil.
Proses difusi molekuler unsteady setiap elemen fluida digambarkan dengan persamaan diferensial:
t
C
x
C
D
A A A
2 2 (2.8)Dimna t adalah waktu berlalu momen elemen permukaan yang dibawa ke permukaan. Sehingga kondisi batasnya adalah :
0 0
...
...
0
...
0
A A ai A A AC
C
x
C
C
x
C
C
t
(2.9)Dimana kondisi batas (2.9) telah memenuhi penyelesaian, integral Persamaan (2.8) memenuhi Laplace transform kondisi batas adalah: t D x erfc C C C C A A Ai A A 2 0 0 (2.10) Dari Persamaan (2.8) Gas Cair
11 A A DAt x A Ai x A t D e C C x C 2 1 2 ) ( 2 0 0
(2.11)Substitusi x = 0 kedalam Persamaan (2.11) D t C C t D C C x C A A Ai A A Ai x A 1 ) ( 2 1 2 ) ( 0 0 0 (2.12)
Substitusi Persamaan (2.11) ke dalam Persamaan (2.12)
t D C C t D C C D R A A Ai A A Ai A ( ) 1 ) ( 0 0 (2.13) t D C C dt t D C C Rdt Q A A t Ai A t A Ai ) 2( ) ( 0 0 0 0
(2.14) (2.15)
A A Ai A Ai LD
C
C
C
C
k
R
'
0(
0)
2
(
0)
(2.16)Maka koefisien tranfer massa didefinisikan sebagai:
A L D k0 2 (2.17)L
v
D
k
A L max
02
(2.18) Model Danckwerts
DA C C D C C Q R Ai A A A Ai ) ( 2 ) ( 2 ' 0 0 12
Danckwerts mengemukakan fraksi permukaan pada waktu tertentu telah berkontak dengan gas selama waktu antar
dan
d
adalah SeSd
. Dimana S adalah fraksi luas permukaan yang diganti dengan liquida dari dalam per satuan waktu.Jadi bila R adalah laju absorpsi sesaat per satuan luas permukaan telah berkontak dengan gas pada waktu t yang untuk absorpsi fisik adalah (CAi – CA0)
AD
maka laju absorpsi rata-rata kedalam liquida adalah harga R yang dirata-ratakan ke seluruh permukaan yang mempunyai waktu antara 0 dan ∞.
Jika hipotesis waktu semua permukaan elemen liquida sama dihilangkan, maka laju absorpsi rata-rata adalah:
d
e
R
S
R
t s
0.
'
(2.19) Substitusi harga A A Ai D C C R( 0) dari Persamaan (2.12) ke dalam Persamaan (2.16)
d
e
DA
C
C
S
R
s A Ai
0 0)
(
'
(2.20)Digunakan integral fungsi gamma (Г): Dan Г(0.5)=
)
1
(
1
1 0
X
ne
xdX
nn
(2.21)13
Dari Persamaan (2.17) λ=S, X=0 dan n=-0.5 substitusikan harga-harga ini ke Persamaan (2.20):
) ( ) ( ' ) ( ) ( ) 5 . 0 ( 1 ) ( ) 1 5 . 0 ( 1 ) ( 0 0 ) ( ' 0 0 0 0 0 0 ) 1 5 . 0 ( 0 0 5 . 0 0 A Ai L A A Ai A A Ai A A Ai A A Ai A A Ai s A A Ai C C k S D C C R S D C C D S C C S D S C C S D S C C d e D S C C R
(2.22) SehinggaS
D
k
L0
A ; A
LD
k
0
(2.23)Absorben yang sekarang sering digunakan sebagai
chemical solvent adalah larutan alkanoamin. Alkaloamin yang
tersedia secara komersial untuk proses absorbsi diantaranya
monoethanolamine (MEA), diethanolamine (DEA),
diisopropanolamine (DIPA), N-methyldiethanolamine (MDEA), dan 2-amino-2-methyl-1-propanol (AMP). Belakangan juga ada pula upaya pemanfaatan Potassium Methionine untuk aktivasi larutan MDEA untuk proses absorbsi CO2.
Untuk mendesain atau mensimulasikan absorbsi yang melibatkan reaksi dibutuhkan. beberapa data penting. Data ini diantaranya
1) Properti fisik (thermal dan transport dari cair dan gas yang terlibat dalam sistem)
2) Data kesetimbangan uap-cair (konfigurasi internal dari column yang digunakan)
3) Data laju reaksi kimia.
2.2 Absorbsi Disertai Reaksi Kimia
Absorbsi kimia adalah absorbsi dimana gas terlarut dalam cairan penyerap disertai reaksi kimia. Misalnya absorbsi CO2 di
14
Diethylethanolamine (DEA). Dalam absorbsi dengan reaksi kimia suatu molekul A (solute), diabsorb ke dalam suatu cairan B (reaktan), dimana komponen A bereaksi dengan komponen B. Reaksi tersebut bisa berlangsung dalam regim cepat, lambat,
reversible, irreversible, dan sembarang orde reaksi. Proses
keseluruhan dapat diperkirakan menjadi 4 tahap (Astarita, 1967). 1. Difusi A ke fase gas menuju interface gas-cair
2. Difusi A dari interface ke dalam cairan, dan difusi B dari cairan menuju interface serta terjadi reaksi antara A dan B 3. Difusi produk dari reaksi dalam fas cair, produk volatil akan
mendifusi ke interface
4. Difusi produk gas menuju fase gas
Adanya reaksi kimia dapat mengubah profil konsentrasi A, gradien konsentrasinya akan naik sehingga mempercepat laju absorbsinya dibandingkan dengan absorbsi fisik. Oleh karena itu, untuk memeperhitungkan pengaruh reaksi kimia terhadap konsentrasi komponen yang mendifusi dalam daerah dekat
interface, maka dalam persamaan difusi unsteady harus
ditambahkan persamaan laju reaksi kimia. Laju absorbsi diturunkan menurut ketiga model perpindahan massa yang dijelaskan sebelumnya. Teori film, teori penetrasi, dan teori pembaharuan permukaan merupakan model-model yang sifatnya sangat teoritis. Model-model ini biasanya mempunyai lingkup penerapan yang relatif lebih luas. Namun pemakaian dari model ini sifatnya praktis, meskipun mempunyai ruang lingkup penerapan yang terbatas, tetapi model ini lebih mudah digunakan dan memerlukan waktu perhitungan yang relatif singkat,.
Pada kasus absorpsi gas A kedalam liquida, ada kemungkinan gas terlarut A bereaksi dengan pelarut/reaktan lain dalam liquida dengan laju reaksi rA. Perhatikan Gambar 2.3,
15
Gambar 2.3 Tranfer Massa Gas ke Dalam Liquida Disertai
Reaksi Kimia
rate in = rate out + accumulation + reaction rate
)
(
)
(
)
(
Adx
r
Adx
t
c
A
dN
N
A
N
A A A A A
(2.24))
(
)
(
A
dx
r
Adx
t
c
A
dN
A
N
A
N
A A A A A
(2.25)x
c
D
N
A A A
fluks difusi A dalam liquida (Fick’s first law)Bila Persamaan (2.24) dibagi dengan A.dx, dan disubstitusi harga NA diperoleh: A A A A r t c dx dC D dx d (2.26)
16 A A A A r t C x C D 2 2 (2.27)
2.2.1 Pengaruh Reaksi Kimia pada Laju Perpindahan Massa
Dalam sistem multifase reaksi kimia mempengaruhi laju perpindahan massa dalam dua cara yang berbeda:
Pada laju reaksi rendah, merubah konsentrasi
perpindahan bulk yang terlarut, sehingga menaikkan
driving force.
Sebaliknya reaksi cepat, gradien konsentrasi dekat
interface mempengaruhi enhancement laju perpindahan
massa.
2.2.2 Enhancement Factor
Dalam absorpsi gas dimana perpindahan massa gas-liquida yang disertai dengan reaksi kimia dalam fase liquida laju absorpsi gas bisa dinaikkan secara signifikan. Secara umum untuk menjelaskan pengaruh konsep enhancement factor ini diterapkan, dimana enhancement factor E didefinisikan sebagai perbandingan laju spesifik absorpsi gas dalam liquida reaktif dengan laju spesifik absorpsi pada kondisi identik dalam liquida non reaktif (perpindahan massa fisika). Beberapa model teoritis telah
dikembangkan untuk menghitung pengaruh ini, karena
pentingnya enhancement factor untuk tujuan perancangan. Model yang paling banyak dipergunakan adalah film model, Higbie
penetration model dan Danckwerts surface renewal model. Enhancement factor E dapat diperkirakan secara numerik
dengan menggunakan Persamaan (2.31) dan menggunakan model transfer massa interface tertentu. Pada reaksi order dua searah persamaan dapat diselesaikan menurut film model.
0 2 2 2 B A A A k C C x C D (2.28)
17 0 2 2 2 B A B B zk C C x C D (2.29)
Dengan kondisi batas: CA = CAi x = 0 CA = CA0 x = δ (2.30) CB = CB0 x = δ
0
dx
dC
B x = 0Van Krevelen dan Hoftijer (1948) telah menyelesaikan persamaan diatas menggunakan metode pendekatan dan hasil dapat direpresentasikan dalam pers (2.31):
1 tanh 1 Ei E Ei M Ei E Ei M E (2.31)
Dimana Ei = enhancement factor yang berhubungan reaksi instan dan 1 0 2
k
C
k
D
M
A B (2.32) Ai A B B C zD C D Ei 0 1 (2.33)18 Ai C k R E 1 ' (2.34) 2.2.3 Regim Reaksi
Dalam fenomena absorpsi reaktif ada dua proses kompetitif yang harus diperhatikan yaitu reaksi dan difusi. Laju relatif proses ini digambarkan sebagai waktu reaksi dan difusi.
Waktu reaksi tR adalah ukuran waktu yang dibutuhkan reaksi
kimia untuk merubah sejumlah konsentrasi reaktan yang terbatas. Waktu difusi tD adalah ukuran waktu yang tersedia fenomena
difusi molekuler terjadi sebelum bercampur dalam fase liquida menjadi konsentrasi yang sama.
Rasio tak berdimensi
R D t t dipergunakan untuk
menghitung laju reaksi dan difusi relatif. Parameter penting lain
adalah Bilangan Hatta yang didefinisikan sebagai
L B A
k
C
k
D
M
2 0 (2.35)Ada tiga regim reaksi yang didefinisikan sebagai laju relatif reaksi dan difusi:
<<1 danM
< 0.02 reaksi ini sangat lambat untuk mendapatkan pengruh yang signifikan pada fenomena difusi dan tidak terjadi rate enhancement. Enhancement factor itu E. Kondisi ini sebagai “Slow Reaction Regime” dalam regim reaksi kimia yang hanya menjaga konsentrasi solut rendah .
--- dan 0.02 < M < 2 ,batas reaksi cepat tertentu “Instantaneous Reaction Regim” tercapai bila semua tahanan transfer massa yang disebabkan kinetika kimia telah dihilangkan, pada titik dan enhancement factor untuk reaksi instan E akan sangat besar. Harga E yang dihitung adalah 102 sampai 103.
>>1 dan M > 2, reaksi ini cukup cepat untuk menghasilkan19
2.3 Alkanolamine
Alkanolamine dapat diklasifikasikan menjadi tiga
berdasarkan struktur kimianya, yaitu primary amine, secondary
amine dan tertiary amine. Primary amine memiliki satu rantai
alkanol dan dua atom hidrogen yang terikat atom nitrogen, contohnya adalah monoethanolamine (MEA). Secondary amine memiliki dua rantai atom alkanol dan satu atom hidrogen yang terikat atom nitrogen, contohnya adalah diethanolamine (DEA) dan diisopropylamine (DIPA). Tertiary amine tidak memiliki atom hidrogen, secara langsung terikat atom nitrogen, contohnya adalah methyldiethanolamine (MDEA) (Cullinane, 2005; Wang, 2011).
Keunggulan senyawa alkanolamine dalam menyerap gas karbon dioksida adalah laju absorpsi cepat dan biaya pelarut murah. Namun terdapat beberapa kelemahan senyawa amine seperti panas absorpsi tinggi, tidak dapat memisahkan senyawa-senyawa merkaptan, konsumsi energi untuk regenerasi pelarut cukup tinggi, dan bersifat korosif.
Alkanolamina adalah senyawa kimia dengan gugus hidroksi (-OH) dan gugus amino (-NH2, -NHR, dan –NR2) pada rantai alkana. Alkanolamina adalah pelarut preferensial yang digunakan oleh kilang minyak dan pabrik gas alam. Berbagai jenis alkanolaminea telah digunakan meliputi Monoethanolamine
(MEA), Diethanolamine (DEA), Diglycolamine (DGA),
Diisopropanolamine (DIPA), dan Methyldiethanolamine
(MDEA). Prefiks ’mono’, ’di’ dan ’tri’ menyatakan derajat substitusi radikal pada gugus amino nitrogen.
Kriebel dkk., (1998) menyarankan bahwa ethanolamines lebih stabil secara kimia, bersih, dan cairan tanpa warna.
Alkanolamines stabil secara kimia, dan dapat dipanaskan hingga
ke titik didih saat dekomposisi, kecuali triethanolamine yang cukup reaktif secara kimia dan dapat terdekomposisi di bawah
boiling point 680 0F. Berdasarkan gugus alkanol yang terikat dengan atom nitrogen, alkanolamina diklasifikasikan menjadi amina primer, sekunder, dan tersier. Maddox dkk., (1998)
20
melaporkan bahwa masing-masing alkanolamina memiliki setidaknya satu gugus hidroksil dan satu gugus amino. Gugus hidroksil mengurangi tekanan uap dan meningkatkan kelarutan di dalam air dimana gugus amino meningkatkan alkalinitas dalam larutan air untuk bereaksi dengan gas asam. Amina primer dan sekunder memiliki ikatan atom nitrogen dengan atom hidrogen yang masih dapat disubsitusi oleh gugus hidroksil, sedangkan atom nitrogen pada amina tersier tidak berikatan dengan atom hidrogen.
Pada proses absorpsi CO2 dari gas alam, biasanya
digunakan pelarut kimia golongan alkanolamina, yaitu
monoethanolamina (MEA), diethanolamina (DEA), dan
metildiethanolamina (MDEA), yang dipilih berdasarkan kecepatan laju absorpsi, kemampuan penyerapan CO2 yang tinggi
dan kemudahan regenerasi. Perbandingan karakteristik pelarut alakanolamina dapat dilihat pada tabel II.1 di bawah ini.
Tabel 2.1 Perbandingan Karakteristik Pelarut Alakanolamina
Pelarut Kelebihan Kekurangan
Monoethanole Amine(MEA) Sangat reaktif terhadap CO2 dan H2S. Mampu menghilangkan CO2 dan H2S secara bersamaan. Recovery CO2 dan H2S tinggi. Harganya paling murah dibanding pelarut amin lainnya. Alat rentan mengalami korosi, terutama jika konsentrasinya di atas 20%wt. Mengalami reaksi irreversible dengan COS dan CS2
sehingga tidak cocok digunakan untuk gas
yang mengandung
kedua senyawa
tersebut.
Tekanan uapnya
tinggi sehingga
21
Pelarut Kelebihan Kekurangan
hilang saat diregenerasi. Energi yang dibutuhkan untuk regenerasi cukup tinggi. Diethanole Amine (DEA) Tekanan uapnya lebih rendah dibanding MEA sehingga mengurangi kehilangan massa saat regenerasi. Dapat digunakan untuk absorpsi gas yang yang mengandung COS dan CS2.
Dapat bereaksi
dengan CO2 secara irreversible sehingga
pelarut ini tak
optimal jika
digunakan untuk
absorpsi gas dengan kandungan CO2 yang tinggi. Methyl Diethanole Amine (MDEA) Tekanan uapnya sangat rendah sehingga dapat digunakan dengan konsentrasi sampai 60%wt. Sangat selektif terhadap CO2. Tidak korosif. Banyak digunakan Akibat keselektifannya yang tinggi terhadap CO2,
maka akan terjadi
H2S slippage
sehingga absorpsi
H2S kurang
maksimal. Oleh
karena itu pelarut ini biasanya digunakan untuk absorpsi gas CO2 tanpa adanya
22
Pelarut Kelebihan Kekurangan
untuk absorpsi dengan kandungan CO2 yang tinggi. Energi untuk regenerasi rendah. Harganya paling mahal di antara pelarut amina lainnya.
(Sumber: Kohl & Nielsen, 1997 ; Kidnay, 2006)
2.4 Jenis Promotor 2.4.1 DL-Methionine
DL-Methionine merupakan salah satu asam amino esensial yang terdapat dalam tubuh manusia, senyawa ini merupakan asam amino dengan gugus amina primer. Dalam keadaan aqueous tanpa adanya zat terlarut lain, secara umum asam amino berada dalam keadaan zwitter ion, dimana terdapat gugus bermuatan negatif (karboksil) dan gugus bermuatan positif (amina). Menurut Majchrowicz (2008) penambahan basa kuat seperti KOH pada zwitter ion ini akan menghilangkan proton pada gugus amina dan menjadikannya molekul bermuatan negatif (ter-deprotonisasi), molekul inilah yang nantinya dapat mengikat karbondioksida dan menjadi karbamat sesuai dengan penelitian yang dilakukan Lerche pada tahun 2012.
3 2
3
H H
H NRCOOH OOCRNH RNH COO
(2.34) 2 2 2 2 ( ) CO H NRCOO OHRNH COO H O (2.35) 2.4.2 Piperazine
Piperazine (PZ) secara bebas larut dalam air dan etilena glikol, tetapi tidak larut dalam dietil eter dan merupakan basa lemah. Piperazine mudah menyerap air dan karbon dioksida dari udara. Meskipun banyak turunan piperazine terbentuk secara alami, piperazine sendiri dapat disintesis dengan mereaksikan
23
amonia beralkohol dengan 1,2-dikloroetana, oleh aksi natrium dan etilena glikol pada etilen diamin hidroklorida, atau dengan pengurangan pyrazine dengan natrium dalam etanol. Piperazine pada umumnya tersedia industri adalah sebagai hexahydrate (C4H10N2. 6H2O) yang meleleh pada 44°C dan mendidih pada
125-130° C
2.5 Kinetika Reaksi
Mekanisme reaksi dari absorbsi CO2 dengan menggunakan
promoter DL-Methionine dalam larutan MDEA adalah sebagai berikut. 1,21 2 1 2 3 2 1 2 3 3 K k CO R R R N H OR R R NH HCO (2.36) 2,22 2 2 ( )2 2 K k CO H NRCOO OHRNH COO HO (2.37) 3,23 2 1 2 3 2 ( )2 1 2 3 K k CO R R R N HNRCOORNH COO R R R NH (2.38) 4,24 2 3 K k CO OHHCO (2.39) 5 2 3 2 3 3 K HCOH OCO H O (2.40) 6 2 2 3 K H NRCOO H SH NRCOO HS (2.41) 7 2 3 3 2 2 ( ) K ( ) RNH COO H OH NR COO H O (2.42) 8 1 2 3 3 1 2 3 2 K R R R N H OR R R NH H O (2.43) 9 2 3 2H OK H O OH (2.44)
24
Untuk sistem CO2-(MDEA-Methionine) nilai k23 dapat
diestimasi dengan persamaan Arhenius, sehingga didapatkan korelasi sebagai berikut. Korelasi ini sesuai hasil eksperimen yang dikerjakan oleh Camacho dkk (2008).
23
6243.5
ln
k
22, 4
T
(2.45) Berdasarkan penelitian yang dilakukan oleh Wen Xu (1992) mengenai studi kinetika absorbsi gas karbon dioksida dalam larutan MDEA yang diaktivasi didapatkan hasil bahwa pada dasarnya reaksi overall antara CO2 dengan MDEA adalahsebagai berikut.
2 2 3 3 3
CO H OR NR NHHCO (2.46) Studi kinetika dari reaksi CO2 dengan MDEA dilakukan
dalam sebuah disk column dan pada tekanan atmosfir. Rate absorpsi dari gas CO2 kedalam larutan MDEA diukur pada
rentang konsentrasi 1.75-4.28 kmol/m3, dan temperatur antara 30-70 C. Data eksperimen dari laju absorbsi digambarkan sebagai hubungan rapid pseudo-first-order reversible reaction.
2 2 2 2 2 1/ 2 * 2 CO CO CO am CO CO N H D k C p p (2.47) 6 21 3984 5.86 10 exp k T (2.48) Dalam larutan MDEA yang telah diaktivasi, model dari laju absorbsi bisa digambarkan sebagai dua paralel rapidpseudo-first-order reversible reaction dan laju reaksi keseluruhan dari
karbon dioksida adalah.
2 2
* 2 am p p CO CO
r k C k C C C (2.49) Dimana Cam dan Cp adalah konsentrasi dari amine dan
potassium methionine. Sedangkan nilai plot Arhenius untuk kp
diberikan pada persamaan berikut.
11
2.98 10 exp 6424 /
p
25
Pinsent et al. Melakukan pengukuran terhadap reaksi antara CO2 dengan ion hidroksida dari 0-40 C. Dimana dinyatakan
bahwa reaksi adalah reaksi orde dua.
2 3 CO OHHCO (2.51) 3 13 6666 ( / ) 4.315 10 exp OH k m kmol s T (2.52) Berdasarkan data eksperimen yang dilakukan oleh Liu dkk (2002). Reaksi yang terjadi saat absorpsi gas CO2 kedalam larutan
MDEA berpromotor potassium methionine adalah sebagai berikut. CO2 + OH HCO-3 (2.53) CO2 + H2O + R3N R3NH + + HCO-3 (2.54) CO2 + H NRCOO2 + OH -2 (CO ) RNH O + H2O (2.55)
Berdasarkan reaksi diatas maka rate reaksi antara CO2 dengan
MDEA adalah sebagai berikut. r1 = kOH(OH
-)(CCO2-C *
CO2) (2.56)
r2 = (kMDEACMDEA+kPCP)(CCO2-C *
CO2) (2.57)
Dimana CMDEA dan CP adalah konsentrasi MDEA dan
potassium methionine. Sedangkan kOH-, kMDEA dan kp adalah
berturut-turut konstanta laju reaksi untuk ion OH-, MDEA dan potassium methionine. Konstanta-konstanta tersebut diperoleh dari penelitian yang dilakukan Xu, dkk (1992).
(
) (2.58)
2.6 Tipe Kolom
Absorpsi termasuk proses pemisahan berdasarkan proses difusi. Kecepatan perpindahan massa tergantung pada luas permukaan bidang batas antara fase uap dan fase cair yang saling mengadakan kontak. Saat merancang alat kontak diusahakan
26
meningkatkan efisiensi pemisahan. Secara umum alat kontak bisa diklasifikasikan sebagai tray/plate dan packing.
2.6.1 Tray Column
Tray atau plate tower adalah kolom pemisah berupa
silinder tegak dimana bagian dalam dari kolom berisi sejumlah
tray atau plate yang disusun pada jarak tertentu (tray/plate spacing) di sepanjang kolom. Cairan dimasukan dari puncak
kolom dan dalam perjalanannya cairan akan mengalir dari tray yang satu ke tray yang lain yang ada di bawahnya. Selama proses berlangsung, di setiap tray akan terjadi kontak fase antara fase cairan dengan fase uap yang dimasukkan dari dasar kolom. Secara keseluruhan kontak antara fase dalam tray tower dapat dipandang sebagai aliran lawan arah (countercurrent), meskipun arus yang sebenarnya terjadi arus silang (crossflow). Komponen pada tray column:
1.Downcomer: lubang tempat masuknya aliran dari atas berupa liquid (plate atas) ke plate bawah (kita memandang plate bawah ini sebagai acuan). 2. Downflow: lubang tempat keluaran liquid dari plate atas
(kita memandang sebagai acuan) ke plate di bawahnya.
3. Cap: penghalang / pengkontak antara liquid dan uap yang dipasang di setiap tray, bentuk seperti topi yang pinggirnya ada slot untuk mengatur bes ar kecilnya gas yang keluar keatas.
4. Slot: tempat bukaan pada cap yang mempunyai
macam-macam bentuk (trapesium, persegi, segitiga) yang berfungsi mengatur bukaan gas yang keluar ke atas sehingga liquid dan gas berkontak secara normal.
5. Baffle: penghalang yang berada di tengah-tengah tray untuk membuat aliran lebih lama berada di tray (penerapan hanya di reverse flow).
27
6. Weir: penghalang yang dipasang di pinggir dari
downflow utk membuat agar volume liquid yang tertampung di tray banyak, sehingga efektifterjadinya kontak antara liquid dan gas. Tray atau plate adalah alat kontak antar fase yang berfungsi sebagai:
1. Tempat berlangsungnya proses perpindahan 2. Tempat terbentuknya keseimbangan
3. Alat pemisah dua fase seimbang Tipe tray atau plate:
1. Bubble Cap Tray
2. Sieve Tray atau Perforated Tray 3. Ballast atau Valve Tray
28
Gambar 2.5 Perbandingan Tipe Tray
2.7 Penelitian yang Sudah Dilakukan
Pemodelan dan simulasi ini merupakan lanjutan dari pemodelan dan simulasi sebelumnya. Pemodelan dan simulasi mengenai absorpsi CO2 terdahulu menggunakan packed column,
sedangkan untuk tray column masih belum begitu banyak
dilakukan penelitian. Penelitian yang sudah dilakukan
29
Tabel 2.2 Penelitian yang Sudah Dilakukan Penulis (tahun) Judul Hasil Bishnoi, S., and Rochelle, G. T. (2000)
Carbon Dioxide Absorption and Solution Equilibrium in
Piperazine Activated
Methyldiethanolamine
Modeling heat
transfer model, energy balance dan mass balance untuk
absorpsi CO2 pada K2CO3 berpromotor DEA Al-Baghli, dkk., (2001)
A rate-based model for the design of gas absorbers for the removal of CO2 and H2S using aqueous solutions of MEA and DEA
Mengajukan
rate-based model untuk
merancang alat
absorber gas CO2
dan H2S
menggunakan larutan MEA dan DEA
Van Loo dkk., (2007)
The removal of carbon dioxide with activated
solutions of methyl-diethanol-amine Dengan menambahkan promotor MEA sebesar 2,5%mol ke dalam larutan MDEA akan menurunkan jumlah tray dari 40 ke 25 Baniadam dkk., (2009) Incorporation of Eulerian-Eulerian CFD framwork in mathematical modeling of chemical absorption of acid gases into methyl diethanol amine on sieve trays
Model matematis
yang memberikan
fenomena distribusi
temperatur serta
nilai enhancment
faktor pada tiap tray Rozi dkk .,
(2009)
Simulasi absorpsi CO2 dan
H2S dengan larutan MDEA
dalam kolom valve-tray
Validasi pada
30 Penulis (tahun) Judul Hasil Ibrahim dkk., (2014) Effect of piperazine on carbon dioxide removal from natural gas using aqueous methyl diethanol amine Penggunaan piperazine sebesar 3% sebagai aktivator akan menurunkan jumlah CO2 yang terkandung di dalam umpan hingga kurang dari 1% Borhani dkk., (2016)
Modeling study on CO2 and H2S simultaneous removal using MDEA solution
Penggunaan rate-based model di dalam absorpsi reaktif antara CO2 dan H2S dengan larutan MDEA di dalam packed column
31
BAB III
METODOLOGI PENELITIAN
Penelitian ini dilakukan secara teoritis dengan mengembangkan model matematik proses absorpsi gas CO2 dari
gas alam ke dalam pelarut MDEA dengan penambahan DL-Methionine di dalam tray column dalam kondisi isotermal. Simulasi ini bisa dipergunakan untuk merancang absorber dan melakukan optimasi pengoperasian unit absorber. Sistem yang dipelajari adalah tray column dengan diameter, tinggi, dan jenis
32
dibawah.
Gambar 3.1 Langkah-langkah pembuatan model matematik
untuk proses absorpsi gas CO2 dari gas alam ke dalam larutan
promotor MDEA dengan aktivator DL-Methionine di dalam tray
column.
Rate-based model
Model matematika pada matlab
Numerical Computation
Simulasi Penyerapan gas CO2 pada
Matlab Studi literatur Data Geometri: Tipe tray Jumlah tray Diameter tray Tinggi weir Tray spacing Jumlah lubang dalam tray Diameter lubang pada tray Kondisi Operasi: Suhu liquid masuk
Suhu gas masuk
Tekanan operasi
Molefraksi CO2,
H2S, N2 Laju alir gas dan Pengembangan model rate-based absorpsi
dengan pendekatan enhancement factor
Penyelesaian numerik pembuatan program dengan software Matlab versi 6.1
Simulasi model terhadap beberapa variabel kondisi Validasi dengan data eksperimen skala pilot-plant Analisis faktor simulasi Output : Distribusi komponen Recovery CO2 dan H2S Error<0.15 ya Tidak
33
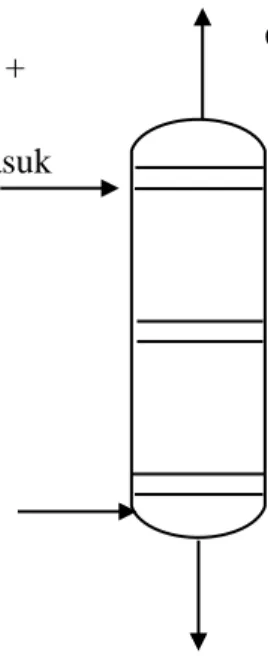
3.1 Sistem yang DitinjauSistem yang ditinjau adalah sistem kolom absorber yang ditunjukkan seperti gambar berikut :
Gambar 3.2 Sistem Absorpsi Gas CO2 dari Gas Alam ke dalam
Larutan MDEA dengan Aktivator DL-Methionine di dalam Tray
Column
Gas alam Masuk
Gas alam Keluar
Larutan
MDEA +
Potassium
Methionine Masuk
LarutanMDEA +
Potassium
Methionine Keluar
34
3.2 Model Matematika3.2.1 Sistem Reaksi Kimia
Mekanisme reaksi dari absorbsi CO2 dengan menggunakan
promoter DL-Methionine dalam larutan MDEA adalah sebagai berikut : 1, 21 2 1 2 3 2 1 2 3 3 K k CO R R R N H OR R R NH HCO 2,22 2 2 ( )2 2 K k CO H NRCOO OHRNH COO H O 3 23, 2 1 2 3
2
(
)
2 1 2 3 K kCO
R R R N
H
NR
COO
RNH COO
R R R NH
8 1 2 3 3 1 2 3 2 K R R R N H OR R R NH H O (3.7) 9 2 3 2H OK H O OH (3.8)3.2.2 Data Kinetika Reaksi
Untuk sistem CO2-(MDEA-Methionine) nilai k23 dapat
diestimasi dengan persamaan Arhenius, sehingga didapatkan korelasi sebagai berikut. Korelasi ini sesuai hasil eksperimen yang dikerjakan oleh Camacho dkk (2008).
23
6243.5
ln
k
22, 4
T
(3.9) 4,24 2 3 K k CO OHHCO 5 2 3 2 3 3 K HCOH OCO H O35
Berdasarkan penelitian yang dilakukan oleh Wen Xu (1992) mengenai studi kinetika absorbsi gas karbon dioksida dalam larutan MDEA yang diaktivasi didapatkan hasil bahwa pada dasarnya reaksi overall antara CO2 dengan MDEA adalah
sebagai berikut.
2 2 3 3 3
CO H OR NR NHHCO (3.10) Studi kinetika dari reaksi CO2 dengan MDEA dilakukan
dalam sebuah disk column dan pada tekanan atmosfir. Rate absorpsi dari gas CO2 kedalam larutan MDEA diukur pada
rentang konsentrasi 1.75-4.28 kmol/m3, dan temperatur antara 30-70 C. Data eksperimen dari laju absorbsi digambarkan sebagai hubungan rapid pseudo-first-order reversible reaction.
2 2 2 2 2 1/ 2 * 2 CO CO CO am CO CO N H D k C p p (3.11) 6 21 3984 5.86 10 exp k T (3.12) Dalam larutan MDEA yang telah diaktivasi, model dari laju absorbsi bisa digambarkan sebagai dua paralel rapidpseudo-first-order reversible reaction dan laju reaksi keseluruhan dari
karbon dioksida adalah.
2 2
* 2 am p p CO CO
36
Dimana Cam dan Cp adalah konsentrasi dari amine dan
potassium methionine. Sedangkan nilai plot Arhenius untuk kp
diberikan pada persamaan berikut.
11
2.98 10 exp 6424 /
p
k T (3.14)
Pinsent et al. Melakukan pengukuran terhadap reaksi antara CO2
dengan ion hidroksida dari 0-40 C. Dimana dinyatakan bahwa reaksi adalah reaksi orde dua.
2 3 CO OHHCO (3.15) 3 13 6666 ( / ) 4.315 10 exp OH k m kmol s T (3.16) Berdasarkan data eksperimen yang dilakukan oleh Liu dkk (2002). Reaksi yang terjadi saat absorpsi gas CO2 kedalam larutan
MDEA berpromotor potassium methionine adalah sebagai berikut. CO2 + OH HCO-3 (3.17) CO2 + H2O + R3N R3NH + + HCO-3 (3.18) CO2 +
H NRCOO
2 + OH -2 (CO ) RNH O + H2O(3.19)Berdasarkan reaksi diatas maka rate reaksi antara CO2 denngan
MDEA adalah sebagai berikut. r1 = kOH(OH
-)(CCO2-C *
CO2) (3.20)
r2 = (kMDEACMDEA+kPCP)(CCO2-C *