Studi Pengaruh pH Proses Pelindian Pada Proses Ekstraksi Titanium
Dioksida Dari Pasir Besi Tasikmalaya Dengan Menggunakan Metode
Hidrometalurgi
Ina Fajria dan Bambang Suharno
Teknik Metalurgi dan Material Fakultas Teknik Universitas Indonesia
ina.fajria@gmail.com
Abstrak
Indonesia saat ini masih memiliki ketergantungan terhadap negara lain dalam pengimporan titanium dioksida, untuk mengurangi ketergantungan tersebut, perlu digunakan pasir besi yang terdapat dalam negeri untuk diproses dengan metode yang lebih efektif dalam memenuhi kebutuhan. Metode yang umum dan mudah dilakukan adalah metode hidrometalurgi dengan melibatkan proses pelindian.
Penelitian ini memanfaatkan pasir besi lokal yang berasal dari Cipatujah, Tasikmalaya, dan dilakukan untuk mengetahui kadar titanium dioksida yang dapat dihasilkan dari pasir besi Tasikmalaya dengan kadar Ti yang termasuk rendah yaitu 4,43%. Selain itu, karena sifat Ti yang amfoter, kondisi ideal saat proses pelindian masih belum jelas, sehingga diharapkan kondisi pH ideal saat proses pelindian dapat diketahui dengan adanya penelitian ini.
Variabel yang digunakan adalah dengan melakukan pelindian dalam kondisi pH yang beragam, yaitu kondisi asam dengan pH 3, kondisi netral, dan kondisi basa dengan pH 9. Hasil penelitian menunjukkan adanya perbedaan %recovery Ti pada setiap perbedaan kondisi tersebut. %Recovery yang dihasilkan dalam kondisi pelindian pH 3 adalah sebesar 50,82%, pH 7 sebesar 25,82%, dan pH 9 sebesar 21,39%.
Study of pH Effect on Leaching Process of Titanium Dioxide Extraction Process from Tasikmalaya Iron Sand Using Hydrometallurgy Method
Abstract
Indonesia currently still has a dependency on other countries in importing titanium dioxide. To reduce dependence on imports from other countries, it is necessary to use iron sand in Indonesia to be processed by methods that are more effective in fulfilling the needs. The method that general and easy to do is a hydrometallurgical method using leaching process.
This study using the local iron sands derived from Cipatujah, Tasikmalaya, to determine the content of titanium dioxide that can be produced from iron sand Tasikmalaya which are has low content of Ti, 4.43%. In addition, because of the natural properties of Ti is amphoteric, the ideal conditions for the leaching process is still unclear, so this study will determined the ideal conditions of pH for the leaching process.
Leaching process carried out in various conditions of pH, ie acidic conditions with pH 3, neutral, and alkaline conditions with pH 9. The results showed a difference %recovery of Ti. The result of %Recovery in the leaching conditions of pH 3 is 50.82%, 25.82% at pH 7, and 21.39% at pH 9.
Keywords : leaching process; Tasikmalaya iron sand; titanium dioxide; hydrometallurgy
Pendahuluan
Titanium termasuk unsur yang jumlahnya banyak terdapat di bumi. Jumlahnya lima kali lebih sedikit dibanding besi, namun seratus kali lipat lebih banyak dibandingkan dengan tembaga[1].
Dalam aplikasinya, pemakaian titanium lebih banyak dalam bentuk titanium dioksida (TiO2)
berupa pigmen. Pigmen titanium dioksida merupakan bahan baku dalam industri cat putih, kertas, produk kosmetik, maupun teknologi canggih seperti sel solar, semikonduktor, peralatan biomedis, dan purifikasi udara[2]. Sejak tahun 1900-an, pemanfaatan TiO2 telah
dikembangkan hingga kini dengan berbagai proses dan metode penelitian. Bijih titanium yang paling banyak digunakan dalam produksi pigmen tersebut adalah ilmenit (FeTiO3) dan rutil
(TiO2). Pada umumnya, untuk menghasilkan pigmen TiO2 yang baik, mineral rutil lebih
efektif untuk digunakan, namun dengan jumlah rutil yang terbatas di alam, mineral ilmenit digunakan sebagai pengganti rutil dengan mengubahnya menjadi rutil sintetik[3].
Dengan penggunaan yang luas, kebutuhan akan pigmen TiO2 semakin meningkat. Di
Indonesia masih sedikit industri yang bergerak dalam bidang produksi pigmen TiO2, sehingga
selama ini Indonesia lebih banyak mengimpor pigmen TiO2, padahal jumlah mineral ilmenit
banyak terdapat di Indonesia. Mineral tersebut dalam ditemukan dalam bentuk pasir besi bertitan yang dapat ditemukan berbagai daerah, salah satunya Tasikmalaya yang hingga saat ini belum dimanfaatkan secara optimal.
Secara umum terdapat dua proses yang paling umum digunakan dalam pembuatan pigmen TiO2. Proses tersebut adalah adalah proses sulfat dan proses klorida[3,4]. Proses sulfat lebih
dulu dikenal sebelum proses klorida. Pada proses ini bijih yang mengandung titanium dilarutkan dalam asam sulfat sehingga membentuk luluhan dari titanium, besi, dan logam sulfat lainnya dalam satu larutan[4]. Pada proses sulfat, bijih dengan kualitas rendah dapat digunakan namun menghasilkan banyak produk sisa yang membutuhkan perlakukan tepat dalam pembuangannya, sehingga proses klorida lebih mudah untuk digunakan. Proses klorida membutuhkan bijih dengan kualitas yang baik seperti rutil alami (94-98% TiO2), rutil sintetik
(92-95% TiO2), atau terak titanium (80-90% TiO2). Proses klorida memiliki lebih banyak
keuntungan seperti produk yang dihasilkan berkualitas baik, proses yang lebih ramah terhadap lingkungan, dan produk sisa yang lebih sedikit[5].
Tidak seperti mineral lainnya, untuk titanium, bentuk pigmen TiO2 lebih banyak digunakan.
Dari total produksi mineral titanium di dunia, 93% aplikasi digunakan dalam bentuk TiO2,
sedangkan dalam bentuk logam hanya sebesar 3%. Karena itu, semakin banyak jumlah TiO2
dalam kandungan mineralnya, semakin tinggi harga jualnya[7]. Titanium (IV) oksida merupakan bentuk oksida titanium yang paling banyak digunakan sebagai pigmen[6].
Tinjauan Teoritis
Kawasan penambangan pasir besi di Tasikmalaya berlokasi di Cipatujah. Kandungan pasir besi di kawasan Cipatujah tersebut sekitar 30-40%. Hasil penelitian tim teknis Dinas Pertambangan dan Energi kabupaten Tasikmalaya, titanium yang terkandung dalam pasir besi Cipatujah hanya mencakup 5-10%[8].
Proses ekstraksi dan pemurnian titanium jauh lebih rumit dibanding proses ekstraksi logam lain seperti besi, aluminium, dan nikel. Hal tersebut dikarenakan sifat fisika logam titanium yang sangat tergantung pada kandungan oksigen, nitrogen, dan karbon yang terjebak dalam logam[9]. Kebanyakan proses ekstraksi titanium dioksida melibatkan proses hidrometalurgi dengan metode pelindian. Pelindian merupakan proses penting dalam hidrometalurgi. Proses ini akan memisahkan produk yang diinginkan dari pengotor dengan menggunakan pelarut yang kemudian hasil dari proses pelindian akan diambil larutan yang mengandung produk yang lebih murni. Pada proses pelindian, terdapat beberapa faktor yang dapat menentukan laju pelindian. Jika proses difusi larutan melalui struktur pori padatan menjadi faktor pengendali, maka material yang diekstraksi harus memiliki ukuran partikel yang kecil. Sedangkan, jika laju transfer larutan dari lapisan luar padatan ke pelarut cukup rendah, maka kecepatan pengadukan dalam proses akan menjadi faktor pengendali yang berperan cukup besar. Pada umumnya, laju ekstraksi dengan proses pelindian dipengaruhi oleh beberapa faktor[10], yaitu: 1. Ukuran Partikel
Partikel dengan ukuran yang kecil akan menyebabkan kontak permukaan yang besar antara padatan dengan pelarut sehingga akan mempercepat transfer massa dan mempercepat pula terjadinya proses difusi pada larutan. Semakin kecil partikel, maka luas permukaan per unit berat semakin besar sehingga laju pelindian akan meningkat. Namun, ukuran partikel yang terlalu kecil dapat menyebabkan permasalahan dalam pemisahan atau penyaringan produk yang diinginkan dengan residu atau pengotornya.
2. Pelarut (Zat Pelindian)
Pelarut yang digunakan dalam proses pelindian harus memiliki selektivitas yang baik terhadap bahan yang akan diambil dan mempunyai viskositas yang lebih rendah agar memudahkan untuk proses resirkulasi pelarut. Semakin besar konsentrasi zat pelindi, semakin meningkat pula laju pelindian.
3. Temperatur
Pada kebanyakan proses pelindian, semakin meningkat temperatur semakin tinggi kinetika proses pelindiannya, dengan kata lain semakin cepat pula kecepatan ekstraksinya. Namun
demikian, peningkatan temperatur sedikit banyak berpengaruh pada proses yang dikontrol oleh mekanisme kimia.
4. Kecepatan Pengadukan
Pengadukan pelarut akan meningkatkan proses difusi sehingga akan meningkatkan transfer atau difusi massa dari permukaan padatan ke larutan. Pengadukan juga berperan untuk mencegah sedimentasi dari sistem suspensi proses ekstraksi.
Kemampuan menyeleksi dari zat pelindian terhadap suatu mineral tertentu yang dalam bijih sangat diperngaruhi oleh konsentrasi dari zat pelindian, semakin meningkatnya konsentrasi zat pelindian, maka jumlah dari mineral berharga yang larut akan semakin bertambah. Selain itu, temperatur juga memberikan sedikit pengaruh terhadap efisiensi proses pelindian, tapi dapat pula mempengaruhi peningkatan jumlah pengotor dalam larutan. Presentase pengotor dalam larutan dapat pula disebabkan oleh waktu kontak yang berlebihan antara pelarut dengan bijih, sehingga waktu kontak optimum harus diketahui agar dapat memaksimalkan recovery logam berharga dan meminimalkan pengotor yang larut[11].
Metode Penelitian
Proses ekstraksi dan pemurnian titanium jauh lebih rumit dibanding proses ekstraksi logam lain seperti besi, aluminium, dan nikel. Hal tersebut dikarenakan sifat fisika logam titanium yang sangat tergantung pada kandungan oksigen, nitrogen, dan karbon yang terjebak dalam logam[9].
Bahan-bahan yang digunakan dalam penelitian ini adalah pasir besi Tasikmalaya sebagai bahan dasar untuk diproses melalui proses ekstraksi dengan metode hidrometalurgi. Pasir besi yang digunakan dalam penelitian ini diambil dari daerah Cipatujah, Tasikmalaya. Untuk pembuatan sampel penelitian, pasir besi Tasikmalaya diayak untuk didapat ukuran partikel sebesar 125 yang kemudian pasir tersebut dipisahkan secara magnetik untuk memisahkan material berdasarkan sifat feromagnetik, paramagnetik, dan diamagnetik dengan menggunakan pemisah magnetik berjenis roll ganda terinduksi sehingga didapat pasir yang bersifat para magnetik yaitu pasir ilmenit. Proses selanjutnya merupakan peleburan dengan menggunakan fluks natrium hidroksida (NaOH) sebagai agen kimia dalam proses peleburan pasir besi Tasikmalaya yang berfungsi untuk mengikat Ti dengan reaksi sebagai berikut: 4FeO.TiO2 + 8NaOH + O2 4Na2TiO3 + 2Fe2O3 + 4H2O dan aditif sebagai agen kimia
untuk mempercepat terjadinya reaksi pengikatan Ti oleh Na yang terjadi dalam proses peleburan pasir besi.
Dalam proses pelindan digunakan zat asam sulfat yang dibuat dengan mencampurkan H2SO4
pekat dengan aquades dengan perbandingan jumlah 1:9. H2SO4 ini digunakan untuk
mengubah pH larutan hasil saring sehingga didapat pH yang bervariasi yaitu 3, 7, dan 9. Perhitungan %recovery titanium pada sampel hasil proses pelindian didapat dengan menggunakan rumus:
Hasil Penelitian dan Pembahasan
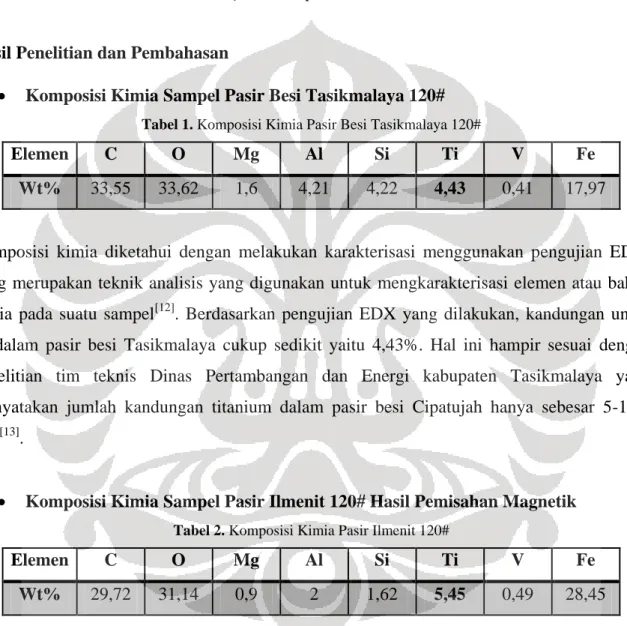
Komposisi Kimia Sampel Pasir Besi Tasikmalaya 120# Tabel 1. Komposisi Kimia Pasir Besi Tasikmalaya 120#
Elemen C O Mg Al Si Ti V Fe
Wt% 33,55 33,62 1,6 4,21 4,22 4,43 0,41 17,97
Komposisi kimia diketahui dengan melakukan karakterisasi menggunakan pengujian EDX, yang merupakan teknik analisis yang digunakan untuk mengkarakterisasi elemen atau bahan kimia pada suatu sampel[12]. Berdasarkan pengujian EDX yang dilakukan, kandungan unsur Ti dalam pasir besi Tasikmalaya cukup sedikit yaitu 4,43%. Hal ini hampir sesuai dengan penelitian tim teknis Dinas Pertambangan dan Energi kabupaten Tasikmalaya yang menyatakan jumlah kandungan titanium dalam pasir besi Cipatujah hanya sebesar 5-10% saja[13].
Komposisi Kimia Sampel Pasir Ilmenit 120# Hasil Pemisahan Magnetik Tabel 2. Komposisi Kimia Pasir Ilmenit 120#
Elemen C O Mg Al Si Ti V Fe
Wt% 29,72 31,14 0,9 2 1,62 5,45 0,49 28,45
Berdasarkan pengujian EDX yang dilakukan, kandungan unsur Ti dalam pasir ilmenit sebanyak 5,54%. Hal ini menunjukkan peningkatan jumlah Ti yang terkandung dibandingkan dengan kandungannya di dalam pasir besi Tasikmalaya.
Pada data hasil pemisahan magnetik terhadap pasir besi Tasikmalaya, didapat hasil peningkatan kadar Ti. Pada sampel awal, didapat jumlah Ti sebesar 4,43%. Sampel awal berupa pasir besi Tasikmalaya tersebut kemudian dipisahkan dengan metode pemisahan magnetik dan manghasilkan Ti sebanyak 5,45%. Hal tersebut menunjukkan peningkatan
jumlah Ti yang terkandung. Dengan adanya peningkatan jumlah tersebut, menunjukkan bahwa pemisahan magnetik cukup efektif untuk dilakukan. Selain peningkatan kadar Ti, jumlah silika yang terkandung juga menurun dari 4,22% menjadi 1,62% yang menunjukkan bahwa pemisahan tersebut juga efektif untuk mengurangi kadar silika dari pasir ilmenit yang akan diambil.
Pengaruh pH Pelindian terhadap Jumlah Endapan Ti(OH)x Hasil Pelindian
Gambar 1. Larutan Hasil Pelindian Sampel (a) variabel pH 3, (b) variabel pH 7, (c) variabel pH 9
Dari gambar di atas, dapat dilihat perbedaan warna larutan yang terbentuk, semakin rendah pH semakin asam larutan, warna larutan tersebut semakin berwarna kuning. Perubahan warna tersebut dapat disebabkan oleh larutan H2SO4 yang ditambahkan menyebabkan warna larutan
yang semula bening menjadi lebih kuning. Berikut ini merupakan tabel data sampel pelindian.
Tabel 3. Data Sampel Pelindian
Sampel pH 3 pH 7 pH 9
Massa NaTiO3 35 gram 35 gram 35 gram
Volume aquades 150 ml 150 ml 150 ml
Volume H2SO4 (yang ditambahkan) ±35 ml ±25 ml ±20ml
Jumlah Endapan TiO2 hasil Pelindian 0,23 gram 4,17 gram 3,64 gram
Berdasarkan data tersebut, didapat grafik jumlah endapan Ti(OH)x hasil proses pelindian
sebagai berikut:
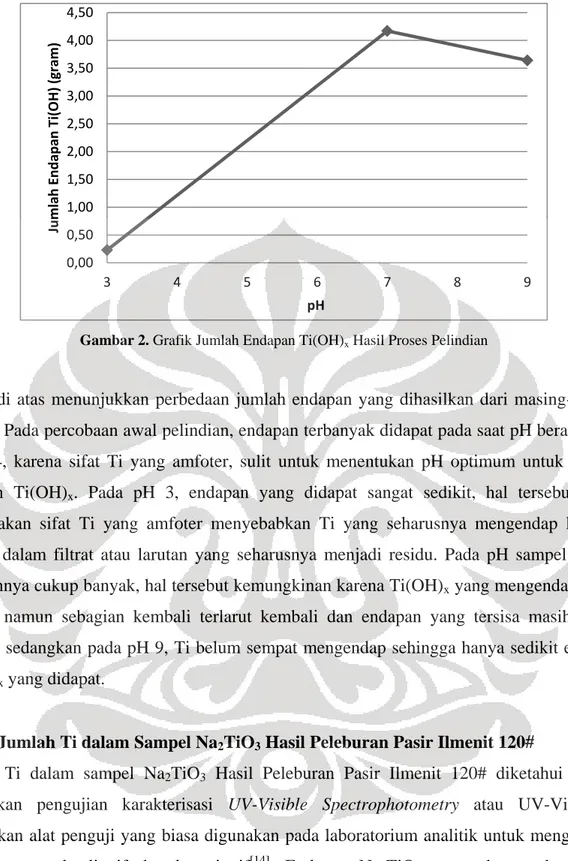
Gambar 2. Grafik Jumlah Endapan Ti(OH)x Hasil Proses Pelindian
Grafik di atas menunjukkan perbedaan jumlah endapan yang dihasilkan dari masing-masing sampel. Pada percobaan awal pelindian, endapan terbanyak didapat pada saat pH berada pada titik 8,4, karena sifat Ti yang amfoter, sulit untuk menentukan pH optimum untuk didapat endapan Ti(OH)x. Pada pH 3, endapan yang didapat sangat sedikit, hal tersebut dapat
dikarenakan sifat Ti yang amfoter menyebabkan Ti yang seharusnya mengendap kembali terlarut dalam filtrat atau larutan yang seharusnya menjadi residu. Pada pH sampel 7 hasil endapannya cukup banyak, hal tersebut kemungkinan karena Ti(OH)x yang mengendap sudah
banyak namun sebagian kembali terlarut kembali dan endapan yang tersisa masih cukup banyak, sedangkan pada pH 9, Ti belum sempat mengendap sehingga hanya sedikit endapan Ti(OH)x yang didapat.
Jumlah Ti dalam Sampel Na2TiO3 Hasil Peleburan Pasir Ilmenit 120#
Jumlah Ti dalam sampel Na2TiO3 Hasil Peleburan Pasir Ilmenit 120# diketahui dengan
melakukan pengujian karakterisasi UV-Visible Spectrophotometry atau UV-Vis yang merupakan alat penguji yang biasa digunakan pada laboratorium analitik untuk menganalisis elemen secara kualitatif dan kuantitatif[14]. Endapan Na2TiO3 merupakan padatan hasil
peleburan pasir ilmenit 120# dengan fluks NaOH dan aditif. Hasil peleburan berupa padatan dihancurkan sehingga didapat padatan dengan ukuran kecil yang dilarutkan dengan aquades. Gambar 3 adalah Na2TiO3 + Fe2O3 hasil peleburan pasir ilmenit. Endapan yang telah
dibersihkan dengan aquades merupakan sampel yang dilakukan pengujian UV-VIS sehingga dapat diketahui jumlah unsur Ti yang tertinggal yang tidak melalui proses pelindian.
0,00 0,50 1,00 1,50 2,00 2,50 3,00 3,50 4,00 4,50 3 4 5 6 7 8 9 Jumlah Endapa n Ti(OH ) (gr am) pH
Gambar 3. Sampel Na2TiO3 Hasil Peleburan Pasir Ilmenit dengan fluks NaOH dan Aditif (kiri: sebelum
dihancurkan, kanan: setelah dihancurkan)
Tabel 4. Jumlah Konsentrasi Ti dalam Endapan Na2TiO3
Elemen Ti
% 11,26
Jumlah Ti dalam Filtrat Residu Hasil Pelindian
Tabel 5. Jumlah Konsentrasi Ti dalam Filtrat Larutan Elemen
Ti
Larutan pH 3 Larutan pH 7 Larutan pH 9
mg/mL 27,1 13,07 10,96
% 2,71 1,307 1,096
Dari ketiga sampel yang dilindi, didapat kandungan Ti terbanyak dimiliki oleh larutan hasil pelindian dengan kondisi pH 3. Hal tersebut dapat disebabkan sifat Ti yang amfoter sehingga Ti yang seharusnya mengendap menjadi Ti(OH)x terlarut kembali, dan pada pH 3 endapan
Ti(OH)x yang didapat sangat dikit dimana kemungkinan Ti terlarut kembali dalam larutan
yang seharusnya menjadi residu hasil pelindian. Begitu juga yang terjadi pada larutan hasil pelindian dalam kondisi pH 7 maupun 9.
Komposisi Kimia Sampel Hasil Roasting
TiO2 yang diuji merupakan hasil proses pelindian berupa endapan yang telah disaring
sehingga didapat pasta berupa Ti(OH)x, pasta tersebut kemudian diroasting untuk
menguapkan H2O sehingga didapat hasil berupa serbuk atau bubuk TiO2. Proses pelindian
dilakukan dalam tiga kondisi berbeda, yaitu pada kondisi asam dengan pH 3, kondisi netral atau pH 7, dan kondisi basa dengan pH 9. Hasil pengujian yang didapat akan dianalisis untuk mengetahui kondisi pH mana yang menghasilkan peningkatan jumlah kandungan Ti terbesar.
Tabel 6. Komposisi Kimia Sampel Hasil Roasting Sampel Elemen C O Na Al Si Ti P/S Fe pH 3 Wt% 25,26 47,98 1,76 14,68 5,43 0,06 2 0,56 pH 7 33,49 41,57 13,82 3,01 2,29 0,10 0,07 0,17 pH 9 30,70 40,22 11,41 7,99 7,99 0,07 1,96 0,18
Analisis Pengaruh pH Pelindian terhadap Kandungan Ti o % Recovery Sampel Hasil Pelindian
Tabel 10. Jumlah Total Ti dalam Sampel
pH 3 pH 7 pH 9
Ti hasil roasting 0,06 % 0,10 % 0,07 %
Ti dalam filtrat 2,71 % 1,307 % 1,096 %
Sampel Ti hasil roasting dan Ti dalam filtrat merupakan jumlah Ti yang dihasilkan oleh proses pelindian, sedangkan sampel sebelum didapat dari jumlah Ti yang terdapat dalam pasir ilmenit hasil pemisahan magnetik berukuran 120#. Dari data tabel di atas, dapat dihitung jumlah persentase recovery hasil proses pelindian yang dilakukan, yaitu:
Dari data di atas, dapat dihitung jumlah persentase recovery hasil proses pelindian yang dilakukan, yaitu:
Tabel 7. Persentase Recovery Ti Hasil Proses Pelindian
pH 3 pH 7 pH 9
%recovery 50,82% 25,82% 21,39%
Jika dibandingkan hasil dari ketiga sampel yang didapat, didapat bentuk grafik %recovery dari ketiga sampel adalah sebagai berikut:
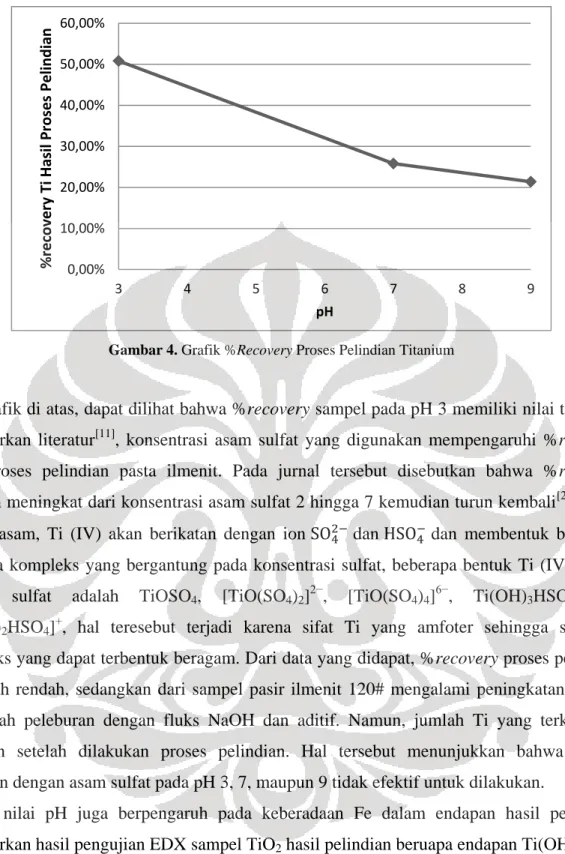
Gambar 4. Grafik %Recovery Proses Pelindian Titanium
Dari grafik di atas, dapat dilihat bahwa %recovery sampel pada pH 3 memiliki nilai terbesar. Berdasarkan literatur[11], konsentrasi asam sulfat yang digunakan mempengaruhi %recovery pada proses pelindian pasta ilmenit. Pada jurnal tersebut disebutkan bahwa %recovery titanium meningkat dari konsentrasi asam sulfat 2 hingga 7 kemudian turun kembali[20]. Pada larutan asam, Ti (IV) akan berikatan dengan ion dan dan membentuk beberapa
senyawa kompleks yang bergantung pada konsentrasi sulfat, beberapa bentuk Ti (IV) dalam larutan sulfat adalah TiOSO4, [TiO(SO4)2]2−, [TiO(SO4)4]6−, Ti(OH)3HSO4 dan
[Ti(OH)2HSO4]+, hal teresebut terjadi karena sifat Ti yang amfoter sehingga senyawa
kompleks yang dapat terbentuk beragam. Dari data yang didapat, %recovery proses pelindian sangatlah rendah, sedangkan dari sampel pasir ilmenit 120# mengalami peningkatan jumlah Ti setelah peleburan dengan fluks NaOH dan aditif. Namun, jumlah Ti yang terkandung menurun setelah dilakukan proses pelindian. Hal tersebut menunjukkan bahwa proses pelindian dengan asam sulfat pada pH 3, 7, maupun 9 tidak efektif untuk dilakukan.
Variasi nilai pH juga berpengaruh pada keberadaan Fe dalam endapan hasil pelindian. Berdasarkan hasil pengujian EDX sampel TiO2 hasil pelindian beruapa endapan Ti(OH)x yang
telah diroasting, jumah Fe yang dihasilkan berbeda-beda, berikut tabel jumlah Fe pada serbuk TiO2 hasil roasting.
Tabel 8. Kandungan Fe dalam Serbuk TiO2 hasil Roasting
Sampel Pasir Ilmenit pH 3 pH 7 pH 9
%Fe 28,45% 0,56% 0,17% 0,18% 0,00% 10,00% 20,00% 30,00% 40,00% 50,00% 60,00% 3 4 5 6 7 8 9 %recovery Ti Ha sil Pro ses Pelin dia n pH
Dari tabel 8, dapat dilihat penurunan jumlah kandungan Fe dari sampel awal berupa pasir ilmenit 120#. Pada sampel pasir ilmenit, jumlah Fe sebesar 28,45%. Penurunan jumlah tersebut dapat disebabkan karena adanya proses pencucian sampel hasil peleburan pasir ilmenit dengan fluks dan aditif berupa Na2TiO3 + Fe2O3 yang telah dihancurkan. Saat
pencucian sampel tersebut dengan aquades, Fe2O3 yang ada mengendap di dasar larutan
sementara Na2TiO3 terlarut bersama aquades, namun masih ada beberapa jumlah Fe yang
terlarut, selain itu Fe dari H2SO4 yang ditambahkan pada proses pelindian kemungkinan
menyebabkan masih adanya jumlah Fe pada hasil pelindian.
Neraca Material
Neraca material merupakan hal penting dalam pengontrolan proses, khususnya dalam pengendalian hasil dari produk. Neraca material merupakan penerapan hukum kekekalan massa dimana massa tidak dapat diciptakan maupun dimusnahkan. Alur proses dari material titanium yang terkandung didalam setiap bagian dari setiap tahapan pengujian, dimulai dari awal material pengumpan yang digunakan kemudian pada tahap pelindian hingga tahap presipitasi dihitung dan disajikan dalam sebuah bentuk tabel neraca material pada kondisi optimum.
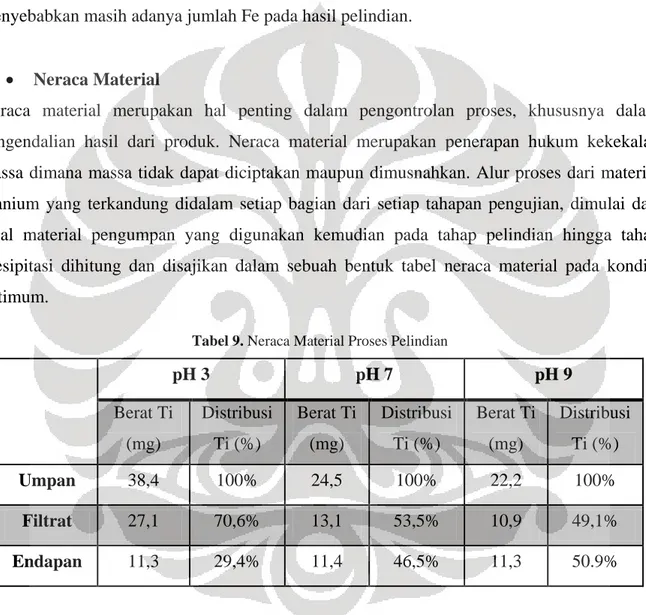
Tabel 9. Neraca Material Proses Pelindian
pH 3 pH 7 pH 9 Berat Ti (mg) Distribusi Ti (%) Berat Ti (mg) Distribusi Ti (%) Berat Ti (mg) Distribusi Ti (%) Umpan 38,4 100% 24,5 100% 22,2 100% Filtrat 27,1 70,6% 13,1 53,5% 10,9 49,1% Endapan 11,3 29,4% 11,4 46,5% 11,3 50.9%
Tabel 9 menunjukkan bahwa pada proses pelindian didapatkan distribusi titanium yang terkandung dalam larutan pada masing-masing pH sebesar 70,6% untuk pH 3, 53,5% untuk pH 7, dan 49,1% untuk pH 9. Sisa dari kandungan titanium yang tidak terdapat dalam filtrat berada di dalam endapan Ti(OH)x yang memiliki distribusi titanium sebesar 29,4% untuk pH
kemudian diroasting untuk menguapkan air dan didapat serbuk TiO2 yang kandungan Ti di
dalamnya sangat rendah.
Kesimpulan
1. Nilai pH pada proses pelindian mempengaruhi jumlah %recovery titanium dari pasir ilmenit 120# menjadi pigmen TiO2. Pada pH 3 %recovery yang dihasilkan sebesar
50,82%, pH 7 25,82%, dan pH 9 21,39%.
2. Pigmen TiO2 berhasil didapatkan dengan mengekstraksi pasir Besi Tasikmalaya
berukuran 120# yang telah diseparasi secara magnetik dengan menggunakan metode hidrometalurgi melalui proses pelindian.
3. Jumlah kandungan Ti yang didapat pada pigmen TiO2 yang dihasilkan sangat sedikit, hal
tersebut dipengaruhi karena kadar Ti yang tertinggal pada filtrat proses presipitasi saat pelindian.
Daftar Referensi
[1] Zhang, W., et al. “A Literature Review of Titanium Metallurgical Processes”.
Hydrometallurgy 108 (2011) 177–188.
[2] Middlemas, Scott, Z. Zak Fang, and Peng Fan. “A New Method for Production of Titanium Dioxide Pigment”. Hydrometallurgy 131–132 (2013) 107–113.
[3] Baba, Alafara A., et al. “Simultaneous Recovery of Total Iron and Titanium from Ilmenite Ore by Hydrometallurgical Processing”. Association of Metallurgical Engineers of Serbia. Scientific Paper UDC: 669.11; 669.295.
[4] DuPont™ Ti-Pure® Titanium dioxide. Brochure. DuPont. 2007
[5] Mehdilo, Akbar, Mehdi Irannajad. “Iron Removing from Titanium Slag for Synthetic Rutile Production”. Department of Mining and Metallurgical Eng. Amirkabir University of Technology, Iran. Physicochemical Problems of Mineral Processing ISSN 2084-4735
[6] Diebold, Ulrike. “The Surface Science of Titanium Dioxide”. Surface Science Report 48 (2003) 53-229
[7] Murty, CVGK, R. Upadhyay, S. Asokan. “Electro Smelting of Ilmenite for Production of TiO2 Slag”. India
[8] Kuznesof, Paul M. “Titanium Dioxide”. Chemical and Technical Assessment. 2006
[9] Sugiarto, Triadi. “Studi Proses Ekstraksi Titanium Oksida dari pasir Besi Cilacap dengan Metode Pelindian Menggunakan Larutan Asam Klorida”. Skripsi. 2001
[10] Habashi, Fathi. Handbook of Extractive Metallurgy Volume 2: Primary Metals, Secondary Metals, Light Metals. Wiley-VCH
[11] Nayl, A.A, H.F. Aly. “Acid Leaching of Ilmenite Decomposed by KOH”.
Hydrometallurgy 97 (2009) 86-93
[12] Campbell, W.C., “Energy Dispersive X-Ray Emission Analysis”. PetroChemical Division. Cleveland. Vol. 104 No. 1236. 1979
[13] Potensi Pasir Besi di Kabupaten Tasikmalaya.
http://regionalinvestment.bkpm.go.id/newsipid/id/commodityarea.php?ia=3206&ic=1 186. (1 April 2013)