TINJAUAN PUSTAKA
2.1. Karbohidrat
Karbohidrat berasal dari pengertian atom karbon yang terhidrasi dengan rumus
(CH2O)n. Tetapi pengertian ini sebenarnya sudah tidak tepat lagi karena banyak
senyawa karbohidrat yang tidak mengandung atom hidrogen dan oksigen dengan
perbandingan 2:1, misalnya gula deoksiribosa yang mempunyai rumus C5H10O4.
Disamping itu banyak pula karbohidrat yang mengandung atom lain seperti
nitrogen, sulfur dan lain-lain yang menunjukkan tidak sesuainya dengan rumus
karbohidrat tersebut. Walaupun demikian, nama karbohidrat ini sampai sekarang
masih terus dipergunakan (Girindra, 1990).
Karbohidrat tersebar luas di dalam tumbuhan dan hewan. Dalam
tumbuhan, glukosa disintesis dari karbondioksida serta air melalui fotosintesis dan
disimpan sebagai pati atau diubah menjadi selulosa yang merupakan kerangka
tumbuhan. Hewan dapat mensintesis sebagian karbohidrat dari lemak dan protein,
tetapi jumlah terbesar karbohidrat dalam jaringan tubuh hewan berasal dari
tumbuhan (Iswari & Yuniastuti, 2006).
Bersama-sama dengan lemak dan protein, karbohidrat memegang peranan
dasar bagi kehidupan di bumi ini. Bukan hanya sebagai sumber energi utama bagi
makhluk hidup, tetapi juga sebagai senyawa yang menyimpan energi kimia. Pada
hewan atau manusia energi disimpan sebagai glikogen dan pada tanaman sebagai
pati. Di samping kedua senyawa tersebut, ada pula karbohidrat pembentuk
tumbuhan, dan peptidoglikan yang terdapat di dinding sel bakteri. Selain terdapat
pada dinding sel bakteri dan tumbuhan, polisakarida juga banyak terdapat pada
dinging sel binatang. Karbohidrat merupakan sumber kalori utama bagi hampir
seluruh penduduk di dunia khususnya bagi penduduk negara yang sedang
berkembang walaupun jumlah kalori yang didapat dihasilkan oleh 1 gram (g)
karbohidrat hanya 4 kalori (kal) dibanding lemak. Karbohidrat mempunyai
peranan penting dalam menentukan karakteristik bahan makanan, misalnya rasa,
warna, tekstur, dan lain-lain. Di alam, karbohidrat merupakan hasil sintesa CO2
dan H2O dengan pertolongan sinar matahari dan hijau daun (chlorophyll). Hasil
fotosintesa ini kemudian mengalami polimerisasi menjadi pati dan
senyawa-senyawa bermolekul besar lain yang menjadi cadangan makanan pada tanaman.
Organisme yang dapat mensintesa biomolekuluntuk keperluan hidupnya dari
bahan-bahan anorganik (misalnya CO2 dan H2O) disebut organisme autotroph.
Sedangkan mikroorganisme pada umumnya, hewan dan manusia yang hanya
dapat mempergunakan hasil sintesa organisme autotroph untuk keperluan
hidupnya disebut organismeheterotroph(Sudarmadji, 1989).
Karbohidrat banyak terdapat dalam bahan nabati, baik berupa gula
sederhana, heksosa, pentosa, maupun karbohidrat dengan berat molekul yang
tinggi seperti pati, pektin, selulosa, dan lignin. Polisakarida seperti pati, banyak
terdapat dalam serealia dan umbi-umbian. Sumber karbohidrat utama bagi bahan
makanan kita adalaah serealia dan umbi-umbian. Misalanya kandungan pati dalam
beras = 78,3%, jagung = 72,4%, singkong = 34,6%, dan talas = 40% (Budianto,
2.2. Klasifikasi Karbohidrat
Karbohirat adalah polihidroksi aldehida atau polihidroksi keton yang mempunyai
rumus molekul umum (CH2O)n. Yang pertama lebih dikenal sebagai golongan
aldosa dan yang kedua adalah ketosa. Dari rumus umum dapat diketahui bahwa
karbohidrat adaalah suatu polimer. Senyawa yang menyusunnya dalah
monomer-monomer (Matorharsono, 1998).
Menurut Yazid dan Nursanti (2006) bahwa dari rumus umum karbohidrat,
dapat diketahui bahwa senyawa ini adalah suatu polimer yang tersusun atas
monomer-monomer. Berdasarkan monomer yang menyusunnya, karbohidrat
dibedakan menjadi 3 golongan, yaitu monosakarida, disakarida dan polisakarida.
2.2.1. Monosakarida
Karbohidrat paling sederhana yang tidak dapat dihidrolisis menjadi karbohidrat
lain. Bentuk lain dibedakan kembali menurut jumlah atom C yang dimiliki dan
sebagai aldosa dan ketosa. Monosakarida yang terpenting adalah glukosa,
galaktosa, dan fruktosa (Yazid & nursanti, 2006).
Menurut Poedjiadi dan Supriyanti (2009), monosakarida ialah karbohidrat
yang sederhana, dalam arti molekulnya hanya terdiri atas beberapa atom karbon
saja dan tidak dapat diuraikan dengan cara hidrolisis menjadi karbohidrat lain.
Tiga senyawa gula yang penting dalam monosakarida adalah glukosa, fruktosa
dan galaktosa.
Tabel 1. Beberapa Jenis Monosakarida
Monosakrida Rumus Molekul Aldosa Ketosa
Triosa C3H6O3 Gliserosa Dihidroksi aseton
Tetrosa C4H8O4 Eritrosa Eritrulosa
Pentosa C5H10O5 Ribosa Ribulosa
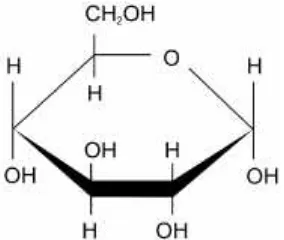
2.2.1.1. Glukosa
kstrosa karena mempunyai sifat dapat m
h kanan. Di alam, glukosa terdapat dalam bua
glukosa dihasilkan dari reaksi antara karbondi
sinar matahari dan klorofil dalam daun. Prose
lukosa yang terbentuk terus digunakan untuk
osa.
6H2O Sinar matahari C6H12O6 + 6O2 klrofil
uk dari glukosa dengan jalan penggabungan m
bentuk rantai lurus maupun bercabang denga
(C6H10O5)n + n H2O
gangan dikenal sirup glukosa, yaitu suatu laruta
gga mempunyai viskositas atau kekentalan yan
eh dari amilum melalui proses hidrolisis dengan a
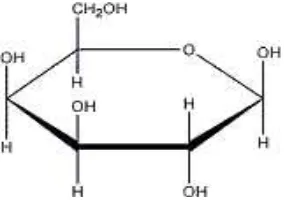
2.2.1.2. Fruktosa
glukosa dalam bentuk
mempunyai rasa kur
Galaktosa mempunya
(Poedjiadi & Supriyant
n glukosa juga mengandung fruktosa. Fruktosa
mempunyai sifat memutar cahaya terpolarisa
but levulosa. Pada umumnya monosakarida
anis. Fruktosa berikatan dengan glukosa mem
asa digunakan sehari-hari sebagai pemanis, b
& Supriyanti, 2009).
Gambar 2. Struktur Fruktosa
jarang terdapat bebas dalam alam. Umunya be
ntuk laktosa, yaitu gula yang terdapat dalam susu.
kurang manis daripada glukosa dan kurang l
punyai sifat memutar bidang cahaya terpolar
2.2.2. Disakarida
Senyawa yang termasuk oligosakarida mempunyai molekul yang terdiri atas
beberapa molekul monosakarida. Dua molekul monosakarida yang berikan satu
dengan yang lain, membentuk satu molekul disakarida. Oligosakarida yang paling
banyak terdapat dalam alam ialah disakarida (Poedjiadi & Supriyanti, 2009).
Disakarida merupakan karbohidrat yang pada hidrolisis menghasilkan 2 molekul
monosakarida yang sama atau berlainan, misalnya sukrosa, maltosa dan laktosa
(Iswari & Yuniastuti, 2006).
Karbohidrat yang tersusun dari dua sampai sepuluh satuan monosakarida.
Oligosakarida yang umum adalah disakarida, yang terdiri atas dua satuan
monosakarida dan dapat dihidrolisis menjadi monosakarida. Contoh: sukrosa,
maltosa, dan laktosa (Yazid & Nursanti, 2006).
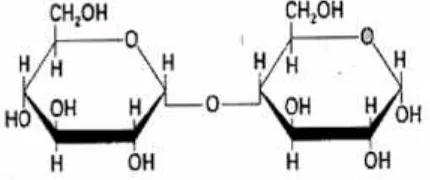
2.2.2.1. Sukrosa
Sukrosa ialah gula yang kita kenal sehari – hari, baik yang berasal dari tebu
maupun bit. Selain dari tebu dan bit, sukrosa terdapat pula pada tumbuhan lain,
misalnya dalam buah nanas dan dalam wortel. Dengan hidrolisis sukrosa akan
terpecah dan menghasilkan glukosa dan fruktosa (Poedjiadi & Supriyanti, 2009).
Sukrosa, berbeda dengan disakarida yang lain. Sukrosa tidak mempunyai
daya mereduksi sama sekali, karena gugus pereduksi kedua satuan itu
ikat-mengikat. Terdiri dari glukosa dan fruktosa. Ikatannya adalah 1,2-glukosidik
(Iswari & Yuniastuti, 2006). Sukrosa mudah dihidrolisis menjadi D-glukosa dan
D-fruktosa. Hidrolisis ini biasa disebut proses inversi dan akan diikuti oleh
jumlah yang sama ant
antara glukosa dan fruktosa. Campuran ini dis
Gambar 4. Struktur Sukrosa
tu disakarida yang terbentuk dari dua molekul
ntara atom karbon nomor 1 dan atom nomor 4,
mpunyai gugus –OH glikosidik dan dengan de
mereduksi. Maltosa merupakan hasil antara
dengan asam maupun dengan enzim (Poedjiadi
osa, sebuah molekul glukosa dihubungkan oleh
bonnya yang pertama dengan gugus hidroksi
ukosa lainnya. Ikatan antara kedua unit monosaka
kosida, sebab atom karbon hemiasetal yang ikut
lah atom karbon dengan konfigurasi α (Girindra
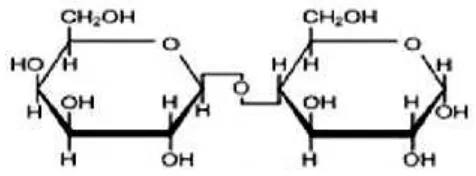
2.2.2.3. Laktosa
laktosa akan menghasilkan galaktosa dan
D-sutu disakarida. Ikatan galaktosa dan glukosa
or 1 pada galaktosa dan atom nomor 4 pada
kul laktosa masih mempunyai gugus –OH glikosi
mempunyai sifat mereduksi dan mutarotasi
ng biasa disebut gula susu terdiri dari D-ga
katan melalui ikatan α (1,4)-glikosidik. Laktosa m
asetal, maka laktosa termasuk disakarida pereduksi
Gambar 6. Struktur Laktosa
tersusun dari sepuluh satuan monosakarida dan
ang. Polisakarida dapat dihidrolisis pleh asa
anya spesifik. Hidrolisis sebagian polisakarida
n dapat digunakan untuk menentukan str
oh: amilum, glikogen, dekstrin, dan selulosa
2.2.3.1. Pati
Pati merupakan bentuk karbohidrat yang disimpan dalam bentuk karbohidrat
tanaman. Pati terdiri dari 2 fraksi yang dapat dipisahkan dengan air panas. Fraksi
terlarut disebut amilosa dan fraksi tidak larut disebut amilopektin. Amilosa
mempunyai struktur lurus dengan ikatan (-(1,4)) D-Glukosa. Sedang amilopektin
mempunyai cabang dengan ikatan (-(1,6)) D-Glukosa. Glukosa sebanyak 4-5%
dari berat total. Sumber pati anatara lain: biji-bijian, akar-akaran, umbi-umbian,
dan buah yang belum matang. Pati merupakan homopolimer glukosa dengan
ikatan a-glikosidik. Berbagai macam pati tidak samaa sifatnya, tergantung dari
panjang rantai C-nya, serta apakah lurus atau bercabang rantai molekulnya
(Budianto, 2009).
Pada umumnya, karbohidrat berupa serbuk putih yang mempunyai sifat
sukar larut dalam pelarut nonpolar, tetapi mudah larut dalam air. Kecuali,
polisakarida bersifat tidak larut dalam air. Amilum dengan air dingin akan
membentuk suspensi dan bila dipanaskan akan terbentuk pembesaran berupa pasta
dan bila didinginkan akan membentuk koloid yang kental semacam gel. Suspensi
amilum akan memberikan warna biru dengan larutan iodium. Hal ini dapat
digunakan untuk mengindetifikasikan adanya amilum dalam suatu bahan.
Hidrolisis sempurna amilum oleh asam atau enzim akan menghasilkan glukosa.
Glikogen mempunyai struktur empiris yang serupa dengan amilum pada
tumbuhan. Pada proses hidrolisis, glikogen menghasilkan pula glukosa karena,
baik amilum maupun glikogen, tersusun dari sejumlah satuan glukosa (Yazid &
2.4. Analisis Karbohidrat
Berbagai cara analisis dapat dilakukan terhadap karbohidrat untuk memenuhi
berbagai keperluan. Dalam ilmu dan teknologi pangan, analisis karbohidrat yang
biasa dilakukan misalnya penentuan jumlahnya secara kuantitatif dalam rangka
menentukan komposisi suatu bahan makanan, penentuan sifat fisisnya atau
kimiawinya dalam kaitannya dengan pembentukan kekentalan, kelekatan,
stabilitas larutan dan tekstur hasil olahannya.
Karbohidrat yang berbentuk polimer memliki ukuran molekul yang sangat
besar dan kompleks serta memiliki satuan monomer berbagai jenis jenis
menyebabkan karbohidrat sulit ditentukan jumlah sebenarnya. Sering jumlah
karbohidrat hanya dapat dinyatakan sebagai jumlah monomer penyusunnya saja
misalnya sebagai heksosa atau pentosa total. Bahkan untuk senyawa yang
homogen (homoglikan) misalnya pati yang terdiri dari monomer glukosa saja,
masih memerlukan kurva standar yang menunjukkan hubungan antara jumlah pati
murni dengan indikatornya (misalnya gula hasil hidrolisanya). Karena terdapat
perbedaan ukuran molekul antara jenis pati yang satu dengan yang lain dan
sulitnya mendapatkan pati yang betul-betul murni yang bebas air dan
senyawa-senyawa lain, maka cara penentuan jumlah pati yang sebenarnya menjadi sangat
sulit
2.4.1 Analisis Kadar Gula
Banyak cara yang dapat digunakan untuk menentukan banyaknya karbohidrat
dalam suatu bahan yaitu antara lain dengan cara kimiawi, cara fisik, cara
enzimatik atau biokimiawi dan cara kromatografi. Penentuan karbohidrat yang
yaitu hidrolisa lebih dahulu sehingga diperoleh monosakarida. Untuk keperluan
ini maka bahan dihidrolisa dengan asam atau enzim pada suatu keadaan yang
tertentu. Salah satu cara untuk menganalisis kadar pati dengan diubah menjadi
gula terlebih dahulu adalah dengan cara Luff Schoorl.
Pada penetuan gula cara Luff Schoorl dimana yang ditentukan bukannya
kuprooksida yang mengendap tetapi dengan menentukan kuprioksida dalam
larutan sebelum direaksikan dengan gula reduksi (titrasi blanko) dan sesudah
direaksikan dengan sampel gula reduksi (titrasi sampel). Penentuannya dengan
titrasi menggunakan Na-tiosulfat. Selisih titrasi blanko dengan titrasi sampel
ekuivalen dengan kuprooksidayang terbentuk dan juga ekuivalen dengan jumlah
gula reduksi yang ada dalam bahan/larutan.
Reaksi yang terjadi selama penentuan karbohidrat cara ini mula-mula
kuprioksida yang ada dalam reagen akan membebaskan iod dari garam K-iodida.
Banyaknya iod yang dibebaskan ekuivalen dengan banyaknya kuprioksida.
Banyaknya iod dapat diketahui dengan titrasi menggunakan Na-tiosulfat. Untuk
mengetahui bahwa titrasi sudah cukup maka diperlukan indikator amilum.
Apabila larutan berubah warna dari biru menjadi putih berarti titrasi sudah selesai.
Agar supaya perubahan warna biru menjadi putih dapat tepat maka penambahan
amilum diberikan pada saat titrasi hampir selesai. Setelah diketahui selisih
banyaknya titrasi blanko dan titrasi sampel kemudian dikonsultasikan dengan
tabel yang sudah tersedia yang menggambarkan hubungan antara banyaknya
Reaksi yang terjadi dalam penetuan gula cara Luff Schoorl dapat
dituliskan sebagai berikut:
R—COH + CuO Cu2O + R—COOH
H2SO4 + CuO CuSO4 + H2O
CuSO4 + 2 KI CuI2 + K2SO4
2 CuI2 Cu2I2 + I2
I2 + 2 Na2S2O3 Na2S4O6 + 2 NaI
I2 + Amilum : Biru (Sudarmadji, 1989).
Untuk dapat dilakukan analisis ini harus dipenuhi syarat-syarat sebagai berikut:
1. Reaksinya harus berlangsung secara cepat. Kebanyakan reaksi ion
memenuhi syarat ini.
2. Reaksinya harus sederhana serta dapat dinyatakan dengan persamaan
reaksi. Bahan yang diselidiki bereaksi sempurna dengan senyawa baku
dengan perbandingan kesetaraan stoikiometris.
3. Harus ada perubahan yang terlihat pada saat titik ekivalen tercapai, baik
secara kimia atau fisika.
4. Harus ada indikator jika syarat 3 tidak terpenuhi. Indikator juga dapat
diamati dengan pengukuran daya hantar listrik (titrasi
potensiometri/konduktometri)
Berikut adalah hal-hal yang diperlukan dalam analisis :
1. Alat pengukur volume seperti buret, pipet volume, dan labu takar yang
ditera secara teliti (telah dikalibrasi)
2. Senyawa pembakuan harus senyawa dengan kemurnian yang tinggi
Disamping itu diperlukan juga neraca analitik untuk menimbang bahan yang
akan diselidiki atau senyawa baku untuk membuat larutan baku (Rohman, 2007).
2.4.2. Analisis Kandungan Air
Analisis kandungan air dapat dilakukan dengan berbagai cara, salah satunya
adalah metode pengeringan(thermogravimetri).
Metode ini prinsipnya menguapkan air yang ada dalam bahan dengan
jalan pemanasan di dalam oven dengan suhu ± 100-110 oC selama 3 jam atau
sampai berat yang konstan. Untuk bahan-bahan yang tidak panas, seperti pada
bahan yang berkadar gula tinggi, minyak, daging, kecap ataupun bahan-bahan
yang lainnya, pemanasan dilakukan pada oven vakum dengan suhu yang lebih
rendah. Suatu bahan yang telah mengalami pengeringan ternyata lebih bersifat
higroskopis dari pada bahan aslinya. Oleh karena itu selama pendingan sebelum
penimbangan, bahan selalu ditempatkan dalam ruang tertutup, yang kering
misalnya dalam eksikator atau desikator yang telah diberi zat penyerap air. Zat
penyerap ini dapat menggunakan kapur aktif, asam sulfat silika gel alumunium
oksida, kalium klorida, dalium hidroksida dan lain-lain (Budianto,2009).
Menurut Sudarmadji (1989) bahwa kelemahan cara ini adalah:
1. Bahan lain disamping air juga ikut menguap dan ikut hilang bersama dengan
uap air misalnya alkohol, asam asetat, minyak atsiri dan lain-lain.
2. Dapat terjadi reaksi selama pemanasan yang menghasilkan air atau zat mudah
menguap lain. Contoh gula mengalami dekomposisi atau karamelisasi, lemak
mengalami oksidasi dan sebagainya.
2.4.3. Analisis Kandungan Abu
Sebagian besar bahan makanan, yaitu 96 % terdiri dari organik dan air
sisanya terdiri dari unsur-unsur mineral. Unsur mineral juga dikenal sebagai zat
anorganik atau abu. Dalam proses pembakaran bahan-bahan organik terbakar
tetapi zat anorganiknya tidak. Karena itulah disebut abu.
Menurut Sudarmadji (1989) bahwa penentuan abu total dapat digunakan untuk berbagai tujuan yaitu diantara lain:
1. Untuk menentukan baik tidaknya suatu proses pengolahan. Misalnya pada
proses penggilingan gandum diharapkan dapat dipisahkan antara bagian
endosperm dengan kulit/katul dan lembaganya. Apabila masih banyak
katul atau lembaga terikut dalam endosperm maka tepung gandum yang
dihasilkan akan akan mempunyai kadar abu yang relatif tinggi. Hal ini
karena pada bagian katul kandungan mineralnya dapat mencapai 20 kali
lebih banyak daripada dalam endosperm.
2. Untuk mengetahui jenis bahan yang digunakan. Penetuan kadar abu dapat
digunakan untuk memperkirakan kandungan buah yang digunakan untuk
membuat Jellyatau marmelade. Kandungan abu juga dapat dipakai untuk menentukan atau membedakanfruit vinegar(asli) atau sintetis.
3. Penentuan kadar abu sangat berguna sebagai parameter nilai gizi bahan
makanan. Adanya kandungan abu yang tidak larut dalam asam yang cukup
tinggi menunjukkan adanya pasir atau kotoran yang lain.
Penentuan abu total dapat dikerjakan dengan pengabuan secara kering atau cara langsung dan dapat pula secara basah atau cara tidak langsung.
Penentuan kadar abu dengan cara ini adalah dengan mengoksidasikan
semua zat organik pada suhu tinggi. Yaitu sekitar 500-600oC yang
kemudian melakukan penimbangan zat yang tertinggal setelah proses
pembakaran. Bahan yang mempunyai kadar tinggi sebelum pengabuan
harus dikeringkan hilang. Baru kemudian dinaikkan sesuai suhunya sesuai
dengan yang dikehendaki.
2. Penentuan Kadar Abu Secara Tidak Langsung (Cara Basah)
Pengabuan basah dapat digunakan untuk diganti sampel dalam usaha
penentuan froce elemen dan logam-logam beracun. Pengabuan cara basah ini prinsipnya adalah memberikan reagen kimia tertentu ke dalam bahan
sebelum dilakukan pengabuan. Berbagai bahan kimia yang sering
digunakan adalah asam sulfat yang ditumbuhkan ke dalam sampel untuk
membantu mempercepat terjadi reaksi oksidasi, campuran asam sulfat dan
potasium sulfat dipergunakan untuk mempercepat dekomposisi sampel.
Campuran asam sulfat, asam sitrat yang berfungsi mempercepat proses
pengabuan dan masih banyak lagi zat-zat kimia yang lain yang membantu
salam proses pengabuan ( Budianto, 2009).
Perbedaan pengabuan cara kering dan cara basah.
1. Cara kering biasa digunakan untuk menentukan total abu dalam suatu
bahan makanan dan hasil pertanian, sedangkankan cara basah untuktrace element.
2. Cara kering untuk penentuan abu yang larut dan tidak larut dalam air serta
abu yang tidak larut dalam asam memerlukan waktu yang relatif lama
3. Cara kering memerlukan suhu yang relatif tinggi, sedang cara basah
dengan suhu relatif rendah.
4. Cara kering dapat digunakan untuk sampel yang relatif banyak, sedang
cara basah sebaiknya sampel sedikit dan memerlukan reagensia yang
kadangkala berbahaya. Karena menggunakan reagensia maka penentuan
cara basah perlu koreksi terhadap reagen yang digunakan (Sudarmadji,