B - 64
KAJIAN ADSORPSIFe(III) PADA KOMPOSIT ARANG KAYU APU (Pistia stratiotesL.)- KITOSAN-GLUTARALDEHIDA
ADSORPTIONSTUDY OF Fe (III) ON COMPOSITE CHARCOALKAYU APU (Pistia stratiotes L.)-CHITOSA-GLUTARALDEHYDE
Umi Baroroh Lili Utami, Radna Nurmasari,Muslimah Murliana Program Studi Kimia FMIPA Universitas Lambung Mangkurat
Jl. A. Yani Km. 36 Banjarbaru Kalimantan Selatan e-mail :liliutami@yahoo.com
ABSTRAK
Salah satu teknik untuk mengurangi pencemaran logam berat Feyang banyak terdapat dalam air asam tambang adalah menggunakan kitosan. Kitosan larut pada kondisi asam, maka kitosan dikompositkan menggunakan arang kayu apu dan glutaraldehida. Penelitian ini bertujuan untuk mengetahui pH optimum, waktu optimunm,kapasitas adsorpsi, dan % recoveri komposit arang kayu apu-kitosan-glutaraldehida. Pengukuran larutan Fe3+ menggunakan Spektrofotometer Serapan Atom (SSA). Hasil penelitian menunjukkan bahwa pH dan waktu optimum adsorpsi Fe3+ terjadi pada pH 4 dan waktu 45 menit dengan kapasitas adsorpsi sebesar 1,011mg/g dan % recoverisebesar 96,25%.
Kata kunci : Pistia stratiotes L., adsorpsi, komposit, kitosan
ABSTRACT
One techniques to reduce the concentration of heavy metal Fe in in acid mine drainage is adsorption by chitosan. To modify solution chitosan in acid condition, chitosan to composited by charcoal kayu apu and glutaraldehyde. The aims of this research were includimg optimum pH, optimum agitation time, to determine adsorption capacity and % recovery of thecomposite charcoal kayu apu-chitosan-glutaraldehyde. The concentration of Fe3+ aqueaus were determination by using Atomic Absortion Spectrofotometer (AAS). Based on the results obtained, the optimum pH was reached at pH 4 optimum agitation time at 45 minutes, and adsorption capacity was 1,011mg/g, % recovery of 96,25
B - 65 PENDAHULUAN
Arang aktif adalah arang yang diaktivasi dengan cara kimia atau fisika sehingga daya serapnya tinggi dengan kadar karbon yang bervariasi. Permukaan arang aktif relatif telah bebas dari deposit hidrokarbon dan
mampu melakukan adsorpsi karena
permukaannya lebih luas dan pori-porinya telah terbuka (Baker, et al. 1997). Selama ini bahan arang aktif yang digunakan berasal dari limbah limbah kayu dan bambu. Selain itu, arang aktif juga dapat dibuat dari tumbuhan air contohnya adalah arang aktif tumbuhan kayu apu (Pistia stratiotes L.). Pada dasarnya semua jenis tanaman air mampu menyerap logam berat dalam jaringan akarnya dan dapat dimanfaatkan sebagai filter biologis maupun sebagai fitoremediator logam berat dalam penanganan limbah. Hasil penelitian Puspita (2011)menunjukkan bahwa kayu apu (Pistia
stratiotes L.) mampu menurunkan kadar krom
dalam air limbah batik sebesar 33,61%. Kitosan adalah kitin yang telah mengalami proses penghilangan gugus asetil dengan nama lain adalah 2-amino-2-deoksi D-glukopiranosa dengan ikatan (1→4) ß (Sanchez et al., 1981). Kitosan mempunyai kemampuan untuk mengikat ion-ion logam, sehingga sangat berguna dalam mengikat ion-ion logam seperti besi (Fe), tembaga (Cu), dan
magnesium (Mg). Kecenderungan kitosan untuk menggumpal dan membentuk gel menimbulkan masalah ketika kitosan akan digunakan sebagai adsorben untuk mengadsorpsi ion logam dalam lingkungan asam (Boddu et al, 2003) Sehingga untuk meningkatkan ketahanan fisiknya maka dilakukan modifikasi fisik kitosan, salah satunya dengan mensintesisnya menjadi berbentuk kitosan bead yang tidak larut dalam asam (Mahmudah et al, 2013).Kitosan bead pada penelitian ini dibuat dengan melapiskan arang aktif kayu apu pada gel kitosan, dimana arang aktif kayu apu berfungsi sebagai material pendukung dan kitosan sebagai adsorben dapat digunakan berulang-ulang. adsorben yang didapat juga selanjutnya diikat silang dengan glutaraldehida yang berfungsi sebagai perantara tautan silang untuk PVA dan beberapa polisakarida lain seperti kitosan (Wang et al., 2004). Hal ini didasarkan atas penelitian Wan Ngah et al.(2002) yang menyatakan bahwa kitosan berikat silang mempunyai ketahanan fisik terhadap asam yang lebih baik daripada kitosan tak berikat silang, sehingga adsorben arang kayu apu terlapis kitosan terikat silang glutaraldehida ini dapat digunakan sebagai adsorben pada pH rendah seperti pada air asam tambang. Oleh sebab itu akan dilakukan penelitian kajian
B - 66
kapasitas adsorpsi Fe pada arang kayu apu yang telah dilapisi kitosan dan terikat silang glutaraldehida.
BAHAN DAN METODE Preparasi Sampel
Tanaman kayu apu dicuci dengan air yang mengalir lalu dipisahkan bagian akar dan daunnya kemudian dipotong-potong dan selanjutnya dikeringkan dengan cara dijemur. Bagian daun yang telah kering selanjutnya diarangkan, dihaluskan dan disaring hingga diperoleh ukuran partikel 60 mesh. Proses aktivasi arang kayu apu pertama-tama dilakukan dengan merendam arang kayu apuselama 24 jam menggunakan HCL 0,1 M sebanyak 2 kali, lalu disaring, dicuci dengan akuades hingga netral dan direndam lagi dengan NaOH 0,1 M selama 24 jam. Arang yang telah direndam dengan NaOH 0,1 M selama 24 jam selanjutnya disaring, dinetralkan, dikeringkan dalam oven yang diatur pada suhu 70°C selama 24 jam kemudian disimpan dalam desikator sampai beratnya konstan.Pengujian kualitas arang kayu apu juga dilakukan berdasarkan SNI 1995 yang meliputi kadar air, kadar zat terbang, kadar abu serta daya jerap iodin. Penetapan variasi perbandingan arang kayu apu:kitosan yang akan digunakan untuk kajian
adsorpsi dilakukan dengan uji kelarutan yang dibagi menjadi 2 tahap meliputi uji kelarutan pada variasi pH dan uji kelarutan pada variasi konsentrasi glutaraldehida. Proses pelapisan kitosan pada arang kayu apu dilakukan dengan membuat gel kitosan, dimana gel kitosan dibuat dengan melarutkan 7 gram kitosan menggunakan asam oksalat 10% sambil diaduk dan dipanaskan pada suhu 40-50°C hingga larut, yang selanjutnya ditambahkan arang kayu apu yang telah diaktivasi sebanyak 5 gram sambil distirer, kemudian gel yang terbentuk dipipet kedalam NaOH 2Myang berfungsi sebagai agen koagulan pembentuk komposit. Komposit yang didapatkan dicuci hingga netral, lalu dikeringkan dalam oven pada suhu 110°C selama 4 jam. Pembuatan ikat silang dengan glutaraldehida dilakukan dengan merendam komposit yang selanjutnya disebut sebagai adsorben A dengan glutaraldehida 2,5% dengan perbandingan pergram adsorben A : 1,5 ml glutaraldehida 2,5%. Adsorben A yang telah diikat silang dengan glutaraldehida 2,5% yang disebut komposit arang-kitosan -glutaraldehida lalu disaring, dicuci hingga netral dan dikeringkan dalam oven pada suhu 110°C selama 4 jam. Komposit arang-kitosan -glutaraldehida inilah yang akan diteliti kajian adsorpsinya terhadap logam Fe3+.
B - 67 Penentuan pH Optimum Adsorpsi Fe3+ oleh Komposit Arang Kayu Apu-Kitosan-Glutaraldehida
Larutan Fe dibuat dengan konsentrasi 10 mg/l dari larutan stok Fe3+ 1000 mg/l. Sebanyak 20 ml larutan Fe3+ 10 mg/l dipipet ke dalam erlenmeyer 50 ml. Kemudian pH larutan di dalam masing-masing Erlenmeyer diatur dengan menambahkan larutan HCl atau NaOH. Variasi pH untuk adsorpsi Fe oleh komposit arang-kitosan -glutaraldehidaadalah 2; 3; 4; 5 dan 6. Ke dalam setiap larutan dimasukkan 0,5 gram komposit arangkitosan -glutaraldehida, kemudian dilakukan pengocokan dengan shaker selama 1 jam. Disaring dan filtrat yang diperoleh dianalisis dengan menggunakan AAS untuk mengetahui jumlah total Fe dalam larutan setelah interaksi.
Penentuan WaktuOptimum Adsorpsi Fe3+ oleh Komposit Arang Kayu Apu-Kitosan-Glutaraldehida
Sebanyak 20 ml larutan Fe3+ 10 mg/l dipipet ke dalam erlenmeyer 50 ml. Ke dalam setiap larutan masukkan 0,5 gramkomposit arang-kitosan -glutaraldehida, kemudian dilakukan pengocokan menggunakan shaker dengan waktu yang bervariasi. Variasi waktu yang diamati dalam penelitian untuk komposit
arang-kitosan -glutaraldehidabervariasi dari 15; 30; 45; dan 60 menit. Setelah interaksi antara adsorben dengan larutan telah berlangsung sesuai dengan waktu yang diinginkan, dilakukan penyaringan. Filtrat yang diperoleh dianalisis dengan menggunakan AAS untuk mengetahui jumlah Fe3+ yang tersisa dalam larutan.
Penentuan Kapasitas Adsorpsi Fe3+ oleh Komposit Arang Kayu Apu-Kitosan-Glutaraldehida
Larutan Fe dibuat dengan variasi konsentrasi awal 10; 25; 50; 75 dan 100 mg/l melalui pengenceran dari larutan stok Fe 1000 mg/l. Selanjutnya ke dalam erlenmeyer 50 ml dipipetkan 20 ml larutan untuk setiap konsentrasi awal dan ditambahkan 0,5 gramkomposit arang-kitosan -glutaraldehidake dalam setiap larutan tersebut. Selanjutnya dilakukan pengocokan dengan shaker selama 45menit. Setiap larutan kemudian disaring dan filtrat yang diperoleh dianalisis menggunakan AAS untuk mengetahui jumlah Fe dalam larutan yang untuk selanjutnya digunakan dalam penentuan kapasitas adsorpsi.
B - 68 Penentuan Persen Recovery Adsorpsi Fe3+ oleh Komposit Arang Kayu Apu-Kitosan-Glutaraldehida
Komposit arang-kitosan
-glutaraldehida ditimbang sebanyak 0,5 gram, dimasukkan ke dalam Erlenmeyer 50 ml yang berisi 20 ml larutan logam dengan kapasitas adsorpsi optimum yang sudah diatur pH optimumnya. Filtrat diambil setelah dikontakkan pada waktu kontak optimum. Adsorben dilarutkan kembali menggunakan HCl 0,1 M dan dikontakkan selama waktu kontak yang digunakan, kemudian disaring dan diambil kembali filtrat hasil saringan.
Recovery adsorben dilakukan sebanyak 2 kali
pengulangan. Filtrat yang dihasilkan
HASIL DAN PEMBAHASAN Uji Kualitas Arang kayu apu
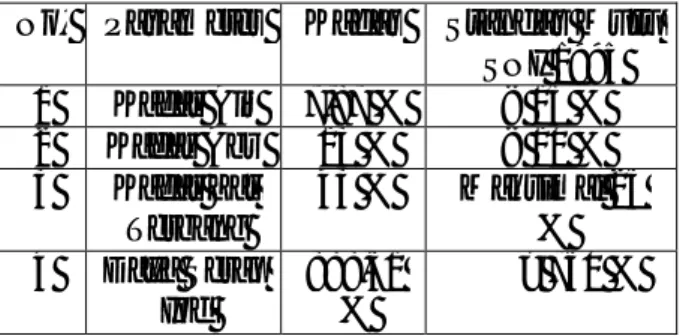
Pengujian kualitas arang kayu apu dilakukan berdasarkan SNI 1995 yang meliputi kadar air, kadar zat terbang, kadar abu serta daya jerap iodin. Hasil uji kualitas arang kayu apu ditunjukkan pada Tabel 1. Tabel 1. Uji kualitas arang kayu apu
No. Parameter Kadar Standar Mutu SNI 1995 1 Kadar Air 7,87 % < 15 % 2 Kadar Abu 13 % < 10 % 3 Kadar Zat Terbang 43 % Maksimal 25 % 4 Daya Serap Iod 888,51 % > 750 %
Pada Tabel 1menunjukkan hasil dari uji kualitas arang kayu apu. Dari hasil uji kualitas, didapatkan kadar air arang kayu apu sebesar 7,875%, dan daya jerap iod sebesar 888,51 mg/g. Nilai kadar air dan daya jerap iod yang didapat telah memenuhi standar uji kualitas arang aktif berdasarkan SNI 1995, dimana persyaratan untuk kualitas arang aktif memiliki kadar air kurang dari 15% dan daya jerap iod lebih besar dari 750 mg/g. Hasil uji kadar abu arang kayu apu yang didapat sebesar 13,5% sedikit lebih besar dari standar yang dipersyaratkan yaitu untuk kadar abu arang aktif kurang dari 10%, sedangkan nilai kadar zat terbang kayu apu sebesar 43% juga lebih besar dibandingkan standar yaitu maksimal 25%. Penetapan kadar zat terbang bertujuan untuk mengetahui jumlah zat atau senyawa yang belum menguap pada proses karbonisasi dan aktivasi, tetapi menguap pada suhu 950ºC. Tingginya kadar zat terbang yang tinggi pada arang kayu apu bisa disebabkan oleh tingginya kerapatan arang kayu apu. Penetapan variasi perbandingan arang kayu apu:kitosan yang akan digunakan untuk kajian adsorpsi dilakukan dengan uji kelarutan yang dibagi menjadi 2 tahap meliputi uji kelarutan pada variasi pH dan uji kelarutan pada variasi konsentrasi glutaraldehida. Hasil uji kelarutan ditunjukkan pada Tabel 2. dan Tabel 3.
B - 69 Tabel 2. Uji kelarutan arang:kitosan pada variasi pH
A: K Berat komposit yang larut (g) pH 2 pH 3 pH 4 pH 5 pH 6 5:5 0,02 0,01 0,05 0,04 0,05 5:6 0,03 0,09 0,03 0,03 0,03 5:7 0,00 0,00 0,00 0,02 0,02 5:8 0,09 0,04 0,10 0,05 0,06 5:9 0,01 0,03 0,04 0,04 0,11
Tabel 3. Uji kelarutan kitosan pada variasi konsentrasi glutaraldehida
% Glu Berat komposit yang larut (g)
1,0 0,15 0,09
1,5 0,08 0,11
2,0 0,09 0,11
2,5 0,02 0,03
Uji kelarutan arang:kitosan pertama-tama dilakukan pada variasi pH. Komposit arang dibuat dengan berat arang 5 gram sedangkan untuk berat kitosan divariasikan dari 5;6;7;8 dan 9 gram. Uji kelarutan pada variasi pH ini dilakukan untuk mengetahui variasi komposit arang kayu apu dan kitosan mana yang paling tidak larut pada rentang pH 2-6 dengan mengurangkan berat awal komposit dengan berat akhir komposit setelah perlakuan. Hasil yang didapat adalah variasi komposit arang kayu apu:kitosan sebesar 5:7 (gram) yang memiliki tingkat kelarutan paling kecil pada semua pH. Berdasarkan hasil ini, maka perbandingan arang kayu apu:kitosan yaitu 5:7 (gram) yang akan digunakan untuk
uji kelarutan selanjutnya yaitu pada variasi konsentrasi glutaraldehida. Uji kelarutan pada variasi konsentrasi glutaraldehida ini dilakukan untuk mengetahui konsentrasi glutaraldehida mana yang akan dipakai untuk pembuatan komposit arang:kitosan terikat silang glutaraldehida. Hasil dari uji kelarutan pada variasi konsentrasi glutaraldehida menunjukkan bahwa komposit arang memiliki tingkat kelarutan paling kecil pada konsentrasi glutaraldehida 2,5%. Maka konsentrasi glutaraldehida 2,5% akan digunakan untuk pengikatan silang komposit arang dan kitosan.
Penentuan pH Adsorpsi Fe3+ oleh Komposit Arang Kayu Apu-Kitosan-Glutaraldehida
Derajat keasaman (pH) adalah salah satu faktor dalam proses adsorpsi yang mampu mempengaruhi terjadinya interaksi ion logam dengan gugus aktif adsorben. Pada umumnya dengan meningkatnya pH maka akan meningkatkan efektifitas adsorpsi logam pada biomassa. Hasil interaksi antara komposit arang kitosan glutaraldehida dengan Fe3+ ditunjukkan pada Tabel 4.
B - 70 Tabel 4. Penentuan pH optimum komposit
arang kayu apu kitosan dan glutaraldehida pH Co (mg/l) Ce (mg/l) Ca (mg/l) % Ca (mg/l) 2 10,361 3,12 7,24 69,87 3 10,361 0,61 9,75 94,10 4 10,361 0,27 10,09 97,38 5 10,361 0,35 10,01 96,61 6 10,361 0,40 9,96 96,13
Ket. :Co = Konsentrasi awal Fe(III) (mg/l) Ce=Konsentrasi pada saatkesetimbangan
(mg/l)
Ca = Konsentrasi ion logam teradsorpsi (mg/l)
= Co - Ce
Gambar 1. Penentuan pH optimum Adsorpsi Fe3+ oleh Komposit Arang Kayu Apu-Kitosan-Glutaraldehida
Pada Tabel 4. menunjukkan bahwa pada saat pH 2, Fe3+ sudah mulai teradsorpsi pada yang berupa arang kayu apu yang terkomposit kitosan dan glutaraldehida sebesar 7,24 mg/l atau sebesar 69,87%. Seiring meningkatnya pH, maka adsorpsi Fe3+ juga semakin bertambah. Adsorpsi mencapai optimum pada pH 4 sebesar 10,09 mg/l yaitu
97,38%. pH optimum yang didapat dalam penelitian ini relatif lebih cepat dicapai bila dibandingkan dengan penelitian Santoso et
al.(2007), dimana adsorpsi Cu2+ menggunakan membran komposit selulosa kitosan yang mencapai pH optimum pada pH 5. Hal ini bisa disebabkan selain bertambahnya gugus fungsi aktif dari arang kayu apu berupa hidroksil dan karboksil, juga karena adanya pengikatan silang menggunakan glutaraldehida. Glutaraldehida memiliki 2 gugus aldehida aktif di kedua ujungnya, pada ujung yang satu gugus aldehida berikatan dengan arang aktif sedangkan ujung satunya berikatan dengan kitosan melalui reaksi pembentukan basa Schiff yang menghasilkan imina, sehingga pada penelitian ini didapatkan pH 4 sebagai pH optimum.
Penentuan WaktuOptimum untuk
Penyerapan Fe3+ oleh Komposit arang-kitosan -glutaraldehida
Waktu kontak optimum yang dicapai dalam penelitian ini relatif lebih cepat bila dibandingkan dengan penelitian Sukardjo et al. (2011) tentang adsorpsi ion logam Cr(VI) menggunakan bead kitosan yang berikatan silang dengan asetaldehida yang mencapai waktu kontak optimum pada menit ke-75. 0 20 40 60 80 100 120 2 3 4 5 6 Io n L o ga m T er ad so rp si (% ) pH
B - 71 Penentuan Kapasitas Adsorpsi Fe3+ oleh Komposit arang-kitosan -glutaraldehida
Kapasitas adsorpsi Fe3+oleh komposit arang-kitosan -glutaraldehida dilakukan pada kondisi pH dan waktu optimum, dimana untuk mengetahui besarnya kapasitas adsorpsi Fe3+ oleh komposit arang-kitosan -glutaraldehida, maka larutan Fe3+ dengan berbagai konsentrasi awal diinteraksikan dengan komposit arang-kitosan -glutaraldehida. Jika konsentrasi logam yang teradsorpsi sudah mencapai maksimum, maka jumlah logam yang teradsorpsi akan relatif konstan. Variasi konsentrasi awal larutan logam yang digunakan adalah 10, 25, 50, 75 dan 100 mg/l. Hasil jumlah Fe(III) yang teradsorpsi dapat dilihat pada Tabel 5.
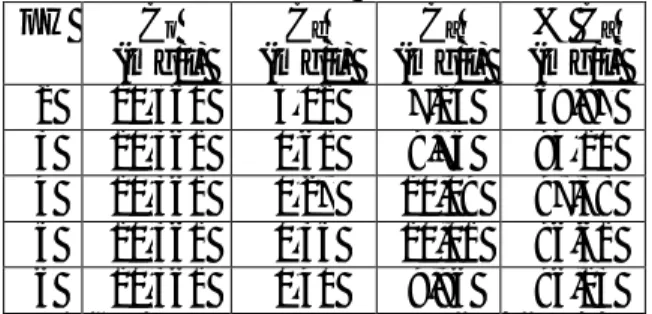
Tabel 5. Konsentrasi Fe3+ yang teradsopsi
komposit arang-kitosan – glutaraldehida Fe3+ Ce (mg/l) Ca (mg/l) % Ca (mg/l) qe (mg/l) Ce/qe 10 1,27 22,08 94,56 0,88 1,44 25 4,55 21,04 82,21 0,84 5,42 50 13,45 28,95 68,29 1,16 11,60 75 36,06 27,65 43,40 1,11 32,49 100 54,15 24,04 31,06 0,98 55,26
Tabel 5 menunjukkan bahwa jumlah Fe3+ yang teradsorpsi meningkat seiring dengan bertambahnya konsentrasi awal larutan Fe3+ yang dikontakkan. Hasil adsorpsi maksimum yang didapatkan pada penelitian ini adalah pada 10 ppm dengan persen logam
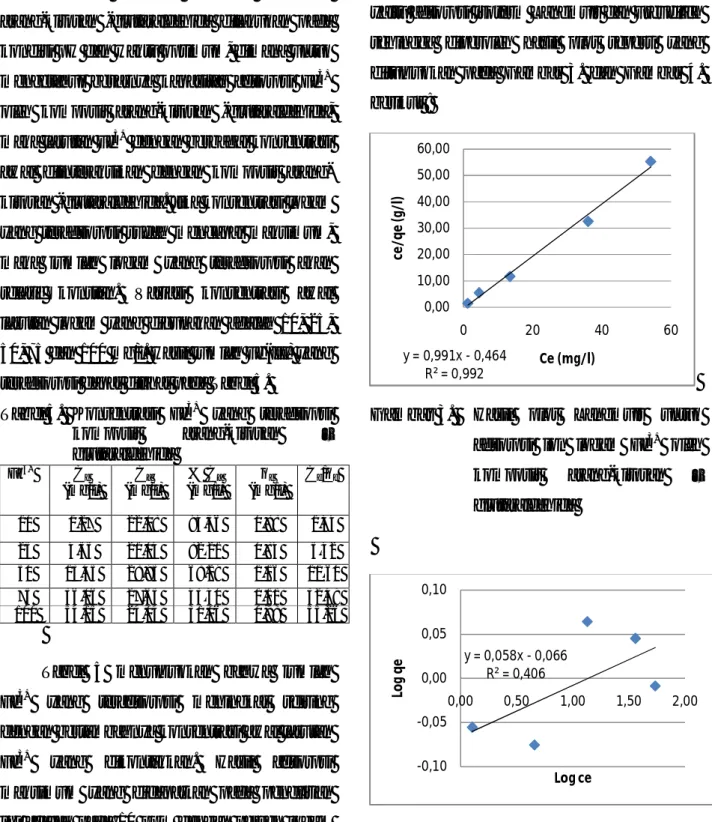
terserap sebesar 94,56%. Kapasitas adsorpsi dapat ditentukan dengan melakukan pendekatan menggunakan dua model adsorpsi, yaitu adsorpsi isoterm Langmuir dan Freudlich sehingga diperoleh hasil plot seperti yang ditunjukkan pada Gambar 3. dan Gambar 4. berikut :
Gambar 3. Hasil plot Langmuir untuk adsorpsi ion logam Fe3+ oleh komposit arang-kitosan – glutaraldehida y = 0,991x - 0,464 R² = 0,992 0,00 10,00 20,00 30,00 40,00 50,00 60,00 0 20 40 60 ce /q e (g /l ) Ce (mg/l) y = 0,058x - 0,066 R² = 0,406 -0,10 -0,05 0,00 0,05 0,10 0,00 0,50 1,00 1,50 2,00 Log q e Log ce
B - 72 Gambar 4. Hasil plot Freundlich untuk
adsorpsi ion logam Fe3+ oleh komposit arang-kitosan -glutaraldehida
Seperti yang terlihat pada Gambar 3. bahwa Fe3+ yang teradsorpsi meningkat seiring dengan bertambahnya konsentrasi awal larutan Fe3+, karena proses adsorpsi terjadi selama permukaan biomassa belum mencapai titik jenuh dan setiap jenis biomassa memiliki kemampuan untuk mengikat ion logam hingga mencapai maksimum. Pola grafik ini ternyata sesuai dengan kurva adsorpsi isoterm Langmuir, dimana nilai koefisien korelasi (R2) untuk isoterm Langmuir lebih mendekati 1 yaitu 0,992 bila dibandingkan model isoterm Freundlich (Gambar 4.) yang memiliki nilai koefisien korelasi 0,406. Ini berarti bahwa adsorpsi terjadi pada permukaan adsorben yang homogen, yaitu adsorben memiliki sejumlah situs aktif yang probabilitas sama untuk berikatan dengan adsorbat. Selama situs aktif belum jenuh oleh adsorbat, maka kenaikan konsentrasi adsorbat akan diikuti pula dengan kenaikan jumlah adsorbat yang diikat.
Penentuan Persen Recovery
Proses recovery berkaitan erat dengan proses pelepasan ion logam yang terikat pada biomassa sehingga dapat digunakan kembali untuk pengikatan ion logam. Proses recovery
dilakukan dengan melarutkan biomassa yang telah terikat logam menggunakan larutan asam encer yaitu HCl 0,1 M. Asam mineral dengan konsentrasi di atas 0,1M tidak cocok digunakan untuk meregenerasi biomassa karena akan merusak biomassa (Susanti et al., 2004). Hasil perolehan kembali (recovery) adsorpsi Fe3+ menggunakan komposit arang-kitosan -glutaraldehida dapat dilihat pada Tabel 6.
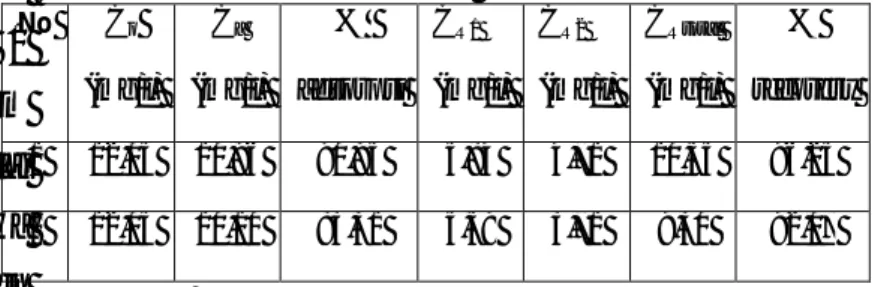
Tabel 6. Data hasil Recavery Fe+ pada
komposit arang-kitosan-glutaraldehida No Co (mg/l) Ca (mg/l) % adsorpsi CR1 (mg/l) CR2 (mg/l) CRtotal (mg/l) % recovery 1 12,05 10,96 90,95 5,84 4,71 10,55 96,25 2 12,05 10,10 83,31 5,59 3,71 9,30 92,07
Data pada Tabel 6. memperlihatkan bahwa pada ulangan pertama, kemampuan adsorben untuk mengadsorpsi Fe3+sebesar 96,25% yang menunjukkan bahwa Fe3+dapat terlepas dengan mudah dari komposit arang-kitosan -glutaraldehida setelah perlakuan dengan HCl 0,1M. Ini dipengaruhi oleh tabrakan antara molekul-molekul oleh tabrakan antara molekul-molekul dalam larutan dengan ikatan kovalen ion logam pada gugus fungsi adsorben sehingga ikatan melemah dan ion logam terlepas kembali ke larutan. . Hasil perolehan kembali ion logam
B - 73
Fe3+ yang teradsorpsi pada adsorben dapat dilihat pada Gambar 5.
Gambar 5. Persen recovery ion logam Fe3+ yang telah teradsorpsi pada kompositarangkitosanglutaraldehid a
Gambar 5. menunjukkan bahwa jumlah Fe3+ yang diperoleh kembali pada ulangan pertama lebih besar dibandingkan dengan jumlah Fe3+ yang didapatkan pada ulangan kedua. Pada recovery-1, Fe3+ yang diperoleh kembali sebesar 96,25%, dan pada
recovery-2 yang dapat diperoleh kembali
sebesar 92,07%. Dalam pengikatan ion Fe3+menggunakan kompositarang kayu apu kitosan dan glutaraldehida ini, gugus yang berperan adalah gugus amino dan karboksilat dari kitosan dengan arang kayu apu sebagai material pendukungnya dan glutaraldehida yang berfungsi sebagai agen pengikat silang antara arang kayu apu dengan kitosan.. Kitosan mempunyai kemampuan untuk mengikat ion-ion logam, sehingga sangat berguna dalam mengikat ion-ion logam seperti
besi (Fe), tembaga (Cu), dan magnesium (Mg). Kitosan membentuk khelat dengan ion logam transisi dengan melepaskan ion hidrogen :
Gambar 6. Reaksi antara kitosan dengan logam transisi(Schmuhl
etal.,2001).
KESIMPULAN
1. pH optimum dan waktu kontak optimum Fe3+ oleh adsorben arang kayu apu termodifikasi kitosan dan glutaraldehida yaitu pada pH = 4 dan t = 45 menit. 2. Kapasitas adsorpsi Fe3+ oleh adsorben
arang kayu apu termodifikasi kitosan dan glutaraldehida sebesar 1,011 mg/g. 3. Persen recovery Fe3+ oleh komposit
arang kayu apu i kitosan dan glutaraldehida didapatkan sebesar 96,25%.
DAFTAR PUSTAKA
Baker, F.S., Miller, C.E., Repik, A.J and E.D Tollens. 1997. Activated carbon. Encyclopedia of separation technology. John Wiley and Sons, New York.
Boddu, V. M. & E. D. Smith. 2003. Removal
of Hexavalent Chromium from
Wastewater Using a New Composite 88 90 92 94 96 98 Recovery 1 Recovery 2 Re co ve ry (% )
B - 74
Chitosan Biosorbent. Environ Science Technology , 37 :4449- 4456.
Mahdian, P. S. 2007. Pengaruh Konsentrasi dan pH Larutan terhadap Adsorpsi Timbal(II) dan Kadmium pada Komposit arang-kitosan -glutaraldehidaiomassa Kayu apu dengan Metode Statis. Sains &
Teknologi, 71 : 3-10.
Mahmudah, R. A & S. E. Cahyaningrum. 2013. Penentuan Konstanta Laju Adsorpsi Ion Logam Cd(II) pada Kitosan Bead dan Kitosan-Silika Bead. UNESA Journal of
Chemistry, 1 : 94- 95.
Puspita, U. R. Asrul S. S.Nuning V. H. 2011. Kemampuan Tumbuhan Air sebagai Agen Fitoremediator Logam Berat Kromium (Cr) yang terdapat pada Limbah Cair Industri Batik.Jurnal Penelitian, 39 : 58-64 .
Sanchez, D; Rha, R & Chokun., 1981. Chitosan Glubes. Journal of Food
Technology, 16: 469- 473.
Santoso, E. Yuwono, H. Ratnawati, Y. The Isoterm Adsorption of Cu2+ Ions in Aquoeus Solutions Cross- Linked
Chitosan- Cellulose Membrane
Composite. The Journal for Technology
and Science , 4 : 106-109.
Schmuhl, HM Krieg & K. Keizer. 2001. Adsorption of Cu(II) and Cr(VI) Ions by Chitosan: Kinetics and Equilibrium Studies. Water SA,27: 1-7.
Sukardjo, J. S. & N. G. Mawarni. 2011. Sintesis Kitosan dari Cangkang Kepiting dan Kitosan yang Dimodifikasi melalui Pembentukan Bead Kitosan Berikatan Silang dengan Asetaldehid sebagai Agen Pengikat Silang untuk Adsorbsi Ion Logam Cr(VI). Jurnal EKOSAINS, 3: 6- 8.
Susanti, E., Y. Utomo, & N. Zakia. 2004. Biosorpsi Ion Logam Berat oleh Ragi Roti. Forum Penelitian Kependidikan (1) :37-50.
Silverstain, R. M., & Bassler, G. C. 1991.
Spectrometric Identification of Organic
Compounds, Second Edition, John Wiley
and Sons, Inc., New York.
Wang T, Turhan M, Gunasekaram S. 2004. Selected Properties of pH-Sensitive, Biodegradable Chitosan-Poly(vinyl alcohol) Hydrogel. Polym Int,53: 911-918. Wan Ngah, W. S., 2002, Removal Copper (II) Ions from Aqueous Solution onto Chitosan and Croos-linked Chitosan Beads, Reactive and Functional Polymers.
Journal of Environmental Sciences , 50 :