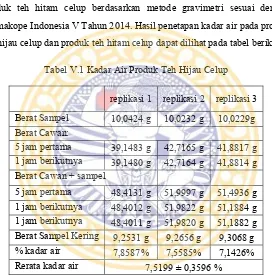
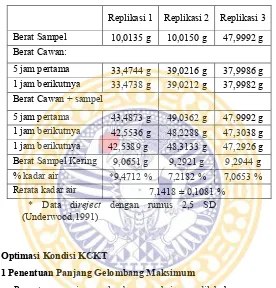
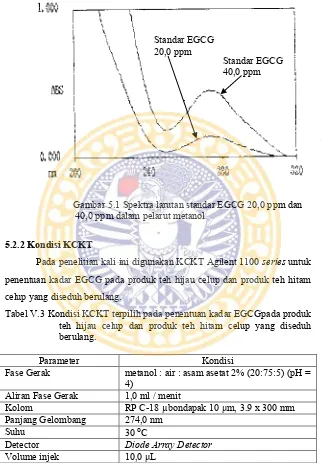
PENENTUAN KADAR (-)-EPIGALOKATEKIN GALAT (EGCG) DALAM PRODUK TEH HIJAU CELUP DAN PRODUK TEH HITAM CELUP PADA PENYEDUHAN BERULANG DENGAN METODE KCKT
Teks penuh
Gambar


Dokumen terkait
Bagi masyarakat Jepun, anime merupakan salah satu saluran yang menonjolkan nilai- nilai dalam budaya mereka~ sarna ada secara sedar ataupun tidak.. Walaupun anime
Pengaruh Bagi Hasil, Promosi, dan Kualitas Pelayanan terhadap Keputusan Penggunaan Jasa Perbankan Syariah Tabungan Mudharabah (Studi Kasus pada Nasabah Bank Muamalat
LKS sangat besar peranannya dalam proses pembelajaran, sehingga seolah-olah penggunaan LKS dapat menggantikan kedudukan seorang guru. Hal ini dapat dibenarkan, apabila LKS
Penelitian ini bertujuan untuk menganalisa pengaruh intensitas pemeriksaan pajak, keadilan, kepatuhan wajib pajak, pengetahuan wajib pajak, sistem perpajakan, diskriminasi,
Apakah penerapan model konseling behavioristik efektif untuk mengatasi perilaku siswa hiperaktif kelas II SD N 2 Golantepus Mejobo Kudus tahun pelajaran 2011/2012,
[r]
Menurut masyarakat dan nelayan yang menjadi responden, kerang ini sangat dominan terdapat di wilayah mangrove Segara Anakan bagian barat dan minimum atau bahkan hampir
Perhitungan harga pokok produksi dengan metode variable costing atau direct costing yang telah dibuat oleh penulis, didapatkan hasil yang berbeda dengan