TUGAS AKHIR – SB091358
POTENSI REGENERASI SEL LEYDIG DAN SEL
SPERMATOGENIK PADA TESTIS MENCIT (
Mus
musculus
) HIPERGLIKEMIK YANG DIINDUKSI
DENGAN EKSTRAK IKAN GABUS (
Channa
st riat a
)
MAHARANI LUKITASARI 1510100013
Dosen Pembimbing
Dra. Nurlit a Abdulgani, M. Si.
Jurusan Biologi
Fakultas Matematika Dan Ilmu Pengetahuan Alam Institut Teknologi Sepuluh Nopember
Surabaya 2014
FINAL PROJECT – SB091358
REGENERATION POTENTIAL OF LEYDIG AND
SPERMATOGENIC CELLS IN HYPERGLYCEMIC
MICE (
Mus musculus
) TESTES INDUCED BY
SNAKEHEAD FISH EXTRACT (
Channa st riat a
)
MAHARANI LUKITASARI 1510100013
Advisor Lect urer
Dra. Nurlit a Abdulgani, M. Si.
Biology Departement
Faculty of Mathematics and Natural Science Sepuluh Nopember Institute of Technology Surabaya 2014
POTENSI REGENERASI SEL LEYDIG DAN SEL
SPERMATOGENIK PADA TESTIS MENCIT (Mus musculus)
HIPERGLIKEMIK YANG DIINDUKSI DENGAN EKSTRAK
IKAN GABUS (Channa striata)
Nama Mahasiswa : Maharani Lukitasari
NRP : 1510 100 013
Jurusan : Biologi
Dosen Pembimbing : Dra. Nurlita Abdulgani, M.Si.
Abstrak
Ekstrak ikan gabus (Channa striata) dapat menurunkan kadar glukosa darah melalui perbaikan struktur histologi pankreas. Penelitian lanjutan dilakukan untuk mengetahui potensi regenerasi sel Leydig dan sel spermatogenik testis mencit
(Mus musculus) hiperglikemik. Mencit jantan galur Balb-C umur
2-3 bulan diinduksi hiperglikemik dengan aloksan monohidrat dosis tunggal 190 mg/kg berat badan secara intraperitoneal. Mencit hiperglikemik diterapi secara oral selama 14 hari menggunakan ekstrak ikan gabus. Preparasi histologi testis menggunakan metode parafin dengan pewarnaan Haematoxylin dan Eosin (H & E) kemudian diamati dengan mikroskop Olympus ® CX21. berdasarkan anova tidak ada pengaruh ekstrak ikan gabus terhadap regenerasi sel leydig, tetapi ada pengaruh pada regenerasi sel spermatogenik. Dengan uji Tukey, diketahui dosis 0.14846 ml/hari dapat meregenerasi sel spermatogenik hingga >90% mencapai kondisi normal.
Kata kunci: Channa striata, hiperglikemik, histologi, testis.
REGENERATION POTENTIAL OF LEYDIG AND SPERMATOGENIC CELLS IN HYPERGLYCEMIC MICE (Mus musculus) TESTES INDUCED BY SNAKEHEAD FISH
(Channa striata) EXTRACT
Student Name : Maharani Lukitasari
NRP : 1510 100 013
Departement : Biologi
Advisor Lecturer : Dra. Nurlita Abdulgani, M.Si.
Abstract.
Snakehead (Channa striata) fish extract can reduce blood
glucose levels trough pancreas histological structure repaired. Further research was conducted to determine the potency of Leydig and spermatogenic cells regeneration in hyperglycemic
mice (Mus musculus) testes. Two to three months Balb-C strain
male mice induced hy perglycemic using alloxan monohydrate single dose of 190 mg / kg body weight intraperitoneally. Hyperglycemic mice treated orally for 14 da ys using snakehead fish extract. Preparation of testicular histology using the paraffin method with Haematoxylin and Eosin staining (H & E) and then observed with an Olympus ® CX21 microscope. Based on ANOVA there is no effect of snakehead fish extract on L eydig cell regeneration, but there is an effect on spermatogenic cell regeneration. Based on Tukey's test, 0.14846 ml /day snakehead fish extract was known to be able to regenerate spermatogenic cells up to > 90% attain normal conditions.
Keywords: Channa striata, histology, hyperglycemic, testes.
KATA PENGANTAR
Alhamdulillah, puji syukur dipanjatkan kepada Allah SWT yang telah melimpahkan rahmat, taufik serta hidayah-Nya sehingga penulis dapat menyelesaikan Tugas Akhir yang berjudul
“Potensi Regenerasi Sel Leydig dan Sel Spermatogenik pada Testis Mencit (Mus Musculus) Hiperglikemik yang Diinduksi dengan Ekstrak Ikan Gabus (Channa Striata)”.
Ucapan terima kasih penulis sampaikan kepada Ibu Dra. Nurlita Abdulgani, M.Si. yang telah membimbing mulai dari masa persiapan hingga tersusunnya Tugas Akhir ini, serta kepada Ibu Ir. Sri Nurhatika, MP. dan Ibu Dr. Enny Zulaika, MP. selaku dosen penguji tugas akhir. Penulis juga mengucapkan terima kasih kepada Ayahanda dan Ibunda, adik-adik serta keluarga atas doa dan kasih sayangnya, juga kepada teman-teman seperjuangan Biologi ITS 2010 atas semangat, bantuan dan kerjasamanya, serta semua pihak yang tidak dapat disebutkan satu per satu yang telah membantu dalam kelancaran penelitian ini.
Penulis menyadari bahwa penulisan Tugas Akhir ini masih jauh dari sempurna. Kritik dan saran yang membangun sangat berarti bagi penulis. Penulis berharap Tugas Akhir ini dapat bermanfaat bagi semua pembaca. Akhir kata, semoga Allah SWT senantiasa memberikan rahmat dan hidayahNya kepada kita semua. Amin.
Surabaya, 12 Juli 2014
Maharani Lukitasari
ABSTRAK ... 1.2 Rumusan Permasalahan ... 1.3 Batasan Masalah ...
2.3 Kandungan Nutrisi Ekstrak Ikan Gabus ... 2.4 Hiperglikemia ... 2.5 Testis ... 2.6 Tubulus Seminiferus ... 2.6.1 Anatomi dan Histologi Tubulus Seminiferus ... 2.6.2 Kerusakan Tubulus Seminiferus ... 2.7 Spermatogenesis ... 2.8 Aloksan ... 2.9 Pengaruh Diabetes Mellitus Terhadap Reproduksi ....
BAB III METODOLOGI
3.1 Waktu dan Tempat Penelitian ... 3.2 Metode yang Digunakan ...
3.2.1 Pemeliharaan mencit (Mus musculus) ...
3.2.3 Terapi mencit hiperglikemik ... 3.2.4 Pengukuran kadar glukosa darah ... 3.2.5 Pembuatan preparat histologi testis mencit ... 3.2.6 Pengamatan mikroskopis ... 3.3 Rancangan Penelitian dan Analisa Data ...
BAB IV HASIL DAN PEMBAHASAN
4.1 Potensi Regenerasi Sel Leydig Testis Mencit
Hiperglikemik Setelah Diinduksi dengan Aloksan ... 4.2 Potensi Regenerasi Sel Spermatogenik Testis
Mencit Hiperglikemik Setelah Diinduksi dengan
DAFTAR GAMBAR
Histologi Tubulus Seminiferus ...
Proses Spermatogenesis dan
Morfologi Spermatozoa ...
Struktur Kimia Aloksan ...
Sel Leydig pada Ruang Intrastitial (tanda panah) dengan Perbesaran
400x ...
Histologi Tubulus Seminiferus
Mencit Perbesaran 1000x ...
DAFTAR TABEL
Halaman
Tabel 2.1
Tabel 2.2
Tabel 4.1
Tabel 4.2
Kandungan Protein Ikan ...
Kandungan Nutrisi Ekstrak Ikan
Gabus dalam 100 milimeter ...
Jumlah Sel Leydig/Bidang Pandang ...
Jumlah Sel Spermatogenik/Bidang
Pandang ...
8
9
28
30
18
33
Lampiran 1
Dokumentasi Hasil Pengamatan Sel Spermatogenik pada Tubulus Seminiferus Kelompok Kontrol
Negatif ...
Dokumentasi Hasil Pengamatan Sel Spermatogenik pada Tubulus Seminiferus Kelompok Kontrol
Positif ...
Dokumentasi Hasil Pengamatan Sel Spermatogenik pada Tubulus Seminiferus Kelompok Terapi
Ekstrak Ikan Gabus Dosis Bawah ...
Dokumentasi Hasil Pengamatan Sel Spermatogenik pada Tubulus Seminiferus Kelompok Terapi
Ekstrak Ikan Gabus Dosis Tengah ...
Dokumentasi Hasil Pengamatan Sel Spermatogenik pada Tubulus Seminiferus Kelompok Terapi
Ekstrak Ikan Gabus Dosis Atas ...
Dokumentasi Hasil Pengamatan Sel Leydig Kelompok Kontrol
Negatif ...
Dokumentasi Hasil Pengamatan Sel Leydig Kelompok Kontrol
Lampiran 2
Dokumentasi Hasil Pengamatan Sel Leydig Kelompok Terapi
Ekstrak Ikan Gabus Dosis Tengah ...
Dokumentasi Hasil Pengamatan Sel Leydig Kelompok Terapi
Ekstrak Ikan Gabus Dosis Atas ...
Data Hasil Pengukuran Kadar
Glukosa Darah Mencit ...
Data hasil Data Hasil Uji
ANOVA Sel Spermatogonium ...
Data hasil Data Hasil Uji
ANOVA Sel Spermatosit...
Data hasil Data Hasil Uji
ANOVA Sel Spermatid ...
Data hasil Data Hasil Uji
ANOVA Sel Leydig ...
Hasil Pengamatan Jumlah Sel
Spermatogenik dan Sel Leydig ...
1.1 Latar Belakang
Diabetes mellitus merupakan kelainan metabolik kronis yang terjadi akibat pankreas tidak dapat memproduksi cukup insulin bagi tubuh atau insulin tubuh tidak dapat digunakan secara efektif ditandai dengan kondisi hiperglikemia yaitu peningkatan kadar gula darah diatas kadar normal. Berdasarkan data World Health Organization, pada tahun 2012 penderita diabetes mellitus (DM) di dunia sudah mencapai 347 juta jiwa. Angka ini diperkirakan akan terus meningkat. Indonesia merupakan negara keempat dengan jumlah penderita DM terbanyak setelah Amerika Serikat, China dan India. Pada tahun 2030 diperkirakan prevalensi DM di Indonesia mencapai 21,3 juta orang. Diabetes mellitus merupakan penyakit yang bersifat kronik dan akan menetap seumur hidup, selain itu juga memberikan pengaruh sistemik yang menyebabkan terjadinya gangguan fungsional tubuh secara umum. Salah satu dampak yang ditimbulkan dari penyakit ini yaitu gangguan fungsi repoduksi pria kaitannya dengan penurunan kualitas sperma yang menjadi salah satu penyebab terjadinya infertilitas pada pria. Di Indonesia, prevalensi infertilitas adalah 12% atau sekitar 3 juta pasangan suami-istri (Suyono, 2005).
Sexton (1997) menyatakan bahwa diabetes mellitus menyebabkan gangguan pada hormon yang mempengaruhi spermatogenesis. Selain itu, terdapat kelainan di dalam proses spermatogenesis itu sendiri yang diikuti dengan adanya gangguan ejakulasi. Pada penderita diabetes didapati penurunan kadar
testosteron secara signifikan disertai penurunan kadar Luteinizing
Hormone (LH) dan Folicle Stimulating Hormon (FSH) (Remzi et
al., 2004). Dampak utama diabetes mellitus terhadap infertilitas
pria adalah akibat adanya peningkatan radikal bebas yang menyebabkan terjadinya stres oksidatif pada sel spermatogenik, sel Leydig dan sel sertoli yang memiliki peran penting dalam prose spermatogenesis. Radikal bebas akan memicu terjadinya
gangguan dan kerusakan pada sel-sel tersebut. kerusakan yang terjadi antara lain apoptosis dan atrofi (Christina, 2005; Warren
et al., 1996 dalam Hassan et al., 2001), serta terjadi penurunan
jumlah sel spermatogenik, volume semen, jumlah, motilitas dan
morfologi sel spermatozoa (Garcia-Diez et al., 1991).
Penurunan kadar testosteron dan peningkatan radikal bebas pada penderita diabetes mellitus dapat mempengaruhi fungsi seksual pria secara umum. Kondisi ini tentunya merupakan masalah besar bagi pria karena berhubungan dengan kesejahteraan hidupnya. Oleh karena itu, diperlukan penanganan dalam berbagai bentuk terapi yang dikembangkan baik untuk mengatasi penyakit diabetesnya maupun dampak dari diabetes itu
sendiri. Menurut Meldawati (2011), peningkatan kadar Reactive
Oxygen Species (ROS) yang ditimbulkan oleh kondisi
hiperglikemik berpotensi menimbulkan stress oksidatif yang tidak dapat diatasi oleh antioksidan endogen.
Stress oksidatif dapat diantisipasi dengan antioksidan eksogen yang dapat memperbaiki kapasitas antioksidan plasma (Endrinaldi, 2007). Salah satu sumber antioksidan eksogen alami di Indonesia adalah albumin yang terdapat pada ikan gabus (Channa striata). Aktivitas antioksidan albumin ikan gabus ini
sebesar 0,14 ± 0.003 mmol/L, atau sebanding dengan 90,93% aktivitas antioksidan vitamin E. Menurut Fadli (2010) dan Sunatrio (2003) ekstrak ikan gabus mengandung 70% protein (3.36 g/100ml), 21% albumin (2.17g/100ml), asam amino lengkap, mineral-mineral penting antara lain Zn (3.43 mg/100ml), Cu (2,34 mg/100ml), dan Fe (0.81 mg/100ml).
Ikan gabus dapat diekstrak untuk memperoleh protein plasma yang mengandung albumin dan nutrien lainnya. Masyarakat telah mengenal berbagai produk berbahan baku ikan gabus, diantaranya olahan dalam bentuk tablet, krim, dan ekstrak cair. Produk olahan ikan gabus tersebut berpotensi untuk meningkatkan kadar albumin pada penderita hypoalbuminemia
dan pasien pasca operasi bedah, menurunkan kadar kolesterol
darah, menurunkan kadar trigliserida darah, menurunkan risiko kematian karena penyakit jantung, mengurangi gejala rematik, serta menurunkan aktivitas pertumbuhan sel kanker (Suprayitno
dkk, 2009; Santoso, 2009). Penelitian Abdulgani et al (2014) juga
telah membuktikan bahwa albumin dari ekstrak ikan gabus mampu memperbaiki struktur sel beta pankreas pada pulau langerhans sehingga dapat menurunkan kandungan glukosa darah pada mencit hiperglikemik. Ditinjau dari berbagai kelebihannya, diduga apabila ekstrak ikan gabus ini dikonsumsi pria dengan gangguan reproduksi maka akan berpotensi untuk meregenerasi sel Leydig dan sel spermatogenik testis. Untuk menguji
kemampuan ekstrak gabus digunakan hewan coba mencit (Mus
musculus) yang dikondisikan hiperglikemik melalui induksi
aloksan. Hasil penelitian ini diharapkan dapat memperluas
pemanfaatan ikan gabus di bidang kesehatan, khususnya dalam
penyembuhan infertilitas pada pria yang disebabkan oleh komplikasi diabetes mellitus.
1.2 Rumusan Permasalahan
Rumusan permasalahan dalam penelitian ini adalah :
1.
Apakah regenerasi sel Leydig pada testis mencithiperglikemik dapat terjadi setelah diinduksi ekstrak ikan gabus?
2.
Apakah regenerasi sel spermatogenik dalam tubulus1.3 Batasan Masalah
Batasan masalah dalam penelitian ini adalah :
1.
Hewan coba dalam penelitian ini adalah mencit (Musmusculus) jantan galur Balb/C, umur 2-3 bulan.
2.
Induksi hiperglikemik menggunakan aloksan monohidratdengan dosis 190 mg/kg berat badan.
1.4 Tujuan
Tujuan penelitian ini adalah:
1. Untuk mengetahui potensi regenerasi sel Leydig pada testis
mencit hiperglikemik setelah diinduksi ekstrak ikan gabus?
2. Untuk mengetahui potensi regenerasi sel spermatogenik
dalam tubulus seminiferus testis mencit hiperglikemik setelah diinduksi ekstrak ikan gabus?
1.5 Manfaat
Hasil penelitian ini diharapkan dapat memperluas
pemanfaatan ikan gabus di bidang kesehatan, khususnya dalam
2.1 Mencit (Mus musculus) Sebagai Hewan Coba
Mencit merupakan hewan yang paling umum digunakan pada penelitian laboratorium sebagai hewan percobaan karena memliki banyak keunggulan, yaitu siklus hidup yang relatif pendek, jumlah anak per kelahiran banyak, variasi sifat-sifatnya tinggi dan mudah dalam penanganannya (Moriwaki, 1994).
Mencit merupakan omnivora alami, sehat, dan kuat, profilik, kecil, dan jinak. Selain itu, hewan ini juga mudah didapat dengan harga yang relatif murah dan biaya ransum yang rendah (Peter, 1976). Menurut Arrington (1972), mencit memiliki taksonomi sebagai berikut:
Kingdom : Animalia
Phylum : Chordata
Classis : Mamalia
Ordo : Rotentia
Familia : Muridae
Genus : Mus
Species : Mus musculus
Para ilmuwan telah memunculkan banyak strain atau galur tikus khusus untuk eksperimen antara lain tikus Wistar albino, Sprague Dawley, Fischer 344, Holtzman albino strain, Long-Evans, dan Balb/C (Gambar 2.1)
Gambar 2.1 Mencit Galur Balb/C (sumber: Dokumentasi Pribadi, 2014)
Balb/C adalah mencit albino yang memiliki bulu pendek halus berwarna putih serta ekor berwarna kemerahan dengan ukuran lebih panjang dari pada badan dan kepala. Mencit galur Balb/C mudah dikembangbiakkan dan mudah dalam penanganan. Mencit galur Balb/C sering digunakan dalam berbagai penelitian khususnya mengenai sel kanker dan tumor.
2.2 Ikan Gabus (Channa striata)
Ikan Gabus (Channa striata) merupakan jenis ikan perairan
umum yang bernilai ekonomis. Ikan gabus merupakan ikan asli perairan daerah tropis seperti Asia dan Afrika. Ikan gabus banyak ditemukan di perairan umum dan belum dibudidayakan secara luas (Santoso, 2009).
Ikan gabus hidup di muara-muara sungai, danau dan dapat pula hidup di air kotor dengan kadar oksigen rendah, bahkan tahan terhadap kekeringan dan dapat ditemukan di berbagai perairan umum di wilayah Indonesia, diantaranya Jawa, Sumatra, Sulawesi, Bali, Lombok, Singkep, Flores, Ambon dan Maluku dengan nama yang berbeda. Di Palembang ikan gabus dikenal dengan sebutan ikan deleg, di Jawa dikenal dengan sebutan ikan kutuk, dan di Kalimantan dikenal dengan ikan ruan atau haruan dan di Sulawesi dikenal dengan ikan dalak. Ikan gabus memijah sepanjang tahun dengan jumlah fekunditas untuk ikan dengan ukuran panjang total 18,5 – 50,5 cm dan bobot 60 – 1.020 gr berjumlah 2.585 – 12.880 butir (Santoso, 2009).
Ikan gabus merupakan ikan buas (karnivora yang bersifat pemakan segala yang predator). Di alam, ikan gabus tidak hanya memangsa benih ikan tetapi juga ikan dewasa dan serangga air lainnya termasuk kodok. Ikan ini memiliki bentuk tubuh hampir
bulat, kepala besar dan agak gepeng mirip kepala ular (snake
head), panjang dan makin ke belakang makin pipih (compressed).
Bagian punggung cembung, perut rata dan kepala pipih seperti
ular (snake head). Warna tubuh pada bagian punggung hijau
gabus tidak memiliki jari-jari keras, mempunyai sirip punggung dan sirip anal yang panjang dan lebar, sirip ekor berbentuk setengah lingkaran, sirip dada lebar dengan ujung membulat. Ikan gabus dapat mencapai panjang 90 – 110 cm. Morfologi ikan gabus disajikan pada Gambar 2.1.
Gambar 2.2 Channa striata (Fishbase, 2014).
Klasifikasi ikan gabus menurut Rahayu (1992) adalah sebagai berikut:
Kingdom : Animalia
Phylum : Chordata
Classis : Actinopterygii
Ordo : Perciformis
Familia : Channidae
Genus : Channa
Species : Channa striata
Ikan gabus hidup di air tawar dan melakukan pemijahan secara alami selama musim hujan (Bijaksana, 2012), memiliki laju pertumbuhan yang cepat, mampu melakukan respirasi pada kondisi air yang sedikit oksigen (Sampath, 1985) dan bertahan pada lingkungan dengan kadar amonia yang tinggi (Ng, 1990).
1. Membentuk jaringan baru dalam masa perkembangan dan pertumbuhan tubuh.
2. Memelihara, memperbaiki, dan mengganti jaringan yang
rusak atau mati.
3. Cadangan energi bila tubuh kekurangan lemak dan
karbohidrat.
4. Sebagai alat transport untuk lipida, oksigen, asam lemak, dan
ion tembaga dalam tubuh
5. Membentuk biokatalisator (enzim), zat pengatur (hormon),
dan antibodi.
6. Membentuk struktur membran plasma bersama-sama lipida
dan karbohidrat
2.3 Kandungan Nutrisi Ekstrak Ikan Gabus
Ikan gabus memiliki kandungan protein yang lebih tinggi dibandingkan jenis ikan lainnya seperti yang tercantum pada Tabel 2.1
Tabel 2.1 Kandungan Protein Ikan.
Jenis Ikan Protein (g%)
Tabel 2.2 Kandungan Nutrisi Ekstrak Ikan Gabus dalam 100
Protein plasma dengan kandungan terbanyak dalam ekstrak ikan gabus adalah albumin. Albumin merupakan sumber antioksidan hewani yang berfungsi sebagai pengikat radikal sehingga berperan dalam proses pembersihan dan penangkapan
Reactive Oxygen Species (ROS) (Sunatrio, 2003). Ekstrak ikan
gabus memiliki aktivitas antioksidan 0,14 ± 0.003 mmol/L, atau sebanding dengan 90,93% aktivitas antioksidan vitamin E. Hal ini menunjukkan ekstrak ikan gabus dapat difungsikan sebagai antioksidan. Albumin melimpah akan gugus (-SH) yang berfungsi sebagai pengikat radikal sehingga berperan dalam proses
pembersihan dan penangkapan ROS (Santoso, 2009). Selain itu
albumin juga bersinergi dengan mineral Zn yang sangat dibutuhkan untuk perkembangan sel maupun pembentukan jaringan sel baru seperti akibat luka dan penyembuhan luka akibat
operasi. Zn membantu sekresi dan metabolisme insulin, serta
melindungi efek kerusakan pankreas. Zn juga berfungsi sebagai antioksidan yang melindungi sel-sel, mempercepat proses penyembuhan luka, mengatur ekspresi dalam limfosit dan protein, memperbaiki nafsu makan dan stabilisasi berat badan (Gibson, 2005). Sedangkan kalsium diyakini dapat meningkatkan sensitivitas, respon dan sekresi insulin (Wilcox, 2005).
sedemikian rupa, dibuat serbuk, kemudian dimasukkan dalam kapsul. Bau amis ikan yang tak disukai itu pun hilang, tak terasa lagi. Hampir semua pasien berkadar albumin rendah yang diberi suplemen dari ikan gabus ini, kadar albuminnya naik lebih cepat ketimbang pemberian albumin lewat infus. Bahkan, pasien berkadar albumin rendah yang diikuti komplikasi penyakit lain seperti tuberculosis, diabetes, patah tulang, stroke, hingga HIV/AIDS, kondisinya bisa lebih baik dengan pemberian ekstrak ikan gabus. Begitu juga pada anak dengan gizi buruk dan berat badan kurang, pemberian biskuit dari ekstrak ikan gabus membuat berat badan balita dapat naik minimal 1 k ilogram per bulan. (Astuti, 2008).
Ikan tersebut memiliki protein yang sangat tinggi, ikan ini dapat dijadikan alternatif sumber albumin bagi penderita hipoalbumin (rendah albumin) dan luka, baik luka pasca operasi maupun luka bakar. Bahkan, di daerah pedesaan, anak laki-laki pasca khitan selalu dianjurkan mengkonsumsi ikan jenis ini agar penyembuhan lebih cepat. Daging ikan tersebut dikukus atau disteam sehingga memperoleh filtrat, yang dijadikan menu ekstra bagi penderita hipoalbumin dan luka. Dalam tubuh manusia, album disintesis oleh hati kira-kira 100-200 mikrogram/g jaringan hati setiap hari. Albumin didistribusikan secara vaskuler dalam plasma dan secara ekstravaskuler dalam kulit, otot, serta beberapa jaringan lain (Yanti, 2009).
2.4 Hiperglikemia
Hiperglikemia merupakan keadaan peningkatan glukosa darah dari rentang kadar puasa normal 80 – 90 mg / dl darah, atau rentang non puasa sekitar 140 – 160 mg /100 ml darah (Corwin, 2001).
Hiperglikemia dapat menyebabkan komplikasi kronik termasuk penyakit kardiovaskular (iskemik miokard, kardiomiopati), gangren, kegagalan kronis ginjal, retinopati serta neuropati. Komplikasi yang lebih serius umum terjadi bila kontrol kadar gula darah buruk. Sehingga pasien dengan diabetes melitus harus benar-benar dapat mengatur diet makanan khususnya dalam konsumsi karbohidrat.
Kondisi hiperglikemia yang menandai terjadinya penyakit diabetes mellitus juga dapat menyebabkan kerusakan sel melalui berbagai cara, salah satunya berawal dari komplikasi mikrovaskular. Adanya komplikasi mikrovaskular akan memicu terjadinya komplikasi fisiologis, biokimia, dan anatomi, antara
lain penebalan m embran (Raskin et al., 1983), penyakit
makrovaskular (Eschwege et al., 1985), glikosilasi protein
(Brownlee et al., 1988), gangguan immunitas seluler (Rayfield et
al., 1982), dan berbagai abnormalitas siklus sel (Lorenzi et al.,
1987). Selain itu, hiperglikemia juga menyebabkan gangguan
sekresi dan aksi insulin (DeFronzo et al., 1988) sehingga akan
timbul kondisi hiperglikemik yang lebih kronis.
Dengan menurunnya insulin dalam darah asupan nutrisi akan meningkat sebagai akibat kelaparan sel. Menurunnya glukosa intrasel menyebabkan sel mudah terinfeksi. Gula darah yang tinggi dapat menyebabkan penimbunan glukosa pada dinding pembuluh darah yang membentuk plak sehingga pembuluh darah menjadi keras (arterisklerosis) dan bila plak itu telepas akan menyebabkan terjadinya thrombus. Thrombus ini dapat menutup aliran darah yang dapat menyebabkan timbulnya penyakit lain (tergantung letak tersumbatnya, missal cerebral dapat menyebabkan stroke, ginjal dapat menyebabkan gagal ginjal, jantung dapat menyebabkan miocard infark, mata dapat menyebabkan retinopati) bahkan kematian.
Hiperglikemi dan defisiensi insulin mampu mempengaruhi struktur maupun fungsi jaringan, termasuk struktur protein sel.
Hiperglikemi akan meningkatkan Reactive Oxygen Spesies
(ROS). (Hayati et al., 2005).
2.5 Testis
Testis merupakan salah satu organ yang penting dalam reproduksi jantan. Testis berfungsi untuk memproduksi sperma dan hormon reproduksi yaitu testosterone (Falk, 2001). Ketika
masa pubertas tiba, tubulus seminiferus akan bekerja dengan
optimal menghasilkan sperma dan hormon-hormon reproduksi seperti testosteron dan androgen. Pada saat itu, secara tidak langsung dibutuhkan kapasitas yang besar dari tubulus
seminiferus yang akan meningkatkan bobot dan volume testis
untuk mendukung proses tersebut. Perkembangan dan peningkatan produksi sperma merupakan suatu hal yang berjalan seiring dengan perkembangan bobot testis (Amann, 1970).
Testis sebagai organ kelamin primer mempunyai dua fungsi yaitu menghasilkan spermatozoa atau sel-sel kelamin jantan, dan mengsekresikan hormone kelamin jantan, testosteron.
Spermatozoa dihasilkan didalam tubulus seminiferus atas
pengaruh FSH (Follicle Stimulating Hormone) sedangkan
testosteron diproduksi oleh sel-sel interstitial dari Leydig atas
pengaruh ICSH (Interstitial Cell Stimulating Hormone)
(Toelihere, 1985).
FSH merupakan glikoprotein yang salah satu fungsinya adalah bersama-sama dengan androgen dalam proses spermatogenesis, sedangkan ICSH merupakan glikoprotein yang memiliki fungsi untuk proses ovulasi dan merangsang sel Leydig untuk mensekresi androgen (Hafez, 1970).
2.6 Tubulus Seminiferus
2.6.1 Anatomi dan Histologi Tubulus Seminiferus
Tubulus seminiferus adalah bagian dari organ reproduksi pria yang terletak di dalam testis yang berperan penting dalam proses spermatogenesis. Tubulus seminiferus berbentuk tabung dengan panjang sekitar 30 – 70 cm dan diameter 150 – 250 μm. Di dalam testis, tubulus seminiferus dimampatkan dan terletak di dalam lobulus testis (Gupta, 2005).
dibedakan menjadi tubulus seminiferus kontortus dan tubulus seminiferus rektus. Tubulus seminiferus kontortus dari masing-masing lobulus testis bergabung membentuk tubulus seminiferus rektus, yang merupakan saluran lurus yang langsung menghubungkan tubulus seminiferus dengan rete testis dibagian posterior testis. Dari rete testis ini selanjutnya spermatozoa akan dialirkan melalui duktus eferentes kemudian memasuki epidydimis dan siap untuk dikeluarkan (Gupta, 2005; Sherwood, 2001).
Gambar 2.3 Histologi Tubulus Seminiferus (Mescher, 2010)
2.6.2 Kerusakan Tubulus Seminiferus
Seperti halnya sel-sel di bagian tubuh yang lainnya, sel-sel penyusun tubulus seminiferus juga dapat mengalami cedera oleh berbagai hal yang mengakibatkan kerusakan struktur maupun fungsi sel tersebut. Oleh karena fungsi utama tubulus seminiferus adalah untuk spermatogenesis maka faktor-faktor yang merusak struktur tubulus seminiferus akan menimbulkan gangguan pada proses spermatogenesis. Secara umum kerusakan tubulus seminiferus dapat digambarkan ke dalam empat kategori (Burkitt, 1993) :
1. Atrofi tubuler yaitu keadaan dimana terjadi kehilangan sel-sel spermatogenik di dalam tubulus seminiferus, menurunnya diameter tubulus seminiferus dan tampak penebalan pada membran basalis
2. Nekrosis tubuler yaitu kerusakan seluruh unsur sel di dalam tubulus seminiferus, terlihat adanya sisa-sisa bahan nekrotik, tampak membrane basalis mengalami kerusakan akibat terjadinya lisis, dan terlihat adanya sel radang.
2.7 Spermatogenesis
Spermatogenesis adalah suatu rangkaian perkembangan sel spermatogonia dari epitel tubulus seminiferus yang mengadakan proliferasi dan selanjutnya berubah menjadi spermatozoa yang bebas. Rangkaian perkembangan ini dapat dibagi menjadi tiga tahap (Gambar 2.4). Tahap pertama, sel spermatogonia mengadakan pembelahan mitosis menghasilkan spermatosit dan sel induk spermatogonia. Tahap kedua, pembelahan meiosis (reduksi) spermatosit primer dan sekunder menghasilkan spermatid yang haploid. Tahap ketiga, perkembangan spermatid menjadi spermatozoa melalui serangkaian metamorfosa yang panjang dan kompleks disebut spermiogenesis (Syahrum, 1994).
Proses spermatogenesis dipengaruhi oleh hormonal. Pada
spermatogenesis, folicle stimulating hormone (FSH) memiliki
peranan penting, yaitu berperan dalam menstimulasi kejadian awal spermatogenesis diantaranya proliferasi spermatogonia (Satriyasa, 2008) dan menunjang tahap pematangan maupun reduksi meiosis spermatosit primer (Turek, 2005). Setelah mengalami proses spermiogenesis (deferensiasi dan maturasi) lebih lanjut spermatid akan menjadi spermatozoa. Jadi dari satu sel spermatogenium yang 2 n pada akhir spermatogenesis akan menghasilkan 4 buah spermazoa yang 1 n.
2.8 Aloksan
Aloksan (2,4,5,6-tetraoksipirimidin; 5,6-dioksiurasil)
merupakan senyawa kimia yang dapat digunakan untuk menginduksi penyakit diabetes melitus. Pada tahun 1943, telah dilakukan penelitian bahwa pemberian aloksan pada kelinci menghasilkan hiperglikemia temporer, yang diikuti hipoglikemia hebat, dan diakhiri dengan kematian hewan. Peristiwa ini berhubungan dengan nekrosis selektif sel-sel β pulau Langerhans (Szkuldelski 2001).
Aloksan sebagai diabetogenik, dapat digunakan secara
intravena, intraperitoneal dan subkutan (Nugroho et al., 2006).
Dosis intravena yang digunakan biasanya 65 mg/kg BB, sedangkan intraperitoneal dan subkutan adalah 2-3 kalinya
(Szkudelski, 2001, R ees et al., 2005). Dosis pemberian aloksan
bervariasi tergantung pada spesies, nutrisi, dan rute pemberiannya (Szkudelski, 2001). Kemampuan aloksan untuk dapat menimbulkan diabetes juga tergantung pada jalur penginduksian, dosis, hewan coba, dan status nutrisinya (Andayani, 2003). Injeksi aloksan dengan dosis 190 mg/kg berat badan pada tikus akan memperlihatkan kenaikan kadar glukosa darah sampai lebih dari 200 m g/dl dalam jangka waktu minimal 48 j am setelah injeksi (Colca et al., 1983).
pada suhu yang lebih rendah. Molekul aloksan memiliki bentuk
yang sangat mirip dengan glukosa (Weaver et al., 1979; Gorus et
al., 1982), seperti yang ditunjukkan oleh Gambar 2.5.
Gambar 2.5 Struktur kimia aloksan (Nugroho 2006).
Karena karakter hidrofiliknya, aloksan dan glukosa tidak dapat menembus lipid bilayer membran plasma. Namun bentuk molekul aloksan yang sangat mirip dengan glukosa menyebabkan transporter glukosa GLUT2 dalam membrane plasma sel β menerima molekul ini sebagai analog glukosa (glukomimetik)
dan mengantarkannya ke dalam sitosol (Weaver et al., 1979;
Gorus et al., 1982).
Mekanisme toksisitas aloksan diawali dengan masuknya aloksan ke dalam sel β pankreas. Kerusakan pada sel β terjadi melalui beberapa proses secara bersamaan, yaitu melalui oksidasi gugus sulfidril dan pembentukan radikal bebas. Aloksan menginduksi pembentukan radikal bebas karena bersifat polar sehingga dapat memberikan satu elektronnya kepada oksigen. Melalui reaksi redoks, asam dialurat dibentuk sebagai hasil reduksi aloksan dengan menghasilkan metabolit intermediet radikal aloksan. Asam dialurat kemudian dioksidasi kembali membentuk aloksan sehingga menghasilkan radikal ion superoksida. Anion superoksida dapat mengalami reaksi
dismutase oleh enzim SOD (Superoxide Dismutase) menjadi
selektif pada sel β pankreas sehingga menghasilkan kondisi hiperglikemia permanen yang merupakan salah satu etiologi dari diabetes mellitus tipe I (Insulin Dependent Diabetes Mellitus) (Szkudelski, 200).
Faktor lain selain pembentukan oksigen reaktif adalah gangguan pada homeostatis kalsium intraseluler. Aloksan dapat meningkatkan konsentrasi ion kalsium bebas sitosolik pada sel β Langerhans pankreas. Efek tersebut diikuti oleh beberapa kejadian : influks kalsium dari cairan ekstraseluler, mobilisasi kalsium dari simpanannya secara berlebihan, dan eliminasinya yang terbatas dari sitoplasma. Influks kalsium akibat aloksan tersebut mengkaibatkan depolarisasi sel β Langerhans, lebih lanjut membuka kanal kalsium tergantung voltase dan semakin menambah masuknya ion kalsium ke sel. Pada kondisi tersebut, konsentrasi insulin meningkat sangat cepat, dan secara signifikan mengakibatkan gangguan pada sensitivitas insulin perifer dalam waktu singkat. Selain kedua faktor tersebut di atas, aloksan juga diduga berperan dalam penghambatan glukokinase dalam proses
metabolisme energi (Szkudelski, 2001; Walde et al., 2002).
2.9 Pengaruh Hiperglikemia Terhadap Reproduksi
Menurut Garris et al. (1984) kondisi h iperglikemik pada
hamster china (Cricetus griseus) dapat menyebabkan kerusakan
struktur endometrium sehingga mengakibatkan meluasnya sel epitel pada lumen dan d egenerasi membran stroma, terjadinya atropi sel-sel uterus dan akumulasi lipid. Berdasarkan penelitian Garris & Garris (2003), pada tikus hiperglikemik terjadi atropi folikel akibat adanya akumulasi lipid. Hal ini ditandai dengan adanya degenerasi jaringan sehingga terjadi depresi fungsi ovarium.
sehingga kadar estrogen dalam tubuh menjadi rendah (Cox et al.,
1994).
Gangguan hormonal akibat kondisi hiperglikemik ini tidak hanya terjadi pada sistem reproduksi betina, namun juga pada sistem reproduksi pria. Diabetes mengakibatkan sejumlah komplikasi dasar yaitu angiopati pada sistem pembuluh darah dan neuropati pada sistem saraf ataupun campuran dari keduanya yang bermanifestasi di berbagai organ dan tempat di seluruh tubuh. Komplikasi dasar tersebut salah satunya dapat mengakibatkan gangguan seksualitas pada pria. Masalah seksual yang sering timbul pada penderita DM pada garis besarnya adalah keluhan seksual dan disfungsi seksual. Keluhan seksual yang sering dijumpai antara lain alat kelamin terasa lembek dan bertambah kecil. Sedangkan disfungsi seksual antara lain impotensi, ejakulasi dini, dan hilanggnya libido. Sexton (1997) menyatakan bahwa DM menyebabkan gangguan pada hormon yang mempengaruhi spermatogenesis. Kelainan di dalam proses spermatogenesis itu sendiri yang diikuti dengan adanya gangguan ejakulasi. Pada penderita diabetes didapati penurunan kadar
testosteron secara signifikan disertai penurunan kadar Luteinizing
Hormon (LH) dan Folicle Stimulating Hormone (FSH) (Remzi et al., 2004).
Dampak utama diabetes melitus terhadap infertilitas pria adalah akibat adanya peningkatan radikal bebas yang menyebabkan terjadinya stres oksidatif terhadap spermatozoa. Kondisi ini akan memicu terjadinya kerusakan pada mitokondria DNA. Selain itu kondisi hiperglikemik juga dapat menyebabkan terjadinya apoptosis dan atrofi pada sel spermatogenik maupun
tubulus seminiferus testis (Warren et al., 1996 dalam Hassan et
al., 2001), serta
menyebabkan penurunan
volume semen,jumlah, motilitas dan morfologi sperma (Garcia-Diez et al.,
1991).
kadar yang rendah ditemukan pada penderita diabetes, dan diketahui kondisi hiperglikemik menurunkan respon kelenjar
pituitary ketika terstimulasi oleh gonadotropin (Garcia-Diez et al.,
3.1 Waktu dan Tempat Penelitian
Penelitian dilakukan di Laboratorium Zoologi jurusan Biologi Institut Teknologi Sepuluh Nopember pada bulan Maret – Mei 2014.
3.2 Metode yang Digunakan
3.2.1 Pemeliharaan mencit (Mus musculus)
Mencit jantan galur Balb/C dengan kisaran umur 2-3 bulan
sebanyak 25 ekor diaklimatisasi di dalam laboratorium selama 2 minggu, 25 ekor mencit tersebut dibagi menjadi 5 kelompok (masing-masing 5 ekor)
− Kelompok K(-) : mencit kontrol negatif (normal).
− Kelompok K(+) : mencit kontrol positif (hiperglikemik).
− Kelompok TB : mencit hiperglikemik yang diberi ekstrak
ikan gabus dengan dosis masing-masing 0,07423 ml/hari.
− Kelompok TT : m encit hiperglikemik yang diberi ekstrak
ikan gabus dengan dosis masing-masing 0,1248 ml/hari.
− Kelompok TA : m encit hiperglikemik yang diberi ekstrak
ikan gabus dengan dosis masing-masing 0,14846 ml/hari. Alas kandang diberi sekam secara merata, serta setiap hari diberi pakan dan minum. Mencit dipuasakan selama 18 j am sebelum pengecekan kadar gula darah yakni pada hari ke-15. Pengecekan dilakukan dengan menggunakan glukometer.
3.2.2
Perlakuan mencit hiperglikemik 3.2.2.1 Pembuatan larutan aloksanMasing-masing mencit ditimbang terlebih dahulu untuk mengetahui berat badan yang berhubungan dengan banyaknya aloksan monohidrat yan g diinduksikan. Dengan menggunakan acuan dosis 190 mg/kg berat badan, dikonversikan ke dalam berat badan mencit dalam satuan gram. Proses penyimpanan sampai proses penyuntikan aloksan sebaiknya dilakukan pada suhu
dingin supaya aloksan tidak rusak. Aloksan yang telah ditimbang kemudian dilarutkan dengan akuades pro-injeksi sebanyak 0,5 cc untuk masing-masing mencit (Jin, 2012).
3.2.2.2 Induksi mencit hiperglikemik dengan aloksan
Setelah pengecekan glukosa darah (yakni pada hari ke-15),
penginduksian aloksan dilakukan pada kelompok K(+), TB, TT
dan TA pada hari ke-16. Masing-masing mencit diinduksi aloksan sebanyak 0,5 cc menggunakan syringe 1 ml secara intraperitoneal. Terlebih dahulu bagian ventral tubuh mencit diusap dengan kapas yang sudah dibasahi dengan alkohol 70% supaya steril. Kemudian syringe yang sudah berisi larutan aloksan, diinjeksikan pada daerah tersebut. Mencit pada kelompok K(-) hanya diinjeksi dengan aquades pro-injeksi saja (Jin, 2012).
3.2.3
Terapi mencit hiperglikemikMencit kelompok TB,TT dan TA yang memiliki kadar glukosa darah >200 mg/dL, siap diterapi menggunakan ekstrak ikan gabus secara oral pada hari ke-20.
− kelompok TB: mencit hiperglikemik yang diberi ekstrak ikan
gabus dengan dosis masing-masing 0,07423 ml/hari.
− kelompok TT: mencit hiperglikemik yang diberi ekstrak ikan
gabus dengan dosis masing-masing 0,1248 ml/hari.
− kelompok TA: mencit hiperglikemik yang diberi ekstrak ikan
gabus dengan dosis masing-masing 0,14846 ml/hari.
Terapi dengan ekstrak ikan gabus ini dilakukan setiap hari selama 14 hari yaitu sampai hari ke-33. Dosis yang digunakan berdasarkan dari perhitungan dosis dari Fakultas kedokteran Hewan Universitas Airlangga.
3.2.4
Pengukuran kadar glukosa darahdari ujung ekor pada kotak sensor di strip. Kemudian ditunggu pada layar glukometer akan muncul angka digital (dinyatakan dalam mg/dL) yang menunjukkan kadar glukosa darah mencit tersebut. Penggunaan strip untuk tiap mencit harus berbeda-beda. Pengecekan kadar glukosa darah dilakukan pada hari ke-15, 19 dan 34 (Padilah, 2009).
3.2.5
Pembuatan preparat histologi testis mencitSampel testis yang telah difiksasi dalam buffer formalin 10%, kemudian dibuat sediaan histologis (metode parafin dan pewarnaan Hematoksilin-Eosin (HE)) dengan tahapan sebagai berikut:
a. Dehidrasi dilakukan dengan memasukkan organ testis tersebut
ke dalam alkohol 70%, 80%, 90%, dan 96%, masing-masing selama 30 menit.
b. Clearing atau dealkoholisasi (pembersihan) dilakukan dengan
memasukkan organ testis tersebut ke dalam xylol sampai jernih atau transparan selama 24 jam.
c. Infiltrasi ke dalam parafin dilakukan di dalam oven pada suhu
56-60˚C. Sebelum masuk ke parafin murni, jaringan dimasukkan ke dalam xylol parafin 3:1, 1:1, dan 1:3. Setelah itu dimasukkan ke dalam paraffin murni, masing-masing perlakuan selama 30 menit.
d. Embedding, jaringan dari parafin murni ditanamkan ke dalam
suatu tempat yang telah berisi parafin cair. Jaringan diletakkan pada bagian dasar tengah dengan posisi melintang.
e. Sectioning (pemotongan) dilakukan dengan memasang holder
di mikrotom, kemudian mengatur ketebalan irisan sebesar 5 mikron pada mikrotom. Lalu diiris secara seri dengan cara memutar pengait mikrotom.
f. Deparafinasi, untuk menghilangkan parafin, sediaan histologis
dimasukkan ke dalam xylol I dan II masing-masing 10 menit. h. Staining (pewarnaan) dilakukan dengan pewarna hematoksilin
dimasukkan ke alkohol 95%, 90%, 80%, 70%, 60%, 50%, 40%, 30%, dan aquades. Dimasukkan ke hematoxylin 7 detik, lalu dicuci dengan air mengalir selama 10 menit, dicelup aquades lalu ke alkohol 30%, 40%, 50%, 60%, 70% beberapa celupan. Dimasukkan ke dalam eosin 1-2 menit, kemudian dicelupkan ke alkohol 70%, 80%, 90%, dan 95%, lalu dikeringkan dengan kertas saring. Dimasukkan xylol selama 15 menit, kemudian sediaan histologis ditetesi canada balsam.
i. Mounting (penutupan) dan labeling (pemberian label) yaitu
penutupan preparat dengan menggunakan kaca penutup dan memberi identitas pada preparat (label), kemudian disimpan dalam kotak sediaan (Volk, 1984)
3.2.6 Pengamatan mikroskopis
Pengamatan secara mikroskopis histologi testis dilakukan dengan menghitung jumlah sel Leydig dan sel spermatogenik (Spermatogonium, Spermatosit, dan spermatid). Pengamatan
mikroskopis menggunakan mikroskop Olympus® CX21
perbesaran 40-1000x.
3.3 Rancangan Penelitian dan Analisa Data
Penelitian ini merupakan penelitian eksperimental menggunakan rancangan acak lengkap (RAL). Uji statistika
menggunakan ANOVA one way. Kemudian dilakukan
perbandingan antara rata-rata jumlah sel Leydig dan sel spermatogenik pada semua kelompok mencit percobaan. Penelitian ini memiliki hipotesa :
H0: Tidak ada potensi regenerasi sel Leydig dan sel
spermatogenik testis mencit hiperglikemik setelah diinduksi ekstrak ikan gabus
H1: Ada potensi regenerasi sel Leydig dan sel spermatogenik
testis mencit hiperglikemik setelah diinduksi ekstrak ikan gabus
Jika H1 diterima maka dilakukan uji Tukey dengan selang
4.1 Potensi Regenerasi Sel Leydig Testis Mencit Hiperglikemik setelah Diinduksi Ekstrak Ikan Gabus
Sel Leydig merupakan sel yang terletak di jaringan interstitialis testis dan berfungsi mengasilkan hormon testosteron, hormon ini berperan dalam proses kehidupan seksual ataupun mempengaruhi tanda-tanda kelamin sekuder laki laki dan juga mempengaruhi proses spermatogenesis. Aktivitas sel Leydig sangat dipengaruhi kadar gonadotropin terutama LH/ICSH, apabila gonadotropin terganggu maka sel Leydig dan proses spermatogenesis pun bisa terganggu (Suryadi, 2007).
Pada penderita diabetes mellitus terjadi tidak sensitifnya insulin dan peningkatan kadar glukosa darah (hiperglikemia) yang berdampak pada testis berupa penurunan jumlah sel Leydig per ruang interstitial (Ballester, 2004). Berkurangnya jumlah sel Leydig menyebabkan penurunan kadar testosteron secara signifikan sehingga akan mengganggu proses spermatogenesis
(Remzi et al., 2004). Gangguan pada spermatogenesis ini diduga
dapat diatasi apabila kadar glukosa kembali pada kadar normal.
Penelitian Abdulgani et al., (2014) membuktikan bahwa
ekstrak ikan gabus dapat menurunkan kadar glukosa darah mencit hiperglikemik. Pada penelitian ini dilakukan penghitungan jumlah sel Leydig untuk mengetahui potensi regenerasi sel Leydig setelah pemberian ekstrak ikan gabus. Hasil anova mengenai pengaruh perlakuan terapi ekstrak ikan gabus terhadap jumlah sel Leydig testis mencit disajikan pada Tabel 4.1.
Hasil anova menunjukan tidak adanya pengaruh perlakuan terhadap jumlah sel Leydig pada semua kelompok perlakuan (p>0.05). Jumlah sel Leydig kelompok K(-) (kontrol negatif) dengan kelompok K(+) (kontrol positif) tidak berbeda secara signifikan. Hal ini menandakan bahwa kondisi hiperglikemik hanya memberikan efek yang kecil terhadap sel Leydig dan regenerasi tidak terjadi, sehingga jumlah sel Leydig kelompok TB
(terapi dosis bawah), TT (terapi dosis tengah), dan TA (terapi dosis atas) juga tidak menunjukkan perbedaan yang signifikan dengan kelompok K(-) dan K(+).
Tabel 4.1 Jumlah Sel Leydig/Bidang Pandang
Perlakuan Jumlah Sel Leydig (Sel)
K(-) 67 ± 15
Kelompok K(-) : mencit kontrol negatif (normal). Kelompok K(+) : mencit kontrol positif (hiperglikemik).
Kelompok TB : mencit hiperglikemik yang diberi ekstrak ikan gabus dengan dosis masing-masing 0,07423 ml/hari.
Kelompok TT : mencit hiperglikemik yang diberi ekstrak ikan gabus dengan dosis masing-masing 0,1248 ml/hari.
Kelompok TA : mencit hiperglikemik yang diberi ekstrak ikan gabus dengan dosis masing-masing 0,14846 ml/hari.
Sel Leydig dirangsang oleh Luteinizing Hormone (LH)
untuk memproduksi testosteron. Testosteron diperlukan untuk perkembangan sel-sel spermatogenik. Oleh karena itu, bila kadar testosteron menurun ada kemungkinan terjadinya penghambatan
pembentukan sel-sel spermatogenik. Penelitian Adewole et al..
(2007) menunjukkan bahwa hiperglikemik menyebabkan penurunan jumlah sel Leydig. Pada penelitian ini terjadi penurunan jumlah sel Leydig pada kelompok perlakuan K(+) namun tidak berbeda signifikan dengan kelompok K(-). Sehingga diambil kesimpulan bahwa jumlah sel Leydig tidak terlalu berpengaruh terhadap spermatogenesis. Diduga kerusakan sel pada kelompok K(+) lebih dipengaruhi oleh hormonal. Stres oksidatif yang terjadi akibat hiperglikemik akan memicu
penurunan kadar LH dan FSH (Nasrolahi et al., 2013). Penurunan
spermatogenesis. Pengamatan histologis pada ruang intrastitial yang ditunjukkan dengan Gambar 4.1 juga tidak memperlihatkan kondisi yang berbeda antar perlakuan.
Gambar 4.1 Sel Leydig pada Ruang Intrastitial (tanda panah) dengan Perbesaran 400x.
4.2 Potensi Regenerasi Sel Spermatogenik Testis Mencit Hiperglikemik setelah Diinduksi Ekstrak Ikan Gabus
Pengamatan jumlah sel spermatogenik pada penelitian ini bertujuan untuk mengetahui potensi dan tingkat regenerasi sel spermatogenik testis mencit yang mengalami kerusakan akibat kondisi hiperglikemik. Hasil anova mengenai jumlah sel-sel spermatogenik testis mencit yang meliputi spermatogonium, spermatosit, dan spermatid disajikan pada Tabel 4.2.
Berdasarkan anova diketahui adanya pengaruh induksi ikan gabus terhadap jumlah sel. Sehingga dilakukan uji Tukey dengan hasil yang tercantum pada Tabel 4.2. Perbedaan yang signifikan (p<0.05) ditemui pada jumlah spermatogonium kelompok perlakuan K(-) dan K(+), jumlah spermatogonium K(+) hanya 55% dari K(-). Hal ini membuktikan bahwa Hiperglikemik memicu kerusakan sel dan gangguan spermatogenesis, sehingga terjadi penurunan jumlah sel spermatogonium.
K(-) K(+)
Setelah dilakukan terapi ekstrak ikan gabus selama 14 hari terjadi peningkatan jumlah spermatogonium pada kelompok TB, TT, dan TA. Jumlah spermatogonium perlakuan TB tidak berbeda secara signifikan (p>0.05) dengan K(+) sehingga disimpulkan bahwa tidak ada potensi regenerasi spermatogonium pada kelompok dengan induksi ekstrak ikan gabus dengan dosis 0,07423 ml/hari. Sedangkan jumlah spermatogonium kelompok perlakuan TT dan TA tidak berbeda signifikan dengan K(-). Tidak adanya perbedaan yang signifikan antara jumlah spermatogonium K(-) dengan TT dan TA menandakan adanya potensi regenerasi spermatogonium mencit hiperglikemik yang hampir mendekati normal setelah diinduksi ekstrak ikan gabus dengan dosis 0,1248 dan 0,14846 ml/hari. Spermatogonium TT mengalami regenerasi mencapai 85% dari jumlah sel normal, sedangkan jumlah spermatogonium TA mencapai 91% dari jumlah sel normal.
Tabel 4.2 Jumlah Sel Spermatogenik/Bidang Pandang
Jenis Sel Jumlah Sel Spermatogenik pada
perlakuan-K(-) K(+) TB TT TA
Spermatogonium 44a± 4 24b±10 26b± 5 37a± 4 40a± 4 Spermatosit 51a± 2 19d± 3 29c± 7 39b± 4 51a± 4 Spermatid 147a±11 27d±15 80c±13 103b±11 139a±46
Keterangan:
Kelompok K(-) : mencit kontrol negatif (normal). Kelompok K(+) : mencit kontrol positif (hiperglikemik).
Kelompok TB : mencit hiperglikemik yang diberi ekstrak ikan gabus dengan dosis masing-masing 0,07423 ml/hari.
Kelompok TT : mencit hiperglikemik yang diberi ekstrak ikan gabus dengan dosis masing-masing 0,1248 ml/hari.
Kelompok TA : mencit hiperglikemik yang diberi ekstrak ikan gabus dengan dosis masing-masing 0,14846 ml/hari.
37% dari jumlah sel normal, dan jumlah spermatid K(+) 18% dari jumlah sel normal. Penurunan jumlah spermatosit disebabkan oleh berkurangnya spermatogonium. Spermatogonium merupakan sel germinal yang akan membelah menjadi spermatosit. Apabila jumlah spermatogonium berkurang maka jumlah spermatosit juga akan ikut berkurang. Begitu pula pada spermatid yang merupakan sel haploid dari pembelahan meiosis spermatosit. Apabila jumlah spermatosit berkurang maka jumlah spermatid akan ikut berkurang. Selain itu penurunan jumlah spermatosit dan spermatid dapat pula disebabkan oleh efek sitotoksik dari kondisi hiperglikemik yang memicu kerusakan sel.
Setelah pemberian ekstrak ikan gabus selama 14 hari terjadi peningkatan jumlah spermatosit dan spermatid pada ketiga kelompok induksi. Jumlah spermatosit dan spermatid kelompok K(+) berbeda signifikan dengan TB, TT, dan TA. Perbedaan yang signifikan antara jumlah spermatosit dan spermatid kelompok K(+) dengan kelompok TB, TT, dan TA menandakan adanya potensi regenerasi sel setelah diinduksi ekstrak ikan gabus. Tingkat regenerasi terbaik ditemukan pada kelompok TA dengan persentase jumlah spermatosit 99% dan spermatid 95% dari jumlah normal. Jumlah sel spermatosit dan spermatid kelompok K(-) tidak berbeda secara signifikan dengan kelompok TA, sehingga dapat disimpulkan bahwa dengan dosis 0,14846 ml/hari dapat terjadi regenerasi spermatosit dan spermatid mendekati normal.
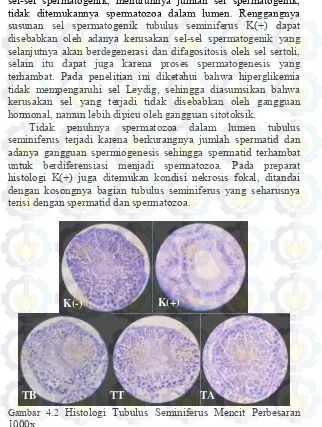
sel-sel spermatogenik, menurunnya jumlah sel spermatogenik, tidak ditemukannya spermatozoa dalam lumen. Renggangnya susunan sel spermatogenik tubulus seminiferus K(+) dapat disebabkan oleh adanya kerusakan sel-sel spermatogenik yang selanjutnya akan berdegenerasi dan difagositosis oleh sel sertoli, selain itu dapat juga karena proses spermatogenesis yang terhambat. Pada penelitian ini diketahui bahwa hiperglikemia tidak mempengaruhi sel Leydig, sehingga diasumsikan bahwa kerusakan sel yang terjadi tidak disebabkan oleh gangguan hormonal, namun lebih dipicu oleh gangguan sitotoksik.
Tidak penuhnya spermatozoa dalam lumen tubulus seminiferus terjadi karena berkurangnya jumlah spermatid dan adanya gangguan spermiogenesis sehingga spermatid terhambat untuk berdiferensiasi menjadi spermatozoa. Pada preparat histologi K(+) juga ditemukan kondisi nekrosis fokal, ditandai dengan kosongnya bagian tubulus seminiferus yang seharusnya terisi dengan spermatid dan spermatozoa.
Gambar 4.2 Histologi Tubulus Seminiferus Mencit Perbesaran 1000x
K(-) K(+)
Pada kelompok mencit yang diterapi dengan ekstrak ikan gabus (TB,TT, dan TA) tampak terjadi pertambahan jumlah sel. Pada ketiga kelompok terapi ditemukan semua jenis sel spermatogenik, yaitu sel spermatogonium, spermatosit, spermatid, dan spermatozoa. Namun pada kelompok TB jumlah sel spermatogenik belum mencapai jumlah normal sehingga lumen tampak luas, selain itu susunan selnya masih terlihat renggang. Pada kelompok TT jumlah sel spermatogenik lebih banyak dari TB, susunan sel terlihat lebih rapat. Pada kelompok TA jumlah sel semakin banyak mengisi tubulus seminiferus sehingga area lumen semakin sempit, jumlah dan kerapatan sel spermatogenik hampir sama dengan normal.
Kondisi hiperglikemia yang menandai terjadinya penyakit diabetes mellitus, dapat menyebabkan kerusakan sel melalui berbagai cara, salah satunya melalui komplikasi mikrovaskular. Adanya komplikasi mikrovaskular akan memicu terjadinya komplikasi fisiologis, biokimia, dan anatomi, antara lain
penebalan m embran (Raskin et al., 1983), penyakit
makrovaskular (Eschwege et al., 1985), glikosilasi protein
(Brownlee et al., 1988), gangguan immunitas seluler (Rayfield et
al., 1982), dan berbagai abnormalitas siklus sel (Lorenzi et al.,
1987) seperti gangguan spermatogenesis yang terjadi pada mencit kelompok kontrol positif di penelitian ini. Selain itu, hiperglikemia juga menyebabkan gangguan sekresi dan aksi
insulin (DeFronzo et al., 1988) sehingga akan timbul kondisi
hiperglikemik yang lebih kronis.
Pada penderita diabetes melitus dengan hiperglikemia kronis
akan terjadi peningkatan aktifitas Protein Kinase C (PKC), Tumor
Necrosis Factor α (TNF α) yang dapat menyebabkan gangguan
Penurunan jumlah sel spermatogenik juga dapat dipicu oleh kerusakan sel-sel karena adanya radikal bebas yang tinggi. Radikal bebas adalah sekelompok bahan kimia baik berupa atom maupun molekul yang memiliki elektron tidak berpasangan pada lapisan luarnya. Radikal bebas merupakan suatu kelompok bahan kimia dengan reaksi jangka pendek yang memiliki satu atau lebih elektron bebas (Droge 2002). Kerusakan sel-sel spermatogenik oleh faktor radikal bebas dapat dicegah dengan mengkonsumsi makanan yang mengandung antioksidan. Antioksidan adalah substansi yang diperlukan tubuh untuk menetralisir radikal bebas dan mencegah kerusakan yang ditimbulkan oleh radikal bebas terhadap sel normal (Drodge, 2002). Cara kerja antioksidan dalam menetralisir radikal bebas yaknimelengkapi kekurangan electron yang dimilikiradikal bebas yang dapat menimbulkan stress oksidatif dengan mengeluarkan spesies oksigen yang potensial bersifat toksik (pro-oksidan), menekan pembentukannya, atau
menekan kerja pro-oksidan tersebut (Ruhe, 2001). Ekstrak ikan
gabus dikenal mengandung antioksidan. Ekstrak ikan gabus mengandung banyak protein. Albumin, sebagai protein plasma dengan kadar terbanyak dalam ekstrak ikan gabus merupakan sumber antioksidan hewani yang berfungsi sebagai pengikat radikal sehingga berperan dalam proses pembersihan dan penangkapan radikal bebas (Sunatrio, 2003).
Ekstrak ikan gabus m emiliki aktivitas antioksidan 0,14 ± 0.003 mmol/l, atau sebanding dengan 90,93% aktivitas antioksidan vitamin E. Albumin merupakan protein yang tersusun oleh asam amino yang memiliki gugus (-SH) sehingga berfungsi sebagai pengikat radikal dan berperan dalam proses pembersihan
radikal bebas (Santoso, 2009). Selain itu albumin juga bersinergi
limfosit dan protein, memperbaiki nafsu makan dan stabilisasi berat badan (Gibson, 2005). Sedangkan kalsium dapat meningkatkan sensitivitas, respon dan sekresi insulin (Wilcox, 2005).
Berdasarkan hasil penelitian dapat disimpulkan bahwa pemberian ekstrak ikan gabus berpotensi untuk meregenerasi sel-sel spermatogenik, yaitu sel-sel spermatogonia, spermatosit, dan spermatid. Regenerasi tersebut disebabkan oleh khasiat ekstrak ikan gabus sebagai antioksidan serta sangat berperan dalam perkembangan sel dan pembentukan jaringan sel baru. Ekstrak ikan gabus membantu sekresi dan metabolisme insulin, serta melindungi efek kerusakan pankreas. Apabila kondisi pankreas telah kembali normal maka jumlah hormon insulin yang diproduksi oleh sel beta pulau langerhans akan kembali seperti semula. Hormon insulin bersama hormon glukagon akan bekerja secara antagonis untuk mengatur homeostasis gkukosa darah. Kadar glukosa darah yang normal akan mencegah munculnya gangguan-gangguan yang dapat memicu keruskan sel.
BAB V
KESIMPULAN DAN SARAN
5.1 Kesimpulan
1. Tidak ada potensi regenerasi sel Leydig pada testis mencit
hiperglikemik setelah diinduksi dengan ekstrak ikan gabus.
2. Ada potensi regenerasi sel spermatogenik dalam tubulus
seminiferus testis mencit hiperglikemik setelah diinduksi dengan ekstrak ikan gabus. Tingkat regenerasi tertinggi pada kelompok perlakuan dosis atas (0,14846 ml/hari) dengan persentase jumlah spermatogonium sebesar 91 % dari jumlah sel normal, spermatosit sebesar 91% dari jumlah sel normal dan spermatid sebesar 99 % dari jumlah sel normal.
5.2 Saran
1. Perlu dilakukan penelitian lebih lanjut mengenai pengaruh
ekstrak ikan gabus terhadap sel spermatogenik dengan variasi lama waktu induksi, sehingga dapat diketahui potensi regenerasi sel spermatogenik dalam rentang waktu induksi yang berbeda.
2. Perlu dilakukan penelitian mengenai kadar hormon
testosteron, sehingga diketahui pengaruh hormonal terhadap spermatogenesis.
3. Perlu dilakukan uji klinis terapi ekstrak ikan gabus pada
manusia.
4. Untuk penelitian yang selanjutnya disarankan menggunakan
hewan coba yang sudah diabetes, atau menggunakan zat diabetogenik lain yang efeknya lebih lama dari aloksan.
Aisyatussoffi, N., dan Arifiyanto, A. 2014. Snakehead (Channa striata) extracts treatment towards hyperglycemic mice (Mus musculus) blood glucose levelsand pancreatic histology Structure. J. Appl. Environ. Biol. Sci., 4:1-6.
Adewole, S.O., Caxton-Martin, E.A., Salako, A.A., Doherty, O.W., dan Naicker, T. 2007. Effects of oxidative stress induced by streptozotocin on the morphology and trace minerals of the
testes of diabetic wistar rats. J. Pharmacologyonline. 2:487-497.
Amann, R. P. 1970. Sperm Production Rates dalam A. D.
Johnson, W. R. Gomes dan N. L. VanDemark (Ed). New York: Academic Press.
Andayani, Y. 2003. Mekanisme Aktivitas Antihiperglikemik
Ekstrak Buncis (Phaseolus vulgaris Linn) pada Tikus Diabetes
dan Identifikasi Komponen Aktif. Disertasi. Bogor: Program
Pasca Sarjana. Institut Pertanian Bogor.
Arrington, L. 1972. Introductory Laboratory Animal. The
Breeding, Care, and Management of Experimental Animal Science. New York: The Interstate Printers and Publishing, Inc.
Ballester, J., Munoz, C., Dominguez, J., Rigau, T., Guinovart, J.J., dan Rodriguez-Gil J.E. 2004. Insulin-dependent diabetes affects testicular function by FSH-and LH-linked mechanisms.
Journal of Andrology 25:706–719.
Baziad, A. 2003. Menopause dan Andropause. Jakarta: Yayasan
Bina Pustaka Sarwono Prawirohardjo.
Bijaksana, U. 2012. Dosmestikasi ikan gabus, Channa Striata
Blkr, upaya optimalisasi perairan rawa di provinsi kalimantan
selatan. Jurnal Lahan Suboptimal 1: 92-101.
Brownlee, M., Cerami, A., dan Vlassara, H. 1988. Advanced glycosylation end products in tissue and the biochemical basis of
diabetic complications. N Engl I Med 318:1315-1321.
Burkitt, H,G. 1993. Functional Histologis, A Text and Colour
Atlas, London: Langman Group.
Campbell, N.A. Reece, J.B., Urry, L.A., Cain, M.L., Wasserman,
S.A., Minorsky, P.V., dan Jackson, B.R. 2008. Biology. San
Francisco: Pearson Benjamin Cummings.
Colca, J. R. 1983. Alloxan inhibition of Ca2+ and calmodulin
dependent protein kinase activity in pancreatic islet. J. Biol.
Chem. 12:7260-7263.
Corwin, E.J. 2001. Buku Saku Patofisiologi. Jakarta: EGC
Cox, N.M., Meurer, K.A., Carlton, C.A., Tubbs, R.C., dan Mannis, D.P. 1994. Effect of diabetes mellitus during the luteal phase of oestrous cycle on p reovulatory follicular function,
ovulation and gonadotrophins in gilts. Journal of Reproduction
and Fertility 101:77-86.
DeFronzo, R.A. 1988. Lilly Lecture 1987: The triumvirate: 0-
cell, muscle, liver: a collusion responsible for NIDDM. Diabetes
37:667-687.
Droge W. 2002. Free radicals in the physiological control of cell
Endrinaldi, E., Yerizel, dan Revilla, G. 2007. Pengaruh pemberian vitamin C dan E terhadap kadar MDA dan kolesterol darah kelinci diabetes melitus (DM) akibat induksi aloksan.
Majalah Kedokteran Andalas,Juli-Desember, 51-56.
Escadon, J.C. dan Cipolla, M. 2001. D iabetes and endothelial
dysfunction ; a clinical perspective. Endocrine Reviews 22: 36–
52.
Eschwege, E., Richard, J.L., Thibult, N., Ducimetiere, P., Warnet, J.M., Claude, J.R., dan Rosselin, G.E. 1985. Coronary heart diseased mortality in relation with diabetes, blood glucose and plasma insulin levels: the Paris prospective study, ten years later.
Horm Metab Res 15:41-46.
Fadli. 2010. Bagusnya Ikan Gabus.. Warta Pasar Ikan. Edisi
No.86, hal 4-5.
Fishbase. 2012. Channa striatus. <http://www.fishbase.org/
summary/CHANNA-STRIATUS.html> [23 Juli 2014].
García-Díez, L.C., Corrales, Hernandez, J.J., Hernandez-Diaz, J., Pedraz, M.J., dan Miralles, J.M. 1991. Semen characteristics and
diabetes mellitus: significance of insulin in male infertility. Arch
Androl 26: 119–128.
Garris, D.R., Williams, S.K., Smith-West, C., dan West, L. 1984. Diabetes-assosiated endometrial disruption in the chinese hamster: structure changes in relation to progressive
hyperglycemia. Experimental Biology and Medicine 17:
293-300.
periluminal epithelial lipoanathrophy. Experimental Biology and Medicine 52:51-58.
Gibson, 2005. Principles of Nutritional Assesment. New York.
Oxford University Prees.
Gorus, F.K., Malaisse, W.J., dan Pipeleers, D.G. 1982. Selective
uptake of alloxan by pancreatic B-cells. Biochem Journal
208:513-515.
Gupta, G.S. 2005. Proteomics of Spermatogenesis. India:
Departmen of Biophysis Panjab University.
Hafez, E.S.E. 1970. Reproduction and Breeding Techniques
for Laboratory Animals. Philadelphia: Lea and Febiger.
Hayati, A., Rahmaninta, A.D., dan Pidada, I.B.R. 2005. Spermatozoa motility and morphological recovery process in mice (Mus musculus) after the induction of 2-methoxyethanol.
Folia Medica Indonesiana, 41: 90-95.
International Diabetes Federation. 2007. World Diabetes Day..
<http://www.worlddiabetesday.org/> [14 November 2013].
Jin, M., Lu, Z., Huang, M., dan Wang, Y. 2012. E ffects of
se-enriched polysacchararides produced by Enterobacter cloacae
Z0206 on alloxan-induced diabetic mice. Int J Biol Macromol.
50:348-352.
Kandeel, F.R., Koussam V.K.T., dan Swerdloff, R.S. 2001. Male sexual function and disorders: physiology, pathophysiology,
Lorenzi, M., Nordberg, J.A., dan Toledo, S. 1987. High glucose prolongs cell-cycle traversal of cultured human endothelial cells.
Diabetes 36:1261-1267.
Manika, W., Tomaszewska, Sutama, I.K., Putu, I.G., dan
Chaniago, T.D. 1991. Reproduksi, Tingkah Laku Dan
Reproduksi Ternak Di Indonesia. Jakarta: PT. Gramedia
Pustaka Utama
Meldawati, 2011. Pengaruh Ekstrak Buah Morinda Citrifolia Linn terhadap Kualitas, Kuantitas Sperma dan Kadar Malondialdehyde
Testis Tikus Wistar Diabetes Mellitus. Tesis. Padang: Universitas
Sumatera Utara.
Mescher, A.L. 2010. Junqueira's Basic Histology Text and
Atlas. Indiana: The McGraw-Hill Companies, Inc.
Moriwaki, K. 1994. Genetic in Wild Mice. Its Application to
Biomedical Research. Tokyo: Karger.
Nasrolahi, O., Khanesi, F., Rahmani, F., dan Razi, M. 2013. Honey and metformin ameliorated diabetes-induced damages in
testes of rat; correlation with hormonal changes. Iran J Reprod
Med. 11: 1013-1020.
Ng, P.K. dan Lim, K.K.P. 1990. Snakeheads (Pisces: Channidae):
Natural history, biology and economic importance. Papers.
Department of Zoology, National University of Singapore, 127-152.
Nugroho, B.A. dan Purwaningsih, E. 2006. Perbedaan Diet
Ekstrak Rumput Laut (Eucheuma sp) dan insulin dalam
menurunkan kadar glukosa darah tikus putih (Rattus norvegicus)
Padilah, I. 2009. U ji Efek Hipogilkemia Fraksi Etil Asetat Biji
Jinten Hitam (Nigella sativa Linn) pada Tikus Putih Jantan
dengan Metode Induksi Aloksan dan Toleransi Glukosa. Skripsi.
Jakarta: UIN Syarif Hidayatullah.
Rahayu, W.P.S., Maamoen, Suliantari, dan Fardiaz, S. 1992.
Teknologi Fermentasi Produk Perikanan. Bogor: Penerbit
Pusat Antar U niversitas Pangan dan Gizi, Institut Pertanian Bogor.
Raskin, P., Pietri, A., Unger, R., dan Shannon, W.A. 1983. The effect of diabetic control on the width of skeletal muscle capillary
basement membrane in patients with type I diabetes mellitus. N
Englj Med 309:1546-1550.
Rayfield, E.J., Ault, M.J., Keusch, G.T., Brothers, M.J., Nechemias, C., dan Smith, H. 1982. Infection and diabetes: the
case for glucose control. Am I Med 72:439-450.
Rees, D,A. and Alcolado, J. C. 2005, Animal models of diabetes
mellitus. Diabetic Medicine, 22 : 359-370.
Remzi, C., Ali, G., Suat, A., Kemal, N., dan Ayegul, J. 2004. Hypotalamic pituitary-gonadal axis hormones and cortisol in both menstrual phases of women with chronic fatigue syndrome and
effect of depressive mood on these hormones. BMC
Musculoskelet Disord, 5:47-51.
Ruhe, R.C. 2001. Use of antioxidant nutrients in the prevention
and treatment of type 2 diabetes. J Am Coll Nutrition.
20:363-369.
Sampath, K. 1985 Food intake, conversion and surfacing activity as a f unction of density and water change frequency in an