BAB II
TINJAUAN PUSTAKA 2.1 Definisi Obat
Obat merupakan semua zat baik kimiawi, hewani, maupun nabati yang dalam dosis layak dapat menyembuhkan, meringankan, atau mencegah penyakit berikut gejalanya. Farmakologi atau ilmu khasiat obat adalah ilmu yang mempelajari pengetahuan obat dengan seluruh aspeknya, baik sifat kimiawi maupun fisikanya, kegiatan fisiologi, resorpsi, dan nasibnya dalam organisme hidup. Dan untuk menyelidiki semua interaksi antara obat dan tubuh manusia khususnya, serta penggunaaan pada pengobatan penyakit, disebut farmakologi klinis (Tan Hoan Tjay dan Kirana Rahardja, 2002).
Obat-obat yang digunakan dalam terapi dapat dibagi dalam 3 (tiga) golongan besar sebagai berikut:
a) Obat farmakodinamis, yang bekerja terhadap tuan rumah dengan jalan mempercepat atau memperlambat proses fisiologi atau fungsi biokimia dalam tubuh misalnya hormon, diuretika, hipnotika dan obat otonom.
b) Obat kemoterapeutis dapat membunuh parasit dan kuman di dalam tubuh tuan rumah. Hendaknya obat ini memiliki kegiatan farmakodinamika yang sekecil-kecilnya terhadap organisme tuan rumah dan berkhasiat membunuh sebesar-besarnya terhadap sebanyak mungin parasit (cacing, protozoa) dan mikroorganisme (bakteri dan virus). Obat-obat neoplasma.
(onkolitika, sitostatika, obat-obat kanker) juga dianggap juga golongan ini.
Obat diagnostis merupakan obat pembantu untuk melakukan diagnosis (pengenalan penyakit), misalnya dari saluran lambung usus (barium sulfat) dan
c) Dan saluran empedu (natriumiopanoat dan asam iod organik lainnya) (Tan Hoan Tjay dan Kirana Rahardja, 2002).
2.2 Tablet
Tablet adalah sediaan padat, dibuat secara kempa-cetak berbentuk rata atau cembung rangkap, umumnya bulat, mengandung satu jenis obat atau lebih dengan atau zat tambahan. Zat tambahan yang digunakan dapat berfungsi sebagai:
a. Zat pengisi, yaitu untuk memperbesar volume tablet. Biasanya yang digunakan Amilum Manihot, Kalsium Fosfat, Kalsium Karbonat dan zat lain yang cocok.
b. Zat pengikat, yaitu agar tablet tidak pecah atau retak, dapat merekat. Biasanya yang digunakan adalah Musilago 10-20%, larutan Metil-cellulosum 5%.
c. Zat penghancur, yaitu agar tablet dapat hancur dalam saluran percernaan.Biasanya yang digunakan Amilum Manihot kering, Gelatin, Natrium Alginat.
d. Zat pelicin, yaitu agar tablet tidak melekat pada cetakan. Biasanya yang digunakan Talkum 5%, Magnesium stearat, Asam stearat.
Menurut (Ansel, 1989) berdasarkan penggunaanya tablet diklasifikasikan sebagai berikut :
a. Tablet Kunyah
Tablet ini harus lembut (segera hancur ketika dikunyah) atau mudah melarut dalam mulut. Pengunyahan dapat mempercepat penghancuran tablet dan memberikan keadaan basa untuk garam-garam logam yang digunakan dalam tablet antasida. Tablet kunyah diberikan pada pasien yang mengalami gangguan menelan tablet. Tablet ini digunakan dalam formulasi tablet untuk anak-anak (dalam sediaan multivitamin). Penggunaan tablet lain ini adalah untuk tablet antasida dan antibiotik. Sediaan ini juga memungkinkan untuk digunakan di tempat yang tidak tersedia air
(Ansel, 1989). b. Tablet sublingual
Tablet yang disisipkan di bawah lidah. Biasanya berbentuk datar, ditujukan untuk obat-obat yang diabsorpsi melalui mukosa oral. Cara ini berguna untuk penyerapan obat yang rusak oleh cairan lambung dan sedikit sekali diabsorpsi oleh saluran pencernaan. Tablet ini dibuat segera melarut untuk memberikan efek yang cepat (Ansel, 1989).
c. Tablet bukal
Tablet yang disisipkan di pipi. Tablet ini dibuat agar hancur dan melarut perlahan-lahan (Ansel, 1989).
d. Tablet triturat
Tablet ini bentuknya kecil dan biasanya silinder. Tablet triturat harus cepat dan mudah larut seutuhnya di dalam air (Ansel, 1989).
e. Tablet hipodermik
Tablet ini digunakan melalui bawah kulit, dibuat dari bahan yang mudah larut (Ansel,1989).
f. Tablet efervesen
Tablet yang menghasilkan gas, dibuat dengan cara kompresi granul yang mengandung garam efervesen atau bahan–bahan lain yang mampu menghasilkan gas ketika bercampur dengan air. Misalnya penggabungan logam karbonat atau bikarbonat dengan tartrat menghasilkan gas CO2 di dalam air. Tablet bentuk ini
mempercepat pelarutan sediaan dan meningkatkan rasa (Ansel, 1989). 2.3 Evaluasi tablet
Untuk menjamin mutu tablet maka dilakukan beberapa pengujian yaitu sebagai berikut:
a. Uji keseragaman bobot
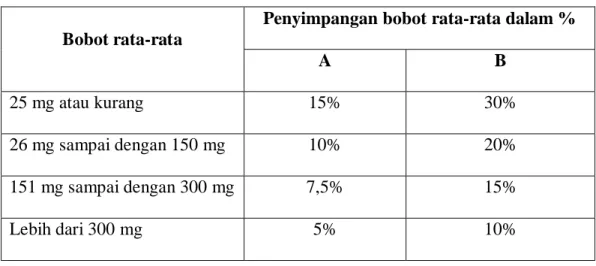
Tablet harus memenuhi uji keseragaman bobot. Keseragaman bobot ini ditetapkan untuk menjamin keseragaman bobot tiap tablet yang dibuat. Tablet-tablet yang yang bobotnya seragam diharapkan akan memiliki kandungan bahan obat yang sama, sehingga akan mempunyai efek terapi yang sama. Keseragaman bobot dapat ditetapkan sebagai berikut: ditimbang 20 tablet, lalu dihitung bobot rata-rata tiap tablet. Kemudian timbang tablet satu persatu, tidak boleh lebih dari 2 tablet bobotnya menyimpang dari bobot rata-rata lebih besar dari yang ditetapkan
pada kolom A dan tidak boleh satu tablet pun bobotnya menyimpang dari rata-rata lebih besar dari yang ditetapkan pada kolom B. Jika perlu gunakan 10 tablet yang lain dan tidak satu tablet yang bobotnya menyimpang lebih besar dari bobot rata-rata yang ditetapkan dalam kolom A maupun kolom B (Dirjen POM, 1984).
Tabel 1. Penyimpangan bobot rata-rata
Bobot rata-rata
Penyimpangan bobot rata-rata dalam %
A B 25 mg atau kurang 15% 30% 26 mg sampai dengan 150 mg 10% 20% 151 mg sampai dengan 300 mg 7,5% 15% Lebih dari 300 mg 5% 10% b. Uji kekerasan
Kekerasan tablet dan ketebalannya berhubungan dengan isi die dan gaya kompresi yang diberikan. Bila tekanan ditambahkan, maka kekerasan tablet meningkat sedangkan ketebalan tablet berkurang. Selain itu metode granulasi juga menentukan kekerasan tablet. Umumnya kekuatan tablet berkisar 4 - 8 kg, bobot tersebut dianggap sebagai batas minimum untuk menghasilkan tablet yang memuaskan. Alat yang di gunakan untuk uji ini adalah hardness tester, alat ini diharapkan dapat mengukur berat yang diperlukan untuk memecahkan tablet (Lachman, 1994).
Cara lain untuk menentukan kekuatan tablet ialah dengan mengukur keregasannya. Gesekan dan goncangan merupakan penyebab tablet menjadi hancur. Untuk menguji keregasan tablet digunakan alat Roche friabilator. Sebelum tablet dimasukkan ke alat friabilator, tablet ditimbang terlebih dahulu. Kemudian tablet dimasukan kedalam alat, lalu alat dioperasikan selama empat menit atau 100 kali putaran. Tablet ditimbang kembali dan dibandingkan dengan berat mula-mula. Selisih berat dihitung sebagai keregasan tablet. Persyaratan keregasan harus lebih kecil dari 0,8 % (Ansel, 1989).
c. Uji waktu hancur
Peralatan uji waku hancur terdiri dari rak keranjang yang mempunyai enam lubang yang terletak vertikal diatas ayakan mesh nomor 10 selama percobahan, tablet diletakkan pada tiap lubang keranjang. kemudiaan keranjang tersebut bergerak naik turun pada larutan transparan dengan kecepatan 29 - 32 putaran per menit. Interval waktu hancur adalah 5 - 30 menit. Tablet dikatakan hancur bila bentuk sisa tablet (kecuali bagian penyalut) merupakan massa dengan inti yang tidak jelas
(Ansel, 1989)
d. Uji penetapan kadar zat berkhasiat
Uji penetapan kadar berkhasiat dilakukan untuk mengetahui apakah tablet tersebut memenuhi syarat sesuai dengan etiket. Bila kadar obat tersebut tidak memenuhi syarat maka obat tersebut tidak memiliki efek terapi yang baik dan tidak layak dikonsumsi. Uji penetapan kadar dilakukan dengan menggunakan
cara-cara yang sesuai pada masing-masing monografi antara lain di Farmakope Indonesia (Ansel, 1989)
2.4 Cimetidin
2.4.1 Tinjauan umum tentang cimetidin ( Dirjen POM 1995) Rumus Bangun :
Nama Kimia : 2- Siano-1 metil-3-[2-[[(5-metilimidazol-4-il) Metil]tio]etil]guanidin [51481-61-9]
Rumus Molekul : C10H16N6S
Berat Molekul : 252,34
Pemerian : Serbuk hablur, putih sampai hampir putih; tidak berbau atau bau merpaktan lemah.
Susut pengeringan : Tidak lebih dari 1,0 % lakukan pengeringan pada suhu 110° selama 2 jam.
Kelarutan : Larut dalam etanol
Cimetidin mengandung tidak kurang dari 98% dan tidak lebih dari 102% C10H16N6S, dihitung terhadap zat yang telah dikeringkan (Farmakope Inonesia IV,
2.4.2 Antihistamin
Sewaktu diketahui bahwa histamin mempengaruhi banyak proses faalan dan patologik, maka dicairkan obat yang dapat mengantagonis efek histamin. Antihistamin misalnya antergen, neontergan, difenildramin dan tripelenamin dalam dosis terapi efektif untuk mengobati udem, eritem, dan pruritus tetapi dapat melawan efek hipersekresi asam lambung akibat histamin. Anihistamin
pengambat reseptor H1, Kedua jenis antihistamin ini bekerja secara kompetitif,
yaitu dengan menghambat interaksi histamin dan reseptor histamin H1 atau H2
(Ganiswara, 1995).
2.4.3 Farmakodinamika Cimetidin
Cimetidin menghambat reseptor H2 secara selektif dan reversible.
Perangsang reseptor H2 akan merangsang sekresi cairan lambung, sehingga pada
pemberian cimetidin sekresi cairan lambung di hambat pengaruh fisiologi cimetidin terhadap reseptor H2 lainya, tidak begitu penting. Walaupun tidak
lengkap cimetidin dapat menghambat sekresi cairan lambung akibat perangsangan obat muskarinik atau gastrin. Cimetidin mengurangi volume dan kadar ion hidrogen cairan lambung. Penurunan sekresi asam lambung mengakibatkan perubahan pepsinogen menjadi pepsin juga menurunan (Ganiswara, 1995).
2.4.4 Farmakokinetik Cimetidin
Bioavaulabilitas oral cimetidin sekitar 70%, sama dengan setelah pemberian IV atau IM. Ikatan protein plasmanya hanya 20%. Absorbsi cimetidin diperlambat oleh makan, sehingga cimetidin diberikan bersama atau segera setelah makan dengan maksud untuk memperpanjang efek pada periode pasca
makan. Absorbsi cimetidin terutama terjadi pada menit ke 60 – 90. Cimetidin masuk ke dalam bentuk asal dalam urin, masa paruh eliminasinya sekitar 2 jam (Ganiswara, 1995).
2.4.5 Efek samping Cimetidin
Efek samping pada obat ini umumnya berhubungan dengan penghambat terhadap reseptor H2; bebrapa efek samping lain tidak berhubungan dengan
penghambat reseptor. Efek samping ini antara lain nyeri kepala, pusing, mual, diare dan impoten (Ganiswara, 1995).
2.4.6 Penetapan Kadar Tablet Cimetidin
Tablet Cimetidin dapat ditetapkan kadarnya secara spektrofotometri ultraviolet dengan pelarut HCL 0,01N ( Pharmacopeia of The People’s Republic of China ).
2.5 Tablet Cimetidin
Tablet cimetidin mengandung cimetidin C10H16N6S, tidak kurang dari
98,0% dan tidak lebih dari 102,0%dari jumlah yang tertera pada etiket (Farmakope Indonesia IV, 1995).
2.5.1 Penetapan Kadar Tablet Cimetidin
Tablet Cimetidin dapat ditetapkan kadarnya secara spektrofotometri ultraviolet dengan panjang gelombang serapan maksimum lebih kurang 218 nm dengan menggunakan larutan HCL 0,01 N sebagai blanko ( Pharmacopeia of The People’s Republic of China ).
2.6 Metode penetapan kadar Cimetidin 2.6.1 Spektrofotometri
Analisis spektrofotometri UV/Visibel merupakan salah satu teknik analisis spektroskopi yang telah lama dikenal dan banyak digunakan di berbagai laboratorium. Hampir sebagian besar laboratorium pengujian memiliki peralatan ini mulai dari yang sederhana atau portable yang bisa dibawa ke lapangan hingga yang telah dilengkapi sistem komputer sesuai dengan tujuan analisis dan aplikasi. Spektrofotometer sering digunakan karena mudah dioperasikan, waktu analisis relatif cepat, hasilnya memiliki ketelitian cukup memadai dan aplikasinya dapat menjangkau di berbagai bidang analisis (Sudjadi, 2007).
Menurut Dachriyanus (2004), Spektrofotometer UV-Visibel adalah pengukuran panjang gelombang dan intensitas sinar ultraviolet dan cahaya tampak yang diabsorbsi oleh sampel. Sinar ultaviolet berada pada panjang gelombang 200-400 nm, sedangkan sinar tampak berada pada panjang 400-800 nm. Sinar ultraviolet dan cahaya tampak memiliki energi yang cukup untuk memperoleh elektron pada kulit terluar ke tingkat energi yang lebih tinggi. Spektrum ini sangat berguna untuk pengukuran secara kuantitatif. Konsentrasi dari sampel di dalam larutan bisa ditentukan dengan mengukur absorban pada panjang gelombang tertentu dengan menggunakan hukum Lambert-Beer (Dachriyanus, 2004).
Hukum Lambert Beer adalah hukum yang menghubungkan linearitas antara absorban dengan konsentrasi larutan sampel. Hukum Lambert Beer biasanya ditulis dengan :
A = ε . b . C A = absorban (serapan)
ε = koefisien ekstingsi molar M-1cm-1 b = tebal kuvet (cm)
C = konsentrasi (M)
Hukum lambert-Beer menyatakan bahwa intensitas yang ditentukan oleh larutan zat penyerap berbanding lurus dengan tebal dan konsentrasi larutan. Dalam hukum Lambert-Beer ada beberapa pembatas yaitu:
- Sinar yang digunakan dianggap kromatis.
- Penyerapan terjadi dalam satu volume yang mempunyai penampang luas yang sama.
- Senyawa yang menyerap dalam larutan tersebut tidak tergantung terhadap senyawa lain di dalam larutan.
- Tidak terjadi peristiwa fluoresensi dan fosforesensi.
Spektofotometer yang sesuai untuk pengukuran di daerah spekrum ultraviolet dan cahaya tampak terdiri dari suatu sistem optik dengan kemampuan menghasilkan cahaya monokromatik dan jangkauan 200 nm hingga 800 nm. Dalam pemeriksaan ini larutan yang dianalisa harus bening, dimana tidak terdapat kotoran. Pada panjang gelombang 240 nm- 280 nm, kesalahan pengukuran tidak boleh ± 0,5. Pada panjang gelombang 280 nm- 320 nm, kesalahan pengukuran tidak boleh ± 1 nm. Serta tidak lebih dari ± 2 nm pada panjang gelombang di atas 320 nm. Spektrofotometer ultraviolet pada panjang gelombang lebih kecil dari 400 nm menggunakan pelarut yang dianalisis tidak berwarna. Sedangkan
spektrofotometer sinar tampak, larutan yang dianalisis memiliki warna (Depkes RI, 1979).
2.6.2 Instrumen
Suatu spektrofotometer tersusun dari sumber spektrum, monokromator, sel pengabsorbsi dan detektor (Khopkar, 1990).
- Sumber
Sumber yang biasa yang digunakan adalah lampu wolfram. Tetapi untuk daerah UV digunakan lampu hidrogen atau lampu deutrium. Kebaikan lampu wolfram adalah energi radiasi yang dibebaskan tidak bervariasi pada berbagai panjang gelombang (Khopkar, 1990).
- Monokromator
Digunakan untuk memperoleh sumber sinar yang monokromatis. Alatnya berupa prisma ataupun grating. Untuk mengarahkan sinar monokromatis yang diinginkan dari hasil penguraian dapat digunakan celah. Jika celah posisinya tetap maka prisma ataupun gratingnya yang dirotasikan untuk mendapatkan aaaa yang diinginkan (Khopkar, 1990).
Pada pengukuran di daerah tampak kuvet kaca dapat digunakan, tetapi untuk pengukuran pada daerah UV kita harus menggunakan sel kuarsa karena gelas tidak tembus cahaya pada daerah ini. Umumnya tebal kuvetnya adalah 10 mm, tetapi yang lebih kecil ataupun yang lebih besar dapat digunakan. Sel yang biasa digunakan berbentuk persegi, tetapi bentuk silinder dapat juga digunakan. Kita harus menggunakan kuvet yang bertutup untuk pelarut organik. Sel yang baik adalah kuarsa atau gelas hasil leburan serta seragam seluruhnya (Khopkar, 1990).
- Detektor
Peranan detektor penerima adalah memberikan respon terhadap cahaya pada berbagai panjang gelombang (Khopkar, 1990).