TUGAS DAN MAKALAH FORMULASI TEKHNOLOGI SEDIAAN STERIL (INJEKSI)
Untuk memenuhi sebagian persyaratan dalam menempuh Mata Kuliah Formulasi Tekhnologi Sediaan Steril
BAB I PENDAHULUAN 1.1.Latar Belakang
Saat ini berbagai bentuk sediaan obat dapat dijumpai dipasaran. Diantaranya adalah sediaan injeksi yang termasuk sediaan steril. Produk steril adalah sediaan teraseptis dalam bentuk terbagi yang bebas dari mikroorganisme hidup. Sediaan parenteral ini merupakan sediaan unik diantara bentuk sediaan obat terbagi, karena sediaan ini disuntikkan melalui kulit atau membran mukosa ke bagian dalam tubuh. Dan kemudian langsung menuju reseptor.
Sediaan tersebut harus bebas dari kontaminasi mikroba dan dari komponen toksik serta harus mempunyai tingkat kemurnian tinggi dan luar biasa. Dalam injeksi intravena memberikan beberapa keuntungan antara lain efek terapi lebih cepat didapat., dapat memastikan obat sampai pada tempat yang diinginkan, cocok unyuk keadaan darurat, untuk obat – obat yang rusak oleh cairan lambung
Sediaan injeksi merupakan sediaan yang sangat penting bagi dunia kesehatan. Karena pada keadaan sakit yang dianggap kronis, pemberian obat minum sudah tidak maksimal lagi , sehingga perlu dan sangat penting untuk di berikan sediaan injeksi, karena akan sangat membantu untuk mempercepat mengurangi rasa sakit pada pasien, sebab sediaan injeksi bekerja secara cepat, dimana obat langsung masuk ke dalam pembuluh darah dan akan bekerja secara optimal pada bagian yang sakit. Sediaan injeksi merupakan salah satu contoh sediaan steril , jadi keamanan dan kebersihan sediaan juga telah di uji.
1.2.RumusanMasalah
1.2.2 Bagaimana pengaruh alat dan bahan steril dalam sediaan injeksi mempengaruhi kualitas sediaan
1.3. Tujuan
1.3.1 Mahasiswa memahami pengertian sediaan steril, 1.3.2 Mahasiswa mengenal macam sediaan steril, 1.3.3 Mahasiswa mengenal proses sterilisasi.
1.3.4 Mengetahui cara membuat sediaan injeksi yang baik dan benar.
1.3.5 Dapat membedakan kualitas sediaan injeksi yang baik dengan yang kurang baik. 1.4. Manfaat
1.4.1 Mampu menerapkan cara membuat sediaan injeksi yang baik dan benar untuk meminimalisir kesalahan pada sediaan injeksi.
1.4.2 Mampu mengetahui kelarutan obat yang tepat dalam pembuatan injeksi.
BAB II
TINJAUAN PUSTAKA
2.1 Definisi
Menurut Farmakope Indonesia Edisi III, injeksi adalah sediaan steril berupa larutan, emulsi, suspensi atau serbuk yang harus dilarutkan atau disuspensikan terlebih dahulu sebelum digunakan, yang disuntikkan dengan cara merobek jaringan ke dalam kulit atau melalui kulit atau melalui selaput lendir.(FI.III.1979)
Sedangkan menurut Farmakope Indonesia Edisi IV, injeksi adalah injeksi yang dikemas dalam wadah 100 mL atau kurang. Umumnya hanya larutan obat dalam air yang bisa diberikan secara intravena. Suspensi tidak bisa diberikan karena berbahaya yang dapat menyebabkan penyumbatan pada pembuluh darah kapiler.(FI.IV.1995)
Sediaan steril injeksi dapat berupa ampul, ataupun berupa vial. Injeksi vial adalah salah satu bentuk sediaan steril yang umumnya digunakan pada dosis ganda dan memiliki kapasitas atau volume 0,5 mL – 100 mL. Injeksi vial pun dapat berupa takaran tunggal atau ganda dimana digunakan untuk mewadahi serbuk bahan obat, larutan atau suspensi
dengan volume sebanyak 5 mL atau pun lebih. (Anonim.Penuntun Praktikum Farmasetika I.2011)
Berdasarkan R.VOIGHT(hal 464) menyatakan bahwa, botol injeksi vial ditutup dengan sejenis logam yang dapat dirobek atau ditembus oleh jarum injeksi untuk menghisap cairan injeksi. Injeksi intravena memberikan beberapa keuntungan :
1. Efek terapi lebih cepat .
2. Dapat memastikan obat sampai pada tempat yang diinginkan. 3. Cocok untuk keadaan darurat.
4. Untuk obat-obat yang rusak oleh cairan lambung.
Sterilisasi adalah proses yang dirancang untuk menciptakan keadaan steril. Secara tradisional keaadan steril adalah kondisi mutlak yang tercipta sebagai akibat penghancuran dan penghilangan semua mikroorganisme hidup. Konsep ini menyatakan bahwa steril adalah istilah yang mempunyai konotasi relative, dan kemungkinan menciptakan kondisi mutlak bebas dari mikroorganisme hanya dapat diduga atas dapat proyeksi kinetis angka kematian mikroba.(Lachman hal.1254)
Dari beberapa pengertian tersebut dapat ditarik kesimpulan bahwa sediaan injeksi adalah sediaan steril berupa larutan, emulsi, suspensi atau serbuk yang harus dilarutkan atau disusupensikan terlebih dahulu sebelum digunakan secara perenteral, suntikan dengan cara menembus, atau merobek jaringan kedalam atau melalui kulit atau selaput lendir.
Sediaan steril untuk sedian perenteral digolongkan menjadi lima jenis yang berbeda yaitu :
a. Obat larutan, atau emulsi yang digunakan untuk injeksi ditandai dengan nama injeksi, contohnya adalah injeksi insulin.
b. Sediaan padat kering atau cairan pekat yang tidak mengandung dapar, pengencer atau bahan tambahan lain dan larutan yang diperoleh setelah penambahan pelarut yang memenuhi persyaratan injeksi. Sediaan ini dapat membedakannya dari nama bentuknya yaitu steril, contohnya Ampicilin Sodium steril.
c. Sediaan seperti tertera pada no 2, tetapi mengandung satu atau lebih dapar, pengencer atau bahan tambahan lain dan dapat dibedakan dari nama bentuknya.yaitu untuk injeksi, contohnya Methicillin Sodium untuk injeksi.
d. Sediaan berupa susupensi serbuk dalam medium cair yang sesuai dan tidak disuntikkansacara intravena atau di dalam saluran spinal, dan dapat dibedakan dari nama bentuknya yaitu susupensi steril. Contoh Cortisao Suspensi steril.
e. Sediaan padat kering dengan bahan pembawa yang sesuai membentuk larutan yang memenuhi semua persyaratan untuk suspensi steril setelah penambahan pembawanya yang sesuai. Dan dapat membedakannya dari nama bentuknya yaitu steril untuk suspensi. Contohnya Ampicilin steril untuk suspensi.
2.2 Rute-rute Injeksi 1. Parenteral Volume Kecil
a. Intradermal
Istilah intradermal (ID) berasal dari kata "intra" yang berarti lipis dan "dermis" yang berarti sensitif, lapisan pembuluh darah dalam kulit. Ketika sisi anatominya mempunyai derajat pembuluh darah tinggi, pembuluh darah betul-betul kecil. Makanya penyerapan dari injeksi disini lambat dan dibatasi dengan efek sistemik yang dapat dibandingkan karena absorpsinya terbatas, maka penggunaannya biasa untuk aksi lokal dalam kulit untuk obat yang sensitif atau untuk menentukan sensitivitas terhadap mikroorganisme. b. Intramuskular
Istilah intramuskular (IM) digunakan untuk injeksi ke dalam obat. Rute intramuskular menyiapkan kecepatan aksi onset sedikit lebih normal daripada rute intravena, tetapi lebih besar daripada rute subkutan.
c. Intravena
Istilah intravena (IV) berarti injeksi ke dalam vena. Ketika tidak ada absorpsi, puncak konsentrasi dalam darah terjadi dengan segera, dan efek yang diinginkan dari obat diperoleh hampir sekejap.
d. Subkutan
Subkutan (SC) atau injeksi hipodermik diberikan di bawah kulit. Parenteral diberikan dengan rute ini mempunyai perbandingan aksi onset lambat dengan absorpsi sedikit daripada yang diberikan dengan IV atau IM.
e. Rute intra-arterial
disuntikkan langsung ke dalam arteri, digunakan untuk rute intravena ketika aksi segera diinginkan dalam daerah perifer tubuh.
f. Intrakardial
Disuntikkan langsung ke dalam jantung, digunakan ketika kehidupan terancam dalam keadaan darurat seperti gagal jantung.
g. Intraserebral
Injeksi ke dalam serebrum, digunakan khusus untuk aksi lokal sebagaimana penggunaan fenol dalam pengobatan trigeminal neuroligia.
h. Intraspinal
Injeksi ke dalam kanal spinal menghasilkan konsentrasi tinggi dari obat dalam daerah lokal. Untuk pengobatan penyakit neoplastik seperti leukemia.
i. Intraperitoneal dan intrapleural
Merupakan rute yang digunakan untuk pemberian berupa vaksin rabies. Rute ini juga digunakan untuk pemberian larutan dialisis ginjal.
j. Intra-artikular
Injeksi yang digunakan untuk memasukkan bahan-bahan seperti obat antiinflamasi secara langsung ke dalam sendi yang rusak atau teriritasi.
k. Intrasisternal dan peridual
Injeksi ke dalam sisterna intracranial dan durameter pada urat spinal. Keduanya merupakan cara yang sulit dilakukan, dengan keadaan kritis untuk injeksi.
l. Intrakutan (i.c)
Injeksi yang dimasukkan secara langsung ke dalam epidermis di bawah stratum corneum. Rute ini digunakan untuk memberi volume kecil (0,1-0,5 ml) bahan-bahan diagnostik atau vaksin.
m. Intratekal
Larutan yang digunakan untuk menginduksi spinal atau anestesi lumbar oleh larutan injeksi ke dalam ruang subarachnoid. Cairan serebrospinal biasanya diam pada mulanya untuk mencegah peningkatan volume cairan dan pengaruh tekanan dalam serabut saraf spinal. Volume 1-2 ml biasa digunakan. Berat jenis dari larutan dapat diatur untuk membuat anestesi untuk bergerak atau turun dalam kanal spinal, sesuai keadaan tubuh pasien.
Untuk pemberian larutan volume besar, hanya rute intravena dan subkutan yang secara normal digunakan.
a. Intravena
Keuntungan rute ini adalah
jenis-jenis cairan yang disuntikkan lebih banyak dan bahkan bahan tambahan banyak digunakan IV daripada melalui SC
cairan volume besar dapat disuntikkan relatif lebih cepat efek sistemik dapat segera dicapai
level darah dari obat yang terus-menerus disiapkan
kebangkitan secara langsung untuk membuka vena untuk pemberian obat rutin dan menggunakan dalam situasi darurat disiapkan.
Kerugiannya adalah meliputi :
gangguan kardiovaskuler dan pulmonar dari peningkatan volume cairan dalam sistem sirkulasi mengikuti pemberian cepat volume cairan dalam jumlah besar;
perkembangan potensial trombophlebitis;
kemungkinan infeksi lokal atau sistemik dari kontaminasi larutan atau teknik injeksi septik
pembatasan cairan berair. b. Subkutan
Penyuntikan subkutan (hipodermolisis) menyiapkan sebuah alternatif ketika rute intravena tidak dapat digunakan. Cairan volume besar secara relatif dapat digunakan tetapi injeksi harus diberikan secara lambat. Dibandingkan dengan rute intravena, absorpsinya lebih lambat, lebih nyeri dan tidak menyenangkan, jenis cairan yang digunakan lebih kecil (biasanya dibatasi untuk larutan isotonis) dan lebih terbatas zat tambahannya.
2.3 Keuntungan injeksi
a. Respon fisiologis yang cepat dapat dicapai segera bila diperlukan, yang menjadi pertimbangan utama dalam kondisi klinik seperti gagal jantung, asma, shok.
b. Terapi parenteral diperlukan untuk obat-obat yang tidak efektif secara oral atau yang dapat dirusak oleh saluran pencernaan, seperti insulin, hormon dan antibiotik.
c. Obat-obat untuk pasien yang tidak kooperatif, mual atau tidak sadar harus diberikan secara injeksi.
d. Bila memungkinkan, terapi parenteral memberikan kontrol obat dari ahli karena pasien harus kembali untuk pengobatan selanjutnya. Juga dalam beberapa kasus, pasien tidak dapat menerima obat secara oral.
e. Penggunaan parenteral dapat menghasilkan efek lokal untuk obat bila diinginkan seperti pada gigi dan anestesi.
f. Dalam kasus simana dinginkan aksi obat yang diperpanjang, bentuk parenteral tersedia, termasuk injeksi steroid periode panjang secara intra-artikular dan penggunaan penisilin periode panjang secara i.m.
g. Terapi parenteral dapat memperbaiki kerusakan serius pada keseimbangan cairan dan elektrolit.
h. Bila makanan tidak dapat diberikan melalui mulut, nutrisi total diharapkan dapat dipenuhi melalui rute parenteral.
i. Aksi obat biasanya lebih cepat. j. Seluruh dosis obat digunakan.
k. Beberapa obat, seperti insulin dan heparin, secara lengkap tidak aktif ketika diberikan secara oral, dan harus diberikan secara parenteral.
l. Beberapa obat mengiritasi ketika diberikan secara oral, tetapi dapat ditoleransi ketika diberikan secara intravena, misalnya larutan kuat dektrosa.
m. Jika pasien dalam keadaan hidrasi atau shok, pemberian intravena dapat menyelamatkan hidupnya.
2.4 Kerugian Injeksi
a. Bentuk sediaan harus diberikan oleh orang yang terlatih dan membutuhkan waktu yang lebih lama dibandingkan dengan pemberian rute lain
b. Pada pemberian parenteral dibutuhkan ketelitian yang cukup untuk pengerjaan secara aseptik dari beberapa rasa sakit tidak dapat dihindari
c. Obat yang diberikan secara parenteral menjadi sulit untuk mengembalikan efek fisiologisnya.
d. Yang terakhir, karena pada pemberian dan pengemasan, bentuk sediaan parenteral lebih mahal dibandingkan metode rute yang lain.
e. Beberapa rasa sakit dapat terjadi seringkali tidak disukai oleh pasien, terutama bila sulit untuk mendapatkan vena yang cocok untuk pemakaian i.v.
f. Dalam beberapa kasus, dokter dan perawat dibutuhkan untuk mengatur dosis.
g. Sekali digunakan, obat dengan segera menuju ke organ targetnya. Jika pasien hipersensitivitas terhadap obat atau overdosis setelah penggunaan, efeknya sulit untuk dikembalikan lagi.
h. Pemberian beberapa bahan melalui kulit membutuhkan perhatian sebab udara atau mikroorganisme dapat masuk ke dalam tubuh. Efek sampingnya dapat berupa reaksi phlebitis, pada bagian yang diinjeksikan.
2.5 Komposisi Injeksi 1. Bahan aktif
Data zat aktif yang diperlukan (Preformulasi) a. Kelarutan
terutama data kelarutan dalam air dari zat aktif sangat diperlukan, karena bentuk larutan air paling dipilih pada pembuaan sediaan steril. Data kelarutan ini diperlukan untuk menentukan bentuk sediaan. Zat aktif yang larut air membentuk sediaan larutan dalam air, zat aktif yang larut minyak dibuat larutan dalam pembawa minyak. Sedangkan zat yang tidak larut dalam kedua pembawa tersebut dibuat sediaan suspensi. Jika zat aktif tidak larut dalam air ada beberapa alternatif yang dapat diambil sebelum memutuskan untuk membuat sediaan suspensi atau larutan minyak yaitu dengan mencari bentuk garam dari zat aktif, melakukan reaksi penggaraman, atau dicari bentuk kompleksnya
b. pH stabilita
pH stabilita adalah pH dimana penguraian zat aktif paling minimal, sehingga diharapkan kerja farmakologinya optimal. pH stabilita dicapai dengan menambahkan asam encer, basa lemah atau dapar.
c. Stabilitas zat aktif
Data ini membantu menentukan jenis sediaan, jenis bahan pembawa, metoda sterilisasi atau cara pembuatan. Beberapa factor yang mempengaruhi penguraian zat aktif adalah: Oksigen (Oksidasi) Pada kasus ini, setelah air dididihkan maka perlu dialiri gas
Air (Hidrolisis) Jika zat aktif terurai oleh air dapat dipilih alternatif : - Dibuat pH stabilitanya dengan penambahan asam/basa atau buffer - Memilih jenis pelarut dengan polaritas lebih rendah daripada air, seperti campuran pelarut air-gliserin-propilenglikol atau pelarut campur lainnya. - Dibuat dalam bentuk kering dan steril yang dilarutkan saat disuntikkan.
Suhu Jika zat aktif tidak tahan panas dipilih metode sterilisasi tahan panas, seperti filtrasi.
Cahaya Pengaruh cahaya matahari dihindari dengan penggunaan wadah berwarna cokelat.
d. Tak tersatukannya (homogenitas) zat aktif ,
Baik ditinjau dari segi kimia, fisika, atau farmakologi. e. Dosis
Data ini menentukan tonisitas larutan dan cara pemberian. f. Rute pemberian
Rute pemberian yang akan digunakan akan berpengaruh pada formulasi, dalam hal: Volume maksimal sediaan yang dapat diberikan pada rute tersebut (Lihat datanya pada bagian rute pemberian).
Pemilihan pelarut disesuaikan dengan rute pemberian
Isotonisitas dari sediaan juga dipengaruhi oleh rute pemberian. Pada larutan intravena isotonisitas menjadi kurang penting selama pemberian dilakukan dengan perlahan untuk memberikan waktu pengenceran dan ’adjust’ oleh darah. Injeksi intraspinal mutlak harus isotonis.
2. Bahan tambahan
a. Antioksidan : Garam-garam sulfurdioksida, termasuk bisulfit, metasulfit dan sulfit adalah yang paling umum digunakan sebagai antioksidan. Selain itu digunakan :Asam askorbat, Sistein, Monotiogliseril, Tokoferol.
b. Bahan antimikroba atau pengawet : Benzalkonium klorida, Benzil alcohol, Klorobutanol, Metakreosol, Timerosol, Butil p-hidroksibenzoat, Metil p-hidroksibenzoat, Propil p-hidroksibenzoat, Fenol.
c. Buffer : Asetat, Sitrat, Fosfat.
e. Gas inert : Nitrogen dan Argon.
f. Bahan penambah kelarutan (Kosolven) : Etil alcohol, Gliserin, Polietilen glikol, Propilen glikol, Lecithin
g. Surfaktan : Polioksietilen dan Sorbitan monooleat. h. Bahan pengisotonis : Dekstrosa dan NaCl
i. Bahan pelindung : Dekstrosa, Laktosa, Maltosa dan Albumin serum manusia. j. Bahan penyerbuk : Laktosa, Manitol, Sorbitol, Gliserin.
3. Bahan Pembawa
Bahan pembawa injeksi dapat berupa air maupun non air. Sebagian besar produk parenteral menggunakan pembawa air. Hal tersebut dikarenakan kompatibilitas air dengan jaringan tubuh, dapat digunakan untuk berbagai rute pemberian, air mempunyai konstanta dielektrik tinggi sehingga lebih mudah untuk melarutkan elektrolit yang terionisasi dan ikatan hydrogen yang terjadi akan memfasilitasi pelarutan dari alkohol, aldehid, keton, dan amin.
Syarat air untuk injeksi menurut USP : Harus dibuat segar dan bebas pirogen
Tidak mengndung lebih dari 10 ppm dari total zat padat. pH antara 5-7
Tidak mengandung ion-ion klorida, sulfat, kalsium dan amonium, karbondioksida, dan kandungan logam berat serta material organik (tanin, lignin), partikel berada pada batas yang diperbolehkan.
a) Air Pro Injeksi
Aqua bidest dengan pH tertentu, tidak mengandung logam berat (timbal, Besi, Tembaga), juga tidak boleh mengandung ion Ca, Cl, NO3, SO4, amonium, NO2, CO3. Harus steril dan penggunaan diatas 10 ml harus bebas pirogen. Aqua steril Pro Injeksi adalah air untuk injeksi yang disterilisasi dan dikemas dengan cara yang sesuai, tidak mengandung bahan antimikroba atau bahan tambahan lainnya
Cara pembuatan : didihkan air selama 30 menit dihitung dari setelah air mendidih di atas api lalu didinginkan. Cara : Aqua p.i + karbon aktif 0,1% dari volume, dipanaskan 60-70oC selama 15 menit. Tidak boleh menggunakan Aqua DM karena ada zat-zat
organik yang tidak bermuatan dapat lolos, ditanggulangi dengan filtrasi karbon adsorben dan filtrasi bakteri.
Air Pro Injeksi Bebas CO2
CO2 mampu menguraikan garam natrium dari senyawa organic seperti barbiturate dan sulfonamide kembali membentuk asam lemahnya yang mengendap. Cara pembuatan : Mendidihkan air p.i selama 20-30 menit lalu dialiri gas nitrogen sambil didinginkan. (Rep. Tek Fa. Steril hal 4)
Air Pro Injeksi bebas O2
Dibuat dengan mendidihkan air p.i selama 20-30 menit dan pada saat pendinginannya dialiri gas nitrogen. Dipakai untuk melarutkan zat aktif yang mudah teroksidasi, seperti apomorfin, klorfeniramin, klorpromazin, ergometrin, ergotamine, metilergotamin, proklorperazin, promazin, promesatin HCl, sulfamidin, turbokurarin.
b) Pembawa Non Air
Pembawa non air digunakan jika: Zat aktif tidak larut dalam air Zat aktif terurai dalam air
Diinginkan kerja depo dalam sediaan Syarat umum pembawa non air . Tidak toksik, tidak mengiritasi dan menyebabkan sensitisasi
Dapat tersatukan dengan zat aktif Inert secara farmakologi
Stabil dalam kondisi di mana sediaan tersebut biasa digunakan
Viskositasnya harus sedemikian rupa sehingga dapat disuntikan dengan muda Harus tetap cair pada rentang suhu yang cukup lebar
Mempunyai titik didih yang tinggi sehingga dapat dilakukan sterilisasi dengan panas Dapat bercampur dengan air atau cairan tubuh
2.6 Syarat-syarat Injeksi
a. Bebas dari mikroorganisme, steril atau dibuat dari bahan-bahan steril di bawah kondisi yang kurang akan adanya kombinasi mikroorganisme (proses aseptik).
c. Bahan-bahan yang bebas dari bahan asing dari luar yang tidak larut. d. Sterilitas
e. Bebas dari bahan partikulat f. Bebas dari Pirogen
g. Kestabilan
h. Injeksi sedapat mungkin isotonis dengan darah. 2.7 Wadah Injeksi
Wadah untuk injeksi termasuk penutup tidak boleh berinteraksi melalui berbagai cara baik secara fisik maupun kimiawi dengan sediaan, yang dapat mengubah kekuatan, mutu atau kemurnian di luar persyaratan resmi dalam kondisi biasa pada waktu penanganan, pengangkutan, penyimpanan, penjualan, dan penggunaan. Wadah terbuat dari bahan yang dapat mempermudah pengamatan terhadap isi. Tipe kaca yang dianjurkan untuk tiap sediaan umumnya tertera dalam masing-masing monografi. (FI Ed. IV, hal 10).
Wadah dan sumbatnya tidak boleh mempengaruhi bahan yang disimpan di dalamnya baik secara kimia maupun secara fisika, yang dapat mengakibatkan perubahan khasiat, mutu dan kemurniannya. (FI ed. III, hal XXXIV)
Bagaimanapun bentuk dan komposisi wadah, wadah pengemas merupakan sumber dari masalah stabilitas sediaan, bahan partikulat, dan sumber pirogen. (Diktat Steril, hal 82)
Ada dua tipe utama wadah untuk injeksi yaitu dosis tunggal dan dosis ganda. Wadah dosis tunggal yang paling sering digunakan adalah ampul dimana kisaran ukurannya dari 1-100 ml. pada kasus tertentu, wadah dosis ganda dan sebagainya berupa vial serum atau botol serum. Kapasitas vial serum 1-50 ml, bentuknya mirip ampul tetapi disegel dengan pemanasan. Ditutup dengan penutup karet spiral. Botol serum juga dapat sebagai botol tipe army dengan kisaran ukuran dari 75-100 ml dan memiliki mulut yang lebar dimana ditutup dengan penutup karet spiral. Labu atau tutup yang lebih besar mengandung 250-2000 ml, digunakan untuk cairan parenteral yang besar seperti NaCl isotonis.
Gelas digunakan untuk sediaan parenteral dikelompokkan dalam tipe I, Tipe II, dan Tipe III (tabel 8). Tipe I adalah mempunyai derajat yang paling tinggi, disusun hampir ekslusif dan barosilikat (silikon dioksida), membuatnya resisten secara kimia terhadap kondisi asam dan basa yang ekstrim. Gelas tipe I, meskipun paling mahal, ini lebih disukai untuk produk terbanyak yang digunakan untuk pengemasan beberapa parenteral. Gelas tipe II adalah gelas soda-lime (dibuat dengan natrium sulfit atau sulfida untuk menetralisasi permukaan alkalinoksida), sebaliknya gelas tipe III tidak dibuat dari gelas soda lime. Gelas tipe II dan III digunakan untuk serbuk kering dan sediaan parenteral larutan berminyak. Tipe II dapat digunakan untuk produk dengan pH di bawah 7,0 sebaik sediaan asam dan netral. USP XXII memberikan uji untuk tipe-tipe gelas berbeda.
Formulator harus mengetahuidan sadar bahwa masing-masing tipe gelas adalah berbeda dan level bahan tambahannya (boron, sodium, potassium, kalsium, besi, dan magnesium) yang berefek terhadap sifat kimia dan fisika. Oleh karena itu, formulator sebaiknya mempunyai semua informasi yang diperlukan dari pembuatan gelas untuk memastikan bahwa formulasi gelas adalah konsisten dan dari batch dan spesifikasi bahan tambahan adalah konsisten ditemukan.
Gelas untuk parenteral volume kecil – Tabel 8
Tipe Definisi Umum Test USP Batas
Ukuran (ml) ml 0,02 N asam I Paling resisten, gelas borosilikat Gelas serbuk Semua 1,0 II Gelas dibuat dari soda lime
Attack water 100 atau kurang lebih 100 0,7 0,2 III Gelas soda lime Gelas
serbuk
Semua 8,5
IV Gelas soda lime-tujuan umum
Gelas serbuk
Semua 15,0
Wadah gelas ambar digunakan untuk produk yang sensitif terhadap cahaya. Warna ambar dihasilkan dengan penambahan besi dan mangan oksida untuk formulasi gelas. Namun demikian, dapat leach ke dalam formulasi dan mempercepat reaksi oksidasi.
Keuntungan wadah gelas :
1. mempunyai daya tahan kimia yang baik sehingga tidak bereaksi dengan kandungan wadah dan tidak mengabsorbsi atau mengeluarkan senyawa organik.
2. Bersifat tidak permeable sehingga apabila ditutup dengan baik maka pemasukan atau hilangnya gas-gas dapat diabaikan.
3. Wadah gelas mudah dicuci karena permukannya licin
4. Bersifat transparan sehingga dapat diamati kandungnnya dalam wadah.
5. Mempunyai sifat kaku, kuat dan bentuknya stabil. Tahan terhadap tusukan dapat divakumkan, dapat dipanaskan pada suhu 121O C pada sterilisasi uap dan 2600 C pada sterilisasi kering tanpa mengalami perubahan bentuk.
Kerugian wadah gelas:
1. mudah pecah dan bobotnya relatif berat.
Wadah yang biasa digunakan untuk sedian injeksi adalah berupa vial atau ampul. Untuk zat aktif yang mudah teroksidasi biasanya digunakan ampul berwarna gelap (biasanya coklat) untuk melindungi sediaan dari cahaya.
Gelas tipe I untuk membuat wadah tiup dalam bentuk tabung, misalnya vial, ampul, badan alat suntik (syringe) dan bagian infus set. Beberapa sediaan parenteral volume kecil dikemas dalam alat suntik gelas sekali pakai (disposable one-trip glass syringe). 2. Karet
Formulasi karet digunakan dalam sediaan parenteral volume kecil untuk penutup vial dan catridge dan penutup untuk pembedahan. Formulasi ini betul-betul kompleks. Tidak hanya mereka mengandung basis polimer karet, tetapi juga banyak bahan tambahan seperti bahan pelunak, pelunak, vulkanishing, pewarna, aktivator dan percepatan, dan antioksidan. Banyak bahan-bahan tambahan ini tidak dikarakteristikkan untuk isi atau pemurnian dan dapat bersumber dari masalah degradasi fisika dan kimia dalam produk parenteral. Seperti gelas, formulator harus bekerja dengan tertutup dengan pembuat karet untuk memilih formulasi karet yang tepat dengan spesifikasi tetap dan karakteristik untuk mempertahankan kestabilan produk.
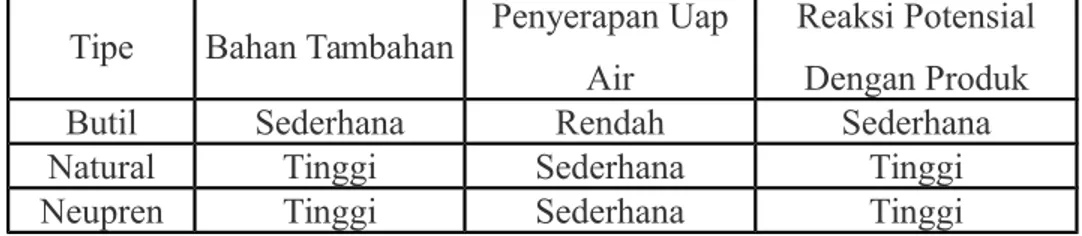
Paling banyak polimer karet digunakan dalam penutup sediaan parenteral volume kecil adalah alami dan butil karet dengan silikon dan karet neopren digunakan jarang. Butil karet lebih disukai karena ini diinginkan sedikit bahan tambahan, mempunyai penyerapan uap air rendah (oleh karena itu, baik untuk serbuk kering steril sensitif
terhadap kelembaban) dan sifat sederhana dengan penghormatan penyerapan gas dan reaktivitas dengan produk farmasetik.
Masalah dengan penutup karet termasuk leaching bahan ke dalam produk, penyerapan bahan aktif atau pengawet antimikroba oleh elastomer dan coring karet oleh pengulangan insersi benang. Coring menghasilkan partikel karet yang berefek terhadap kualitas dan keamanan potensial produk.
Silikonisasi penutp karet adalah umum dilakukan untuk memfasilitasi pergerakan karet melalui peralatan sepanjang proses dan peletakan ke dalam vial. Akan tetapi, silikon tidak bercampur dengan obat hidrofilik, khususnya protein. Kontak yang luar biasa dengan karet tersilikonisasi dapat menghasilkan agregasi protein. Pembuatan elastomer mempunyai perkembangan formulasi yang tidak menginginkan penggunaan silikon untuk menggunakan dalam operasi produksi kecepatan tinggi.
3. Plastik
Pengemasan plastik adalah sangat penting untuk bentuk sediaan mata yang diberikan oleh botol plastic fleksibel, orang yang bersangkutan memeras untuk mengeluarkan tetesan larutan steril, suspensi atau gel. Wadah plastic parenteral volume kecil lain dari produk mata menjadi lebih luas dipakai karena pemeliharaan harga, eliminasi kerusakan gelas dari kenyamanan penggunaan. Seperti formulasi karet, formulasi plastik dapat berinteraksi dengan produk, menyebabkan masalah fisika dan kimia. Formulasi plastik adalah sedikit. Kompleks daripada karet dan cenderung mempunyai potensial lebih rendah untuk bahannya. Paling umum digunakan plastik polimer untuk sediaan mata adalah polietilen densitas rendah. Untuk sediaan parenteral volume kecil yang lain, formulasi polyolefin lebih luas digunakan sebaik polivinil klorida, polipropilen, poliamida (nilon), polikarbonat dan kopolimer (seperti etilen-vinil asetat).
Tabel 9- Komponen karet Dapat Diautoklaf Digunakan Dalam Sediaan Parenteral Volume Kecil
Tipe Bahan Tambahan Penyerapan Uap Air
Reaksi Potensial Dengan Produk
Butil Sederhana Rendah Sederhana
Natural Tinggi Sederhana Tinggi
Polisopren Tinggi Sederhana Sederhana
Silikon Sederhana Sangat tinggi Rendah
4. Container / wadah
Tipe wadah yang paling umum digunakan untuk sediaan parenteral volume kecil adalah gelas atau vial polietilen dengan penutup karet dan besi. Gelas ampul digunakan paling banyak untuk sistem pengemasan parenteral volume kecil, tetapi jarang digunakan sekarang karena masalah aprtikel gelas ketika leher ampul dibuka. Masing-masing pembedahan dan wadah catridge mempunyai peningkatan popularitas dan penggunaan karena kenyamanan mereka dibandingkan vial dan ampul. Vial dan ampul menginginkan kemunduran produk dari kemasan. Injeksi, sebaliknya produk-produk dalam pembedahan dan catridge adalah siap untuk diberikan. Keduanya digunakan untuk parenteral volume besar (LVP).
Wadah plastik digunakan untuk penggunaan produk mata. Salep dengan tube logam digunakan untuk kemasan salep mata steril.
2.8 Cara Penyegelan Ampul
Ampul dapat ditutup dengan melelehkan bagian gelas dari leher ampul sehingga membentuk segel penutup atau segel tarik. Segel penutup dibuat dengan melelehkan sebagian gelas pada bagian atas leher ampul bulatan gelas dan menutup bagian yang terbuka. Segel tarik dibuat dengan memanaskan leher dari suatu ampul yang berputar di daerah ujungnya kemudian menarik ujungnya hingga membentuk kapiler kecil yang dapat diputar sebelum bagian yang meleleh tersebut ditutup.
2.9 Cara Pengisian Ampul.
Untuk pengisian ampul, jarum hipodermik panjang adalah penting karena lubangnya kecil. Jarum harus dimasukkan ke dalam ampul sampai di bawah. Leher ampul, tetapi tidak cukup jauh untuk masuk ke dalam larutan yang dimasukkan ke dalam ampul. Jarum harus dikeluarkan dari ampul tanpa menggunakan tetes larutan pada dinding primer dari leher ampul. Metode ini digunakan untuk mencegah pengurangan dan pengotoran jika ampul disegel.
2.10 Evaluasi
Dilakukan setelah sediaan disterilkan dan sebelum wadah dipasang etiket dan dikemas 2.10.1 Evaluasi Fisika
Bahan Partikulat dalam Injeksi <751> ( FI> ed IV, hal. 981-984). Penetapan Volume Injeksi Dlam Wadah <1131> (FI ed. IV Hal 1044). Uji Keseragaman Bobot dan Keseragaman Volume (FI ed III hal. 19) Uji Kejernihan Larutan (FI ED. IV, hal 998)
Uji Kebocoran (Goeswin Agus, Larutan Parenteral)
Pada pembuatan kecil-kecilan hal ini dapat dilakukan dengan mata tetapi untuk produksi skala besar hal ini tidak mungkin dikerjakan.
Wadah-wadah takaran tunggal yang masih panas setelah selesai disterilkan dimasukkan kedalam larutan biru metilen 0,1%. Jika ada wadah-wadah yang bocor maka larutan biru metilen akan dimasukkan kedalamnya karena perbedaan tekanan di luar dan di dalam wadah tersebut. Cara ini tidak dapat dilakukan untuk larutan-larutan yang sudah berwarna.
Wadah-wadah takaran tunggal disterilkan terbalik, jika ada kebocoran maka larutan ini akan keluar dari dalam wadah. Wadah-wadah yang tidak dapat disterilkan, kebocorannya harus diperiksa dengan memasukkan wadah-wadah tersebut ke dalam eksikator yang divakumkan. Jika ada kebocoran akan diserap keluar.
Uji Kejernihan dan Warna ( Goeswin Agus, Larutan Parenteral, HAL 201)
Umumnya setiap larutan suntik harus jernih dan bebas dari kotoran-kotoran. Uji ini sangat sulit dipenuhi bila dilakukan pemeriksaan yang sangat teliti karena hampir tidak ada larutan jernih. Oleh sebab itu untuk uji ini kriterianya cukup jika dilihat dengan mata biasa saja yaitu menyinari wadah dari samping dengan latar belakang berwarna hitam dan putih. Latar belakang warna hitam dipakai untuk menyelidiki kotoran-kotoran berwarna muda, sedangkan latar belakang putih untuk menyelidiki kotoran-kotoran berwarna gelap.
2.10.2 Evaluasi Biologi
Uji Efektivitas Pengawet Antimikroba <61> (FI ed IV, HAL 854-855) Uji Sterilitas <71> (FI ed. IV, HAL 855-863)
Uji Pirogen <231> (FI ed. IV, HAL. 908-909)
Uji Kandungan Zat Antimikroba <441> (FI ed. IV, HAL. 939-942) 2.10.3 Evaluasi Kimia
Uji Identifikasi (Sesuai dengan monografi sediaan masing-masing) Penetapan Kadar (Sesuai dengan monografi sediaan masing-masing
2.11 Penandaaan
Pada etiket tertera nama sediaan, untuk sediaan cair tertera persentase atau jumlah zat aktif dalam volume tertentu, cara pemberian, kondisi penyimpanan dan tanggal kadaluarsa, nama pabrik pembuat dan atau pengimpor serta nomor lot atau bets yang menunjukkan identitas. Nomor lot dan nomor bets dapat memberikan informasi tentang riwayat pembuatan lengkap meliputi seluruh proses pengolahan, sterilisasi, pengisian, pengemasan, dan penandaan.
Bila dalam monografi tertera berbagai kadar zat aktif dalam sediaan parenteral volume besar, maka kadar masing-masing komponen disebut dengan nama umum misalnya injeksi Dekstrosa 5% atau Injeksi Dekstrosa (5%).
Bila formula lengkap tidak tertera dalam masing-masing monografi, Penandaan mencakup informasi berikut :
1. Untuk sediaan cair, persentase isi atau jumlah tiap komponen dalam volume tertentu, kecuali bahan yang ditambahkan untuk penyesuaian pH atau untuk membuat larutan isotonik, dapat dinyatakan nama dan efek bahan tersebut
2. Sediaan kering atau sediaan yang memerlukan pengenceran sebelum digunakan, jumlah tiap komponen, komposisi pengencer yang dianjurkan, jumlah yang diperlukan untuk mendapat konsentrasi tertentu zat aktif dan volume akhir larutan yang diperoleh , uraian singkat pemerian larutan terkonstitusi, cara penyimpanan dan tanggal kadualarsa.
Pemberian etiket pada wadah sedemikian rupa sehingga sebagian wadah tidak tertutup oleh etiket, untuk mempermudah pemeriksaan isi secara visual.
2.12 Pengemasan dan Penyimpanan
Volume injeksi wadah dosis tunggal dapat memberikan jumlah tertentu untuk pemakaian parenteral sekali pakai dan tidak ada yang memungkinkan pengambilan isi dan pemberian 1 liter. (FI Ed. IV, Hal 11)
Untuk penyimpanan obat harus disimpan sehingga tercegah cemaran dan penguraian, terhindar pengaruh udara, kelembaban, panas dan cahaya.
Kondisi penyimpanan tergantung pada sediaannya, misalnya kondisi harus disimpan terlindung cahaya, disimpan pada suhu kamar, disimpan di tempat sejuk, disimpan di temapat dingin (FI Ed. III, Hal XXXIV)
BAB III
PRAFORMULASI DAN FORMULASI
3.1 Praformulasi
Praformulasi sangat penting dilakukan dalam setiap pengembangan sediaan farmsi karena meliputi penelitian farmasetik dan analitik bahan obat untuk menunjang proses pengembangan formulasi.
Sifat suatu sediaan dapat mempengaruhi secara bermakna kecepatan onset efek terapi dari suatu obat, lamanya efek tersebut, dan bentuk pola absorbsi yang dicapai. Oleh karena itu pengembangan praformulasi dan formulasi untuk suatu produk steril harus diintregasikan secara hati – hati dengan pemberian yang dimaksud pada seorang pasien.
Sifat kimia dan fisika suatu obat harus ditentukan, interaksinya dengan tiap bahan yang diinginkan harus dikaji, dan efek dari masing - masing tahap kestabilannya harus diselidiki dan dimengerti.
Semua komponen harus memiliki kualitas yang sangat baik. Kontaminasi fisika dan kimia tidak hanya menyebabkan iritasi kejaringan tubuh, tetapi jumlah kontaminasi yang sangat kecil tersebut juga dapat menyebabkan degradasi produk sebagai hasil dari perubahan kimia, khususnya selama waktu pemanasan bila digunakan sterilisasi panas.
3.1.1 Cakupan studi praformulasi untuk sediaan injeksi. a. Organoleptis
Oragnoleptis adalah studi praformulasi yang harus dilakukan untuk mengetahui pemerian zat aktif terdiri dari warna, bentuk, aroma dan rasa zat aktif dengan menggunakan terminologi deskriptif. Uji organoleptis sangat berguna dalam melakukan identifikasi awal mengenai suatu zat yang akan dibuat suatu sediaan. Uji ini dilakukan dengan tujuan mengetahui bentuk dari bahan yang akan digunakan dalam formulasi, agar tidak salah dalam mengambil bahan-bahan untuk formulasi. Dalam menentukan zat yang akan digunakan, dapat mengamatinya dari segi bentuk, warna, rasa juga aroma.
Warna memegang peranan penting dalam identifikasi suatu sediaan sebelum membuat suatu sediaan injeksi. Karena hal yang akan dilihat pertama kali adalah warna dari bahan-bahan itu.Warna biasanya merupakan fungsi inheren kimia obat karena terkait dengan ketidakjenuhan. Intensitas warna terkait dengan keberadaan konjugasi ketidakjenuhan di samping keberadaan khromofor , seperti –NH2, -NO2 dan –CO- (keton) yang mengintensifkan warna.
2. Bentuk
Bentuk juga memegang peranan yang sangat penting dalam identifikasi. Setelah menentukan warna, biasanya yang dilihat terlebih dahulu adalah bentuk dari bahan itu. Sehingga akan benar-benar yakin bahwa yang digunakan dalam formulasi adalah bahan-bahan yang tepat.
3. Bau / Aroma
Sebagian zat memiliki aroma yang khas dan kemungkinan bau yang inheren (terkait) dengan keberadaan gugus fugsional yang terdapat dalam molekul obat. Adakalanya zat sama sekali tidak berbau atau dapat pula berbau pelarut residu pelarut. Hal ini penting karena dalam farmakope ada ketentuan batas maksimal pelarut yang diperbolehkan ada dalam obat (terutama karena alas an toksisitas).
Dengan uji organoleptis, dapat mempermudah identifikasi suatu bahan. Terutama bahan yang mengandung aroma yang khas.
Daftar beberapa istilah organoleptik dalam FI Ed. IV.
Warna Rasa Aroma Bentuk
Putih Hampir putih Putih kekuningan Kuning Kuning pucat Kuning kecoklatan Krem Krem pucat Keabu-abuan Asam Asin Pahit Manis Membakar Dingin Pedas Tidak berasa Sedikit pahit
Sedikit beraroma cuka Aroma Khas
Aroma menusuk Aroma aromatik Aroma lemah
Aroma seperti sulfida Praktis tidak beraroma Tidak beraroma Aroma amin ringan
Hablur Berserat Granul Serbuk halus
Partikel seperti pasir Serbuk ruah
Higroskopis Serbuk amorf Serpihan
Merah tua Merah muda Merah jingga Merah Coklat Sangat pahit
Aroma minyak permen
Aroma tidak enak seperti merkapton
Aroma asam klorida lemah
Bentuk jarum
b. Analisis fisikokimia
Data analitik zat aktif, yang mencakup data kualitatif, data kuantitatif dan kemurnian. 1. Data kualitatif dan data kuantitatif
Analisis ini merupakan bagian penting dalam studi praformulasi yaitu untuk penetapan identitas dan kadar zat aktif. Untuk penetapan kualitatif biasanya digunakan kromatografi lapis tipis, spectrum serapan inframerah, reaksi warna, spectrum serapan ultraviolet dan reaksi lainnya. Penetapan kadar zat aktif biasanya dilakukan dengan metode spektrofotometri, kromatografi gas, kromatografi cair kinerja tinggi (KCKK), titrasi kompleksometri, asam basa, argentometri, iodometri, dan sebagainya. Penetapam kadar dilakukan dengan tujuan untuk mengetahui kadar dari zat aktif yang akan digunakan dalam pembuatan sediaan.
2. Kemurnian
Praformulasi harus mempunyai daya memahami kemurnian suatu zat aktif. Ketidakmurnian dapat mempengaruhi stabilitas, misalnya kontaminasi logam dengan kadar seperjuta (ppm) dapat merusak beberapa golongan senyawa tertentu. Kemurnian juga dapat memberikan efek yang lain bagi untuk efek terapi yang di harapkan. Metode lain yang berguna dalam menilai kemurnian adalah analisis termal gravimetri dan diferensial. Mengetahui kemurnian suatu bahan dimaksudkan untuk agar bahan aktif atau bahan tambahan yang digunakan tidak mengalami kontaminan sehingga sediaan steril yang dihasilkan memiliki efek terapi yang maksimal.
3. Struktur dan bobot molekul
Dari struktur molekul, peneliti dapaat membuat penilaian awal menyangkut sifat potensial dan reaktivitas fungsional dari molekul bahan aktif obat.
Suhu lebur suatu bahan secara termodinamika didefinisikan sebagai suhu dimana fase cair dan padat berada dalam kesetimbangan. Penentuan suhu lebur merupakan indikasi pertama dari kemurnian bahan karena keberadaan jumlah relative kecil pengotor dapat terdeteksi dengan penurunan atau pelebaran suhu lebur.
5. Profil analitik termal
Selama sintesis dan isolasi, sampel kemungkinan diekspose terhadap perubahan suhu lingkungan proses yang dapat menunjukkan profil termal apabila sampel dipanaskan antara suhu kamar dan suhu leburnya. Apabila tidak ada masalah karena panas, sampel tidak akan mengabsorbsi atau melepas panas sebelum mencapai suhu leburnya.
6. Higroskopisitas
Senyawa dikatakan higroskopis jika senyawa tersebut menarik / mengambil kelembapan dan suhu pada kondisi spesifik dalam jumlah signifikan. Tingkat higroskopis yang tinggi dapat mempengaruhi efek yang tidak dikehendaki dari sifat fisika dan kimia suatu bahan obat yang menyebabkan terjadinya perubahan sehingga secara farmasetik sulit atau tidak mungkin dilakukan penanganan secara memuaskan.
7. Spectra absorben
Molekul dengan struktur tidak jenuh mampu mengabsorbsi cahaya pada rentang frekuensi spesifik. Derajat ketidakjenuhan yang diikuti dengan keberadaan gugus khromofor akan mempengaruhi jumlah absorbsi, baik sinar ultraviolet maupun sinar tampak akan diabsorbsi.
8. Konstanta ionisasi
Memberikan informasi tentang ketergantungan kelarutan dari senyawa pada pH formulasi. pKa biasanya ditentukan secara titrasi potensiometrik pH atau analisis pH kelarutan.
9. Aktivitas optikal
Molekul yang mampu memutar cahaya dan cahaya terpolarisasi secara merata dinyatakan sebagai aktif secara optic. Jika bekerja dengan suatu senyawa yang aktif secara optic selama penelitian praforlmulasi, maka sangat penting untuk memantau rotasi optic tersebut karena penentuan kuantitatif secara kimia saja tidak cukup. (Agoes, Goeswin. 2009)
c. Sifat-sifat fisikomekanik / karakteristik fisik
Sifat-sifat fisikomekanik mencakup ukuran partikel, luas permukaan, pembahasan higroskopisitas, aliran serbuk, karakteristik pengempaan dan bobot jenis.
1. Uraian Fisik
Uraian fisik dari suatu obat sebelum pengembangan bentuk sediaan penting untuk dipahami, kebanyakan zat obat yang digunakan sekarang adalah bahan padat. Kebanyakan obat tersebut merupakan senyawa kimia murni yang berbentuk amorf atau kristal. Obat cairan digunakan dalam jumlah yang lebih kecil, gas bahkan lebih jarang lagi. Untuk mengembangkan bentuk sediaan maka perlu diketahui tentang uraian fisik suatu bahan agar mempermudah dalam menentukan metode membuat sediaan.
2. Pengujian Mikroskopik
Pengujian mikroskopik dari zat murni (bahan obat) merupakan suatu tahap penting dalam kerja (penelitian) praformulasi. Pengujian ini memberikan indikasi atau petunjuk tentang ukuran partikel dari zat murni seperti juga struktur kristal. Pengujian mikroskopik bertujuan untuk mengetahui tentang ukuran partikel. Sehingga pada saat pembuatan sediaan tetes mata akan diketahui ukuran partikel jika memang bentuk sediaan adalah suspensi.
3. Ukuran Partikel
Ukuran partikel zat yang larut dalam air tidak merupakan masalah kecil, kecuali dalam bentuk agregat besar, tetapi adakalanya diperlukan untuk meningkatkan kecepatan pelarutan untuk mengurangi waktu proses manufaktur.
Karakterstik ukuran dan bentuk partikel dapat ditentukan melalui evaluasi dengan mikroskop electron, optik, atau dengan alat polarisasi yang dapat membuat foto bentuk dan ukuran partikel.
Karakteristik morfologi bahan aktif obat direkam melalui sketsa atau yang lebih teliti melalui fotomikrograf, merupakan dokumen permananen untuk dibandingkan dengan bets selanjutnya.
Sifat-sifat fisika dan kimia tertentu dari zat obat dipengaruhi oleh distribusi ukuran partikel, termasuk laju disolusi obat, bioavailabilitas, keseragaman isi, rasa, tekstur, warna dan kestabilan. Sifat-sifat seperti karateristik aliran dan laju sedimentasi
juga merupakan faktor-faktor penting yang berhubungan dengan ukuran partikel. Ukuran partikel dari zat murni dapat mempengaruhi formulasi produk. Khususnya efek ukuran partikel terhadap absorpsi obat. Keseragaman isi dalam bentuk sediaan padat sangat tergantung kepada ukuran partikel dan distribusi bahan aktif pada seluruh formulasi yang sama.
4. Koefisien Partisi dan Konstanta Disosiasi
Koefisien Partisi Merupakan ukuran lipofilisitas dari suatu senyawa. Diukur dengan menetapkan konsentrasi kesetimbangan suatu obat dalam suatu fasa air (biasanya air) dan suatu fasa minyak (biasanya oktanol atau chloroform) yang satu dengan lainnya berkontak pada suhu konstan. Kebanyakan obat yang larut lemak akan lewat dengan proses difusi pasif sedangakn yang tidak larut lemak akan melewati pembatas lemak dengan transport aktif. Karena hal ini maka perlu mengetahui koefisien partisi dari suatu obat.
Khusus untuk obat yang bersifat larut air maka perlu pula diketahui konstanta disosiasi agar diketahui bentuknya molekul atau ion. Bentuk molekul lebih muda terabsorpsi daripada bentuk ion.
5. Polimerfisme
Suatu formulasi yang penting adalah bentuk kristal atau bentuk amorf dari zat obat tersebut. Bentuk-bentuk polimorfisme biasanya menunjukkan sifat fisika kimia yang berbeda termasuk titik leleh dan kelarutan. Bentuk polimorfisme ditunjukkan oleh paling sedikit sepertiga dari senua senyawa-senyawa organik.
6. Kelarutan
Suatu sifat kimia fisika yang penting dari suatu zat obat adalah kelarutan, terutama kelarutan sistem dalam air. Suatu obat harus memiliki kelarutan dalam air agar manjur dalam terapi. Agar suatu obat masuk kedalam sistem sirkulasi dan menghasilkan suatu efek terapeutik, obat pertama-tema harus berada dalam bentuk larutan. Senyawa-senyawa yang relative tidak larut seringkali menunjukkan absorpsi yang tidak sempurna atau tidak menentu.
Dalam pembuatan sediaan injeksi kelarutan sangat penting untuk pengembangan larutan yang dapat disuntikkan baik secara intravena maupun intramuscular. Garam asam
atau basa mempresentasikan kelompok obat yang dapat mencapai kelarutan obat dalam air yang dibutuhkan. Kelas obat lain, baik berupa molekul netral maupun asam atau basa sanagt lemah umumnya tidak dapat disolubilisasi dalam air dalam rentang pH yang sesuai, sehingga memerlukan penggunaan pelarut non air seperti PEG 300 dan 400, propilen glikol, gliserol, etilalkohol, minyak lemak, etiloleat, dan benzilbenzoat.
7. Disolusi
Perbedaan aktivitas biologis dari suatu zat obat mungkin diakibatkan oleh laju disolusi. Laju disolusi adalah waktu yang diperlukan bagi obat untuk melarut dalam cairan pada tempat absorpsi. Untuk obat yang diberikan secara oral dalam bentuk padatan, laju disolusi adalah tahap yang menentukan laju absorpsi. Akibatnya laju disolusi dapat mempengaruhi onset, intensitas dan lama respon serta bioavailabilitas. 8. Kestabilan
Salah satu aktivitas yang paling penting dalam praformulasi adalah evaluasi kestabilan fisika dari zat obat murni. Pengkajian awal dimulai dengan menggunakan sampel obat dengan kemurnian yang diketahui. Adanya pengotoran akan menyebabkan kesimpulan yang salah dalam evaluasi tersebut.
Pengkajian praformulasi yang dihubungkan dengan fase praformulasi termasuk kestabilan obat itu sendiri dalam keadaan padat, kestabilan fase larutan dan kestabilan dengan adanya bahan penambah.
Ketidak stabilan kimia dari zat obat dapat mengambil banyak bentuk, karena obat-obat yang digunakan sekarang adalah dari konstituen kimia yang beraneka ragam. Secara kimia, zat obat adalah alcohol, fenol, aldehid, keton, ester-ester, asam-asam, garam-garam, alkaloid, glikosida, dan lain-lain. Masing-masing dengan gugus kimia relative yang mempunyai kecenderungan berbeda terhadap ketidak stabilan kimia. Secara kimia proses kerusakan yang paling sering meliputi hidrolisis dan oksidasi.
d. Karakteristik Larutan 1. Konstanta disosiasi
Konstanta disosiasi digunakan untuk mengetahui Ph dalam proses pembuatan
sediaan steril.
(terdisosiasi) membentuk ion hidronium dan basa konjugasinya. Hubungan dengan pembuatan sediaan injeksi yaitu sediaan harus sesuai dengan pH yang hampir sama dengan pH darah supaya jika obat di suntikkan dalam tubuh dan tercampur dalam darah maka tidak terjadi nyeri. Dan efek terapinya tercapai. 2. Kelarutan
Semua sifat fisika atau kimia bahan aktif langsung atau tidak langsung akan dipengaruhi oleh kelarutan. Dalam larutan ideal, kelarutan bergantung pada suhu lebur. Hubungan dengan pembuatan sediaan injeksi yaitu sediaan harus larut dalam pembawanya sehingga ketika sediaan tersebut di suntikkan efek terapinya bisa tercapai dengan cepat.
3. Disolusi
Disolusi merupakan tahap pembatas laju absorbsi suatu obat menuju sirkulasi sistemik.Uji ini digunakan untuk mengetahui waktu zat aktif mulai dilepaskan untuk memperoleh kadar yang tinngi dalam darah.
4. Stabilitas
Stabilitas fisika dan kimia dari bahan aktif murni sangat perlu untuk dievaluasi karena jika terdapat keberadaan pengotor dapat menyebabkan kesimpulan yang salah. Hubungan dengan pembuatan injeksi karena pada sediaan injeksi keadaan harus steril dan bebas dari keberadaan pengotor.
Studi praformulasi pada dasarnya berguna untuk menyiapkan dasar yang rasional untuk pendekatan formulasi, Untuk memaksimalkan kesempatan keberhasilan memformulasi produk yang dapat diterima oleh pasien dan akhirnya menyiapkan dasar untuk mengoptimalkan produksi obat dari segi kualitas dan penampilan.
3.2 Formulasi
Formulasi suatu produk sediaan injeksi meliputi kombinasi dari satu atau lebih bahan dengan zat obat untuk menambahkan kenikmatan, kemampuan terima, atau kefektifan produk tersebut. Zat terapetis suatu senyawa kimia yang mudah mengalami karakteristik reaksi kimia dan fisika dari golongan senyawa dimana zat tersebut termasuk didalamnya. Oleh karena itu harus dibuat penilaian hati-hati untuk setiap kombinasi dua bahan atau lebih untuk memastikan apakah terjadi interaksi merugikan atau tidak dan jika terjadi, cara untuk memodifikasi formulasi sehingga reaksi dapat dihilangkan atau dikurangi.
Jumlah keterangan yang tersedia untuk pembuat formulasi sehubungan dengan sifat fisika dan kimia dari suatu zat terapetis, keterangan sehubungan dengan sifat dasar harus diperoleh, termasuk bobot molekul, kelarutan, kemurnian, sifat koligatif dan reaktifitas kimia.
Jadi dalam formulasi sediaan injeksi dapat dirinci sebagi berikut: a. Zat Aktif (active ingredients)
b. Zat Pembawa/Pelarut
Zat pembawa berair atau zat pembawa tidak berair c. Zat Tambahan (nonactive ingredients/ excipients)
Macam-macam zat pembantu atau excipients dalam pembuatan sediaan injeksi meliputi Zat antibakteri, antioksidan, dapar, dan pembantu isotonis.
Sebelum mengembangkan formulasi sediaan farmasi dalam bentuk sediaan injeksi, penting sekali terkumpul data yang meliputi bahan:
a. Zat aktif b. Zat tambahan c. Zat terlarut
Zat terlarut harus bebas dari kontaminasi mikroba dan pirogen. Hal ini tidak hanya memerlukan kualitas kimia yang sesuai seperti yang diperoleh, tetapi juga kondisi penyimpanan yang dirancang untuk mencegah kontaminasi, terutama setelah lama dibuka.
d. Wadah
Bahan utama dari berbagai bahan plastik yang digunakan untuk wadah adalah polimer termoplastik. Kebanyakan bahan plastik yang digunakan dalam bidang medis mempunyai jumlah bahan tambahan yang relatif rendah, beberapa mengandung sejumlah pokok plastisator, pengisi, zat antistatis, antioksidan. Wadah gelas juga biasa digunakan untuk produk yang dapat disuntikkan, gelas pada dasarnya tersusun dari silikon dioksida tetrahedron, dimodifikasi secra fisika kimia dengan oksida-oksida seperti oksida natrium, kalium, kalsium, magnesium, aluminium, boron, besi.
Formulasi Umum R/ Zat Aktif Antibakteri
Pengisotonis Antioksidan Pendapar 3.1.1 Zat Aktif
Zat aktif merupakan bahan yang diharapkan memberikan efek terapetik atau efek lain yang diharapkan. Sebagian besar zat aktif yang digunakan untuk sediaan injeksi bersifat larut air atau dipilih bentuk garamnya yang larut air.
Data zat aktif yang diperlukan, meliputi : a. Kelarutan
Terutama data kelarutan dalam air dari zat aktif sangat diperlukan, karena bentuk larutan air paling dipilih pada pembuatan sediaan steril. Data kelarutan ini diperlukan untuk menentukan bentuk sediaan. Zat aktif yang larut air membentuk sediaan larutan dalam air, zat aktif yang larut minyak dibuat larutan dalam pembawa minyak. Kelarutan obat akan berpengaruh pada volume injeksi, jika mudah larut maka volume yang diberikan kecil. Sedangkan zat tidak larut dalam kedua pembawa tersebut dibuat sediaan suspense atau dengan kosolven.
Jika zat aktif tidak larut dalam air ada beberapa alternatif yang dapat diambil sebelum memutuskan untuk membuat sediaan suspensi atau larutan minyak yaitu dengan mencari bentuk garam dari zat aktif, melakukan reaksi penggaraman, atau dicari bentuk kompleksnya.
b. pH Stabilita
pH Stabilita adalah pH dimana penguraian zat aktif paling minimal, sehingga diharapkan kerja farmakologinya optimal. pH stabilita dicapai dengan menambahkan asam encer, basa lemah atau dapar.
c. Stabilitas Zat Aktif
Beberapa faktor yang mempengaruhi penguraian zat aktif adalah 1. Oksigen (Oksidasi)
Pada kasus ini, setelah air didihkan maka perlu dialiri gas nitrogen dan ditambahkan antioksidan.
2. Air (Hidrolisis)
Dibuat pH stabilitanya dengan penambahan asam basa atau buffer.
Memilih jenis pelarut dengan polaritas lebih rendah daripada air, seperti campuran pelarut air-gliserin-propilenglikol atau pelarut campur lainnya.
Dibuat dalam bentuk kering dan steril yang dilarutkan saat disuntikkan. 3. Suhu
Jika zat aktif tidak tahan panas dipilih metode sterilisasi tahan panas, seperti filtrasi. 4. Cahaya
Pengaruh cahaya matahari dihindari dari penggunaan wadah berwarna coklat. d. Tak tersatukannya zat aktif
Dapat ditinjau dari segi kimia, fisika, atau farmakologi. e. Dosis
Data ini dapat menentukan tonsisitas larutan dan cara pemberian. f. Rute Pemberian
Rute formulasi yang akan digunakan dapat berpengaruh pada formulasi, dalam hal : 1. Volume maksimal sediaan yang dapat dibrikan pada rute tersebut.
2. Pemilihan pelarut dapat disesuaikan dengan rute pemberian.
3. Isotonisitas dri sediaan juga dipengaruhi oleh rute pemberian. Pada larutan intravena iotonisitas menjadi kurang penting selama pemberian dilakukan dengan perlahan untuk memberikan waktu pengenceran dan “adjust” oleh darah. Injeksi intraspinal mutlak harus isotonis.
3.1.2 Bahan Pelarut dan Pembawa Obat Suntik
Bahan pembawa injeksi dapat berupa air maupun non air 1. Pelarut dan Pembawa Air untuk Obat Suntik
Sebagian besar produk parenteral menggunakan pembawa air. Hal tersebut dikarenakan kompabilitas air dengan jaringan tubuh, dapat digunakan untuk berbagai rute pemberian, air mempunyai konsta dielektrik tinggi sehingga lebih mudah untuk melarutkan elektrolit yang terionisasi dan ikatan hidrogen yang terjadi akan memfalitasi pelrut dari alkohol, aldehid, keton dan amin.
Syarat air untuk injeksi menurut USP, yaitu : a. Harus dibuat segar dan bebas pirogen
c. pH antara 5-7
d. Tidak mengandung ion-ion klorida, sulfat, kalsium dan amonium, karbondioksida dan kandungan logm berat serta meterial organik (tanin, lignnin). Partikel berada pada batas yang diperbolehkan.
Jenis pelarut dan pembawa air yang dapat digunakan untuk obat suntik adalah a. WFI (Water for Injection)
Pelarut yang paling sering digunakan dalam obat suntik secara besar– besaran adalah air untuk injeksi atau disebut WFI (Water for Injection). Persyaratan WFI menurut standar BP (2001) dan EP (2002) tidak boleh mengandung :
Total karbonorganik tidak boleh lebih dari 0,5 mg per liter. Klorin tidak boleh lebih dari 0,5 ppm.
Ammonia tidak boleh lebih dari 0,1 ppm. Nitrat tidak noleh lebih dari 0,2 ppm.
Logam berat (Cu, Fe, Pb) tidak boleh lebih dari 0,1 ppm. Oksidator tidak boleh lebih dari 5 ppm.
Bebas pirogen. pH 5,0– 7,0
Penyimpanan air untuk injeksi (WFI) harus disimpan dalam wadah yang tertutup rapat pada temperature dibawah atau diatas kisaran temperature ideal mikroba dapat tumbuh. Air untuk obat suntik bertujuan dalam waktu 24 jam sesudah penampungan
b. Air Pro Injeksi
Aqua bidest dengan pH tertentu, tidak mengandung logam berat (timbal, besi, tembaga), juga tidak boleh mengandung ion Ca, Ck, NO3, SO4, amonium, NO2, CO3. Harus steril dan penggunaan diatas 10 ml harus bebas pirogen.
Aqua steril pro injeksi adalah air untuk injeksi yang disterilkan dan dikemas dengan cara yang sesuai, tidak mengandung bahan antimikroba atau bahan tambahan lainnya.
Cara pembuatan : didihkan air selama 30 menit dihitung dari setelah air mendidih di atas api lalu didinginkan.
CO2 mampu menguraikan garam natrium dari senyawa organik seperti barbiturate dan sulfonamide kembali membentuk asam lemahnya yang mengendap.
Cara pembuatan : mendidihkan air selama 20-30 menit lalu dialiri gas nitrogen sambil didinginkan.
d. Air Pro Injeksi Bebas O2
Dibuat untuk melarutkan zat aktif yang mudah teroksidasi, seperti apomorfin, klorfenoiramin, klorpromazin, ergotamine, metilergotamin, proklorperazin, promazin, promestatin, HCL, sulfamidin, turbokukarin.
Cara pembuatan : mendidihkan air selama 20-30 menit dan pada saat pendinginannya dialiri gas nitrogen.
e. Bacteriostatic Water for Injection
Merupakan air steril untuk obat suntik yag mengandungsatu atau lebih zat antimikroba yang sesuai.
f. Sodium Chloride Injection adalah
Merupakan larutan steril dan isotonic natrium klorida dalamair untuk obat suntik. Larutan tidak mengandung zat antimikroba.
g. Bacteriostatic Sodium Chloride Injection
Merupakan larutan steril dan isotonic natriumklorida dalam air untuk obat suntik. Larutan mengandung satu atau lebih zatantimikroba yang sesuai dan harus tertera dalam etiket.
2. Pelarut dan Pembawa Non Air a. Minyak
Merupakan lemak tidak berba uatau hampir tidak berbau, tidak tengik. Harus memenuhi persyaratan uji paraffin padat seperti yang tertera pada minyak mineral, tangas pendingin, dipertahankan suhu 10o C, bilangan penyabunan antara 185-200, bilangan iodium 79-128 seperti tertera pada lemak dan minyak lemak dan memenuhi persyaratan sebagaiberikut :
Bahan tak tersabunkan : Memenuhi syarat Bahan Tak Tersabunkan seperti tertera dalam lemak dan minyak lemak.
Asam lemak bebas : Tidak lebih dari 2,0 mL NaOH 0,002 N LV diperlukan untuk menetralkan asam lemak bebas dalam 10 gram minyak lemak.
Monogliserida dan gliserida sintetik dari asam lemak : Dapat digunakan jika berupa cairan dan tetap jernih kalau didinginkan pada suhu 10o C dan bilangan iodium tidak lebih dari 140.
Olea neutralisata ad injectionem. Setiap Farmakope mencantumkan jenis minyak tumbuhan (nabati) yang berbeda – beda. Minyak kacang (Oleum Arachidis), minyak zaitun (Oleum Olivarum), minyak mendel, minyak bunga matahari, minyak kedelai, minyak biji kapuk,dan minyak wijen (Oleum Sesami) adalah beberapa jenis minyak yang digunakan sebagai pembawa injeksi. Minyak harus netral secara fisiologis dan dapat diterima tubuh dengan baik. Persyaratan untuk tingkat ini adalah tingkat kemurnian yang tinggi dan menunjukkan bilangan asam dan bilangan peroksida yang rendah. Minyak setelah disterilkan disebut Olea netralisata ad injectionem.
b. Bukan minyak
Pelarut dan pembawa bukan minyak yaitu : Alcohol, Propylenglycol, Glycerine, dan lain – lain dicampur air dapat dipakai sebagai pelarut obat suntik, di samping melarutkan, ternyata mempertinggi stabilitasobat dan larutannya pula.
Pembawa non air digunakan jika : Zat aktif tidak larut dalam air Zat aktif terurai dalam air
Diinginkan kerja depo dalam sediaan Syarat umum pembawa non air
Tidak toksik, tidak mengiritasi dan menyebabkan sesitisasi Dapat tersatukan dengan zat aktif
Inert secara farmakologi
Stabil dalam kondisi dimana sediaan tersebut biasa digunakan
Viskositasnya harus sedemikian rupa sehingga dapat disuntikkan dengan mudah Harus tetap cair pada rentang suhu yang cukup lebar
Mempunyai titik didih yang tinggi sehingga dapat dilakukan sterilisasi dengan panas Dapat bercampur dengan air atau cairan tubuh
Jenis pelarut non air dan air yang dapat digunakan sebagai pembawa sediaan injeksi adalah
a. Pelarut non air yang dapat bercampur dengan air
Pelarut organik yang dapat bercampur dengan air dapat dijadikan kosolven dalam sediaan injeksi. Bertujuan untuk meningkatkan kelarutan suatu zat aktif yang kurang larut dalam air serta meningkatkan stbilitas zat tertentu yang mudah terhidrolisis. Pelarut yang dapat digunakan adalah etanol, propilenglikol dan gliserin. Campuran pelarut yang dapat menyebabkan iritasi atau peningkatan toksisitas, terutama jika digunakan dalam konsentrasi tinggi. Larutan yang mengandung etanol dengan konsentrsi tinggi dapat menimbulkan rasa sakit ketika disuntikkan. Beberapa produk yang dapt diberikan secara intravena dengan kecepatan injeksi yang terlalu cepat dapat menyebabkan pengendapan obat di dalam pembuluh darah.
b. Pelarut air yang tidak dapat bercampur dengan air
Penggunaan pelarut minyak bertujuan untuk meningkatkan kelarutan zat aktif dan untuk membuat sediaan lepas lambat. Injeki pembawa minyak hanya diberikan secara intra muskular. Salah satu persyaratan minyak untuk parenteral adalah harus tetap jernih bila didinginkan sampai 10oC untuk menjamin kestabilan dan kejernihan selama disimpan di lemari pendingin.
Jenis pembawa non air yang tidak dapat bercampur dengan air dan dapat digunakan sebagai pembawa sediaan injeksi adalah
1. Minyak lemak. Karena :
Campuran ester asam lemak dan gliserol
Minyak berasal dari tumbuhan, seperti minyak kacang, biji kapas, jagung, wijen, kenari, jarak dan zaitun.
Pada label sediaan harus dicantumkan jenis pembawa minyak yang digunakan karena pada beberapa orang dapat menimbulkan reaksi alergi.
Minyak mineral tidak dapat digunakan karena tidak dapat dimetabolisme oleh tubuh. Minyak yang digunakan harus berbentuk cair pada suhu kamar dan tidak boleh
menjadi tengik. Untuh mencegah ketengikan akibat oksidasi maka dalam formulas dapat ditambahkan antioksidan seperti : BHA, BHT, tokoferol, propilgalat, dll.
Minyak wijen (sesame oil) lebih banyak digunakan untuk sebagian besar injeksi pembawa minyak, karena merupakan minyak yang paling stabil dibandingkan minyak tumbuhan lain (kecuali terhadap cahaya) dan didalamnya sudah mengandung antioksidan alami.
Minyak tumbuhan sering menimbiulkan rasa nyeri sehingga perlu penambahan benzil alkohol 5% sebagai anastetik lokal.
Tidak boleh mengandung minyak mineral atau parrafin cair (karena tidak dapat dimetabolisme dal tubuh dan dapat menimbulkan rekasi terhadap jaringan atau tumor). Minyak nabati yang banyak digunakan : Ol. Arachidis (minyak kacang), Ol. Gossypii, Ol. Sesami (minyak wijen), Ol. Terebinthinae, Ol. Maydis, Ol. Olivarium Netral, Ol. Amigdalarum.
2. Isopropil miristat
Ester asam lemak yang mempunyai viskositas rendah.
Sebagai pembawa tunggal atau kombinasi dengan minyak lemak.
Digunakan jenis yang bebas peroksida karena mencegh teroksidasinya bahan berkhasiat dan minyak yang digunakan.
3. Benzil benzoate
Merupakan cairan berminyak yang tidak berwarna dan bau yang khas. Biasanya digunakan bersama dengan pembawa lain (sebagai kosolven) misal pada injeksi dimerkapol dan hidroksiprogesteron.
4. Etil oleat
Viskositas lebih rendah dan lebih mudah diabsorbsi oleh jaringan dibandingkan dengan minyak lemak.
Sebagai pembawa tunggal atau kosolven dalam injeksi hormon seperti injeksi dioksikortison asetat, estradiol monobenzoat, progesterondan testosteron propinoat. 3.1.3 Zat Tambahan
Zat tambahan pada sediaan steril digunakan untuk : Meningkatkan kelarutan zat aktif
Menjaga stabilitas zat aktif
Mempermudah dan menjaga keamanan pemberian Syarat bahan tambahan :
Inert secara farmakologi , fisika, maupunkimia Tidak toksik dalam jumlah yang diberikan Tidak mempengaruhi pemeriksaan obat a. Pengatur Tonisitas
1. Isotonis
Jika suatu larutan konsentrasinya sama besar dengan konsentrasi dalam sel darah merah sehingga tidak terjadi pertukaran cairan diantara keduanya, maka larutan tersebut dikatakan isotonis (ekivalen dengan 0,9% NaCl).
Sel darah merah dalam larutan :
Hipotonis : mengembang kemudian pecah, karena air berdifusi ke dalam sel (hemolysis). Keadaan hipotonis kurang dapat ditoleransi, karena pecahnya sel bersifat irreversible
Hipertonis : kehilangan air dan mengkerut (krenasi), keadaan ini cukup dapat ditoleransi
Larutan perlu isotonis agar :
Mengurangi kerusakan jaringan dan iritasi Mengurangi hemolisis sel darah
Mencegah ketidakseimbangan elektrolit Mengurangi sakit pada daerah injeksi
Larutan isotonis tidak selalu mungkin karena :
Konsentrasi obat tinggi, tetapi batas volume injeksi kecil Variasi dosis pemberian
Metode pemberian
Pertimbangan stabilitas produk 2. Isoosmotik
Jika suatu larutan memiliki tekanan osmose sama dengan tekanan osmose serum darah, maka larutan dikatakan isoosmotik.
3. Hipotonis
Turunnya titik beku kecil, yaitu tekanan osmosenya lebih rendah dari serumdarah, sehingga menyebabkan air akan melintasi membrane sel darah merah yang semi permeabel memperbesar volume sel darah merah dan menyebabkan peningkatan tekanan dalam sel. Tekanan yang lebih besar menyebabkan pecahnya sel– sel darah merah, yang disebut Hemolisa.
4. Hipertonis
Turunnya titik beku besar, yaitu tekanan osmosenya lebih tinggi dari serum darah,sehingga menyebabkan air keluar dari sel darah merah melintasi membranesemipermeabel dan mengakibatkan terjadinya penciutan sel– sel darah merah, yangdisebut Plasmolisa.
Beberapa cara dapat menjadikan larutan isotonis : a. Penurunan titik beku
W = (0,52– a) / b
W = jumlah (g) bahan pembantu isotonic dalam 100 ml larutan
a = turunnya titik beku air akibat zat terlarut, dihitung denganmemperbanyak nilai untuk larutann 1% b/v. b = turunnya titik beku air yang dihasilkan oleh 1% b/v bahan pembantuisotonis.
b. Kesetaraan dengan garam natrium klorida
Ekivalensi natrium klorida memberikan jumlah natrium klorida (g) yang menghasilkan tekanan osmotic sama seperti 1 gram bahan obat dnegan syarat bahwa baik natrium klorida maupun bahan obat berada dalam larutan bervolume sama. Maka, 1 gram bahan obat ekuivalen dengan tekanan osmoticdari x gram natrium klorida. Dengan bantuan ekuivalensi natrium klorida, kitadapat menghitung volume air yang dibutuhkan untuk membuat larutan bahanobat isotonik.
c. Kesetaraan volume isotonic
Perhitungan didasarkan pada kenyataan bahwa larutan isotonic ditambahlarutan isotonic hasilnya larutan isotonic.
Rumus : V = w x E x 111,1
V = volume larutan bahan obat isotonic yang dicari (ml) w = masa bahan obat (g) dan larutan yang dibuat E = ekuivalensi natrium klorida
111,1 = volume larutan isotonic (ml) yang mengandung 1 gram natriumklorida = 111,1 ml d. Perhitungan dengan tetapan Liso
Berlaku bila tidak ada data pada tabel penurunan titik beku.Tahapan perhitungan : 1. Cari bahan molekul obat.
2. Berdasarkan struktur kimia senyawa, tentukan tipe isotoniknya 3. Cari harga Liso dari tabel berdasarkan tipe isotonic
4. Hitung dengan rumus Dt f = Liso. C penurunan titik beku. 5. Hitung selisih penurunan titik beku.
6. Hitung kekurangan tonisitas.
7. Dengan melihat tabel, hitung kekurangan zat untuk mencapai isotonic. e. Cara faktor disosiasi (Farmakope Belanda VI)
Telah ditetapkan bahwa larutan NaCl 0,9% b/v isotonis dengan cairan tubuh. Tekanan osmosis larutan sebanding dengan jumlah bagian-bagian dalam larutan. Dalam larutan encer, dapat dikatakan bahwa garam-garam terdisosiasi sempurna.
NaCl Na+ + Cl -(Fa/Ma)xa
Dari sebuah molekul NaCl terbentuk 2 (dua) ion. Jadi faktor disosiasi NaCl = 2; lebih tepat sebetulnya 1,8 karena ada sedikit kesetimbangan reaksi.
Jadi faktor isotonisnya adalah:
fa = faktor disosiasi zat-zat yang mendekati keadan yang sebenarnya; untuk zat-zat yang tidak terdisosiasi seperti glukosa dan gliserin = 1 ; untuk asam lemah dan basa lemah = 1,5 dan untuk asam kuat dan basa kuat =1,8
Ma= bobot molekul zat.
a, b, c,.... dan seterusnya adalah kadar zat dalam larutan dalam satuan g/liter. Jadi larutan isotonis dapat dihitug dari NaCl 0,9% b/v tersebut, yaitu:
= (f.NaCl/M.NaCl)x kadar NaCl ( dalam satuan gram/liter)
= (1,8/ 58,5)x9 = 0,28 (berarti setiap larutan yang mempunyai faktor isontonis = 0,28 adalah isotonis).
Dapat kita turunkan rumus sebagai berikut
Rumus :