FORMULASI SEDIAAN EMULGEL EKSTRAK ETANOLIK RIMPANG TEMU PUTIH (Curcuma zedoaria Berg. Roscoe) DENGAN GLISERIN
SEBAGAI PENETRATION ENHANCER DAN PENGUJIAN AKTIVITASNYA SEBAGAI ANTIINFLAMASI
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat
Memenuhi Gelar Sarjana Farmasi (S. Farm.)
Program Studi Farmasi
Oleh : Lulu Margathe NIM : 108114085
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2014
i
FORMULASI SEDIAAN EMULGEL EKSTRAK ETANOLIK RIMPANG TEMU PUTIH (Curcuma zedoaria Berg. Roscoe) DENGAN GLISERIN
SEBAGAI PENETRATION ENHANCER DAN PENGUJIAN AKTIVITASNYA SEBAGAI ANTIINFLAMASI
SKRIPSI
Diajukan Untuk Memenuhi Salah Satu Syarat
Memenuhi Gelar Sarjana Farmasi (S. Farm.)
Program Studi Farmasi
Oleh : Lulu Margathe NIM : 108114085
FAKULTAS FARMASI
UNIVERSITAS SANATA DHARMA YOGYAKARTA
2014
iii
v
PRAKATA
Puji syukur dan terima kasih penulis panjatkan kepada Tuhan Yang
Maha Pengasih dan Penyayang atas semua berkat dan penyertaan-Nya sehingga
penulis dapat menyelesaikan skripsi yang berjudul “Formulasi Sediaan Emulgel
Ekstrak Etanolik Rimpang Temu Putih (Curcuma zedoaria Berg. Roscoe) dengan
Gliserin Sebagai Penetration Enhancer dan Pengujian Aktivitasnya Sebagai
Antiinflamasi” sebagai salah satu syarat memperoleh gelar Sarjana Farmasi (S.
Farm.) di Fakultas Farmasi, Universitas Sanata Dharma, Yogyakarta.
Penulis menyadari dalam penyusunan naskah ini, penulis telah
mendapatkan bantuan doa, bimbingan, arahan, saran dan kritik yang membangun
dari berbagai pihak. Pada kesempatan ini, penulis hendak menyampaikan
ungkapan terimakasih yang sebesar-besarnya kepada :
1. Papi dan Mami atas kerja keras dan kasih sayangnya kepada penulis serta
senantiasa mendoakan dan mendukung penulis selama menyusun skripsi.
2. Dekan Fakultas Farmasi Universitas Sanata Dharma Yogyakarta.
3. Ibu Christofori Maria Ratna Rini Nastiti, M. Pharm., Apt. selaku Kaprodi
Fakultas Farmasi Universitas Sanata Dharma, sekaligus dosen pembimbing
yang selalu memberikan arahan, bimbingan, masukan, semangat serta
motivasi semenjak pembuatan proposal hingga selesainya penelitian skripsi
ini.
4. Bapak Ipang Djunarko M. Sc., Apt. selaku dosen penguji skripsi yang telah
memberikan waktu, saran dan masukan demi kesempurnaan skripsi ini.
vii
5. Bapak Yohanes Dwiatmaka, M. Si. selaku dosen penguji skripsi yang telah
memberikan waktu, saran dan masukan demi kesempurnaan skripsi ini.
6. Semua dosen-dosen farmasi yang telah sabar mendidik serta memberikan ilmu
kepada penulis selama menempuh pendidikan di Fakultas Farmasi Universitas
Sanata Dharma, Yogyakarta.
7. Segenap laboran dan karyawan, Bapak Musrifin, Bapak Heru, Bapak
Wagiran, dan Mas Darto yang telah membantu selama penelitian berlangsung.
8. Koko dan Cici, yang walaupun jauh namun selalu memberikan doa, semangat
dan motivasi kepada penulis.
9. Teman-teman skripsi sahabat senasib sepenanggungan Samuel Meinardus
Dwi Prasetyo, Odilia Arum Narwastu, Sekar Wulan Kinanti Herlambang,
Angga Zakharia, dan Fransiskus Asisi Dian Kristianto.
10.Sahabat-sahabatku Stephanie Cinthya Wibowo, Felicia Aniska, dan Oei Maria
Dewiyani Sandjaja, atas doa, semangat, dukungan, motivasi, dan persahabatan
yang berkesan sampai selamanya.
11.Tomas Indra Waskitha Utama yang selalu menemani penulis dengan doa,
semangat, kasih sayang dan kesabaran.
12.Teman-teman angkatan 2010 Fakultas Farmasi Universitas Sanata Dharma
yang juga memberikan warna selama masa perkuliahan penulis.
13.Semua pihak yang tidak dapat penulis sebutkan satu persatu yang telah
memberikan doa, bantuan, dan dukungan selama penelitian skripsi.
Penulis menyadari bahwa penyusunan skripsi ini masih banyak
kekurangan mengingat keterbatasan kemampuan serta pengalaman yang dimiliki.
Oleh sebab itu, kritik dan saran yang membangun sangat diperlukan oleh penulis
untuk menyempurnakan skripsi ini. Semoga skripsi ini dapat bermanfaat bagi
perkembangan ilmu pengetahuan.
Yogyakarta, 24 Mei 2014
Penulis
ix
DAFTAR ISI
Halaman
HALAMAN JUDUL ... i
HALAMAN PERSETUJUAN PEMBIMBING ... ii
HALAMAN PENGESAHAN ... iii
PERNYATAAN PERSETUJUAN PUBLIKASI ... iv
PERNYATAAN KEASLIAN KARYA ... v
PRAKATA ... vi
A. Jenis dan Rancangan Penelitian ... 21
B. Variabel Penelitian dan Definisi Operasional ... 21
1. Variabel penelitian ... 21
2. Definisi operasional ... 22
C. Bahan Penelitian ... 23
D. Alat Penelitian ... 23
E. Tata Cara Penelitian ... 23
1. Pembuatan ekstrak etanol rimpang temu putih ... 23
2. Formula ... 24
5. Uji aktivitas antiinflamasi temu putih dalam sediaan emulgel ... 27
a. Penyiapan hewan uji ... 27
b. Pembuatan larutan NaCl 0,9% ... 27
c. Pembuatan suspensi karagenan 1% ... 27
d. Uji aktivitas antiinflamasi ... 27
e. Perhitungan respon daya antiinflamasi ... 28
F. Analisis Hasil ... 29
BAB IV. HASIL DAN PEMBAHASAN ... 30
A. Hasil Determinasi Tanaman ... 30
B. Hasil Standarisasi Ekstrak ... 30
C. Hasil Sifat Fisik dan Stabilitas Emulgel ... 31
1. Uji organoleptis ... 31
2. Uji pH ... 31
3. Viskositas ... 32
4. Daya sebar ... 33
5. Stabilitas sediaan ... 33
D. Pengujian Efek Antiinflamasi Emulgel ... 35
E. Hasil Uji Antiinflamasi Emulgel ... 38
BAB V. KESIMPULAN DAN SARAN ... 44
A. Kesimpulan ... 44
B. Saran ... 44
DAFTAR PUSTAKA ... 45
LAMPIRAN ... 48
BIOGRAFI PENULIS ... 77
xiii
DAFTAR TABEL
Halaman
Tabel I. Formula Acuan (100 g) ... 24
Tabel II. Formula Emulgel Modifikasi (100 g) ... 25
Tabel III. Hasil Uji Sifat Fisik dan Stabilitas Emulgel ... 31
Tabel IV. Hasil Uji Sifat Fisik Emulgel ... 32
Tabel V. Hasil Pergeseran Viskositas ... 34
Tabel VI. Hasil Pergeseran Viskositas dengan Menggunakan Statistik ... 34
Tabel VII. Hasil % Reduksi Udema Kaki Tikus ... 39
Tabel VIII. Hasil Uji Statistik % Reduksi Udema Pada Jam Ke-4 ... 40
Tabel IX. Hasil Uji Statistik % Reduksi Udema Pada Jam Ke-24 ... 42
DAFTAR GAMBAR
Halaman
Gambar 1. MekanismeInflamasi ... 9
Gambar 2. Voltaren Emulgel® ... 10
Gambar 3. Temu Putih (Curcumazedoaria Berg. Roscoe Roscoe) ... 11
Gambar 4. Struktur dari Kurkuminoid ... 13
Gambar 5. Mekanisme Antiinflamasi Kurkumin ... 14
Gambar 6. Struktur Gliserin ... 17
Gambar 7. Mekanisme Karagenan sebagai Agen Inflamasi ... 18
xv
DAFTAR LAMPIRAN
Halaman
Lampiran 1. Determinasi Tanaman Rimpang Temu Putih ... 48
Lampiran 2. Analisis Kurkumin ... 49
Lampiran 3. Analisis Kadar Air Ekstrak ... 51
Lampiran 4. Ethical Clearance ... 55
Lampiran 4. Sifat Fisik dan Stabilitas Emulgel ... 56
Lampiran 5. Hasil Uji Antiinflamasi Emulgel ... 62
Lampiran 6. Hasil Analisis Aktivitas Antiinflamasi Menggunakan Software R 3.0.1 ... 66
Lampiran 7. Emulgel Antiinflamasi ... 76
INTISARI
Rimpang temu putih (Curcuma zedoaria Berg. Roscoe) diketahui dapat berkhasiat sebagai antiinflamasi, dan dari kandungannya yang memiliki aktivitas tersebut adalah kurkumin. Ekstrak etanolik rimpang temu putih diyakini dapat diformulasikan ke dalam bentuk sediaan topikal. Penelitian ini bertujuan untuk memformulasi ekstrak etanolik rimpang temu putih ke dalam sediaan emulgel dan mengamati aktivitas antiinflamasi serta pengaruh penambahan penetration enhancer.
Penelitian ini termasuk dalam penelitian eksperimental murni dengan menguji aktivitas antiinflamasi dari sediaan emulgel yang dilakukan terhadap tikus betina galur Wistar. Konsentrasi ekstrak yang digunakan dalam formulasi sediaan gel ini adalah 7% dengan kontrol negatif menggunakan basis emulgel dan kontrol positif menggunakan Voltaren Emulgel®. Analisis data menggunakan R 3.0.1 dengan taraf kepercayaan 95%.
Hasil penelitian menunjukkan bahwa sediaan emulgel ekstrak temu putih memiliki aktivitas inflamasi dengan viskositas yang memenuhi kriteria untuk formula 1 dan 2 dengan nilai 316,7 ± 20,8 dan 373,3 ± 25,3, sedangkan untuk formula 3 dan 4 tidak memenuhi syarat dengan nilai 456,7 ± 20,8 dan 520 ± 26,5. Untuk daya sebar, semua formula memenuhi persyaratan dengan nilai masing-masing berada diantara rentang 3 – 5 cm. Penambahan konsentrasi gliserin sebagai penetration enhancer pada formulasi sediaan emulgel ekstrak temu putih memiliki pengaruh terhadap peningkatan aktivitas antiinflamasi yang diukur melalui persentase reduksi udema telapak kaki belakang tikus.
Kata Kunci: Curcuma zedoaria Berg. Roscoe, kurkumin, emulgel, antiinflamasi,
penetration enhancer
xvii
ABSTRACT
White turmeric (Curcuma zedoaria Berg. Roscoe) is known to have an anti-inflammatory effect, and the substance that responsible for the effect is curcumin. The ethanolic extract from white turmeric can be possibly incorporated in to a topical solution. This research aimed to formulate the extract as an emulgel, and to observe the effect of anti-inflammatory and the addition of penetration enhancer in the efficacy of the emulgels.
The research is categorized as purely experimental research by testing the activity of the anti-inflammatory emulgel to the Wistar strain female rats. The concentration of the extract that was applied in the preparation of the gel is 7%, with the basis of emulgel as the negative control, and Voltaren Emulgel® as positive control. The data analysis was done using R 3.0.1 with 95% confidence interval.
The result of this experiment indicated that the emulgel extract of white turmeric showed an anti-inflammatory activity with the viscosity which met the criteria for formula 1 and 2 with the values of 316,7 ± 20,8 and 373,3 ± 25,3, and does not fulfill the criteria for formula 3 and 4 with the values of 456,7 ± 20,8 and 520 ± 26,5, respectively. The spreading coefficient for all the formulations fulfilled the criteria with the values in between 3 - 5 cm. The addition of glycerine as a penetration enhancer to the emulgel extract of white turmeric has an influence on the increase in anti-inflammatory activity which were measured by the percentage of edema reduction of rats’ feet.
Key words : Curcuma zedoaria Berg. Roscoe, curcumin, emulgel, antiinflammation, penetration enhancer
BAB I PENGANTAR
A. Latar Belakang
Dalam kehidupan sehari-hari, terkadang manusia dapat mengalami
peradangan akibat adanya luka atau infeksi mikroba, virus, atau yang lain. Adanya
reaksi imun pada manusia akan menyebabkan timbulnya suatu peradangan
(inflamasi) sebagai reaksi perlindungan terhadap luka maupun infeksi mikroba
tersebut. Bagian yang paling sering untuk mengalami luka adalah jaringan kulit.
Pada lapisan kulit juga terdapat agen pro-inflamasi seperti sitokin TNF-α, IL-1,
dan IL-6 (Necas, 2013).
Radang (inflamasi) merupakan mekanisme pertahanan tubuh disebabkan
adanya respons jaringan terhadap pengaruh-pengaruh merusak, baik bersifat lokal
maupun yang masuk ke dalam tubuh. Pengaruh-pengaruh yang merusak sel sering
disebut noksi. Noksi dapat berupa fisika (panas, dingin, benturan), kimia
(obat-obatan), dan infeksi bakteri, parasit (Mutschler, 1986).
Inflamasi merupakan reaksi yang timbul untuk menghadapi agen-agen
perusak (seperti mikroba) yang terdiri dari reaksi vascular, migrasi maupun
aktivasi leukosit, dan reaksi sistemik. Inflamasi sering disebut sebagai suatu
reaksi penyembuhan jaringan. Inflamasi dapat memicu rangkaian proses
penyembuhan ataupun mengganti jaringan yang sudah rusak dengan yang baru.
Peradangan seperti ini dapat diatasi dengan memberikan obat anti
inflamasi kepada penderita. Obat anti inflamasi akan menekan efek anti inflamasi
2
sehingga peradangan akan berkurang. Obat Antiinflamasi yang banyak digunakan,
terutama dari kelompok obat-obat anti inflamasi nonsteroid (NSAID) dan
sebahagian kecil dari golongan Anti inflamasi steroid (AIS). Kerja utama
obat-obat (NSAID) sebagai penghambat isoenzim COX-1 (cyclooxygenase-1) dan
COX-2 (cyclooxygenase-2). Enzim cyclooxygenase ini berperan dalam memacu
pembentukan prostaglandin dan tromboksan dari arachidonic acid. Prostaglandin
merupakan molekul pembawa pesan pada proses inflamasi (radang).
Obat antiinflamasi golongan NSAID dan kortikosteroid sama-sama
memiliki kemampuan untuk menekan tanda dan gejala inflamasi, namun kedua
golongan obat ini yang biasa digunakan dalam pengobatan inflamasi seringkali
menimbulkan efek yang merugikan dan berbahaya seperti kerusakan
gastrointestinal, nefrotoksik dan hepatotoksik (Katzung, 2002).
Adanya efek samping yang ditimbulkan oleh obat antiinflamasi golongan
NSAID tentunya akan merugikan konsumen, apalagi sebagian besar obat
antiinflamasi yang dijual di pasaran dikonsumsi secara per-oral. Perlu adanya
alternatif bentuk sediaan lain untuk efek lokal yang lebih menjamin keamanan
konsumen, yaitu bentuk sediaan topikal. Selain itu, perlu adanya alternatif obat
antiinflamasi yang zat aktifnya berasal dari tanaman karena memiliki efek
samping yang lebih kecil dibandingkan obat hasil sintesis kimia.
Zaman sekarang ini pengetahuan tentang manfaat tanaman untuk
kesehatan telah dikembangkan lebih lanjut. Para ilmuwan sudah melanjutkan
penelitian terhadap komponen aktif yang terkandung di dalam bahan-bahan yang
berasal dari alam. Salah satu tumbuhan yang dapat digunakan sebagai anti
3
inflamasi adalah temu putih (Curcumazedoaria Berg. Roscoe). Bagian yang biasa
digunakan untuk pengobatan adalah rimpangnya. Dari rimpangnya banyak
kandungan yang dapat berfungsi sebagai antiradang, salah satunya adalah
kurkumin. Aktivitas antiradang kurkumin pertama kali dilaporkan oleh Grieve
pada tahun 1971 (Dalimartha, 1999). Kurkumin dapat berfungsi sebagai
antiinflamasi dengan menekan aktivitas dari fosfolipase, lipooksigenase, COX-2,
leukotrien, prostaglandin, nitrit oxide, MCP-1, tumor necrosis factor-alpha
(TNF-α), interleukin (IL) (Chainani-Wu, 2003).
Bentuk-bentuk sediaan topikal ada beberapa macam antara lain krim, gel,
emulgel, salep, dan pasta. Sediaan emulgel mempunyai kelebihan diantaranya
memiliki viskositas dan daya lekat yang tinggi sehingga tidak mudah mengalir
pada permukaan kulit, tidak meninggalkan bekas, hanya berupa lapisan tipis
seperti film saat pemakaian, dapat membawa obat yang bersifat hidrofobik dan
tidak larut air, stabilitas yang lebih baik, memungkinkan biaya produksi yang
lebih rendah, dapat menjadi sediaan lepas terkendali untuk obat dengan waktu
paruh pendek (Mohamed, 2004).
Adanya emulgel yang merupakan sediaan topikal ini dapat menjadi
alternatif sistem penghantaran obat antiinflamasi karena dengan cara pengolesan
maka tidak memberikan efek samping pada sistem pencernaan, zat aktif obat juga
tidak mengalami first-pass effect di hati. Keuntungan lain adalah efek pengobatan
yang diberikan bersifat lokal, sehingga reaksi inflamasi yang timbul secara kasat
mata dapat langsung diobati tanpa merusak sistem organ yang lain. Untuk sediaan
yang mengandung zat aktif dari bahan alam, penggunaan emulgel dapat
4
disarankan karena mampu membawa obat yang bersifat hidrofobik seperti
kurkumin dan stabilitas zat aktif serta penampilan fisiknya tetap terjaga.
Gliserin akan menambah daya penetrasi zat aktif di dalam sediaan,
sehingga dapat berfungsi sebagai suatu penetration enhancer (Stinchcomb and
Banks, 2010). Penambahan gliserin diharapkan dapat meningkatkan daya hantar
zat aktif obat melalui lapisan kulit sehingga efikasi dari sediaan bisa lebih
Roscoe) dapat dibuat dengan sifat fisik yang memenuhi kriteria?
b. Apakah sediaan emulgel dengan ekstrak Temu Putih (Curcuma zedoaria
Berg. Roscoe) memiliki aktivitas antiinflamasi?
c. Bagaimanakah pengaruh gliserin yang digunakan sebagai penetration
enhancer pada formulasi sediaan emulgel ekstrak Temu Putih (Curcuma
zedoaria Berg. Roscoe)?
2. Keaslian penelitian
Pada penelitian Delly Ramadon (2012) berjudul “Penetapan Daya Penetrasi Secara In Vitro Sediaan Gel dan Emulgel yang Mengandung Kapsaisinoid dari Ekstrak Buah Cabai Rawit (Capsicum frutescens L.)”.
5
Dalam penelitian ini, yang dilakukan adalah membandingkan daya penetrasi
antara sediaan gel dan emulgel. Didapatkan bahwa sediaan emulgel memiliki
daya penetrasi yang lebih baik daripada gel.
Pada penelitian Paulina Maya (2011) yang berjudul “Efek Antiinflamasi Benzoil Eugenol secara Topikal terhadap Edema Kaki yang Diinduksi Formalin 6,5% pada Mencit Jantan Galur Swiss”. Dalam penelitian ini, yang dilakukan adalah mengukur persentase reduksi udema kaki
tikus dengan menggunakan metode jangka sorong.
Pada penelitian Octa Rahadian Pius (2012) yang berjudul “Prediksi Komposisi Optimum Gliserin dan Virgin Coconut Oil (VCO) sebagai
Penetration Enhancer dalam Formula Emulsi A/M Tonik Rambut Ekstrak Etanol-Air Biji Kemiri (Aleurites moluccana (L.) Willd) : Aplikasi Desain Faktorial”. Dalam penelitian ini, yang dilakukan adalah menggunakan gliserin sebagai penetration enhancer pada sediaan.
Namun, sejauh penelusuran yang telah dilakukan oleh penyusun,
penelitian dengan judul “Formulasi Sediaan Emulgel Ekstrak Etanolik Rimpang Temu Putih (Curcuma zedoaria Berg. Roscoe) dengan Gliserin sebagai Penetration Enhancer dan Pengujian Aktivitasnya Sebagai Antiinflamasi” belum pernah dilakukan.
6
3. Manfaat penelitian
a. Manfaat teoretis
Manfaat teoritis dalam penelitian ini adalah dapat menambah
pengetahuan mengenai aktivitas anti inflamasi dari sediaan topikal dengan
zat aktif Temu Putih (Curcuma zedoaria Berg. Roscoe).
b. Manfaat praktis
Manfaat praktis dalam penelitian ini adalah dapat menghasilkan
emulgel Temu Putih (Curcuma zedoaria Berg. Roscoe) yang efektif dan
berkualitassebagai sediaan antiinflamasi topikal.
B. Tujuan Penelitian 1. Tujuan umum
Tujuan umum penelitian ini adalah untuk menghasilkan sediaan
emulgel dengan zat aktif berupa ekstrak etanol rimpang Temu Putih (Curcuma
zedoaria Berg. Roscoe) yang memiliki aktivitas antiinflamasi.
2. Tujuan khusus
Tujuan khusus penelitian ini adalah untuk:
a. Memastikan bahwa sifat fisik dari sediaan emulgel esktrak etanol rimpang
Temu Putih (Curcuma zedoaria Berg. Roscoe) memenuhi kriteria.
7
b. Mengetahui ada tidaknya aktivitas anti inflamasi dari ekstrak etanol
rimpang Temu Putih (Curcuma zedoaria Berg. Roscoe) pada sediaan
emulgel.
c. Mengetahui pengaruh penambahan konsentrasi Gliserin sebagai
penetration enhancer pada formulasi sediaan emulgel ekstrak etanol
rimpang Temu Putih (Curcumazedoaria Berg. Roscoe).
Inflamasi adalah respons protektif setempat yang ditimbulkan oleh
cedera atau kerusakan jaringan, yang berfungsi menghancurkan, mengurangi, atau
mengurung suatu agen pencedera maupun jaringan yang cedera itu. Pada bentuk
akut ditandai oleh tanda klasik yaitu : nyeri (dolor), panas (kalor), kemerahan
(rubor), bengkak (tumor), dan hilangnya fungsi (fungsiolesa) (Sudoyo, 2007).
Gejala-gejala ini merupakan akibat dari gangguan aliran darah yang
terjadi akibat kerusakan jaringan dalam pembuluh pengalir terminal, gangguan
keluarnya plasma darah (eksudasi) ke dalam ruang ekstrasel akibat meningkatnya
ketelapan kapiler dan perangsangan reseptor nyeri. Respon ini disebabkan oleh
pembebasan bahan-bahan mediator (histamine, serotonin, prostaglandin, kinin)
(Sudoyo, 2007).
Gejala inflamasi yang dapat teramati adalah pemerahan (rubor), panas
(calor), pembengkakan (tumor), nyeri (dolor), dan gangguan fungsi (fungsio
laesa). Gejala tersebut dapat terjadi karena adanya gangguan aliran darah akibat
kerusakan jaringan dalam pembuluh pengalir terminal, gangguan keluarnya
plasma darah ke ruang esktrasel akibat meningkatnya ketebalan kapiler dan
perangsangan reseptor nyeri (Mutschler, 1986).
9
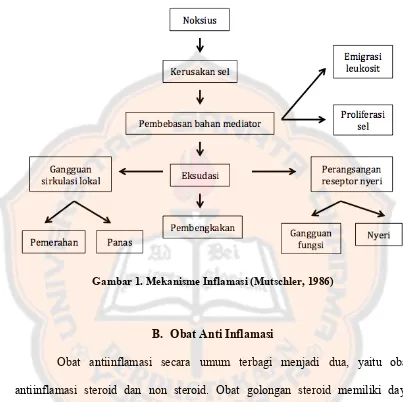
Mekanisme terjadinya peradangan :
Gambar 1. Mekanisme Inflamasi (Mutschler, 1986)
B. Obat Anti Inflamasi
Obat antiinflamasi secara umum terbagi menjadi dua, yaitu obat
antiinflamasi steroid dan non steroid. Obat golongan steroid memiliki daya
antiinflamasi yang kuat yang mekanismenya berdasarkan rintangan sintesis
prostaglandin dan leukotriene dengan menghambat fosfolipase (Tjay, 2002).
Obat Anti-Inflamasi Non Steroid (OAINS) dapat menghambat sistem
enzim, siklooksigenase maupun lipooksigenase intraseluler, yang nantinya akan
berpengaruh terhadap respon inflamasi yang terjadi serta menurunkan produksi
berbagai komponen prostaglandin (Babb, 1992).
10
C. Voltaren Emulgel®
Voltaren Emulgel® dapat diaplikasikan 3 atau 4 kali sehari. Jumlah yang
dibutuhkan tergantung pada area yang sakit. 2 sampai 4 gram Voltaren Emulgel®
diketahui dapat mengobati area seluas 400-800 cm2. Lama waktu pemakaian
didasarkan pada indikasi dan respon yang didapat (MIMS, 2014).
Voltaren Emulgel® mengandung dietilamin diklofenak (tiap 11,6 mg
dietilamin diklofenak setara dengan 10 mg natrium diklofenak). Voltaren
Emulgel® juga mengandung dietilamin, polimer asam akrilik, cetomacrogol 1000,
isopropyl alcohol, paraffin cair, parfum, propilen glikol, dan air. Basis dari
Voltaren Emulgel® adalah gel emulsi minyak dalam air (MIMS, 2014).
Gambar 2. Voltaren Emulgel® (Novartis, 2011)
11
D. Temu Putih (Curcuma zedoaria Berg. Roscoe)
Gambar 3. Tanaman Temu Putih (Anonim, 2013)
Tanaman Temu Putih (Curcuma zedoaria Berg. Roscoe) memiliki nama
daerah Koneng Tegal (Sunda), Temu Pepet (Jawa). Di berbagai negara dikenal
dengan nama White Tumeric (Inggris), Kencur atau Ambhalad (India), Dan
Cedoaria (Spanyol), Er-chu (China). Klasifikasi tanaman temu putih adalah
sebagai berikut:
1. Divisi : Spermathopyta
2. Anak Divisi : Angiospermae
3. Kelas : Monocotyledonae
4. Bangsa : Zingiberales
5. Suku : Zingiberaceae
6. Marga : Curcuma
7. Jenis : Curcuma zedoaria Berg. Roscoe (CCRC, 2014).
Tanaman temu putih berupa terna tahunan, tinggi mencapai 2 m, tumbuh
tidak berkelompok. Daun berbentuk lanset memanjang berwarna merah
lembayung di sepanjang tulang tengahnya. Bunga keluar dari rimpang samping,
menjulang ke atas membentuk bongkol bunga yang besar. Mahkota bunga
12
berwarna putih, dengan tepi bergaris merah tipis atau kuning. Rimpang berwarna
putih atau kuning muda, rasa sangat pahit (CCRC, 2014).
Temu putih berasal dari Himalaya, India, dan terutama tersebar di
negara-negara Asia meliputi China, Vietnam, dan Jepang. Temu putih tumbuh liar
di Sumatra (Gunung Dempo), di hutan jati Jawa Timur, banyak pula dijumpai di
Jawa Barat dan Jawa Tengah, di ketinggian sampai 1000 dpl (CCRC, 2014).
Kandungan kimia rimpang temu putih terdiri dari kurkuminoid
(diarilheptanoid), minyak atsiri, polisakarida serta golongan lain. Diarilheptanoid
yang telah diketahui meliputi kurkumin, demetoksikurkumin,
bisdemetoksikurkumin, dan 1,7 bis (4-hidroksifenil)-1,4,6-heptatrien-3-on.
Minyak atsiri berupa cairan kental kuning emas mengandung monoterpen dan
sesquiterpen. Monoterpen terdiri dari monoterpen hidrokarbon (alfa pinen,
D-kamfen), monoterpen alkohol (D-borneol), monoterpen keton (D-kamfer),
monoterpen oksida (sineol). Seskuiterpen pada curcuma zedoaria terdiri dari
berbagai golongan dan berdasarkan penggolongan yang dilakukan terdiri dari
golongan bisabolen, elema, germakran, eudesman, guaian dan golongan
spironolakton. Kandungan lain meliputi etil-p-metoksisinamat,
3,7-dimetillindan-5-asam karboksilat (CCRC, 2014).
E. Kurkumin
Kurkumin merupakan senyawa fitokimia yang berwarna kuning-orange
yang secara praktis tidak larut dalam air. Kurkumin merupakan senyawa yang
terdapat dari ekstrak tanaman bergenus Curcuma. Senyawa ini dapat diperoleh
13
dengan ekstraksi menggunakan etanol. Struktur dari Kurkumin (C21H20O6)
pertama kali ditemukan pada tahun 1815 oleh Vogel dan Pellatier (Aggarwal,
Kumar, Shishodia, 2005).
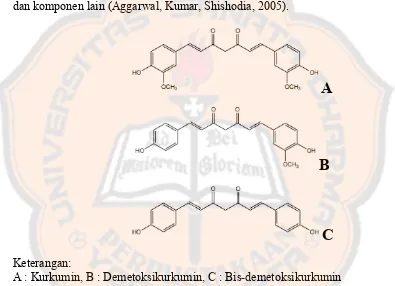
Kurkumin memiliki senyawa derivat lain yang dinamakan kurkuminoid.
Kurkuminoid meliputi kurkumin, demetoksikurkumin, bis-demetoksikurkumin,
dan komponen lain (Aggarwal, Kumar, Shishodia, 2005).
Keterangan:
A : Kurkumin, B : Demetoksikurkumin, C : Bis-demetoksikurkumin
Gambar 4. Struktur dari kurkuminoid (Aggarwal, Kumar, Shishodia, 2005)
Kurkumin yang terkandung dalam rimpang temu putih terbukti memiliki
efek antiradang. Aktivitas antiradang kurkumin pertama kali dilaporkan oleh
Grieve pada tahun 1971 (Dalimartha, 1999).
@
14
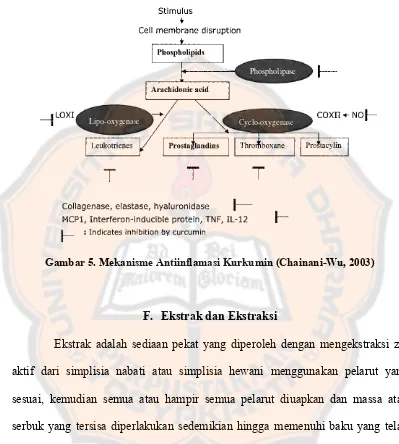
Mekanisme kerja kurkumin sebagai agen antiinflamasi :
Gambar 5. Mekanisme Antiinflamasi Kurkumin (Chainani-Wu, 2003)
F. Ekstrak dan Ekstraksi
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat
aktif dari simplisia nabati atau simplisia hewani menggunakan pelarut yang
sesuai, kemudian semua atau hampir semua pelarut diuapkan dan massa atau
serbuk yang tersisa diperlakukan sedemikian hingga memenuhi baku yang telah
ditetapkan (Depkes RI, 1995).
Ekstraksi adalah kegiatan penarikan kandungan kimia yang dapat larut
sehingga terpisah dari bahan yang tidak dapat larut dengan pelarut cair. Simplisia
yang akan diekstrak mengandung senyawa aktif yang dapat larut dan senyawa
yang tidak dapat larut dan mempunyai struktur kimia yang berbeda-beda yang
Lipo-oxygenase Cyclo-oxygenase Phospholipase
15
dapat mempengaruhi kelarutan dan stabilitas senyawa-senyawa tersebut terhadap
suhu, udara, cahaya, dan logam berat (Depkes RI, 1986).
G. Maserasi
Maserasi adalah suatu metode ekstraksi menggunakan pelarut dengan
beberapa kali pengocokan atau pengadukan pada temperatur ruangan (kamar).
Secara teknologi termasuk ekstraksi dengan prinsip metode pencapaian
konsentrasi pada kesetimbangan. Maserasi kinetik berarti dilakukan pengadukan
yang kontinu (terus menerus). Remaserasi berarti dilakukan pengulangan
penambahan pelarut setelah dilakukan penyaringan maserat pertama dan
seterusnya (Depkes RI, 1986).
H. Emulgel
Emulgel adalah emulsi, baik itu tipe minyak dalam air (M/A) maupun air
dalam minyak (A/M), yang dibuat menjadi sediaan gel dengan mencampurkan
bahan pembentuk gel (Mohamed, 2004). Emulsi adalah suatu sistem yang tidak
stabil secara termodinamika yang mengandung paling sedikit dua fase cair yang
tidak bercampur, di mana satu di antaranya didispersikan sebagai globul-globul
dalam fase cair lain. Fase tersebut terdiri dari fase hidrofil, umumnya adalah air,
dan fase lipofil (hidrofob) yaitu minyak mineral, minyak tumbuhan, atau pelarut
lipofil seperti kloroform, benzen, dan sebagainya. Untuk menstabilkan emulsi
dibutuhkan emulgator atau bahan pengemulsi (Voigt, 1995).
16
Pada emulgel, emulsi dicampurkan ke dalam basis gel yang telah dibuat
secara terpisah. Kapasitas gel dari sediaan emulgel membuat formulasi emulsi
menjadi lebih stabil karena adanya penurunan tegangan permukaan dan tegangan
antar muka secara bersamaan dengan meningkatknya viskositas dari fase air
(Khullar, Deepinder, Nimrata, dan Seema, 2012).
Keuntungan emulgel sebagai bentuk sediaan antara lain adalah dapat
membawa obat yang bersifat hidrofobik dan tidak larut air; stabilitas yang lebih
baik; memungkinkan biaya produksi yang lebih rendah; dapat menjadi sediaan
lepas terkendali untuk obat dengan waktu paruh pendek (Mohamed, 2004).
I. Penetration Enhancer
Penetration enhancer didefinisikan sebagai substansi yang inert secara
farmakologi, tapi dapat berinteraksi dengan barrier stratum korneum ketika
dikombinasikan dengan formulasi transdermal dan dapat mengurangi ketahanan
kulit saat transpor obat (Chantasart, 2012).
Senyawa yang dapat berfungsi sebagai penetration enhancer antara lain:
1. Golongan Alkohol dan Glikol
Alkohol rantai pendek dan senyawa golongan glikol dapat
meningkatkan absorpsi dengan cara meningkatkan fluiditas dari lapisan lipid
pada stratum korneum dengan berinteraksi dengan protein stratum korneum.
2. Amina dan Amida
Senyawa meliputi urea dan derivatnya, asam amino dan esternya,
amida, seperti azone dan derivatnya. Azone banyak diteliti karena dapat
17
meningkatkan permeasi obat dalam spektrum luas. Golongan ini bekerja
dengan cara meningkatkan fluiditas dari lapisan lipid pada stratum korneum.
3. Asam Lemak dan Esternya
Asam lemak tidak jenuh lebih aktif daripada asam lemak jenuh.
Mekanisme aksinya adalah meningkatkan kelarutan dari obat, meningkatkan
partisi obat, meningkatkan penetrasi pelarut dan mengubah struktur barrier
kulit.
4. Terpene
Terpene dapat meningkatkan permeasi perkutan dari obat hidrofilik maupun
hidrofobik. Terpene juga dapat meningkatkan permeasi dari senyawa polar
(Rosen, 2005).
J. Gliserin
Gliserin merupakan nama lain dari gliserol, propan-triol,
1,2,3-propantriol, 1,2,3-trihidroksipropan gliserol dan E422. Sifatnya tidak berwarna,
tidak berbau, higroskopis, rasanya manis, dan berupa cairan viskos. Gliserin dapat
bercampur dengan air (Parfitt, 1999).
Gambar 6. Struktur Gliserin (Rowe, Sheskey, Quinn, 2009)
Gliserin dapat digunakan sebagai penetration enhancer dalam rentang
konsentrasi 0,1-20% (Stinchcomb and Banks, 2010).
18
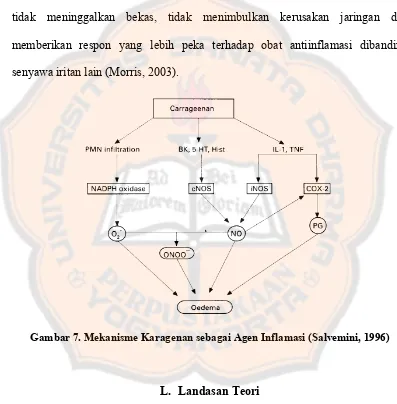
K. Karagenan
Karagenan merupakan salah satu agen pengiritasi. Karagenan merupakan
mukopolisakarida yang tersusun atas monomer galaktosa sulfat. Penggunaan
karagenan sebagai penginduksi radang memiliki beberapa keuntungan antara lain:
tidak meninggalkan bekas, tidak menimbulkan kerusakan jaringan dan
memberikan respon yang lebih peka terhadap obat antiinflamasi dibanding
senyawa iritan lain (Morris, 2003).
Gambar 7. Mekanisme Karagenan sebagai Agen Inflamasi (Salvemini, 1996)
L. Landasan Teori
Temu putih dapat digunakan sebagai antiinflamasi. Kurkumin yang
terkandung dalam rimpang temu putih terbukti memiliki efek antiradang (Grieve,
1971). Kurkumin dapat berfungsi sebagai antiinflamasi dengan menekan aktivitas
dari fosfolipase, lipooksigenase, COX-2, leukotrien, prostaglandin, nitrit oxide,
MCP-1, tumor necrosis factor-alpha (TNF-α), interleukin (IL) (Chainani-Wu,
19
2003). Senyawa kurkumin ini tentu saja kurang nyaman apabila diaplikasikan
langsung ke tubuh melalui kulit sehingga perlu adanya suatu formulasi sediaan
topikal sehingga tidak lengket saat diaplikasikan ke kulit. Sediaan topikal yang
dipilih dalam penelitian ini adalah Emulgel.
Emulgel merupakan dua sistem gabungan, yaitu sistem emulsi dan sistem
gel. Emulgel memiliki stabilitas yang baik selama penyimpanan dalam waktu
yang lama. Selain itu juga dari segi estetika, penampilan sediaan emulgel lebih
baik dari sediaan topikal lainnya. Keuntungan emulgel sebagai bentuk sediaan
antara lain adalah dapat membawa obat yang bersifat hidrofobik dan tidak larut
air, stabilitas yang lebih baik, memungkinkan biaya produksi yang lebih rendah,
dapat menjadi sediaan lepas terkendali untuk obat dengan waktu paruh pendek
(Mohamed, 2004).
Penambahan zat yang berfungsi sebagai penetration enhancer akan
menambah daya permeasi senyawa antiinflamasi tersebut sehingga efek inflamasi
dapat dikurangi. Gliserin dapat digunakan sebagai penetration enhancer dalam
rentang konsentrasi 0,1-20% (Stinchcomb and Banks, 2010). Mekanismenya
dalam meningkatkan absorpsi obat dengan cara meningkatkan fluiditas dari
lapisan lipid pada stratum korneum dengan berinteraksi dengan protein stratum
korneum (Rosen, 2005).
20
M. Hipotesis
1. Sediaan emulgel dengan esktrak etanol rimpang temu putih dapat dihasilkan
dengan sifat fisik yang memenuhi kriteria.
2. Sediaan emulgel dengan ekstrak temu putih memiliki aktivitas sebagai
antiinflamasi.
3. Penambahan konsentrasi gliserin memiliki pengaruh sebagai penetration
enhancer pada formulasi sediaan emulgel ekstrak etanol rimpang temu putih.
BAB III
METODE PENELITIAN
A. Jenis dan Rancangan Penelitian
Penelitian yang dilakukan merupakan jenis penelitian ekperimental
murni dengan rancangan acak pola searah.
B. Variabel Penelitian dan Definisi Operasional 1. Variabel penelitian
a. Variabel bebas
Konsentrasi gliserin sebagai penetration enhancer yang akan digunakan.
b. Variabel tergantung
Sifat fisik gel yang meliputi viskositas, daya sebar dan tebal udema pada
telapak kaki tikus.
c. Variabel pengacau terkendali
Jenis tikus, umur tikus, jenis kelamin tikus, kecepatan dan lama
pengadukan sediaan emulgel temu putih, wadah penyimpanan, dan kondisi
penyimpanan.
d. Variabel pengacau tak terkendali
Kondisi patofisiologis tikus, suhu dan kelembaban ruangan.
22
2. Definisi Operasional
a. Emulgel adalah sediaan semisolid hasil emulsifikasi dan penambahan
carbopol 940 yang mengandung ekstrak etanol temu putih dengan
konsentrasi 7% yang dibuat sesuai dengan formula yang tercantum dalam
penelitian ini.
b. Inflamasi adalah reaksi tubuh terhadap mikroorganisme dan benda asing
yang ditandai oleh panas, bengkak, nyeri, dan gangguan fungsi organ
tubuh. Dalam penelitian ini adalah bengkak (udema).
c. Aktivitas antiinflamasi adalah kemampuan emulgel temu putih untuk
mereduksi udema pada telapak kaki tikus ditunjukkan dengan % reduksi
udema.
d. Sifat fisikadalah parameter untuk mengetahui kualitas emulgel temu putih
yang dihasilkan.
e. Viskositas adalah kemampuan tahanan dari sediaan emulgel temu putih
untuk mengalir.
23
C. Bahan Penelitian
Bahan yang digunakan dalam penelitian ini adalah temu putih (BPTO),
etanol 70% (Bratachem), carbopol (Bratachem), gliserin (Bratachem), tween 80
(Bratachem), paraffin cair (Bratachem), metil paraben (Bratachem), trietanolamin,
span 80, propil paraben (Laboratorium FTS-Solid Fakultas Farmasi Universitas
Sanata Dharma Yogyakarta), Karagenan, NaCl (Laboratorium Biofarmasetika
Fakultas Farmasi Universitas Sanata Dharma Yogyakarta), Voltaren Emulgel®
(NOVARTIS), aquadest steril, hewan uji tikus (Laboratorium Imono Fakultas
Farmasi Universitas Sanata Dharma Yogyakarta).
D. Alat Penelitian
Alat yang digunakan dalam penelitian ini adalah orbital shaker (Optima),
rotary evaporator (Buchi Labortechnik AG CH-9230), mixer (Phillips),
waterbath (Memmert), viscotester (Rion VT-04), indikator pH universal
(MERCK), termometer, neraca analitik, alat uji daya sebar, alat-alat gelas
(Laboratorium FTS-Solid Fakultas Farmasi Universitas Sanata Dharma
Yogyakarta), spuit, jangka sorong Digital Caliper (Wipro).
E. Tata Cara Penelitian 1. Pembuatan ekstrak etanol rimpang temu putih
Bahan baku serbuk ditimbang sebanyak 20 gram, lalu dimasukkan ke
dalam wadah maserasi. Sebanyak 200 ml etanol 70% ditambahkan sebagai
pelarut. Maserasi dilakukan dengan menggunakan orbital shaker selama 1x24
24
jam. Dilakukan penyaringan dengan corong Buchner dan kertas saring untuk
mengambil ekstrak. Ekstrak yang sudah diambil kemudian dimasukkan ke
rotary evaporator untuk menguapkan sisa etanol. Dilakukan proses
penguapan pelarut dengan waterbath dengan suhu 70oC. Dilakukan
pengovenan pada suhu 40o C untuk menghitung bobot tetap.
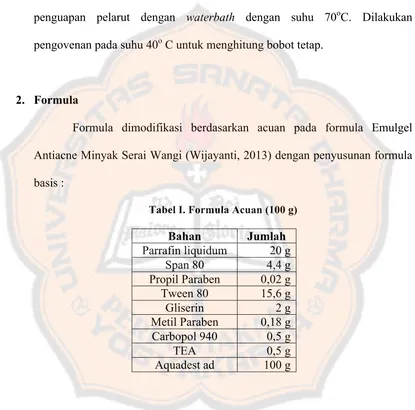
2. Formula
Formula dimodifikasi berdasarkan acuan pada formula Emulgel
Antiacne Minyak Serai Wangi (Wijayanti, 2013) dengan penyusunan formula
basis :
Tabel I. Formula Acuan (100 g)
Bahan Jumlah
Parrafin liquidum 20 g Span 80 4,4 g
25
Komposisi formula setelah dimodifikasi sebagai berikut:
Tabel II. Formula Emulgel Modifikasi (100 g)
Nama Bahan F1 F2 F3 F4
F1 : Formula dengan ekstrak 7% dan gliserin 0% F2 : Formula dengan ekstrak 7% dan gliserin 2,5% F3 : Formula dengan ekstrak 7% dan gliserin 5% F4 : Formula dengan ekstrak 7% dan gliserin 10%
3. Pembuatan emulgel temu putih
Carbopol didispersikan pada aquadest, didiamkan hingga
mengembang sempurna selama 24 jam. Bahan-bahan ditimbang, lalu
dipisahkan menurut fase minyak dan fase air. Fase minyak yaitu paraffin cair,
propil paraben, dan Span 80, sedangkan fase air yaitu gliserin, aquadest, metil
paraben, dan Tween 80. Kedua fase dipanaskan hingga suhu 50°C di atas
waterbath, lalu dicampur dengan menggunakan mixer 300 rpm selama ± 5
menit. Setelah terbentuk emulsi, ditambahkan carbopol 940 yang telah
dikembangkan 1x24 jam. Ekstrak temu putih ditambahkan, diaduk kembali ±
5 menit. Kemudian trietanolamin (TEA) ditambahkan sedikit demi sedikit
sambil diaduk perlahan ± 5 menit. Sesekali dicek pH, hingga didapatkan pH
sekitar 6. Sediaan dimasukkan dalam wadah kedap cahaya.
26
4. Uji sifat fisik emulgel temu putih
a. Organoleptis
Pemeriksaan organoleptis meliputi bentuk, warna dan bau yang
diamati secara visual.
b. Pengukuran pH
Pengukuran pH dilakukan menggunakan indicator universal,
yaitu dengan memasukkan pH universal yang berbentuk strip ke dalam
emulgel, lalu ditentukan pHnya dengan membandingkan warnanya
dengan standar warna yang ada.
c. Uji daya sebar
Sebanyak 1 gram emulgel diletakkan di atas kaca bulat berskala.
Diatasnya diletakkan kaca bulat lain dengan beban seberat 50 gram,
didiamkan selama 1 menit, lalu dicatat penyebarannya. Uji dilakukan
setelah 48 jam dari pembuatan, hingga setelah 1 bulan penyimpanan.
Dilakukan 3 kali replikasi.
d. Uji viskositas
Pengukuran viscotester menggunakan alat Viscometer Rion seri
VT 04. Emulgel dimasukkan perlahan-lahan ke dalam wadah dan
dipasang pada viscotester. Viscotester dinyalakan. Nilai viskositas
emulgel diperoleh dengan mengamati gerakan jarum petunjuk pada
viscotester setelah jarum stabil. Uji dilakukan setelah 48 jam dari
pembuatan, hingga setelah 1 bulan penyimpanan. Dilakukan 3 kali
replikasi.
27
5. Uji aktifitas antiinflamasi rimpang temu putih dalam sediaan emulgel a. Penyiapan hewan uji
Hewan uji yang digunakan dalam penelitian ini adalah tikus
betina, galur Wistar, usia 2-3 bulan, dengan berat badan 120-150 gram.
Sebelum digunakan, tikus dipuasakan 18-24 jam dan tetap diberi minum.
Kelompok perlakuan terdiri dari kontrol negatif karagenan 1%, kontrol
positif Natrium Diklofenak, kontrol basis sediaan emulgel dan kelompok
perlakuan emulgel ekstrak etanol Temu Putih (Curcuma zedoaria Berg.
Roscoe).
b. Pembuatan larutan NaCl 0,9%
NaCl ditimbang sebanyak 0,225 g, dilarutkan dalam 25 ml
aquadest.
c. Pembuatan suspensi karagenan 1%
Karagenan ditimbang sebanyak 0,2 mg, dilarutkan dalam larutan
NaCl fisiologis 0,9% dalam labu takar 20 ml.
d. Uji aktivitas antiinflamasi
Hewan uji dibagi menjadi tiga kelompok, yaitu :
1) Kelompok kontrol positif
Kaki belakang hewan uji diukur menggunakan jangka sorong
sebelum disuntik karagenan 1%. Karagenan 1% disuntikkan secara
subplantar pada kaki belakang tikus. Diukur udema setelah 2 jam
pemberian karagenan 1%, dan dilakukan pengolesan Voltaren
Emulgel®. Diamati penurunan udema pada waktu 4 jam dan 24 jam.
28
2) Kelompok kontrol negatif
Kaki belakang hewan uji diukur menggunakan jangka sorong
sebelum disuntik karagenan 1%. Karagenan 1% disuntikkan secara
subplantar pada kaki belakang tikus. Diukur udema setelah 2 jam
pemberian karagenan 1%, tidak dilakukan pengolesan apapun.
Diamati penurunan udema pada waktu 4 jam dan 24 jam.
3) Kelompok emulgel ekstrak temu putih
Kaki belakang hewan uji diukur menggunakan jangka sorong
sebelum disuntik karagenan 1%. Karagenan 1% disuntikkan secara
subplantar pada kaki belakang tikus. Diukur udema setelah 2 jam
pemberian karagenan 1%, dan dilakukan pengolesan emulgel ekstrak
temu putih. Diamati penurunan udema pada waktu 4 jam dan 24 jam.
e. Perhitungan respon daya antiinflamasi
Perhitungan respon dilakukan dengan mengukur tebal udema
yang terjadi pada kaki tikus dengan menggunakan jangka sorong. Lalu
dihitung persentase reduksi udema dari tiap sediaan dengan menggunakan
rumus :
% reduksi udema=!"#$% !"#$!!"#$% !"#$%
!"#$% !"#$ x 100%
(Kharat, 2010).
29
F. Analisis Hasil
Data organoleptis dilakukan secara kualitatif. Daya sebar dilihat dari
hasil uji daya sebar. Viskositas emulgel dilihat dari nilai yang tertera pada
viscotester pH emulgel dilihat dari warna pada pH indikator. Data yang ada dari
48 jam hingga 1 bulan penyimpanan.
Hasil aktivitas antiinflamasi emulgel ekstrak Temu Putih (Curcuma
zedoaria Berg. Roscoe)dianalisis secara statistik dengan Test Shapiro Wilk untuk
melihat distribusi data. Jika distribusi data normal, dilanjutkan dengan Levene
Test untuk melihat kehomogenan data. Jika data homogen dilanjutkan dengan
menggunakan ANOVA satu arah dengan taraf kepercayaan 95%, selanjutnya
dilakukan uji Tukey dengan menggunakan aplikasi program R versi 3.0.1.
30 BAB IV
HASIL DAN PEMBAHASAN
A. Hasil Determinasi Tanaman
Pada penelitian ini, bahan yang digunakan adalah rimpang tanaman temu
putih yang diperoleh dari Balai Penelitian Tanaman Obat Tawangmangu.
Determinasi tanaman dilakukan oleh Balai Penelitian Tanaman Obat
Tawangmangu untuk memastikan bahwa tanaman yang digunakan oleh peneliti
benar-benar rimpang tanaman temu putih dengan nama ilmiah Curcuma zedoaria.
Dan hasil yang didapatkan tanaman yang digunakan benar adanya rimpang temu
putih.
B. Hasil Standarisasi Ekstrak
Pada penelitian ini dilakukan standarisasi ekstrak yang meliputi
penetapan kadar kurkumin dan pengujian kadar air yang terkandung dalam
ekstrak etanol rimpang temu putih. Standarisasi ekstrak dilakukan oleh
Laboratorium Penelitian dan Pengembangan Terpadu (LPPT) Universitas Gadjah
Mada Yogyakarta. Dari hasil standarisasi diketahui bahwa kandungan kurkumin
dalam ekstrak etanol rimpang temu putih sebesar 87,53 ppm dan kadar airnya
sebesar 24,25%.
31
C. Hasil Uji Sifat Fisik dan Stabilitas Emulgel
Sifat fisik dari emulgel meliputi viskositas dan daya sebar, sedangkan
stabilitasnya dinyatakan dalam respon pergeseran viskositas. Sediaan dapat
dikatakan baik apabila dapat memenuhi persyaratan sifat fisik dan stabil selama
masa penyimpanan. Pengujian sifat fisik dan stabilitas ini diukur selama 28 hari
dengan rentang waktu hari ke-2, ke-7, ke-14, ke-21 dan ke-28.
Tabel III. Hasil Uji Organoleptis
Formula
Kriteria F1 F2 F3 F4
Warna Coklat Muda Coklat Muda Coklat Muda Coklat Muda
Bau Khas Khas Khas Khas
pH 5,5 ± 0 5,5 ± 0 5,5 ± 0 5,5 ± 0
Keterangan :
F1 = Formula dengan ekstrak 7% dan gliserin 0% F2 = Formula dengan ekstrak 7% dan gliserin 2,5% F3 = Formula dengan ekstrak 7% dan gliserin 5% F4 = Formula dengan ekstrak 7% dan gliserin 10%
1. Uji organoleptis
Uji organoleptis meliputi pengamatan warna dan bau.
2. Uji pH
Uji pH dilakukan dengan menggunakan kertas pH indikator. Dari tabel III dapat
dilihat bahwa pH semua formula berkisar antara 5-6. pH yang dimiliki semua
formula sudah masuk dalam range. pH sediaan kulit yang diperbolehkan berkisar
antara 5-6 (Heater and Adam, 2012).
32
Tabel IV. Hasil Uji Sifat Fisik Emulgel
Formula Viskositas (d.Pa.s) Daya Sebar (cm) F1 316,7 ± 20,8 4,91 ± 0,04
F2 373,3 ± 25,2 4,34 ± 0,04
F3 456,7 ± 20,8 3,95 ± 0,05
F4 520 ± 26,5 3,68 ± 0,05
3. Viskositas
Viskositas dikatakan sebagai suatu besaran yang menunjukkan
ketahanan dari suatu cairan untuk dapat mengalir. Viskositas suatu bentuk
sediaan akan berpengaruh terhadap proses aplikasi ke kulit dan proses
pengemasan sediaan tersebut.
Pengukuran viskositas dilakukan 48 jam setelah pembuatan.
Pemilihan waktu ini diharapkan pada 48 jam saat pembuatan, sediaan sudah
tidak akan berubah, tidak terkena pengaruh dari luar lagi. Pengukuran
dilakukan dengan menggunakan viscotester, menggunakan putaran nomor 2.
Pada bentuk sediaan semisolid, viskositas akan berbanding terbalik
dengan daya sebar. Semakin kecil viskositas yang didapat, maka semakin
besar daya sebarnya, dan sebaliknya. Peneliti menentukan rentang viskositas
sekitar 250 – 400 d.Pa.s, hal ini dikarenakan agar sediaan tidak terlalu kental
dan juga tidak terlalu encer, sehingga nyaman untuk diaplikasikan.
Dari Tabel IV dapat dilihat bahwa respon viskositas yang didapat ada
yang masuk ke dalam range yang telah ditentukan, dan ada yang tidak.
Formula 3 dan 4 tidak masuk ke dalam range. Hal ini dimungkinkan karena
adanya penambahan jumlah gliserin dalam jumlah yang cukup banyak,
sehingga sangat membuat sediaan semakin kental.
33
4. Daya sebar
Pengukuran daya sebar dikatakan bertujuan untuk mengetahui
seberapa besar diameter penyebaran suatu sediaan saat diaplikasikan ke kulit.
Pengukuran dilakukan setelah 48 jam pembuatan. Pengukuran daya sebar
dilakukan dengan cara meletakkan sediaan diatas kaca bundar berskala, dan
diberi beban 50 gram selama 1 menit.
Pada bentuk sediaan semisolid, daya sebar akan berbanding terbalik
dengan viskositas. Semakin kecil daya sebar yang didapat, maka semakin
besar viskositasnya, dan sebaliknya. Peneliti menentukan rentang daya sebar
sekitar 3-5 cm, hal ini dikarenakan agar sediaan tidak terlalu kental dan juga
tidak terlalu encer, sehingga nyaman untuk diaplikasikan.
Dari Tabel IV dapat dilihat bahwa respon daya sebar yang didapat
masuk ke dalam range yang telah ditentukan.
5. Stabilitas sediaan
Stabilitas sediaan selama masa penyimpanan dapat diuji dengan
menggunakan perbandingan antara hari ke-2 dan ke-28. Hari ke-28
diasumsikan sebagai lamanya sediaan akan digunakan setelah dari awal
kemasan dibuka. Stabilitas sediaan dapat dilihat dari % pergeseran viskositas
yang dimiliki sediaan. % pergeseran viskositas dapat dihitung dengan
menggunakan rumus :
% pergeseran viskositas=!"#$%#"&'# !"#$ !"!! !!"#$%#"&'# !"#$ !"!!"
!"#$%#"&'# !"#$ !"!! x 100%
34
Dari rumus di atas, didapatkan perhitungan pergeseran viskositas
sebagai berikut :
Tabel V. Hasil Pergeseran Viskositas
Formula % Pergeseran Viskositas F1 22,073 ± 2,356
F2 6,937 ± 6,021
F3 15,303 ± 1,747
F4 7,523 ± 5,371
Pergeseran viskositas yang baik adalah dibawah 10% (Wiranata,
2011). Dari hasil perhitungan, formula 1 dan 3 tidak masuk dalam range,
sedangkan formula 2 dan 4 masuk.
Dilakukan juga perhitungan pergeseran viskositas dengan
menggunakan statistik. Yang dibandingkan adalah hari ke-2 dan ke-28. Hasil
p-value yang didapatkan adalah sebagai berikut :
Tabel VI. Hasil Pergeseran Viskositas dengan Menggunakan Statistik
Formula p-value Keterangan F1 0,008 BB
menghasilkan nilai p-value < 0,05, hal ini berarti sediaan pada hari ke-2 dan
ke-28 berbeda bermakna, dengan kata lain tidak stabil secara statistik.
Sedangkan untuk formula 2 dan 4 memiliki p-value > 0,05, berarti sediaan
35
pada hari ke-2 dan ke-28 berbeda tidak bermakna, dengan kata lain stabil
secara statistik.
Dari kedua hasil perhitungan diatas, dapat disimpulkan bahwa sediaan
dengan formula 1 dan 3 tidak stabil selama penyimpanan, sedangkan sediaan
dengan formula 2 dan 4 stabil selama penyimpanan. Ketidakstabilan suatu
sediaan dapat disebabkan oleh suhu dan kondisi ruang penyimpanan yang
tidak dijaga dengan baik.
D. Pengujian Efek Antiinflamasi Emulgel
Pengujian efek antiinflamasi dilakukan untuk mengetahui apakah sediaan
emulgel benar memiliki efek antiinflamasi dan juga untuk mengetahui seberapa
besar efek antiinflamasi yang dapat dihasilkan oleh sediaan emulgel tersebut.
Inflamasi ditandai dengan terjadinya pembengkakan (udema) pada suatu bagian,
dalam penelitian ini adalah kaki tikus akibat injeksi suspensi karagenan 1%.
Sedangkan antiinflamasi adalah suatu kemampuan untuk mengurangi
pembengkakan (udema), dalam penelitian ini adalah sediaan emulgel. Aktivitas
antiinflamasi dari ekstrak dapat dilihat dari ada tidaknya kemampuan sediaan
emulgel untuk menurunkan udema yang terjadi.
Penelitian ini menggunakan tikus betina galur Wistar. Pemilihan hewan
uji ini dikarenakan tidak sulit untuk didapatkan, apabila dibandingkan dengan
yang jantan. Tikus jantan memiliki kelebihan apabila dilakukan untuk suatu
pengujian, maka tidak akan mudah terpengaruh dengan hormon yang ada dalam
tubuh tikus itu sendiri. Namun, karena yang dibutuhkan adalah jaringan kulit pada
36
telapak kaki tikus dan proses inflamasi tidak dpengaruhi oleh hormon, maka
dipilih tikus betina sebagai hewan uji.
Hewan uji dibagi menjadi 10 kelompok perlakuan. Kelompok pertama
merupakan kelompok kontrol positif adalah Voltaren Emulgel® yang mengandung
Dietilamin Diklofenak. Kelompok kedua merupakan kelompok kontrol negatif
yaitu karagenan 1% sebagai zat penginduksi udema. Selanjutnya kelompok
perlakuan basis emulgel dengan kadar gliserin 0%, 2,5%, 5%, dan 10%.
Kelompok perlakuan basis ini dianggap termasuk kontrol negatif, yang dapat
digunakan sebagai perbandingan dengan sediaan yang mengandung ekstrak.
Kelompok yang terakhir merupakan kelompok perlakuan emulgel dengan ekstrak
etanol temu putih 7% dengan kadar gliserin pada tiap formula adalah 0%, 2,5%,
5%, dan 10%.
Pada penelitian ini, tebal udema kaki tikus diukur dengan menggunakan
jangka sorong. Jangka sorong memiliki beberapa kelebihan dalam
penggunaannya, antara lain, mudah digunakan, memiliki angka yang cukup
akurat, dan tidak diperlukannya mengorbankan hewan uji seperti metode potong
kaki.
Agen penginduksi inflamasi yang digunakan adalah suspensi karagenan
1% yang dilarutkan dalam NaCl 0,9%. Selain itu karagenan dikatakan memiliki
beberapa kelebihan sebagai agen penginduksi, antara lain tidak menimbulkan
bekas, tidak menimbulkan kerusakan jaringan dan memberikan respon yang lebih
peka terhadap obat anti-inflamasi. Pembengkakan yang dihasilkan oleh karagenan
melalui dua tahap setelah diinjeksikan ke tubuh. Yang pertama adanya pelepasan
37
histamine, serotonin, dan bradikinin, lalu yang kedua pelepasan prostaglandin
yang nantinya akan menyebabkan migrasi leukosit ke lokasi radang (Foye, 1981).
Kontrol positif yang digunakan pada penelitian ini adalah Voltaren
Emulgel® yang mengandung natrium dietilamin. Kontrol positif ini dipilih karena
sudah beredar di pasaran dan telah teruji aktivitas antiinflamasinya. Natrium
diklofenak dapat menghambat sintesis prostaglandin.
Pada kelompok kontrol negatif, yaitu suspensi karagenan 1%, kaki
belakang mencit diinduksi dengan menggunakan suspensi karagenan 1%, dan
tidak diberi perlakuan apapun. Hal ini dilakukan untuk melihat bagaimana kondisi
kaki tikus tanpa perlakuan apapun, untuk membandingkan hasilnya dengan
kelompok perlakuan.
Pada kelompok kontrol positif, yaitu Voltaren Emulgel®, kaki belakang
mencit diinduksi dengan menggunakan suspensi karagenan 1%, lalu dioles
Voltaren Emulgel® pada waktu 2 jam setelah injeksi.
Pada kelompok basis sediaan, sama halnya dengan kontrol positif, kaki
belakang mencit diinduksi dengan menggunakan suspensi karagenan 1%, lalu
dioles basis sediaan tiap formula pada waktu 2 jam setelah injeksi.
Pada kelompok perlakuan sediaan yang mengandung ekstrak etanol
rimpang temu putih. Sama halnya dengan kontrol positif, kaki belakang mencit
diinduksi dengan menggunakan suspensi karagenan 1%, lalu dioles emulgel
ekstrak temu putih tiap formula pada waktu 2 jam setelah injeksi.
Kadar ekstrak temu putih yang dikandung tiap sediaan sama, yaitu
sebesar 7%. Yang berbeda dari tiap sediaan adalah konsentrasi gliserin yang
38
diduga dapat berfungsi sebagai penetration enhancer yang nantinya dapat
mempercepat proses permeasi obat ke dalam jaringan kulit.
Waktu pengolesan sediaan ditentukan oleh peneliti setelah 2 jam melalui
hasil orientasi waktu pembengkakan yang paling optimal. Orientasi dilakukan
dengan menginduksi kaki bagian belakang tikus dengan karagenan 1%, lalu
udema diukur selama 6 jam setiap 30 menit. Dari hasil didapatkan bahwa bengkak
yang paling optimum terjadi pada jam kedua setelah induksi karagenan 1%.
Setelah itu udema diukur lagi pada waktu 4 jam dan 24 jam setelah
injeksi. Pada waktu 4 jam setelah injeksi, diharapkan sediaan sudah mampu untuk
menunjukkan aktivitas antiinflamasinya. Sedangkan pada saat 24 jam untuk
melihat bagaimana kemampuan reduksi udema dari sediaan secara total.
E. Hasil Uji Antiinflamasi Emulgel
Hasil uji antiinflamasi emulgel berupa % reduksi udema kaki tikus pada
tiap kelompok perlakuan di pengukuran waktu 4 jam dan 24 jam.
Dari tabel VII dapat dilihat bahwa % reduksi yang paling besar adalah
dari kelompok perlakuan sediaan emulgel dengan ekstrak 7% dan gliserin 10%,
sedangkan % reduksi udema yang paling kecil adalah dari kelompok basis
sediaan. Pada kelompok perlakuan sediaan dengan ekstrak, dapat dilihat bahwa
semakin bertambahnya kadar gliserin yang digunakan, semakin besar penurunan
udema yang terjadi. Dari hal ini dapat dikatakan bahwa kadar gliserin disini juga
memiliki pengaruh dalam sediaan. Fungsinya sebagai penetration enhancer dapat
39
membawa obat lebih cepat masuk ke dalam jaringan kulit dan menurunkan efek
inflamasi lebih cepat.
Tabel VII. Hasil % Reduksi Udema Kaki Tikus
Kelompok Perlakuan
% Reduksi Udema Kaki Tikus jam ke-4
% Reduksi Udema Kaki Tikus jam ke-24
F1 = Formula dengan ekstrak 7% dan gliserin 0% F2 = Formula dengan ekstrak 7% dan gliserin 2,5% F3 = Formula dengan ekstrak 7% dan gliserin 5% F4 = Formula dengan ekstrak 7% dan gliserin 10%
Untuk mengetahui kekuatan antiinflamasinya, maka dilakukan analisis
statistik terhadap % reduksi udema pada tiap jam pengukuran.
Tabel VIII menunjukkan bahwa kelompok kontrol positif memiliki
kesamaan dengan kelompok ekstrak, hal ini ditunjukkan dari nilai p-value nya
yang berada diatas 0,05. Dapat dikatakan bahwa emulgel memiliki kemampuan
yang sama dalam mereduksi udema dengan kontrol positif secara statistik.
Kelompok kontrol positif jika dibandingkan dengan kelompok kontrol
negatif dan kelompok basis memiliki perbedaan yang bermakna yang ditunjukkan
dari nilai p-value nya yang berada dibawah 0,05. Dapat disimpulkan bahwa
kelompok kontrol negatif dan kelompok basis tidak memiliki kemampuan untuk
mereduksi udema seperti yang dimiliki kelompok kontrol positif.
40
Tabel VIII. Hasil Uji Statistik % Reduksi Udema Pada Jam Ke-4
Perlakuan p-value Keterangan
Kontrol positif
F1 = Formula dengan ekstrak 7% dan gliserin 0% F2 = Formula dengan ekstrak 7% dan gliserin 2,5% F3 = Formula dengan ekstrak 7% dan gliserin 5% F4 = Formula dengan ekstrak 7% dan gliserin 10%
Tabel VIII juga menunjukkan bahwa kelompok kontrol negatif memiliki
kesamaan dengan kelompok basis dan berbeda dengan semua kelompok ekstrak.
Hal ini ditunjukkan dengan nilai p-value masing-masing perbandingan. Dapat
disimpulkan bahwa kelompok kontrol negatif dan basis tidak memiliki
41
kemampuan mereduksi udema atau tidak memiliki pengaruh pada penurunan
udema kaki tikus, sedangkan kelompok ekstrak memiliki kemampuan mereduksi
udema, sehingga dikatakan memiliki perbedaan secara statistik.
Tabel VIII menunjukkan bahwa pada jam ke-4, semua kelompok ekstrak
tidak memiliki perbedaan dilihat dari nilai p-value nya. Dapat dikatakan bahwa
penambahan gliserin sebagai penetration enhancer pada jam ke-4 tidak terlihat,
karena tidak ada perbedaan diantara semua kelompok sediaan.
Dilanjutkan dengan analisis statistik untuk pengukuran reduksi udema
pada jam ke-24.
Tabel IX menunjukkan bahwa setelah 24 jam kelompok kontrol positif
memiliki kesamaan dengan kelompok ekstrak 0% hingga ekstrak 5%, hal ini
ditunjukkan dari nilai p-value nya yang berada diatas 0,05. Dapat dikatakan
bahwa emulgel memiliki kemampuan yang sama dalam mereduksi udema dengan
kontrol positif secara statistik. Namun, dengan kelompok ekstrak 10% dikatakan
berbeda secara statistik. Untuk melihat apakah berbedanya lebih tinggi atau lebih
rendah, dilakukan uji T-test. Dari hasil uji T-test didapatkan bahwa kelompok
ekstrak 10% lebih tinggi daripada kelompok kontrol positif. Dari hasil ini dapat
disimpulkan bahwa kelompok ekstrak 10% memiliki kemampuan yang lebih baik
dalam mereduksi udema daripada kontrol positif.
Kelompok kontrol positif jika dibandingkan dengan kelompok kontrol
negatif dan kelompok basis memiliki perbedaan yang bermakna yang ditunjukkan
dari nilai p-value nya yang berada dibawah 0,05. Dapat disimpulkan bahwa
setelah 24 jam kelompok kontrol negatif dan kelompok basis juga tidak memiliki
42
kemampuan untuk mereduksi udema seperti yang dimiliki kelompok kontrol
positif.
Tabel IX. Hasil Uji Statistik % Reduksi Udema Pada Jam Ke-24
Perlakuan p-value Keterangan
Kontrol positif
F1 = Formula dengan ekstrak 7% dan gliserin 0% F2 = Formula dengan ekstrak 7% dan gliserin 2,5% F3 = Formula dengan ekstrak 7% dan gliserin 5% F4 = Formula dengan ekstrak 7% dan gliserin 10%
43
Dari tabel IX dapat dilihat bahwa setelah 24 jam kelompok kontrol
negatif memiliki kesamaan dengan kelompok basis dan berbeda dengan semua
kelompok ekstrak. Hal ini ditunjukkan dengan nilai p-value masing-masing
perbandingan. Dapat disimpulkan bahwa setelah 24 jam kelompok kontrol negatif
dan basis tidak memiliki kemampuan mereduksi udema atau tidak memiliki
pengaruh pada penurunan udema kaki tikus, sedangkan kelompok ekstrak
memiliki kemampuan mereduksi udema, sehingga dikatakan memiliki perbedaan
secara statistik.
Tabel IX menunjukkan bahwa pada jam ke-24, kelompok ekstrak 0%,
kelompok ekstrak 2,5%, dan kelompok ekstrak 5% memiliki perbedaan dengan
kelompok ekstrak 10% dilihat dari nilai p-value nya. Dapat dikatakan bahwa
penambahan gliserin sebagai penetration enhancer pada jam ke-24 sudah terlihat,
dengan adanya penambahan gliserin sebanyak 10% membuat udema lebih banyak
tereduksi daripada konsentrasi yang lebih kecil.
Pengukuran persentase reduksi udema dari emulgel tidak hanya dapat
dilakukan pada waktu jam ke-4 dan jam ke-24 saja, melainkan dapat diukur juga
pada selang waktu antara jam ke-4 sampai jam ke-24. Dengan waktu pengukuran
yang lebih banyak akan didapatkan hasil profil penurunan udema yang lebih baik.
44
BAB V
KESIMPULAN DAN SARAN
A. Kesimpulan
1. Sediaan emulgel ekstrak temu putih memiliki viskositas yang memenuhi
syarat untuk formula 1 dan 2, sedangkan untuk formula 3 dan 4 tidak
memenuhi syarat. Untuk daya sebar, semua formula memenuhi persyaratan.
Untuk formula yang paling optimal adalah F2.
2. Sediaan emulgel ekstrak temu putih memiliki aktivitas antiinflamasi.
3. Penambahan konsentrasi gliserin sebagai penetrationenhancer pada formulasi
sediaan emulgel ekstrak temu putih memiliki pengaruh terhadap aktivitas
antiinflamasi yang diukur melalui persentase reduksi udema.
B. Saran
1. Perlu dilakukan metode lain yang lebih akurat untuk mengukur daya penetrasi
dari suatu bahan dalam formulasi.
2. Perlu dilakukan penggantian bahan lain selain gliserin yang dapat berfungsi
sebagai penetration enhancer.