Monocystis SEBAGAI PARASIT CACING TANAH
ANDY DARMAWAN
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
ANDY DARMAWAN. Monocystis sebagai Parasit Cacing Tanah. Dibimbing oleh TARUNI SRI PRAWASTI dan BAMBANG SURYOBROTO.
Monocystis merupakan kelompok Gregarina parasit yang umum menyerang Annelida.
Pheretima darnleiensis merupakan Annelida yang biasa menjadi inang Monocystis. Dalam penelitian ini dilakukan pengamatan terhadap Monocystis yang ditemukan pada cacing tanah
Pheretima darnleiensis yang diperoleh dari lingkungan sekitar kampus IPB Gunung Gede dan Baranangsiang. Monocystis menginfeksi cacing tanah Pheretima darnleiensis dengan intensitas 500 – 1 074 000 oocyst/mm3
cairan vesikula seminalis. Intensitas Monocystis pada cacing tanah berkaitan dengan lokasi ditemukannya cacing tanah. Tropozoit bulat hingga agak oval dengan diameter 38.85 μm – 126.91 μm, nukleus bulat dengan diameter 7.77 μm – 12.95 μm. Gametosit bulat dengan diameter 7.77 μm – 12.95 μm. Oocyst seperti lemon dengan ukuran 7.77 μm – 15.45 μm x 3.88 μm – 7.77 μm.
ABSTRACT
ANDY DARMAWAN. Monocystis as Earthworm Parasite. Supervised by TARUNI SRI PRAWASTI and BAMBANG SURYOBROTO.
Monocystis is parasite gregarine which infects Annelid. Pheretima darnleiensis is a common host for Monocystis. In this research, Monocystis in Pheretima darnleiensis which were collected from Zoology and Baranangsiang, Department of Biology Faculty of Mathematic and Natural Science IPB, were examined. Oocyst concentration which found in earthworm was 500 – 1 074 000 oocyst/mm3 seminal vesicle liquid. Monocystis load was related with location of
Monocystis SEBAGAI PARASIT CACING TANAH
ANDY DARMAWAN
Skripsi
sebagai salah satu syarat untuk memperoleh gelar
Sarjana Sains pada
Departemen Biologi
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul Skripsi :
Monocystis
SEBAGAI PARASIT CACING TANAH
Nama
: Andy Darmawan
NIM
: G34103002
Menyetujui,
Dra. Taruni Sri Prawasti
Dr. Bambang Suryobroto
NIP.131284837
NIP.131779503
Mengetahui,
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Prof. Dr. Ir. Yonny Koesmaryono, M.S.
NIP.131473999
PRAKATA
Terima kasih kepada Tuhan YME sehingga karya ilmiah ini dapat diselesaikan. Penulis juga mengucapkan terima kasih kepada Ibu Dra. Taruni Sri Prawasti dan Bapak Dr. Bambang Suryobroto selaku pembimbing, Bapak Ir. Hadisunarso selaku dosen penguji atas sarannya, Bapak Ir. Tri Heru Widarto, M.Sc. untuk diskusinya, Mbak Tini dan Pak Djupri untuk bimbingan di laboratorium, seluruh staf zoologi dan anggota zoologi atas kebersamaannya, dan orang tua penulis atas dukungannya.
Semoga karya ilmiah ini bermanfaat bagi ilmu pengetahuan.
Bogor, Agustus 2007
RIWAYAT HIDUP
DAFTAR ISI
Halaman
DAFTAR GAMBAR... vii
PENDAHULUAN Latar Belakang...1
Tujuan...1
Waktu dan Tempat... 1
BAHAN DAN METODE Bahan dan Alat... 1
Pengambilan sampel... 1
Pengamatan Monocystis... 2
Penghitungan jumlah Monocystis...2
HASIL Pengamatan Monocystis... 2
Penghitungan jumlah Monocystis...3
PEMBAHASAN... 4
SIMPULAN...5
SARAN... 5
DAFTAR GAMBAR
Halaman
1 Organ dalam cacing ... 2
2 Oocyst ... 2
3 Gametosit dengan dua tropozoit ... 2
4 Gametosit dengan residual body ... 3
5 Gametosit dengan oocyst ... 3
6 Tropozoit dengan sperma ... 3
1
PENDAHULUAN
Latar Belakang
Monocystis merupakan kelompok
Gregarina parasit yang umum menyerang Annelida (Omoto & Cartwright 2003). Cacing tanah merupakan Annelida yang biasa menjadi inang Monocystis (Field & Michiels 2006). Monocystis banyak ditemukan pada akhir musim panas (Brown 1950). Derajat infestasi Monocystis sangat bervariasi dengan kisaran antara 0 hingga 34 900 000 per individu cacing (Field et al. 2003).
Monocystis pada cacing tanah banyak ditemukan pada vesikula seminalis sesuai dengan pola hidupnya yang memakan sitoplasma morula sperma (Morgan 1999). Namun, Monocystis juga dapat ditemukan pada periviseral selom, intestinum, dan nefridia (Bandyopadhyay et al. 2005, 2006a, 2006b, Bandyopadhyay & Mitra 2005).
Siklus hidup Monocystis berawal dari termakannya oocyst oleh cacing tanah, lalu oocyst tersebut masuk ke saluran pencernaan. Sista tercerna sehingga sporozoit dapat keluar dan bergerak ke vesikula seminalis (Kudo 1946, Wallace & Taylor 1997). Sporozoit (n) tersebut tumbuh menjadi tropozoit dewasa dan dua tropozoit akan melakukan fusi plasma (syzygy) membentuk gametosit. Dalam gametosit tersebut akan terjadi pembelahan inti tanpa diikuti pembelahan sitoplasma sehingga membentuk banyak gamet. Gamet di satu tropozoit akan befusi dengan gamet pada tropozoit yang lain membentuk zigot (2n). Selanjutnya zigot diselubungi kapsul membentuk oocyst. Di dalam oocyst akan terbentuk sporozoit hasil dari pembelahan meiosis dan mitosis (Wallace & Taylor 1997). Oocyst akhirnya dilepas ke lingkungan kembali. Walaupun Monocystis menginfeksi organ reproduksi, tetapi Monocystis tidak ditransmisikan lewat reproduksi seksual cacing. Transmisi utama Monocystis adalah dengan termakannya Monocystis yang terdapat di tanah oleh cacing (Field & Michiels 2006).
Berdasarkan Wallace dan Taylor (1997), kelas sporozoa merupakan parasit dan memiliki spora. Inang mereka tersebar dari Protozoa hingga Chordata. Monocystis termasuk dalam kingdom Protista (Bandyopadhyay et al. 2006a, 2006b), filum Apicomplexa (Omoto & Cartwright 2003), kelas Sporozoa, subklas Teleosporidia (dengan karakteristik spora sederhana tanpa filamen polar, spora dengan atau tanpa membran dengan 1 – banyak sporozoit), ordo
Gregarinida (dengan karakteristik tropozoit dewasa ekstraseluler, besar; zigot non-motil; sporozoit terselubungi), subordo Eugregarinina (siklus hidup tanpa schizogoni), famili Monocystidae (dengan karakteristik spora dengan ekstrimitas yang mirip, biconical; sporadin soliter, ujung anterior sporadin tidak terdiferensiasi), genus
Monocystis (dengan karakteristik bentuk tropozoit bervariasi dan motil; sporulasi dalam cyst tidak sempurna; spora biconical
simetris tanpa duri dengan 8 sporozoit) (Wallace & Taylor 1997).
Dalam penelitian ini dilakukan pengamatan terhadap Monocystis yang ditemukan pada cacing tanah Pheretima darnleiensis yang diperoleh dari lingkungan sekitar kampus IPB Gunung Gede dan Baranangsiang. Pheretima endemik di Asia Tenggara dan kepulauan Malaya dari India Selatan hingga Jepang (Stephenson 1930). Brusca dan Brusca (1990) memasukkan
Pheretima ke dalam kingdom Animalia, filum Annelida, kelas Oligochaeta. Sedangkan Stephenson (1930) memasukkan Pheretima ke dalam ordo Oligochaeta, sub ordo Neooligochaeta, series Megascolecina, famili Megascolecidae, sub famili Megascolecinae, genus Pheretima Kinb..
Tujuan
Penelitian ini bertujuan untuk mempelajari keberadaan parasit Monocystis pada cacing tanah Pheretima darnleiensis.
Waktu dan Tempat
Penelitian mulai dilaksanakan bulan Januari tahun 2007 sampai bulan Juni 2007 di Laboratorium Zoologi IPB.
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah: cacing tanah, eter, NaCl fisiologis, eosin 1%, haematoxylin ehrlich 1%, xilol, entellan, alkohol seri (30%, 50%, 70%, 80%, 95%, alkohol absolut), dan air.
Alat-alat yang digunakan dalam penelitian ini adalah: gunting, pinset, nampan bedah, jarum, cawan petri, pipet sel darah putih, haemocytometer, mikroskop cahaya, kaca preparat serta kaca penutup, fotomikroskop, dan komputer.
Pengambilan sampel
2
wet mount smear. Cacing tanah diambil dari beberapa tempat, yaitu: kebun kampus Gunung Gede, tanah galian, tanah di tempat sampah, tanah bekas kandang sapi, dan aspal. Pengambilan cacing tanah dilakukan dengan mengorek tanah dengan ranting pohon atau batang kayu. Cacing tanah yang tampak diambil dan dibawa ke laboratorium. Selanjutnya cacing tanah dicatat ciri-cirinya, antara lain: bentuk tubuh, warna, seta, warna serta posisi klitelum, dan bentuk prostomium untuk memastikan spesiesnya.
Pengamatan Monocystis
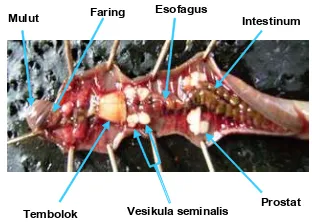
Cacing dibius dengan eter, lalu dibedah (Gambar 1).
Mulut
Tembolok Vesikula seminalis Prostat Faring Esofagus
Intestinum
Gambar 1 Organ dalam cacing
Vesikula seminalis atau spermateka diletakkan di atas kaca preparat, ditetesi dengan NaCl, dan selanjutnya diacak dengan gunting. Cairan selom dibuat preparat smear. Olesan dibiarkan kering udara, lalu difiksasi dengan alkohol 70%, diwarnai dengan haematoxylin ehrlich 1%, lalu eosin 1%. Dehidrasi dengan alkohol 30%, 50%, 70%, 80%, 95%, dan 100%. Penjernihan dengan merendam olesan dalam xilol 2 x 15 menit. Terakhir, olesan ditutup dengan entellan. Preparat diamati dengan mikroskop cahaya. Pengukuran objek dilakukan dengan mikrometer. Objek yang baik difoto dengan menggunakan fotomikroskop.
Penghitungan jumlah Monocystis
Vesikula seminalis diambil, lalu diacak dengan menggunakan gunting. Cairan vesikula seminalis dihisap dengan pipet sel darah putih, lalu diencerkan dengan menambahkan NaCl 85% hingga pengenceran 100 kali. Bila cairan vesikula seminalis terlalu sedikit, maka pengenceran dilakukan hingga 200 kali. Kedua ujung pipet ditutup, lalu dikocok agar homogen. Larutan vesikula seminalis diteteskan di atas haemositometer,
lalu dilakukan penghitungan dengan menggunakan counter.
HASIL
Karakter eksternal cacing: tubuh silindris, warna coklat gelap, prostomium epilobus, seta
perichaetine, klitelum bersifat annular pada segmen XIII – XV, lubang betina pada segmen XIV, sepasang lubang jantan pada segmen XVIII, tanda genital terdapat pada daerah sebelum dan setelah klitelum.
Karakter internal cacing: tembolok pada segmen VIII, 4 pasang spermateka pada segmen VI – XI, 2 pasang vesikula seminalis pada segmen XI dan XII, testes metandric
sepasang pada segmen XI, prostat pada segmen XVIII.
Pengamatan Monocystis
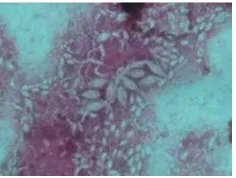
Dalam pengamatan tampak beberapa fase hidup Monocystis, yaitu: oocyst, gametosit, dan tropozoit.
Oocyst berbentuk seperti lemon, berkelompok, panjang 7.77 μm – 15.45 μm, lebar 3.88 μm – 7.77 μm dengan kedua ujung lancip. Spora di dalamnya tidak terlalu tampak jelas.
Gambar 2 Oocyst (perbesaran 10 x 40).
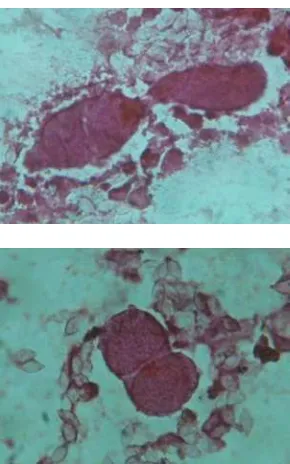
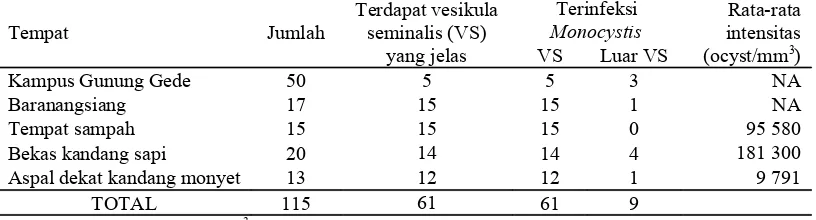
Gametosit bulat, berkelompok, diameter 77.7 μm – 264.18 μm. Pada fase awal, tampak dua tropozoit yang berfusi di dalam suatu cyst. Pada fase lebih lanjut, terdapat banyak oocyst di dalamnya yang merupakan hasil dari pembelahan inti. Ada juga yang masih memiliki residual body.
3
Gambar 4 Gametosit dengan residual body
(perbesaran 10 x 40).
Gambar 5 Gametosit dengan oocyst (perbesaran 10 x 40).
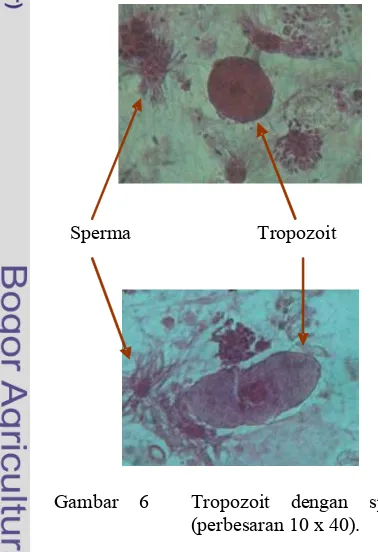
Tropozoit soliter atau berkelompok di dekat gametosit, berbentuk bulat hingga agak oval dengan diameter 38.85 μm – 126.91 μm, nukleus agak di tengah dengan diameter nukleus 7.77 μm – 12.95 μm. Tampak juga tropozoit yang sedang berfusi (syzygy).
Gambar 6 Tropozoit dengan sperma (perbesaran 10 x 40).
Gambar 7 Syzygy (perbesaran 10 x 40).
Penghitungan jumlah Monocystis
Cacing diambil dari kebun di depan laboratorium biokimia sebanyak 50 ekor, Baranangsiang sebanyak 17 ekor, tempat sampah zoologi sebanyak 15 ekor, tanah bekas kandang sebanyak 20 ekor, dan aspal di dekat kandang monyet sebanyak 13 ekor.
Enam puluh satu ekor dari 115 cacing yang diperoleh memiliki vesikula seminalis yang jelas. Cacing yang tidak memiliki vesikula seminalis yang jelas diambil spermateka beserta cairan selomnya. Sebanyak 70 ekor cacing terinfeksi
Monocystis dengan derajat infestasi berkisar antara 500 oocyst/mm3
– 1 074 000 oocyst/mm3 (47 sampel yang dihitung).
4
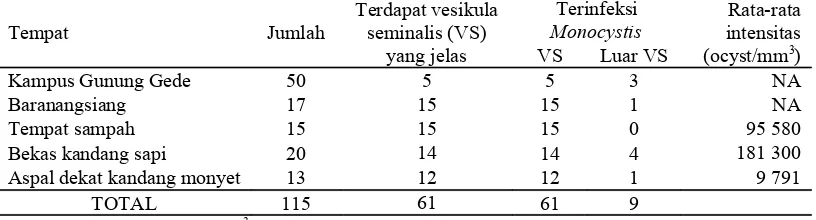
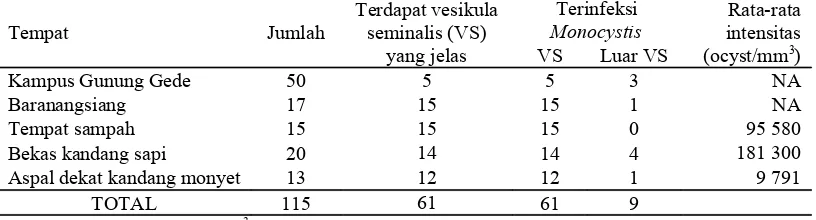
Tabel 1 Jumlah cacing yang terinfeksi Monocystis
Tempat Jumlah Terdapat vesikula seminalis (VS) yang jelas Terinfeksi Monocystis
VS Luar VS
Rata-rata intensitas (ocyst/mm3)
Kampus Gunung Gede 50 5 5 3 NA
Baranangsiang 17 15 15 1 NA
Tempat sampah 15 15 15 0 95 580
Bekas kandang sapi 20 14 14 4 181 300
Aspal dekat kandang monyet 13 12 12 1 9 791
TOTAL 115 61 61 9
Minimum = 500 oocyst / mm3
Maksimum = 1 074 000 oocyst / mm3
Rata-rata = 149 600 oocyst / mm3
Standar deviasi = 214 902 NA = tidak dihitung
PEMBAHASAN
Cacing diperoleh dari lima tempat, yaitu: kebun kampus Gunung Gede, Baranangsiang, tempat sampah, bekas kandang sapi, dan aspal dekat kandang monyet. Tanah tempat hidup cacing pada kebun kampus Gunung Gede ditumbuhi rumput liar dan relatif keras. Sama halnya dengan tanah bekas kandang sapi. Tanah di Baranangsiang merupakan tanah bekas galian yang ditumbuhi pohon. Tanah di tempat sampah terdapat sampah plastik dan sampah organik. Aspal di dekat kandang monyet ditumbuhi rumput di beberapa tempat. Intensitas Monocystis dihitung berdasarkan cacing yang ditemukan di tempat sampah, bekas kandang sapi, dan aspal di dekat kandang monyet. Intensitas Monocystis pada cacing tanah asal Baranangsiang dan kebun kampus Gunung Gede tidak dihitung. Hal ini disebabkan pada saat itu belum diperoleh metode yang tepat untuk menghitung intensitas Monocystis. Perbedaan lokasi cacing tanah berhubungan dengan intensitas
Monocystis yang ditemukan pada cacing tanah.
Identifikasi cacing tanah berdasarkan Sims & Easton (1972) dan juga dicocokkan dengan cacing yang diperoleh Santi (2006). Cacing yang diperoleh adalah Pheretima darnleiensis.
Cacing yang ditemukan di kebun kampus Gunung Gede sebanyak 50 ekor. Hanya 5 ekor yang memiliki vesikula seminalis jelas dan 8 ekor terinfeksi Monocystis. Rendahnya prevalensi Monocystis mungkin berkaitan dengan keberadaan vesikula seminalis.
Monocystis banyak ditemukan pada vesikula seminalis sehubungan dengan tersedianya sperma yang melimpah dan sedikitnya selomosit pada vesikula seminalis (Reinhart & Dollahon 2003). Selomosit yang berada di
cairan selom memfagosit Monocystis yang berada di luar vesikula seminalis sehingga jarang ditemukan Monocystis di luar vesikula seminalis.
Cacing tanah yang diperoleh tidak selalu memiliki vesikula seminalis yang jelas. Beberapa cacing tanah tidak memiliki vesikula seminalis seperti Chaetogaster. Namun, menurut Stepehenson (1930)
Pheretima darnleiensis merupakan cacing yang memiliki vesikula seminalis. Vesikula seminalis yang tidak jelas pada cacing tanah dapat disebabkan oleh beberapa hal: (1) Cacing belum cukup matang untuk bereproduksi seksual, (2) Vesikula seminalis berdegenerasi karena cacing sudah tidak bereproduksi lagi (Stephenson 1930), (3) Cacing baru kawin, selomosit membersihkan vesikula seminalis sehingga vesikula seminalis mengecil (Stephenson 1930).
Berdasarkan hasil analisis data, diperoleh kesimpulan bahwa ada hubungan antara intensitas Monocystis dengan lokasi tempat ditemukannya cacing. Pada tempat sampah rata-rata infestasi Monocystis 95 580 oocyst/mm3, pada tanah bekas kandang
181 300 oocyst/mm3
, dan pada aspal dekat kandang monyet 9 791 oocyst/mm3. Hal ini
berkaitan dengan penyebaran Monocystis
yang secara dominan lewat termakannya oocyst Monocystis oleh cacing (Field & Michiels 2006). Oocyst bersifat nonmotil dan berada di vesikula seminalis. Kemungkinan penyebaran oocyst terjadi setelah cacing inangnya mati.
5
Kemungkinan daerah tersebut terkontaminasi dengan bahan kimia yang dibuang sehingga mematikan oocyst Monocystis. Demikian pula pada tempat sampah. Daerah bekas kandang sapi letaknya jauh dari laboratorium biokimia, intensitas Monocystis pada cacing relatif lebih tinggi. Hal ini menguatkan dugaan bahwa kualitas tanah berpengaruh terhadap intensitas
Monocystis.
Monocystis merupakan parasit yang memiliki inang spesifik, tetapi dapat juga ditemukan spesies Monocystis yang sama pada cacing yang berbeda spesiesnya. Misalnya M. ventrosa ditemukan pada
Lumbricus rubellus dan L. Castaneus. M. ventrosa memiliki ciri-ciri tropozoit berukuran 109 – 183 μm, diameter nukleus mencapai 43 μm, diameter gametosit 185 – 223 μm, oocyst 17 – 25 μm, serta ujung anterior dan posterior dapat dibedakan (Wallace & Taylor 1997).
Monocystis yang diperoleh dalam
penelitian memiliki ciri-ciri tropozoit berbentuk bulat hingga agak oval dengan diameter 38.85 – 126.91 μm, diameter nukleus 7.77 – 12.95 μm, diameter gametosit 77.7 – 264.18 μm, oocyst kedua ujungnya lancip dengan panjang 7.77 – 15.45 μm dan lebar 3.88 – 7.77 μm. Berdasarkan ciri-ciri tesebut, Monocystis yang diperoleh dalam penelitian bukanlah M. ventrosa.
Sebagai parasit, Monocystis juga mempengaruhi pertumbuhan cacing tanah. Namun, Monocystis tidak berpengaruh terhadap produksi kokon cacing (Field & Michiels 2005).
Dalam penelitian, setiap vesikula seminalis terinfeksi Monocystis. Namun,
Monocystis jarang ditemukan pada
spermateka atau cairan selom. Ukuran oocyst, gametosit, dan tropozoit bervariasi (lihat hasil). Sesuai dengan pernyataan Wallace dan Taylor (1997) yang menyatakan bahwa bentuk tropozoit Monocystis bervariasi, bentuk tropozoit yang ditemukan tidak selalu oval, ditemukan juga bentuk yang membulat. Pada beberapa sampel yang terinfeksi
Monocystis hanya ditemukan oocyst tanpa gametosit atau tropozoit. Hal ini dimungkinkan karena sedikitnya Monocystis
yang menginfeksi cacing.
SIMPULAN
Monocystis menginfeksi cacing tanah
Pheretima darnleiensis dengan intensitas 500 – 1 074 000 oocyst/mm3
. Intensitas
Monocystis pada cacing tanah berkaitan dengan lokasi ditemukannya cacing tanah.
SARAN
Jumlah sampel serta lokasi pengambilan sampel perlu ditambah dan perlu ditemukan cara penghitungan Monocystis yang lebih baik.
DAFTAR PUSTAKA
Bandyopadhyay PK, Bhowmik B, Mitra AK. 2005. Observations on a new species of
Monocystis Stein, 1884 (Protozoa: Apicomplexa: Monocystidae) Monocystis levinei sp. nov. from an Indian earthworm (Annelida: Oligochaeta) Eutyphoeus incommodus. Zootaxa 1016:15–19. Bandyopadhyay PK, Mallik P, Gocmen B,
Mitra AK. 2006a. Monocystis
apporectodae sp. nov. (Protista:
Apicomplexa: Eugregarinida), from an Indian earthworm Apporectodea trapezoides Duges. Turkiye Parazitoloji Dergisi 30(1):50–52.
Bandyopadhyay PK, Mallik P, Gocmen B, Mitra AK. 2006b. Monocystis metaphirae
sp. nov. (Protista: Apicomplexa: Monocystidae) from the earthworm
Metaphire houlleti (Perrier). Turkiye Parazitoloji Dergisi 30(1):53–55.
Bandyopadhyay PK, Mitra AK. 2005. Observations on two new species of
Monocystis Stein, 1848 (Protozoa: Apicomplexa: Monocystidae) Monocystis
darjeelingensis sp.n. and M.
ranaghatensis sp.n. from earthworms (Annelida: Oligochaeta) of West Bengal, India. Animal Biology 55(2):123–132. Brown FAJr, editor. 1950. Selected
Invertebrate Types. New York: J Wiley. Brusca RC, Brusca GJ. 1990. Invertebrates.
Sunderland: Sinauer Inc.
Field SG, Michiels NK. 2005. Parasitism and growth in the earthworm Lumbricus terrestris: fitness costs of the gregarine parasite Monocystis sp. J Parasitol
130:397-403.
Field SG, Michiels NK. 2006. Acephaline gregarine parasites (Monocystis sp.) are not transmitted sexually among their lumbricid earthworm host. J Parasitol
92(2):292–297.
6
earthworm Lumbricus terrestris. Can J Zool 81:1161-1167.
Kudo RR. 1946. Protozoology, ed ke-3. Springfield: Charles C Thomas.
Morgan M. 1999. Monocystis. www.microscopy-uk.net/mag/artmar99/ cystis.html [4 Jun 2006].
Omoto CK, Cartwright DC. 2003. Investigating the Diversity of Parasitic Protozoa Using Gregarine Parasites of Invertebrates. www.zoo.utoronto. ca/able/volumes/vol-24/6-omoto.pdf - [4 Jun 2006].
Reinhart M, Dollahon N. 2003. Response of coelomocytes from Lumbricus terrestris to native and non-native eukaryotic parasites.
Pedobiologia 47:710-716.
Santi AUP. 2006. Beberapa aspek biologi cacing tanah Pheretima darnleiensis
(Fletcher) [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Sheridan P. 1998. Monocystis: Earthworm Parasites. www.carolina. com/manuals/ manuals3/Monocystis%20Earthworm%20 Parasite.pdf – [4 Jun 2006].
Sims RW, Easton EG. 1972. A Numerical Revision of the Earthworm Genus Pheretima auct. (Megascolecidae: Oligochaeta) with the Recognition of New Genera & an Appendix on the Earthworms Collected by the Royal Society North Bordeo Expedition. London: British Museum (Natural History).
Stephenson J. 1930. The Oligochaeta. Oxford: Clarendon Press.
Monocystis SEBAGAI PARASIT CACING TANAH
ANDY DARMAWAN
DEPARTEMEN BIOLOGI
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
ANDY DARMAWAN. Monocystis sebagai Parasit Cacing Tanah. Dibimbing oleh TARUNI SRI PRAWASTI dan BAMBANG SURYOBROTO.
Monocystis merupakan kelompok Gregarina parasit yang umum menyerang Annelida.
Pheretima darnleiensis merupakan Annelida yang biasa menjadi inang Monocystis. Dalam penelitian ini dilakukan pengamatan terhadap Monocystis yang ditemukan pada cacing tanah
Pheretima darnleiensis yang diperoleh dari lingkungan sekitar kampus IPB Gunung Gede dan Baranangsiang. Monocystis menginfeksi cacing tanah Pheretima darnleiensis dengan intensitas 500 – 1 074 000 oocyst/mm3
cairan vesikula seminalis. Intensitas Monocystis pada cacing tanah berkaitan dengan lokasi ditemukannya cacing tanah. Tropozoit bulat hingga agak oval dengan diameter 38.85 μm – 126.91 μm, nukleus bulat dengan diameter 7.77 μm – 12.95 μm. Gametosit bulat dengan diameter 7.77 μm – 12.95 μm. Oocyst seperti lemon dengan ukuran 7.77 μm – 15.45 μm x 3.88 μm – 7.77 μm.
ABSTRACT
ANDY DARMAWAN. Monocystis as Earthworm Parasite. Supervised by TARUNI SRI PRAWASTI and BAMBANG SURYOBROTO.
Monocystis is parasite gregarine which infects Annelid. Pheretima darnleiensis is a common host for Monocystis. In this research, Monocystis in Pheretima darnleiensis which were collected from Zoology and Baranangsiang, Department of Biology Faculty of Mathematic and Natural Science IPB, were examined. Oocyst concentration which found in earthworm was 500 – 1 074 000 oocyst/mm3 seminal vesicle liquid. Monocystis load was related with location of
1
PENDAHULUAN
Latar Belakang
Monocystis merupakan kelompok
Gregarina parasit yang umum menyerang Annelida (Omoto & Cartwright 2003). Cacing tanah merupakan Annelida yang biasa menjadi inang Monocystis (Field & Michiels 2006). Monocystis banyak ditemukan pada akhir musim panas (Brown 1950). Derajat infestasi Monocystis sangat bervariasi dengan kisaran antara 0 hingga 34 900 000 per individu cacing (Field et al. 2003).
Monocystis pada cacing tanah banyak ditemukan pada vesikula seminalis sesuai dengan pola hidupnya yang memakan sitoplasma morula sperma (Morgan 1999). Namun, Monocystis juga dapat ditemukan pada periviseral selom, intestinum, dan nefridia (Bandyopadhyay et al. 2005, 2006a, 2006b, Bandyopadhyay & Mitra 2005).
Siklus hidup Monocystis berawal dari termakannya oocyst oleh cacing tanah, lalu oocyst tersebut masuk ke saluran pencernaan. Sista tercerna sehingga sporozoit dapat keluar dan bergerak ke vesikula seminalis (Kudo 1946, Wallace & Taylor 1997). Sporozoit (n) tersebut tumbuh menjadi tropozoit dewasa dan dua tropozoit akan melakukan fusi plasma (syzygy) membentuk gametosit. Dalam gametosit tersebut akan terjadi pembelahan inti tanpa diikuti pembelahan sitoplasma sehingga membentuk banyak gamet. Gamet di satu tropozoit akan befusi dengan gamet pada tropozoit yang lain membentuk zigot (2n). Selanjutnya zigot diselubungi kapsul membentuk oocyst. Di dalam oocyst akan terbentuk sporozoit hasil dari pembelahan meiosis dan mitosis (Wallace & Taylor 1997). Oocyst akhirnya dilepas ke lingkungan kembali. Walaupun Monocystis menginfeksi organ reproduksi, tetapi Monocystis tidak ditransmisikan lewat reproduksi seksual cacing. Transmisi utama Monocystis adalah dengan termakannya Monocystis yang terdapat di tanah oleh cacing (Field & Michiels 2006).
Berdasarkan Wallace dan Taylor (1997), kelas sporozoa merupakan parasit dan memiliki spora. Inang mereka tersebar dari Protozoa hingga Chordata. Monocystis termasuk dalam kingdom Protista (Bandyopadhyay et al. 2006a, 2006b), filum Apicomplexa (Omoto & Cartwright 2003), kelas Sporozoa, subklas Teleosporidia (dengan karakteristik spora sederhana tanpa filamen polar, spora dengan atau tanpa membran dengan 1 – banyak sporozoit), ordo
Gregarinida (dengan karakteristik tropozoit dewasa ekstraseluler, besar; zigot non-motil; sporozoit terselubungi), subordo Eugregarinina (siklus hidup tanpa schizogoni), famili Monocystidae (dengan karakteristik spora dengan ekstrimitas yang mirip, biconical; sporadin soliter, ujung anterior sporadin tidak terdiferensiasi), genus
Monocystis (dengan karakteristik bentuk tropozoit bervariasi dan motil; sporulasi dalam cyst tidak sempurna; spora biconical
simetris tanpa duri dengan 8 sporozoit) (Wallace & Taylor 1997).
Dalam penelitian ini dilakukan pengamatan terhadap Monocystis yang ditemukan pada cacing tanah Pheretima darnleiensis yang diperoleh dari lingkungan sekitar kampus IPB Gunung Gede dan Baranangsiang. Pheretima endemik di Asia Tenggara dan kepulauan Malaya dari India Selatan hingga Jepang (Stephenson 1930). Brusca dan Brusca (1990) memasukkan
Pheretima ke dalam kingdom Animalia, filum Annelida, kelas Oligochaeta. Sedangkan Stephenson (1930) memasukkan Pheretima ke dalam ordo Oligochaeta, sub ordo Neooligochaeta, series Megascolecina, famili Megascolecidae, sub famili Megascolecinae, genus Pheretima Kinb..
Tujuan
Penelitian ini bertujuan untuk mempelajari keberadaan parasit Monocystis pada cacing tanah Pheretima darnleiensis.
Waktu dan Tempat
Penelitian mulai dilaksanakan bulan Januari tahun 2007 sampai bulan Juni 2007 di Laboratorium Zoologi IPB.
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah: cacing tanah, eter, NaCl fisiologis, eosin 1%, haematoxylin ehrlich 1%, xilol, entellan, alkohol seri (30%, 50%, 70%, 80%, 95%, alkohol absolut), dan air.
Alat-alat yang digunakan dalam penelitian ini adalah: gunting, pinset, nampan bedah, jarum, cawan petri, pipet sel darah putih, haemocytometer, mikroskop cahaya, kaca preparat serta kaca penutup, fotomikroskop, dan komputer.
Pengambilan sampel
1
PENDAHULUAN
Latar Belakang
Monocystis merupakan kelompok
Gregarina parasit yang umum menyerang Annelida (Omoto & Cartwright 2003). Cacing tanah merupakan Annelida yang biasa menjadi inang Monocystis (Field & Michiels 2006). Monocystis banyak ditemukan pada akhir musim panas (Brown 1950). Derajat infestasi Monocystis sangat bervariasi dengan kisaran antara 0 hingga 34 900 000 per individu cacing (Field et al. 2003).
Monocystis pada cacing tanah banyak ditemukan pada vesikula seminalis sesuai dengan pola hidupnya yang memakan sitoplasma morula sperma (Morgan 1999). Namun, Monocystis juga dapat ditemukan pada periviseral selom, intestinum, dan nefridia (Bandyopadhyay et al. 2005, 2006a, 2006b, Bandyopadhyay & Mitra 2005).
Siklus hidup Monocystis berawal dari termakannya oocyst oleh cacing tanah, lalu oocyst tersebut masuk ke saluran pencernaan. Sista tercerna sehingga sporozoit dapat keluar dan bergerak ke vesikula seminalis (Kudo 1946, Wallace & Taylor 1997). Sporozoit (n) tersebut tumbuh menjadi tropozoit dewasa dan dua tropozoit akan melakukan fusi plasma (syzygy) membentuk gametosit. Dalam gametosit tersebut akan terjadi pembelahan inti tanpa diikuti pembelahan sitoplasma sehingga membentuk banyak gamet. Gamet di satu tropozoit akan befusi dengan gamet pada tropozoit yang lain membentuk zigot (2n). Selanjutnya zigot diselubungi kapsul membentuk oocyst. Di dalam oocyst akan terbentuk sporozoit hasil dari pembelahan meiosis dan mitosis (Wallace & Taylor 1997). Oocyst akhirnya dilepas ke lingkungan kembali. Walaupun Monocystis menginfeksi organ reproduksi, tetapi Monocystis tidak ditransmisikan lewat reproduksi seksual cacing. Transmisi utama Monocystis adalah dengan termakannya Monocystis yang terdapat di tanah oleh cacing (Field & Michiels 2006).
Berdasarkan Wallace dan Taylor (1997), kelas sporozoa merupakan parasit dan memiliki spora. Inang mereka tersebar dari Protozoa hingga Chordata. Monocystis termasuk dalam kingdom Protista (Bandyopadhyay et al. 2006a, 2006b), filum Apicomplexa (Omoto & Cartwright 2003), kelas Sporozoa, subklas Teleosporidia (dengan karakteristik spora sederhana tanpa filamen polar, spora dengan atau tanpa membran dengan 1 – banyak sporozoit), ordo
Gregarinida (dengan karakteristik tropozoit dewasa ekstraseluler, besar; zigot non-motil; sporozoit terselubungi), subordo Eugregarinina (siklus hidup tanpa schizogoni), famili Monocystidae (dengan karakteristik spora dengan ekstrimitas yang mirip, biconical; sporadin soliter, ujung anterior sporadin tidak terdiferensiasi), genus
Monocystis (dengan karakteristik bentuk tropozoit bervariasi dan motil; sporulasi dalam cyst tidak sempurna; spora biconical
simetris tanpa duri dengan 8 sporozoit) (Wallace & Taylor 1997).
Dalam penelitian ini dilakukan pengamatan terhadap Monocystis yang ditemukan pada cacing tanah Pheretima darnleiensis yang diperoleh dari lingkungan sekitar kampus IPB Gunung Gede dan Baranangsiang. Pheretima endemik di Asia Tenggara dan kepulauan Malaya dari India Selatan hingga Jepang (Stephenson 1930). Brusca dan Brusca (1990) memasukkan
Pheretima ke dalam kingdom Animalia, filum Annelida, kelas Oligochaeta. Sedangkan Stephenson (1930) memasukkan Pheretima ke dalam ordo Oligochaeta, sub ordo Neooligochaeta, series Megascolecina, famili Megascolecidae, sub famili Megascolecinae, genus Pheretima Kinb..
Tujuan
Penelitian ini bertujuan untuk mempelajari keberadaan parasit Monocystis pada cacing tanah Pheretima darnleiensis.
Waktu dan Tempat
Penelitian mulai dilaksanakan bulan Januari tahun 2007 sampai bulan Juni 2007 di Laboratorium Zoologi IPB.
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan dalam penelitian ini adalah: cacing tanah, eter, NaCl fisiologis, eosin 1%, haematoxylin ehrlich 1%, xilol, entellan, alkohol seri (30%, 50%, 70%, 80%, 95%, alkohol absolut), dan air.
Alat-alat yang digunakan dalam penelitian ini adalah: gunting, pinset, nampan bedah, jarum, cawan petri, pipet sel darah putih, haemocytometer, mikroskop cahaya, kaca preparat serta kaca penutup, fotomikroskop, dan komputer.
Pengambilan sampel
2
wet mount smear. Cacing tanah diambil dari beberapa tempat, yaitu: kebun kampus Gunung Gede, tanah galian, tanah di tempat sampah, tanah bekas kandang sapi, dan aspal. Pengambilan cacing tanah dilakukan dengan mengorek tanah dengan ranting pohon atau batang kayu. Cacing tanah yang tampak diambil dan dibawa ke laboratorium. Selanjutnya cacing tanah dicatat ciri-cirinya, antara lain: bentuk tubuh, warna, seta, warna serta posisi klitelum, dan bentuk prostomium untuk memastikan spesiesnya.
Pengamatan Monocystis
Cacing dibius dengan eter, lalu dibedah (Gambar 1).
Mulut
Tembolok Vesikula seminalis Prostat Faring Esofagus
Intestinum
Gambar 1 Organ dalam cacing
Vesikula seminalis atau spermateka diletakkan di atas kaca preparat, ditetesi dengan NaCl, dan selanjutnya diacak dengan gunting. Cairan selom dibuat preparat smear. Olesan dibiarkan kering udara, lalu difiksasi dengan alkohol 70%, diwarnai dengan haematoxylin ehrlich 1%, lalu eosin 1%. Dehidrasi dengan alkohol 30%, 50%, 70%, 80%, 95%, dan 100%. Penjernihan dengan merendam olesan dalam xilol 2 x 15 menit. Terakhir, olesan ditutup dengan entellan. Preparat diamati dengan mikroskop cahaya. Pengukuran objek dilakukan dengan mikrometer. Objek yang baik difoto dengan menggunakan fotomikroskop.
Penghitungan jumlah Monocystis
Vesikula seminalis diambil, lalu diacak dengan menggunakan gunting. Cairan vesikula seminalis dihisap dengan pipet sel darah putih, lalu diencerkan dengan menambahkan NaCl 85% hingga pengenceran 100 kali. Bila cairan vesikula seminalis terlalu sedikit, maka pengenceran dilakukan hingga 200 kali. Kedua ujung pipet ditutup, lalu dikocok agar homogen. Larutan vesikula seminalis diteteskan di atas haemositometer,
lalu dilakukan penghitungan dengan menggunakan counter.
HASIL
Karakter eksternal cacing: tubuh silindris, warna coklat gelap, prostomium epilobus, seta
perichaetine, klitelum bersifat annular pada segmen XIII – XV, lubang betina pada segmen XIV, sepasang lubang jantan pada segmen XVIII, tanda genital terdapat pada daerah sebelum dan setelah klitelum.
Karakter internal cacing: tembolok pada segmen VIII, 4 pasang spermateka pada segmen VI – XI, 2 pasang vesikula seminalis pada segmen XI dan XII, testes metandric
sepasang pada segmen XI, prostat pada segmen XVIII.
Pengamatan Monocystis
Dalam pengamatan tampak beberapa fase hidup Monocystis, yaitu: oocyst, gametosit, dan tropozoit.
Oocyst berbentuk seperti lemon, berkelompok, panjang 7.77 μm – 15.45 μm, lebar 3.88 μm – 7.77 μm dengan kedua ujung lancip. Spora di dalamnya tidak terlalu tampak jelas.
Gambar 2 Oocyst (perbesaran 10 x 40).
Gametosit bulat, berkelompok, diameter 77.7 μm – 264.18 μm. Pada fase awal, tampak dua tropozoit yang berfusi di dalam suatu cyst. Pada fase lebih lanjut, terdapat banyak oocyst di dalamnya yang merupakan hasil dari pembelahan inti. Ada juga yang masih memiliki residual body.
2
wet mount smear. Cacing tanah diambil dari beberapa tempat, yaitu: kebun kampus Gunung Gede, tanah galian, tanah di tempat sampah, tanah bekas kandang sapi, dan aspal. Pengambilan cacing tanah dilakukan dengan mengorek tanah dengan ranting pohon atau batang kayu. Cacing tanah yang tampak diambil dan dibawa ke laboratorium. Selanjutnya cacing tanah dicatat ciri-cirinya, antara lain: bentuk tubuh, warna, seta, warna serta posisi klitelum, dan bentuk prostomium untuk memastikan spesiesnya.
Pengamatan Monocystis
Cacing dibius dengan eter, lalu dibedah (Gambar 1).
Mulut
Tembolok Vesikula seminalis Prostat Faring Esofagus
Intestinum
Gambar 1 Organ dalam cacing
Vesikula seminalis atau spermateka diletakkan di atas kaca preparat, ditetesi dengan NaCl, dan selanjutnya diacak dengan gunting. Cairan selom dibuat preparat smear. Olesan dibiarkan kering udara, lalu difiksasi dengan alkohol 70%, diwarnai dengan haematoxylin ehrlich 1%, lalu eosin 1%. Dehidrasi dengan alkohol 30%, 50%, 70%, 80%, 95%, dan 100%. Penjernihan dengan merendam olesan dalam xilol 2 x 15 menit. Terakhir, olesan ditutup dengan entellan. Preparat diamati dengan mikroskop cahaya. Pengukuran objek dilakukan dengan mikrometer. Objek yang baik difoto dengan menggunakan fotomikroskop.
Penghitungan jumlah Monocystis
Vesikula seminalis diambil, lalu diacak dengan menggunakan gunting. Cairan vesikula seminalis dihisap dengan pipet sel darah putih, lalu diencerkan dengan menambahkan NaCl 85% hingga pengenceran 100 kali. Bila cairan vesikula seminalis terlalu sedikit, maka pengenceran dilakukan hingga 200 kali. Kedua ujung pipet ditutup, lalu dikocok agar homogen. Larutan vesikula seminalis diteteskan di atas haemositometer,
lalu dilakukan penghitungan dengan menggunakan counter.
HASIL
Karakter eksternal cacing: tubuh silindris, warna coklat gelap, prostomium epilobus, seta
perichaetine, klitelum bersifat annular pada segmen XIII – XV, lubang betina pada segmen XIV, sepasang lubang jantan pada segmen XVIII, tanda genital terdapat pada daerah sebelum dan setelah klitelum.
Karakter internal cacing: tembolok pada segmen VIII, 4 pasang spermateka pada segmen VI – XI, 2 pasang vesikula seminalis pada segmen XI dan XII, testes metandric
sepasang pada segmen XI, prostat pada segmen XVIII.
Pengamatan Monocystis
Dalam pengamatan tampak beberapa fase hidup Monocystis, yaitu: oocyst, gametosit, dan tropozoit.
Oocyst berbentuk seperti lemon, berkelompok, panjang 7.77 μm – 15.45 μm, lebar 3.88 μm – 7.77 μm dengan kedua ujung lancip. Spora di dalamnya tidak terlalu tampak jelas.
Gambar 2 Oocyst (perbesaran 10 x 40).
Gametosit bulat, berkelompok, diameter 77.7 μm – 264.18 μm. Pada fase awal, tampak dua tropozoit yang berfusi di dalam suatu cyst. Pada fase lebih lanjut, terdapat banyak oocyst di dalamnya yang merupakan hasil dari pembelahan inti. Ada juga yang masih memiliki residual body.
3
Gambar 4 Gametosit dengan residual body
(perbesaran 10 x 40).
Gambar 5 Gametosit dengan oocyst (perbesaran 10 x 40).
Tropozoit soliter atau berkelompok di dekat gametosit, berbentuk bulat hingga agak oval dengan diameter 38.85 μm – 126.91 μm, nukleus agak di tengah dengan diameter nukleus 7.77 μm – 12.95 μm. Tampak juga tropozoit yang sedang berfusi (syzygy).
Gambar 6 Tropozoit dengan sperma (perbesaran 10 x 40).
Gambar 7 Syzygy (perbesaran 10 x 40).
Penghitungan jumlah Monocystis
Cacing diambil dari kebun di depan laboratorium biokimia sebanyak 50 ekor, Baranangsiang sebanyak 17 ekor, tempat sampah zoologi sebanyak 15 ekor, tanah bekas kandang sebanyak 20 ekor, dan aspal di dekat kandang monyet sebanyak 13 ekor.
Enam puluh satu ekor dari 115 cacing yang diperoleh memiliki vesikula seminalis yang jelas. Cacing yang tidak memiliki vesikula seminalis yang jelas diambil spermateka beserta cairan selomnya. Sebanyak 70 ekor cacing terinfeksi
Monocystis dengan derajat infestasi berkisar antara 500 oocyst/mm3
– 1 074 000 oocyst/mm3 (47 sampel yang dihitung).
4
Tabel 1 Jumlah cacing yang terinfeksi Monocystis
Tempat Jumlah Terdapat vesikula seminalis (VS) yang jelas Terinfeksi Monocystis
VS Luar VS
Rata-rata intensitas (ocyst/mm3)
Kampus Gunung Gede 50 5 5 3 NA
Baranangsiang 17 15 15 1 NA
Tempat sampah 15 15 15 0 95 580
Bekas kandang sapi 20 14 14 4 181 300
Aspal dekat kandang monyet 13 12 12 1 9 791
TOTAL 115 61 61 9
Minimum = 500 oocyst / mm3
Maksimum = 1 074 000 oocyst / mm3
Rata-rata = 149 600 oocyst / mm3
Standar deviasi = 214 902 NA = tidak dihitung
PEMBAHASAN
Cacing diperoleh dari lima tempat, yaitu: kebun kampus Gunung Gede, Baranangsiang, tempat sampah, bekas kandang sapi, dan aspal dekat kandang monyet. Tanah tempat hidup cacing pada kebun kampus Gunung Gede ditumbuhi rumput liar dan relatif keras. Sama halnya dengan tanah bekas kandang sapi. Tanah di Baranangsiang merupakan tanah bekas galian yang ditumbuhi pohon. Tanah di tempat sampah terdapat sampah plastik dan sampah organik. Aspal di dekat kandang monyet ditumbuhi rumput di beberapa tempat. Intensitas Monocystis dihitung berdasarkan cacing yang ditemukan di tempat sampah, bekas kandang sapi, dan aspal di dekat kandang monyet. Intensitas Monocystis pada cacing tanah asal Baranangsiang dan kebun kampus Gunung Gede tidak dihitung. Hal ini disebabkan pada saat itu belum diperoleh metode yang tepat untuk menghitung intensitas Monocystis. Perbedaan lokasi cacing tanah berhubungan dengan intensitas
Monocystis yang ditemukan pada cacing tanah.
Identifikasi cacing tanah berdasarkan Sims & Easton (1972) dan juga dicocokkan dengan cacing yang diperoleh Santi (2006). Cacing yang diperoleh adalah Pheretima darnleiensis.
Cacing yang ditemukan di kebun kampus Gunung Gede sebanyak 50 ekor. Hanya 5 ekor yang memiliki vesikula seminalis jelas dan 8 ekor terinfeksi Monocystis. Rendahnya prevalensi Monocystis mungkin berkaitan dengan keberadaan vesikula seminalis.
Monocystis banyak ditemukan pada vesikula seminalis sehubungan dengan tersedianya sperma yang melimpah dan sedikitnya selomosit pada vesikula seminalis (Reinhart & Dollahon 2003). Selomosit yang berada di
cairan selom memfagosit Monocystis yang berada di luar vesikula seminalis sehingga jarang ditemukan Monocystis di luar vesikula seminalis.
Cacing tanah yang diperoleh tidak selalu memiliki vesikula seminalis yang jelas. Beberapa cacing tanah tidak memiliki vesikula seminalis seperti Chaetogaster. Namun, menurut Stepehenson (1930)
Pheretima darnleiensis merupakan cacing yang memiliki vesikula seminalis. Vesikula seminalis yang tidak jelas pada cacing tanah dapat disebabkan oleh beberapa hal: (1) Cacing belum cukup matang untuk bereproduksi seksual, (2) Vesikula seminalis berdegenerasi karena cacing sudah tidak bereproduksi lagi (Stephenson 1930), (3) Cacing baru kawin, selomosit membersihkan vesikula seminalis sehingga vesikula seminalis mengecil (Stephenson 1930).
Berdasarkan hasil analisis data, diperoleh kesimpulan bahwa ada hubungan antara intensitas Monocystis dengan lokasi tempat ditemukannya cacing. Pada tempat sampah rata-rata infestasi Monocystis 95 580 oocyst/mm3, pada tanah bekas kandang
181 300 oocyst/mm3
, dan pada aspal dekat kandang monyet 9 791 oocyst/mm3. Hal ini
berkaitan dengan penyebaran Monocystis
yang secara dominan lewat termakannya oocyst Monocystis oleh cacing (Field & Michiels 2006). Oocyst bersifat nonmotil dan berada di vesikula seminalis. Kemungkinan penyebaran oocyst terjadi setelah cacing inangnya mati.
4
Tabel 1 Jumlah cacing yang terinfeksi Monocystis
Tempat Jumlah Terdapat vesikula seminalis (VS) yang jelas Terinfeksi Monocystis
VS Luar VS
Rata-rata intensitas (ocyst/mm3)
Kampus Gunung Gede 50 5 5 3 NA
Baranangsiang 17 15 15 1 NA
Tempat sampah 15 15 15 0 95 580
Bekas kandang sapi 20 14 14 4 181 300
Aspal dekat kandang monyet 13 12 12 1 9 791
TOTAL 115 61 61 9
Minimum = 500 oocyst / mm3
Maksimum = 1 074 000 oocyst / mm3
Rata-rata = 149 600 oocyst / mm3
Standar deviasi = 214 902 NA = tidak dihitung
PEMBAHASAN
Cacing diperoleh dari lima tempat, yaitu: kebun kampus Gunung Gede, Baranangsiang, tempat sampah, bekas kandang sapi, dan aspal dekat kandang monyet. Tanah tempat hidup cacing pada kebun kampus Gunung Gede ditumbuhi rumput liar dan relatif keras. Sama halnya dengan tanah bekas kandang sapi. Tanah di Baranangsiang merupakan tanah bekas galian yang ditumbuhi pohon. Tanah di tempat sampah terdapat sampah plastik dan sampah organik. Aspal di dekat kandang monyet ditumbuhi rumput di beberapa tempat. Intensitas Monocystis dihitung berdasarkan cacing yang ditemukan di tempat sampah, bekas kandang sapi, dan aspal di dekat kandang monyet. Intensitas Monocystis pada cacing tanah asal Baranangsiang dan kebun kampus Gunung Gede tidak dihitung. Hal ini disebabkan pada saat itu belum diperoleh metode yang tepat untuk menghitung intensitas Monocystis. Perbedaan lokasi cacing tanah berhubungan dengan intensitas
Monocystis yang ditemukan pada cacing tanah.
Identifikasi cacing tanah berdasarkan Sims & Easton (1972) dan juga dicocokkan dengan cacing yang diperoleh Santi (2006). Cacing yang diperoleh adalah Pheretima darnleiensis.
Cacing yang ditemukan di kebun kampus Gunung Gede sebanyak 50 ekor. Hanya 5 ekor yang memiliki vesikula seminalis jelas dan 8 ekor terinfeksi Monocystis. Rendahnya prevalensi Monocystis mungkin berkaitan dengan keberadaan vesikula seminalis.
Monocystis banyak ditemukan pada vesikula seminalis sehubungan dengan tersedianya sperma yang melimpah dan sedikitnya selomosit pada vesikula seminalis (Reinhart & Dollahon 2003). Selomosit yang berada di
cairan selom memfagosit Monocystis yang berada di luar vesikula seminalis sehingga jarang ditemukan Monocystis di luar vesikula seminalis.
Cacing tanah yang diperoleh tidak selalu memiliki vesikula seminalis yang jelas. Beberapa cacing tanah tidak memiliki vesikula seminalis seperti Chaetogaster. Namun, menurut Stepehenson (1930)
Pheretima darnleiensis merupakan cacing yang memiliki vesikula seminalis. Vesikula seminalis yang tidak jelas pada cacing tanah dapat disebabkan oleh beberapa hal: (1) Cacing belum cukup matang untuk bereproduksi seksual, (2) Vesikula seminalis berdegenerasi karena cacing sudah tidak bereproduksi lagi (Stephenson 1930), (3) Cacing baru kawin, selomosit membersihkan vesikula seminalis sehingga vesikula seminalis mengecil (Stephenson 1930).
Berdasarkan hasil analisis data, diperoleh kesimpulan bahwa ada hubungan antara intensitas Monocystis dengan lokasi tempat ditemukannya cacing. Pada tempat sampah rata-rata infestasi Monocystis 95 580 oocyst/mm3, pada tanah bekas kandang
181 300 oocyst/mm3
, dan pada aspal dekat kandang monyet 9 791 oocyst/mm3. Hal ini
berkaitan dengan penyebaran Monocystis
yang secara dominan lewat termakannya oocyst Monocystis oleh cacing (Field & Michiels 2006). Oocyst bersifat nonmotil dan berada di vesikula seminalis. Kemungkinan penyebaran oocyst terjadi setelah cacing inangnya mati.
5
Kemungkinan daerah tersebut terkontaminasi dengan bahan kimia yang dibuang sehingga mematikan oocyst Monocystis. Demikian pula pada tempat sampah. Daerah bekas kandang sapi letaknya jauh dari laboratorium biokimia, intensitas Monocystis pada cacing relatif lebih tinggi. Hal ini menguatkan dugaan bahwa kualitas tanah berpengaruh terhadap intensitas
Monocystis.
Monocystis merupakan parasit yang memiliki inang spesifik, tetapi dapat juga ditemukan spesies Monocystis yang sama pada cacing yang berbeda spesiesnya. Misalnya M. ventrosa ditemukan pada
Lumbricus rubellus dan L. Castaneus. M. ventrosa memiliki ciri-ciri tropozoit berukuran 109 – 183 μm, diameter nukleus mencapai 43 μm, diameter gametosit 185 – 223 μm, oocyst 17 – 25 μm, serta ujung anterior dan posterior dapat dibedakan (Wallace & Taylor 1997).
Monocystis yang diperoleh dalam
penelitian memiliki ciri-ciri tropozoit berbentuk bulat hingga agak oval dengan diameter 38.85 – 126.91 μm, diameter nukleus 7.77 – 12.95 μm, diameter gametosit 77.7 – 264.18 μm, oocyst kedua ujungnya lancip dengan panjang 7.77 – 15.45 μm dan lebar 3.88 – 7.77 μm. Berdasarkan ciri-ciri tesebut, Monocystis yang diperoleh dalam penelitian bukanlah M. ventrosa.
Sebagai parasit, Monocystis juga mempengaruhi pertumbuhan cacing tanah. Namun, Monocystis tidak berpengaruh terhadap produksi kokon cacing (Field & Michiels 2005).
Dalam penelitian, setiap vesikula seminalis terinfeksi Monocystis. Namun,
Monocystis jarang ditemukan pada
spermateka atau cairan selom. Ukuran oocyst, gametosit, dan tropozoit bervariasi (lihat hasil). Sesuai dengan pernyataan Wallace dan Taylor (1997) yang menyatakan bahwa bentuk tropozoit Monocystis bervariasi, bentuk tropozoit yang ditemukan tidak selalu oval, ditemukan juga bentuk yang membulat. Pada beberapa sampel yang terinfeksi
Monocystis hanya ditemukan oocyst tanpa gametosit atau tropozoit. Hal ini dimungkinkan karena sedikitnya Monocystis
yang menginfeksi cacing.
SIMPULAN
Monocystis menginfeksi cacing tanah
Pheretima darnleiensis dengan intensitas 500 – 1 074 000 oocyst/mm3
. Intensitas
Monocystis pada cacing tanah berkaitan dengan lokasi ditemukannya cacing tanah.
SARAN
Jumlah sampel serta lokasi pengambilan sampel perlu ditambah dan perlu ditemukan cara penghitungan Monocystis yang lebih baik.
DAFTAR PUSTAKA
Bandyopadhyay PK, Bhowmik B, Mitra AK. 2005. Observations on a new species of
Monocystis Stein, 1884 (Protozoa: Apicomplexa: Monocystidae) Monocystis levinei sp. nov. from an Indian earthworm (Annelida: Oligochaeta) Eutyphoeus incommodus. Zootaxa 1016:15–19. Bandyopadhyay PK, Mallik P, Gocmen B,
Mitra AK. 2006a. Monocystis
apporectodae sp. nov. (Protista:
Apicomplexa: Eugregarinida), from an Indian earthworm Apporectodea trapezoides Duges. Turkiye Parazitoloji Dergisi 30(1):50–52.
Bandyopadhyay PK, Mallik P, Gocmen B, Mitra AK. 2006b. Monocystis metaphirae
sp. nov. (Protista: Apicomplexa: Monocystidae) from the earthworm
Metaphire houlleti (Perrier). Turkiye Parazitoloji Dergisi 30(1):53–55.
Bandyopadhyay PK, Mitra AK. 2005. Observations on two new species of
Monocystis Stein, 1848 (Protozoa: Apicomplexa: Monocystidae) Monocystis
darjeelingensis sp.n. and M.
ranaghatensis sp.n. from earthworms (Annelida: Oligochaeta) of West Bengal, India. Animal Biology 55(2):123–132. Brown FAJr, editor. 1950. Selected
Invertebrate Types. New York: J Wiley. Brusca RC, Brusca GJ. 1990. Invertebrates.
Sunderland: Sinauer Inc.
Field SG, Michiels NK. 2005. Parasitism and growth in the earthworm Lumbricus terrestris: fitness costs of the gregarine parasite Monocystis sp. J Parasitol
130:397-403.
Field SG, Michiels NK. 2006. Acephaline gregarine parasites (Monocystis sp.) are not transmitted sexually among their lumbricid earthworm host. J Parasitol
92(2):292–297.
5
Kemungkinan daerah tersebut terkontaminasi dengan bahan kimia yang dibuang sehingga mematikan oocyst Monocystis. Demikian pula pada tempat sampah. Daerah bekas kandang sapi letaknya jauh dari laboratorium biokimia, intensitas Monocystis pada cacing relatif lebih tinggi. Hal ini menguatkan dugaan bahwa kualitas tanah berpengaruh terhadap intensitas
Monocystis.
Monocystis merupakan parasit yang memiliki inang spesifik, tetapi dapat juga ditemukan spesies Monocystis yang sama pada cacing yang berbeda spesiesnya. Misalnya M. ventrosa ditemukan pada
Lumbricus rubellus dan L. Castaneus. M. ventrosa memiliki ciri-ciri tropozoit berukuran 109 – 183 μm, diameter nukleus mencapai 43 μm, diameter gametosit 185 – 223 μm, oocyst 17 – 25 μm, serta ujung anterior dan posterior dapat dibedakan (Wallace & Taylor 1997).
Monocystis yang diperoleh dalam
penelitian memiliki ciri-ciri tropozoit berbentuk bulat hingga agak oval dengan diameter 38.85 – 126.91 μm, diameter nukleus 7.77 – 12.95 μm, diameter gametosit 77.7 – 264.18 μm, oocyst kedua ujungnya lancip dengan panjang 7.77 – 15.45 μm dan lebar 3.88 – 7.77 μm. Berdasarkan ciri-ciri tesebut, Monocystis yang diperoleh dalam penelitian bukanlah M. ventrosa.
Sebagai parasit, Monocystis juga mempengaruhi pertumbuhan cacing tanah. Namun, Monocystis tidak berpengaruh terhadap produksi kokon cacing (Field & Michiels 2005).
Dalam penelitian, setiap vesikula seminalis terinfeksi Monocystis. Namun,
Monocystis jarang ditemukan pada
spermateka atau cairan selom. Ukuran oocyst, gametosit, dan tropozoit bervariasi (lihat hasil). Sesuai dengan pernyataan Wallace dan Taylor (1997) yang menyatakan bahwa bentuk tropozoit Monocystis bervariasi, bentuk tropozoit yang ditemukan tidak selalu oval, ditemukan juga bentuk yang membulat. Pada beberapa sampel yang terinfeksi
Monocystis hanya ditemukan oocyst tanpa gametosit atau tropozoit. Hal ini dimungkinkan karena sedikitnya Monocystis
yang menginfeksi cacing.
SIMPULAN
Monocystis menginfeksi cacing tanah
Pheretima darnleiensis dengan intensitas 500 – 1 074 000 oocyst/mm3
. Intensitas
Monocystis pada cacing tanah berkaitan dengan lokasi ditemukannya cacing tanah.
SARAN
Jumlah sampel serta lokasi pengambilan sampel perlu ditambah dan perlu ditemukan cara penghitungan Monocystis yang lebih baik.
DAFTAR PUSTAKA
Bandyopadhyay PK, Bhowmik B, Mitra AK. 2005. Observations on a new species of
Monocystis Stein, 1884 (Protozoa: Apicomplexa: Monocystidae) Monocystis levinei sp. nov. from an Indian earthworm (Annelida: Oligochaeta) Eutyphoeus incommodus. Zootaxa 1016:15–19. Bandyopadhyay PK, Mallik P, Gocmen B,
Mitra AK. 2006a. Monocystis
apporectodae sp. nov. (Protista:
Apicomplexa: Eugregarinida), from an Indian earthworm Apporectodea trapezoides Duges. Turkiye Parazitoloji Dergisi 30(1):50–52.
Bandyopadhyay PK, Mallik P, Gocmen B, Mitra AK. 2006b. Monocystis metaphirae
sp. nov. (Protista: Apicomplexa: Monocystidae) from the earthworm
Metaphire houlleti (Perrier). Turkiye Parazitoloji Dergisi 30(1):53–55.
Bandyopadhyay PK, Mitra AK. 2005. Observations on two new species of
Monocystis Stein, 1848 (Protozoa: Apicomplexa: Monocystidae) Monocystis
darjeelingensis sp.n. and M.
ranaghatensis sp.n. from earthworms (Annelida: Oligochaeta) of West Bengal, India. Animal Biology 55(2):123–132. Brown FAJr, editor. 1950. Selected
Invertebrate Types. New York: J Wiley. Brusca RC, Brusca GJ. 1990. Invertebrates.
Sunderland: Sinauer Inc.
Field SG, Michiels NK. 2005. Parasitism and growth in the earthworm Lumbricus terrestris: fitness costs of the gregarine parasite Monocystis sp. J Parasitol
130:397-403.
Field SG, Michiels NK. 2006. Acephaline gregarine parasites (Monocystis sp.) are not transmitted sexually among their lumbricid earthworm host. J Parasitol
92(2):292–297.
5
Kemungkinan daerah tersebut terkontaminasi dengan bahan kimia yang dibuang sehingga mematikan oocyst Monocystis. Demikian pula pada tempat sampah. Daerah bekas kandang sapi letaknya jauh dari laboratorium biokimia, intensitas Monocystis pada cacing relatif lebih tinggi. Hal ini menguatkan dugaan bahwa kualitas tanah berpengaruh terhadap intensitas
Monocystis.
Monocystis merupakan parasit yang memiliki inang spesifik, tetapi dapat juga ditemukan spesies Monocystis yang sama pada cacing yang berbeda spesiesnya. Misalnya M. ventrosa ditemukan pada
Lumbricus rubellus dan L. Castaneus. M. ventrosa memiliki ciri-ciri tropozoit berukuran 109 – 183 μm, diameter nukleus mencapai 43 μm, diameter gametosit 185 – 223 μm, oocyst 17 – 25 μm, serta ujung anterior dan posterior dapat dibedakan (Wallace & Taylor 1997).
Monocystis yang diperoleh dalam
penelitian memiliki ciri-ciri tropozoit berbentuk bulat hingga agak oval dengan diameter 38.85 – 126.91 μm, diameter nukleus 7.77 – 12.95 μm, diameter gametosit 77.7 – 264.18 μm, oocyst kedua ujungnya lancip dengan panjang 7.77 – 15.45 μm dan lebar 3.88 – 7.77 μm. Berdasarkan ciri-ciri tesebut, Monocystis yang diperoleh dalam penelitian bukanlah M. ventrosa.
Sebagai parasit, Monocystis juga mempengaruhi pertumbuhan cacing tanah. Namun, Monocystis tidak berpengaruh terhadap produksi kokon cacing (Field & Michiels 2005).
Dalam penelitian, setiap vesikula seminalis terinfeksi Monocystis. Namun,
Monocystis jarang ditemukan pada
spermateka atau cairan selom. Ukuran oocyst, gametosit, dan tropozoit bervariasi (lihat hasil). Sesuai dengan pernyataan Wallace dan Taylor (1997) yang menyatakan bahwa bentuk tropozoit Monocystis bervariasi, bentuk tropozoit yang ditemukan tidak selalu oval, ditemukan juga bentuk yang membulat. Pada beberapa sampel yang terinfeksi
Monocystis hanya ditemukan oocyst tanpa gametosit atau tropozoit. Hal ini dimungkinkan karena sedikitnya Monocystis
yang menginfeksi cacing.
SIMPULAN
Monocystis menginfeksi cacing tanah
Pheretima darnleiensis dengan intensitas 500 – 1 074 000 oocyst/mm3
. Intensitas
Monocystis pada cacing tanah berkaitan dengan lokasi ditemukannya cacing tanah.
SARAN
Jumlah sampel serta lokasi pengambilan sampel perlu ditambah dan perlu ditemukan cara penghitungan Monocystis yang lebih baik.
DAFTAR PUSTAKA
Bandyopadhyay PK, Bhowmik B, Mitra AK. 2005. Observations on a new species of
Monocystis Stein, 1884 (Protozoa: Apicomplexa: Monocystidae) Monocystis levinei sp. nov. from an Indian earthworm (Annelida: Oligochaeta) Eutyphoeus incommodus. Zootaxa 1016:15–19. Bandyopadhyay PK, Mallik P, Gocmen B,
Mitra AK. 2006a. Monocystis
apporectodae sp. nov. (Protista:
Apicomplexa: Eugregarinida), from an Indian earthworm Apporectodea trapezoides Duges. Turkiye Parazitoloji Dergisi 30(1):50–52.
Bandyopadhyay PK, Mallik P, Gocmen B, Mitra AK. 2006b. Monocystis metaphirae
sp. nov. (Protista: Apicomplexa: Monocystidae) from the earthworm
Metaphire houlleti (Perrier). Turkiye Parazitoloji Dergisi 30(1):53–55.
Bandyopadhyay PK, Mitra AK. 2005. Observations on two new species of
Monocystis Stein, 1848 (Protozoa: Apicomplexa: Monocystidae) Monocystis
darjeelingensis sp.n. and M.
ranaghatensis sp.n. from earthworms (Annelida: Oligochaeta) of West Bengal, India. Animal Biology 55(2):123–132. Brown FAJr, editor. 1950. Selected
Invertebrate Types. New York: J Wiley. Brusca RC, Brusca GJ. 1990. Invertebrates.
Sunderland: Sinauer Inc.
Field SG, Michiels NK. 2005. Parasitism and growth in the earthworm Lumbricus terrestris: fitness costs of the gregarine parasite Monocystis sp. J Parasitol
130:397-403.
Field SG, Michiels NK. 2006. Acephaline gregarine parasites (Monocystis sp.) are not transmitted sexually among their lumbricid earthworm host. J Parasitol
92(2):292–297.
6
earthworm Lumbricus terrestris. Can J Zool 81:1161-1167.
Kudo RR. 1946. Protozoology, ed ke-3. Springfield: Charles C Thomas.
Morgan M. 1999. Monocystis. www.microscopy-uk.net/mag/artmar99/ cystis.html [4 Jun 2006].
Omoto CK, Cartwright DC. 2003. Investigating the Diversity of Parasitic Protozoa Using Gregarine Parasites of Invertebrates. www.zoo.utoronto. ca/able/volumes/vol-24/6-omoto.pdf - [4 Jun 2006].
Reinhart M, Dollahon N. 2003. Response of coelomocytes from Lumbricus terrestris to native and non-native eukaryotic parasites.
Pedobiologia 47:710-716.
Santi AUP. 2006. Beberapa aspek biologi cacing tanah Pheretima darnleiensis
(Fletcher) [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Sheridan P. 1998. Monocystis: Earthworm Parasites. www.carolina. com/manuals/ manuals3/Monocystis%20Earthworm%20 Parasite.pdf – [4 Jun 2006].
Sims RW, Easton EG. 1972. A Numerical Revision of the Earthworm Genus Pheretima auct. (Megascolecidae: Oligochaeta) with the Recognition of New Genera & an Appendix on the Earthworms Collected by the Royal Society North Bordeo Expedition. London: British Museum (Natural History).
Stephenson J. 1930. The Oligochaeta. Oxford: Clarendon Press.