PENGARUH SUHU REAKSI TERHADAP DERAJAT KRISTALINITAS
DAN KOMPOSISI HIDROKSIAPATIT DIBUAT DENGAN MEDIA AIR
DAN CAIRAN TUBUH BUATAN (SYNTHETIC BODY FLUID)
Oleh :
EKO FIRMAN PURNAMA
G74102024
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
EKO FIRMAN PURNAMA. Pengaruh Suhu Reaksi Terhadap Derajat Kristalinitas dan Komposisi Hidroksiapatit Dibuat dengan Media Air dan Cairan Tubuh Buatan (Synthetic Body Fluid) Dibimbing oleh SITI NIKMATIN dan RATIH LANGENATI
Hidroksiapatit sangat dekat dengan komponen tulang dan mineral gigi. Kalsium berikatan dengan gugus fosfat, hidroksida dan karbonat. Hidroksiapatit yang digunakan sebagai implant pada tulang harus memiliki sifat biokompatibel dan bioaktif. Biokompatibel adalah kemampuan material untuk menyesuaikan dengan kecocokan tubuh penerima, sedangkan bioaktif adalah kemampuan material bereaksi dengan jaringan dan menghasilkan ikatan kimia yang sangat baik. Pada penelitian ini digunakan dua pelarut yaitu pelarut air dan pelarut cairan tubuh sintetik (Synthetic Body Fluid-SBF). SBF adalah larutan yang mengandung ion-ion yang komposisinya mendekati cairan tubuh manusia (blood plasma) sehingga pada saat diimplant didalam tubuh HAp sintetik dengan pelarut SBF tersebut dapat cepat mudah diserap dan diterima oleh tubuh.
Pada pengeringan menggunakan freeze drying dihasilkan gas CO2 dari ion karbonat saat
pembuatan HAp akan tertahan sehingga tidak banyak hilang dibandingkan pemanasan dalam oven yaitu dihasilkan butir kristal yang lebih halus. Variasi temperatur 40, 70 dan 90oC saat pemanasan pembuatan HAp, dengan variasi temperatur dihasilkan perbedaan derajat kristalinitas pada setiap temperatur. Karakterisasi senyawa HAp dengan menggunakan X-Ray Difraction (XRD) dengan tujuan melihat derajat kristalinitas dari kristal apatit dan fase yang ada,Fourier Transform Infrared
(FTIR) mengidentifikasi kandungan gugus kompleks dalam senyawa HAp, Scanning Electron Microscophy (SEM) memberikan penjelasan yang detail dari permukaan, memberikan informasi penumbuhan kristal dan melihat morfologi serbuk hidroksiapatit, Atomic Absorption Spectroscopy
(AAS) digunakan untuk mengukur kadar Ca, Mg, K, dan Na ; dan Spektroskopi UV-Vis digunakan untuk mengukur kadar fosfor.
Kata kunci: hidroksiapatit, cairan tubuh buatan, freeze drying, derajat kristalinitas, XRD, FTIR, SEM, AAS dan UV-Vis.
ABSTRACT
Hydroxyapatite is very close to our life as the main component of bone and tooth minerals. Calcium bounded with phosphate group, hydroxide, and carbonate. Hydroxyapatite used for implant in bone must have biocompatible and bioactive behavior. Biocompatibility is the ability of a material to perform with an appropriate host response in a specific application, whereas bioactive is ability material responded with tissue and result chemical bone well. This research used two solutions aquadest and Synthetic Body Fluid (SBF). SBF is a solution containing ions composition nearly equal to this of blood plasma when implanted in body HAp synthetic can easy to absorb and host response.
In drying use freeze drying resulted carbon gas from carbonate content trapped to protect vaporize compared with heating in oven, freeze drier result a smoother grain size. Temperature variation in 40, 70, and 90oC when heating precipitation HAp resulted different crystalinity degree for those temperatures. Characterization of HAp powder used X-Ray Difraction (XRD) analysis showed crystalinity degree and phase of apatite crystal. Fourier Transform Infrared (FTIR) was used for identified group complex contains in HAp, Scanning Electron Microscophy (SEM) explained detail of surface area, give information growth of crystal and showed morphology HAp powder, Atomic Absorption Spectroscopy (AAS) determined calcium, magnesium, kalium, and natrium contents; and UV-Vis Spectroscopy determined phosphorus content.
PENGARUH SUHU REAKSI TERHADAP DERAJAT KRISTALINITAS
DAN KOMPOSISI HIDROKSIAPATIT DIBUAT DENGAN MEDIA AIR
DAN CAIRAN TUBUH BUATAN (SYNTHETIC BODY FLUID)
Skripsi
Sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
Pada Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Oleh :
EKO FIRMAN PURNAMA
G74102024
DEPARTEMEN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul
: Pengaruh Suhu Reaksi Terhadap Derajat Kristalinitas
dan Komposisi Hidroksiapatit Dibuat dengan Media Air
dan Cairan Tubuh Buatan
(
Synthetic Body Fluid
)
Nama
: Eko Firman Purnama
NRP
: G74102024
Menyetujui :
Pembimbing I
Pembimbing II
Siti Nikmatin, M.Si
Ir. Ratih Langenati, M.T
NIP.
132282667
NIP.
330003891
Mengetahui :
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Institut Pertanian Bogor
Dr. Ir. Yonny Koesmaryono, M.S
NIP. 131473999
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 18 Juni 1984 sebagai anak pertama dari dua bersaudara dari pasangan Suhardi dan Martini.
Penulis menyelesaikan pendidikan dasar di SD Negeri 17 Kebayoran Lama Selatan pada tahun 1996, pendidikan menengah tingkat pertama di SMP YPUI Kebayoran Lama Selatan tahun 1999, dan melanjutkan ke SMA 47 Jakarta.
Pada tahun 2002, penulis diterima di Institut Pertanian Bogor (IPB) melalui jalur Undangan Seleksi Masuk IPB (USMI) sebagai mahasiswa di Departemen Fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam.
PRAKATA
Segala puji kepada Allah SWT tuhan semesta alam yang telah melimpahkan nikmat Iman dan nikmat Islam, Sholawat serta Salam semoga tetap tercurah kepada suri tauladan ummat Rasulullah Muhammad SAW.
Suatu kebahagiaan yang sangat besar, karya ini akhirnya dapat diselesaikan dengan penuh perjuangan dan kesabaran untuk melaluinya. Skripsi ini berjudul Pengaruh Suhu Reaksi Terhadap Derajat Kristalinitas dan Komposisi Hidroksiapatit Dibuat dengan Media Air dan Cairan Tubuh Buatan (Synthetic Body Fluid)
Merupakan kebanggaan bagi penulis, dan patutlah penulis haturkan terima kasih kepada : 1. Siti Nikmatin, M.Si selaku pembimbing I dalam penelitian ini yang telah membimbing penulis
dengan penuh motivasi, petunjuk, dan kesabaran dari awal hingga akhir.
2. Ir. Ratih Langenati, M.T selaku pembimbing II yang telah membimbing penulis dari mulai di laboratorium sampai karakterisasi dengan penuh kesabaran dengan senyumnya yang ceria. 3. Dr. Kiagus Dahlan dan Jajang Juansah, M.Si sebagai dosen penguji seminar usul, dan
Akhiruddin Maddu, M.Si sebagai dosen penguji seminar hasil untuk semua masukannya. 4. Ir. Hanedi Darmasetiawan, M.S selaku komisi pendidikan Departemen Fisika.
5. Mba Yessie untuk semua saran dan motivasinya yang telah diberikan dan seluruh dosen karyawan Departemen Fisika khususnya Bapak Firman atas segala perhatian dan bantuannya. 6. Bapak Ngatijo dan Bapak Basril atas bantuannya sintesa dan pengeringan freeze drying Hap. 7. Bapak Bambang Sugeng dan Bapak Sulistyo Giat atas bantuannya dalam karakterisasi XRD. 8. Bapak Arif untuk pelaksanaan karakterisasi ICP.
9. Bapak Andung dan Bapak Nusin atas bantuannya dalam analisa SEM.
10. Bapak Maskur dan Bapak Cecep yang telah membantu pelaksanaan karakterisasi FTIR. 11. Bapak Rahmat dan Bapak Wawan yang telah membantu pelaksanaan karakterisasi AAS dan
UV-Vis.
12. Teman seperjuangan dalam penelitian ini “Arifianto”.
13. Ibunda dan Ayahanda yang senantiasa mendo’akan Ananda baik diwaktu pagi, siang dan malam. Serta didikan dan kasih sayang yang selalu tercurah. Semoga Allah SWT membalas segalanya dengan balasan yang lebih baik dan mengangkat Ibunda dan Ayahanda ketempat tertinggi disisi Allah SWT.
14. Adikku yang selalu membuat keceriaan dan menghiburku saat pulang ke rumah, sehingga dapat menghilangkan kejenuhan. Semoga Allah SWT membalasnya dengan kebaikan.
15. Semua sepupuku, pakde, dan bule yang tidak bisa disebutkan satu persatu, telah memberi dukungan sepenuhnya kepada penulis.
16. Kepada kekasihku yang selalu memberi semangat kapanpun dan dimanapun juga kasih sayangnya kepada penulis. Raihlah cita-citamu dengan serius, tekun dan kerja keras, juga diiringi dengan do’a.
17. Keluarga besar LBB Foton terutama kepada Abah Uci Sanusi, Pak Eko, dan seluruh staf pengajar yang selalu memberi dorongan semangat dan motivasi untuk menyelesaikan karya ini dengan sebaik-baiknya.
18. Alumni SMAN 47 Jakarta tercinta khususnya ANGKATAN 2002 (Fajri, Sony, Melly, Adam, Lisna, Ucok, P-Man, dan masih banyak lagi...) atas semua bantuan dan support-nya.
19. Keluarga besar ELVO : Nick Kabon, Sonny Jhintol, Lutpan Thoghe, Arif Komti, MR-1 Dower, Eko Jhambie, Ted Song, Ryan, A-6, dan No2.
20. Rekan-rekan seperjuangan FISIKA ’39 di ELVO, Kos Bravo, Salsabila, dan Kos-kosan yang lainnya Aletta, Teguh, Budi, Didit. Terima kasih atas segala bantuan dan kerjasamanya, semoga kita tetap menjaga silaturahmi sampai tua nanti.
21. Rekan-rekan FISIKA ’37, FISIKA ’38, FISIKA ’40, FISIKA ’41, INSTEK ’39, dan ELTEK ’40 atas dukungan serta bantuannya kepada penulis.
22. Rekan-rekan seperjuangan di HIMAFI dan dalam kegiatan BEM FMIPA. Terima kasih atas dukungan, keceriaannya, dan rasa kebersamaannya.
Semoga karya ini dapat bermanfaat bagi kita semua.
Bogor, Maret 2006
DAFTAR ISI
Halaman
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... vii
PENDAHULUAN ... 1
Latar Belakang ... 1
Batasan Masalah ... 2
Hipotesis ... 2
Tujuan Penelitian ... 2
Waktu dan Tempat Penelitian ... 2
TINJAUAN PUSTAKA ... 2
Presipitasi Hidroksiapatit dengan Synthetic Body Fluid (SBF) ... 2
Pengaruh Ion dari SBF pada Hidroksiapatit ... 3
Prinsip Freeze Drying ... 3
Prefreezing ... 3
Primary Drying ... 4
Secondary Drying ... 4
Identifikasi Hidroksiapatit dengan XRD ... 4
Identifikasi Hidroksiapatit denganFTIR ... 5
Morfologi Hidroksiapatit dengan SEM ... 5
Identifikasi Hidroksiapatit denganAAS ... 6
Identifikasi Hidroksiapatit dengan Spektroskopi UV-Vis ... 6
BAHAN DAN METODE ... 7
Bahan dan Alat ... 7
Metode Penelitian ... 7
Preparasi Sampel ... 7
Pengeringan ... 8
Karakterisasi dengan XRD ... 8
Karakterisasi dengan FTIR ... 8
Karakterisasi dengan SEM ... 8
Karakterisasi dengan (AAS) dan Spektroskopi UV-Vis ... 8
HASIL DAN PEMBAHASAN ... 10
Sintesa Hidroksiapatit ... 10
Analisa Derajat Kristalinitas dengan XRD ... 10
Identifikasi Gugus Anion PO43-, CO32-dan H2O dengan FTIR ... 12
Morfologi dengan SEM ... 14
Identifikasi Unsur Kation Ca, Mg, Na, K, dan P dengan AAS dan Spektroskopi UV-Vis .... 14
SIMPULAN DAN SARAN ... 15
Simpulan ... 15
Saran ... 15
DAFTAR PUSTAKA ... 15
DAFTAR TABEL
Halaman
1. Komposisi ion-ion dalam blood plasma dan SBF ... 3
2. Senyawa pembuatan larutan SBF ... 7
3. Data XRD untuk kristalinitas HAp pelarut air ... 11
4. Persentase kristalinitas HAp pelarut air ... 11
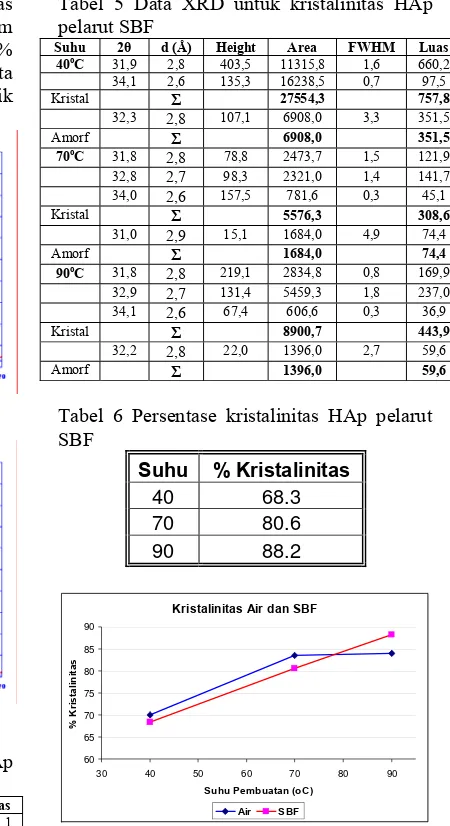
5. Data XRD untuk kristalinitas HAp pelarut SBF ... 11
6. Persentase kristalinitas HAp pelarut SBF ... 11
7. Hasil pengukuran kation HAp sintetik dengan AAS dan UV-Vis ... 15
8. Rasio molar Ca/P HA sintetik ... 15
DAFTAR GAMBAR
Halaman 1. Struktur kristal hidroksiapatit ... 12. Diagram fasa air ... 4
3. Kurva sublimasi air ... 4
4. Proses terjadinya difraksi oleh kisi kristal ... 5
5. Skema SEM ... 6
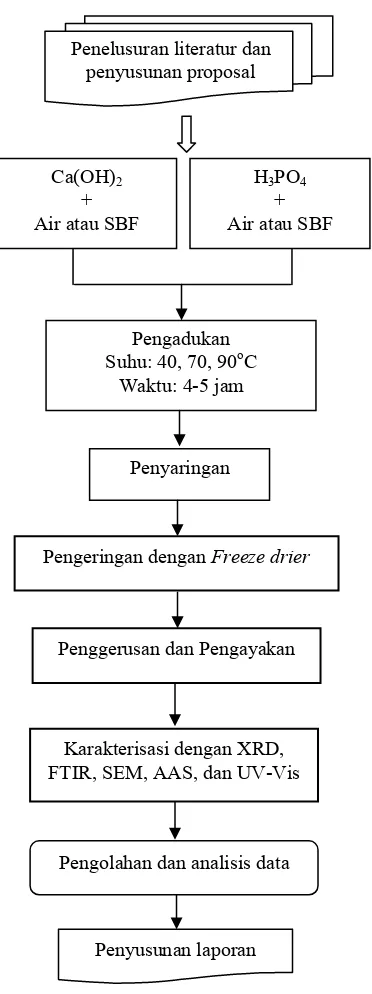
6. Diagram alir penelitian ... 9
7. Pola XRD HAp pelarut air ... 10
8. Pola XRD HAp pelarut SBF ... 10
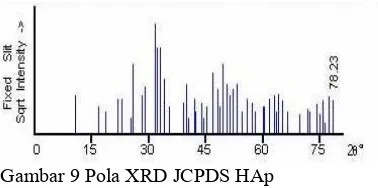
9. Pola XRD JCPDS HAp ... 10
10. Penghilangan background XRD... 11
11. Penghilangan amorf XRD ... 11
12. Persentase kristalinitas HAp pelarut air dan SBF ... 11
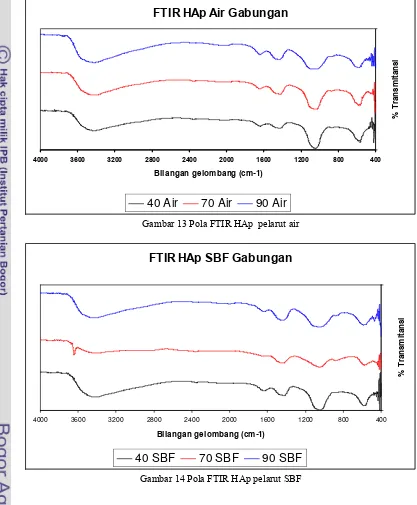
13. Pola FTIR HAp pelarut air ... 13
14. Pola FTIR HAp pelarut SBF ... 13
15. Morfologi HAp sintetik dengan perbesaran 40.000 kali (a). HAp 40oC air, (b). HAp 70oC air, (d). HAp 40oC SBF, (e). HAp 70oC SBF ... 14
16. Morfologi HAp sintetik dengan perbesaran 40.000 kali (c). HAp 90oC air, (f). HAp 90oC SBF... 14
DAFTAR LAMPIRAN
Halaman 1. Pola XRD serta hkl HAp pelarut air dan SBF dengan variasi suhu pembuatan ... 182. Data JCPDS hidroksiapatit ... 21
3. Spektrum IR HAp pelarut air dan SBF dengan variasi suhu pembuatan ... 22
PENDAHULUAN
Latar Belakang
Hidroksiapatit mendekati komponen tulang dan mineral gigi. Kalsium yang terdapat dalam tulang berbentuk senyawa dan berikatan dengan gugus fosfat, hidroksida dan karbonat. Senyawa HAp dalam tulang terdapat dua bentuk fase yaitu fase amorf dan fase kristal sedangkan fase stabil kristal HAp lebih dikenal dengan nama hidroksiapatit (HAp) [1].
Hidroksiapatit atau HAp menurut definisi Hideki (1991) adalah senyawa mineral dari anggota kelompok mineral apatit dengan rumus kimia Ca(10-x)Ax(PO4)(6-y)BBy(OH)(2-z)Cz. Campuran apatit memiliki karakteristik struktur kristal umum dengan sistem heksagonal dengan dimensi sel a = 9.423 Å dan c = 6.875 Å.
Disamping komponen utamanya kalsium dan fosfat, tulang atau gigi juga mengandung ion magnesium, natrium, dan kalium yang menempati posisi A. Sedangkan ion karbonat, klorid atau fluorid menempati posisi B atau C. Besar kecilnya jumlah kation dan anion tergantung dari fungsi tulang tersebut, misalnya pada gigi kandungan fluoridnya lebih besar dibandingkan pada tulang lainnya. Pada tulang anak-anak kandungan magnesiumnya lebih besar dibandingkan dengan tulang pada orang dewasa dan lain sebagainya.
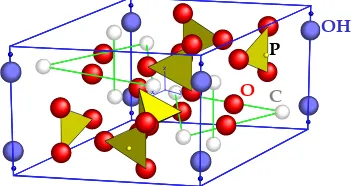
Struktur hidroksiapatit hampir menyerupai fluorapatit dengan struktur hidroksiapatit, atom F digantikan dengan gugus OH. Struktur kristal hidroksiapatit yang diproyeksikan sepanjang sumbu-c ditunjukan pada Gambar 1. Pada Gambar 1 terdapat dua atom bebas Ca dalam satuan sel. Atom Ca(2) dikelilingi oleh 6 atom oksigen milik gugus PO4 dan gugus OH, sedangkan atom Ca(1)
struktur oktahedral dikelilingi oleh 6 atom oksigen. Atom Ca(2) membentuk segitiga normal yang tersusun bertumpuk sepanjang sumbu-c dan saling berputar 60o dari satu sama lain. Dalam struktur fluorapatit letak atom F pada pusat segitiga Ca(2), dalam struktur hidroksiapatit gugus OH tidak terletak pada pusat tetapi diganti diatas atau dibawah pusat segitiga. Atom P dikelilingi oleh 4 atom oksigen berbentuk tetrahedron. Berbentuk teratur atau hanya sedikit terdistorsi [1].
Hidroksiapatit yang digunakan sebagai implant pada tulang harus memiliki sifat biokompatibel dan bioaktif. Biokompatibel adalah kemampuan material untuk menyesuaikan dengan kecocokan tubuh
penerima, sedangkan bioaktif adalah kemampuan material bereaksi dengan jaringan dan menghasilkan ikatan kimia yang sangat baik. Hidroksiapatit yang berasal dari makhluk hidup biasa disebut biological hydroxyapatite atau bio-HAp, contohnya tulang manusia, gigi, tulang ikan, tulang hewan, dll. Bio-HAp dapat digunakan di bidang medis antara lain pada bidang ortopedi, bedah gigi dan mulut (maxilofacial), bedah plastik dan rekonstruksi, bedah neurologi serta bedah mata ataupun sebagai
drug carrier. Bahan ini dapat diperoleh dari manusia yang bersangkutan disebut autograft, dari manusia lainnya disebut allograft, dan dari hewan disebut xenograft. Pemakaian
autograft biasanya tidak menimbulkan reaksi penolakan dari tubuh, hanya saja ketersediaannya terbatas dan mempersyaratkan pembedahan. Sedangkan pemakaian allograft dan xenograft kadang-kadang menimbulkan reaksi penolakan dari tubuh, dapat menjadi sarana perpindahan penyakit dan ketersediaannya pun terbatas [2].
Keterbatasan-keterbatasan tersebut memicu perkembangan riset dibidang biomaterial untuk mengatasinya termasuk HAp. Bahan HAp yang dibuat secara sintesa kimia disebut HAp sintetik. Keunggulan dari HAp sintetik dibanding dengan lainnya adalah bahan ini mempunyai karakter dapat menyatu dengan tulang manusia atau matriksnya, cocok dengan matriksnya, kemurnian bahan, komposisi fasa dan mikrostruktur.
Hal tersebut berpengaruh secara signifikan manakala bahan tersebut digunakan sebagai bahan tulang tiruan, bahan tambalan gigi, atau drug carrier ketika kontak langsung dengan jaringan tubuh, khususnya sifat
resorbability, biodegradation, cytotoxicity
ataupun carcinogenicity. Pada pemakaian tertentu sifat mekanik juga diperhitungkan sesuai dengan peruntukannya, sifat-sifat tersebut sangat menentukan durability dan masa pakai dalam tubuh manusia [2].
x y z
OH
C P
Gambar 1 Struktur kristal hidroksiapatit. (Putlayev, Valery. 2002. Inorganic Materials Lab. Moscow State University)
Batasan Masalah
1. Pada penelitian ini digunakan dua pelarut yaitu pelarut air dan pelarut cairan tubuh sintetik (Synthetic Body Fluid) SBF. SBF adalah larutan yang mengandung ion-ion yang komposisinya mendekati cairan tubuh manusia (blood plasma).
2. Variasi temperatur yang digunakan saat pemanasan adalah 40, 70 dan 90oC.
3. Pengeringan dilakukan dengan menggunakan freeze drier.
4. Karakterisasi HAp sintetik menggunakan alat X-Ray Difraction
(XRD), Fourier Transform Infrared
(FTIR), Scanning Electron Microscophy (SEM), Atomic Absorption Spectroscopy (AAS), dan Spektroskopi UV-Vis.
Hipotesis
1. Penggunaan pelarut cairan tubuh sintetik (Synthetic Body Fluid) SBF diharapkan menghasilkan HAp yang memiliki kandungan unsur mendekati karakter tulang dan meningkatkan sifat biokompatibel dan bioaktif dari hidroksiapatit sehingga lebih mudah diterima tubuh dibandingkan dengan penggunaan pelarut air.
2. Peningkatan temperatur reaksi pembuatan HAp diharapkan dapat meningkatkan derajat kristalinitas HAp.
3. Pengeringan menggunakan freeze drier diharapkan gas CO2 dari ion
karbonat saat pembuatan HAp akan tertahan sehingga tidak banyak hilang.
Tujuan Penelitian
1. Membuat senyawa hidroksiapatit menggunakan pelarut cairan tubuh sintetik (Synthetic Body Fluid) SBF dan air.
2. Mengetahui pengaruh variasi temperatur reaksi 40, 70 dan 90oC saat pembuatan terhadap derajat kristalinitas HAp.
3. Mengetahui adanya ion karbonat hasil pengeringan menggunakan
freeze drier.
4. Melakukan karakterisasi senyawa HAp dengan menggunakan X-Ray Difraction (XRD), Fourier Transform Infrared (FTIR),
Scanning Electron Microscophy
(SEM), Atomic Absorption Spectroscopy (AAS), dan Spektroskopi UV-Vis.
Waktu dan Tempat Penelitian
Preparasi sampel, karakterisasi FTIR dan SEM dilaksanakan di Laboratorium P2TBDU, karakterisasi XRD di Laboratorium P3IB BATAN Puspiptek Serpong, sedangkan karakterisasi AAS dan spektroskopi UV-Vis dilakukan di Laboratorium Terpadu IPB. Waktu yang diperlukan penelitian ini adalah delapan bulan dari Juli 2005 sampai Februari 2006, meliputi penyusunan proposal, penelitian (penyiapan alat dan bahan, percobaan, karakterisasi, analisa dan evaluasi), serta penyusunan laporan.
TINJAUAN PUSTAKA
Presipitasi Hidroksiapatit dengan Synthetic Body Fluid (SBF)
Salah satu indikator yang dimiliki oleh kristal hidroksiapatit adalah rasio perbandingan Ca/P yaitu sebesar 1,667. Jika konsentrasi masing-masing komponen penyusun senyawa HAp yang ingin disintesis diketahui kadarnya, maka akan mudah melakukan pendekatan dengan menggunakan rasio ini. Harga perbandingan Ca/P sebesar 1,667 bisa dihasilkan jika kondisi pH dan kadar karbonat dalam solusi larutan dapat terkontrol dengan baik [3]. Harga perbandingan Ca/P ini harus mendekati nilai sebenarnya yang terdapat dalam jaringan keras.
Tampieri (2002) dan Geros (1991) menyatakan bahwa adanya karbonat dalam HA disebut juga carbonated Hydroxyapatite
atau (CHAp) akan meningkatkan biokompatibel dan bioaktif. Pada jenis HAp ini karbonat dapat menempati posisi hidroksil (OH-) (CHAp tipe A) dan atau fosfat (PO43-)
(CHAp tipe B). Untuk mendapatkan CHAp dapat diperoleh dengan mengalirkan gas CO2
selama proses pembuatan dengan metode basah. Dalam hal ini, gas CO2 menjadi sumber
karbonat yang akan terikat pada posisi hiroksil atau fosfat dari HAp yang dibuat. Sumber karbonat yang diperlukan dapat diperoleh bila media yang digunakan juga mengandung ion karbonat [4].
mengganti pelarut air dengan Synthetic Body Fluids (SBF) sebagai pelarut dalam pembuatan. Pembuatan serbuk HAp menggunakan metoda basah dengan bahan baku kalsium hidroksida sebagai sumber kalsium dan asam fosfat sebagai sumber fosfat dengan pelarut air atau dengan pelarut SBF.
Synthetic Body Fluids (SBF) adalah model larutan yang sangat disukai sebagai simulasi bagian inorganik dari plasma darah. Plasma darah adalah larutan yang mengandung variasi garam, gula, asam amino, dan mineral-mineral sepanjang sel darah. Bagian inorganik plasma darah mengandung konsentrasi ion berbeda seperti sodium, kalsium, magnesium, dan ion klorin. Serta bersifat metastabil karena derajat supersaturasi ke apatit tidak cukup tinggi untuk melampaui energi aktivasi inti apatit (Li et al 1993) [5]. SBF dapat dibuat dengan mencampurkan reaktan NaCl, NaHCO3, KCl,
K2HPO43H2O, MgCl26H20, CaCl2, dan
Na2SO4 kedalam air. Saat plasma darah pada
temperatur 36,5oC larutan SBF menjadi buffer pada pH 7,25 ; pada keadaan seperti ini konsentrasi ion plasma darah dan SBF mendekati sama. Komposisi SBF seperti Tabel 1.
SBF memiliki konsentrasi yang sama dengan cairan tubuh. Kandungan ion-ion dalam SBF memiliki peranan penting pembentukan fase apatit murni dalam sintetis basah. Presipitasi HAp dengan SBF yang mengandung sejumlah kation sebagai media pelarut dalam presipitasi, menunjukan stabil jika dipanaskan pada 1600 oC dalam udara yaitu kehadiran B-CHAp menurunkan kristalinitas, meningkatkan kelarutan dalam uji coba invitro dan invivo dan meningkatkan sifat mirip dengan tubuh HAp sintetis [6]. Tabel 1 Komposisi ion-ion dalam blood plasma dan SBF [2]
Konsentrasi (mM) Ion
Blood plasma SBF
Na+ 142,0 141,3
K+ 5,0 5,0
Mg2+ 1,5 1,5
Ca2+ 2,5 2,5
Cl- 103,0 164,4
HCO3- 27,0 26,9
HPO42- 1,0 1,0
SO42- 0,5 0,5
Pengaruh Ion dari SBF pada Hidroksiapatit
Ion Mg pada SBF dapat menggantikan ion Ca, kontribusinya seperti dilakukan ion CO32- menyebabkan turunnya derajat
kristalinitas HAp dan menstabilkan substitusi karbonat pada kisi. Pensubstitusian ion Mg pada serbuk HAp menunjukan meningkatkan bioreabsorbilitas (mempunyai permukaan yang reaktif dan interaksi lingkungan fisiologis untuk digantikan oleh jaringan lunak atau keras) dibandingkan HAp stoikiometri.
Ion karbonat (CO32-) di dalam tubuh
mempunyai dua kemungkinan, akan menggantikan ion fosfat (PO43-) atau ion
hidroksil (OH-). Jika yang digantikan adalah ion OH-, maka akan terbentuk kristal apatit tipe A. Sedangkan jika yang digantikan adalah ion PO43-, maka akan terbentuk kristal apatit
tipe B. Pada umumnya apatit biologi maupun sintesis yang diperoleh dengan presipitasi pada temperatur rendah adalah karbonat tipe B, sedangkan apatit yang diproduksi dari reaksi padat dan temperatur tinggi akan diperoleh karbonat tipe A [7].
Selain itu ion Na berasal dari larutan SBF akan berada dekat posisi OH yang menyebabkan penurunan tingkat dehidroksilasi pada temperatur tinggi. Sehingga dapat dilihat bahwa mineral-mineral yang terdapat dalam SBF dapat meningkatkan biokompatibel dan bioaktif HAp.
Prinsip Freeze drying
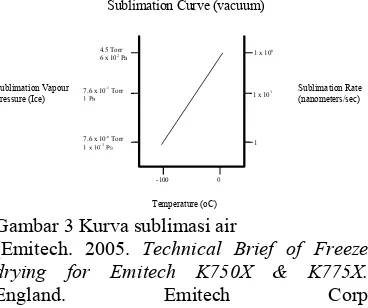
Freeze drying merupakan proses pembekuan air dalam endapan basah dan menghilangkannya dengan proses sublimasi (Gambar 3). Sublimasi terjadi ketika sebuah cairan beku mengalir langsung menuju keadaan gas tanpa melewati fase cair, dengan metode freeze drying material tidak akan pernah melalui fase cair. Pada temperatur dan tekanan normal air dalam endapan basah akan dikeringkan oleh evaporasi dan akan mengalami gaya tegangan permukaan antara cairan dan permukaan uap, bagaimanapun pada tekanan dibawah titik tripel fase padat dapat berubah menjadi fase uap rata-ratanya tergantung temperatur dengan hilangnya fase cair dan tekanan pada titik tripel relatif vakum [8].
Proses freeze drying terdiri dari tiga langkah yaitu prefreezing, primary drying, dan secondary drying [9].
Prefreezing
Metode dan temperatur akhir prefreezing
dry bahan, pada prefreeze temperatur diturunkan dibawah suhu eutetik (suhu standar suatu bahan untuk membeku) sebelum dilakukan proses freeze drying. Pendinginan sangat cepat menghasilkan kristal es yang kecil dan strukturnya dapat dilihat secara mikroskop. Sedangkan pendinginan lambat menghasilkan kristal yang besar dan matriks yang terbentuk sangat sedikit.
Primary Drying
Setelah proses prefreeze, kondisi harus dipertahankan dalam bentuk es yang dalam proses selanjutnya es akan dihilangkan menggunakan sublimasi dengan bantuan pompa vakum untuk menarik es dan air menjadi kering. Parameter yang harus dikontrol baik-baik adalah temperatur dan tekanan. Sublimasi rata-rata es hasil pendinginan tergantung dari perbedaan tekanan uap dari produk dibandingkan tekanan uap cold trap dalam alat.
Diagram fasa (Gambar 2) menjelaskan kebanyakan produk membeku dengan baik dibawah eutetiknya (titik A), lalu temperatur naik dibawah temperatur kritis (titik B) dengan turunnya tekanan, pada titik ini proses
freeze drying mulai. Pompa vakum adalah komponen penting sistem freeze dry dan digunakan pada tekanan lebih rendah dari lingkungan sekitar (titik C), lalu temperatur kolektor (titik D) harus lebih rendah dibandingkan temperatur produk.
Komponen ketiga yang penting dalam sistem
freeze drying adalah energi. Energi disuplai dalam bentuk panas.
Secondary Drying
Setelah primary freeze dying selesai dan semua es tersublimasi, hasil terlihat kering tetapi residual moisture content (sisa kandungan air dalam bahan) masih tinggi sekitar 7-8%. Pengeringan lanjutan diperlukan pada tekanan yang lebih tinggi untuk mereduksi residual moisture content menjadi nilai optimum, proses ini dinamakan
isothermal desorption. Hasil yang diharapkan berupa sampel dengan kandungan air hampir tidak ada.
Gambar 2 Diagram fasa air
(Labconco. 1998. A Guide To Freeze drying for the Laboratory. U.S.A. Labconco Corp
http://www.labconco.com [22 Februari 2005])
1 x 106
1 x 103
1
0 -100 4.5 Torr 6 x 102Pa
7.6 x 10-3 Torr 1 Pa
7.6 x 10-6 Torr 1 x 10-3Pa
Sublimation Rate (nanometers/sec) Sublimation Vapour
Pressure (Ice)
Temperature (oC) Sublimation Curve (vacuum)
Gambar 3 Kurva sublimasi air
(Emitech. 2005. Technical Brief of Freeze drying for Emitech K750X & K775X.
England. Emitech Corp
http://www.emitech.co.uk [23 April 2005])
Identifikasi Hidroksiapatit dengan XRD
Alat X-Ray Diffraction (XRD) digunakan untuk mengetahui struktur kristal, perubahan fasa dan derajat kristalinitas. Difraksi sinar X oleh atom-atom yang tersusun didalam kristal akan menghasilkan pola yang berbeda bergantung pada konfigurasi atom-atom pembentuk kristal.
Elektron yang dipancarkan dengan tegangan sangat tinggi menumbuk target (Cu, Cr, Fe, Co, Mo dan W). Energi kinetik elektron yang menumbuk target diantaranya berubah menjadi panas dan sinar-x, sinar-x yang dipancarkan dalam peristiwa ini terdistribusi secara tidak kontinu dengan λ yang berbeda.
sinar-x dengan panjang gelombang tertentu dan disebut dengan berkas sinar-x karakterisasi Kα dan Kβ.
Sinar-x ditembakan pada material sehingga terjadi interaksi dengan elektron dalam atom. Ketika foton sinar-x bertumbukan elektron, beberapa foton hasil tumbukan akan mengalami pembelokan dari arah datang awal. Jika panjang gelombang hamburan sinar-x tidak berubah (foton sinar-x tidak kehilangan banyak energi) dinamakan hamburan elastik (hamburan Thompson) dan terjadi transfer momentun dalam proses hamburan. Sinar-x ini yang digunakan untuk pengukuran sebagai hamburan sinar-x yang membawa informasi distribusi elektron dalam material.
Gelombang yang terdifraksikan dari atom-atom berbeda dapat saling mengganggu dan distribusi intensitas resultannya termodulasi kuat oleh interaksi ini. Syarat terjadinya difraksi harus memenuhi hukum Bragg 2d sin θ = n λ. Jika atom-atom tersusun periodik dalam kristal, gelombang terdifraksi akan terdiri dari interferensi maksimun tajam (peak) yang simetri, peak yang terjadi berhubungan dengan jarak antar atom, Gambar 4.
Gambar 4 Proses terjadinya difraksi oleh kisi kristal.
(__.2005. Introduction to X-ray Diffraction. Materials Research Laboratory. University of California
http://www.mrl.ucsb.edu/mrl/index.html
[25 Februari 2005])
Pola XRD serbuk HA akan diperoleh dalam jangkauan 2θ 10o sampai 70o memproduksi radiasi CuKα dengan panjang gelombang 0.154 nm. Analisis difrraksi sinar-X dengan tujuan melihat ukuran kristal, fase dan derajat kristalinitas dari kristal HAp yang ada. Perhitungan derajat kristalinitas menggunakan pendekatan luas segitiga karena sederhana dan mudah dimengerti
Identifikasi Hidroksiapatit denganFTIR
Spektroskopi inframerah Fourier Transform Infrared (FTIR) dapat mengidentifikasi kandungan gugus kompleks dalam senyawa HAp, tetapi tidak dapat digunakan untuk menentukan unsur-unsur penyusunnya. Spektroskopi inframerah memanfaatkan energi vibrasi gugus penyusun senyawa HA, yaitu: gugus PO43-, gugus CO32-,
gugus OH-. Gugus PO43- mempunyai 4 mode
vibrasi, yaitu:
1. Vibrasi simetri stretching (v1) dengan bilangan gelombang sekitar 956 cm-1. 2. Vibrasi simetri bending (v2) dengan
bilangan gelombang sekitar 430-460 cm-1.
3. Vibrasi asimetri stretching (v3) dengan bilangan gelombang sekitar 1040-1090 cm-1.
4. Vibrasi asimetri bending (v4) dengan bilangan gelombang sekitar 575-610 cm-1.
Hadirnya karbonat berpengaruh dalam proses presipitasi dan kristalisasi senyawa HAp. Bentuk pita v3 dan v4 yang tidak simetri merupakan tanda bahwa senyawa HAp tidak seluruhnya dalam bentuk amorf. Spektrum hidroksiapatit dapat diteliti yaitu pada v4
dalam bentuk belah dengan maksimum 562 cm-1 dan 602 cm-1. Pita absorpsi v3
mempunyai dua puncak maksimum yaitu pada bilangan gelombang 1090 cm-1 dan 1030 cm-1. Pita absorpsi v1 dapat dilihat pada bilangan gelombang 960 cm-1.
n
λ
Pita absorpsi OH- dapat terlihat juga dalam spektrum hidroksiapatit yaitu disekitar 3576 cm-1 dan 632 cm-1. Air dapat hadir dalam kristal maupun pada permukaan kristal tersebut. Air diatas permukaan kristal apatit akan hilang dan tidak dapat balik pada pemanasan di bawah suhu 2000C [10]. Pita serapan energi untuk gugus karbonat dapat diamati pada bilangan gelombang disekitar 1545, 1450, dan 890 cm-1. Kristal apatit tipe B mempunyai daerah bilangan gelombang disekitar 1465, 1412, 873 cm-1.
Morfologi Hidroksiapatit dengan SEM
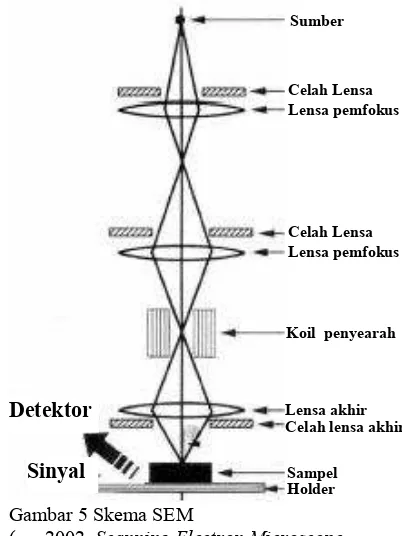
Gambar 5 Skema SEM
(__. 2002. Scanning Electron Microscope.
Oxford Univ.
http://www.unl.edu/CMRAcfem/semoptic.htm [20 Desember 2005])
Pemercepat elektron (electron gun) menghasilkan pancaran elektron monokromatis. Lensa pemfokus pertama menghasilkan pancaran dan batas arus, pada celah lensa berfungsi untuk mengurangi pembelokan sudut.
Lensa pemfokus kedua membentuk pelemahan (pancaran sinar koheren), celah lensa dikendalikan untuk mengurangi pembelokan sudut dari pancaran lensa pertama.
Pancaran yang dilewatkan lensa kedua dan mengalami proses scan oleh koil penyearah untuk membentuk gambar dan diteruskan ke lensa akhir untuk difokuskan ke sampel. Interaksi pancaran elektron dengan sampel dan elektron yang dipantulkan diterima oleh detektor. Detektor akan menghitung elektron-elektron yang diterima dan menampilkan intensitasnya. Proses terus berulang sampai proses scan selesai. Skema kerjanya dapat dilihat pada Gambar 5.
Pada pengukuran menggunakan SEM, sampel haruslah merupakan zat yang dapat menghantarkan arus listrik seperti halnya logam, karena hidroksiapatit tidak dapat menghantarkan arus listrik maka sebelum dianalisis terlebih dahulu dilapisi logam.
Logam emas lebih disukai karena emas merupakan logam inert dan bersifat konduktif.
Identifikasi Hidroksiapatit AAS
Atomic Absorption Spectroscopy (AAS) digunakan untuk mengukur kadar Ca, Mg, K, dan Na. Spektoskopi serapan atom (AAS) menggunakan prinsip penyerapan energi sinar oleh atom. Energi ini diberikan dari luar yang berasal dari lampu. AAS dapat dibagi menjadi dua proses besar: (1) Produksi atom bebas dari sampel. (2) Serapan radiasi dari sumber luar oleh atom. Serapan radiasi oleh atom bebas dalam suatu nyala, melibatkan transisi atom dari populasi tinggi pada tingkat dasar (ground state) ke tingkat eksitasi elektronik. Biasanya transisi terjadi antara tingkat dasar dan tingkat eksitasi pertama, yang dikenal dengan garis resonansi pertama. Garis resonansi pertama memilki absorbtivitas yang paling tinggi.
Spektrokopi ini berguna untuk penentuan unsur-unsur logam. Logam yang ingin ditentukan dalam senyawa hidroksiapatit adalah kalsium. Pengaruh ion magnesium pun akan ditentukan kadar persennya dengan menggunakan spektroskopi ini. Atom-atom kalsium atau magnesium dalam larutan akan diuapkan dalam api dengan temperatur tinggi, yang menyebabkan terurainya ikatan-ikatan kimia di dalam senyawa hidroksiapatit. Atom-atom tersebut akan menyerap sinar dari sumber (lampu). Intensitas awal dan intensitas akhir dari sinar tersebut akan diukur. Banyaknya sinar yang diserap menunjukan besarnya konsentrasi atau kadar logam tersebut dalam larutan.
Identifikasi Hidroksiapatit dengan Spektroskopi UV-Vis
Spektroskopi Ultraviolet-Visible digunakan untuk mengukur kadar fosfor, cara
kerjanya dengan memanfaatkan panjang gelombang pada daerah ultraviolet dan cahaya tampak. Panjang gelombang ini dihasilkan oleh sumber lampu yang memiliki panjang gelombang spesifik, sebagai contoh lampu hidrogen dan deuterium (160-375 nm), atau tungsten (350-2500 nm). Spektroskopi ini digunakan untuk mengukur kandungan molekul atau gugus yang terdapat dalam senyawa hidroksiapatit. Prinsip kerja alat ini adalah dengan menghitung transmitansi dari sinar yang dilewatkan oleh larutan yang ingin diukur kadarnya. Besar transmitansi dari larutan akan menunjukkan kadar penyusun senyawa tersebut sesuai dengan panjang gelombang yang digunakan.
Celah lensa akhir
Detektor Sinyal Sumber Celah Lensa Lensa pemfokus Celah Lensa Lensa pemfokus
Koil penyearah
Lensa akhir
BAHAN DAN METODE
Bahan dan Alat
Bahan yang digunakan dalam penelitian ini adalah :
1. Ca(OH)2 50 g
2. H3PO4 44,43 g
3. Pelarut SBF 1 l
a. 6,547 g NaCl 99,5% b. 2,268 g NaHCO3 99,5 %
c. 0,373 g KCl 99,0 %
d. 0,178 g Na2HPO4.2H2O 99,5 %
e. 0,305 g MgCl2.6H2O 98 %
f. 0,368 g CaCl2.2H2O 99 %
g. 0,071 g Na2SO4
h. 6,057 g (CH2OH)3CNH2 99,2 %
i. 40 g HCl 1 Molar 4. Air 1 l
Alat yang digunakan dalam penelitian ini adalah :
1. Water bath 2. Ball mill 3. Vibroseive 4. Saringan analitik 5. Buret
6. Beaker glass 7. Labu reaksi 8. Termometer 9. Magnetik stirer 10. Hotplate 11. Neraca analitik 12. pH multimeter 13. Pompa vakum 14. Corong keramik 15. Kertas saring 16. Cawan keramik 17. Statip
18. Pengaduk 19. Spatula 20. Pipet
21. Lumpang dan alu 22. Sikat
23. Freezer
24. Freeze Drier
25. Pompa vakum
Metode Penelitian
Preparasi Sampel
Membuat larutan asam: 1. Senyawa H3PO4 44,43 g.
2. H2O 300 ml pada sebuah becker
glass 500 ml.
3. Dituangkan 44,43 g H3PO4 dalam
300 ml H2O.
Membuat suspensi dasar: 1. Senyawa Ca(OH)2 50 g.
2. H2O 500 ml pada sebuah becker
glass ukuran 1 l.
3. Dituangkan 50 g Ca(OH)2 dalam 500
ml H2O.
4. Lalu diaduk dan dipanaskan suspensi dasar dengan menggunakan magnetik stirrer pada 300 r/min.
5. Pemanasan dilakukan dengan variasi suhu 40, 70 dan 90oC secara terpisah untuk menghasilkan HAp dengan derajat kristalin rendah, sedang dan tinggi.
6. Setelah itu masukan larutan asam kedalam larutan kalsium hidroksida, tetes demi tetes dan memakan waktu sekitar 4-5 jam. Pada suhu 70°C dan 90°C terjadi penguapan yang mengakibatkan pH turun sampai kisaran 5-6 sehingga pengaturan kebasaan pada pH 9 dicapai dengan penambahan larutan ammonium hidroksida (NH4OH) 12%. Setelah
larutan asam habis, biarkan campuran tersebut selama 2 jam kemudian didiamkan selama 24 jam. 7. Saring dan cuci endapan yang
diperoleh dengan aquades sebanyak ± 2000 ml.
Dalam pembuatan hidroksiapatit digunakan dua macam pelarut yaitu air dan SBF. Pelarut SBF akan digunakan untuk menggantikan pelarut air.
Tabel 2 Senyawa pembuatan larutan SBF[2]
No Senyawa Massa
(g)
1 NaCl 99,5 % 6,547
2 NaHCO3 99,5 % 2,268
3 KCl 99,0 % 0,373
4 Na2HPO4.2H2O 99,5 % 0,178
5 MgCl2.6H2O 98 % 0,305
6 CaCl2.2H2O 99 % 0,368
7 Na2SO4 0,071
8 (CH2OH)3CNH2 99,2 % 6,057
9 HCl 1 Molar 40
Preparasi pelarut SBF 1 liter.
Pertama-tama siapkan 960 ml air lalu tuangkan air 200 ml untuk di sterrier pada suhu 35oC setelah itu masukan urutan pencampuran :
1. 6,547 g NaCl 99,5% 2. 2,268 g NaHCO3 99,5 %
3. 0,373 g KCl 99,0 %
5. 0,305 g MgCl2.6H2O 98 %
6. 15 g HCl 1 Molar
7. 0,368 g CaCl2.2H2O 99 %
8. 0,071 g Na2SO4
9. 6,057 g (CH2OH)3CNH2 99,2 %
10. 25 g HCl 1 Molar
Dalam pencampuran diberi selang 2 menit setiap tahapnya dengan tujuan agar dapat larut secara merata dan pemasukan HCl dengan 2 tetes per detik.
Setelah membuat SBF, maka SBF tersebut digunakan sebagai pelarut dalam preparasi sampel pengganti air.
Pengeringan
Endapan yang diperoleh dari proses diatas diuapkan kandungan airnya menggunakan teknik vakum yaitu dengan metode freeze drying. Proses freeze drying
sebagai berikut :
1. Endapan dibekukan (prefreezing) pada suhu -80oC selama 24 jam lalu ditahan selama 1 jam.
2. Endapan dikeringkan (primary drying) pada suhu -40oC selama 72 jam dalam keadaan vakum menggunakan pompa vakum.
3. Dihaluskan dengan menggunakan lumpang dan dimasukan ke ball mill
selama 15 menit.
4. Diayak menggunakan saringan dengan urutan:
a. 250 µm (60 mesh). b. 180 µm (80 mesh). c. 90 µm (170 mesh). Karakterisasi dengan XRD
Alat XRD yang digunakan Shimadzu XRD 610.
Preparasi sample XRD:
1. Disiapkan sampel yang sudah dikeringkan dan diayak ± 2 gram. 2. Kemudian sampel dimasukan
kedalam holder yang berukuran 2 x 2 cm2.
3. Holder berisi sampel dikait pada diffraktometer.
4. Pada komputer di set nama sampel, sudut awal, sudut akhir, dan kecepatan analisa. Sudut awal pada 10o dan sudut akhir pada 70o kecepatan baca di set 2o per menit 5. Setelah itu di run
Karakterisasi dengan FTIR
Alat FTIR yang digunakan Jasco FTIR-410.
Preparasi sampel :
1. Dua miligram sampel dicampur dengan 20 mg KBr
2. Kemudian dibuat pelet lalu di cek dengan jangkauan bilangan gelombang 4000-400 cm-1. Untuk menghilangkan absorpsi latar belakang, pelet KBr selalu disertakan pada setiap pengukuran.
Karakterisasi dengan SEM
Alat SEM yang digunakan SEM JEOL Preparasi sampel SEM:
1. Sampel diletakan pada plat aluminium yang memiliki dua sisi. 2. Kemudian dilapisi dengan lapisan
emas setebal 48 nm.
3. Sampel yang telah dilapisi diamati menggunakan SEM dengan tegangan 22 kV dan perbesaran 40.000 kali. Karakterisasi dengan AAS dan Spektroskopi UV-Vis
Alat AAS yang digunakan Varin Spectra A30 dan untuk spektroskopi UV-Vis Shimadzu UV-VIS 1700.
Preparasi sampel AAS:
1. Sampel HA ditimbang sebanyak 0,5 gram.
2. Lalu ditambah 5 ml asam nitrat pekat (H2NO3).
3. Sampel didestruksi pada suhu 100oC selama 1 jam. Setelah itu diangkat dan dinginkan.
4. Masukan larutan tersebut ke labu ukur 100 ml dan dibilas dengan air suling.
5. Saring dengan kertas whatman 40. 6. Siap diukur dengan AAS
Preparasi sampel UV-Vis:
1. Pipet sebanyak 50 ml masing-masing standar P, masukan kedalam erlenmeyer 125 ml dan 50 ml larutan HA.
2. Tambahkan 2 ml pereaksi amonium molybdat dan 0.25 ml stanous klorida, aduk dan diamkan selama 10 menit.
Pengeringan dengan Freeze drier
Penyaringan
Penggerusan dan Pengayakan Pengadukan Suhu: 40, 70, 90oC
Waktu: 4-5 jam Ca(OH)2
+ Air atau SBF
H3PO4
+ Air atau SBF Penelusuran literatur dan
penyusunan proposal
Penyusunan laporan Karakterisasi dengan XRD, FTIR, SEM, AAS, dan UV-Vis
Pengolahan dan analisis data
HASIL DAN PEMBAHASAN
Sintesa Hidroksiapatit
Telah dibuat hidroksiapatit dengan pelarut SBF dan air dengan variasi suhu pembuatan pada 40, 70, dan 90oC.
Saat pembuatan hidroksiapatit kondisi pH dipertahankan 9. Untuk pembuatan pada suhu 40 dan 70oC tidak terjadi penurunan pH (stabil). Namun untuk suhu 90oC terjadi penurunan pH secara signifikan mencapai nilai pH 5-6, kondisi ini akibat penguapan air yang sangat tinggi. Ini dapat diatasi dengan menambahkan larutan amonium hidroksida (NH4OH) 12% sampai pH mencapai 9.
Endapan yang dihasilkan lalu dikeringkan dengan menggunakan freeze drier.
Analisa Derajat Kristalinitas dengan XRD
Kristalinitas didefinisikan sebagai fraksi berat kristalinitas dalam suatu bahan. Semakin teratur susunan atom dalam bahan, semakin tinggi tingkat kristalinitasnya.
Jika dilihat pada pola XRD HAp pelarut air (Gambar 7), terlihat bahwa dengan semakin naik suhu pembuatan, maka semakin naik juga derajat kristalinitasnya. Ini diperlihatkan pada semakin tingginya intensitas dan semakin sempitnya lebar setengah puncak (FWHM) pada 2θ 31,7o (40oC) dan 31,9o (70o dan 90oC).
Pada Gambar 8, terlihat terjadi perbedaan pola difraksi pada suhu 70oC. Kondisi demikian diakibatkan adanya preferred orientation yaitu orientasi bias dari satu atau lebih permukaan kristal partikel sehingga intensitasnya berubah-ubah. Perubahan intensitas untuk kristal diimbangi dengan perubahan intensitas amorf, sehingga tidak berpengaruh pada perhitungan derajat kristalinitas. Untuk nilai FWHM semakin mengecil dengan semakin naiknya suhu pembuatan pada 2θ 31,9o (40oC) dan 31,8o (70o dan 90oC).
Pada pola XRD dapat dilihat terbentuknya kristal pada sudut 2θ antara 31o sampai 34o, pola ini sesuai dengan data (JCPDS) Joint Committee on Powder Diffraction Standards (Gambar 9). Data XRD bertujuan untuk mencari derajat kristalinitas akibat pengaruh variasi suhu saat pembuatan.
XRD HAp Air
0 800
10 20 30 40 50 60 70
2θ In te n s it y
40 Air 70 Air 90 Air
Gambar 7 Pola XRD HAp pelarut air
XRD HAp SBF
0 1000
10 20 30 40 50 60 70
2θ In te n s it y
40 SBF 70 SBF 90 SBF
Gambar 8 Pola XRD HAp pelarut SBF
Gambar 9 Pola XRD JCPDS HAp
Derajat kristalinitas dihitung dengan membandingkan fraksi luas kristalin dengan penjumlahan fraksi luas kristalin dan fraksi luas amorf. Data yang diambil dalam perhitungan tidak semuanya, karena pembentukan kristal HAp paling dominan hanya terjadi pada jangkauan 2θ 31o sampai 34o pada hkl (211), (300), dan (202).
dapat dilihat pada Tabel 3 dan Tabel 5. Luas kristalin dan luas amorf dimasukan kedalam persamaan sehingga dihasilkan nilai % kristalinitas pada Tabel 4 dan Tabel 6. Data Tabel 4 dan Tabel 6 diplot pada grafik Gambar 12.
Gambar 10 Penghilangan background XRD
Gambar 11 Penghilangan amorf XRD
Tabel 3 Data XRD untuk kristalinitas HAp pelarut air
Suhu 2θ d (Å) Height Area FWHM Luas
40o
C 31,7 2,8 134,9 3649,5 1,6 211,1
33,8 2,6 51,3 5549,9 0,9 44,8
Kristal Σ 9199,4 255,9
32,2 2,8 33 2162,7 3,3 109,5
Amorf Σ 2162,7 109,5
70o
C 31,9 2,8 203,4 3353,5 0,9 180,9 33,0 2,7 120,3 5470,8 1,8 219,1
34,1 2,6 64,5 3209,8 0,7 46,6
Kristal Σ 12034,1 446,6
32,5 2,8 31,0 1909,3 2,8 88,2
Amorf Σ 1909,3 88,2
90o
C 31,9 2,8 231,4 3383,3 0,8 182,4 33,0 2,7 147,8 5807,7 1,7 257,2
34,1 2,6 70,8 793,8 0,6 44,1
Kristal Σ 9984,8 483,6
32,5 2,8 32,1 1992,0 2,9 92,2
Amorf Σ 1992,0 92,2
Tabel 4 Persentase Kristalinitas HAp pelarut air
Suhu % Kristalinitas
40 70.0
70 83.5
90 84.0
Tabel 5 Data XRD untuk kristalinitas HAp pelarut SBF
Suhu 2θ d (Å) Height Area FWHM Luas
40o
C 31,9 2,8 403,5 11315,8 1,6 660,2
34,1 2,6 135,3 16238,5 0,7 97,5
Kristal Σ 27554,3 757,8
32,3 2,8 107,1 6908,0 3,3 351,5
Amorf Σ 6908,0 351,5
70o
C 31,8 2,8 78,8 2473,7 1,5 121,9
32,8 2,7 98,3 2321,0 1,4 141,7
34,0 2,6 157,5 781,6 0,3 45,1
Kristal Σ 5576,3 308,6
31,0 2,9 15,1 1684,0 4,9 74,4
Amorf Σ 1684,0 74,4
90o
C 31,8 2,8 219,1 2834,8 0,8 169,9 32,9 2,7 131,4 5459,3 1,8 237,0
34,1 2,6 67,4 606,6 0,3 36,9
Kristal Σ 8900,7 443,9
32,2 2,8 22,0 1396,0 2,7 59,6
Amorf Σ 1396,0 59,6
Tabel 6 Persentase kristalinitas HAp pelarut SBF
Suhu % Kristalinitas
40 68.3
70 80.6
90 88.2
Kristalinitas Air dan SBF
60 65 70 75 80 85 90
30 40 50 60 70 80 90
Suhu Pembuatan (oC)
% K ris ta li n ita s Air SBF
Gambar 12 Persentase kristalinitas HA pelarut air dan SBF
Perhitungan kristalinitas :
(Fraksi luas kristalin) Kristalinitas =
(Fraksi luas kristalin + fraksi luas amorf)
Fraksi luas kristalin/amorf : FWHM x height
Dari hasil grafik dapat dilihat bahwa kurva derajat kristalinitas HAp dengan pelarut SBF berbentuk linear, persentase kristalinitas meningkat sebanding dengan kenaikan suhu pada saat pembuatan. Untuk kurva derajat kristalinitas HAp pelarut air tidak linear, terdapat lengkung mulai suhu 70 sampai 90
o
hilang sehingga tidak ada lagi pembentukan kristal. Dapat disimpulkan pada grafik memperlihatkan dengan semakin tinggi suhu pembuatan maka semakin banyak kristal yang terbentuk karena susunan atom dalam bahan semakin teratur.
Identifikasi Gugus Anion PO43-, CO32-dan
H2O dengan FTIR
Dari spektra FTIR HAp pelarut air (berasal dari kalsium hidroksida Ca(OH)2
dengan asam fosfat H3PO4) seperti pada
Gambar 13 menunjukan bahwa HAp pelarut air memiliki:
¾ Pita serapan fosfat PO43- pada
bilangan gelombang 586 cm-1, 1038 cm-1, 1045 cm-1, dan 1057 cm-1. ¾ Pita serapan substitusi CO32– pada
bilangan gelombang 870 cm-1, 874 cm-1, 1435 cm-1, dan 1441 cm-1. ¾ Pita serapan H2O pada bilangan
gelombang 1639 cm-1, 1641 cm-1, 1643 cm-1, 3423 cm-1, 3427 cm-1, dan 3431 cm-1.
Gugus PO43- vibrasi asimetri stretching
(v3) pada bilangan gelombang 1038 cm-1, 1045 cm-1, dan 1057 cm-1. Vibrasi asimetri
bending (v4) pada bilangan gelombang 586 cm-1, untuk vibrasi simetri stretching (v1) dan vibrasi simetri bending (v2) tidak terdeteksi bilangan gelombangnya. Terlihat pada suhu 40, 70, dan 90oC dengan pita serapan 1038 cm-1, 1045 cm-1, dan 1057 cm-1 gugus PO4
3-memperlihatkan bentuk pita tidak simetris, ini menunjukan kristal yang terbentuk. Dengan semakin naiknya suhu pembuatan pita serapan gugus PO43- semakin tidak simetri, sehingga
menunjukan kristal yang terbentuk semakin banyak. Pita serapan 586 cm-1 terdapat belahan kecil dan tidak simetri yang menandakan terjadi kristalisasi dalam jumlah sedikit.
Pita serapan v2 karbonat pada bilangan gelombang 870 cm-1 dan 874 cm-1 tidak mengalami perubahan bentuk dan pita serapan
v3 karbonat pada bilangan gelombang 1435 cm-1 dan dan 1441 cm-1 yang merupakan pita serapan vibrasi stretching asimetri lemah. Pita serapan untuk gugus karbonat memperlihatkan tidak simetri yang menunjukan terbentuknya kristal terutama untuk bilangan gelombang 1435 cm-1 dan 1441 cm-1.
Spektra FTIR HAp pelarut air menunjukan pita serapan H2O pada bilangan
gelombang 1639 cm-1, 1641 cm-1, dan 1643 cm-1 menunjukan deformasi (perubahan bentuk) senyawa H2O, sedangkan 3423 cm-1,
3427 cm-1, dan 3431 cm-1 menunjukan kondisi H2O terikat dalam HA.
Spektra FTIR HAp pelarut SBF seperti pada Gambar 14 menunjukan bahwa HAp pelarut SBF memiliki :
¾
Pita serapan fosfat PO43- padabilangan gelombang 582 cm-1, 584 cm-1, 586 cm-1, 1043 cm-1, 1051 cm-1, dan 1059 cm-1.
¾
Pita serapan substitusi CO32– padabilangan gelombang 868 cm-1, 880 cm-1, 881 cm-1, 1429 cm-1, 1441 cm
-1
, dan 1446 cm-1.
¾
Pita serapan H2O pada bilangangelombang 1639 cm-1, 1641 cm-1, 3411 cm-1, 3427 cm-1, 3437 cm-1, dan 3645 cm-1.
Gugus fosfat yang dimiliki hanya mode vibrasi asimetri stretching (v3) dan asimetri bending (v4) pada bilangan gelombang 1043 cm-1, 1051 cm-1, dan 1059 cm-1 untuk v3, mode v4 untuk 582 cm-1 dan 584 cm-1. Mode vibrasi simetri stretching (v1) dan vibrasi simetri bending (v2) tidak terdeteksi bilangan gelombangnya. Terlihat pada suhu 40, 70, dan 90oC dengan pita serapan 1043 cm-1, 1051 cm
-1
, dan 1059 cm-1 bentuk pita serapan yang tidak simetris menunjukan terbentuknya kristal. Pita serapan 582 cm-1, 584 cm-1, dan 586 cm-1 terlihat adanya belahan sedikit dan tidak simetris menunjukan terjadi kristalinitas dalam jumlah sedikit.
Pada gugus karbonat (CO32–) terlihat pita
serapan bilangan gelombang 880 cm-1, 881 cm-1 merupakan mode v2 dan mode v3 1441 cm-1, 1446 cm-1 merupakan pita serapan vibrasi stretching asimetri lemah. Pita serapan gugus karbonat terlihat jelas bentuk tidak simetri pada 1429 cm-1, 1441 cm-1, 1446 cm-1, dan tidak terlihat jelas pada 868 cm-1, 880 cm
-1
, 881 cm-1 yang menunjukan terbentuknya kristal. HAp yang menggunakan pelarut SBF terlihat persentase transmitansinya lebih rendah dibandingkan HAp dengan pelarut air, ini menunjukan konsentrasi karbonat yang terkandung dalam HAp pelarut SBF lebih besar dibandingkan HA pelarut air.
Spektra FTIR HAp pelarut SBF memiliki pita serapan H2O pada bilangan gelombang
1639 cm-1, 1641 cm-1 menunjukan deformasi (perubahan bentuk) senyawa H2O; 3411 cm-1,
3427 cm-1, 3437 cm-1 menunjukan kondisi H2O terikat dalam HA, sedangkan 3645 cm-1
menunjukan H2O yang bebas tidak terikat
bebas. Secara keseluruhan HAp pelarut air dan SBF persentase transmitansinya cukup rendah yang memperlihatkan kandungan H2O
cukup banyak, ini akibat faktor pengeringan pada suhu rendah.
FTIR HAp Air Gabungan
0 30
400 800
1200 1600
2000 2400
2800 3200
3600 4000
Bilangan gelombang (cm-1)
%
T
ran
sm
it
an
si
40 Air
70 Air
90 Air
Gambar 13 Pola FTIR HAp pelarut air
FTIR HAp SBF Gabungan
0 30
400 800
1200 1600
2000 2400
2800 3200
3600 4000
Bilangan gelombang (cm-1)
%
T
ran
sm
it
an
si
40 SBF
70 SBF
90 SBF
Morfologi Hidroksiapatit dengan SEM
Hasil analisa SEM untuk melihat morfologi hidroksiapatit pelarut air dan SBF dapat dilihat pada Gambar 15.
Pada HAp pelarut air, serbuknya terlihat gumpalan, akan tetapi dengan semakin naiknya suhu pembuatan, luas permukaan butir mengecil sehingga gumpalan yang terbentuk semakin kecil, ini menunjukan pembentukan kristal semakin meningkat. Dapat dilihat pada Gambar 15.a-15.c.
HAp dengan pelarut SBF serbuknya membentuk serpihan memanjang dan runcing (tidak terjadi penggumpalan) sangat terlihat jelas dengan semakin naiknya suhu pembuatan, ini menunjukan pembentukan kristal semakin meningkat. Bentuk serpihan memanjang dan runcing akibat pengaruh ion-ion yang terkandung dalam SBF. Dapat dilihat pada Gambar 15.d-15.f.
Ukuran gumpalan serbuk HAp pelarut air suhu 40oC (±500 nm), 70oC (±300 nm), dan 90oC (±200 nm). Untuk serbuk HAp pelarut SBF suhu 40oC (±650 nm), 70oC (±450 nm), dan 90oC (±150 nm).
Identifikasi Unsur Kation Ca, Mg, Na, K, dan P denganAAS dan Spektroskopi UV-Vis
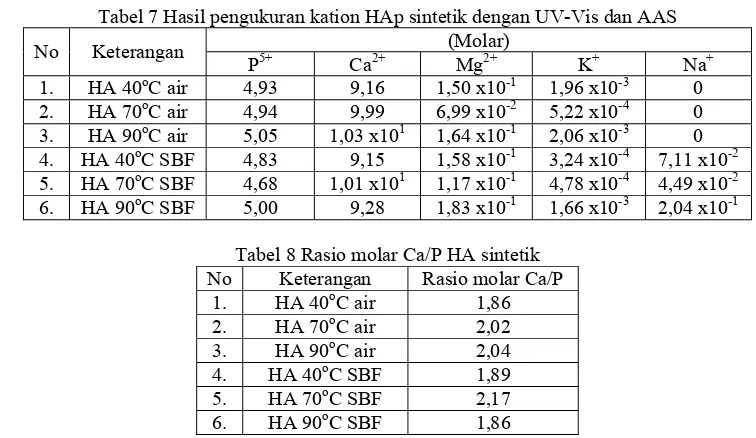
Kation-kation yang terdapat dalam HAp sintetik seperti Na+, K+, Mg2+, Ca2+ dan P5+ diidentifikasi menggunakan AAS. Data hasil pengukuran dengan AAS ditunjukkan pada Tabel 8.
HAp dengan pelarut air untuk ion Na+ tidak terdeteksi karena kandungannya yang sangat sedikit sekali. Sedangkan HAp dengan pelarut SBF memiliki kandungan ion Na+ yang dihasilkan dari senyawa penyusun SBF. Kondisi ion Mg+2 kandungannya lebih besar pada HAp dengan pelarut SBF karena terdapat tambahan konsentrasi dari senyawa penyusun SBF.
Nilai rasio molar perbandingan Ca/P dari HAp dengan pelarut air dan SBF mengalami kenaikan dan penurunan. Hal ini dipengaruhi oleh perubahan konsentrasi kandungan ion-ion P5+, Mg2+, K+, dan Na+ selama proses pembuatan. Kemungkinan pertama karena ada ion kalsium tidak habis bereaksi dengan ion fosfat sehingga pada akhir reaksi membentuk CaO seperti ditunjukan hasil XRD pada 2θ 37o sampai 38o. Kemungkinan kedua adanya konsentrasi ion Mg2+ yang mengalami perubahan akibat substitusi dengan sebagian ion Ca2+.
Gambar 15 Morfologi HAp sintetik dengan perbesaran 40.000 kali (a). HAp 40oC air, (b). HAp 70oC air, (d). HAp 40oC SBF, (e). HAp 70oC SBF
a
d
c
f
Gambar 16 Morfologi HAp sintetik dengan perbesaran 40.000 kali (c). HAp 90oC air, (f). HAp 90oC SBF.
Tabel 7 Hasil pengukuran kation HAp sintetik dengan UV-Vis dan AAS (Molar)
No Keterangan
P5+ Ca2+ Mg2+ K+ Na+
1. HA 40oC air 4,93 9,16 1,50 x10-1 1,96 x10-3 0 2. HA 70oC air 4,94 9,99 6,99 x10-2 5,22 x10-4 0 3. HA 90oC air 5,05 1,03 x101 1,64 x10-1 2,06 x10-3 0 4. HA 40oC SBF 4,83 9,15 1,58 x10-1 3,24 x10-4 7,11 x10-2 5. HA 70oC SBF 4,68 1,01 x101 1,17 x10-1 4,78 x10-4 4,49 x10-2 6. HA 90oC SBF 5,00 9,28 1,83 x10-1 1,66 x10-3 2,04 x10-1
Tabel 8 Rasio molar Ca/P HA sintetik No Keterangan Rasio molar Ca/P
1. HA 40oC air 1,86 2. HA 70oC air 2,02 3. HA 90oC air 2,04 4. HA 40oC SBF 1,89 5. HA 70oC SBF 2,17 6. HA 90oC SBF 1,86
SIMPULAN DAN SARAN
Simpulan
Berdasarkan hasil XRD, didapatkan hasil bahwa semakin bertambahnya suhu reaksi pada saat pembuatan hidroksiapatit maka derajat kristalinitasnya semakin meningkat.
Pola pita serapan FTIR yang tidak simetri menunjukan adanya kristal yang terbentuk. Untuk HAp pelarut SBF diperlihatkan gugus CO32- dengan pita serapan lebih tajam
dibandingkan HAp pelarut air.
Hasil SEM memperlihatkan morfologi HAp pelarut air yang berbentuk gumpalan bulat, sedangkan HAp pelarut SBF membentuk serpihan memanjang.
Nilai rasio molar perbandingan Ca/P untuk HAp pelarut SBF dipengaruhi ion Mg2+. Semakin tinggi konsentrasi ion Mg2+ yang terkandung dalam hidroksiapatit maka nilai perbandingan Ca/P semakin turun akibat substitusi ion Mg2+ dengan ion Ca2+.
Saran
Bagi yang akan melanjutkan penelitian ini, untuk pembuatan HAp sintetik pada suhu tinggi agar memperhatikan perubahan pH yang terjadi setiap saat. Pengeringan menggunakan freeze drier disarankan untuk memvariasikan suhu pengeringan ,diusahakan dibawah suhu -40oC.
DAFTAR PUSTAKA
[1] Aoki, H. 1991. Science and Medical Application of Hydroxyapatite. JAAS. Tokyo.
[2] Ratih, Ngatijo, Widjaksana, Latief A, Bambang. 2003. Aplikasi Hidroksiapatit Di Bidang Medis. Yogyakarta: Proc. [3] Elliott, J.C. 1973. The Problem of
[4] Tampieri, A., Etc. 2002. Towards Tissue Bio-Engineering: Vietnam-Italy Seminar on Technology and Application of Advanced Ceramics. Hanoi: Proc.
[5] Kalpana, S., Turlapati, P. 2002. Control of Polymer-Mineral Interfacial Behavior in Poly(Acrylic Acid)-Hydroxyapatite Nanocomposites for Bone Replacement.
North Dakoda State University. Dept of Civil Engineering.
[6] Elena, Anna, Giancarlo, Ratih, Monica, Simone. 2005. Nucleation of Biomimetic Apatite In Synthetic Body Fluid : Dense and porous Scaffold Development. J Biomaterial 26 2835-2845.
[7] Bigi, A., E. Foresti, R. Gregorini, A. Ripamonti, N. Noveri, and J. S. Shah. 1992. The Role of Magnesium on the Structure of Biological Apatites, Calc. Tiss. Int. 50:439-444.
[8] Emitech. 2005. Technical Brief of Freeze drying for Emitech K750X & K775X.
England. Emitech Corp
http://www.emitech.co.uk
[23 April 2005].
[9] Labconco. 1998. A Guide To Freeze drying for the Laboratory. U.S.A. Labconco Corp http://www.labconco.com [22 Februari 2005].
[10] Soejoko, D. S., and Sri Wahyuni. 2002.
Spektroskopi Inframerah Senyawa Kalsium Fosfat Hasil Preipitasi, Makara seri Sains, Vol. 6 No. 3, 117-120.
[11] Avès, P., Sierra, G., Sànchez, L. 2003. A Scanning Electron Microscopy (SEM) Study of The Hydroxyapatite Sol-Gel Coating Over MA956 Alloy. J Biomaterials Center. Havana University. [12] Bayraktar. 2000. Biomimetic Preparation
of HA Powder at 37oC in Urea and Enzyme Urease Containing Synthetic Body Fluid. Turkey. J Medical Science. [13] Cullity, B D., Stock S R. 2001. Element
of X-Ray Diffraction 3rd Ed. U.S.A. Prentice Hall.
[14] Hidayat, Y. 2005. Pengaruh Ion Karbonat, Magnesium, dan Fluor Dalam Presipitasi Senyawa Kalsium Fosfat: Karakterisasi Dengan Menggunakan Atomic Absorption Spectroscopy (AAS), Spektroskopi UV-VIS, Dan Fourier Transform Infrared (FTIR)
[15] Jennifer, Nelesh, William, Christine. 2004. Nanoscale Morphology of Apatite Precipitate Onto Synthetic Hydroxyapatite From Simulated Body Fluid. J Biomaterial.
[16] Markovic, M., Fowler, B., Tung, M. 2004. Preparation and Comprehensive Characterization of a Calcium Hydroxyapatite Reference Material.
U.S.A. J of Research of the National Institute of Standards and Technology Vol 109 Number 6 p 553-568.
[17] Maria, Marise, Luciana, Herman, Wander. 2004. Synthesis Control and Characterization of Hydroxyapatite Prepared by Wet Precipitation Process. J Material Research, Vol. 7, No. 4, Hal 625-630.
[18] Notonegoro H A. 2003. Analisis Hasil Spektroskopi Inframerah dan Difraksi Sinar X Pertumbuhan Kristal Apatit pada Mukoza Ampela Ayam, Skripsi S1 Jurusan Fisika FMIPA UI (Pembimbing D. S. Soejoko), Depok.
[19] Sastrohamidjojo H. 1992. Spektroskopi Inframerah. Liberty. Yogyakarta.
[20] Norman B. Colthup, Lawrence H. Daly, Stephen E. Wiberley. 1975. Introduction to Infrared and Raman Spectroscopy. Academic Press. United Kingdom.
[21] __.2005. Introduction to X-ray Diffraction. Materials Research Laboratory. University of California
http://www.mrl.ucsb.edu/mrl/index.html
[25 Februari 2005]
[22] __. 2002. Scanning Electron Microscope.
Oxford Univ.
Lampiran 1 Pola XRD serta hkl HAp pelarut air dan SBF dengan variasi suhu pembuatan
HAp 40oC air
HAp 90oC air
HAp 70oC SBF
Lampiran 3 Spektrum IR HAp pelarut air dan SBF dengan variasi suhu pembuatan
FTIR 40 Air
58
6
87
4
10
45
143
5
16
41
342
3
0 1 2 3 4 5 6 7 8 9 10
400 800
1200 1600
2000 2400
2800 3200
3600 4000
Bilangan gelombang (cm-1)
%
T
ran
sm
it
a
n
si
FTIR 70 Air
586
874
1038
14
35
1
643
3427
0 1 2 3 4 5 6 7 8 9 10
400 800
1200 1600
2000 2400
2800 3200
3600 4000
Bilangan gelombang (cm-1)
%
T
ra
n
sm
it
an
FTIR 90 Air
586
870
1
057
144
1
16
39
3431
0 1 2 3 4 5 6 7 8 9 10
400 800
1200 1600
2000 2400
2800 3200
3600 4000
Bilangan gelombang (cm-1)
%
T
ran
sm
it
an
si
FTIR 40 SBF
58
4
86
8
10
43
14
29
16
41
34
27
0 1 2 3 4 5 6 7 8 9 10
400 800
1200 1600
2000 2400
2800 3200
3600 4000
Bilangan gelombang (cm-1)
%
T
ran
s
m
it
an
s
FTIR 70 SBF
34
11 1641
1446
1
051
88
1 58
2
3
645
0 1 2 3 4 5 6 7 8 9 10
400 800
1200 1600
2000 2400
2800 3200
3600 4000
Bilangan gelombang (cm-1)
%
T
ran
sm
it
an
si
FTIR 90 SBF
586
880
105
9
1
441
1639
3
437
0 1 2 3 4 5 6 7 8 9 10
400 800
1200 1600
2000 2400
2800 3200
3600 4000
Bilangan gelombang (cm-1)
%
T
ra
n
sm
it
an
FTIR HAp Air Gabungan
400 800
1200 1600
2000 2400
2800 3200
3600 4000
Bilangan gelombang (cm-1)
%
T
ran
sm
it
an
si
0 30
40 Air
70 Air
90 Air
FTIR HAp SBF Gabungan
0 30
400 800
1200 1600
2000 2400
2800 3200
3600 4000
Bilangan gelombang (cm-1)
%
T
ran
sm
it
an
si
Lampiran 4 Morfologi HAp pelarut air dan SBF dengan variasi suhu pembuatan
HAp 40oC air
HAp 70oC air
HAp 40oC SBF
HAp 70oC SBF
![Tabel 2 Senyawa pembuatan larutan SBF[2]](https://thumb-ap.123doks.com/thumbv2/123dok/475559.328522/15.595.326.509.468.628/tabel-senyawa-pembuatan-larutan-sbf.webp)