38
LAMPIRAN 1
DATA BAHAN BAKU
L1.1 KOMPOSISI ASAM LEMAK BAHAN BAKU RBDPO HASIL ANALISA GCMS
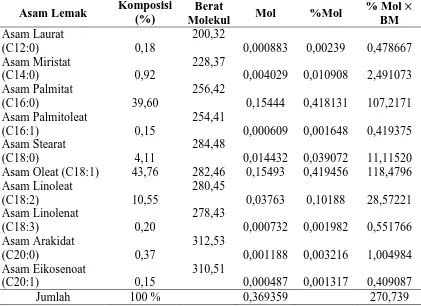
Tabel L1.1 Komposisi Asam Lemak RBDPO
Asam Lemak Komposisi (%)
Berat
Molekul Mol %Mol
% Mol × BM Asam Laurat
(C12:0) 0,18
200,32
0,000883 0,00239 0,478667 Asam Miristat
(C14:0) 0,92
228,37
0,004029 0,010908 2,491073 Asam Palmitat
(C16:0) 39,60
256,42
0,15444 0,418131 107,2171 Asam Palmitoleat
(C16:1) 0,15
254,41
0,000609 0,001648 0,419375 Asam Stearat
(C18:0) 4,11
284,48
0,014432 0,039072 11,11520 Asam Oleat (C18:1) 43,76 282,46 0,15493 0,419456 118,4796 Asam Linoleat
(C18:2) 10,55
280,45
0,03763 0,10188 28,57221 Asam Linolenat
(C18:3) 0,20
278,43
0,000732 0,001982 0,551766 Asam Arakidat
(C20:0) 0,37
312,53
0,001188 0,003216 1,004984 Asam Eikosenoat
(C20:1) 0,15
310,51
0,000487 0,001317 0,409087
Jumlah 100 % 0,369359 270,739
Dari perhitungan, maka diperoleh berat molekul rata-rata FFA RBDPO sebesar 270,739 g/mol
39
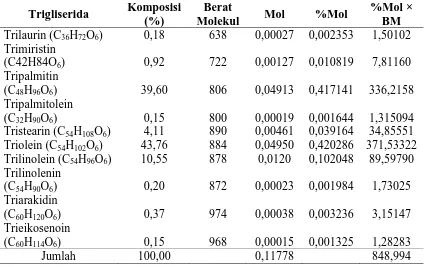
L1.2 KOMPOSISI TRIGLISERIDA BAHAN BAKU RBDPO Tabel L1.2 Komposisi Trigliserida RBDPO Trigliserida Komposisi
(%)
Berat
Molekul Mol %Mol
%Mol × BM Trilaurin (C36H72O6) 0,18 638 0,00027 0,002353 1,50102
Trimiristin
(C42H84O6) 0,92 722 0,00127 0,010819 7,81160
Tripalmitin
(C48H96O6) 39,60 806 0,04913 0,417141 336,2158
Tripalmitolein
(C32H90O6) 0,15 800 0,00019 0,001644 1,315094
Tristearin (C54H108O6) 4,11 890 0,00461 0,039164 34,85551
Triolein (C54H102O6) 43,76 884 0,04950 0,420286 371,53322
Trilinolein (C54H96O6) 10,55 878 0,0120 0,102048 89,59790
Trilinolenin
(C54H90O6) 0,20 872 0,00023 0,001984 1,73025
Triarakidin
(C60H120O6) 0,37 974 0,00038 0,003236 3,15147
Trieikosenoin
(C60H114O6) 0,15 968 0,00015 0,001325 1,28283
Jumlah 100,00 0,11778 848,994
Dari perhitungan, maka diperoleh berat molekul rata-rata FFA RBDPO sebesar 848,994g/mol.
L1.3 KADAR FFA RBDPO
Kadar FFA =
10 × sampel berat BM × V × T = 10 × 65,24 270,739 × 11 × 0,25 = 1,141
40
LAMPIRAN 2
DATA HASIL PENELITIAN
L2.1 DATA HASIL ANALISIS DENSITAS BIODIESEL Tabel L2.1 Hasil Analisa Densitas Biodiesel Jumlah DES
(b/b)
Rasio Molar Reaktan
Suhu (0C)
Densitas Biodiesel (gr/ml)
ChCl : Glukosa (2:1) 1% 6 : 1 40 859,9290
ChCl : Etilen Glikol (1:2) 1% 6 : 1 40 858,1560
L2.2 DATA HASIL ANALISIS VISKOSITAS KINEMATIK BIODIESEL Tabel L2.2 Hasil Analisa Viskositas Biodiesel
Jumlah DES (b/b) Rasio Molar Reaktan Suhu (0C)
Waktu Alir (detik) trata-rata Biodiesel (detik) Viskositas Kinematik (cSt)
t1 t2 t3
ChCl :
Glukosa (2:1) 1%
6 : 1 40 1403 1389 1354 1382 4,679 ChCl : Etilen
Glikol (1:2) 1%
6 : 1 40 1198 1183 1189 1190 4,037
L2.3 DATA YIELD DAN KEMURNIAN METIL ESTER
Tabel L2.3 Hasil Analisa Yield dan Kemurnian Biodiesel
Jenis DES Jumlah DES (b/b) Kemurnian Yield (%)
Tanpa DES 0 % 98,1575 92,7916
ChCl : Glukosa (2:1)
1 % 97,7474 89,7973
5 % 91,1296 71,2025
10 % 77,0846 51,4925
15% 31,3670 19,1234
20% 19,4753 10,5426
ChCl : Etilen Glikol (1:2)
1 % 97,9361 91,3417
5 % 95,0412 86,6459
10 % 94,5140 85,1886
15% 93,4707 83,4381
20% 92,3292 80,7880
41
LAMPIRAN 3
CONTOH PERHITUNGAN
L3.1 PERHITUNGAN KADAR FFA RBDPO
Kadar FFA =
10 × sampel berat BM × V × T
Keterangan: T = Normalitas larutan NaOH V = Volume larutan NaOH terpakai
M = Berat molekul FFA (BM FFA RBDPO = 270,739 g/mol)
Normalitas NaOH = 0,25 N
Volume larutan NaOH yang terpakai = 11 ml
BM FFA = 270,739 g/mol
Berat RBDPO = 7,05 g
Kadar FFA =
sampel massa × 10 M × V × T % = 7,05 × 10 270,015 × 11 × 25 , 0 % = 10,53 %
L3.2 PERHITUNGAN KEBUTUHAN METANOL Massa RBDPO = 20 g
Metanol : RBDPO = 6 : 1 (mol/mol) % katalis = 1 % (b/b) BM Trigliserida = 848,994 g/mol Mol RBDPO =
Trigliseri BM Massa = g/mol 848,994 g 20
= 0,02355 mol
BM Trigliserida
42 Mol RBDPO =
1 6
× 0,02355 = 0,14134 mol
Maka, massa metanol = mol metanol × BM Metanol = 0,14134 × 32
= 4,5230 g Volume metanol =
ρ m = g/ml 7918 , 0 g 4,5230
= 5,71 ml
Untuk kebutuhan metanol yang lainnya sama dengan perhitungan di atas.
L3.3 PERHITUNGAN DENSITAS BIODIESEL
Volume piknometer =
air densitas
air berat
= 5,64 ml
Densitas sampel =
piknometer volume
sampel berat
Berat piknometer kosong = 15,45 g = 0,01545 kg Berat piknometer + biodiesel = 20,28 g = 0,02028 kg Berat biodiesel = 4,83 g = 0,00483 kg
Densitas minyak biodiesel =
0,00000564 kg 0,00483
= 856,382 kg/m3 Untuk data yang lainnya sama dengan perhitungan di atas.
L3.4 PERHITUNGAN VISKOSITAS BIODIESEL
sg = air densitas sampel densitas Viskositas sampel = k ×sg ×t Dimana t = waktu alir
Kalibrasi air :
ρair (40 oC) = 992,925 kg/m3= 0,992925 g/m3
Viskositas air (40 oC) = 0,6321 × 10-3 kg/m.s
0,00000564 m3
43 tair = 188 detik
sgair= 1
Viskositas air = k × sg × t 0,6321 × 10-3 kg/m.s = k × 1 × 188 s
k = 3,3622 × 10-6 kg/m.s2
Viskositas Biodiesel t rata-rata biodiesel= 1273 detik
sg biodiesel = 3
3 kg/m 992,925 kg/m 856,382 = 0,862 Viskositas biodiesel = k × sg × t
= 3,3622 × 10-6 × 0,862 × 1273 = 0,00368 kg/m.s
Viskositas kinematik = 3
kg/m 382 , 856 kg/m.s 0,00308
= 4,308 × 10-6 m2/s = 4,308 mm2/s
= 4,308 cSt
Untuk data yang lainnya sama dengan perhitungan di atas.
L3.5 PERHITUNGAN YIELD METIL ESTER
Yield = 100%
baku bahan massa kemurnian praktik biodiesel × × massa
Yield = 100%
gr 30 98,1575 gr 36 , 28 × ×
Yield = 92,7916 %
Untuk data lainnya mengikuti contoh perhitungan di atas.
44
LAMPIRAN 4
DOKUMENTASI PENELITIAN
L4.1 BAHAN BAKU RBDPO
Gambar L4.1 Bahan Baku RBDPO
L4.2 PROSES TRANSESTERIFIKASI
Gambar L4.2 Proses Transesterifikasi
45 L4.3 FOTO PEMISAHAN METIL ESTER
Gambar L4.3 Foto Pemisahan Metil Ester
Gambar L4.3 Foto Pemisahan Metil Ester
L4.4 FOTO PRODUK AKHIR BIODIESEL
Gambar L4.4 Foto Produk Akhir Biodiesel
46 L4.5 FOTO ANALISIS DENSITAS
Gambar L4.5 Foto Analisis Densitas
L4.6 FOTO ANALISIS VISKOSITAS
Gambar L4.6 Foto Analisis Viskositas
47
LAMPIRAN 5
HASIL ANALISIS BAHAN BAKU RBDPO DAN
BIODIESEL
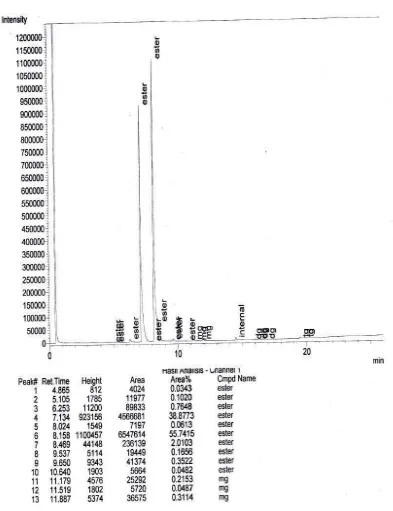
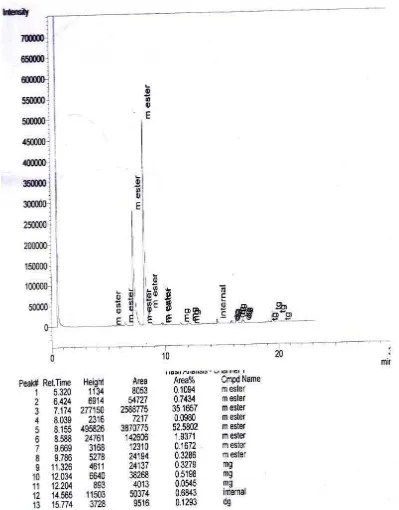
L5.1 HASIL ANALISIS KOMPOSISI ASAM LEMAK RBDPO
Gambar L5.1 Hasil Analisis Kromatogram GC-MS Asam Lemak RBDPO
Gambar L5.1 Hasil Analisis Kromatogram GC-MS Asam Lemak RBDPO
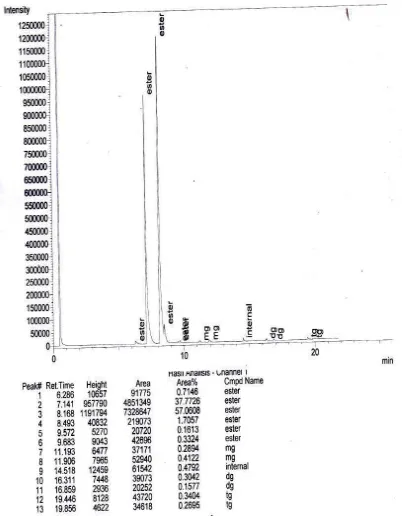
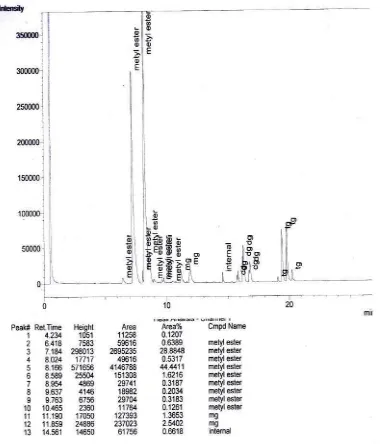
48 L5.2 HASIL ANALISIS BIODIESEL
Gambar L5.2 Hasil Analisis Kromatogram GC Biodiesel Run 1 (Tanpa Co-Solvent)
49
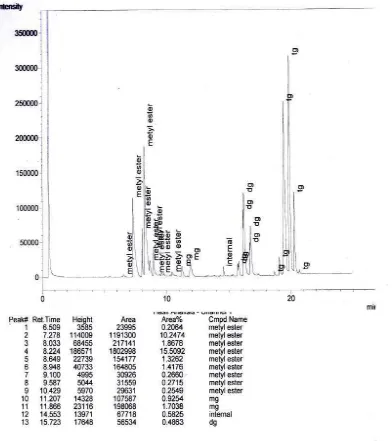
Gambar L5.3 Hasil Analisis Kromatogram GC Biodiesel Run 2 (Co-Solvent DES berbasis ChCl/D-Glukosa (2:1) = 1 %)
50
Gambar L5.4 Hasil Analisis Kromatogram GC Biodiesel Run 3 (Co-Solvent DES berbasis ChCl/D-Glukosa = 5 %)
51
Gambar L5.5 Hasil Analisis Kromatogram GC Biodiesel Run 4 (Co-Solvent DES berbasis ChCl/D-Glukosa (2:1) = 10 %)
52
Gambar L5.6 Hasil Analisis Kromatogram GC Biodiesel Run 5 (Co-Solvent DES berbasis ChCl/D-Glukosa (2:1) = 15 %)
53
Gambar L5.7 Hasil Analisis Kromatogram GC Biodiesel Run 6 (Co-Solvent DES berbasis ChCl/D-Glukosa (2:1) = 20 %)
54
Gambar L5.8 Hasil Analisis Kromatogram GC Biodiesel Run 7 (Co-Solvent DES berbasis ChCl/Etilen Glikol (1:2) = 1 %)
55
Gambar L5.9 Hasil Analisis Kromatogram GC Biodiesel Run 8 (Co-Solvent DES berbasis ChCl/Etilen Glikol (1:2) = 5 %)
56
Gambar L5.10 Hasil Analisis Kromatogram GC Biodiesel Run 9 (Co-Solvent DES berbasis ChCl/Etilen Glikol (1:2) = 10 %)
57
Gambar L5.11 Hasil Analisis Kromatogram GC Biodiesel Run 10 (Co-Solvent DES berbasis ChCl/Etilen Glikol (1:2) = 15 %)
58
Gambar L5.12 Hasil Analisis Kromatogram GC Biodiesel Run 11 (Co-Solvent DES berbasis ChCl/Etilen Glikol (1:2) = 20 %)
31
DAFTAR PUSTAKA
[1] Dai, Yuntao., Jaap Van Spronsen, Geert-Jan Witkamp, Robert Verpoorte, Young Hae Choi, Natural Deep Eutectic Solvents As New Potential Media For Green Technology, Analytica Chimica Acta (2012) 1-31
[2] Tang, Baokun., Kyung Ho Row, Recent Developments In Deep Eutectic Solvents In Chemical Sciences, Springer-Verlag Wien (2013) 402-751
[3] Yusof, Rizana., Emilia Abdulmalek, Kamaliah Sirat, Mohd Basyaruddin, Abdul Rahman, Tetrabutylammonium Bromide (TBABr)-Based Deep Eutectic Solvents (DESs) and Their Physical Properties, Molecules 2014, 19, 8011-8026
[4] Rafiee, Ezzat., Sara Eavani, A New Organic–Inorganic Hybrid Ionic Liquid Polyoxometalate For Biodiesel Production, Journal of Molecular Liquids 199 (2014) 96–101
[5] Hayyan, Adeeb., Mohd Ali Hashim, Maan Hayyan, Farouq S. Mjallic, Inas M. AlNashef, A New Processing Route For Cleaner Production Of Biodiesel Fuel Using A Choline Chloride Based Deep Eutectic Solvent, Journal of Cleaner Production 65 (2014) 246-251
[6] Shahbaz, K., F.S. Mjalli, M.A. Hashim, I.M. AlNashef, Eutectic Solvents For The Removal Of Residual Palm Oil-Based Biodiesel Catalyst, Separation and Purification Technology 81 (2011) 216–222
[7] Durand, E., J. Lecomte, P. Villeneuve, Deep Eutectic Solvents: Synthesis, Application, And Focus On Lipase-Catalyzed Reactions, Eur. J. Lipid Sci. Technol. 2013, 115, 379–385
32
[8] Shahbaz, K., Saeid Baroutian, Farouq Sabri Mjalli, Mohd Ali Hashim, Inas Muen AlNashef, Prediction Of Glycerol Removal From Biodiesel Using Ammonium And Phosphunium Based Deep Eutectic Solvents Using Artificial Intelligence Techniques, Chemometrics and Intelligent Laboratory Systems 118 (2012) 193–199
[9] Ru, Juanjian., Yixin Hua, Jian Li, Cunying Xu, Yan Li, DingWang, Cancan Qi, Yafei Jie, Effects Of Existence Formand Concentration Of Pbo On The Conductivity Of Choline Chloride–Urea Deep Eutectic Solvent, Journal of Molecular Liquids 199 (2014) 208–214
[10] Zhao, Hua., Cheng Zhang, Tanisha D. Crittle, Choline-Based Deep Eutectic Solvents For Enzymatic Preparation Of Biodiesel From Soybean Oil, Journal of Molecular Catalysis B: Enzymatic 85– 86 (2013) 243– 247
[11] Gu, Ling., Wei Huang, Shaokun Tang, Songjiang Tian, Xiangwen Zhang, A Novel Deep Eutectic Solvent For Biodiesel Preparation Using A Homogeneous Base Catalyst, Chemical Engineering Journal 259 (2015) 647–652
[12] Veljković,Vlada B., Olivera S.Stamenković, Marija B.Tasić, The Waste Water Treatment In The Biodiesel Production With Alkali-Catalyzed Transesterification, Renewable and Sustainable Energy Reviews 32 (2014) 40 – 60
[13] Guldhe, Abhishek., Bhaskar Singh, Taurai Mutanda, Kugen Permaul, Faizal Bux, Advances In Synthesis Of Biodiesel Via Enzyme Catalysis: Novel And Sustainable Approaches, Renewable and Sustainable Energy Reviews 41 (2015)1447–1464
[14] Shahbazi, Mohammad Reza., Behnam Khoshandam, Masoud Nasiri, Majeed Ghazvini, Biodiesel Production Via Alkali-Catalyzed
33
Transesterificationof Malaysian RBD Palm Oil – Characterization, Kinetics Model, Journal Of The Taiwan Institute Of Chemical Enggineers 43 (2012) 504-510
[15] Liu, Yu-Ting., Yan-An Chen, Yan-Jun Xing, Synthesis and Characterization Of Novel Ternary Deep Eutectic Solvents, Chinese Chemical Letters 25 (2014) 104–106
[16] Azizi, Najmedin., Sahar Dezfooli, Mohammad Mahmoudi Hashemi, Greener Synthesis Of Spirooxindole In Deep Eutectic Solvent, Journal of Molecular Liquids 194 (2014) 62–67
[17] Lin, Yuan-Chung., Po-Ming Yang, Shang-Cyuan Chen, Jia-Fang Lin, Improving Biodiesel Yields From Waste Cooking Oil Using Ionic Liquids As Catalysts With A Microwave Heating System, Fuel Processing Technology 115 (2013) 57–62
[18] Maugeri, Zaira., Pablo DomÍnguez de MarÍa, Whole-Cell Biocatalysis in Deep Eutectic-Solvents/Aqueous Mixtures, ChemCatChem (2014), 1–3
[19] Wan, Hui., Zuowang Wu, Wen Chen, Guofeng Guan, Yuan Cai, Chong Chen, Zhong Li, Xiaoqin Liu, Heterogenization of Ionic Liquid Based on Mesoporous Material Asmagnetically Recyclable Catalyst for Biodiesel Production, Journal of Molecular Catalysis A: Chemical 398 (2015) 127–132
[20] Durand, E., J. Lecomtea, B. Baréaa, G. Piomboa, E. Dubreucqb, P. Villeneuve, Evaluation of Deep Eutectic Solvents as New Media for Candida Antarctica B Lipase Catalyzed Reactions, Process Biochemistry 47 (2012) 2081–2089
34
[21] Shahbaz, K., F.S. Ghareh Bagh, F.S. Mjalli, I.M. AlNashef, M.A. Hashim, Prediction of refractive index and density of deep eutectic solventsusing atomic contributions, Fluid Phase Equilibria 354 (2013) 304– 311
[22] Harris, Robert Christopher., Physical Properties Of Alcohol Based Deep Eutectic Solvents, University Of Leicester 2008
[23] Lloyd, David., Tuomas Vainikka, Kyösti Kontturi, The Development Of An All Copper Hybrid Redox Flow Battery Usingdeep Eutectic Solvents, Electrochimica Acta 100 (2013) 18– 23
[24] Boisset, Aurélien., Johan Jacquemin, Mérièm Anouti, Physical Properties Of A New Deep Eutectic Solvent Based On Lithium Bis[(Trifluoromethyl)Sulfonyl]Imide And N-Methylacetamide As Superionic Suitable Electrolyte For Lithium Ion Batteries And Electric Double Layer Capacitors, Electrochimica Acta 102 (2013) 120– 126
[25] Maugeri, Zaira., Pablo DomÍnguez de MarÍa, Novel choline-chloride-based deep-eutectic-solvents with renewable hydrogen bond donors: levulinic acid and sugar-based polyols, The Royal Society of Chemistry 2 (2012), 421–425
[26] Taubert, Jenny., Srini Raghavan, Effect Of Composition Of Post Etch Residues (PER) On Their Removal In Choline Chloride–Malonic Acid Deep Eutectic Solvent (DES) System, Microelectronic Engineering 114 (2014) 141–147
[27] Hayyan, Adeeb, Mohd Ali Hashima, Maan Hayyana, Farouq S. Mjalli b, Inas M. AlNashef, A novel ammonium based eutectic solvent for the treatment of free fatty acid and synthesis of biodiesel fuel, Industrial Crops and Products 46 (2013) 392– 398
35
[28] Silitonga, A. S., H. H. Masjuki., T. M. I. Mahlia., H. C. Ong., W. T. Chong., M. H. Boosroh., Overview Properties Of Biodiesel Diesel Blends From Edible And Non-Edible Feedstock, Renewable and Sustainable Energy Reviews 22 (2013) 346–360
[29] Buasri, Achanai., Nattawut Chaiyut, Vorrada Loryuenyong, Chao Rodklum, Techit Chaikwan, Nanthakrit Kumphan, Continuous Process for Biodiesel Production in Packed Bed Reactor from Waste Frying Oil Using Potassium Hydroxide Supported on Jatropha curcas Fruit Shell as Solid Catalyst, Applied Sciences ISSN 2076-3417 (2012)
[30] Yaakob, Zahira., Masita Mohammada, Mohammad Alherbawi, Zahangir Alam, Kamaruzaman Sopian, Overview Of The Production Of Biodiesel From Waste Cooking Oil, Renewable and Sustainable Energy Reviews 18 (2013) 184–193
[31] Samart, Chanatip ., Chaiyan Chaiya ,Prasert Reubroycharoen, Biodiesel Production By Methanolysis Of Soybean Oil Using Calcium Supported On Mesoporous Silica Catalyst, Energy Conversion And Management 51 (2010) 1428–1431
[32] Takase, Mohammed., Weiwei Feng, Wei Wang, Xiaoyun Guc, Yang Zhuc, Ting Li, Liuqing Yang, Xiangyang Wua, Silybum marianum oil as a new potential non edible feedstock for biodiesel: A comparison of its production using conventional and ultrasonic assisted method, Fuel Processing Technology 123 (2014) 19–26
[33] Pazouki, Mohammad., Farzane Zamani, Seyed Amir Hossein, Zamzamian, Ghasem. Najafpour, Study on Reaction Conditions in Whole Cell Biocatalyst Methanolysis of Pretreated Used Cooking Oil, Bioenergy Technology (2011) 93-100
36
[34] Zhang, Pingbo., Qiuju Han, Mingming Fan, Pingping Jiang, A Novel Waste Water Scale-Derived Solid Base Catalyst For Biodiesel Production, Fuel 124 (2014) 66–72
[35] Santi ,Valerio De., Fabio Cardellini, Lucia Brinchi , Raimondo Germani, Novel Brønsted Acidic Deep Eutectic Solvent As Reaction Media For Esterification Of Carboxylic Acid With Alcohols, Tetrahedron Letters 53 (2012) 5151–5155
[36] Fang, Zhen., Richard L. Smith, Jr, Xinhua Qi, Production of Biofuels and Chemicals with Ionic Liquids, Springer Science Business Media Dordrecht 2014
[37] Wu, Sheng-Hong., Alvin R. Caparangab, Rhoda B. Lerona, Meng-Hui Li, Vapor Pressure Of Aqueous Choline Chloride-Based Deep Eutectic Solvents (Ethaline, Glyceline, Maline And Reline) At 30–70 0C, Thermochimica Acta 544 (2012) 1– 5
[38] Wagle, Durgesh V., Hua Zhao, Gary A. Baker, Deep Eutectic Solvents : Sustainable Media for Nanoscale and Functional Materials, Accounts of Chemical Research (2014)
[39] Bagh, F.S. Ghareh., K. Shahbaz, F.S. Mjalli, I.M. AlNashef, M.A. Hashim, Electrical Conductivity of Ammonium and Phosphonium Based Deepeutectic Solvents: Measurements and Artificial Intelligence-Based Prediction, Fluid Phase Equilibria 356 (2013) 30– 37
[40] Ali, Emad., Mohamed K. Hadj-Kali, Sarwono Mulyono, Inas Alnashef, Anis Fakeeha, Farouq Mjalli, Adeeb Hayyan, Solubility of CO2 in Deep
Eutectic Solvents: Experiments and Modelling Using the Peng– Robinson Equation of State, Chemical Engineering Research and Design 92 (2014) 1898–1906
37
[41] Boocock, David G.B.., Samir K. Konar, V. Mao, C. Lee, Sonia Buligan, Fast Formation of High-Purity Methyl Esters from Vegetable Oils, J.Am. Oil Chem.Soc. 75 (1998) 1167 – 1172.
[42] Hua Zhao., Gary A. Baker, Shaletha Holmes, Protease Activation in Glycerol-Based Deep Eutectic Solvents, Journal of Molecular Catalysis B: Enzymatic 72 (2011) 163– 167
[43] Hidayat, Arif., Rochmadi, Karna Wijaya, Annisa Nurdiawati, Winarto Kurniawan, Hirofumi Hinode, Kunio Yoshikawa, Arief Budiman, Esterification of Palm Fatty Acid Distillate with High Amount of Free Fatty Acids using Coconut Shell Char Based Catalyst, Energy Procedia 75 ( 2015 ) 969 – 974
[44] Ramadhas, A.S., C. Muraleedharan, S. Jayaraj, Performance and Emission Evaluation of a Diesel Engine Fueled with Methyl Esters of Rubber Seed Oil, Renewable Energy 30 (2005) 1789–1800
[45] Encinar, José M., Ana Pardal, Nuria Sánchez, An Improvement to the Transesterification Process by the use of Co-solvents to Produce Biodiesel, Fuel 166 (2016) 51-58
[46] Zhang,Qinghua., Karine De Oliveira Vigier, Se´bastien Royer and Franc¸ ois Je´roˆme, Deep eutectic solvents: syntheses, properties and
applications41(2012) 7108-7146
12
BAB III
METODOLOGI PENELITIAN
3.1 Lokasi dan Waktu Penelitian
Penelitian dilakukan di Laboratorium Proses Industri Kimia, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera utara, Medan. Penelitian ini dilakukan selama lebih kurang 6 bulan.
3.2 Bahan dan Peralatan 3.2.1 Bahan Penelitian
Pada penelitian ini bahan yang digunakan antara lain: 1. Minyak sawit (RBDPO)
2. DES ChCl:glukosa 3. DES ChCl:etilen glikol 4. Metanol (CH3OH)
5. Etanol (C2H5OH)
6. Aquadest (H2O)
7. Kalium Hidroksida (KOH) 8. Phenolftalenin (C20H14O4)
3.2.2 Peralatan Penelitian
Pada penelitian ini peralatan yang digunakan antara lain : 1. Labu leher tiga
2. Termometer 3. Magnetic Stirrer 4. Hot plate
5. Gabus 6. Erlenmeyer 7. Corong Pemisah
8. Beaker Glass
9. Gelas Ukur 10. Neraca Digital
13 11. Batang Pengaduk
12. Corong Gelas 13. Pipet Tetes 14. Statif dan Klem 15. Stopwatch 16. Piknometer
17. Viskosimeter Ostwald 18. Karet Penghisap 19. Buret
20. Gabus
3.3 Rancangan Percobaan Sintesis Biodiesel
Reaksi transesterifikasi untuk sintesis biodiesel dilakukan dengan variabel tetap berupa rasio molar metanol : RBDPO (A), konsentrasi katalis KOH (B), kecepatan pengadukan (C), suhu reaksi (D) dan waktu reaksi (E) serta variabel bebas berupa jenis DES (X1 dan X2) dan konsentrasi DES (Y1, Y2, Y3, Y4, Y5 dan Y6).
[image:30.595.114.525.480.625.2]Adapun level kode dan kombinasi perlakuan penelitian dapat dilihat pada tabel 3.1 dan 3.2 berikut:
Tabel 3.1 Level Kode Rancangan Percobaan Sintesis Biodiesel Variabel
Perlakuan
Jenis DES Konsentrasi DES (% wt)
1 2 3 4 5 6
X1
Y 0 1 5 10 15 20
X2
14 Tabel 3.2 Rancangan Percobaan Sintesis Biodiesel
Run Kecepatan Pengadukan (rpm) Waktu (jam) Suhu (0C)
Konsentrasi Katalis (% wt) Rasio molar metanol : RBDPO Jenis DES Konsentrasi DES 1
A B C D D
X1
Y1
2 Y2
3 Y3
4 Y4
5 Y5
6 Y6
7
X2
Y2
8 Y3
9 Y4
10 Y5
11 Y6
3.4 Prosedur Penelitian Proses Sintesis Biodiesel
Adapun Prosedur Penelitian proses sintesis biodiesel dilakukan berdasarkan metode yang di peroleh dari Shahbazi, dkk.,(2012) dan Gu, dkk.,(2015) yaitu [14][11] :
1. RBDPO 30 gram, metanol 8,487 ml, katalis KOH 0,3 gram dan co-solvent deep eutectic solvents (DES) 0,3 gram disiapkan
2. RBDPO 30 gram dimasukkan ke dalam labu leher tiga dan dipanaskan di atas hot plate hingga mencapai suhu reaksi 60 0C
3. Metanol 8,487 ml, co-solvent DES 0,3 gram, dan katalis KOH 0,3 gram dimasukkan ke dalam labu leher tiga 500 ml yang telah berisi RBDPO sambil diaduk dengan kecepatan pengadukan 600 rpm selama 1 jam
4. Hot plate dimatikan dan campuran didinginkan hingga mencapai suhu kamar
5. Campuran reaksi dimasukkan ke dalam corong pemisah dan dibiarkan hingga terbentuk 2 lapisan.
6. Lapisan bawah yang merupakan campuran gliserol, metanol, KOH dan DES dipisahkan dari lapisan atas
15
7. Air panas ditambahkan ke dalam corong pemisah yang berisi lapisan atas dan dikocok untuk mengekstrak pengotor yang masih ada hingga terbentuk kembali 2 lapisan.
8. Lapisan bawah dibuang kembali dan perlakuan ini diulang beberapa kali hingga air cucian berwarna bening.
9. Lapisan atas dikeringkan yang merupakan metil ester. 10. Metil ester yang telah kering ditimbang dan dianalisis.
11. Prosedur di atas diulangi untuk variabel proses lainnya seperti yang telah dijelaskan pada rancangan percobaan.
3.4.1 Sketsa Percobaan Proses Sintesis Biodiesel
[image:32.595.105.530.334.491.2]
Gambar 3.1 Rangkaian Peralatan Sintesis Biodiesel dari RBDPO Secara Transesterifikasi Menggunakan Katalis KOH dan Deep Eutectic Solvents (DES)
sebagai Co-Solvent 1
2
3 4
5 6
7
8 9
4. Labu leher tiga 5. Heater
6. Refluks kondensor
Keterangan gambar: 1. Statif dan klem 2. Stirrer
3. Termometer
7. Ember
8. Selang air masuk 9. Selang air keluar
16 3.4.2 Prosedur Analisis
3.4.2.1 Analisis Kadar Free Fatty Acid (FFA) Bahan Baku RBDPO dengan Metode Tes AOCS Official Method Ca 5a-40
Untuk analisis kadar FFA bahan baku RBDPO sesuai dengan AOCS Official Method Ca 5a-40 dengan prosedur sebagai berikut
1. Bahan baku sebanyak 7,05 ± 0,05 gram dimasukkan ke dalam erlenmeyer. 2. Ditambahkan etanol 95% sebanyak 75 ml.
3. Campuran dikocok kuat dan dilakukan titrasi dengan NaOH 0,25 N dengan indikator fenolftalein 3-5 tetes. Titik akhir tercapai jika warna larutan berwarna merah rosa dan warna ini bertahan selama 10 detik.
Kadar FFA = T x V x BM berat sampel x 10
Dimana: T = normalitas larutan NaOH V = volum larutan NaOH terpakai M = berat molekul FFA
3.4.2.2 Analisis Komposisi Bahan Baku Minyak Sawit dan Biodiesel yang dihasilkan menggunakan GCMS
Komposisi bahan baku RBDPO serta biodiesel yang dihasilkan akan dianalisis menggunakan instrumen GCMS pada Laboratorium Pusat Penelitian Kelapa Sawit (PPKS).
3.4.2.3 Analisis Densitas Biodiesel yang Dihasilkan dengan Metode Tes OECD 109
Untuk analisis densitas menggunakan metode tes OECD 109. Untuk pengukuran densitas ini menggunakan peralatan utama yaitu piknometer. Perbedaan berat kosong dan penuh dihitung pada suhu 20 oC.
3.4.2.4 Analisis Viskositas Biodiesel yang Dihasilkan dengan Metode Tes ASTM D 445
Viskositas adalah ukuran hambatan cairan untuk mengalir secara gravitasi, untuk aliran gravitasi dibawah tekanan hidrostatis, tekanan cairan sebanding dengan kerapatan cairan. Satuan viskositas dalam cgs adalah cm2 per detik (Stokes). Satuan
17
SI untuk viskositas m2 per detik (104 St). Lebih sering digunakan centistokes (cSt) (1cSt =10-2 St = 1 mm2/s). Untuk analisis viskositas menggunakan metode tes ASTM D-445. Untuk pengukuran viskositas ini menggunakan peralatan utama yaitu viskosimeter Ostwald tube tipe kapiler, viscosimeter holder dan bath pemanas pada 37,8oC. Termometer yang digunakan dengan ketelitian 0,02oC dan menggunakan stop watch dengan ketelitian 0,2 detik.
3.5 Flowchart Penelitian Proses Sintesis Biodiesel
Metanol 8,487 ml, co-solvent DES 0,3 gram dan katalis KOH 0,3 gram dimasukkan ke dalam labu leher tiga 500 ml sambil diaduk dengan kecepatan pengadukan 600 rpm selama 1 jam
Campuran reaksi dimasukkan ke dalam corong pemisah dan dibiarkan hingga terbentuk 2 lapisan.
Lapisan bawah yang merupakan campuran gliserol, metanol, katalis KOH dan co-solvent DES dipisahkan dari lapisan atas
Air panas ditambahkan ke dalam corong pemisah yang berisi lapisan atas dan dikocok sehingga terbentuk kembali 2 lapisan RBDPO 30 gram, metanol 8,487 ml, katalis KOH 0,3 gram dan co-solvent
deep eutectic solvents (DES) 0,3 gram disiapkan
Hot plate dimatikan dan campuran didinginkan hingga mencapai suhu kamar Mulai
RBDPO 30 gram dimasukkan ke dalam labu leher tiga 500 ml dan dipanaskan di atas hot plate hingga mencapai suhu reaksi 60 0C
Lapisan bawah dibuang kembali dan perlakuan ini diulang beberapa kali hingga air cucian berwarna bening.
A
18
Gambar 3.2 Flowchart Proses Sintesis Biodiesel
Selesai
Metil ester yang telah kering ditimbang dan dianalisis
Prosedur di atas diulangi untuk variabel proses lainnya seperti yang telah dijelaskan pada rancangan percobaan
A
Lapisan atas yang merupakan metil ester dikeringkan
19
BAB IV
HASIL DAN PEMBAHASAN
4.1 DEEP EUTECTIC SOLVENT (DES)
Deep Eutectic Solvent (DES) merupakan campuran suatu garam dan suatu
senyawa Hydrogen Bond Donor (HBD) yang menghasilkan suatu cairan bening (colourless liquid) dengan freezing point yang jauh di bawah freezing point komponen penyusunnya [38]. Dimana karakteristik DES sangat dipengaruhi oleh jenis dan rasio molar garam dan HBD penyusunnya [27].
[image:36.595.106.518.478.580.2]Dalam penelitian ini DES yang digunakan berbasis ChCl (garam) dan D-Glukosa/Etilen Glikol (HBD) dengan rasio molar ChCl : D-Glukosa dan ChCl : Etilen Glikol masing-masing 2:1 dan 1:2. DES diperoleh dengan memanaskan garam ChCl dan HBD D-Glukosa/Etilen Glikol pada rasio molar yang ditentukan secara bersamaan hingga suhu 80 0C dan sambil diaduk menggunakan magnetic stirrer selama 2 jam, lalu setelah proses pemanasan selesai diperoleh cairan bening (colourless liquid) yang disebut DES [27]. Pada tabel 4.1. ditunjukkan karakteristik DES yang diperoleh.
Tabel 4.1 Karakteristik Deep Eutectic Solvent (DES) pada Suhu 30 0C (± 2 0C) Karakteristik
DES
Jenis DES
ChCl : D-Glukosa = 2:1 ChCl : Etilen Glikol = 1:2 Wujud Colourless liquid Colourless liquid
Titik beku 10 0C - 20 0C < 10 0C
Densitas 1,26352 gr/ml 1,11576 gr/ml
Ph 7,05 7,05
Viskositas - 26,4476 cP
Pada penelitian Hayyan, dkk.,(2013) dilaporkan bahwa DES berbasis ChCl dan D-Glukosa pada rasio molar 2:1 memiliki nilai freezing point terendah dibandingkan DES pada rasio molar lainnya [27]. Pada penelitian Bagh, dkk.,(2013) menyebutkan bahwa DES berbasis ChCl dan Etilen Glikol pada rasio molar 1:2 memiliki nilai freezing point terendah dibandingkan DES pada rasio molar lainnya [39]. Dimana freezing point terendah ini menunjukkan titik eutektik DES yang diperolah dari ikatan hidrogen antara garam ChCl dan HBD pada rasio molar yang tepat [40]. Hal ini menjadi pertimbangan pemilihan DES berbasis ChCl dan
20
Glukosa/Etilen Glikol dengan rasio molar ChCl : D-Glukosa dan ChCl : Etilen Glikol masing 2:1 dan 1:2.
Dalam reaksi transesterifikasi, minyak dan metanol tidak larut sehingga terdapat dua fasa dalam reaksi. Hal ini menyebabkan perpindahan massa antara metanol dan minyak menurun sehingga mempengaruhi laju reaksi pada tahap awal. Co-solvent adalah pelarut yang dapat meningkatkan kelarutan metanol dan minyak
sehingga menjadi satu fasa dan meningkatkan laju reaksi [41]. Dalam penelitian ini, DES digunakan sebagai co-solvent dalam sintesis biodiesel karena DES memiliki kemampuan solvasi atau pelarutan yang unik [11]. Dalam bidang lain DES telah diaplikasikan sebagai pelarut dalam reaksi kimia, proses pemisahan dan pemurnian, elektrokimia dan material kimia [11]. Namun, penggunaan DES sebagai co-solvent dalam sintesis biodiesel masih sedikit, yaitu diantaranya dilaporkan oleh Zhao, dkk.,(2011), yaitu DES sebagai co-solvent dalam reaksi enzimatik sintesis biodiesel [42] dan Gu, dkk.,(2015), yaitu dalam sintesis biodiesel melalui reaksi transesterifikasi menggunakan katalis basa [11]. Oleh karena itu, pada penelitian ini DES diaplikasikan sebagai co-solvent dalam sintesis biodiesel dari RBDPO menggunakan katalis basa KOH. Dimana, diharapkan DES yang digunakan dapat meningkatkan kelarutan minyak dengan metanol dan meningkatkan kemampuan katalis.
4.2 ANALISIS BAHAN BAKU REFINED, BLEACHED AND
DEODORIZED PALM OIL (RBDPO)
Bahan baku minyak yang digunakan dalam penelitian ini adalah Refined, Bleached and Deodorized Palm Oil (RBDPO). RBDPO adalah minyak kelapa sawit
yang telah mengalami proses penyulingan, pemutihan dan penghilangan bau sehingga menyebabkan RBDPO lebih baik digunakan sebagai bahan baku dalam produksi biodiesel dari pada minyak kelapa sawit mentah (CPO) [14].
Adanya asam lemak bebas (FFA) dalam lemak atau minyak merupakan komponen yang sangat mengganggu, terutama dalam reaksi transesterifikasi minyak (trigliserida) menggunakan katalis basa. Hal ini karena asam lemak bebas dapat membentuk sabun melalui reaksi netralisasi dengan katalis basa, sehingga menyebabkan berkurangnya metil ester yang dihasilkan [41 dan 43]. Kadar FFA bahan bakuyang baik untuk sintesis biodiesel adalah <2%. Sintesis biodiesel melalui
21
reaksi transesterifikasi tidak akan terjadi jika FFA dalam minyak sekitar 3 % [44]. Selain itu, kadar air dalam reaksi sintesis biodiesel harus kurang dari sekitar 1 % dan sebaiknya kurang dari 0,5% [41].
[image:38.595.115.524.355.524.2]Dari hasil analisis kadar FFA dan kadar air pada bahan baku RBDPO yang digunakan diperoleh kadar FFA sebesar 1,141 % dan kadar air sebesar 0,02 %. Hal ini menunjukkan bahwa bahan baku RBDPO yang digunakan sesuai standar untuk reaksi transesterifikasi sintesis biodiesel menggunakan katalis basa KOH. Selanjutnya RBDPO dianalisis menggunakan GC (Gas Chromatography) untuk mengetahui komposisi asam lemak yang terkandung di dalamnya serta untuk menghitung berat molekul RBDPO (dalam bentuk trigliserida). Pada tabel 4.2 ditunjukkan komposisi asam lemak RBDPO yang diperoleh dari kromatogram hasil analisis GC.
Tabel 4.2 Komposisi Asam Lemak RBDPO No.
Puncak
Retention Time
(menit) Komponen Penyusun
Komposisi % (b/b)
1 13,630 Asam Laurat (C12:0) 0,1781
2 16,606 Asam Miristat (C14:0) 0,9201
3 19,318 Asam Palmitat (C16:0) 39,6016
4 19,590 Asam Palmitoleat (C16:1) 0,1549
5 21,590 Asam Stearat (C18:0) 4,1055
6 21,916 Asam Oleat (C18:1) 43,7615
7 22,426 Asam Linoleat (C18:2) 10,5534
8 23,139 Asam Linolenat (C18:3) 0,2038
9 23,858 Asam Arakidat (C20:0) 0,3712
10 24,247 Asam Eikosenoat (C20:1) 0,1511
Dari hasil analisis GC diperoleh komponen asam lemak tertinggi pada bahan baku RBDPO adalah asam lemak jenuh berupa asam palmitat (C16:0) sebesar 39,6016
% dan asam lemak tidak jenuh berupa asam oleat (C18:1) sebesar 43,7615 %.
Berdasarkan data komposisi asam lemak RBDPO pada tabel 4.2 diperoleh berat molekul RBDPO (dalam bentuk trigliserida) sebesar 848,9948 gr/mol sedangkan berat molekul FFA RBDPO sebesar 270,7391gr/mol. Selain itu, dapat dilihat bahwa komposisi asam lemak tak jenuh dan asam lemak jenuh pada RBDPO masing-masing adalah sebesar 54,82% dan 45,18 %.
22 4.3 ANALISIS YIELD BIODIESEL
Pada penelitian ini, biodiesel diperoleh melalui reaksi transesterifikasi RBDPO dengan metanol menggunakan katalis basa (KOH) dan co-solvent Deep Eutectic Solvent (DES). Dimana pengaruh jenis dan konsentrasi DES sebagai
co-solvent dalam sintesis biodiesel ini merupakan parameter utama. Pada tabel 4.3
[image:39.595.108.517.235.349.2]ditunjukkan hasil analisis yield biodiesel yang diperoleh. Tabel 4.3 Data Yield Biodiesel Konsentrasi DES
(% (b/b))
Yield Biodiesel (%)
ChCl : D-Glukosa = 2:1 ChCl : Etilen Glikol = 1:2
0 92,7916 92,7916
1 89,7973 91,3417
5 71,2025 86,6459
10 51,4925 85,1886
15 19,1234 83,4381
20 10,5426 80,7880
Reaksi transesterifikasi dilakukan pada rasio molar RBDPO : metanol = 6:1, suhu reaksi 60 0C, kecepatan pengadukan 600 rpm, waktu reaksi 60 menit, konsentrasi katalis KOH 1% (b/b) dan konsentrasi co-solvent DES yang bervariasi untuk kedua jenis DES, yaitu 0; 1; 5; 10; 15 dan 20 % (b/b). Setelah reaksi transesterifikasi selesai campuran didiamkan selama 1 menit hingga terbentuk 2 lapisan. Lapisan bawah yang terdiri dari gliserol, katalis KOH, metanol dan DES dipisahkan dari lapisan atas yang mengandung fatty acid metil ester/FAME (biodiesel). Lalu lapisan atas dicuci dengan air panas (70 0C) sebanyak 3 kali untuk membuang pengotor-pengotor yang masih terikut. Selanjutnya biodiesel yang diperoleh dianalisis menggunakan GC (Gas Chromatography) untuk mengetahui yield biodiesel yang diperoleh.
4.3.1
PENGARUH PENAMBAHAN DES BERBASIS ChCl/D-GLUKOSA SEBAGAI CO-SOLVENT TERHADAP YIELD BIODIESELPada penelitian ini biodiesel disintesis dengan dan tanpa penambahan DES sebagai co-solvent untuk melihat pengaruhnya terhadap yield biodiesel. Pada gambar 4.1 ditunjukkan pengaruh penambahan DES berbasis ChCl/D-Glukosa sebagai co-solvent terhadap yield biodiesel.
23
Gambar 4.1 Pengaruh Konsentrasi DES berbasis ChCl/D-Glukosa terhadap Yield Biodiesel
Dari grafik di atas dapat dilihat bahwa tanpa penambahan co-solvent DES dihasilkan biodiesel dengan yield tertinggi, yaitu 92,7916 %. Sedangkan dengan penambahan co-solvent DES dengan konsentrasi yang semakin meningkat, yaitu 1; 5; 10; 15 dan 20 % (b/b) diperoleh yield biodiesel yang semakin menurun, yaitu sebesar 89,7973; 71,2025; 51,4925; 19,1234 dan 10,5426 %.
DES merupakan pelarut yang memiliki kemampuan solvasi (pelarut) yang baik, sehingga penambahan DES sebagai co-solvent dalam sintesis biodiesel ini diharapkan dapat meningkatkan kelarutan metanol dengan minyak dalam reaksi transesterifikasi sehingga meningkatkan yield biodiesel [11,45,41]. Boocock (1999) juga menyebutkan bahwa penambahan co-solvent akan meningkatkan kelarutan minyak dan alkohol sehingga yield biodiesel juga akan meningkat [41]. Namun, dari hasil penelitian yang dilakukan diperoleh bahwa penambahan DES berbasis ChCl/D-Glukosa sebagai co-solvent dalam reaksi transesterifikasi menurunkan yield biodiesel.
Pada penelitian sebelumnya yang dilakukan oleh Gu, dkk.,(2015) mengenai sintesis biodiesel dari rapeseed oil menggunakan co-solvent DES berbasis ChCl/Gliserol pada rasio molar 1:2 diperoleh bahwa penambahan co-solvent DES 9,27 % (b/b) mampu meningkatkan yield biodiesel hingga 98 % [11]. Nilai ini lebih tinggi dibandingkan yield biodiesel tanpa penambahan co-solvent DES, yaitu hanya berkisar 91 %. Selanjutnya, pada penelitian Gu, dkk.,(2015) juga disebutkan bahwa
0 20 40 60 80 100
0 5 10 15 20 25
Y
ie
ld
(%)
Konsentrasi DES (% b/b)
24
penambahan co-solvent DES dengan konsentrasi yang semakin meningkat menjadi 10 % (b/b) dan 20 % (b/b) diperoleh yield biodiesel menurun, yaitu masing-masing sebesar 95 % dan 88 % [11]. Jika dibandingkan dengan sintesis biodiesel dengan penambahan co-solvent DES berbasis ChCl/D-Glukosa pada konsentrasi yang sama, yaitu 10 % dan 20 %, dari hasil penelitian diperoleh yield biodiesel 51,4925 % dan 10,5426 %. Yield biodiesel dengan penambahan co-solvent DES berbasis ChCl/D-Glukosa ini jauh menurun dibandingkan dengan penambahan co-solvent DES berbasis ChCl/Gliserol pada penelitian Gu, dkk.,(2015) [11].
[image:41.595.108.529.395.482.2]Hal ini mungkin disebabkan oleh perbedaan karakteristik yang dimiliki oleh masing-masing DES karena jenis HBD yang berbeda pada DES akan menghasilkan karakteristik DES yang berbeda pula. Sehingga akan mempengaruhi kemampuan DES sebagai co-solvent dalam sintesis biodiesel. Perbedaan karakteristik DES berbasiss ChCl/Gliserol pada rasio molar 1:2 dan DES berbasis ChCl/D-Glukosa pada rasio molah 2:1 ditunjukkan pada tabel 4.4 berikut ini.
Tabel 4.4 Karakteristik DES Berbasis ChCl/D-Glukosa dan ChCl/Gliserol
Spesifikasi Jenis DES
ChCl : D-Glukosa = 2:1 ChCl : Gliserol = 1:2
Freezing Point 10 0C – 20 0C -40 0C [Zhang 2012]
Densitas 1,26352 gr/ml (30 0C) 1,18 gr/ml (25 0C) [Zhang 2012]
pH 7,05 (30 0C) -
Viskositas Tidak dapat di ukur (30 0C) 259 cP (25 0C) [Zhang 2012] Dari tabel 4.4 dapat di lihat bahwa DES berbasis ChCl/D-Glukosa memiliki freezing point dan densitas yang lebih tinggi dibandingkan DES berbasis
ChCl/Gliserol. Sedangkan untuk nilai viskositasnya, dari hasil penelitian diperoleh bahwa viskositas DES berbasis ChCl/D-Glukosa tidak dapat diukur pada suhu ruangan karena berwujud turbid white liquid (cairan kental putih). Dimana hal ini menandakan viskositas DES tinggi. Viskositas dan densitas yang tinggi pada DES berbasis ChCl/D-Glukosa dapat menyebabkan kelarutan metanol dan minyak semakin menurun, sehingga menghambat perpindahan masssa antara metanol dan minyak. Hal ini akan menyebabkan konversi ke arah produk menjadi menurun, sehingga yield biodiesel yang dihasilkan dari sintesis biodiesel menggunakan co-solvent DES berbasis D-Glukosa lebih rendah dibandingkan yield biodiesel tanpa
menggunakan co-solvent. Oleh karena itu, penambahan co-solvent DES berbasis D-Glukosa yang semakin meningkat akan menyebabkan yield biodiesel semakin
25
menurun. Hal ini juga didukung oleh penelitian Yusof, dkk.,(2014) yaitu bahwa pemilihan DES sebagai suatu pelarut sangat dipengaruhi oleh viskositas DES [3]. Hal ini karena viskositas DES berhubungan erat dengan kemampuan cairan untuk mengangkut massa dalam cairan, sehingga apabila DES memiliki viskositas tinggi maka akan menyebabkan konversi produk rendah. Pada penelitian Hayyan, dkk.,(2013) juga disebutkan bahwa pengukuran densitas sangat penting terutama dalam bidang mekanika fluida dan perpindahan massa [27].
Oleh karena itu dapat disimpulkan bahwa DES berbasis ChCl/D-Glukosa tidak cocok digunakan sebagai co-solvent dalam sintesis biodiesel karena memiliki karakteristik yang tidak sesuai sebagai sebuah co-solvent, yaitu memiliki densitas dan viskositas yang tinggi.
[image:42.595.133.472.439.642.2]4.3.2 PENGARUH PENAMBAHAN DES BERBASIS ChCl/ETILEN GLIKOL SEBAGAI CO-SOLVENT TERHADAP YIELD BIODIESEL Pada gambar 4.2 ditunjukkan pengaruh penambahan DES berbasis ChCl/Etilen Glikol sebagai co-solvent terhadap yield biodiesel.
Gambar 4.2 Pengaruh Konsentrasi DES berbasis ChCl/Etilen Glikol terhadap Yield Biodiesel
Dari grafik pada gambar 4.2 dapat dilihat bahwa tanpa penambahan co-solvent DES dihasilkan biodiesel dengan yield tertinggi, yaitu 92,7916 % dan sama
0 20 40 60 80 100
0 5 10 15 20 25
Y
ie
ld
(%)
Konsentrasi DES (% b/b)
26
halnya dengan penambahan co-solvent DES berbasis ChCl/D-Glukosa yang telah dibahas dalam sub bab sebelumnya, penambahan co-solvent DES berbasis ChCl/Etilen Glikol juga menurunkan yield biodiesel dan semakin tinggi konsentrasi DES, yield biodiesel yang diperoleh juga semakin menurun. Dari hasil penelitian pada konsentrasi DES 1; 5; 10; 15 dan 20 % (b/b) diperoleh yield biodiesel sebesar 91,3417; 86,6459; 85,1886; 83,4381 dan 80,7880 %.
Oleh karena itu, hasil penelitian yang diperoleh tidak sejalan dengan penelitian Gu, dkk.,(2015), yaitu penambahan co-solvent DES berbasis ChCl/gliserol pada rasio molar 1:2 sebanyak 9,27 % (b/b) mampu meningkatkan yield biodiesel hingga 98%, dimana nilai ini lebih tinggi dari yield biodiesel tanpa penambahan co-solvent DES, yaitu hanya berkisar 91 % [11]. Sedangkan dari hasil penelitian yang
diperoleh, penambahan co-solvent DES berbasis ChCl/Etilen Glikol pada setiap konsentrasi yang ditentukan semuanya menurunkan yield biodiesel.
Setiap DES memiliki karakteristik yang berbeda sesuai dengan jenis dan rasio komponen penyusunnya, sehingga akan mempengaruhi kemampuan DES sebagai co-solvent dalam sintesis biodiesel [27]. Oleh karena itu ditinjau karakteristik kedua
[image:43.595.105.528.462.548.2]DES, yaitu pada tabel 4.5 berikut ini.
Tabel 4.5 Karakteristik DES Berbasis ChCl/Etilen Glikol dan ChCl/Gliserol
Spesifikasi Jenis DES
ChCl : Etilen Glikol = 1:2 ChCl : Gliserol = 1:2
Freezing Point <10 0C -40 0C [Zhang 2012]
Densitas 1,11576 gr/ml (30 0C) 1,18 gr/ml (25 0C) [Zhang 2012]
pH 7,05 (30 0C) -
Viskositas 26,4476 (30 0C) 259 cP (25 0C) [Zhang 2012] Dari tabel 4.5. dapat dilihat bahwa DES berbasis ChCl/Etilen Glikol pada rasio molar 1:2 yang digunakan dalam penelitian ini memiliki karakteristik yang lebih baik dari DES berbasis ChCl/Gliserol pada rasio molar 1:2 yang digunakan pada penelian Gu, dkk.,(2015) [11]. DES berbasis ChCl/Etilen Glikol memiliki densitas dan viskositas yang jauh lebih rendah dibandingkan DES berbasis ChCl/Gliserol. Oleh karena itu, seharusnya DES berbasis ChCl/Etilen Glikol dapat meningkatkan kelarutan metanol dan minyak, sehingga perpindahan massa antara metanol dan minyak juga semakin meningkat. Dimana hal ini akan meningkatkan konversi ke arah produk, sehingga yield biodiesel yang diperoleh semakin
27
Gliserol Ester
Trigliserida Alkohol
DES
meningkat. Akan tetapi, dari hasil penelitian diperoleh hasil sebaliknya, yaitu penggunaan DES berbasis ChCl/Etilen Glikol sebagai co-solvent dalam sintesis biodiesel menurunkan yield biodiesel. Bahkan penambahan DES pada konsentrasi 1% saja sudah menurunkan yield biodiesel.
DES berbasis garam ChCl dan HBD Etilen Glikol pada rasio molar 1: 2 merupakan DES yang memiliki freezing point terendah dibandingkan dengan DES pada rasio molar lainnya, dimana pada rasio molar tersebut gugus hidroksil pada HBD Etilen Glikol memiliki kemampuan yang kuat untuk membentuk interaksi ikatan hidrogen dengan anion halida dari ChCl [11,46].
O
CH2 OC R1 R1 COO R’ CH2 OH
O
HC OC R2 + 3R’OH R2 COO R’ + HC OH
O
H2C OC R3 R3 COO R’ H2C OH
[image:44.595.113.522.278.516.2]
Gambar 4.3 Reaksi Transesterifikasi sintesis Biodiesel dengan penambahan DES sebagai co-solvent
Pada gambar 4.3 dapat di lihat metanol yang mengandung gugus hidroksil OH- juga mungkin akan mengikat anion halida ChCl dalam DES sehingga menghasilkan beberapa molekul metanol bebas dalam reaksi dan dengan demikian akan menghambat reaksi dan menurunkan yield biodiesel yang diperoleh [11]. Selain itu jumlah metanol yang tersedia untuk reaksi transesterifikasi sintesis biodiesel juga akan berkurang dan menyebabkan menurunnya yield biodiesel.
Oleh karena itu dapat disimpulkan bahwa sintesis biodiesel dari RBDPO menggunakan co-solvent DES berbasis ChCl/Etilen Glikol pada kondisi reaksi
Katalis
28
tertentu dalam penelitian ini tidak cocok. Hal ini karena penambahan co-solvent DES berbasis ChCl/Etilen Glikol pada konsentrasi 1% saja sudah menurunkan yield biodiesel. Oleh karena itu, dalam kasus sintesis biodiesel menggunakan co-solvent DES perlu diamati pemilihan jenis bahan baku minyak yang digunakan, pemilihan jenis DES serta pemilihan kondisi reaksi yang sesuai untuk reaksi tersebut. Sehingga dapat diperoleh kondisi reaksi yang cocok untuk menghasilkan yield biodiesel yang tinggi dalam sintesis biodiesel dari bahan baku minyak tertentu dengan jenis DES tertentu.
29
BAB V
KESIMPULAN DAN SARAN
5.1 KESIMPULAN
Adapun kesimpulan yang dapat diambil dari penelitian yang telah dilakukan adalah:
1. Jenis HBD penyusun DES sangat mempengaruhi karakteristik DES, sehingga juga mempengaruhi kemampuan DES ketika diaplikasikan sebagai co-solvent dalam sintesis biodiesel.
2. DES berbasis ChCl:Etilen Glikol=1:2 memiliki karakteristik yang lebih baik dari DES berbasis ChCl:D-Glukosa=2:1, yaitu meliputi titik beku, densitas dan viskositas yang lebih rendah.
3. Penggunaan DES berbasis ChCl:D-Glukosa=2:1 dan ChCl:Etilen Glikol=1:2 sebagai co-solvent dalam sintesis biodiesel dari RBDPO menurunkan yield biodiesel.
4. DES berbasis ChCl:D-Glukosa=2:1 tidak cocok diaplikasikan sebagai co-solvent dalam sintesis biodiesel dari RBDPO karena memiliki densitas dan
viskositas yang tinggi.
5. DES berbasis ChCl:Etilen Glikol=1:2 tidak cocok diaplikasikan sebagai co-solvent dalam sintesis biodiesel dari RBDPO karena memiliki ikatan hidrogen
yang sangat kuat.
5.2 SARAN
Adapun saran yang dapat diberikan adalah:
1. Peneliti menyarankan untuk meninjau pengaruh rasio molar minyak dan metanol, waktu reaksi, suhu reaksi dan dosis katalis yang berbeda pada sintesis biodiesel dengan menggunakan co-solvent DES.
2. Peneliti menyarankan untuk melakukan analisis karakteristik DES dan analisis komposisi bahan baku minyak terlebih dahulu untuk mengetahui apakah keduanya dapat melarut dengan baik.
30
3. Peneliti menyarankan untuk menggunakan jenis minyak lain sebagai bahan baku pada sintesis biodiesel dengan menggunakan co-solvent DES, misalnya CPO.
5
BAB II
TINJAUAN PUSTAKA
2.1 Perkembangan Industri Kimia
Banyak proses kimia yang melibatkan larutan homogen untuk meningkatkan laju reaksi. Namun, sebagian besar pelarut yang digunakan untuk reaksi adalah senyawa organik volatil yang mudah menguap ke atmosfer [15]. Pelarut organik volatil yang digunakan dalam jumlah besar sebagai media reaksi dalam industri kimia sehari-hari berkontribusi sebagai sumber utama pencemaran lingkungan, sehingga pergantian pelarut berbahaya yang mudah menguap dengan pelarut yang mimiliki karakteristik yang lebih baik terhadap lingkungan, kesehatan dan keselamatan merupakan suatu keharusan pada semua industri, seperti peningkatan biodegradabilitas. Polusi dalam ekologi sintetis kimia dapat dihasilkan melalui produk samping atau bahan awal yang tidak bereaksi serta media reaksi seperti pelarut dan katalis. Oleh karena hal tersebut, maka pengembangan teknologi hijau dengan hasil yang tinggi menjadi sangat penting dan ditemukan bahwa cairan ionik/ionic liquids (ILs) menarik untuk digunakan dalam banyak reaksi organik [16].
ILs didefinisikan sebagai garam yang memiliki wujud cair pada suhu di bawah 100 °C [17]. ILs telah muncul sebagai pelarut baru yang sesuai untuk sejumlah aplikasi dan baru-baru ini cairan ionik (ILs) telah mendapat perhatian dalam kimia modern karena penggunaannya yang luas, termasuk dalam bidang katalisis, sintesis, analisis dan penyerapan gas [18,19]. ILs memiliki sifat fleksibilitas, tidak volatil, tidak korosif, immiscibility dengan banyak pelarut organik, memiliki hasil reaksi yang lebih tinggi dan selektif pada berbagai aplikasi untuk menggantikan katalis homogen asam atau katalis heterogen konvensional [19]. Penyiapan ILs sebagai pelarut bebas dalam suatu proses secara jelas muncul sebagai alternatif yang unggul dan dalam beberapa kasus untuk melarutkan substrat yang polaritasnya berbeda membuat ILs menjadi pilihan pelarut ionik yang lebih menarik [18]. Akan tetapi, meskipun semua sifat ILs berharga, seperti tekanan uap yang rendah, stabilitas kimia dan stabilitas termal yang luar biasa dan dapat di daur ulang, ILs tetap tidak sehijau yang diharapkan [16]. ILs masih memiliki keterbatasan, seperti dalam hal biaya, pemurnian dan toksisitas. Dimana saat ini hal tersebut tidak
6
jelas (tergantung pada struktur spesies kationik) dan untuk mendapat ILs dengan kemurnian yang tinggi tidak mudah karena adanya pengotor akan dapat mempengaruhi sifat fisikokimia dan aktifitasnya [20]. Hal tersebut merupakan rintangan penting untuk implementasi praktis lanjut dari ILs [18].
Selanjutnya, dalam beberapa tahun terakhir muncul deep eutectic solvent (DES) yang dianggap sebagai calon alternatif untuk menggantikan ILs. DES telah mencapai peningkatan karena menjadi perhatian penting, baik dalam bidang akademik maupun dalam bidang industri karena aplikasi potensinya sebagai pelarut ramah lingkungan [21].
2.2 Deep Eutectic Solvent (DES)
Istilah DES telah diciptakan sebagai alasan untuk membedakan DES dengan ILs dan juga untuk mencerminkan depresi titik beku yang besar pada campuran eutektik. Dimana telah diamati depresi titik beku pada campuran eutektik dapat sebanyak beberapa ratusan 0C [22]. Deep eutectic solvent (DES) terbentuk ketika garam halida organik (biasanya choline cloride/ChCl) dikombinasikan dengan bahan yang mampu membentuk kompleks dengan halida (seperti urea) untuk membentuk suatu material yang cair pada kondisi kamar [23]. DES adalah larutan ion yang membentuk suatu eutektik dengan titik lebur lebih rendah daripada salah satu dari komponen penyusunnya [24]. Alasan dinamakan DES adalah karena ketika dua komponen ditambahkan bersama-sama dalam rasio yang tepat titik eutektik dapat dilihat. Titik eutektik campuran dapat dilihat dari gambar dibawah ini yang merupakan suatu rasio molar dua senyawa yang mengupayakan titik lebur serendah mungkin [22].
7
Gambar 2.1 Diagram Representasi Teori Titik Eutektik Campuran [22]
2.3 Sintesis Deep Eutectic Solvent (DES)
Salah satu bidang terbesar DES adalah penggunaan garam amonium kuaterner dan pengompleks donor ikatan hidrogen. Berbagai donor ikatan hidrogen yang telah diamati melibatkan asam polikarboksilat, poliamida dan polyalkohol. DES mudah untuk disintesis dalam keadaan murni karena tidak reaktif dengan air dan sebagain besar biodegradable. Meskipun prinsip dasar cara DES bekerja sangat mirip dengan ILs, DES tidak dianggap sebagai ILs karena DES tidak mengandung anion dan kation sepenuhnya. DES mengandung kation dan anion dan lebih penting lagi terdapat penyumbang spesies ikatan hidrogen juga. Hasil akhirnya sama, yaitu terbentuk cairan yang terdiri atas kation dan anion, namun rute pengurangan energi kisi dari sistem berbeda. Hal ini terjadi melalui donor ikatan hidrogen pengompleks untuk anion dan dengan menggambar densitas elektron pada anion dari kation. Hasil pemisahan dalam interaksi anion/kation yang lebih lemah merupakan saat ILs mencapai suhu leleh rendahnya [22]. Selain itu, biaya yang rendah untuk mensintesis DES membuat DES lebih diinginkan dari ILs untuk banyak aplikasi, seperti yang membutuhkan sintesis skala besar suatu bahan fungsional baru atau yang berbasis pada perangkat energi [24]. Pelarut ion DES juga telah digunakan untuk waktu yang lama karena sifat pelarutnya yang menarik. DES pertama kali yang dilaporkan adalah dari campuran choline cloride (ChCl) (garam organik) dan urea (donor hidrogen ikatan) pada perbandingan 1:2 mol dan DES tersebut meleleh pada suhu terendah 13
Melting point of A
Melting point of B Liquid L
B + L B + L
A + B
Eutectic Point
Solid A
doped
with B
Solid B
doped
with A
8
0
C. Campuran dari ZnCl2 dengan ChCl pada perbandingan molar 1:2 juga dilaporkan
memiliki titik beku dari 23 0C [15]
Sintesis DES dapat dibentuk dengan mengaduk secara perlahan garam dan donor ikatan hidrogen pada suhu 100 0C sampai jernih dan cairan homogen terbentuk (biasanya antara 0,5-2 jam). Rasio choline cloride/ChCl:donor ikatan hirogen yang berbeda juga diuji (dari 1:0,5 mol s/d 1:2 mol) untuk mengetahui kombinasi yang tepat yang akan mengarah pada depresi eutektik campuran dan hebatnya, semua DES yang dibentuk menunjukkan titik leleh di bawah 100 0C [25].
2.4 Aplikasi Deep Eutectic Solvent (DES) dalam Bidang Biodiesel
Taubert, dkk.,(2014) telah melaporkan beberapa aplikasi dari DES sebagai pengganti pelarut organik konvensional dalam reaksi biologis [26]. Selain itu, DES dalam reaksi kimia juga telah banyak digunakan, seperti ekstraksi gliserol dari biodiesel, elektrodeposisi dan ekstraksi logam, pemisahan dan pemurnian proses, elektrokimia, sebagai bahan kimia, sebagai co-solvent dalam sintesis organik dan anorganik dan sebagai biokatalisis [26,25].
Dari berbagai aplikasi penggunaan DES tersebut, Gu, dkk.,(2015) melaporkan penggunaan DES berbasis choline chloride/gliserol (1:2) menjadi co-solvent dalam sintesis biodiesel menggunakan NaOH sebabagai katalis. Hasil
penelitian menunjukkan bahwa FAME dapat diperoleh hingga yield 98 % [11]. Selain itu, penggunaan DES sebagai co-solvent dalam sintesis biodiesel ini memiliki kelebihan, seperti meminimalkan jumlah penggunaan pelarut volatil (metanol), mempercepat dan memudahkan pemurnian biodiesel yang diperoleh.
Hayyan, dkk.,(2013) juga telah melaporkan penggunaan DES dalam pengolahan minyak yang memiliki kandungan asam lemak bebas tinggi dan melakukan sintesis biodiesel. Dalam penelitian digunakan low grade crude palm oil (LGCPO) atau minyak sawit mentah kelas rendah yang memiliki kandungan asam lemak bebas yang tinggi kandungan (FFA) yang diperkenalkan sebagai kemungkinan bahan baku alternatif dalam produksi biodiesel. Pengolahan awal LGCPO dilakukan dengan menggunakan DES yang terdiri dari donor ikatan hidrogen berbasis ammonium (yaitu p-toluenesulfonic acid monohydrate/PTSA) dan garam (yaitu N,N-diethylenethanol ammonium chloride). Pada reaksi esterifikasi yang dilakukan,
9
kandungan FFA dari LGCPO berkurang dari 9,5 % menjadi kurang dari 1%. Dari hasil penelitian pada kandungan FFA 0.6±0.01% dan diperoleh konversi FFA menjadi FAME 93,67 % dan diperoleh yield sebesar 93 % [27].
2.5 Sintesis Biodiesel
Berdasarkan pengamatan yang dilakukan oleh banyak peneliti, biodiesel (metil ester) dapat dihasilkan dari minyak nabati, lemak hewani atau minyak goreng bekas. Secara global, ada lebih dari 350 tanaman yang diidentifikasi sebagai sumber potensial untuk produksi biodiesel. Baru-baru ini, biodiesel dari minyak nabati yang merupakan sumber daya terbarukan telah menjadi lebih menarik karena manfaatnya terhadap lingkungan, terutama minyak kelapa sawit karena memiliki kandungan minyak yang tinggi dan tingkat produksi yang tinggi untuk memenuhi kebutuhan energi di masa depan. Di Asia, biodiesel dominan berasal dari minyak sawit, di Amerika berasal dari minyak kedelai dan di Eropa dominan dari minyak kanola Beragam bahan baku yang tersedia untuk produksi biodiesel tersebut merupakan salah satu faktor yang paling signifikan untuk produksi biodiesel [28].
Biodiesel didefinisikan sebagai asam lemak metil ester (FAME) atau asam lemak etil ester (FAEE) dari minyak nabati atau lemak hewani [29]. Saat ini, biodiesel sangat diminati untuk dikembangkan karena emisinya yang lambat dan sifat kimianya yang tidak beracun, biodegradable dan memiliki karbon yang netral [30]. Kandungan oksigen yang tinggi (≈10wt%) pada biodiesel memungkinkan pembakaran sempurna pada mesin, sehingga menghasilkan emisi gas buang seperti jumlah partikulat, hidrokarbon, gas CO, CO2 dan SOx yang lebih rendah dan
menjadikan bahan bakar biodiesel ramah lingkungan [13]. Keuntungan yang signifikan antara biodiesel dan bahan bakar diesel konvensional berbasis fosil adalah emisi mesin lebih bersih, merupakan sumber energi terbarukan dan dapat sebagai properti pelumas superior, sehingga menjadikannya sebagai bahan bakar alternatif yang sangat baik [29].
Biodiesel diproduksi melalui reaksi transesterifikasi minyak nabati atau lemak hewani dengan metanol (etanol) untuk mendapatkan mono alkil ester, seperti yang ditunjukkan dalam gambar 2.1 [31].
10
Gliserol Ester
Alkohol O
CH2 OC R1 R1 COO R’ CH2 OH
O
HC OC R2 + 3R’OH R2 COO R’ + HC OH
O
H2C OC R3 R3 COO R’ H2C OH
[image:53.595.114.512.97.187.2]
Gambar 2.2 Reaksi Transesterifikasi [32]
Alkohol dengan rantai pendek seperti metanol, etanol, dan butanol adalah alkohol yang banyak digunakan dalam sintesis biodiesel. Pemilihan alkohol didasarkan pada beberapa faktor termasuk pertimbangan biaya dan kinerjanya. Dari beberapa jenis alkohol yang banyak digunakan, metanol dan etanol jauh lebih disukai. Hal tersebut dikarenakan metanol lebih murah dan menguntungkan dari segi sifat fisika maupun sifat kimia dan etanol merupakan alkohol yang ramah lingkungan karena dihasilkan dari sumber daya terbarukan [32].
Namun, terdapat setidaknya dua hambatan terkait dengan sintesis biodiesel dengan proses konvensional, yaitu: (1) adanya keterbatasan perpindahan massa dan laju reaksi yang rendah karena sistem biphasic antara campuran minyak dengan metanol dan (2) terjadi kesulitan dalam pemurnian produk (menghapus pengotor, seperti sabun, residu katalis, sisa metanol, gliserol dan air) [11].
Sejumlah proses telah dikembangkan untuk sintesis biodiesel, diantaranya melibatkan katalis kimia, katalis enzim dan bahkan menggunakan reaksi non-katalitik superkritis, microwave dan ultrasonik [30,29]. Katalis kimia basa seperti alkali (NaOH, KOH, dan NaOCH3) telah banyak digunakan karena menghasilkan
konversi yang tinggi dari trigliserida menjadi metil ester [34,33]. Katalis alkali juga telah terbukti lebih praktis diterapkan dalam industri karena waktu reaksi yang singkat dan bersifat non-korosif, sedangkan katalis asam menimbulkan korosi pada peralatan dan laju reaksi yang relatif lambat [32,34]. Selain itu, katalis alkali juga lebih murah bila dibandingkan dengan enzim [32]. Akan tetapi, katalis alkali juga memiliki kekurangan, yaitu dapat terjadi saponifikasi pada produk, terutama terjadi pada minyak atau lemak dengan kadar asam lemak bebas yang lebih dari 0,5% (b/b) atau kadar air di atas 2% (v/v) [31]. Selain itu, transesterifikasi menggunakan katalis kimia memiliki beberapa kelemahan yang tidak dapat dihindari, seperti
Trigliserida
Katalis
11
membutuhkan energi dan konsumsi metanol yang tinggi, menghasilkan sejumlah besar limbah pada saat pemurnian biodiesel dan kesulitan dalam pemulihan gliserol [33]. Sedangkan gliserol masih dapat digunakan untuk industri sabun dan kosmetik [32].
Saat ini, sintesis biodiesel dengan reaksi proses yang baru dan reaktor yang baru juga semakin diteliti, seperti reaksi non-katalitik superkritis, ultrasonik dan microwave, reaktor baru dan sebagainya [11]. Sintesis biodiesel menggunakan reaksi
non-katalitik superkritis memiliki kelebihan, yaitu merupakan metode alternatif yang memecahkan masalah saponifikasi dalam sintesis biodiesel serta menghasilkan tingkat reaksi yang lebih tinggi jika dibandingkan dengan transesterifikasi konvensional. Namun, persyaratan suhu tinggi, tekanan tinggi dan rasio molar tinggi antara alkohol dan minyak membuat proses ini mahal untuk skala industri [33,31]. Selain itu, penggunaan co-solvents seperti n-heksana, benzena, tetrahidrofuran (THF) dan cairan ionik juga diperkenalkan sebagai co-solvents untuk meningkatkan miscibility minyak dan metanol serta untuk meningkatkan aktivitas katalis. Akan
tetapi, meskipun banyak upaya penelitian tersebut, banyak dari metode baru masih memiliki masalah, seperti hasil produk yang rendah, proses canggih, konsumsi energi yang tinggi, biaya tinggi dan bahaya lingkungan [11].
Deep eutectic solvent (DES) baru-baru ini muncul sebagai generasi baru
dalam pelarut ionik dengan biaya rendah. Beberapa penulis juga manyatakan DES sebagai ILs yang baik karena DES memiliki sifat fisik dan sifat pelarut yang sebanding dengan ILs, seperti densitas, viskositas, indeks bias, konduktivitas dan tegangan permukaan [35,36]. Akan tetapi, DES memiliki kelebihan, yaitu tidak beracun, tidak reaktif dengan air dan biodegradable, sehingga berpotensi sebagai pelarut ramah lingkungan yang dapat menggantikan ILs dalam berbagai aplikasi industri karena karakteristik yang sama tersebut [37,3].
1
BAB I
PENDAHULUAN
1.1 Latar Belakang
Pada zaman ini, teknologi yang ramah lingkungan mendapat perhatian penting dalam bidang kimia, hal ini bertujuan untuk melestarikan lingkungan dan mengurangi pengaruh negatif dari penggunaannya. Teknologi yang ramah lingkungan membantu pengurangan penggunaan media yang berbahaya dengan mengendalikan sifat fisik media, seperti suhu dan tekanan [1].
Dengan munculnya teknologi yang ramah lingkungan tersebut, banyak peneliti yang tertarik pada pengembangan pelarut organik yang ramah lingkungan [2]. Selama beberapa dekade terakhir, cairan ionik/ionic liquids (ILs) adalah salah satu pelarut organik ramah lingkungan yang banyak menarik perhatian karena memiliki sifat fisik yang unik, yaitu titik lebur yang rendah, volatilitas yang rendah, stabilitas termal yang tinggi, polaritas tinggi, kemampuan perangsangan yang baik, sesuai untuk berbagai macam kelarutan dan memiliki kemampuan yang baik untuk penggunaan kembali [3,4]. Namun, terdapat masalah dalam penggunaan ILs secara luas, yaitu biaya tinggi, masalah pemurnian, toksisitas dan biodegradabilitas yang rendah [3,2]. Hal ini menyebabkan ILs tidak tersedia untuk skala industri dan biaya sintesisnya yang tinggi menjadi kendala penggunaannya secara luas dalam industri [5,6].
Baru-baru ini, pelarut alternatif untuk ILs telah ditemukan, yaitu deep eutectic solvent (DES) [5]. DES memiliki kelebihan dalam hal biaya dan dampak
lingkungan dibandingkan dengan ILs serta sintesisnya telah banyak dikembangkan [7]. DES disintesis dari campuran garam halida organik dengan suatu senyawa organik sebagai donor ikatan hidrogen/hydrogen bond donor (HBD) yang mampu membentuk ikatan hidrogen dengan ion halida [8]. DES sedang banyak digunakan dalam penelitian dan industri karena potensinya sebagai pelarut yang ramah lingkungan, tidak toksik, tidak reaktif dengan air, biodegradable, titik leleh rendah dan sintesisnya mudah dan murah untuk menghasilkan DES dengan kemurnian yang tinggi [8,9]. DES telah diterapkan di berbagai bidang termasuk sebagai katalis dalam bidang biologi, sintesis organik, pembubaran dan proses ekstraksi, bahan kimia dan
2
elektrokimia [9]. Selain itu, DES saat ini banyak diterapkan dalam bidang sintesis biodiesel, seperti sebagai pelarut dalam penghilangan katalis dari biodiesel [6], sebagai pelarut dalam penghilangan gliserol dari biodiesel [8], sebagai media dalam reaksi enzimatik sintesis biodiesel [10] dan sebagai co-solvent dalam sintesis biodiesel [11].
Shahbaz, dkk.,(2011) telah melaporkan penggunaan DES berbasis choline chloride (ChCl) dan methyltriphenylphosphonium bromide (MTPB) sebagai garam
halida organik serta gliserol, ethylene glycol dan 2,2,2-trifluoroacetamide sebagai donor ikatan hidrogen menjadi pelarut dalam pemurnian biodiesel dari katalis basa KOH. Efisiensi penyisihan KOH rata-rata masing-masing 98,59% dan 97,57% untuk DES ChCl: gliserol dan MTPB: gliserol. Hasil penelitian menunjukkan DES berpotensi digunakan sebagai pelarut untuk pemurnian biodiesel dari katalis kimia yang digunakan [6].
Shahbaz, dkk.,(2012) juga melaporkan penggunaan DES berbasis choline chloride (ChCl) dan methyltriphenylphosphonium bromide (MTPB) sebagai garam
halida organik serta gliserol, ethylene glycol dan 2,2,2-trifluoroacetamide sebagai donor ikatan hidrogen yang digunakan menjadi pelarut dalam pemurnian biodiesel dari gliserol. Hasil penelitian menunjukkan bahwa DES berbasis gliserol sebagai ikatan donor hidrogen memiliki efisiensi removal yang lebih rendah dan DES berbasis phosphunium sebagai garam halida organik jauh lebih efisien [8].
Zhao, dkk.,(2013) juga melaporkan penggunaan DES berbasis choline chloride/gliserol (1:2) dalam reaksi enzimatik sintesis biodiesel. Hasil penelitian
menunjukkan konversi trigliserida mencapai 88 % dalam waktu 24 jam [10].
Gu, dkk.,(2015) juga melaporkan penggunaan DES berbasis choline chloride/gliserol (1:2) menjadi co-solvent dalam sintesis biodiesel menggunakan
NaOH sebagai katalis. Hasil penelitian menunjukkan bahwa fatty acid methyl ester (FAME) dapat diperoleh hingga yield 98 %[11]. Selain itu, penggunaan DES sebagai co-solvent dalam sintesis biodiesel ini memiliki kelebihan, seperti meminimalkan
jumlah penggunaan pelarut volatil (metanol), mempercepat dan memudahkan pemurnian biodiesel yang diperoleh. Dimana, saat ini sumber energi alternatif telah menjadi perhatian besar dan menyebabkan banyak negara di seluruh dunia mendorong penggunaan biodiesel sebagai bahan bakar transportasi [12,13]. Hal
3
tersebut terjadi karena selama dekade terakhir konsumsi minyak dunia meningkat, sehingga dunia berada di ambang krisis energi [12].
Berdasarkan beberapa penggunaan deep eutectic solvent (DES) dalam bidang biodiesel, maka peneliti berminat untuk mengaplikasikan DES berbasis ChCl sebagai garam halida dengan golongan sakarida (glukosa) dan alkohol (etilen glikol) sebagai HBD menjadi co-solvent dalam sintesis biodiesel dari minyak sawit (RBDPO).
1.2 Rumusan Masalah
Baru-baru ini, penggunaan deep eutectic solvent (DES) dalam sintesis biodiesel semakin meningkat, salah satunya sebagai co-solvent. Penggunaan DES sebagai co-solvent dalam sintesis biodiesel ini memiliki kelebihan, seperti meminimalkan jumlah penggunaan pelarut volatil (metanol), mempercepat dan memudahkan pemurnian biodiesel yang diperoleh. Oleh sebab itu, perlu diteliti penggunaan DES berbasis ChCl sebagai garam halida dengan golongan sakarida (glukosa) dan alkohol (etilen glikol) sebagai HBD menjadi co-solvent dalam sintesis biodiesel dari minyak sawit (RBDPO).
1.3 Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah:
1. Mengamati pengaruh konsentrasi DES sebagai co-solvent dalam sintesis biodiesel terhadap yield biodiesel yang diperoleh
2. Mengamati pengaruh jenis HBD DES terhadap yield biodiesel yang diperoleh
1.4 Manfaat Penelitian
Manfaat dari penelitian yang dilakukan adalah:
1. Memberikan alternatif pelarut ramah lingkungan dalam sintesis biodiesel 2. Memberikan informasi mengenai DES berbasis ChCl sebagai garam halida
dengan golongan sakarida (glukosa) dan alkohol (etilen glikol) sebagai HBD dapat digunakan sebagai co-solvent dalam sintesis biodiesel
4 1.5 Ruang Lingkup
1. Penelitian dilakukan di Laboratorium Proses Industri Kimia, Departemen Teknik Kimia, Fakultas Teknik, Universitas Sumatera utara, Medan.
2. Bahan baku yang digunakan adalah deep eutectic solvent (DES) berbasis choline chloride (ChCl) sebagai garam halida dengan glukosa (C6H12O6) dan
etilen glikol (C2H6O2) sebagai HBD, kalium hidroksida (KOH), metanol
(CH3OH) dan minyak sawit (RBDPO).
3. Reaksi transesterifikasi untuk sintesis