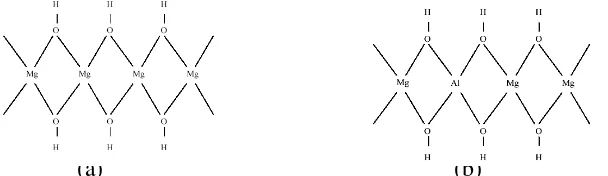Karakterisasi zn/al-hydrotalcite like dalam ragam rasio mol zn/al
Disusun Oleh : ISNANI AZIZ ZULAIKHA
NIM : M0300030
SKRIPSI
Ditulis dan diajukan untuk memenuhi sebagian persyaratan mendapatkan gelar Sarjana Sains Kimia
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS SEBELAS MARET SURAKARTA
2005
HALAMAN PENGESAHAN
Pembimbing I
Dipertahankan di depan Tim Penguji Skripsi pada : Hari : Selasa
Tanggal : 20 Desember 2005
Anggota Tim Penguji :
saya juga tidak terdapat kerja atau pendapat yang pernah ditulis atau diterbitkan oleh orang lain, kecuali yang secara tertulis diacu dalam naskah ini dan disebutkan dalam daftar pustaka.
Surakarta, Desember 2005
ISNANI AZIZ ZULAIKHA
ABSTRAK
Isnani Aziz Zulaikha, 2005. KARAKTERISASI Zn/Al-HYDROTALCITE LIKE
DALAM RAGAM RASIO MOL Zn/Al. Skripsi. Jurusan Kimia. Fakultas MIPA. Universitas Sebelas Maret
Sintesis dilakukan pada kisaran pH 8,5-9,5 dalam variasi rasio mol Zn/Al 1,0 (R1); 2,0 (R2); 3,0 (R3) dan 4,0 (R4) dengan perlakukan hydrothermal pada suhu 800C selama 20 jam. Material hasil sintesis selanjutnya dikarakterisasi dengan X-Ray Diffraction,Differential Thermal Analyzer dan Fourier Transform Infra Red. Penentuan Zn/Al-HTL yang paling berpotensi sebagai sorben didasarkan pada data Surface Area Analyzer dan hasil uji sorpsi terhadap anion chromat.
Hasil penelitian menunjukkan bahwa Zn/Al-HTL berhasil disintesis dengan metode kopresipitasi. Zn/Al-HTL R2 memiliki kristalinitas relatif paling tinggi, kemurnian 82% dan ukuran kristal terbesar (40,77 nm). Kondisi kristal yang baik ini ternyata tidak mendukung Zn/Al-HTL R2 sebagai sorben terbaik karena pada kenyataannya Zn/Al-HTL R2 memiliki luas permukaan yang kecil (16,35 m2/g) dan termasuk material mikropori dengan diameter 1,285 nm. Luas permukaan terbesar dimiliki oleh Zn/Al-HTL R1 (39,79 m2/g) sebagai material mesopori dengan diameter pori 3,58 nm. Hasil Uji sorpsi pada Zn/Al-HTL R1 terhadap anion chromat (31,48%) mendukung Zn/Al-HTL R1 sebagai material hasil sintesis yang paling berpotensi sebagai sorben.
Kata kunci : hydrotalcite like, rasio mol Zn/Al, karakterisasi, luas permukaan, uji sorpsi, sorben.
ABSTRACT
Isnani Aziz Zulaikha, 2005. CHARACTERISATION Zn/Al-HYDROTALCITE IN BEING VARIED THE RATIO MOLE Zn/Al. Thesis. Department of Chemistry. Mathematic and Science Faculty. Sebelas Maret University.
Zn/Al-Hydrotalcite Like (Zn/Al-HTL) in the variation of the ratio mole Zn/Al had been synthesized by direct co-precipitation method. This Material was made by mixing the solution ZnCl2 and AlCl3 in the solution NaCO3. The research was carried out to get Zn/Al-HTL material that most potential as sorbent.
Results of the research showed that Zn/Al-HTL synthesis with co-precipitation method was successful. Zn/Al-HTL R2 had highest relative crystallinity, purity 82% and the measurement of biggest crystal (40,77 nm). The condition for good crystal this evidently did not support Zn/Al-HTL R2 as the best sorbent because in fact Zn/Al-HTL R2 had the the small surface area (16,35 m2/g) and including micro-pores material with the diameter 1,285 nm. The biggest surface area was owned by Zn/Al-HTL R1 (39,79 m2/g) as mesopori material with the diameter of pores 3,58 nm. Results of the sorption test to Zn/Al-HTL R1 against anion chromat (31,48%) supported Zn/Al-HTL R1 as material results of the synthesis that most potential as sorbent.
Key words : hydrotalcite like, ratio mole Zn/Al, characterisation, surface area, sorption test, sorbent
MOTTO
Janganlah bersedih, sesungguhnya Alloh bersama kita
(QS. At-Taubah : 40)
Dan Aku tidak menciptakan jin dan manusia melainkan supaya mereka
PERSEMBAHAN
Bapak dan Ibu tercinta,
Terima kasih banyak atas kasih sayang dan pengorbanannya yang tak
terkira
Mbak Ika atas kebijaksanaannya
Adek-adekku Nur, Sodiq dan Mariyati untuk semuanya
Seluruh keluargaku sekarang dan yang akan datang
Dan teruntuk Calon Suamiku yang bersabar terhadap ketentuan-Nya
KATA PENGANTAR
Puji syukur ke hadirat Rabb semesta alam, atas limpahan kenikmatan dan rahmatNya sehingga penulis dapat menyelesaikan penulisan skripsi. Sholawat dan salam semoga senantiasa terlimpahkan kepada uswah dan qudwah, nabiyulloh Muhammad Saw.
Skripsi ini tidak akan selesai tanpa adanya bantuan dari banyak pihak, karena itu penulis menyampaikan terima kasih kepada :
1. Bapak Drs. Marsusi, M.S. selaku Dekan FMIPA UNS
2. Bapak Dr. Sentot Budi Rahardjo, Ph.D. selaku Ketua Jurusan Kimia. 3. Bapak Drs. Eddy Heraldy, M.Si. selaku Pembimbing I
4. Bapak Abu Masykur, M.Si. selaku Pembimbing II
5. Ibu Triana Kusumaningsih, M.Si. selaku Pembimbing Akademik 6. Bapak Drs. Mudjijono, Ph.D. selaku Ketua Sub Lab Kimia Pusat UNS
7. Ibu Desy Suci Handayani, M.Si. selaku Ketua Laboratorium Kimia FMIPA UNS
8. Bapak-Ibu Dosen Jurusan Kimia UNS
9. Seluruh staf dan laboran Laboratorium Kimia FMIPA dan Laboratorim Pusat MIPA Sub Lab Kimia
12.Semua pihak yang tidak dapat kami sebutkan satu persatu
Semoga Alloh SWT memberikan balasan dengan yang lebih baik. Amin.
Penulis menyadari bahwa banyak kekurangan dalam penulisan skripsi ini. Oleh karena itu, penulis mengharapkan kritik dan saran untuk menyempurnakannya. Namun demikian, penulis berharap semoga karya kecil ini bermanfaat bagi pembaca.
A. Tinjauan Pustaka ... 6
a. Identifikasi Material Hydroalcite ... 12
b. Penentuan Kristalinitas ... 13
c. Penentuan Kemurnian ... 13
d. Penentuan Ukuran Kristal ... 13
e. Penentuan Luas Permukaan ... 14
f. Penentuan Distribusi Ukuran Pori ... 15
g. Analisis Gugus Fungsi ... 17
h. Analisis Molekul H2O ... 18
i. Hubungan Kristalinitas Dengan Faktor Lain ... 19
5. Mekanisme Sorpsi Pada Hydrotalcite ... 19
a. Adsorpsi Permukaan ... 20
b. Pertukaran Anion dan Interkalasi ... 20
6. Pengukuran Kapasitas Sorpsi Hydrotalcite Terhadap Chromat ... 20
B. Kerangka Pemikiran ... 22
C. Hipotesis ... 23
BAB III. METODOLOGI PENELITIAN ... 24
1. Skema Percobaan ... 26
a. Sintesis Zn/Al-Hydrotalcite Like ... 26
b. Karakterisasi Zn/Al-Hydrotalcite Like ... 27
2. Preparasi Larutan Prekursor ... 27
3. Sintesis Zn/Al- Hydrotalcite Like ... 28
4. Karakterisasai Zn/Al-Hydrotalcite Like ... 28
a. Identifikasi material hasil sintesis, penentuan kemurnian, kristalinitas relatif dan ukuran kristal relatif ... 28
b. Penentuan Luas Permukaan, rata-rata jejari pori, dan distribisi ukuran pori Zn/Al-HTL ... 28
c. Analisis Gugus Fungsi ... 29
d. Analisis Molekul H2O ... 29
5. Penentuan Zn/Al-hydrotalcie-Like yang paling berpotensi sebagai sorben ... 29
a. Penentuan Panjang Gelombang Maksimum ... 29
b. Pembuatan Kurva Kalibrasi Larutan Standar ... 29
c. Analisa Sampel ... 30
E. Teknik Pengumpulan dan Analisis Data ... 30
BAB IV. PEMBAHASAN ... 32
A. Sintesis Zn/Al-Hydrotalcite Like………. 32
B. Identifikasi Material Hasil Sintesis ……….. 32
1. Identifikasi kristal dengan XRD ………..…………... 32
2. Identifikasi Gugus Fungsi Material Hasil Sintesis ………. 33
3. Identifikasi Molekul H2O Pada Material Hasil Sintesis ... 34
C. Karakterisasi Zn/Al-Hydrotalcite Like………. 35
1. Pergeseran Nilai d dari Zn/Al-HTL Hasil Sintesis ... 35
2. Penentuan Kemurnian ………. 37
3. Penentuan Kristalinitas Relatif ………. 38
4. Penentuan Ukuran Kristal ……… 39
5. Penentuan Distribusi Pori ………. 40
7. Uji Sorpsi Zn/Al-HTL Hasil Sintesis ………... 42
8. Hubungan Kristalinitas Dengan Faktor lain ... 42
D. Potensi Zn/Al-HydrotalciteLike Sebagai Sorben ... 43
1. Peninjauan dari Data SAA ……….. 43
2. Peninjauan dari Data Uji Sorpsi ... 44
BAB V. KESIMPULAN DAN SARAN ……… 45 A. Kesimpulan ... 45 B. Saran ... 46 DAFTAR PUSTAKA ... 47
LAMPIRAN ... 50
Halaman
Tabel 1. Perbandingan Massa Bahan Awal Pembuatan Zn/Al-HTL ………….. 27
Tabel 2. Data Puncak Produk pada Berbagai Rasio ……… 33
Tabel 3. Perubahan Harga d dari Zn/Al-HTL pada Berbagai Rasio …………... 35
Tabel 4. Tingkat Kemurnian Zn/Al-HTL pada Berbagai Rasio ……….. 37
Tabel 5. Kristalinitas Relatif Zn/Al-HTL pada Berbagai Rasio ………. 38
Tabel 6. Ukuran Kristal Relatif Zn/Al-HTL pada Berbagai Rasio …………... 39
Tabel 7. Distribusi Pori Zn/Al-HTL pada Berbagai Rasio ………. 40
Tabel 8. Luas Permukaan Zn/Al-HTL pada Berbagai Rasio ……….. 41
Tabel 9. Hasil Uji Sorpsi Zn/Al-HTL pada Berbagai Rasio ………... 42
DAFTAR GAMBAR
Gambar 1. (a) Struktur Brucite; (b) Struktur Hydrotalcite... 7
Gambar 2. (a) Struktur Single Layered Hydroxide, (b) Struktur Double Layered Hydroxide………...………..………. 8
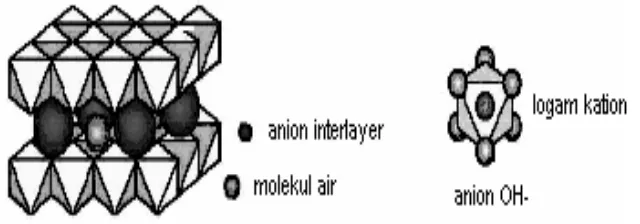
Gambar 3. Sruktur Hydrotalcite dengan Anion Interlayer... 8
Gambar 4. Difraksi Sinar X Pada Bidang Kristal ... 12
Gambar 5. Tahapan Sintesis Zn/Al-HTL ...………... 26
Gambar 6. Tahapan Karakterisasi Zn/Al-HTL ……….. 27
Gambar 7. Data XRD dari Produk pada Berbagai Rasio .………….………… 32
Gambar 8. Spektra IR Produk R1 ...………...………... 33
Gambar 9. Termogram Differential Produk R1………...……….. 34
Gambar 10. Pergeseran Difraktogram XRD Pada (003)………. 36
Gambar 11. Pengotor ZnO Pada Zn/Al-HTL R4 ..……….………… 37
Gambar 12. Luas Permukaan Spesifik Zn/Al-HTL pada Berbagai Rasio ...…. 42
Gambar 13. Hubungan Kristalinitas dengan Faktor Lain ……….. 43
DAFTAR LAMPIRAN Halaman Lampiran 1. Data X-Ray Diffraction Zn/Al-HTL Hasil Sintesis ... 50
Lampiran 3. Perhitungan Tingkat Kemurnian Zn/Al-HTL ... 55
Lampiran 4. Joint Committee Powder on Difraction Standards (JCPDS) ZnO ... 59
Lampiran 5. Perhitungan Ukuran Kristal Zn/Al-HTL ………... 60
Lampiran 6. Data Isoterm Zn/Al-HTL Hasil Sintesis Dari SAA ... 61
Lampiran 7. Data Luas Perrmukaan BET Zn/Al-HTL ... 65
Lampiran 8. Perhitungan Luas Permukaan t-plot Zn/Al-HTL ... 69
Lampiran 9. Data Distribusi Pori Zn/Al-HTL Dengan BJH ... 73
Lampiran 10. Data Distribusi Pori Zn/Al-HTL Dengan DVR ... 77
DAFTAR TABEL LAMPIRAN Halaman Tabel lampiran 1. Perhitungan Tingkat Kemurnian Zn/Al-HTL R1... 55
Tabel lampiran 2. Perhitungan Tingkat Kemurnian Zn/Al-HTL R2... 56
Tabel lampiran 3. Perhitungan Tingkat Kemurnian Zn/Al-HTL R3... 57
Tabel lampiran 4. Perhitungan Tingkat Kemurnian Zn/Al-HTL R4... 58
Tabel lampiran 6. Perhitungan Luas Permukaan t-plot Zn/Al-HTL R1... 69 Tabel lampiran 7. Perhitungan Luas Permukaan t-plot Zn/Al-HTL R2 .... 70 Tabel lampiran 8. Perhitungan Luas Permukaan t-plot Zn/Al-HTL R3 .... 71 Tabel lampiran 9. Perhitungan Luas Permukaan t-plot Zn/Al-HTL R4 ... 72
BAB I
PENDAHULUAN
A. Latar Belakang Masalah
(Heraldy et al, 2005), karenanya kation atau senyawa-senyawa yang bermuatan positif (kationik) dalam perairan akan terikat kuat. Orthman, Zhu, and Lu (2000) melaporkan bahwa penyumbang terbesar dari tercemarnya air tidak lain adalah akibat banyaknya senyawa-senyawa dalam limbah cair maupun sumber air baku alam yang bermuatan negatif (anionik). Oleh karena itu, kurang tepat dan efektif bila sorben yang digunakan adalah sorben yang memiliki lapisan permukaan yang negatif pula. Senyawa anionik akan lebih tepat diserap menggunakan lempung anionik karena memiliki lapisan permukaan positif.
Lempung anionik yang sering dikenal sebagai senyawa serupa hydrotalcite
(hydrotalcite-like) dituliskan sebagai [MII1-xMIIIx(OH)2]x+ [Xm-x/m .nH2O]x- dengan MII dapat berupa Mg2+, Zn2+, Mn2+,...; MIII dapat berupa Al3+, Cr3+, Fe3+…;dan Xm- dapat berupa Cl-, NO3-, CO32-, PO43-,… (Lakraimi, Legrouri, Barong, De Roy, dan Besse; 2000). Hydrotalcite (HT) dalam bentuk naturalnya adalah suatu hidroksikarbonat dari magnesium dan aluminium dengan rumusan [Mg6Al2(OH)16]2+ CO32- .4H2O. Semua kelompok senyawa yang hampir sama dengan HT baik yang natural maupun sintesis disebut Hydrotalcite-Like (HTL). Lempung anionik memiliki struktur lapisan permukaan yang bermuatan positif serta daerah antar-lapisnya yang bermuatan negatif sebagai anion penyeimbang Dengan struktur ini diharapkan spesies anionik yang berukuran besar dapat mengalami sorpsi pada permukaan melalui proses adsorpsi, sedangkan spesies anionik yang berukuran kecil akan masuk ke daerah interlayer yang ukuran porinya terbatas dan kemudian akan mengalami proses pertukaran anionik dengan anion pada daerah interlayer yang memang mudah sekali dipertukarkan (Orthman et al, 2000).
Keberadaan HTL di alam sangat jarang dibandingkan dengan lempung kationik yang melimpah (Bejoy, 2001 dalam Wright, 2002). Meski demikianHTL merupakan salah satu mineral yang menarik, prospektif dan menjanjikan karena dapat disintesis dengan mudah, murah serta menghasilkan material yang dapat berguna dalam berbagai aplikasi (Tong et al, 2003).
pada penelitian ini. Pada metode kopresipitasi, semua kation mengendap secara simultan dalam rasio mol sesuai dengan rasio mol awalnya.
Newman et al (1998) melaporkan bahwa rasio Mg2+/Al3+ pada material HT menentukan jumlah dan susunan muatan anion penyeimbang. Rasio secara khas berada pada kisaran antara 1,0 sampai 4,0. Karbonat adalah satu-satumya anion yang bebas dari kontaminasi karbon dioksida dan segera bergabung terikat kuat pada interlayer (Newman et al, 1998), maka dalam penelitan ini digunakan karbonat sebagai bahan anion interlayernya.
Kühn dan Pöllmann (2004) telah melakukan sintesis Zn-Al-LDH dengan
beberapa anion interlayer. Mereka menyimpulkan bahwa pH optimal sintesis untuk anion interlayer monovalen antara 7,0-7,5, sedangkan untuk anion divalen pada kisaran pH 8,5–9,5.
Hickey (2001) menemukan bahwa perlakuan hydrothermal menunjukkan peningkatan kristalinitas HT yang terbentuk. Proses ini dilakukan dengan menempatkan endapan HT pada suhu sedang selama beberapa jam. Reichle (1985) menemukan kalau pemanasan selama 18 jam pada suhu 650C dan 2000C menghasilkan bentuk kristal yang berbeda. Kühn dan Pöllmann (2004) juga telah melakukan sintesis Zn/Al-HTL-anion
nitrat dengan variasi suhu perlakuan hydrothermal dan mendapatkan kondisi optimum pada pemanasan 800C, sedangkan Wright (2002) melakukan sintesis HT dengan perlakuan pemanasan 800C selama 20 jam.
Lakraimi et al (2000) menyatakan banyak penelitian yang mempelajari kemampuan penukaran dari lempung anionik ini, juga tentang penggunaan HT sebagai sorben untuk anion organik dan anion anorganik. Orthman et al (2000) telah meneliti kemampuan HT dalam menyerap zat warna acid blue 29 sebesar 99% dan mencapai waktu kontak optimum satu jam. Wright (2002) juga mensintesis HT dan diserapkan pada zat warna organik, didapatkan kapasitas sorpsinya 90% dalam waktu kontak optimum dua jam.
B. Perumusan Masalah
1. Identifikasi Masalah
Zn/Al-HTL dapat disintesis dengan beberapa metode, antara lain elektrokimia, sintesis hidrotermal, pertukaran ion maupun sintesis secara langsung dengan kopresipitasi. Rasio mol Zn/Al secara khas berada pada kisaran antara 1,0 sampai 4,0. Anion interlayer pada Zn/Al-HTL dapat berupa monoanionik ataupun dianionik seperti Cl-, CH3COO-, SO42- ataupun CO32-. Adapun perlakuan hydrothermal dalam metode kopresipitasi ini dapat dilakukan pada beberapa variasi suhu dan waktu yang berbeda.
Hasil sintesis dari Zn/Al-HTL dapat dikarakterisasi dengan X-Ray Diffraction
(XRD) untuk identifikasi material hasil, menganalisis kristalinitas relatif, kemurnian dan ukuran kristal relatifnya. Gugus fungsi pada senyawa hasil dapat dianalisis dengan
Fourier Transform Infra Red (FTIR) dan Nuclear Magnetic Resonance (NMR). Termo
Gravimetry-Differential Thermal Analyzer (TG-DTA) dapat digunakan untuk
mengetahui keberadaan molekul H2O dalam kristal. Luas permukaan pada struktur Zn/Al-HTL hasil sintesis dapat diukur dengan Surface Area Analyzer (SAA) atau dengan metode Metilen Biru. Pada aplikasi sorpsi Zn/Al-HTL dapat diterapkan untuk anion organik maupun anion anorganik.
2. Batasan Masalah
Metode sintesis yang digunakan adalah sintesis dengan cara kopresipitasi
secara langsung. Rasio mol Zn/Al dibuat mulai dari 1,0 sampai 4,0 dengan interval
1,0; sedangkan anion interlayer yang digunakan adalah CO32-. Perlakuan
hydrothermal dilakukan pada suhu 80oC selama 20 jam.
Zn/Al-HTL hasil sintesis dikarakterisasi dengan XRD untuk identifikasi
material hasil, menentukan kristalinitas relatif, kemurnian dan ukuran kristal
relatifnya. SAA digunakan untuk menentukan luas permukaan dan distribusi pori
Zn/Al-HTL hasil sintesis, sedangkan gugus fungsinya dianalisis dengan FTIR.
membuktikan bahwa Zn/Al-HTL hasil sintesis dapat berlaku sebagai adsorben
dilakukan uji sorpsi terhadap anion anorganik CrO42- dengan waktu kontak selama 2 jam.
3. Rumusan Masalah
Dari identifikasi dan batasan masalah di atas, maka dapat dirumuskan permasalahan yang diteliti sebagai berikut : a. Apakah material padatan yang terbentuk memang Zn/Al-HTL ?
b. Apakah rasio mol Zn/Al yang berbeda akan memberikan hasil Zn/Al-HTL yang berbeda dalam hal kemurnian, kristalinitas relatif, ukuran kristal relatif, luas permukaan, serta distribusi pori maupun kemampuan sorpsinya ?
c. Pada rasio mol berapakah Zn/Al-HTL memiliki potensi terbaik sebagai sorben ?
C.Tujuan Penelitian
Penelitian ini bertujuan untuk :a. Mensintesis Zn/Al-HTL sebagai salah satu sorben anion. b. Mengetahui karakteristik Zn/Al-HTL hasil sintesis.
c. Mengetahui rasio mol Zn/Al yang paling berpotensi sebagai sorben.
D.Manfaat Penelitian
Dari hasil penelitian ini diharapkan dapat memberikan manfaat sebagai berikut:
a. Memberikan alternatif sorben yang mudah disintesis untuk menyerap anion pencemar lingkungan.
BAB II
LANDASAN TEORI
A.
Tinjauan Pustaka
1. Hydrotalcite
Lempung merupakan salah satu mineral yang banyak dijumpai pada permukaan bumi dan telah digunakan oleh manusia selama berabad-abad. Lempung merupakan material serbaguna yang penggunaannya tersebar dalam berbagai bidang, seperti keramik, material bangunan, katalis, dan adsorben (Scoonheydt, 1991).
Lempung bisa sebagai kationik maupun anionik dengan sifat masing-masing yang sangat berbeda. Lempung kationik lebih banyak ditemukan di alam dan memiliki struktur muatan yang berlawanan dengan struktur muatan lempung anionik atau
Layered Double Hydrokside yang biasa disebut dengan LDH (Hickey, 2001).
Lempung kationik terdiri dari lapisan-lapisan alumino silikat atau magnesio silikat yang bemuatan negatif dan ion positif yang terinterkalasi dalam daerah interlayer, biasanya logam-logam alkali. Material ini memiliki sejumlah sifat diantaranya difusi kationik dan keasaman permukaan sehingga dengan sifat ini lempung kationik dapat digunakan sebagai penukar kation, sorben maupun katalis. Lempung kationik juga bisa dibuat dari lapisan netral yang diubah menjadi lapisan negatif dengan penggantian SiIV dengan MIII atau MIII dengan MII. Muatan negatif dinetralkan dengan ion-ion positif dalam daerah interlayer sehingga material ini disebut kationik (Rajamathi, Thomas, dan Kamath; 2001).
(a) (b) 2. Struktur dan Sifat Hydrotalcite
a. Struktur Hydrotalcite
Hydrotalcite dalam bentuk naturalnya adalah suatu hidroksikarbonat dari magnesium dan aluminium dengan formula [Mg6Al2(OH)16]2+ CO32-. 4H2O. Semua kelompok senyawa yang hampir sama dengan hydrotalcite baik yang natural maupun sintesis disebut dengan senyawa yang serupa hydrotalcite ( Hydrotalcite-like/HTL). Secara umum lempung anionik ini dapat dituliskan [MII1-xMIII(OH)2]x+ [Xm-x/m .nH2O]x- dengan MII dapat berupa Mg2+, Zn2+, Mn2+ dan sebagainya; MIII dapat berupa Al3+, Cr3+, Fe3+…; dan Xm- dapat berupa Cl-, NO3-, CO32-, PO43-,… (Lakraimi, et al; 2000).
Struktur kimia hydrotalcite (HT) didasarkan pada struktur senyawa brucite, Mg(OH)2. Senyawa brucite adalah senyawa yang tersusun atas tatanan heksagonal dari ion hidroksida. Lembaran-lembaran dari situs oktahedral ditempati oleh ion-ion Mg2+, seperti terlihat dalam gambar 1.
Gambar 1. (a) Struktur brucite; (b) Struktur hydrotalcite (Hickey, 2001)
Struktur Layered Single Hydroxide (LSH) seperti Mg(OH)2 (brucite), memiliki lapisan hidroksida dengan ikatan yang sama kuat sehingga dapat
dipisahkan dan diinterkalasi dengan molekul polar yang tidak bermuatan. Adapun struktur LDH terbentuk dengan menggantikan sepertiga bagian dari kation divalen pada lapisan hidroksida logam dengan ion trivalent seperti Al3+, Fe3+, Cr3+.
Gambar 2. (a) Struktur LSH, (b) Struktur LDH (Arrhenius, 2003)
Dengan dasar senyawa brucite ini, beberapa ion Mg2+ pada senyawa HT digantikan oleh aluminium yang bermuatan positif lebih besar tetapi jari-jarinya tidak jauh berbeda. Hal ini menjadikan brucite sebagai jaringan muatan positif.
HT terdiri dari tumpukan lapisan-lapisan hidroksida dari magnesium dan aluminium yang bermuatan positif sehingga membutuhkan anion di antara lapisan tersebut (anion interlayer) untuk menyeimbangkan muatannya (Orthman et al, 2000). Struktur HT dengan anion interlayer ditunjukkan pada Gambar 3.