I. PENDAHULUAN
A. Latar Belakang
Nanoteknologi diyakini akan menjadi suatu konsep teknologi yang akan melahirkan revolusi industri baru di abad 21 (Anonim, 2011). Sekarang ini nanoteknologi memiliki cakupan yang luas di berbagai bidang, seperti kedokteran, elektronik, kimia, lingkungan, kosmetik dan teknologi terapan. Secara garis besar nanoteknologi meliputi tujuh kelompok nanomaterial yakni, nanomaterial berbasis karbon, nanokomposit, nanologam, nanomaterial biologi, nanopolimer, nanoglas, dan nanokeramik (UPM Biomaterial Laboratory, 2005).
atom ditentukan oleh atom-atom di permukaan, karena atom pada permukaanlah yang akan bersentuhan langsung dengan material lain (Ahmad, 2004).
Dari berbagai penelitian nanomaterial yang sudah dikenal diantaranya adalah titanium dioksida atau titania yang merupakan salah satu oksida inorganik dan merupakan bahan semikonduktor yang telah lama menarik perhatian para peneliti. Titanium merupakan logam transisi yang memiliki sifat unsur yang ditentukan oleh konfigurasi elektron pada elektron di subkulit terluar ns dan
subkulit sebelumnya (n-1)d yang menyebabkan kecenderungan perbedaan sifat
periodik. Titanium merupakan logam putih yang sangat bercahaya yang memiliki berat jenis rendah, kekuatan yang baik, mudah dibentuk dan memiliki resistansi korosi yang tinggi (Force and Lynd, 1984). Karena sifatnya yang memiliki tingkat kestabilan dan kereaktifan yang tinggi bila terkena cahaya, maka TiO2 menjadi salah satu fotokatalis yang paling banyak digunakan
hingga dikenal sebagai fotokatalis yang ramah lingkungan (Arif et al; Fatimah,
2005;Rong et al., 2006).
TiO2 memiliki sifat yang unik dan dapat diaplikasikan dalam berbagai
aplikasi fotokatalis. Penelitian khusus tentang fotokatalis TiO2 telah banyak
dilakukan untuk berbagai aplikasi yang sangat menjanjikan mulai dari fotovoltaik dan fotokatalis hingga elektrokromik, sensor titanium dioksida juga digunakan dalam proses seperti pengolahan air limbah industri, self-cleaning
kaca dan cat (Orqun et al., 2007; Gratzel et al., 2003; Mills et al., 1994). Untuk
senyawa lain untuk meningkatkan aktivitas fotokatalisnya. Pada penelitian yang dilakukan Houas, TiO2 digunakan sebagai aplikasi fotokalis komponen
aktif, TiO2 digunakan dalam fasa anatase (Houas et al., 2000).
Dalam penelitian ini akan dilakukan sintesis komposit titania silika. Komposit merupakan kombinasi dari dua atau lebih unsur secara makroskopis yang berbeda bentuk dan komposisi materialnya namun pada dasarnya tidak dapat dipisahkan (Schwartz, 1984). Pada penelitian ini sebagai sumber TiO2
digunakan TiCl3. TiCl3 digunakan karena pada proses sintesis TiO2 dapat
dilakukan dengan mereaksikan TiCl3 dengan air menggunakan reaksi hidrolisis
dengan tingkat keasaman yang tinggi (Cassaignon et al., 2007), harganya yang
relatif lebih murah bila dibandingkan sumber TiO2 lain seperti Ti(OC4H9)4,
titanium tetraisopropoksida Ti(OC3H7)4, titanium sulfat Ti(SO4)2 (Panpae et al., 2007; Senain et al, 2008; Reyes et al., 2008). Sebagai sumber silika akan
digunakan sekam padi yang diekstrak menggunakan metode kimia hingga diperoleh silika sol. SiO2 digunakan untuk meningkatkan aktivitas TiO2
sebagai fotokatalis. Pemakaian silika dari sekam padi ini adalah karena merupakan sumber nabati bukan dari bahan sintesis diharapkan paduan TiO2
(sintesis) dengan SiO2 (nabati) akan memberikan kombinasi yang unik. Silika
dari sekam padi merupakan salah satu material yang memiliki aplikasi yang cukup luas dan terus berkembang hingga penelitian skala nano. Silika umumnya digunakan sebagai bahan elektroda (Wang et al., 2003; Ganjali et al., 2009), membran penukar ion untuk sel bahan bakar (Reichman et al., 2006;
Duvdevani et al., 2006), sebagai fasa diam untuk kolom kromatografi, sebagai
et al., 2003 ), dan sebagai penyangga untuk nanokatalis (Gole and White, 2001;
Kolasinki, 2008).
Komposit titania-silika dapat menjadi katalis dan adsorben yang baik jika titania diaplikasikan dalam fasa anatase dan silika dalam fasa amorf (Balachandaran et al., 2010), fasa anatase pada TiO2 dapat bertahan hingga
suhu 650 °C (Ahmad et al., 2008) dan fasa amorf SiO2 dapat bertahan hingga
750°C (Sembiring, 2007) dalam penelitian ini akan dilakukan kalsinasi pada suhu 500 oC, sehingga dengan keadaan tersebut diharapkan dapat diperoleh
komposit titania-silika dengan kemampuan fotokatalis yang baik, karena sifat amorf silika sekam padi menunjukkan sifat reaktif yang dapat dengan mudah bereaksi sehingga sangat berpotensi untuk dimanfaatkan dalam aplikasi pendukung bahan fotokatalis.
B. Rumusan Masalah
Perumusan masalah dalam penelitian ini adalah untuk mengetahui:
1. Bagaimana cara mensintesis komposit titania silika dengan menggunakan metode sol-gel dari bahan TiCl3 dan silika sekam padi
dalam variasi perbandingan molar.
2. Bagaimana kemampuan bahan sebagai fotokatalis dalam mengurai zat warna.
C. Batasan Masalah
Pada penelitian ini, akan dibatasi pada pembahasan sintesis dan karakterisasi komposit titania silika berbasis TiCl3 dan sekam padi yang
terbentuk dengan variasi perbandingan molar silika menggunakan metode sol-gel dan uji fotokatalis bahan tersebut.
D. Tujuan Penelitian
Tujuan dari penelitian ini adalah:
1. Mengetahui cara mensintesis titania silika dengan menggunakan metode sol-gel.
E. Manfaat Penelitian
Adapun manfaat dari penelitian ini adalah:
1. Dapat mensintesis komposit titania-silika dari bahan TiCl3 dan sekam
padi dengan variasi perbandingan molar dengan metode sol-gel.
2. Memberikan informasi variasi perbandingan molar yang baik untuk digunakan sebagai bahan fotokatalis.
3. Mendapatkan karakteristik TiCl3 dan silika sekam padi untuk didesain
II. TINJAUAN PUSTAKA
A. Titanium Dioksida
TiO2 adalah salah satu material yang banyak diteliti karena sifatnya yang menarik.
Meskipun telah ditemukan lebih dari 200 tahun yang lalu dan telah diteliti sejak 85 tahun yang lalu namun hingga kini penelitian tentang TiO2 masih aktif dan
tetap dikembangkan (Hoffmann et al., 1995). TiO2 ditemukan pertama kalinya
pada tahun 1821, dan tahun 1916 telah dikomersialkan sebagai zat pewarna putih.
Titanium oksida atau yang lebih sering disebut titania adalah keluarga (IV) oksida yang merupakan semikonduktor dengan celah terlarang 3,0 untuk rutil dan 3,2 eV untuk fasa anatase (Hoffmann et al., 1995; Fujishima et al., 1999). Secara kimia
titanium dioksida dituliskan dengan lambang TiO2. Senyawa ini biasa digunakan
sebagai pigmen pada cat tembok (Braun et al., 1992), tabir surya (Zallen and
Moret, 2006) pasta gigi (Yuan and Chen, 2005) solar sel, sensor, perangkat memori serta sebagai fotokatalis.
kerak bumi) 0,6% mineral TiO2 yang utama adalah FeTiO3 (iliminite), CaTiO3
(perovskite). Titanium memiliki indeks bias (n) yang sangat tinggi yaitu 2,4 dalam
bentuk bubuk dan 2,7 dalam bentuk lapisan tipis (Dongsun et al., 2007). Ti juga
tahan terhadap degradasi warna akibat sinar matahari dengan titik lebur 1885˚C. Ada dua bentuk alotropi dan lima isotop alami dari unsur yaitu 46 sampai Ti-50 dengan Ti-48 yang paling banyak terdapat di alam (73,8%) (Merck, 2000).
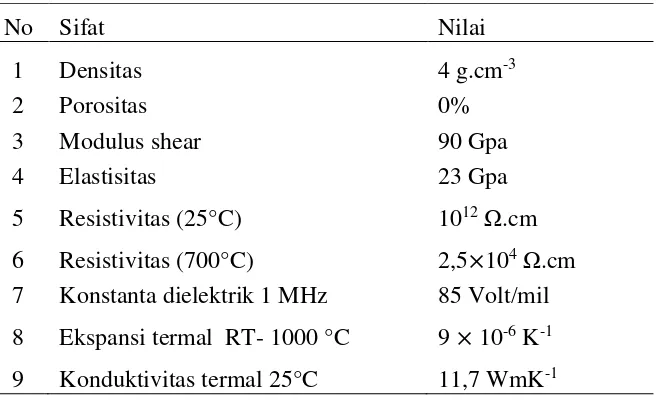
Secara fisika titanium memiliki sifat seperti yang ditunjukkan pada Tabel 2.1. Titanium memiliki massa jenis yang rendah, tahan karat, memiliki biokompabilitas yang tinggi dengan tubuh (Supriyanto dkk., 2007) sehingga dapat digunakan sebagai produk implan dalam tubuh. Kristal TiO2 bersifat asam dan
tidak larut dalam air, asam klorida, asam sulfat encer dan alkohol namun larut dalam asam sulfat pekat dan asam fluorida.
Tabel 2.1. Sifat fisika TiO2
7 Konstanta dielektrik 1 MHz 85 Volt/mil 8 Ekspansi termal RT- 1000 °C 9 × 10-6 K-1
B. Struktur Kristal TiO2
TiO2 dibuat dari ilmenite dan rutil, yang menghasilkan dua bentuk alotropi atau
bentuk struktur kristal yang berbeda dari unsur yang sama, yaitu anatase dan rutil. TiO2 memiliki tiga fasa polymorpik yaitu rutil (tetragonal, 4,120 g/cm3), anatase
(tetragonal, 3,894 g/cm3), dan brookite (4,120 g/cm3 orthorombik). Fasa anatase
dan rutil memiliki struktur kristal tetragonal, namum memiliki perbedaan grup ruang (space group). Anatase memiliki grup ruang IA1/amd dengan empat unit
dalam satu unit sel dan rutile memiliki P42/mnm dengan dua unit TiO2 dalam satu
unit sel (Zhang et al., 1999).
Pada proses fotokatalisis fasa rutil maupun anatase dapat digunakan namun dalam aplikasinya anatase memiliki potensi yang paling besar untuk digunakan sebagai fotokatalis (Tanaka et al., 1991) karena memiliki struktur kisi yang sesuai dengan
aktivitas fotokatalis yang tinggi. Struktur rutil lebih stabil pada suhu tinggi dan anatase pada suhu rendah. Struktur rutil dan anatase dapat digambarkan dengan TiO6 oktahedra, di mana setiap ion Ti4+ dikelilingi oleh enam ion O2-. Struktur
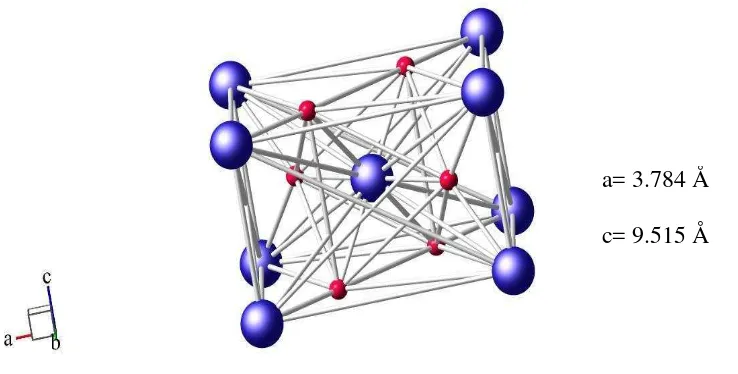
Gambar 2.1. Struktur anatase TiO2 (Howard et al., 1992). Pemodelan kristal
menggunakan Ball and Stick Beta 8.1(BS) (Kang and Ozawa, 2004).
Gambar 2.2. Struktur rutil TiO2 (Kennedy and Stampe, 1991). Pemodelan kristal
menggunakan Ball and Stick Beta 8.1(BS) (Kang and Ozawa, 2004).
Untuk beberapa aplikasi struktur rutil lebih banyak digunakan daripada anatase karena memiliki sifat fisik yang unik misalnya berkilau, keras dan tahan terhadap korosi. Sel satuan pada rutil adalah tetragonal dengan atom-atom logam terletak pada sudut-sudutnya. Struktur rutil dari TiO2 pada umumnya dapat digambarkan
a= 4.593 Å c= 2.959 Å
sebagai suatu distorsi barisan oksida heksagonal tertutup dengan setengah dari oktahedral diduduki oleh atom Ti. Struktur brokit dari TiO2 mengkristal dalam
struktur orthorombik, yang memiliki simetri yang polimorf (memiliki struktur kristal yang tidak teratur) dan akan berubah menjadi fasa rutil pasda temperatur sekitar 750°C (Chen., et al 2008).
Fasa brookite sangat jarang terjadi dalam fasa TiO2, fasa brookite terjadi pada
temperatur 200oC dengan densitas sebesar 4,133 gram/cm3 dan memiliki empat
molekul titania dengan unsur titanium memiliki empat ion positif serta dua ion negatif dari oksigen. Fasa brookite memiliki kesetabilan pada temperatur 200oC
sampai 400oC, dan fasa ini tidak terbentuk sama sekali pada selang temperatur
600oC sampai 800oC (Bakardjieva et al., 2006). Dalam skala nanometer, brookite
dapat digunakan sebagai lapisan tipis dengan mengabsorbsi energi foton dari suatu cahaya. Dengan demikian akan mempercepat peristiwa fotolistrik dengan celah terlarang sebesar 3,5 eV untuk satu molekul titania sehingga fasa ini juga baik digunakan sebagai fotokatalis.
C. Fotokatalis TiO2
Titanium dioksida adalah material yang dikenal luas sebagai fotokatalis didasarkan pada sifat semikonduktornya. Fotokatalisis merupakan suatu proses reaksi katalis dengan bantuan cahaya tampak (visible light) atau UV. Selain itu,
diantara oksida logam yang lain, titanium dioksida dikenal tidak beracun (non toxic), memiliki stabilitas termal cukup tinggi, dan kemampuannya yang dapat
cahaya ultraviolet dengan baik, bersifat inert dalam reaksi, memiliki kemampuan oksidasi yang tinggi dan termasuk zat organik yang sulit terurai dan secara umum TiO2 memiliki aktivitas fotokatalisis yang lebih tinggi dari pada fotokatalisis lain
seperti ZnO, CdS, WO2, dan SnO2 (Okamoto et al., 1985).
Sifat fotokatalitik titanium dioksida pertama kali ditemukan oleh Akira fujishime pada tahun 1967 dan diterbitkan pada tahun 1972 (Fujishime et al.,
1999). Titanium dioksida memiliki potensi untuk digunakan dalam produksi energi sebagai fotokatalis, dapat melakukan hidrolisis yaitu memecah air menjadi hidrogen dan oksigen. Dalam proses fotokatalis, semikonduktor TiO2
membutuhkan serapan energi yang lebih besar dari selang energinya. Aktifitas fotokatalis ini membutuhkan penyerapan sinar ultraviolet (UV) untuk membentuk
dua pasangan elektron dan lubang (hole).
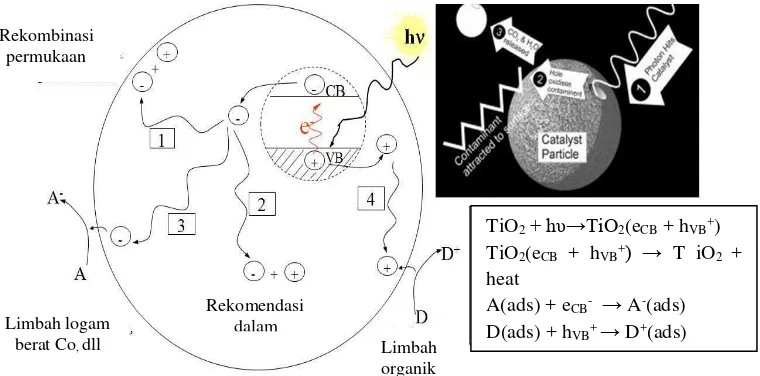
Gambar 2.3. Mekanisme fotokatalis (Banarjee et al., 2006).
Absorpsi foton dan pasangan elektron-lubang serta migrasi elektron dan lubang, (1) dan (2) merupakan proses rekombinasi elektron-lubang pada permukaan, (3) reduksi akseptor elektron, (4) oksidasi donor elektron. Energi absorpsi foton akan mengakibatkan elektron tereksitasi dari pita valensi ke pita konduksi sehingga mengakibatkan transfer elektron ke molekul oksigen membentuk ion radikal superoksida (*O2) dan transfer elektron dari molekul air ke lubang pita valensi
membentuk radikal hidroksil (*OH).
Sebagai fotokatalis yaitu bahan yang berfungsi mempercepat reaksi yang diinduksi oleh cahaya, TiO2 mempunyai struktur semikonduktor yang memiliki
struktur elektronik yang dikarakterisasi oleh adanya pita valensi terisi dan pita konduksi yang kosong. Kedua pita tersebut dipisahkan oleh celah terlarang (band gap energy) sebesar 3,2 eV untuk anatase dan 3,0 eV untuk fasa rutil. TiO2 dalam
diamati pada penelitian terjadi pada pemanasan TiO2 serbuk mulai dari suhu
120oC hingga menjadi fasa anatase sempurna pada 500 oC. Kemudian pemanasan
pada suhu 700 oC mulai terbentuk kristal rutil (Ollis and Elkabi, 1991) dan terjadi
penurunan luas permukaan serta pelemahan aktivitas fotokatalis secara drastis.
Fotokatalis TiO2 dapat menjadi fotodegradasi yang baik untuk penetrasi limbah,
seperti penumbuhan bakteri eschericha coli melalui bantuan sinar fotokatalis yang telah berhasil dilakukan dan hasilnya bakteri tersebut mati (Sunada et al., 2003).
TiO2 mampu memacu reaksi oksidasi pada polutan dalam limbah hingga terurai.
D. Silika (SiO2)
Silika yang memiliki rumus kimia SiO2, sebagian silika besar yang terdapat di
alam adalah pasir atau kwarsa yang merupakan komponen penyususn kerak bumi terbesar. Silika memiliki sejumlah kristal seperti yang ditampilkan pada Tabel 2.2. kecuali pada silika stishovite dan silika fiber, semua bentuk kristal adalah SiO4
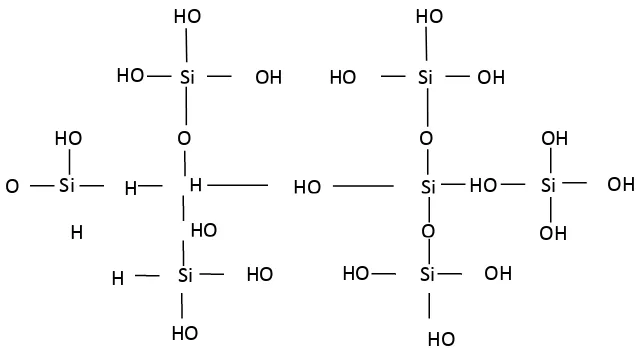
tetrahedral dengan satu atom silika dikelilingi oleh empat atom oksigen, seperti di tunjukkan pada Gambar 2.4. Panjang dari tiap ikatan silikon-oksigen bervariasi
tiap bentuk kristal, misalnya α-quartz memiliki panjang ikatan 161 nm, dimana α
Tabel 2.2. Struktur kristalin silika
No bentuk kristal kelas kristal keterangan
1 α-quartz Rhomboheedral α 3 α-tridymite orhorhombic
4 β-tridymite hexagonal β
-tridymite berubah menjadi α
-cristobalite pada 1470 °C 5 α-cristobalite tetragonal
6 β-critobalite Kubik melebur pada 1705°C 7 Keatite tetragonal tekanan tinggi
8 Coesite monoklinik Keatite
9 Stishovite tetragonal Coesite 10 melanophlogite Kubik
11 Fibrous orthorhombik
12 Faujasite Kubik
Sumber : Holleman dan Wiberg, 2001.
Meskipun silika memiliki rumus kimia sederhana, namun silika memiliki banyak bentuk struktur kristal seperti pada Tabel 2.2 masing-masing dengan karakteristik struktur serta sifat kimia dan fisik sendiri. SiO2 adalah SiO4 tetrahedral, dimana
setiap atom silika terikat pada empat atom oksigen dan setiap atom oksigen terikat pada dua atom silika.
Gambar 2.4. Struktur ikatan tetrahedral SiO2 (Hench and West, 1990).
Silika merupakan bahan kimia yang pemanfaatan dan aplikasinya sangat luas dalam berbagai bidang termasuk elektronik seperti pembuatan bahan semikonduktor, mekanik, medis, dan bahan bangunan. Silika memiliki ketahanan yang baik terhadap abrasi, memiliki stabilitas termal yang tinggi, isolator listrik yang baik tidak mudah larut dalam bahan kimia.
Silika merupakan bahan yang paling berlimpah di bumi, diantaranya dapat diperoleh dari berbagai sumber mineral seperti olivine, zircon, andalucite dan phyllosiloxide (Reigh et al., 1997), Meskipun jumlahnya melimpah namun
sebagian besar silika yang digunakan dalam aplikasi teknologi merupakan silika sintesis seperti yang diperoleh dari bahan nabati seperti ampas tebu (Hanafi dan Nandang, 2010), limbah jagung berupa janggel dan kelobot jagung (Christiawan dan Darmanto, 2010) dan juga dari sekam padi. Silika sintesis memiliki luas permukaan yang lebih tinggi daripada silika alam. Silika nabati memberikan sifat adsorbsi yang lebih baik dan memiliki struktur katalis yang baik sebagai pendukung untuk fotokatalis heterogen. Meskipun silika memiliki rumus kimia yang sederhana SiO2, tapi dapat ditemukan dalam berbagai bentuk dengan
karakteristik masing-masing.
E.Silika Sekam Padi
struktur adsorpsi dan katalis sebagai pendukung terbaik untuk fotokatalis heterogen.
Sekam padi merupakan residu penggilingan padi. Komponen organik yang terkandung dalam sekam padi adalah selulosa (33-34%) lignin (19-47%) dan hemiselulosa (17-26 %) (Nuryono dkk, 2003). Sekam ini memiliki kandungan silika yang tinggi (Anggraini, 2009) dan memiliki kemurnian yang sangat tinggi yaitu sekitar 94,5% (Daifullah et al., 2003). Silika sekam padi memiliki
kereaktifan yang tinggi, sehingga sekam padi sangat berpotensi sebagai sumber pembuatan silika.
Aplikasi silika sebagai material, antara lain sebagai bahan elektroda (Wang et al.,
2003; Ganjali et al., 2009), membran penukar ion untuk sel bahan bakar
(Reichman et al., 2006; Duvdevani et al., 2006), sebagai fasa diam untuk kolom
kromatografi (Chen et al., 2005), sebagai bahan tambal gigi (Xu et al., 2004),
filler untuk polimer (Kim et al., 2003), dan sebagai penyangga untuk nanokatalis
(Gole and White, 2001; Kolasinki, 2008).
F. Nanokomposit Titania Silika
Nanokomposit dapat ditemukan di alam, contohnya adalah kulit tiram dan tulang (Anonim, 2009). Ikatan antar partikel yang terjadi pada material nanokomposit memainkan peran penting dalam peningkatan dan pembatasan sifat material. Partikel-partikel yang berukukuran nano itu mempunyai luas permukaan interaksi yang tinggi. Makin banyak partikel yang berinteraksi, semakin kuat pula material. Inilah yang membuat ikatan antarpartikel makin kuat, sehingga sifat mekanik materialnya bertambah. Namun penambahan partikel-partikel nano tidak selamanya akan meningkatkan sifat mekaniknya. Ada batas optimum yang mana saat dilakukan penambahan, kekuatan material justru makin berkurang.
Pada umumnya material nanokomposit menunjukkan perbedaan sifat mekanik, listrik, optik, elektrokimia, katalis dan struktur yang berbeda dibandingkan dengan material penyusunnya. Dengan mendesain partikel nano dalam komposit memungkinkan untuk meningkatkan sifat katalis dari fotokatalis. Partikel-partikel yang berukuran nano memiliki luas permukaan interaksi yang tinggi. Makin banyak partikel yang berinteraksi, makin tinggi kinerja dari katalis.
Komposit memiliki kekuatan yang dapat diatur (tailorability), tahanan lelah
(fatigue resistance) yang baik, tahan korosi, dan memiliki kekuatan jenis (rasio
Umumnya pada penelitian tujuan pembuatan nanokomposit bukan untuk mendapat sifat katalis tapi untuk tujuan kekuatan bahan. Namun tidak sedikit juga penelitian sebelumnya dengan berbagai metode untuk membuat bahan nanokomposit untuk tujuan sifat katalis diantaranya adalah SiO2-TiO2 yang
padat. Karakteristik dari produk nanokomposit ini baik ukuran pori, muatan permukaan, kekuatan mekanik, dan adsorbsi serta kemampuan katalitiknya tergantung pada keadaan sintesis dan jenis interaksi yang terjadi antara TiO2 dan
SiO2 (Gao and Wachs 1999).
Titania silika merupakan oksida campuran yang mimiliki banyak aplikasi terlebih dibidang katalis baik sebagai katalis sendiri atau sebagai katalis pendukung. Pada komposit titania-silika, material titania merupakan bahan dasar sebagai penguat dan silika sebagai matriks (Liu and Cheng, 1995). Di dalamnya terdapat dua bentuk interaksi yaitu interaksi gaya fisika (seperti gaya Van der Walls) dan ikatan kimia antara Ti-O-Si (Gao and Wachs, 1999). Dalam sintesis nanokomposit titania silika metode preparasi yang paling banyak digunakan adalah hidrolisis sol-gel, koopresipitasi, deposisi uap kimia (CVD), presipitasi, impregnasi.
G. Metode Sol-Gel
Metode sol-gel adalah metode yang banyak digunakan dalam sintesis berbagai bahan keramik (Pierre et al., 2002; Lu et al., 2003 ). Dalam proses kimia, sol
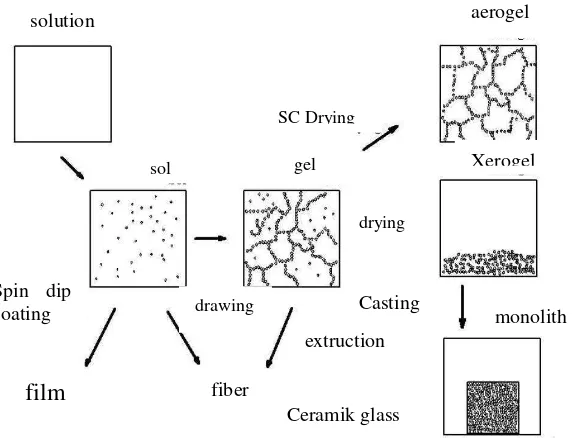
dibentuk melalui hidrolisis dan polimerisasi reaksi dari prekursor, yang biasanya logam garam anorganik atau senyawa organik logam seperti alkoksida logam (Mauritz, 2002). Proses perubahan fasa pada metode sol -gel ditunjukkan pada Gambar 2.5.
Gambar 2.5. Perubahan struktur setelah proses sol-gel (Hench and West,1990).
Sol merupakan koloid yang tersusun atas fasa terdispersi berupa padatan dan fasa pendispersinya berupa cairan (partikel dalam cairan) sementara gel merupakan koloid yang fasa terdispersinya berupa padatan.
Secara umum proses sol-gel didefinisikan sebagai pembentukan jaringan oksida dengan reaksi polikondensasi yang progresif dari molekul prekursor pada medium cair (Indayaningsih dkk., 1999). Dengan proses sol-gel dapat dihasilkan material yang memiliki kemurnian dan kekuatan yang lebih tinggi dibanding bahan yang dibuat dengan metode lainnya. Metode sol-gel dapat dapat digunakan
untuk preparasi bahan seperti struktur berpori, serat tipis, serbuk padat dan film tipis.
H. Mikroskop Elektron
Mikroskop elektron atau lebih dikenal dengan Scanning Electron Microscopy (SEM) pertama kali dipublikasikan fisikawan Jerman Max Knoll pada 1935 dengan mendeskripsikan teori SEM. Pada 1942 tiga ilmuwan Amerika yaitu Vladimir Kosma Zworykin, James Hillier, dan Snijder, benar-benar membangun sebuah mikroskop elektron metode pemindaian dengan resolusi hingga 50 nm atau magnifikasi (perbesaran) 8.000 kali.
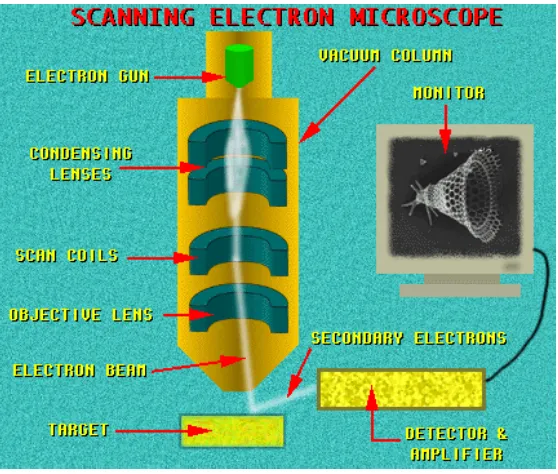
Mikroskop elektron memiliki beberapa perangkat yaitu:
1. Senjata elektron (elektron gun), biasanya berupa filamen yang terbuat dari unsur yang mudah melepas elektron.
2. Lensa untuk elektron, berupa lensa magnetis karena elektron yang bermuatan negatif dapat dibelokkan oleh medan magnet.
3. Sistem vakum, karena elektron sangat kecil dan ringan maka jika ada molekul udara yang berjalan menuju target akan terpencar oleh tumbukan sebelum mengenai target.
Gambar 2.6. Skema prinsip kerja SEM.
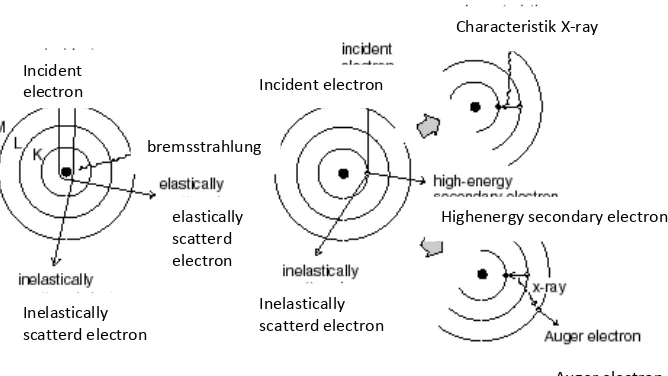
Gambar 2.7. Pantulan elastik dan nonelastik yang dihasilkan oleh sistem SEM.
Dalam aplikasinya saat ini SEM dipadu dengan EDS yaitu suatu alat yang digunakan untuk mendeteksi unsur-unsur yang terkandung pada sampel yang diuji dan memberikan gambaran kemurnian suatu sampel. Pada prinsipnya EDS mendeteksi unsur dalam sampel melalui densitas atau berat molekulnya suatu atom. Setiap atom memiliki densitas yang berbeda yang akan dikarakterisasi EDS yang akan memberikan informasi jenis atom tersebut. Densitas yang lebih besar akan memantulkan lebih banyak elektron sehingga tampak lebih cerah dari atom berdensitas rendah.
Dari pantulan inelastis didapat sinyal elektron sekunder dan karakteristik sinar X sedangkan dari pantulan elastis didapatkan sinyal backscattered electron. Elektron
sekunder menghasilkan topografi dari benda yang dianalisisa, perbedaan permukaan yang tinggi berwarna lebih cerah dari permukaan rendah. Sedangkan
backscattered elektron memberikan perbedaan berat molekul dari atom-atom yang
menyusun permukaan, atom dengan berat molekul tinggi akan berwarna lebih cerah daripada atom dengan berat molekul rendah. Permukaan yang tinggi akan lebih banyak melepaskan elektron dan menghasilkan gambar yang lebih cerah dibandingkan permukaan yang rendah atau datar.
EDS dihasilkan dari karakteristik sinar-X, yaitu dengan menembakkan sinar-X pada posisi yang ingin diketahui komposisinya. Kemudian akan diperoleh puncak tertentu yang mewakili suatu unsur yang terkandung. Dengan EDS bisa membuat pemetaan elemen dengan memberikan warna berbeda-beda dari masing-masing elemen di permukaan bahan. EDS bisa digunakan untuk menganalisis secara kunatitatif dari persentase masing-masing elemen. Prinsip kerja dari SEM-EDS ini adalah sebagai berikut:
1. Sebuah senjata elektron memproduksi elektron dan dipercepat dengan anoda 2. Lensa magnetik memfokuskan elektron menuju ke sampel.
3. Sinar elektron yang terfokus memindai keseluruhan sampel dengan diarahkan oleh koil.
I. Resistivitas
Resistivitas merupakan nilai tahanan jenis pada suatu material yang dapat diketahui dengan melihat hubungan antar hukum ohm dan medan listriknya, pengukuran ini bergantung pada dimensi ruang dari sampel (Soedojo, 2004).
Pengukuran resistivitas dari sampel dapat dihitung menggunakan persamaan 1 berikut:
� =
��� (2.1)Dimana ρ merupakan resistivitas bahan dengan satuan ohmmeter (Ωm), R adalah
tahanan dengan satuan Ω, A adalah luas bahan (m2) dan l adalah panjang kawat
(m).
Pengukuran resistivitas sampel nanokomposit TiO2/SiO2 dilakukan menggunakan
metode pengukuran 4 titik (four probe). Proses pengukuran dilakukan dengan
mengalirkan arus I ke bahan melalui elektroda arus dan tegangan V yang muncul sebagai akibat arus yang dialirkan yang diukur melalui elektroda potensial yang letaknya diantara elektroda arus. Nilai ρ untuk pengukuran ini adalah:
� = �.∆�
� �. �� (2.2)
dengan resistivitas (ρ) satuan ohm centimeter (Ω.cm), k adalah faktor geometri,
ΔV adalah tegangan (volt), I = kuat arus (ampere). Diagram pengukuran
Gambar 2.8. Diagram pengukuran resistivitas sampel.
J. XRD
Sinar-X merupakan gelombang elektromagnetik dengan panjang gelombang 0,5
sampai 2,5 Å (0,05-2,5 nm), panjang gelombang tersebut mendekati jarak antar
atom kristal (Hasen dan Chan, 1992). Sinar-X ditemukan pertama kali oleh
Wilhelm Concard Roentgen pada tahun 1895, di Universitas Wurtzburg, Jerman.
Sinar-X dihasilkan oleh tumbukan antara elektron kecepatan tinggi dengan logam
target. Prinsip analisis XRD didasarkan pada atom-atom dalam suatu struktur
bahan yang didifraksikan pada panjang gelombang tertentu pada sudut-sudut (2θ) tertentu. Identifikasi struktur fasa yang ada pada sampel secara umum dilakukan dengan menggunakan standar melalui data base Join Commite on Powder Diffraction Standar, JCPDS (1996) International Centre for Diffraction Data,
ICPDF (1978). Salah satu contoh perangkat sinar-x dapat dilihat pada gambar 2.9
Sampel
Gambar 2.9. Oxford Xcalibur PD X-Ray Diffractometer-Cu-source.
III. METODE PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini telah dilaksanakan selama empat bulan, yaitu pada bulan Juni 2012 sampai bulan Desember 2012 di Laboratorium Fisika Material, Laboratorium Kimia Instrumentasi dan karakterisasi sampel dilakukan di Laboratorium Kimia Biomassa dan Laboratorium Geologi P3GL Pasteur Bandung.
B. Alat dan Bahan Penelitian
1. Alat
Penelitian ini menggunakan alat percobaan antara lain, beaker glass, neraca,
gelas ukur, labu ukur, beaker glass, kompor listrik, spatula, magnetic strirer,
botol semprot, pipet tetes (1 ml), mortal dan pastle, cawan tahan panas, furnace,
cetakan (die), dan penekan hidrolik.
2. Bahan
Preparasi bahan dalam penelitian ini adalah larutan titanium klorida 15% (TiCl3),
sekam padi, aquades, aquabides, 500 g natrium hidro (III) karbonat (NaHCO3),
C. Prosedur Penelitian
Sintesis TiO2 dilakukan dengan beberapa tahapan yaitu preparasi silika dari sekam
padi, preparasi komposit TiO2/SiO2, pressing, kalsinasi, karakterisasi sampel.
1. Preparasi Silika Sol dari Sekam Padi
Dalam sintesis titania-silika digunakan silika dari sekam padi yang diperoleh dari proses ekstraksi sekam padi untuk memperoleh sol silika. Proses ekstraksi dilakukan menggunakan 1 kg sekam padi yang telah dibersihkan dengan air hingga bersih dan merendamkannya. Kemudian sekam padi yang telah tenggelam diambil sebab kandungan silikanya relatif tinggi dan direndam kembali dengan air panas selama 6 jam. Setelah itu, sekam padi yang telah di pisahkan tersebut di kering anginkan hingga benar-benar kering dan siap untuk diekstraksi. Proses ekstraksi dilakukan dengan melarutkannya sebanyak 50 g dengan larutan KOH
5% di dalam beaker glass dan diaduk hingga sekam padi tenggelam dalam larutan
tersebut. Kemudian campuran tersebut dipanaskan hingga mendidih selama 30 menit menggunakan kompor listrik dan tetap diaduk. Proses pelarutan dan pemanasan berguna untuk memperoleh hasil ekstraksi silika yang optimal, kemudian silika sol disaring dengan menggunakan saringan. Hasil
penyaringannya (silika sol) dituangkan ke dalam beaker glass dan dilakukan
proses penjenuhan (penuaan) selama 24 jam agar memperoleh silika sol (Si(OH)4)
2. Sintesis Nanokomposit Titania Silika
Pada proses sintesis nanokomposit titania-silika dilakukan dengan metode sol-gel
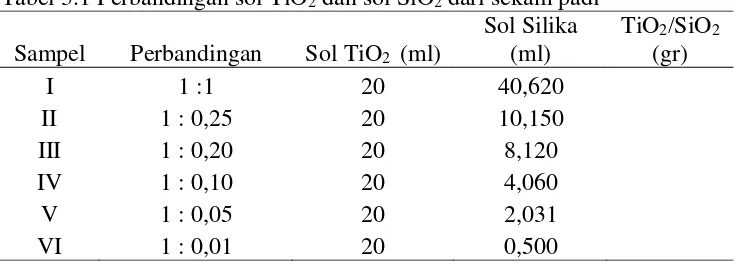
dengan perbandingan molar titania dan silika yang bervariasi yaitu sepeti pada Tabel 3.1. Proses sintesis nanokomposit titania-silika dilakukan dengan meneteskan sol silika yang diekstrak dari silika sekam padi dengan menggunakan pipet tetes yang berukuran 1 ml ke dalam beaker glass yang telah berisiskan TiCl3
15%. Pada saat meneteskan sol silika dibarengi dengan penambahan NaHCO3 4%
sebanyak 20 ml kedalam TiCl3 15%. Kemudian pada setiap sampel dilakukan
proses penuaan selama 24 jam. Kemudian dilakukan penyaringan, pembersihan dengan bayclin, pengeringan, dan penggerusan pada setiap sampel.
Tabel 3.1 Perbandingan sol TiO2 dan sol SiO2 dari sekam padi
Sampel titania yang telah dipreparasikan kemudian dipellet dengan tujuan untuk merubah bentuk sampel dari serbuk menjadi padatan dan berbentuk pellet yang memiliki berat 1 g dengan diameter dan tingginya sebesar 3 mm untuk semua sampel. Pada proses pressing digunakan penekan hidrolik yang dapat diatur
besar tekanannya. Langkah-langkah yang dilakukan dalam proses pressing adalah
berbentuk silinder dengan diameter 1,2 cm dan alat press, kemudian sampel
bubuk sebanyak 1 g dimasukkan ke dalam cetakan (die) dan selanjutnya ditekan
dengan alat pressing dengan skrup yang diputar ke dalam dengan berat beban
sebesar 8 ton. Langkah terakhir adalah mengeluarkan pellet dari cetakan dan alat
pressing dengan cara sekrup diputar keluar untuk membuka alat cetak kemudian
tuas dipompa untuk mengeluarkan pellet dari cetakan.
5. Kalsinasi
Pada proses kalsinasi dilakukan dengan menggunakan furnace Alat ini telah disediakan penyesuaian temperatur yang terkendali secara otomatis dengan sistem digital. Pada penelitian ini, kalsinasi dilakukan pada eman sampel pellet dengan temperatur 500oC dengan waktu penahanan selama 10 jam. Proses kalsinasi
dilakukan sesuai dengan prosedur berikut:
1. Menyiapkan sampel pellet dan sampel serbuk ke dalam cawan tahan panas.
2. Setelah itu memasukkan ke dalam furnace dan menghidupkannya dengan
saklar diputar dengan posisi hidup (ON).
3. Kemudian memberi kenaikkan temperatur sebesar 3oC/menit dan
menahannya selama 10 jam. Setelah selesai,
4. mematikan furnace dengan saklar diputar kembali pada posisi mati (OFF).
D. Karakterisasi Sampel
1 SEM-EDS
Proses karakterisasi SEM-EDS dilakukan untuk melihat dan mengetahui mikrostruktur dari sampel yang terbentuk serta untuk mengetahui komposisi senyawa atau unsur yang terbentuk.
Pada penelitian ini SEM-EDS dilakukan dengan prosedur percobaanya sebagai berikut:
1. Membersihkan sampel pellet dengan ultrasonic cleaner menggunakan
media aceton.
2. Membuka pintu specimen chamber dengan cara mengklik tombol VENT
kemudian gas nitrogen akan keluar dan membiarkannya beberapa menit (dengan tegangan tinggi keadaan “OFF”).
3. Memasukkan sampel pellet ke dalam sarung satu per satu dan menempelkannya ke specimen holder yang mana masing-masing ukuran
sampel pellet akan diatur dengan tinggi ketebalan sekitar 10 mm dengan sebuah pendekatan kunci Allen. Selanjutnya memasukkan sampel pellet ke dalam specimen chamber dan menutup kembali pintu specimen chamber
dengan cara mengklik tombol PUMP.
4. Mendapatkan sebuah gambar morfologi dari sampel pellet dapat dilakukan dengan cara melakukan pre-check (suatu analisis image manual yang dapat
5. Melakukan pengamatan hasil image dari sampel pellet dengan cara
mengatur fokus, kontras, dan kecerahan pada software video control group.
6. Mengeluarkan sample pellet berserta sarungnya di dalam sepecimen chamber kemudian itu menunggu keadaan vakum “OK”, kemudian
mengklik “RPM 60%”.
2. XRD
Pengujian ini dilakukan untuk melihat fasa yang terbentuk pada komposit TiO2
-SiO2 yang disintesis. Alat yang digunakan adalah Shimadzu XD 610, dengan
prosedur sebagai berikut:
1. Mengatur tegangan anoda 30kV dan kuat arus 15 mA.
2. Meletakkan sampel yang akan dianalisis pada kaca dan memasangkan pada sampel holder dengan lilin perekat dan meletakkan pada sampel stand dibagian goniometer.
3. Memasukkan paramater pengukuran pada softwere komputer. 4. Memulai analisi dengan perintah start pada menu komputer.
5. Melihat dan mengambil hasil analisis.
3. Uji Foto Katalis
1. Lima buah beaker glass 1000 mL masing-masing diisi dengan 500 mL aquades
2. kemudian menambahkan methylene blue dengan konsentrasi 0,001 gr dan
distirer hingga homongen.
3. Mengambil 30 ml dari larutan tersebut kedalam gelas kimia.
4. Menambahkan 1 gr sampel TiO2-SiO2 kedalam larutan methylene blue
dan di stirer hingga homogen.
5. Menyinari dengan lampu UV Ultra Vitalux 230 E27 Osram.
6. Mengambil larutan setiap 20 menit penyinaran sebanyak 2 kali pengambilan.
7. Melakukan dengan metode yang sama di bawah sinar matahari pada pukul 10.00- 14.00 WIB.
8. Melakukan uji scan UV-Vis.
4. Uji Resistivitas
Metode yang digunakan dalam pengukuran resistivitas sampel adalah metode 4 titik yang dilakukan sebagai berikut
1. Meletakkan sampel pelet pada papan PCB.
2. Menghubungkan kawat tembaga dengan 4 buah elektroda pada sampel pelet dengan jarak antar kawat (A)
3. Menghubungkan dua elektroda terluar dengan ampere meter untuk mengetahui arus I yang mengalir ke sampel dan dua elektroda dalam
4. Mengukur besarnya arus yang mengalir dan tegangan pada ampere meter dan voltmeter sehingga didapatkan nilai resistivitas masing-masing.
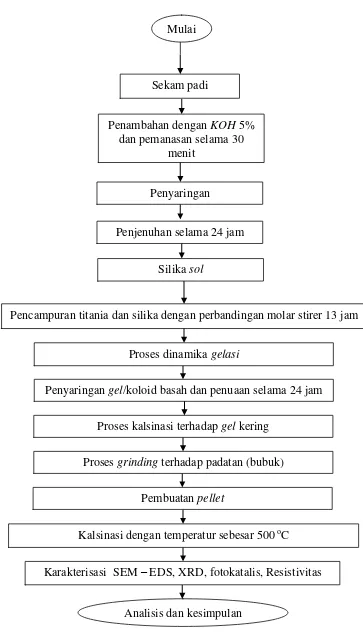
E. Diagram Alir
Gambar 3.1. Diagram alir penelitian. Sekam padi
Mulai
Silika sol
Silika
Analisis dan kesimpulan Penambahan dengan KOH 5%
dan pemanasan selama 30 menit
Penyaringan
Penjenuhan selama 24 jam
Penyaringan gel/koloid basah dan penuaan selama 24 jam
Karakterisasi SEM – EDS, XRD, fotokatalis, Resistivitas Proses kalsinasi terhadap gel kering
Proses grinding terhadap padatan (bubuk)
Kalsinasi dengan temperatur sebesar 500 oC
Pembuatan pellet
Pencampuran titania dan silika dengan perbandingan molar stirer 13 jam
Oleh
VIOLINA SITORUS 0817041059
JURUSAN FISIKA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM UNIVERSITAS LAMPUNG
i Nama : Violina Sitorus
NPM : 0817041059 Jurusan : Fisika
Fakultas : Matematika dan Ilmu Pengetahuan Alam
MENYETUJUI,
1. Pembimbing 2. Ketua Jurusan
Posman Manurung, Ph.D Dr. Yanti Yulianti
ii 1. Tim Penguji
Ketua : Posman Manurung, Ph.D ...
Penguji Bukan Pembimbing : Dra. Dwi Asmi, M.Si., Ph.D ...
2. Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam
Prof . Suharso, Ph.D
iii
SEBAGAI FUNGSI VARIASI PERBANDINGAN MOLAR
Telah dilakukan uji fotokatalis bahan TiO2 yang ditambahkan SiO2 pada zat warna
metylen biru sebagai fungsi perbandingan molar. Preparasi bahan dilakukan dengan metode sol-gel. Setelah serangkaian proses dilakukan kalsinasi pada temperatur 500oC selama 8 jam. Uji difraksi sinar-X (XRD) dengan ulasan
mikroskop elektron (SEM) juga dilakukan untuk analisis struktur dan mikrostruktur, serta dilakukan analisis scan uv-vis dan uji resistivitas untuk mengetahui daya fotokatalisis bahan dan daya hantar listrik dari bahan. Struktur sampel masih menunjukkan masih dominan fasa amorf. Mikrostruktur menunjukkan adanya percampuran aglomerasi dan butir-butir kecil dalam skala nano. Daya urai bahan pada zat warna yang terbaik adalah pada perbandingan 1:0,05 dan 1:0,001. Resistivitas titania silika yang terukur bertut-turut adalah sebesar 8,5 x 104Ω cm, 7,35 x 104 Ω cm, 3,3 x 104 Ω cm, 3,59 x 104 Ω cm 2,16 x
104 Ω cm dan 2,23 x 104 Ω cm. Hasil terbaik yang diperoleh adalah sampel E dan
iv
The photocatalyst test TiO2-SiO2 material for methylene blue as a molar
comparision function has been done. Material preparation using sol-gel method. After the several process calcination at 500oC for 8 hour had been done. The
difraction X-ray and Scanning electron microskopy used for stucture and microstructure analyst, Scanning UV-Vis and resistivity test also was done to knowed photocatalyst degradation and elictrical conductivity. The structure of sample showed the dominant amorph fase. Microstructure showed aglomeration and smallest grains mixtured in a nano scale, then the best comparison as a photocatalyst power for the substance colour showed 1:0,05 and 1:0,001. Resistivity of sampel are 8,5 x 104Ω cm, 7,35 x 104 Ω cm, 3,3 x 104 Ω cm, 3,59 x
104 Ω cm 2,16 x 104 Ω cm dan 2,23 x 104 Ω cm, sample E and F had have the
smallest resistivity. The best ratio of molar for TiO2-SiO2 are E and F sample.
v
Penulis dilahirkan di Tigadolok, Sumatera Utara pada tanggal 16 Januari 1991 Sebagai anak ke dua dari dua bersaudara putri bapak M. Sitorus dan Ibu M. Sihombing.
Penulis menyelesaikan pendidikan Sekolah Dasar pada SD Negeri 091444 Dolok Maraja pada tahun 2002, Sekolah Menengah Pertama di SMPN 1 Jorlang Hataran pada tahun 2005 dan Sekolah Menengah Atas di SMAN 1 Dolok Panribuan pada Tahun 2008. Pada tahun 2008 penulis diterima sebagai mahasiswa Universitas Lampung, Jurusan Fisika, Fakultas Matematika dan Ilmu Pengetahuan Alam melalui jalur SMNPTN.
vii
2010 penulis mendapat hibah PKMP dengan judul “Preparasi Nanosilika Dari
Silika Sekam Padi Dengan Metode Sol-Gel Dinamis Memanfaatkan Energi Ultrasound” dan berhasil mengikuti Pekan Karya Ilmiah Nasional ke XXIII di Bali pada tahun 2010. Pada tahun 2011 penulis menyelesaikan Kerja Praktik Lapangan di Pusat Teknologi Bahan Industri Nuklir, BATAN Serpong Tangerang dengan Judul “Pengembangan Komponen Baterai Mikro Lapisan Tipis
vii
Puji dan syukur penulis panjatkan kehadirat Tuhan Yang Maha Esa, karena penulis menyadari atas berkat dan lindunganNya maka penelitian dan penulisan
skripsi yang berjudul “Uji Fotokatalis Bahan TiO2-SiO2 pada Methylene Blue
sebagai Fungsi Variasi Perbandingan Molar“ dapat terselesaikan. Skripsi ini
merupakan deskripsi yang menginformasikan data-data sesungguhnya yang diperoleh dari penelitian dan merupakan salah satu syarat dalam menyelesaikan program sarjana fisika di Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Lampung.
Penulis berharap penulisan ini dapat bermanfaat untuk penulisan selanjutnya dan disempurnakan pada masa mendatang. Penulis sangat mengharapakan kritik dan saran dari pembaca yang bersifat membangun demi penyempurnaan penulisan laporan ini. Penulis juga berterimakasih kepada semua pihak yang telah membantu baik dalam penelitian dan penulisan skripsi ini dapat terselesaikan.
Bandar Lampung, Januari 2013
viii
memelihara engkau Tidak Untuk Selama-lamanya dibiarkanNya orang benar itu goyah
(Mazmur 55:23)
How You Treat Your Self Is How You Are Inviting The World To Treat You.
Berdoa Sambil Bekerja, dan selalu Bersyukur, Percaya Tuhan Punya Rencana dalam setiap apa yang Kita
ix
Dengan rasa syukur atas kasih dan anugrah Tuhan Yesus Kristus karya kecil ini kupersembahkan untuk Papa Mama dan Abang yang sangat kukasihi semoga damai sejahtra Allah selalu berserta kita...
x
Puji dan syukur penulis panjatkan kehadirat Tuhan Yang Maha Esa, karena penulis menyadari atas berkat dan lindunganNya skripsi ini dapat diselesaikan.
Skripsi dengan judul “Uji Fotokatalis Bahan TiO2-SiO2 pada Methylene Blue
sebagai Fungsi Variasi Perbandingan Molar” adalah salah satu syarat untuk
memperoleh gelar sarjana Sains di Universitas Lampung.
Dalam kesempatan ini penulis mengucapkan terimakasih tiada terbatas kepada: 1. Bapak Posman Manurung sebagai dosen pembimbing, yang telah memberikan bimbingan, saran solusi, pengarahan, motivasi dan bantuan yang begitu besar dalam penyelesaian skripsi ini.
2. Ibu Dra. Dwi Asmi, M.Si, Ph.D sebagai Dosen Penguji yang telah memberikan saran solusi pengarahan dan bantuan yang begitu besar dalam penyelesaian skripsi ini.
3. Bapak Arif Surtono, M.Si dan bapak Amir Supriyanto, M.Si sebagai dosen Pembimbing Akademik penulis yang selalu memberikan motivasi dan bimbingan selama penulis menjadi mahasiswa.
xi Unila.
7. Mas Idam di Laboratorium Kimia Biomassa FMIPA Unila.
8. Bapak Nugroho Susanto dan Pak Sungadi di laboratorium Zoologi FMIPA Unila.
9. Ibu Dwi di Laboratorium P3GL Pasteur Bandung.
10.Revy Susi M partner penelitian, sahabat dan teman berbagi suka dan duka dalam kuliah dan penelitian.
11.Indra Pardede, Pascoli Hanes, Yuant Tiando, Iwan M Ridwan, Rizky Sastia S, Sisca Aprila, Laila Kurniati, Mardalena dan Melinda safitri teman-teman di laboratorium yang selalu membantu dan menemani dalam penelitian.
12.Teman-teman Fisika 2008 yang selalu memberi dukungan dan membantu dalam penelitian
13.Sahabatku terkasih Dessy Natalia dan semua teman-temanku di GIG dan semua orang yang kukasihi yang mungkin tidak dapat disebutkan terimakasih untuk semua semangat dan perhatian dan kebersamaannya.
14.Semua pihak yang terkait dalam penyelesaian penelitian dan skripsi ini.
xiii
I. Resistivitas ... 25
J. XRD ... 26
III. METODE PENELITIAN A. Waktu dan Tempat Penelitian ... 28
B. Alat dan Bahan Penelitian ... 28
C. Prosedur Penelitian ... 29
D. Karakterisasi Sampel ... 32
IV. HASIL DAN PEMBAHSAN A. Hasil Preparasi Sol Silika ... 37
B. Hasil Preparasi Titania Silika ... 38
C. Analisis Struktur Kristal Titania-Silika ... 41
D. Analisis morfologi Permukaan TiO2-SiO2 ... 44
E. Hasil Uji Fotokatalitik TiO2-SiO2 ... 50
F. Hasil Pengukuran Resistivitas Titania-Silika ... 59
V. KESIMPULAN DAN SARAN A. Kesimpulan ... 61
B. Saran ... 62
DAFTAR PUSTAKA ... 63
xiv
Gambar Halaman
2.1. Struktur anatase TiO2 ... 10
2.2. Struktur rutile TiO2 ... 10
2.3. Mekanisme fotokatalis ... 13
2.4. Struktur ikatan tetrahedral SiO2 ... 15
2.5. Perubahan struktur pada proses sol-gel ... 20
2.6. Skema prinsip kerja SEM ... 22
2.7. Pantulan elastik dan nonelastik yang terjadi pada sistem SEM ... 23
2.8. Diagram pengukuran resistivitas sampel ... 26
2.9. Oxford xcalibur PD X-Ray diffraction-Cu-Source ... 27
3.1. Diagram alir penelitian ... 36
4.1. Sol hasil ekstraksi ... 38
4.2. Proses Ekstraksi nanokomposit titania silika (a). Proses stirer nanokomposit titania-silika (b). Nanokomposit titania-silika 10 jam stirer (c). Proses penuaan (d). Gel nanokomposit yang telah dibersihkan (e). Gel titania-silika yang dipanaskan 100˚C... 39
4.3. Sampel pelet titania-silika ... 40
xv
(e). Sampel E dengan perbandingan 1: 0,05 (f). Sampel F dengan
perbandingan 1:0,001 ... 44 4.6. Hasil karakterisasi EDS untuk (a). Sampel A dan (b). Sampel B
titania-silika ... 46 4.7. Hasil karakterisasi EDS untuk (a). Sampel C dan (b). Sampel D
titania-silika ... 48 4.8. Hasil karakterisasi EDS untuk (a). sampel E dan (b). sampel F
titania-tilika ... 49 4. 9. Spektrum absorpsi methylene blue ... 52
4.10. Proses uji aktifitas fotokatalitik TiO2-SiO2 pada penguraian methylene blue dengan aktivasi (a). Lampu UV
(b). Sinar matahari ... 52 4.11. Spektrum absorpsi (a). Spektrum vis 1:1 (b). Spektrum UV 1:1
sampel A ... 54 4.12. Spektrum absorpsi (a). Spektrum vis 1:0,25 (b). Spektrum UV
1:0,25 sampel B ... 54 4.13. Spektrum absorpsi (a). Spektrum vis 1:0,20 (b). Spektrum UV
1:0,20 sampel C ... 55 4.14. Spektrum absorpsi (a). Spektrum vis 1:0,10 (b). Spektrum UV
1:0,10 sampel D ... 56 4.15. Spektrum absorpsi (a). Spektrum vis 1:0.05 (b). Spektrum UV
1:0.05 sampel E ... 57 4.16. Spektrum absorpsi (a). Spektrum vis 1:0.001 (b). Spektrum UV
1:0,001 sampel F ... 57 4.17. Hasil uji resistivitas sample A, B, C, D, D, E dan F ... 59
16
Tabel Halaman 2.1. Sifat fisika TiO2 ... 8
2.2. Struktur kristalin silika ... 15 3.1. Perbandingan sol silika dengan sol TiO2 ... 30