Lampiran 1. Identifikasi Tumbuhan
Lampiran 3. Tumbuhan Pecut Kuda
Tumbuhan Pecut Kuda
Lampiran 4. Hasil Pemeriksaan Mikroskopik
Keterangan:
1. Rambut kelenjar 2. Stomata tipe diasitik 3. Epidermis
4. Lapisan gabus
5. Pembuluh kayu dengan penebalan jala
1
3 2
Lampiran 5. Perhitungan Hasil Pemeriksaan Karakterisasi Simplisia Pecut Kuda dan Ekstrak Pecut Kuda
1. Perhitungan Penetapan Kadar Air a. % Kadar Air = � �
� � � X 100% Berat sampel = 5,011 g
Volume air = 0,4 mL
% Kadar air =
g 5,011 ml 0,4
x 100% = 7,98%
b. Berat sampel = 5,012 g Volume air = 0,5 mL
% Kadar air =
g
5,012
ml
0,5
x 100% = 9,97%
c. Berat sampel = 5,004 g Volume air = 0,4 mL
% Kadar air =
g 5,004 ml 0,4
x 100% = 7,99%
% Kadar air rata-rata =
3
7,99% 9,97%
7,98%
Lampiran 5. (lanjutan)
2. Perhitungan Penetapan Kadar Sari Larut dalam Air % Kadar Sari Larut Dalam Air = � � �
� � � x x 100% a. Berat sampel = 5,0193 g
Berat sari = 0,2042 g
% Kadar sari larut dalam air = , �
, �
x
x 100% = 20,34 %b. Berat sampel = 5,0110 g Berat sari = 0,2021 g
% Kadar sari larut dalam air =
, �, �
x
x 100% = 20,16 %
c. Berat sampel = 5,0187 g Berat sari = 0,201 g
% Kadar sari larut dalam air = , �
, �
x
x 100% = 20,02 %
% Kadar sari larut dalam air rata-rata =
3
20,02% 20,13%
20,34%
Lampiran 5. (lanjutan)
a. Perhitungan Penetapan Kadar Sari Larut dalam Etanol % Kadar Sari Larut Dalam Etanol = � � �
� � � x x 100% a. Berat sampel = 5,0092 g
Berat sari = 0,284 g
% Kadar sari larut dalam etanol = , �
, �
x
x 100% = 29,35 %b. Berat sampel = 5,0010 g Berat sari = 0,294 g
% Kadar sari larut dalam etanol = , �
, �
x
x 100% = 29,34 %c. Berat sampel = 5,0086 g Berat sari = 0, 273 g
% Kadar sari larut dalam etanol = , �
, �
x
x 100% = 27,25 %% Kadar sari larut dalam etanol rata-rata =
3
27,25% 29,34%
28,34%
Lampiran 5. (lanjutan)
b. Perhitungan Penetapan Kadar Abu Total % Kadar Abu Total = � �
� � � X 100% a. Berat sampel = 3,06 g
Berat abu = 0,16 g % Kadar abu total = , �
, � x 100% = 5,22 %
b. Berat sampel = 3,08 g Berat abu = 0,18 g , �
, � x 100% = 5,26 %
% Kadar abu total = , �
, � x 100% = 5,84 %
c. Berat sampel = 3,04 g Berat abu = 0,16 g % Kadar abu total = , �
, � x 100% = 5,26 %
% Kadar abu total rata-rata = 5,44%
3
% 26 , 5 % 5,84 %
Lampiran 5. (lanjutan)
c. Perhitungan Penetapan Kadar Abu Tidak Larut Asam % Kadar Abu Tidak Larut Asam = � �
� � � X 100% a. Berat sampel = 3,06 g
Berat abu = 0,01 g
% Kadar abu tidak larut dalam asam = , �
, � X 100% = 0,32 %
b. Berat sampel = 3,08 g Berat abu = 0,02 g
% Kadar abu tidak larut dalam asam = , �
, � X 100% = 0,64 %
c. Berat sampel = 3,04 g Berat abu = 0,01 g
% Kadar abu tidak larut dalam asam = , �
, � X 100% = 0,32 %
% Kadar abu yang tidak larut dalam asam rata-rata
= 0,42% 3
% 32 , 0 0,64%
0,0,32%
Lampiran 5. (lanjutan)
d. Perhitungan Penetapan Kadar Air Ekstrak % Kadar Air = � �
� � � x 100% a. Berat sampel = 5,091 g ,
, �
x 100% = 3,92 %
Volume air = 0,3 mL % Kadar air = ,
, �
x 100% = 5,89 %
b. Berat sampel = 5,090 g Volume air = 0,4 mL % Kadar air = ,
, �
x 100% = 7,85 %
c. Berat sampel = 5,092 g Volume air = 0,2 mL % Kadar air = ,
, �
x 100% = 3,92 %
% Kadar air rata-rata =
3
3,92% %
85 , 7 %
5,89
Lampiran 5. (Lanjutan)
e. Perhitungan Penetapan Kadar Abu Total Ekstrak % Kadar Abu Total = � �
� � � X 100% a. Berat sampel = 3,04 g
Berat abu = 0,07 g % Kadar abu total = , �
, � X 100% = 2,3 %
b. Berat sampel = 3,03 g
Berat abu = 0,12 g
% Kadar abu total = , �
, � X 100% = 3,96 %
c. Berat sampel = 3,06 g
Berat abu = 0,10 g
% Kadar abu total = , �
, � X 100% = 3,26 %
% Kadar abu total rata-rata
= 3,17% 3
% 26 , 3 3,96%
2,3%
Lampiran 5. (Lanjutan)
f. Perhitungan Penetapan Kadar Abu Tidak Larut Asam Ekstrak % Kadar Sari Larut Dalam Etanol = � � �
� � � x x 100% a. Berat sampel = 3,06 g
Berat abu = 0,02 g , �
, � X 100% = 0,65 %
% Kadar abu tidak larut dalam asam = , �
, � X 100% = 0,65 %
b. Berat sampel = 3,04 g Berat abu = 0,01 g
% Kadar abu tidak larut dalam asam = , �
, � X 100% = 0,32 %
c. Berat sampel = 3,05 g Berat abu = 0,02 g
% Kadar abu tidak larut dalam asam = , �
, � X 100% = 0,65 %
% Kadar abu yang tidak larut dalam asam rata-rata
0,54%
3
% 65 , 0 0,32%
0,65%
Lampiran 6. Alat yang digunakan
Modifikasi alat penampung urin
Lampiran 6. (Lanjutan)
Lampiran 7. Data volume urin (mL), kadar natrim urin (meq/L), kadar kalium dalam urin (meq/L), pH dalam urin setelah pemberian ekstrak dan pembanding (furosemid)
Parameter Kontrol CMC-Na
0,5%
Furosemid 10 mg/kg bb
Ekstrak Crude Etanol Pecut Kuda Dosis100 mg/kg bb Dosis150 mg/kg bb Dosis200 mg/kg bb 1. Volume
urin (mL)
1,5 5,0 2,9 3,2 3,9
0,8 4,5 3,1 3,5 3,7
1.6 3,7 2,5 3,9 3,6
1,2 4,0 2,7 3,3 3,3
1,3 4,1 3,0 3,4 3,6
Rata-rata ± Sd 1,28 ± 0,31 4,26 ± 0,50 2,84 ± 0,24 3,46 ± 0,27 3,62 ± 0,21 2. Kadar
natrium (meq/L)
38,44 94,39 50,25 60,79 73,31
27,68 98,05 49,84 69,82 91,11
34,35 91,22 59,70 63,08 76,28
29,31 94,76 52,55 61,13 73,25
26,51 87,03 60,89 61,85 71,77
Rata-rata ± Sd 31,25 ± 5,00 93,09 ± 4,16 53,64 ± 4,49 63,33 ± 3,73 77,14 ± 7,97 3. Kadar
kalium (meq/L)
15,38 47,08 34,61 35,36 40,06
22,86 51,34 29,42 36,75 41,50
22,46 52,30 30,04 37,65 43,19
20,18 45,40 27,13 30,61 38,47
18,93 52,83 26,93 36,11 39,06
Rata-rata ± Sd 19,96 ± 3,03 49,79 ± 3,3 29,62 ± 3,10 35,29 ± 2,75 40,4 ± 1,91 4. pH urin
(mL)
7,1 7,2 7,0 7,1 7,7
7,0 6,9 6,8 7,6 7,3
7,1 7,4 7,5 7,4 7,3
7,5 7,5 7,3 7,4 7,4
7,2 6,9 7,0 7,3 7,6
Lampiran 8. Contoh dosis perhitungan dosis CMC-Na 0,5% - Perhitungan CMC-Na 0,5% pada tikus 200 mg
x 200g ml
100 g 1
Lampiran 9. Contoh Perhitungan Dosis Furosemid Furosemid yang digunakan mengandung 40 mg
- Menurut FI edisi III, penetapan kadar tablet = 20 tablet, maka diambil 20 tablet furosemid, digerus dan ditimbang berat totalnya = 3415,5 mg - Berat bahan aktif furosemid dalam 20 tablet furosemid adalah
= 40 mg/tab x 20 tab = 800 mg.
- Serbuk tablet furosemid yang digunakan :
mg
=
X, mg X = 42,69 mg ≈ 43 mg
- Volume yang diberikan = x BB Misal BB tikus = 200 g
Lampiran 10. Contoh Perhitungan Dosis Dari Crude Ekstrak Etanol Pecut Kuda
- Untuk dosis 100 mg/kg bb pada tikus 200 g
mg 20 g 200 x g 1000 bb mg/kg 00 1
Volume yang diberikan = x 10ml 2ml
mg 100
mg 20
- Untuk dosis 150 mg/kg bb pada tikus 20
mg 30 g 200 x g 1000 bb mg/kg 150
Volume yang diberikan = x 10ml 2ml
mg 100
mg
30
- Untuk dosis 200 mg/kg bb pada tikus 200 g
mg 40 g 200 x g 1000 bb mg/kg 200
Volume yang diberikan = x 10ml 2ml
mg 100
mg
Lampiran 11. Hasil pengujian AAS dari volume urin untuk kadar Na+ dan K+
No Kelompok pengujian Tikus konsentrasi
Na+ K+
1. Kontrol CMC-Na 0,5%
1 1,7683 1,2000
2 1,2737 1,7854
3 1,5801 1,7524
4 1,3487 1,5741
5 1,2199 1,4772
2. Furosemid dosis 10 mg/kg bb
1 4,3421 3,6729
2 4,5105 4,0048
3 4,1963 4,0800
4 4,3591 3,5415
5 4,0598 4,1211
3. CEEPK dosis 100 mg/kg bb
1 2,3118 2,7003
2 2,2927 2,2952
3 2,5163 2,3436
4 2,4173 2,1168
5 2,3642 2,1013
4. CEEPK dosis 150 mg/kg bb
1 2,7966 2,7584
2 3,2120 2,8670
3 2,9020 2,9368
4 2,8121 2,3882
5 2,8454 2,8166
5. CEEPK dosis 200 mg/kg bb
1 3,3726 3,1248
2 4,1914 3,2372
3 3,5092 3,3690
4 3,3698 3,0007
Lampiran 12. Contoh perhitungan kadar elektrolit (lanjutan)
- Kadar Na = x volume(ml) x Faktor pengenceran sampel
berat
mcg/ml i
konsentras
Pembacaan pada AAS = 1,7683mcg
0,88415
mcg/ml
884,15
5
x
ml
100
x
ml
1
mcg/ml
1,7683
Meq/L = x 1meq
Na BM (mg/ml) Na kadar meq/l 38,44 meq/ml 0,03844 meq 1 x 23 mg/ml
0,88415
- Kadar K = x volume(ml) x Faktor pengenceran
sampel berat
mcg/ml i
konsentras
Pembacaan pada AAS = 1,200 0 mcg
0,6000
mcg/ml
600
5
x
ml
100
x
ml
1
mcg/ml
1,2000
Meq/L = x 1meq
Na BM (mg/ml) K kadar meq/l 15,38 meq/ml 0,0153 meq 1 x 39 mg/ml
Lampiran 13. Data Kalibrasi Natrium Dengan AAS, Perhitungan Persamaan Garis Regresi Dan Koefisien Korelasi
No Konsentrasi (µg/mL) (X)
Absorbansi (Y)
1. 0,0000 -0,0006
2. 1,0000 0,1448
3. 2,0000 0,2736
4. 3,0000 0,4153
5. 4,0000 0,5673
6. 5,0000 0,7067
No X Y XY X² Y²
1 0,0000 -0,0006 0,0000 0,0000 0,00000036
2 1,0000 0,1448 0,1448 1,0000 0,02096704
3 2,0000 0,2736 0,5472 4,0000 0,07485696
4 3,0000 0,4153 1,2459 9,0000 0,17247409
5 4,0000 0,5673 2,2692 16,0000 0,32182929
6 5,0000 0,7067 3,5335 25,0000 0,49942489
∑ X = 15,0000
∑ Y = 2,1071
∑ XY =
7,7406 ∑ X² = 55
∑ Y² = 1,08955263 X =
2,5,0000
Y = 0,351183 a = ∑XY − ∑ Xx ∑ Y / n∑ X²− ∑ X ² / n
a = , ,− − , x ,, / / a = ,
Y = a X + b b = Y – a X
= 0,35118 – (0,14131 x 2,5,0000) = -0,00209
Maka persamaan garis regresinya adalah: Y = 0,14131X - 0,00209 -0,00209
r = ∑XY− [ ∑X ∑Y
n ]
√(∑X²– ∑X ² / n ) ∑Y²− ∑Y ² / n
r = 7,7406 –[
15,0000 2,1071
6 ]
Lampiran 14. Data Kalibrasi Kalium Dengan AAS, Perhitungan Persamaan Garis Regresi Dan Koefisien Korelasi
No Konsentrasi (µg/mL) (X)
Absorbansi (Y)
1. 0,0000 -0,0007
2. 1,0000 0,0502
3. 2,0000 0,1052
4. 3,0000 0,1593
5. 4,0000 0,2051
6. 5,0000 0,2565
No X Y XY X² Y²
1 0,0000 -0,0007 0,0000 0,0000 0,00000049
2 1,0000 0,0502 0,0502 1,0000 0,00252004
3 2,0000 0,1052 0,2104 4,0000 0,01106704
4 3,0000 0,1593 0,4779 9,0000 0,02537649
5 4,0000 0,2051 0,8204 16,0000 0,04206601
6 5,0000 0,2565 1,2825 25,0000 0,06579225
∑ X = 15,0000
∑ Y = 0,7756
∑ XY = 2,8414
∑ Y = 55,0000
∑ Y² = 0,14682232
X = 2,5,0000
Y = 0,12926
a= ∑XY∑X²− ∑− ∑XxX ² / n ∑Y / n
a= 2,841455,0000− 15,0000 x 0,7756− 15,00 2/ 6 / 6 a= 0,05159
Y = a X + b b = Y – a X
= 0,12926 – (0,05159 x 2,5,0000) = 0,00029
Maka persamaan garis regresinya adalah: Y = 0,05159 X + 0,00029
r = ∑XY− [ ∑X ∑Y
n ]
√(∑X²– ∑X ² / n ) ∑Y²− ∑Y ² / n
r = 2,8414 –[
15,0000 0,7756
6 ]
√(55,0000−15,0000 26 )(0,14682232− 0,7756 26 )
r =0,9024
0,9026
lampiran 15. Skema pembutan ekstrak etanol crude pecut kuda dan uji aktivitas diuretik
dimaserasi dengan etanol 96% selama 5 hari
didiamkan selama 2 hari
diuapkan dengan rotary evaporator
dikeringkan
uji aktifitas diuretik
dikondisikan selama 2 minggu
dipuasakan selama ± 18 jam diberi ekstrak crude etanol pecut kuda
Serbuk simplisia pecut kuda
Ekstrak kental etanol ampas
maserat maserat
Ekstrak crude etnaol pecut kuda
Tikus
Urin
Volume Elektrolit
pH urin
Kadar Na+ dan
Lampiran 16. Hasil data statistik ANAVA dengan uji Tukey Hasil perhitungan ANAVA dari volume urin
Sum of
Squares Df
Mean
Square F Sig.
Between Groups
25,626 4 6,407 60,669 ,000
Within Groups 2,112 20 ,106
Total 27,738 24
Hasil volume urin dengan menggunakan perhitungan Tukey kelompok
N
Subset for alpha = 0.05
1 2 3 4
Tukey HSDa
CMC-Na 5 1,2800
CEEPK 100 mg 5 2,8400
CEEPK 150 mg 5 3,4600
CEEPK 200 mg 5 3,6200
Furosemid 10 mg
5 4,2600
Hasil perhitungan kadar natrium secara ANAVA Sum of
Squares Df
Mean
Square F Sig.
Between Groups
10991,067 4 2747,767 98,031 ,000
Within Groups 560,592 20 28,030
Total 11551,658 24
Hasil kadar natrium dari urin dengan menggunakan perhitungan Tukey kelompok
N
Subset for alpha = 0.05
1 2 3 4
Tukey HSDa
CMC-Na 5 31,2580
CEEPK 100 mg 5 53,6460
CEEPK 150 mg 5 63,3340
CEEPK 200 mg 5 77,1440
Furosemid 10 mg
5 93,0900
Hasil perhitungan kadar kalium secara ANAVA Sum of
Squares Df
Mean
Square F Sig.
Between Groups
2518,088 4 629,522 76,420 ,000
Within Groups 164,754 20 8,238
Total 2682,842 24
Hasil kadar kalium dari urin dengan menggunakan perhitungan Tukey Kelompok
N
Subset for alpha = 0.05
1 2 3 4
Tukey HSDa
CMC-Na 5 19,9620
CEEPK 100 mg 5 29,6260
CEEPK 150 mg 5 35,2960
CEEPK 200 mg 5 40,4560
Furosemid 10 mg
5 49,7900
Hasil perhitungan pH urin secara ANAVA Sum of
Squares Df
Mean
Square F Sig.
Between Groups
,412 4 ,103 2,004 ,133
Within Groups 1,028 20 ,051
Total 1,440 24
Hasil pH dari urin dengan menggunakan perhitungan Tukey kelompok
N
Subset for alpha = 0.05
1 Tukey
HSDa
CEEPK 100 mg 5 7,120
CMC-Na 5 7,180
Furosemid 10 mg
5 7,180
CEEPK 150 mg 5 7,360
CEEPK 200 mg 5 7,460
DAFTAR PUSTAKA
Adha, A.C., (2009). Pengaruh Pemberian Ektrak Etanol Daun Alpukat (Persea americana Mill.) Terhadap Aktivitas Diuretik. Skripsi. Fakultas Kedokteran Hewan Institut Pertanian Bogor.
Anna. (2011). Uji Efek Diuretik Ekstrak Etanol 70 % Daun Ceplukan (Physalis angulate L.). Skripsi. Universitas Muhammadiyah Surakarta. Surakarta. Halaman 2.
Arliani, R.L., Bodhi, W., Wullur, A.C. (2015). Uji Efek Diuretik Infusa Daun Sambung Nyawa (Gynura procumbens (Blume) Miq.) Pada Tikus Putih jantan Galur Wistar (Rattus norvegicus). PHARMACON Jurnal Ilmiah Farmasi. Manado: Program Studi Farmasi FMIPA UNSRAT. Vol. 4 No. 4.
Asif, M., Qaisar, J., Atif, M., Amin, M., dan Muhammad, Q. (2014). Diuretic Activity of Achyranthes aspera Linn. Crude Aqueous Extract in Albino Rats. University Of Benin, Benin City, Nigeria. Tropical Journal of Pharmaceutical Research. 13(12): 2039-2045.
Barasi, M. (2007). Nutrition at a Glance. Penerjemah: Hermin. (2009). At a Glance: Ilmu Gizi. Jakarta: Penerbit Erlangga. Halaman 52.
Calista. (2010). Ekstraksi senyawa aktif dari tumbuhan liar pecut kuda sebagai obat herbal antikanker menggunakan metode ramah lingkungan. Skripsi. Universitas Katolik Widya Mandala Surabaya.
Dalimartha, S. (2000). Atlas Tumbuhan Obat Indonesia. Jilid 2 Jakarta: Pustaka Bunda. Halaman 146-148.
Darmono, S. (2011). Buku Ajar Farmakologi Eksperimental. Jakarta: Universitas Indonesia. Halaman 110-115.
Depkes R.I., (1995). Materia Medika Indonesia. Jilid VI. Jakarta : Depkes RI. Halaman. 321,325,333-334,336.
Depkes R.I., (1989). Material Medika Indonesia. Jilid V. Jakarta: Depkes RI. Halaman 455-459.
Depkes RI. (2000). Parameter Standar Umum Ekstrak Tumbuhan Obat. Edisi IV. Jakarta: Departemen Kesehatan RI. Halaman 1-11.
Ditjen POM., (1979). Farmakope Indonesia. Edisi III. Jakarta: Departemen Kesehatan RI. Halaman 33.
Djauhariya, E. (2004). Gulma Berkhasiat Obat. Jakarta: Penebar Swadaya. Halaman 5.
Edwin, K.J. (2012). Diuretik dalam Buku Goodman & Gilman’s Dasar Farkamologi Terapi . Edisi 10 Vol 2. Jakarta: EGC. Halaman 744.
Farnsworth, N.R. (1966). Biologycal and Phytochemical Screening of Plants. Journal of Pharmaceutical Sciense. Volume 55. Pages 262-264.
Frans, A., dan Aminah, D. (2014). Uji Aktivitas Antihipertensi Ekstrak Etanol Daun Legundi (Vitex trifolia L.) Pada Tikus Hipertensi Yang Diinduksi Efinefrin. Skripsi. Medan: Fakultas Farmasi Universitas Sumatera Utara. Halaman 2.
Gandjar, I.G. dan Rohman, A. (2007).Kimia Farmasi Analisis. Yogyakarta: Pustaka Pelajar. Halaman 298-299, 305-312, 319-321.
Guyton dan Hall. (1997). Buku Ajar Fisiologi Kedokteran. Edisi IX. Jakarta: EGC. Halaman 289-345.
Handayani, N. Fatimawali. Dan Gayatri, C. (2014). Uji Efektivitas Diuretik Ekstrak Etanol Biji Salak (Salacca zalacca varietas zalacca (gaert.) Voss) Pada Tikus Putih Jantan Galur Wistar (Rattus norvegicus). Diakses 17 September 2015. Diambil dari: PHARMACON Jurnal Ilmiah Farmasi UNSRAT Vol. 3 No. 3 ISSN 2302-2493. Program Studi Farmasi FMIPA Unsrat Manado, 95115.
Harborne, J.B. (1987). Metode Fitokimia Penuntun Cara Modern Menganalisa Tumbuhan. Edisi II. Penerjemah: Kosasih Padmawinata Dan Iwang Soediro. Bandung: ITB. Halaman 152.
Harris, D.C. (2007). Quantitative Chemical Analysis. USA: W. H. Freeman and Company. Pages. 455.
Hartono, A. (1991). Prinsip Diet Penyakit Ginjal. Jakarta: Penerbit Arcan. Halaman 1-2.
Idu, M., Omogbai, F. Amaechina and J.E. Ataman, (2006). Some Cardovascular Effects Of Aqueous Extract Of The Leaves Of Stachytarpheta jamaicensis (L.) Vahl. Int. J. Pharmacol., 2: 163-165.
Kebamo, S., Eyasu, M., Asfaw, D., dan Bekesho, G. (2015). Evaluation of Diuretic Activity of Different Solvent Fractions of Methanol Extract of Crissa edulis Root Bark in Rats. Ethipia. Medicinal Chemistry. 5(11).
Khopkar, S.M. (1985). Konsep Dasar Kimia Analitik. Jakarta: UI-press. Halaman 275, 283.
Lingga, S.I., Gayatri, C., Widya, A.L. (2014). Uji Efek Ekstrak Etanol Patikan Kebo (Euphorbia hirta linn.) Sebagai Diuretik Pada Tikus Jantan Jantan Galur Wistar (Rattus Norvegicus Sp.). Jurnal Ilmiah Farmasi Vol.3 No.3. Universitas Sam Ratulangi.
Manggung, R.E. (2008). Pengujian Toksisitas Akut Lethal Dose 50 (LD50) Ekstrak Etanol Buah Belimbing Wuluh (Avverhoa bilimbi L) Pada Mencit (Mus musculus). Skripsi. Fakultas Kedokteran Hewan. Institut Pertanian Bogor.
Mukrima. (2008). Uji Efek Antifungi Ekstrak n-Butanol Akar Pecut Kuda Terhadap Candida Albicans dan Analisa KLT- Bioautografi. Skripsi. Fakultas MIPA, Universitas Pancasakti, Makassar
Mutaqqin, A., dan Kumala, S. (2011). Asuhan Keperawatan Gangguan Sistem Perkemihan. Jakarta: Salemba Medika. Halaman 25-26.
Nafrialdi. (2007). Diuretik dan Antidiuretik dalam Buku Farmakolgi dan Terapi. Jakarta: Badan Penerbit FK UI. Halaman 389,392,402.
Neal, M.J. (2006). At a Glance Famakologi Medis. Edisi V. Jakarta: Penerbit Erlangga. Halaman 34-35.
Mycek, M.J., Richard, A. H., dan Pamela, C.C. (2001). Farmakologi Ulasan Bergambar. Edisi II. Alih Bahasa: Azwar Agoes. Jakarta: Widya Medika. Halaman 226-236.
O’Callaghan, C. (2006). At a Glance Sistem Ginjal. Edisi II. Jakarta: Penerbit
Erlangga. Halaman 12-13.
Parmar, N.S., dan Prakash, S. (2006). Screening Methods in Pharmacology. Kawali: Institute of Pharmacheutical Science and Technology. Halaman 241-245.
Siswandono, Bambang S. 1995. Kimia Medisinal. Surabaya : Airlangga University Press. Halaman 222, 239-243.
Standarisasi National Indonesia. (2007). Cara Uji Kadar Logam Berat dalam Spesimen Manusia dangan Metode AAS. Surabaya: Balai Besar Laboratorium Kesehatan. Halaman 2-4.
Suratman, Listyawati S, Sutarno. (2003). Sifat Fisik Dan Kandungan Nacl Urin Tikus Jantan (Rattus norvegicus L.) Jantan Setelah Pemberian Ekstrak Rimpang Alang-alang (Imperata Cylindrica L.) Secara Oral. Biofarmasi 1 (1): 7-12, ISSN: 1693-2242. Jurusan Biologi FMIPA Universitas Sebelas Maret. Surakarta 57126.
Syamsuni, H.A. (2006). Ilmu Resep. Jakarta: Penerbit Buku Kedokteran EGC. Halaman 263-264.
Thomson, A.D., dan Cotton, R.E. (1997). Catatan Kuliah Patologi. Di terjemahkan oleh Maulani R.F. Jakarta: Buku Kedokteran EGC. Halaman 289.
Venkatesh, K., Upendra, R., Kiranmayi, G., Narasimha, N., Mukharjee, N., Vinay, V., Phanindra, K. (2013). Phytochemical Screening And Evaluation Of Diuretic Activity Of Ethanolic And Chloroform Extracts Of Mussaenda Erythrophylla In Rats. Andhra Pradesh, India. Diambil dari: International Journal Of Biological & Pharmaceutical Research; 4(1): 8-10.
BAB III
METODE PENELITIAN
Penelitian ini bersifat eksperimental yang terdiri dari beberapa tahapan meliputi: pengumpulan pecut kuda, identifikasi tumbuhan, pembuatan simplisia pecut kuda, karakterisasi simplisia, skrining fitokimia, pembuatan crude ekstrak etanol pecut kuda, dan pengujian efek diuretik. Data yang diperoleh di analisis secara ANAVA (analisis variansi) dan dilanjutkan dengan uji beda rata-rata Tukey menggunakan program statistical and product service solution (SPSS) 18.0.
3.1 Alat dan Bahan 3.1.1 Alat-alat
Alat-alat yang digunakan dalam penelitian ini adalah alat-alat gelas laboratorium, neraca listrik, pH meter, timbangan hewan, rotary evaporator, mortir dan stamper, oral sonde, seperangkat alat pengujian diuresis berupa modifikasi kandang metabolik, Spektrofotometer Serapan Atom (SSA).
3.1.2 Bahan-bahan
Bahan tumbuhan yang digunakan dalam penelitian ini adalah herba pecut kuda. Bahan kimia yang digunakan kecuali dinyatakan lain adalah berkualitas pro analisis yaitu etanol 96%, karboksi metil selulosa natrium (CMC-Na, saline, aqua bidestilata, baku kalium, baku natrium, dan tablet furosemid).
3.1.3 Pengumpulan Herba Pecut Kuda
ini adalah herba pecut kuda yang diambil dari daerah Bukit Simarsayang, Kota Padang Sidimpuan, Provinsi Sumatera Utara.
3.2 Identifikasi Tumbuhan
Identifikasi tumbuhan dilakukan oleh Lembaga Ilmu Pengetahuan Indonesia (LIPI) Pusat Penelitian dan Pengembangan Biologi Bogor. Hasil identifikasi tumbuhan dapat dilihat pada lampiran 1 halaman 52.
3.3 Pembuatan Simplisia
Tumbuhan yang digunakan pada penelitian ini adalah herba pecut kuda yang masih segar. Tumbuhan dicuci hingga bersih kemudian ditiriskan, dirajang kasar dan ditimbang, diperoleh berat basah sebesar 2,1 kg. Selanjutnya herba pecut kuda tersebut dikeringkan dalam lemari pengering pada temperatur ± 40º C sampai kering. Simplisia yang telah kering diblender menjadi serbuk, ditimbang dan diperoleh berat simplisia sebesar 600 g. Lalu dimasukkan ke dalam wadah botol plastik bertutup rapat dan disimpan pada suhu kamar.
3.4 Pembuatan Larutan Pereaksi
3.4.1 Pereaksi Bouchardat
Sebanyak 4 g kalium iodida ditimbang, dilarutkan dalam air suling secukupnya, kemudian sebanyak 2 g iodium dilarutkan dalam larutan kalium iodida, setelah larut dicukupkan volume dengan air suling hingga 100 mL.
3.4.2 Pereaksi Dragendroff
Sebanyak 8 g bismuth (III) nitrat dilarutkan dalam 20 mL asam nitrat pekat, pada wadah lain sebanyak 27,2 g kalium iodida dilarutkan dalam 50 mL air suling, kemudian kedua larutan dicampurkan dan didiamkan sampai memisah sempurna. Selanjutnya diambil lapisan jernih dan diencerkan dengan air suling hingga 100 mL.
3.4.3 Pereaksi Mayer
Sebanyak 1,3596 g raksa (II) klorida ditimbang, kemudian dilarutkan dalam air suling hingga 60 mL. pada wadah lain ditimbang 5 g kalium iodida lalu dilarutkan dalam 10 mL air suling, kemudian keduanya dicampur dan ditambahkan air suling hingga 100 mL.
3.4.4 Pereaksi besi (III) klorida 1% b/v
Sebanyak 1 g besi (III) klorida ditimbang, kemudian dilarutkan dengan air hingga 100 mL.
3.4.5 Pereaksi Molish
Sebanyak 3 g α-naftol ditimbang, kemudian dilarutkan dalam asam nitrat
0,5 N hingga 100 mL.
3.4.6 Pereaksi timbal (II) asetat 0,4 M
3.4.7 Pereaksi asam klorida 2 N
Sebanyak 1,7 mL asam klorida pekat diencerkan dalam air suling hingga 100 mL.
3.4.8 Pereaksi Natrium Hidroksida 2 N
Sebanyak 8,002 g kristal natrium hidroksida ditimbang, kemudian dilarutkan dalam air suling hingga 100 mL
3.4.9 Pereaksi Lieberman-Bouchardat
Sebanyak 5 mL asam asetat anhidrat dicampurkan dengan 5 mL asam sulfat pekat, lalu tambahkan 50 mL etanol kedalam campuran tersebut.
3.4.10 Pereaksi Kloralhidrat
Sebanyak 50 g kloralhidrat dilarutkan dalam 20 mL air suling.
3.5 Karakterisasi Simplisia
Pemeriksaan karakterisasi simplisia meliputi pemeriksaan makroskopik dan mikroskopik, penetapan kadar air, penetapan kadar sari larut dalam air, penetapan kadar sari larut dalam etanol, penetapan kadar abu total, penetapan kadar abu tidak larut dalam asam (Depkes R.I, 1995).
3.5.1 Pemeriksaan Makroskopik dan Organoleptik
Pemeriksaan makroskopik dan organoleptik dilakukan dengan mengamati bentuk, rasa, bau, dan warna dari simplisia herba pecut kuda.
3.5.2 Pemeriksaan Mikroskopik
kloralhidrat dan ditutup dengan kaca penutup kemudian diamati dibawah mikroskop.
3.5.3 Penetapan Kadar Air
Penetapan kadar air dilakukan dengan metode Azeotropi (destilasi toluen). Alat terdiri dari alas bulat 500 mL, alat penampung, pendingin, tabung penyambung dan tabung penerima 10 mL. Caranya:
a. penjenuhan toluene
Sebanyak 200 mL toluena dan 2 mL air suling dimasukkan ke dalam labu alas bulat, dipasang alat penampung dan pendingin, kemudian didestilasi selama 2 jam. Destilasi dihentikan dan dibiarkan dingin selama 30 menit, kemudian volume air dalam tabung penerima dibaca dengan ketelitian 0,05 mL (WHO, 1992).
b. penetapan kadar air simplisia
3.5.4 Penetapan Kadar Sari Larut Air
Sebanyak 5 g serbuk yang telah dikeringkan, dimaserasi selama 24 jam dalam 100 mL air-kloroform (2,5 mL kloroform dalam air suling 1000 mL) dalam labu bersumbat sambil sesekali dikocok selama 6 jam pertama, dibiarkan selama 18 jam, kemudian disaring. Diuapkan 20 mL filtrat sampai kering dalam cawan penguap yang berdasar rata yang telah dipanaskan dan ditara. Sisa dipanaskan pada suhu 105oC sampai bobot tetap. Hitung kadar dalam persen sari yang larut dalam air dihitung terhadap bahan yang telah dikeringkan diudara (Depkes R.I, 1995).
3.5.5 Penetapan Kadar Sari Larut Etanol
Sebanyak 5 g serbuk simplisia yang telah dikeringkan dimasersi selama 24 jam dalam 100 mL etanol 96% dalam labu bersumbat sambil dikocok sesekali selama 6 jam pertama, kemudian dibiarkan selama 18 jam. Kemudian disaring, 20 mL filtrat diuapkan sampai kering dalam cawan dangkal berdasarkan rata yang telah ditara dan sisanya dipanaskan pada suhu 105oC sampai bobot tetap. Kadar sari larut dalam etanol dihitung terhadap bahan yang telah dikeringkan diudara (Depkes R.I, 1995).
3.5.6 Penetapan Kadar Abu Total
3.5.7 Penetapan Kadar Abu Tidak Larut Asam
Abu yang telah diperoleh dalam penetapan abu didinginkan dengan 25 mL asam klorida encer selama 5 menit, bagian yang tidak larut dalam asam dikumpulkan, disaring dengan kertas saring bebas abu, cuci dengan air panas, dipijarkan sampai bobot tetap, kemudian didinginkan dan ditimbang. Kadar abu yang tidak larut asam dihitung terhadap bobot yang dikeringkan diudara (Depkes R.I, 1995).
3.6 Skrining Fitokimia
Skrining fitokimia serbuk simplisia dan crude ekstrak etanol pecut kuda meliputi: pemeriksaan senyawa golongan alkaloid, flavanoid, glikosida, tanin, saponin dan steroid/triterpenoid
3.6.1 Pemeriksaan Alkaloid
Serbuk simplisia dan crude ekstrak etanol pecut kuda ditimbang sebanyak 0,5 g kemudian ditambahkan 1 mL asam klorida 2 N dan 9 mL air suling, dipanaskan diatas penangas air selama 2 menit, didinginkan dan disaring. Filtrat yang diperoleh dipakai untuk uji alkaloida: diambil 3 tabung reaksi, lalu kedalamnya dimasukkan 0,5 mL filtrat.
Pada masing-masing tabung reaksi:
1. Tabung 1 ditambahkan 2 tetes pereaksi Mayer 2. Tabung 2 ditambahkan 2 tetes pereaksi Bauchardat 3. Tabung 3 ditambahkan 2 tetes pereaksi Dragendorff
3.6.2 Pemeriksaan Flavonoid
Sebanyak 10 g simplisia dan crude ekstrak etanol pecut kuda masing-masing ditambahkan 10 mL air panas, dididihkan selama 5 menit dan disaring dalam keadaan panas, ke dalam 5 mL filtrat ditambahkan 0,1 g serbuk magnesium dan 1 mL asam klorida pekat dan 2 mL amil alkohol, dikocok dan dibiarkan memisah. Flavonoida positif jika warna merah atau kuning atau jingga pada lapisan amil alkohol (Farnsworth, 1966).
3.6.3 Pemeriksaan Glikosida
Simplisia dan crude ekstrak etanol pecut kuda masing-masing ditimbang sebanyak 3 g, lalu disari dengan 30 mL campuran etanol 96% dengan air (7:3) dan 10 mL asam klorida 2 N, direfluks selama 2 jam, didinginkan dan disaring. Diambil 20 mL filtrat ditambahkan 25 mL air suling dan 25 mL timbal (II) asetat 0,4 M, dikocok, didiamkan 5 menit lalu disaring. Filtrat disari dengan 20 mL campuran isopropil dan kloroform (2:3), dilakukan berulang kali sebanyak 3 kali. Sari air dikumpulkan dan diuapkan pada temperatur tidak lebih dari 50º C. Sisanya dilarutkan dalam 2 mL air dan 5 tetes pereaksi Molish. Kemudian secara perlahan-lahan ditambahkan 2 mL asam sulfat pekat melalui dinding tabung, terbentuknya cincin berwarna ungu pada batas kedua cairan menunjukkan ikatan gula (Depkes, R.I. 1995).
3.6.4 Pemeriksaan Saponin
dengan penambahan 1 tetes asam klorida 2 N menunjukkan adanya saponin (Depkes, R.I. 1995).
3.6.5 Pemeriksaan Steroida/Triterpenoid
Sebanyak 1 g serbuk simplisia dan crude ekstrak etanol pecut kuda dimaserasi dengan 20 mL eter selama 2 jam, disaring, setelah itu filtrate yang diperoleh diuapkan dengan menggunakan cawan penguap dan pada sisanya ditambahkan 2 tetes pereaksi Lieberman-Bourchad. Apabila terbentuk warna ungu atau merah yang berubah menjadi biru atau hijau menunjukkan adanya steroid/triterpenoid yang terkandung di dalam simplisia atau ekstrak (Harbone, 1987).
3.6.6 Pemeriksaan Tanin
Sebanyak 0,5 g sampel disari dengan 10 mL air suling, disaring lalu filtratnya diencerkan dengan air suling sampai tidak berwarna. Diambil 2 mL larutan lalu ditambahkan 1 sampai 2 tetes pereaksi besi (III) klorida. Terjadi warna biru atau hijau kehitaman menunjukkan adanya tanin (Farnsworth, 1966).
3.7 Pembuatan Ekstrak Herba Pecut Kuda
dienaptuangkan. Maserat yang diperoleh diuapkan dengan menggunaka rotary evaporator ± 40oC kemudian dipekatkan (Ditjen POM, 1979).
3.8 Penyiapan Bahan Uji, Obat Pembanding, dan Kontrol
Crude ekstrak etanol pecut kuda dibuat dalam bentuk suspensi
menggunakan CMC-Na 0,5%. Obat pembanding furosemid dibuat dalam bentuk suspensi menggunakan CMC-Na 0,5%. Kontrol negatif yang digunakan adalah suspensi CMC-Na 0,5%.
3.8.1 Pembuatan Suspensi CMC Na 0,5%
Sebanyak 0,5 g CMC-Na ditaburkan dalam lumpang yang berisi 10 mL air suling panas. Didiamkan selama 15 menit lalu digerus hingga diperoleh massa yang transparan, digerus sampai homogen, diencerkan dengan air suling, dihomogenkan dan dimasukkan ke labu tentukur 100 mL, dicukupkan volumenya dengan air suling hingga garis tanda.
3.8.2 Pembuatan Suspensi Furosemid
Tablet furosemid digerus dan diambil 43 mg dimasukkan kedalam lumpang dan ditambahkan suspensi CMC-Na 0,5 % sedikit demi sedikit sambil digerus sampai homogen, lalu dimasukkan kedalam labu tentukur 10 mL, kemudian dicukupkan volumenya hingga 10 mL.
3.9 Penyiapan Hewan Percobaan
minuman yang sama. Setelah satu minggu, dipilih tikus yang sehat ditandai dengan berat badan yang stabil atau meningkat.
3.10 Pengujian Efek Diuretik Crude Ekstrak Etanol Pecut Kuda
Hewan yang digunakan sebanyak 25 ekor tikus jantan yang setiap kelompok terdiri dari 5 ekor tikus. Tikus dipuasakan tidak diberi makan selama ±18 jam dengan tetap diberi minum, kemudian bobot tikus ditimbang. Tikus diberikan NaCl 0,9 % secara oral dengan dosis 20 mL/kg bb. Masing-masing tikus diberi perlakuan yang dibagi menjadi 5 kelompok yaitu kelompok kontrol negatif diberikan CMC-Na 0,5%, kontrol pembanding diberikan furosemid 10 mg/kg bb, dan pemberian bahan obat crude ekstrak etanol pecut kuda dosis 100, 150, 200 mg/kg bb. Tikus diletakkan di dalam kandang metabolik yang telah dimodifikasi. Volume urin yang diekskresikan dicatat setiap jam dan akumulasinya selama 5 jam sebagai urin total, diukur pH urin, serta ditentukan kadar elektrolit natrium dan kalium dalam urin menggunakan Spektrofotometer Serapan Atom (Atomic Absorbsion Spectrofotometer/ AAS).
3.11 Pengukuran pH Urin
dicelupkan dalam larutan tersebut. Dibiarkan alat menunjukkan harga pH sampai konstan. Angka yang ditunjukkan pH meter merupakan pH sampel.
3.12 Pembuatan Kurva Kalibrasi
3.12.1 Pembuatan Kurva Kalibrasi Natrium
Larutan baku natrium (konsentrasi 1000 µg/mL) dipipet sebanyak 2,5 mL, dimasukkan ke dalam labu tentukur 50 mL dan dicukupkan hingga garis tanda dengan akuabides (konsentrasi 50 µg/mL).
Larutan untuk kurva kalibrasi natrium dibuat dengan memipet (0,5; 1; 1,5; 2; 2,5) mL dari larutan baku 50 µg/mL, masing-masing dimasukkan ke dalam labu tentukur 25 mL dan dicukupkan hingga garis tanda dengan akuabides (larutan ini mengandung (1; 2; 3; 4; 5) µg/mL dan diukur absorbansinya pada panjang gelombang 589,0 nm dengan nyala udara asetilen.
3.12.2 Pembuatan Kurva Kalibrasi Kalium
Larutan baku kalium (konsentrasi 1000 µg/mL) dipipet sebanyak 2,5 mL, dimasukkan ke dalam labu tentukur 50 mL dan dicukupkan hingga garis tanda dengan akuabides (konsentrasi 50 µg/mL).
3.13 Penentuan Kadar Natrium dan Kalium dengan Spektrofotometer Serapan Atom
Sebanyak 1 mL urin dimasukkan ke dalam labu tentukur 50 mL kemudian dicukupkan dengan akuades sampai 50 mL. Dipindahkan ke dalam erlemeyer dan ditambahkan 5 mL HNO3 pekat dan beberapa batu didih.
Didihkan secara perlahan-lahan kemudian diuapkan dengan hotplate hingga volume urin total tinggal 20 mL, saring. Filtrat dimasukkan ke dalam labu tentukur 100 mL dicukupkan dengan akuades sampai garis tanda. Faktor pengenceran untuk penentuan kadar natrium pada urin adalah 5 kali, faktor pengenceran untuk penentuan kadar kalium pada urin adalah 5 kali. Selanjutnya diukur menggunakan alat SSA (SNI, 2004).
3.14 Analisis Data
BAB IV
HASIL DAN PEMBAHASAN
4.1 Hasil Identifikasi Tumbuhan
Hasil identifikasi tumbuhan yang dilakukan di Lembaga Ilmu Pengetahuan Indonesia (LIPI) Pusat Penelitian dan Pengembangan Biologi Bogor menunjukan bahwa tumbuhan yang digunakan adalah pecut kuda (Stachytarpheta jamaicensis (L.) Vahl). Suku Verbenaceae. Hasil identifikasi tumbuhan dapat dilihat pada Lampiran 1 halaman 52.
4.2Hasil Pemeriksaan Karakterisasi 4.2.1 Hasil Pemeriksaan Makroskopik
Hasil pemeriksaan makroskopik simplisia pecut kuda menunjukkan simplisia berwarna coklat, tekstur rapuh, berbau khas, dan pahit. Selain itu pemeriksaan makroskopik ini dilakukan untuk mengetahui morfologi dan karakterisasi dari simplisia tanaman, sehingga dapat dipastikan bahwa simplisia yang dipakai adalah benar.
4.2.2 Hasil Pemeriksaan Mikroskopik
Hasil pemeriksaan mikroskopik serbuk simplisia pecut kuda terlihat adanya rambut kelenjar, pembuluh kayu dengan penebalan jala, stomata tipe diasitik, lapisan gabus dapat dilihat pada Lampiran 4 halaman 56.
4.2.3 Hasil Pemeriksaan Karakterisasi Simplisia dan Ekstrak
[image:47.595.113.478.248.386.2]Menurut Depkes RI (1995), standarisasi suatu simplisia dan ekstrak adalah pemenuhan terhadap persyaratan sebagai bahan obat dan menjadi penetapan nilai untuk berbagai parameter produk. Hasil pemeriksaan karakterisasi simplisia dan ekstrak pecut kuda terlihat pada Tabel 4.1.
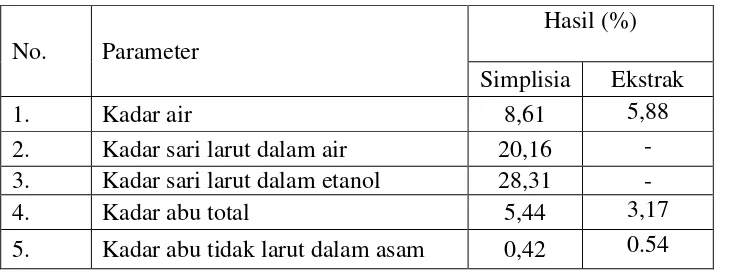
Tabel 4.1 Hasil pemeriksaan karakterisasi simplisia dan ekstrak pecut kuda.
No. Parameter
Hasil (%) Simplisia Ekstrak
1. Kadar air 8,61 5,88
2. Kadar sari larut dalam air 20,16 -
3. Kadar sari larut dalam etanol 28,31 -
4. Kadar abu total 5,44 3,17
5. Kadar abu tidak larut dalam asam 0,42 0.54
Hasil penetapan kadar air simplisia dan crude ekstrak etanol pecut kuda diperoleh 8,61% dan 5,88%, hal ini sesuai dengan standarisasi kadar air simplisia secara umum dengan syarat yaitu tidak lebih dari 10% (Depkes, RI., 1985). Jika kadar air lebih dari 10% dapat terjadi proses pembusukan, dan untuk mendapatkan simplisia yang tidak mudah rusak oleh mikroba seperti jamur sehingga dapat disimpan dalam waktu yang lebih lama.
Penetapan kadar sari larut air untuk mengetahui banyaknya senyawa yang dapat larut dalam air (bersifat polar) yang terkandung pada simplisia. Penetapan kadar sari larut etanol dilakukan untuk mengetahui kandungan senyawa kimia yang larut dalam etanol (bersifat polar atau non polar).
tidak larut asam, senyawa anorganik yang tidak larut adalah silikat yang menunjukkan pengotor pasir.
4.3 Hasil Pemeriksaan Skrining dan Ekstrak
[image:48.595.145.508.331.464.2]Skrining fitokimia terhadap serbuk simplisia dan crude ekstrak etanol pecut kuda dilakukan untuk mendapatkan informasi golongan senyawa metabolit sekunder yang terdapat di dalamnya. Hasil skrining fitokimia serbuk simplisia dan crude ekstrak etanol pecut kuda dapat dilihat pada Tabel 4.2.
Tabel 4.2 Hasil pemeriksaan skrining fitokimia serbuk simplisia dan crude ekstrak etanol pecut kuda.
No Parameter Pecut kuda
Serbuk simplisia Ekstrak Etanol
1 Alkaloida + +
2 Flavonoida + +
3 Saponin - -
4 Tannin + +
5 Glikosida + +
6 Steroida/Triterpenoida + +
Keterangan: (+) positif = mengandung golongan senyawa (-) negatif = tidak mengandung golongan senyawa
Hasil skrining menunjukkan bahwa simplisia pecut kuda mengandung senyawa golongan alkaloid, flavonoid, tanin, glikosida, dan steroid/triterpenoid. Hasil skrining ekstrak etanol pecut kuda menunjukkan adanya senyawa golongan alkaloid, flavonoid, steroid/terpenoid, tanin, dan glikosida.
4.4 Hasil Pengujian Efek Diuretik
kelompok pembanding Furosemid dosis 10 mg/kg bb, dengan parameter pengukuran volume urin, pH urin, kadar natrium dan kadar kalium dalam urin tikus jantan.
4.4.1 Hasil Volume Urin
[image:49.595.113.513.360.624.2]Volume urin berkaitan erat dengan penggunaan diuretik karena dapat menyebabkan terjadinya diuresis. Pengukuran jumLah urin bermanfaat untuk menentukan adanya gangguan faal ginjal dan kelainan dalam keseimbangan cairan tubuh (Suratman dkk, 2003). Hasil pengukuran volume urin dapat dilihat pada Tabel 4.3.
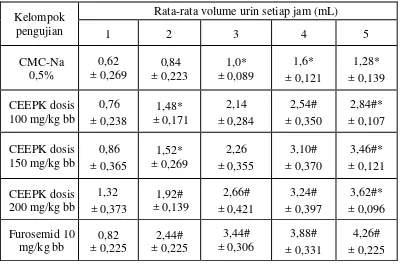
Tabel 4.3 Hasil pengukuran volume urin rata-rata setiap jam selama 5 jam
Kelompok pengujian
Rata-rata volume urin setiap jam (mL)
1 2 3 4 5
CMC-Na 0,5% 0,62 ± 0,269 0,84 ± 0,223 1,0* ± 0,089 1,6* ± 0,121 1,28* ± 0,139 CEEPK dosis
100 mg/kg bb
0,76 ± 0,238 1,48* ± 0,171 2,14 ± 0,284 2,54# ± 0,350 2,84#* ± 0,107 CEEPK dosis
150 mg/kg bb
0,86 ± 0,365 1,52* ± 0,269 2,26 ± 0,355 3,10# ± 0,370 3,46#* ± 0,121 CEEPK dosis
200 mg/kg bb
1,32 ± 0,373 1,92# ± 0,139 2,66# ± 0,421 3,24# ± 0,397 3,62#* ± 0,096 Furosemid 10 mg/kg bb 0,82 ± 0,225 2,44# ± 0,225 3,44# ± 0,306 3,88# ± 0,331 4,26# ± 0,225 Keterangan:
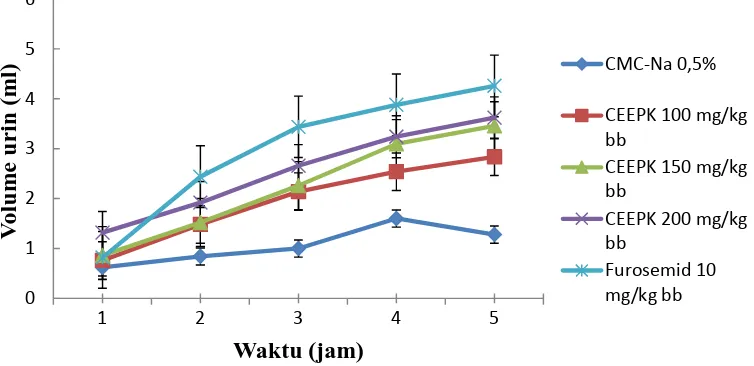
Profil volume urin terhadap waktu ditunjukkan pada Gambar 4.1.
Gambar 4.1 Volume urin rata-rata setiap jam selam 5 jam
Pada Tabel 4.3 dan Gambar 4.1 menunjukkan bahwa jam ke-5 semua sediaan uji dan kelompok pembanding sudah menunjukkan efek diuretik. CEEPK dosis 200 mg/kg bb paling baik dalam pengeluaran urin. Hal tersebut sudah terlihat pada jam ke-2, dimana CEEPK dosis 200 mg/kg bb ini mempunyai aktivitas diuretik hampir sama dengan furosemid dosis 10 mg/kg bb tetapi pada jam ke-3 sampai jam ke-5 furosemid dosis 10 mg/kg bb mengalami peningkatan pengeluaran urin yang lebih besar dibandingkan sediaan uji. Menurut Tjay dan Raharja (2007) furosemide memiliki waktu paruh yang singkat (1-2 jam) dengan onset 0,5-1 jam setelah pemberian secara peroral dan bertahan 4-6 jam. Pada CEEPK dosis 150 mg/kg bb dengan dosis 100 mg/kg bb sudah memberikan efek dalam pengeluaran urin pada jam ke-3, dimana CEEPK dosis 100 mg/kg bb yang mempunyai efek diuretik paling rendah dibandingkan dengan dosis 200 mg/kg bb dan 150 mg/kg bb.
Pengukuran volume urin pada jam ke-5 sebagai urin total pada setiap 0 1 2 3 4 5 6
1 2 3 4 5
V olu m e u rin (m l) Waktu (jam) CMC-Na 0,5%
CEEPK 100 mg/kg bb
CEEPK 150 mg/kg bb
CEEPK 200 mg/kg bb
Tabel 4.4 Hasil pengukuran volume total urin tikus pada kelompok uji
No Kelompok Pengujian N Rata-rata ± SEM (mL)
1 Kontrol
CMC-Na 0,5% 5
1,28* ± 0,139
2 CEEPK dosis
100 mg/kg bb 5
2,84#* ± 0,107
3 CEEPK dosis
150 mg/kg bb 5
3,46#* ± 0,121
4 CEEPK dosis
200 mg/kg bb 5
3,62#* ± 0,096 5 Furosemid dosis
10 mg/kg bb 5
4,26# ± 0,225 Keterangan:
(#) Berbeda signifikan terhadap kontrol negatif (p < 0,05) (*) Berbeda signifikan terhadap kontrol positif (p < 0,05)
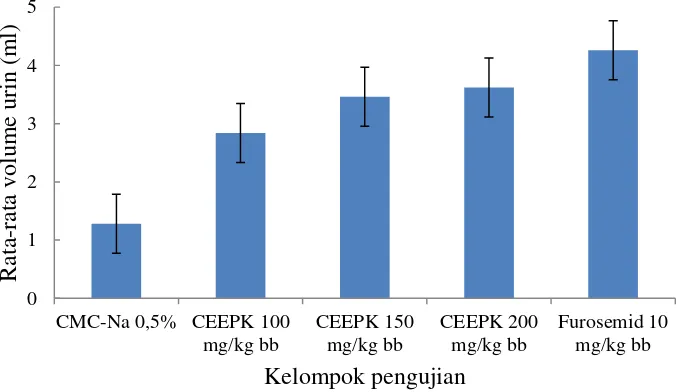
Pada Tabel 4.4 dapat dilihat bahwa volume urin rata- rata untuk kontrol negatif CMC-Na 0,5% 1,28 ± 0,139 mL, kelompok pembanding furosemid 4,26 ± 0,225 mL, kelompok uji CEEPK dosis 100 mg/kg bb 2,84 ± 0,107 mL, CEEPK dosis 150 mg/kg bb 3,46 ± 0,121 mL, CEEPK dosis 200 mg/kg bb 3,62 ± 0,096 mL.
CEEPK dapat meningkatkan pengeluaran volume urin terhadap tikus jantan. Pemberian CEEPK dengan dosis 100, 150, 200 mg/kg bb mempunyai pengeluaran volume urin lebih besar dibandingkan dengan tikus kontrol negatif tetapi tidak lebih banyak daripada kontrol pembanding dengan nilai signifikansi (p < 0,05). Hal tersebut disebabkan kontrol negatif tidak mempunyai efek diuretik sedangkan kontrol pembanding furosemid menghasilkan peningkatan volume urin yang lebih besar dari semua kelompok, hal ini dikarenakan furosemid merupakan obat diuretik kuat yang dapat menghambat reabsorbsi dari natrium dan kalium. Menurut Siswandono, (1995) furosemid merupakan diuretik turunan sulfonamid, memiliki aktivitas diuresis saluretik yang kuat, aktivitasnya 8-10 kali diuretik tiazid.
[image:52.595.129.468.451.647.2]Untuk mempermudah pengamatan volume urin total pada masing-masing kelompok kontrol, pembanding dan kelompok uji, dapat dilihat pada Gambar 4.2
Gambar 4.2 Volume total urin pada tikus jantan
Selanjutnya peningkatan volume urin yang dihasilkan oleh pengujian 0
1 2 3 4 5
CMC-Na 0,5% CEEPK 100 mg/kg bb
CEEPK 150 mg/kg bb
CEEPK 200 mg/kg bb
Furosemid 10 mg/kg bb
R
ata
-ra
ta
volum
e urin (
ml
)
kelompok kontrol negatif, dan melihat aktivitas diuretik yang merupakan hasil perbandingan volume urin kelompok uji terhadap volume urin pembanding. Tabel 4.5 Aktivitas diuretik dan indeks diuretik
Kelompok perlakuan
Volume urin ± SEM (mL)
Aktivitas diuretik Indeks duretik CMC-Na 0,5%
1,28 ± 0,139 0,30 1
CEEPK dosis
100 mg/kg bb 2,84 ± 0,107
0,66 2,21
CEEPK dosis
150 mg/kg bb 3,46 ± 0,121
0,81 2,70
CEEPK dosis
200 mg/kg bb 3,62 ± 0,096
0,84 2,82
Furosemid dosis
10 mg/kg bb 4,26 ± 0,225
1 3,32
Menurut Asif, (2013) nilai indeks diuretik lebih besar dari 1,50 dinyatakan memilik aktivitas diuretik kuat, nilai indeks diuretik mulai dari 1,00-1,50 memiliki aktivitas diuretik sedang, dan nilai indeks diuretik 0,72 – 1,00 memiliki aktivitas diuretik lemah.
Berdasarkan hasil yang diperoleh pada Tabel 4.5 ketiga sediaan uji memiliki nilai indeks diuretik sebagai berikut CEEPK dosis 100 mg/kg bb yaitu 2,21, CEEPK dosis 150 mg/kg bb yaitu 2,70, dan CEEPK dosis 200 mg/kg bb yaitu 3,32 hasil ini menunjukkan bahwa crude ekstrak etanol pecut kuda memiliki aktivitas diuretik yang kuat. CEEPK dosis tertinggi yaitu 200 mg/kg bb menunjukkan aktivitas diuretik sebesar 84% dibandingkan dengan furosemid. 4.4.2 Hasil Kadar Natrium
Natrium adalah kation utama dalam darah dan cairan ekstraselular yang
dalam pengaturan cairan tubuh, termasuk tekanan darah dan keseimbangan asam basa
(Barasi, 2007).
Kurva kalibrasi diperoleh dengan cara mengukur absobansi dari larutan baku kalium dengan panjang gelombang 589 nm berdasarkan hasil pengukuran kurva kalibrasi untuk natrium diperoleh persamaaan garis regresi yaitu:
Y= , X - 0,00209 dengan nilai r = 0,9998. Hal ini menunjukkan adanya korelasi linier yang menyatakan adanya hubungan antara X (konsentrasi) dan Y (absorbansi).
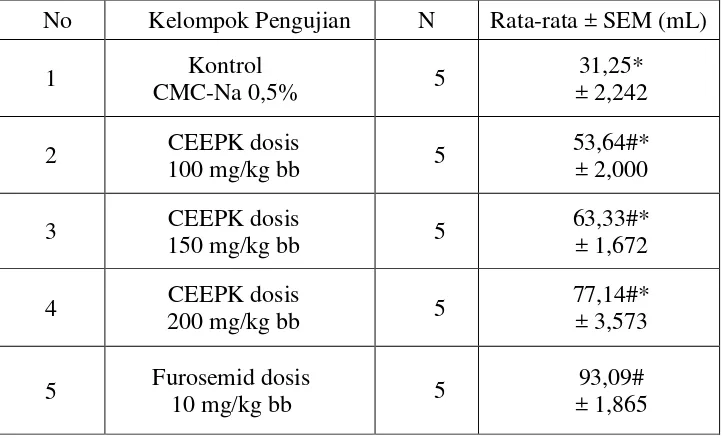
[image:54.595.115.476.387.606.2]Hasil pengukuran kadar natrium dalam urin tikus jantan pada kelompok uji dapat dilihat pada Tabel 4.6.
Tabel 4.6 Kadar natrium dalam urin tikus pada kelompok uji
No Kelompok Pengujian N Rata-rata ± SEM (mL)
1 Kontrol
CMC-Na 0,5% 5
31,25* ± 2,242
2 CEEPK dosis
100 mg/kg bb 5
53,64#* ± 2,000
3 CEEPK dosis
150 mg/kg bb 5
63,33#* ± 1,672
4 CEEPK dosis
200 mg/kg bb 5
77,14#* ± 3,573 5 Furosemid dosis
10 mg/kg bb 5
93,09# ± 1,865
Keterangan:
furosemid dosis 10 mg/kg bb 93,09 ± 1,1865 meq/L, CEEPK dosis 100 mg/kg bb 53,64 ± 2,00 meq/L, CEEPK dosis 150 mg/kg bb 63,33 ± 1,672 meq/L, CEEPK 200 mg/kg bb 77,14 ± 3,573 meq/L.
Berdasarkan hasil yang diperoleh, CEEPK dengan dosis 100 mg/kg bb, 150 mg/kg bb, dan 200 mg/kg bb menunjukkan efek diuretik terhadap kadar natrium dalam urin. Dari ketiga dosis tersebut, CEEPK dengan dosis 200 mg/kg bb mempunyai efek pengeluaran natrium yang paling baik terhadap volume urin dengan nilai signifikansi 0,00 (p < 0,05). CEEPK dosis 100 mg/kg bb tidak mempunyai perbedaan yang nyata terhadap pengeluaran kadar natrium dalam urin dengan CEEPK dosis 150 mg/kg bb diperoleh nilai signifikansi (p > 0,05).
Pemberian CEEPK dengan dosis 100, 150, 200 mg/kg bb mempunyai efek diuretik terhadap pengeluaran natrium lebih besar dibandingkan dengan tikus kontrol negatif CMC-Na 0,5% tetapi tidak lebih banyak daripada kontrol pembanding dengan nilai signifikansi 0,00 (p < 0,05). Hal ini menunjukkan bahwa furosemid lebih kuat untuk pengeluaran natrium dalam urin tikus sedangkan CMC-Na 0,5% adalah sebagai kontrol negatif dalam penelitian ini.
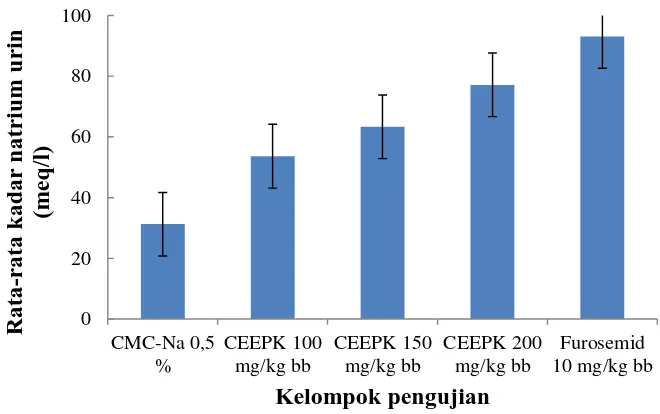
Untuk mempermudah pengamatan kadar natrium dari masing-masing kelompok kontrol, pembanding dan kelompok uji, dapat dilihat pada grafik Gambar 4.3
Gambar 4.3 Kadar natrium urin tikus jantan 4.4.3 Hasil Kadar Kalium
Kalium merupakan ion intraselular dan dihubungkan dengan mekanisme pertukaran dengan natrium. Peningkatan asupan kalium dalam diet telah dihubungkan dengan penurunan tekanan darah, karena kalium memicu natriuresis (kehilangan natrium melalui urin) (Barasi, 2007).
Kurva kalibrasi diperoleh dengan cara mengukur absobansi dari larutan baku kalium dengan panjang gelombang 766,5 nm berdasarkan hasil pengukuran kurva kalibrasi untuk kalium diperoleh persamaaan garis regresi yaitu Y= 0,05159 X + 0,00029 dengan nilai r = 0,9997. Hal ini menunjukkan adanya korelasi linier yang menyatakan adanya hubungan antara X (konsentrasi) dan Y (absorbansi).
0 20 40 60 80 100 CMC-Na 0,5 % CEEPK 100 mg/kg bb CEEPK 150 mg/kg bb CEEPK 200 mg/kg bb Furosemid 10 mg/kg bb
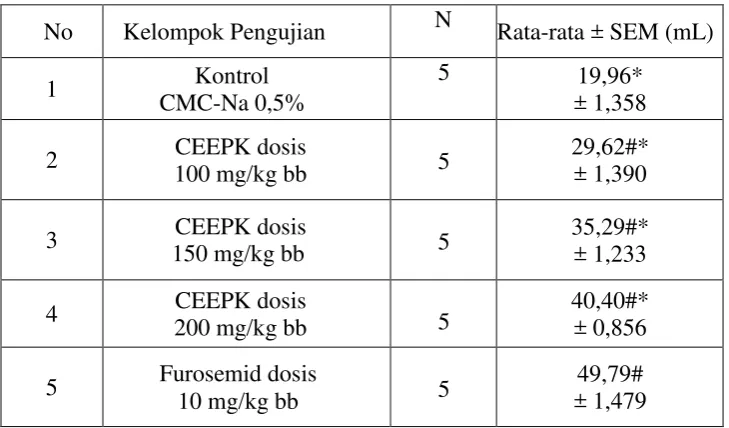
Tabel 4.7 Kadar kalium dalam urin tikus pada kelompok uji
No Kelompok Pengujian N Rata-rata ± SEM (mL)
1 Kontrol
CMC-Na 0,5%
5 19,96*
± 1,358
2 CEEPK dosis
100 mg/kg bb 5
29,62#* ± 1,390
3 CEEPK dosis
150 mg/kg bb 5
35,29#* ± 1,233
4 CEEPK dosis
200 mg/kg bb 5
40,40#* ± 0,856 5 Furosemid dosis
10 mg/kg bb 5
49,79# ± 1,479
Keterangan:
(#) Berbeda signifikan terhadap kontrol negatif (p < 0,05) (*) Berbeda signifikan terhadap kontrol positif (p < 0,05)
Pada Tabel 4.7 dapat dilihat dari hasil rata-rata yang diperoleh untuk kontrol negatif CMC-Na 0,5% 19,96 ± 1,358 meq/L, kontrol pembanding furosemid dosis 10 mg/kg bb 49,79 ± 1,479 meq/L, CEEPK dosis 100 mg/kg bb 29,62 ± 1,390 meq/L, CEEPK dosis 150 mg/kg bb 35,29 ± 1,233 meq/L, CEEPK 200 mg/kg bb 40,40 ± 0,856 meq/L.
Pemberian CEEPK dengan dosis 100, 150, 200 mg/kg bb mempunyai efek diuretik terhadap pengeluaran kalium lebih besar dibandingkan dengan tikus kontrol negatif CMC-Na 0,5% tetapi tidak lebih banyak daripada kontrol pembanding dengan nilai signifikansi 0,00 (p < 0,05). Hal ini menunjukkan bahwa furosemid lebih kuat untuk pengeluaran kalium dalam urin tikus sedangkan CMC-Na 0,5% adalah sebagai kontrol negatif dalam penelitian ini. Penelitian ini menunjukkan bahwa semakin banyak dosis ekstrak yang diberikan maka semakin banyak mempengaruhi pengeluaran volume urin dan ekskresi kalium.
meningkatkan ekskresi air dan menyebabkan volume urin bertambah (Lingga, 2014).
[image:59.595.135.469.228.424.2]Untuk mempermudah pengamatan kadar kalium dari masing-masing kelompok kontrol, pembanding dan kelompok uji, dapat dilihat pada grafik Gambar 4.4
Gambar 4.4 Kadar kalium urin tikus jantan
Selanjutnya berdasarkan pengukuran kadar natrium dan kadar kalium pada urin tikus maka dapat diketahui rasio Na+/K+. Rasio Na+/K+ dapat dilihat pada
[image:59.595.113.509.586.753.2]Tabel 4.8.
Tabel 4.8 Ratio kadar natrium dan kalium dalam urin tikus jantan Kelompok
perlakuan
Kadar Na+ Kadar K+ Na+/K+
CMC-Na 0,5% 31,25 ± 2,242 19,96 ± 1,358 1,56 CEEPK dosis
100 mg/kg bb 93,09 ± 1,865 49,79 ± 1,479
1,86 CEEPK dosis
150 mg/kg bb 53,64 ± 2,000 29,62 ± 1,390
1,81 CEEPK dosis
200 mg/kg bb 63,33 ± 1,672 35,29 ± 1,233
1,79 Furosemid dosis
10 mg/kg bb 77,14 ± 3,573 40,40 ± 0,856
Hasil pengamatan yang tertera pada Tabel 4.8 diperoleh rasio Na+/K+
kontrol negatif 1,56, CEEPK dosis 100 mg/kg bb 1,86, CEEPK dosis 150 mg/kg bb 1,81, CEEPK dosis 200 mg/kg bb 1,79, dan pembanding furosemid adalah 1,90, nilai tersebut tidak lebih besar dari nilai ratio Na+/K+ CEEPK dosis 100, 150, 200 mg/kg bb karena furosemid merupakan diuretik yang menyebabkan pengeluaran natrium yang besar sehingga air banyak dieksresikan juga mengeluarkan kalium yang besar karena merupakan diuretik boros kalium.
Menurut Parmar, dan Prakash, (2006) nilai ratio Na+/K+ dapat
menentukan saliuretik, jika rasio Na+/K+ lebih besar dari 2 merupakan aktivitas natriuretik yang baik, rasio Na+/K+ lebih besar dari 10 diindikasikan sebagai hemat kalium, dan rasio Cl-/Na+ + K+ untuk memperkirakan diuretik penghambat karbonik anhidrase. Menurut Kebamo, et. Al., (2015) rasio Na+/K+ dihitung untuk mengetahui indeks pengeluaran aldosteron (aktivitas natriuretik). Aldosteron berfungsi menjaga keseimbangan ion natrium dalam darah. Menurut Guyton (1994), apabila konsentrasi aldosteron meningkat maka sisa natrium akan direabsorspsi dari bagian dalam tubulus distal dan duktus koligens sehingga pada dasarnya tidak ada natrium keluar kedalam urin, sebaliknya jika konsentrasi aldosteron dikurangi maka sisa natrium tidak direabsorpsi dari tubulus distal sehingga natrium keluar bersama urin.
4.4.4 Hasil Pengukuran pH urin
Derajat keasaman (pH) menyatakan konsentrasi ion hidrogen (H+) yang
terus-menerus ke dalam tubulus ginjal dan diekskresikan ke dalam urin, maka akan menyebabkan urin bersifat basa. Sebaliknya apabila sejumLah ion H+ difiltrasi secara terus-menerus ke dalam tubulus ginjal dan diekskresikan ke dalam urin, maka akan menyebabkan urin bersifat asam. Kemampuan ginjal sebagai sistem pengatur asam – basa yang paling kuat dan hanya memerlukan waktu beberapa jam untuk menyesuaikan kembali konsentrasi ion H+ tersebut. Apabila
konsentrasi H+ berubah dari normal, maka ginjal akan mengekskresikan urin yang asam/ basa, dengan demikian juga dapat membantu menyesuaikan konsentrasi ion H+ cairan tubuh kembali normal (Guyton, 1997).
[image:61.595.115.478.417.632.2]Hasil pengukur pH dalam urin pada tikus jantan dapat dilihat pada Tabel 4.9
Tabel 4.9 Hasil pengukur pH dalam urin pada tikus jantan
No Kelompok Pengujian N Rata-rata ± SEM (mL)
1 Kontrol
CMC-Na 0,5% 5
7,180 ± 0,086
2 CEEPK Dosis
100 mg/kg bb 5
7,12 ± 0,121
3 CEEPK dosis
150 mg/kg bb 5
7,360 ± 0,081
4 CEEPK dosis
200 mg/kg bb 5
7,46 ± 0,080 5 Furosemid dosis
10 mg/kg bb 5
7,18 ± 0,121 Keterangan:
(#) Berbeda signifikan terhadap kontrol negatif (p < 0,05) (*) Berbeda signifikan terhadap kontrol positif (p < 0,05)
mg/kg bb adalah 7,120 ± 0,121, dosis 150 mg/kg bb adalah 7,36 ± 0,251, dosis 200 mg/kg bb adalah 7,46 ± 0,080, kelompok pembanding furosemid dosis 10 mg/kg bb 7,18 ± 0,121.
Berdasarkan hasil yang diperoleh CEEPK dosis 100 mg/kg bb, 150 mg/kg bb, dan 200 mg/kg bb menunjukkan hasil pH urin tidak mempunyai perbedaan yang nyata yaitu dengan nilai signifikansi ( p > 0,05).
Pemberian dosis CEEPK dosis 100, 150, 200 mg/kg bb jika dibandingkan dengan kelompok kontrol (CMC-Na 0,5%) dan kelompok pembanding furosemid dosis 10 mg juga tidak mempunyai perbedaan yang nyata yaitu dengan nilai signifikansi (p > 0,05).
Menurut Adha (2009) pH normal dari urin tikus berkisar 7.3 – 8.5. Hasil penelitian ini menunjukkan bahwa pH yang didapat normal yaitu berkisar antara 7 - 7,5. Kontrol pembanding maupun kontrol uji tidak mempengaruhi nilai pH urin yang berarti ekstrak tidak mempengaruhi asam / basa cairan tubuh. Pengukuran pH dilakukan untuk mengetahui apakah ekstrak yang di uji termasuk golongan diuretik penghambat karbonik anhidrase. Golongan diuretik penghambat karbonik anhidrase dapat menyebabkan pH urin menjadi basa karena ekskresi HCO3- yang
cepat di urin. Hal ini seiring dengan penghambatan terhadap titrable acid dan adanya sekresi ammonia di sistem duktus pengumpul, yang mengakibatkan pH urin menjadi sekitar 8 dan menimbulkan asidosi metabolik (Edwin, 2012).
Gambar 4.5 pH urin tikus jantan 6.8
6.9 7 7.1 7.2 7.3 7.4 7.5
CMC-Na 0,5 % CEEPK 100 mg/kg bb
CEEPK 150 mg/kg bb
CEEPK 200 mg/kg bb
Furosemid 10 mg/kg bb
ra
ta
-ra
ta
pH
urin
[image:63.595.128.458.88.304.2]BAB V
KESIMPULAN DAN SARAN 5.1 Kesimpulan
Berdasarkan penelitian ini dapat disimpulkan bahwa crude ekstrak etanol pecut kuda dosis 100, 150, 200 mg/kg bb memiliki aktivitas diuretik dengan meningkatkan volume urin, kadar natrium dan kadar kalium dalam urin tetapi tidak mempengaruhi pH dari urin tersebut. Dosis efektif dari crude ekstrak etanol pecut kuda adalah dosis 200 mg/kg bb menunjukkan bahwa dosis tersebut memberikan efek diuretik yang mendekati hasil dengan furosemid 10 mg/kg bb.
5.2 Saran
BAB II
TINJAUAN PUSTAKA
2.1 Uraian Tumbuhan
Pecut kuda tumbuh liar di tepi jalan, tanah lapang dan tempat- tempat terlantar lainnya. Tanaman yang berasal dari Amerika ini dapat ditemukan di daerah cerah, sedang, terlindung dari sinar matahari dan pada ketinggian 1- 1500 m dpl. Pecut kuda merupakan terna tahunan, tumbuh tegak, tinggi ± 50 cm, tumbuh liar disisi jalan daerah pinggir kota, tanah kosong yang tidak terawat. Daun letak berhadapan, bentuk bulat telur, tepi bergerigi, tidak berambut. Bunga duduk tanpa tangkai pada bulir - bulir yang berbentuk pecut, panjang 4 - 20 cm. bunga mekar tidak berbarengan, kecil - kecil warna ungu, putih (Dalimartha, 2000).
2.1.1 Sistematika tumbuhan
Kedudukan kategori taksa untuk jenis pecut kuda di dalam sistematika tumbuhan adalah sebagai berikut :
Divisi : Spermatophyta Sub divisi : Angiospermae Class : Dicotyledoneae Ordo : Lamiales Famili : Verbenaceae Genus : Stachytarpheta
2.1.2 Nama lokal
Jawa: jarong (Sunda), biron, karomenal, sekar laru, ngadirenggo (jawa) (Dalimartha, 2000).
2.1.3 Nama asing
Yu long Bian (Cina), Snakeweed (Inggris) (Dalimartha, 2000). 2.1.4 Kandungan kimia
Pecut kuda mengandung glikosida, flavonoid dan alkaloid (Dalimartha, 2000).
2.1.5 Khasiat tumbuhan
Herba pecut kuda (Stachytarpheta jamaicensis (L.) Vahl) digunakan sebagai obat infeksi dan batu saluran kencing, rematik, sakit tenggorokan, pembersih darah, haid tidak teratur, keputihan, hepatitis A. Bunga dan tangkainya untuk pengobatan radang hati sedangkan akarnya untuk pengobatan keputihan (Dalimartha, 2000).
2.2 Metode Ekstraksi
Ekstrak adalah sediaan pekat yang diperoleh dengan mengekstraksi zat aktif dari simplisia nabati atau hewani menggunakan pelarut yang sesuai, kemudian semua atau hampir semua pelarut diuapkan (Depkes, RI., 2000).
(Depkes, RI., 2000). Tujuan utama ekstraksi adalah untuk mendapatkan atau memisahkan sebanyak mungkin zat-zat yang memiliki khasiat pengobatan (Syamsuni, 2006).
Metode ekstraksi yang umum digunakan antara lain yaitu: a. Maserasi
Maserasi adalah proses penyarian simplisia menggunakan pelarut dengan beberapa kali pengocokan atau pengadukan pada temperatur ruangan, sedangkan remaserasi merupakan pengulangan penambahan pelarut setelah dilakukan penyaringan maserat pertama, dan seterusnya (Depkes, RI., 2000).
b. Perkolasi
Perkolasi adalah proses penyarian simplisia dengan pelarut yang selalu baru sampai sempurna yang umumnya dilakukan pada temperatur ruangan. Serbuk simplisia yang akan diperkolasi tidak langsung dimasukkan kedalam bejana perkolator, tetapi dibasahi atau dimaserasi terlebih dahulu dengan cairan penyari sekurang-kurangnya selama 3 jam (Depkes, RI., 2000).
c. Refluks
Refluks adalah proses penyarian simplisia dengan menggunakan alat pada temperatur titik didihnya dalam waktu tertentu dimana pelarut akan terkondensasi menuju pendingin dan kembali ke labu (Depkes, RI., 2000).
d. Sokletasi
e. Digesti
Digesti adalah proses penyarian dengan pengadukan kontinu pada temperatur lebih tinggi dari temperatur kamar, yaitu secara umum dilakukan pada temperatur 40-50°C (Depkes, RI., 2000).
f. Infundasi
Infundasi adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90°C selama 15 menit (Depkes, RI., 2000).
g. Dekoktasi
Dekoktasi adalah proses penyarian dengan menggunakan pelarut air pada temperatur 90°C selama 30 menit (Depkes, RI., 2000).
2.3 Ginjal
Ginjal terletak dibelakang selaput rongga perut, berbentuk seperti kacang polong. Masing-masing ginjal mempunyai panjang kurang lebih 11 hingga 13 cm, lebar 5 hingga 7,5 cm, tebal 2,5 cm dan berat antara 115 dan 170 gram (Hartono, 1991). Ginjal terdiri atas unit-unit fungsional yang dinamakan nefron dan pada setiap ginjal terdapat 1 hingga 1,5 juta nefron. Nefron merupakan tubulus (pipa) yang panjangnya kurang lebih 6 cm dan tersusun dari bagian komponen yang dirancang menurut ciri anatomi serta fungsional yang khas. Kelima komponen nefron tersebut adalah kapsul bowman, tubulus kontortus proksimal, ansa Henle, tubulus kontortus, distal dan saluran pengumpul (Hartono, 1991).
elektrolit, dll, ekskresi produk sampah, contohnya urea, dan memainkan peranan penting dalam keseimbangan asam-basa (Thomson dan Cotton, 1997).
2.4 Mekanisme Pembentukan Urin
Proses pembentukan urin dimulai dengan filtrasi sejumLah besar cairan yang bebas protein dari kapiler glomerulus ke kapsula Bowman. Kebanyakan zat dalam plasma, kecuali protein, difiltrasi secara bebas sehingga konsentrasinya pada filtrat glomerolus dalam kapsula Bowman hampir sama dengan dalam plasma. Ketika cairan yang telah difiltrasi ini meninggalkan kapsul Bowman dan mengalir melewati tubulus, cairan diubah oleh reabsorbsi air dan zat terlarut spesifik yang kembali ke dalam darah atau oleh sekresi zat- zat lain dari kapiler peritubulus ke dalam tubulus (Muttaqin, dan Kumala, 2011).
Gambar 2.1 Organ – organ yang membentuk saluran urin (O’Callaghan, 2006).
2.5 Diuretik
Gambar 2.2 Nefron (O’Callaghan, 2006).
Penggolongan diuretik berdasarkan mekanisme kerja dan tempat kerja adalah sebagai berikut:
a. Turunan tiazid
Tiazid bekerja terutama pada segmen awal tubulus distal, dimana tiazid menghambat reabsorpsi NaCl dengan terikat pada simport yang berperan untuk kotranspor Na+/Cl-. Terjadi peningkatan ekskresi Cl- dan Na+ disertai H2O. Beban
Na+ yang meningkat dalam tubulus distal menstimulasi pertukaran Na+ dengan K+ dan H+, meningkatkan sekresinya, dan menyebabkan hipokalemia dan alkalosis metabolik, contoh obatnya adalah hidroklorotiazid dan metolazon (Neal, 2006).
b. Diuretik lengkungan (loop diuretic)
paling efektif, karena bagian asendens bertanggung jawab untuk reabsorpsi 25-30% NaCl yang difiltrasi dan tubulus distal tidak mampu untuk mengkompensasi kenaikan muatan Na+ sehingga diekskresikan bersama air ke dalam urin, contoh
obatnya adalah furosemid, bumetanid, torsemid dan asam etakrinat (Mycek, dkk. 2001).
c. Diuretik hemat kalium
Antagonis aldosteron secara kompetitif menghambat ikatan aldosteron pada reseptor sitoplasma sehingga meningkatkan ekskresi Na+ (Cl- dan H
2O) dan
menurunkan sekresi K+. Contoh obatnya adalah spironolakton yang merupakan diuretik lemah, karena hanya 2% dari reabsorpsi Na+ total yang berada di bawah kendali aldosteron (Neal, 2006).
d. Diuretik osmotik
Diuretik osmotik seperti manitol atau gliserol, difiltrasi di glomerulus dan kemudian tidak direabsorpsi. Saat filtrat bergerak di sepanjang nefron, terjadi reabsorpsi air dan konsentrasi diuretik osmotik, natrium kemudian direabsorpsi tanpa air, akhirnya reabsorpsi natrium juga dihambat dan kembali ke dalam lumen (O’Callaghan, 2006).
e. Inhibitor karbon anhidrase
anhidrase menyebabkan peningkatan ekskresi HCO3- yang cepat di urin yang
dapat mengakibatkan peningkatan pH urin dan menimbulkan asidosis metabolik, contoh obatnya adalah asetazolamid (Edwin, 2012).
2.6 Furosemid
Furosemid merupakan diuretik turunan sulfonamid, memiliki aktivitas diuresis saluretik yang kuat, aktivitasnya 8-10 kali diuretik tiazid. Awal kerja obat terjadi dalam 0,5-1 jam setelah pemberian oral, dengan masa kerja yang relatif pendek 6-8 jam. Penyerapan furosemid dalam saluran cerna cepat, ketersediannya 60-69% pada subyek normal, dan 91-99% obat terikat oleh plasma protein. Kadar darah maksimal dicapai 0,5-2 jam setelah pemberian secara oral, dengan waktu paruh biologis 2 jam. Furosemid digunakan untuk pengobatan hipertensi ringan dan moderat karena dapat menurunkan tekanan darah (Siswandono & Bambang 1995).
2