POTENSI
KAEMPFEROL
DAUN
SIRSAK
SEBAGAI
PENGHAMBAT
PROLIFERASI
SEL
KANKER
RAJI
BAIQ
AYU
APRILIA
MUSTARIANI
SEKOLAH
PASCASARJANA
INSTITUT
PERTANIAN
BOGOR
BOGOR
2011
PERNYATAAN
MENGENAI
TESIS
DAN
SUMBER
INFORMASI
Dengan ini saya menyatakan bahwa tesis Potensi Kaempferol Daun Sirsak sebagai Penghambat Proliferasi Sel Kanker Raji adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam daftar pustaka di bagian akhir tesis ini.
Bogor, Juli 2011
ABSTRACT
BAIQ AYU A. MUSTARIANI. Potential of Kaempferol Soursop Leaves as Inhibitor Raji Cancer Cell Proliferation. Under direction of SUMINAR S. ACHMADI, IRMA H. SUPARTO, and SILMI MARIYA.
Leaves of soursop (Annona muricata) has been widely studied, particularly as anti-cancer, but research on flavonoids as anticancer partion isolated from the leaves of the soursop has not been found. Therefore, the purpose of this study is to determine the effectiveness of flavonoids isolated from leaves of the soursop in inhibiting cancer cell proliferation using Raji cells (ATCC CCL-86), Extraction was done by maceration technique using successive solvents, i.e. n-hexane, CH2Cl2 and MeOH-H2O. Separation of active extract used preparative thin layer chromatography. Methanolic activity assay extract was performed on normal cells to determination initial concentration on cancer cells showed, that the lowest inhibition was at concentrations of 1000 µg mL-1 − 500 µg mL-1 with percent inhibition 48% and 31%, respectively. The flavonoids produced a single spot on thin layer chromatograph with Rf value of 0.87. Identification of flavonoids by UV-Vis spectrometer and high performance liquid chromatography confirmed that the flavonoid was kaempferol. Kaempferol extract obtained wastested on Raji cells and Vero cells. For Raji cells the methanolic extract inhibited 76% of the cells at concentration of 250 µg mL-1 but for the normal cells it only inhibited 20%. These results suggest that kaempferol from the soursop leaf can inhibit cell proliferation of Raji cells but gives minimal toxic effect on Vero cells.
Keywords: Annona muricata, flavonoids, kaempferol, cancer cell proliferation.
RINGKASAN
BAIQ AYU A. MUSTARIANI. Potensi Kaempferol Daun Sirsak sebagai Penghambat Proliferasi Sel Kanker Raji. Dibimbing oleh SUMINAR S. ACHMADI, IRMA H. SUPARTO, dan SILMI MARIYA.
Sirsak (Annona muricata) merupakan salah satu tanaman dari famili Annonaceae yang sangat potensial dalam mengobati penyakit kanker. Biji dan daun sirsak sebagai antikanker secara empiris telah banyak digunakan, akan tetapi senyawa yang lebih banyak diteliti sebagai agen antikanker pada sirsak adalah senyawa asetogenin yang merupakan suatu poliketida, yaitu salah satu metabolit sekunder dari famili Annonaceae. Penelitian tentang senyawa-senyawa lain dalam tanaman ini yang diperkirakan aktif sebagai antikanker belum banyak ditelusuri di antaranya ialah senyawa flavonoid. Beberapa penelitian melaporkan bahwa senyawa flavonoid dari genus sirsak memiliki aktivitas dalam menghambat sel kanker. Senyawa flavonoid yang berpotensi menghambat sel kanker pada famili Annonaceae di antaranya ialah kaempferol. Penelitian terhadap daun sirsak sendiri lebih banyak dilaporkan dalam bentuk ekstrak kasarnya sehingga masih perlu dilakukan penelusuran lebih lanjut tentang aktivitas senyawa flavonoid dari daun sirsak dengan menguji pada sel kanker. Oleh sebab itu tujuan penelitian ini ialah ingin mengisolasi potensi senyawa flavonoid kaempferol dari daun sirsak yang berpotensi sebagai antikanker dengan menguji efektivitas isolat flavonoid dari daun sirsak dalam menghambat pertumbuhan sel kanker Raji.
Metode isolasi flavonoid dari daun sirsak terdiri atas beberapa tahap, yaitu pemilihan tumbuhan dan subjek uji, penentuan kadar air, uji flavonoid, ekstraksi flavonoid kaempferol, pemilihan eluen terbaik, fraksinasi menggunakan kromatografi lapis tipis preparatif, dan uji aktivitas penghambatan proliferasi terhadap sel Vero (ATCC CCl-81) dan sel Raji (ATCC CCL 86).
Kandungan flavonoid ditentukan dalam serbuk daun dan dalam ekstrak kasar daun. Berdasarkan uji fitokimia secara kualitatif, serbuk daun dan ekstrak kasar daun sirsak positif mengandung flavonoid. Proses ekstraksi senyawa flavonoid dilakukan dengan metode maserasi dengan n-heksana dan metanol yang dilanjutkan dengan partisi menggunakan diklorometana dan campuran metanol air. Dari hasil ekstraksi ini diperoleh rendemen sebesar 10.62%. Ekstrak kasar diujikan terlebih dahulu pada sel Vero untuk menentukan konsentrasi yang tepat guna diujicobakan pada sel kanker yang tidak merusak sel normal. Berdasarkan hasil pengujian ekstrak kasar, ekstrak hasil fraksinasi daun sirsak yang diujikan adalah di bawah 500 µg mL-1 agar tidak menghambat proliferasi sel normal.
Pemilihan eluen terbaik untuk mengisolasi senyawa kaempferol menggunakan kromatografi lapis tipis (KLT) dan diperoleh spot tunggal dengan eluen HCO2H-H2O-MeOH. Ekstrak kasar selanjutnya dihidrolisis dengan HCl untuk melepaskan ikan glikosida yang terikat dengan flavonoid menjadi aglikonnya. Dari 5 g ekstrak kasar metanol yang dihidrolisis diperoleh rendemen sebesar 34.61%. Ekstrak kasar dipisahkan melalui kromatografi lapis tipis preparatif (KLTP) menggunakan eluen dari hasil KLT. Hasil pemisahan dengan KLTP selanjutnya diuapkan hingga pekat dan diperoleh rendemen sebesar 23.45%. Hasil identifikasi dengan spektrometer UV-Vis menunjukkan satu
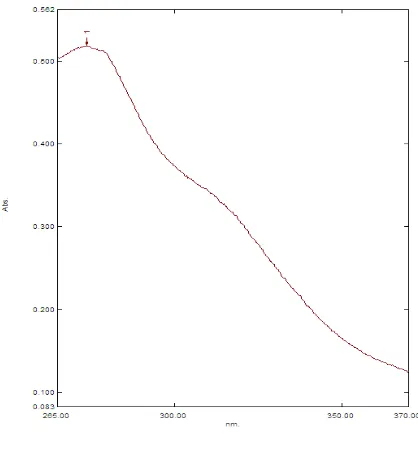
puncak serapan maksimum di daerah panjang gelombang 250-280 nm. Kaempferol merupakan salah satu jenis dari aglikon flavonoid flavonol. Aglikon flavonoid, yaitu flavonol, teridentifikasi pada serapan di daerah panjang gelombang 250-280 nm. Spektrum kromatografi cair kinerja tinggi menguatkan bahwa senyawa yang dihasilkan merupakan senyawa kaempferol dengan waktu retensi yang hampir sama antara waktu retensi kaempferol standar dengan kaempferol dari ekstrak hasil KLTP (kromatografi lapis tipis preparatif).
Dari hasil uji pada sel Vero, kaempferol sampai dengan konsentrasi 250 µg mL-1 minimal menghambat proliferasi sel sebesar 19.77% sedangkan konsentrasi di bawah 100 µg mL-1 tidak menunjukkan penghambatan. Akan tetapi pada konsentrasi 250 µg mL-1 terjadi peningkatan hambatan proliferasi sel Raji sampai 76.36%. Data penghambatan sel kanker tersebut menunjukkan bahwa kaempferol dari daun sirsak toksisitasnya kecil terhadap sel Vero dan memberi penghambatan yang besar pada pertumbuhan sel kanker Raji. Berdasarkan hasil perhitungan nilai IC50, hasil uji penghambatan terhadap sel Vero memperlihatkan bahwa ekstrak kasar, baru dapat menghambat sel normal di atas 500 µg mL-1 dengan nilai IC50 922.88 µg mL-1.. Dari uji kaempferol hasil fraksinasi dengan KLTP pada sel Vero dan sel Raji terlihat bahwa persen penghambatan pada sel kanker Raji lebih besar daripada sel Vero bahkan pada sel Vero dapat dikatakan tidak memiliki IC50 karena pada konsentrasi 250 µg mL-1 ekstrak kaempferol hanya menghambat proliferasi sel sebesar 19.77%. Dengan demikian dapat disimpulkan bahwa aktivitas ekstrak kaempferol terhadap sel hanya spesifik menghambat proliferasi sel kanker Raji akan tetapi tidak menghambat proliferasi sel Vero.
Kata kunci: Annona muricata, flavonoid, kaempferol, proliferasi sel kanker.
©
Hak
Cipta
Milik
IPB,
tahun
2011
Hak
Cipta
dilindungi
Undang-undang
POTENSI
KAEMPFEROL
DAUN
SIRSAK
SEBAGAI
PENGHAMBAT
PROLIFERASI
SEL
KANKER
RAJI
BAIQ
AYU
APRILIA
MUSTARIANI
Tesis
Sebagai salah satu syarat untuk memperoleh gelar Magister Sains pada
Program Studi Kimia
SEKOLAH
PASCASARJANA
INSTITUT
PERTANIAN
BOGOR
BOGOR
2011
HALAMAN
PENGESAHAN
Judul Tesis : Potensi Kaempferol Daun Sirsak sebagai Penghambat Proliferasi Sel Kanker Raji
Nama : Baiq Ayu Aprilia Mustariani NRP : G451090041
Program Studi : Kimia
Disetujui Komisi Pembimbing
Prof. Dr. Ir. Suminar S. Achmadi Ketua
Dr. dr. Irma H. Suparto, M.S Silmi Mariya, S.Si, M.Si
Anggota Anggota
Diketahui
Ketua Program Studi Dekan Sekolah Pascasarjana Kimia
Prof. Dr. Purwantiningsih Sugita, M.S Dr. Ir. Dahrul Syah, M.Sc.Agr.
Tanggal Ujian: 14 Juli 2011 Tanggal Lulus:
PRAKATA
Puji dan syukur saya panjatkan ke hadirat Allah SWT atas rahmat dan karunia-Nya sehingga karya ilmiah ini dapat diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Desember sampai Juni 2011 ini ialah Potensi Kaempferol Daun Sirsak sebagai Penghambat Proliferasi Sel Kanker Raji.
Ucapan terima kasih yang tulus kepada Ibu Prof. Dr. Ir. Suminar S. Achmadi selaku Ketua Komisi Pembimbing, Ibu Dr. dr. Irma H. Suparto, M.S, dan Ibu Silmi Mariya S.Si, M.Si selaku Anggota Komisi Pembimbing, atas segala curahan waktu, bimbingan, arahan, serta dorongan moral kepada saya, serta kepada Ibu Dr. Laksmi Ambarsari, M.S. selaku penguji luar komisi yang telah memberikan banyak saran untuk perbaikan tesis saya. Di samping itu, penghargaan penulis sampaikan pada Pusat Studi Satwa Primata Institut Pertanian Bogor yang telah menyediakan sarana pengujian bahan. Ungkapan terima kasih juga disampaikan kepada mamiq, mama serta seluruh keluarga, atas segala doa dan kasih sayangnya serta kepada Kementerian Agama Republik Indonesia yang telah mendanai pendidikan penulis selama menjalani Program Pascasarjana Kimia.
Semoga karya ilmiah ini bermanfaat
Bogor, Juli 2011
Baiq Ayu Aprilia Mustariani
RIWAYAT
HIDUP
Penulis dilahirkan di Darmaji pada tanggal 09 April 1984 dari pasangan Bapak H. L. Mustajab AMa.Pd. dan Ibu Baiq Husnin AMa. Penulis merupakan anak kedua dari dua bersaudara.
Tahun 2002, penulis lulus dari MAN 2 Mataram dan pada tahun yang sama lulus seleksi masuk Universitas Mataram melalui jalur Seleksi Penerimaan Mahasiswa Baru. Pendidikan sarjana ditempuh di Program Studi Pendidikan Kimia Universitas Mataram, lulus pada tahun 2007. Pada tahun 2009, penulis mengikuti seleksi Beasiswa Utusan Daerah (BUD) yang diselenggarakan oleh Kementerian Agama Republik Indonesia dan diterima di Program Studi Kimia pada Program Pascasarjana IPB. Selama mengikuti perkuliahan, penulis menjadi asisten mata kuliah Kimia Dasar pada tahun ajaran 2010/2011.
DAFTAR
ISI
Halaman
DAFTAR TABEL ...xiv
DAFTAR GAMBAR ...xiv
DAFTAR LAMPIRAN ...xv
PENDAHULUAN ...1
Latar Belakang ...1
Tujuan Penelitian ...2
Manfaat ...2
BAHAN DAN METODE ...3
Tempat Penelitian ...3
Bahan Tumbuhan dan Subjek Uji ...3
Penentuan Kadar Air ...3
Uji Flavonoid ...4
Ekstraksi Flavonoid Kaempferol ...4
Pemilihan Eluen Terbaik ...5
Fraksionasi Menggunakan Kromatografi Lapis Tipis Preparatif ...5
Uji Aktivitas Penghambatan Proliferasi terhadap Sel Vero dan Sel Raji ...5
HASIL ...7
Kadar Air ...7
Kandungan Flavonoid ...7
Ekstrak Flavonoid ...7
Efektivitas Metanol Terhadap Proliferasi Sel Vero ...8
Kaempferol Hasil Kromatografi Lapis Tipis Preparatif ...8
Identitas Flavonoid ...9
Penghambatan Proliferasi Sel Vero dan Sel Raji ...11
PEMBAHASAN ...15
SIMPULAN DAN SARAN ...18
DAFTAR PUSTAKA ...19
LAMPIRAN ...21
DAFTAR
TABEL
Halaman 1 Penghambatan proliferasi ekstrak kasar daun sirsak terhadap sel
Vero ... ... 8
2
Nilai IC50 dari ekstrak kasar dan ekstrak keampferol terhadap sel Vero dan Sel Raji ...
14
DAFTAR
GAMBAR
Halaman 1 Hasil uji fitokimia flavonoid pada serbuk daun dan ekstrak
metanolik ... 7 2 Profil KLT eluen terbaik ekstrak kasar daun sirsak ...9
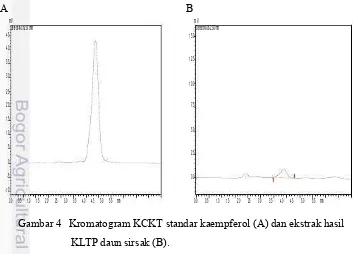
3 Spektrum UV-Vis ekstrak daun sirsak dalam metanol ... 10 4 Kromatogram KCKT standar kaempferol dan ekstrak hasil KLTP ....10
5 Kurva penghambatan proliferasi ekstrak hasil KLTP daun sirsak terhadap sel Vero dan sel Raji ...11 6 Sel Raji tanpa pemberian ekstrak dan sel Raji yang diberi ekstrak
kaempferol 250 µg mL-1 ...12 7 Sel Vero normal (kontrol) pada uji MTT dan sel Vero setelah
pemberian ekstrak ...12 8 Sel Raji normal (kontrol) pada uji MTT dan sel Raji setelah
pemberian ekstrak ... ... 13
DAFTAR
LAMPIRAN
Halaman
1 Hasil determinasi tanaman sirsak ...21
2 Bagan alir penelitian ... 22
3 4 Bagan alir metode MTT ... 23
Data hasil uji penghambatan ekstrak kasar terhadap sel Vero ... 24
5 Kromatogram standar kaempferol pada konsentrasi 10 µg mL-1 ...25
6 Kromatogram hasil KLTP daun sirsak ...26
7 Penentuan kadar kaempferol dalam daun sirsak hasil KLTP ... 8 Data hasil penghambatan flavonoid kaempferol dari daun sirsak terhadap proliferasi sel Vero ... 27 28 9 Data hasil penghambatan flavonoid kempferol dari daun sirsak terhadap proliferasi sel Raji ...39
10 Gambar sel Vero ...30
PENDAHULUAN
Latar Belakang
Sirsak (Annona muricata) merupakan salah satu tanaman famili dari Annonaceae yang sangat potensial dalam mengobati penyakit kanker. Biji dan daun sirsak sebagai antikanker secara empiris telah banyak digunakan, akan tetapi senyawa yang lebih banyak diteliti sebagai agen antikanker pada sirsak adalah senyawa annonaceous asetogenin yang merupakan suatu poliketida, salah satu metabolit sekunder dari famili Annonaceae (Etcheverry et al.1994, Coloma et al. 2002). Penelitian tentang senyawa-senyawa lain dalam tanaman ini yang diperkirakan aktif sebagai antikanker belum banyak ditelusuri di antaranya ialah senyawa flavonoid.
Hasil penelitian Vega et al. (2007) menunjukkan bahwa golongan flavonoid daun A. dioca, salah satu genus dari sirsak memiliki aktivitas dalam menghambat pertumbuhan sel kanker karsinoma Ehrlich. Hasil ini membuktikan bahwa senyawa flavonoid famili Annonaceae memiliki aktivitas farmakologis sebagai antikanker. Penelitian yang dilakukan oleh Santos & Salatino (2000) menunjukkan bahwa kandungan golongan flavonoid daun genus Annona di antaranya adalah kuersetin dan kaempferol. Kedua senyawa ini diduga berpotensi sebagai antikanker sebagaimana diindikasikan oleh Liu et al. (2005), Vega et al. (2007), Yoshida et al. (2008), dan, Luo et al. (2010).
Tujuan Penelitian
Penelitian ini bertujuan menguji efektivitas isolat flavonoid dari daun sirsak dalam menghambat pertumbuhan sel kanker Raji secara in vitro.
Manfaat Penelitian
BAHAN DAN METODE
Tempat Penelitian
Penelitian dilakukan di Laboratorium Kimia Organik, Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahun Alam, Institut Pertanian Bogor (IPB). Uji penghambatan proliferasi terhadap sel secara in vitro dilakukan di Pusat Studi Satwa Primata (PSSP) IPB.
Bahan Tumbuhan dan Subjek Uji
Bahan yang digunakan adalah daun sirsak tua yang diperoleh dari kebun Pusat Studi Biofarmaka IPB. Untuk keperluan identifikasi tumbuhan, sampel dikirim ke Herbarium Bogoriense, Bogor. Pada tahap awal daun sirsak dibersihkan dengan air. Selanjutnya daun dikeringkan dalam oven dengan suhu 40 ºC selama 72 jam, lalu dijadikan serbuk untuk kemudian diekstraksi. Subjek uji yang digunakan adalah penghambatan aktivitas sel Vero (ATCC CCL-81) dan sel Raji (ATCC CCL-86). Kedua jenis sel ini diperoleh dari PSSP
Penentuan Kadar Air
Cawan porselin dikeringkan pada suhu 105 °C dalam oven selama 30 menit, kemudian didinginkan dalam eksikator dan ditimbang. Sebanyak 5 g serbuk daun sirsak dimasukkan ke dalam cawan dan dipanaskan dalam oven pada suhu 105 °C selama 3 jam, kemudian cawan diangkat dan didinginkan dalam eksikator selama 30 menit. Cawan dengan sampel ditimbang hingga diperoleh bobot konstan (AOAC 2006). Persen kadar air dihitung dengan persamaan:
% Kadar air = 100%
Dengan:
Uji Flavonoid
Uji kualitatif flavonoid dilakukan mengacu pada Harborne (1987). Sebanyak 1 g sampel berupa serbuk kering ditambahkan 10 mL air panas kemudian dididihkan selama 5 menit dan disaring. Sebanyak 10 mL filtrat ditambahkan 0.5 gram serbuk Mg, 1 mL HCl pekat, dan 1 mL amil alkohol kemudian dikocok dengan kuat. Uji positif ditandai dengan munculnya warna merah, kuning, atau jingga pada lapisan amil alkohol.
Ekstraksi Flavonoid Kaempferol
Ekstraksi flavonoid (Lampiran 1) mengacu pada Vega et al. (2007). Serbuk daun sirsak kering diekstraksi dengan maserasi menggunakan pelarut n-heksana dan metanol. Ekstraksi diawali dengan menggunakan pelarut n-heksana untuk menghilangkan kandungan lemak, selanjutnya sampel disaring dan dipisahkan. Ekstrak n-heksana dibuang dan residu dari hasil maserasi dengan n-heksana dikeringkan dengan diangin-anginkan di udara terbuka. Ekstraksi dilanjutkan dengan menggunakan pelarut metanol. Residu dari pelarut n-heksana dimaserasi dengan metanol dan selanjutnya ekstrak metanol dipartisi dengan diklorometana dan campuran metaol air dengan nisbah 2:1 untuk memberikan fraksi hidroalkohol dan diklorometana. Fraksi diklorometana dibuang dan yang digunakan adalah fraksi metanolik. Sebagian fraksi metanolik dipisahkan untuk uji hayati dan uji flavonoid, dan sebagian lain dihidrolisis dengan HCl 1.8 N. Larutan yang dihasilkan diekstraksi dengan amil alkohol. Selanjutnya fase organik diambil dan dicuci dengan air sampai pH fase organik konstan. Hasil hidrolisis diuapkan dengan penguap putar pada suhu 40 ºC dan dilakukan uji flavonoid dan uji penghambatannya terhadap sel kanker. Rendemen ekstrak dihitung dengan persamaan:
% Rendemen ekstrak = × 100 %
dengan
Pemilihan Eluen Terbaik
Eluen terbaik untuk mengisolasi senyawa kaempferol dipilih dengan menggunakan kromatografi lapis tipis (KLT). Pelat KLT yang digunakan adalah jenis silika G60F254. Ekstrak pekat ditotolkan pada pelat KLT, setelah kering, langsung dielusi dalam ruang elusi yang telah dijenuhkan oleh uap eluen pengembang. Eluen yang digunakan yaitu HCO2H-H2O-MeOH. Noda hasil elusi diamati di bawah lampu UV pada panjang gelombang 254 dan 366 nm.
Fraksionasi Menggunakan Kromatografi Lapis Tipis Preparatif
Ekstrak metanol hasil hidrolisis dipisahkan dengan menggunakan kromatografi lapis tipis preparatif (KLTP). Fraksi yang diperoleh selanjutnya dikerok, dilarutkan, dan didekantasi dengan pelarut awalnya, yaitu metanol, kemudian disaring lalu diuapkan. Hasil fraksinasi dengan KLTP kemudian diidentifikasi kandungan senyawa flavonoidnya dengan spekrofotometer kromatografi cair kinerja tinggi (KCKT) dan diuji aktivitas antikankernya pada sel kanker secara in vitro.
Uji aktivitas Penghambatan Proliferasi terhadap Sel Vero dan Sel Raji
(Sigma, USA) sebanyak 10 µL/sumur selama 4 jam hingga terbentuk formazan berwarna ungu pada sel hidup. Selanjutnya ditambahkan HCl ke dalam isopropanol 0.1 N sebanyak 100 µL/sumur kemudian diinkubasi kembali selama 10 menit dan dibaca serapannya dengan menggunakan spektrofotometer ELISA reader dengan panjang gelombang 595 nm. Penghambatan pertumbuhan sel kanker dihitung menggunakan rumus berikut:
% penghambatan = Serapan kontrol – serapan perlakuan
Serapan kontrol × 100 %
Dari % penghambatan yang diperoleh selanjutnya ditentukan penghambatan sel kanker dari setiap konsentrasi senyawa flavonoid yang diujikan dan ditentukan aktivitas penghambatan yang terbesar dari senyawa flavonoid yang diperoleh.
HASIL
Kadar Air
Kadar air sampel daun sirsak adalah, 5.24 %. Kadar air dalam suatu bahan yang dapat mengurangi aktivitas mikrob 3-7%. Kadar air pada kisaran tersebut juga lebih stabil dan terhindar dari enzim oksidasi.
Kandungan Flavonoid
Kandungan flavonoid ditentukan dalam dua tahap, yaitu pada serbuk daun dan ekstrak metanolik daun. Berdasarkan uji flavonoid dengan uji fitokimia secara kualitatif, serbuk daun dan ekstrak metanolik daun sirsak positif mengandung flavonoid. Secara kualitatif dapat dilihat dari intensitas warna ekstrak metanolik dan serbuk yang tidak berbeda dari intensitas warna serbuk daun. Hal ini menunjukkan bahwa pelarut metanol yang telah dipartisi dengan diklorometana dan air efektif dalam mengekstrak flavonoid dari daun sirsak. Intensitas warna flavonoid yang terkandung dalam daun sirsak dapat dilihat pada Gambar 1.
A B
Gambar 1 Hasil uji fitokimia flavonoid pada serbuk daun (A) dan ekstrak metanol (B).
Ekstrak Flavonoid
Efektivitas Ekstrak Metanol terhadap Proliferasi sel Vero
Ekstrak metanolik diujikan terlebih dahulu pada sel normal. Uji pendahuluan ini dilakukan untuk menentukan konsentrasi yang diperlukan guna diujicobakan pada sel kanker yang tidak merusak sel normal.
Uji pendahuluan dari ekstrak metanolik pada sel Vero menggunakan berbagai konsentrasi, mulai dari 25000 µg mL-1 sampai 500 µg mL-1. Hasilnya dapat dilihat pada Tabel 1. Semakin tinggi konsentrasi ekstrak semakin besar pula penghambatannya pada proliferasi sel Vero. Penghambatan ekstrak metanolik daun sirsak menurun pada konsentrasi 1000 µg mL-1 dan 500 µg mL-1 dengan penghambatan masing-masing 47.65% dan 31.49%. Berdasarkan hasil ini, ekstrak hasil fraksinasi daun sirsak yang diujikan adalah di bawah 500 µg mL-1 agar tidak menghambat proliferasi sel normal.
Tabel 1 Penghambatan proliferasi ekstrak kasar daun sirsak terhadap sel Vero.
Konsentrasi ekstrak µg mL-1
Rata-rata
serapan
% Penghambatan proliferasi
25000 0.032 80.37
15000 0.037 77.1
10000 0.033 79.96
5000 0.042 74.03
1500 0.046 71.98
1000 0.085 47.65
500 0.112 31.49
Kaempferol Hasil Kromatografi Lapis Tipis Preparatif
LT A)
T. KT
H, Vis
30 a b
A
B
Gambar 2 Profil KL eluen terbaik ekstraak kasar dauun sirsak (A menggunnakan eluen HCCO2H:H2O:MeOH dan profil KLT setelah hidrolisis (B).
Eksstrak kasar dipisahkann menggunnakan KLTPP dengan eluen dari hasil KLT, yaittu HCO2H:H2O:MeOH untuk meemperoleh senyawa kaaempferol. Hasil pemisahan dengan KLTP selaanjutnya diiuapkan hinngga pekat dan dipeeroleh rendemen sebanyak 223.45%.
Iddentitas Flaavonoid
Gambar 3 Spektrum UV-Vis ekstrak daun sirsak dalam metanol.
Hasil analisis menunjukkan bahwa ekstrak yang diperoleh memiliki waktu retensi yang hampir sama dengan standar kaempferol (≥ 90%) yang diperoleh dari Sigma-Aldrich, USA, sehingga diyakini bahwa senyawa yang diperoleh merupakan senyawa kaempferol (Gambar 4). Gambar hasil KCKT menunjukkan bahwa waktu retensi yang diperoleh dari ekstrak hasil KLTP ialah 3.395 dan standar kaempferol memiliki waktu retensi 3.384.
A B
mV DetectorACh2:370nm 45 40 35 mV DetectorACh2:370nm 15.0 12.5 30 10.0 25 20 15 10 5 0 -5 -10
0.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5 min
7.5 5.0 2.5 0.0
0.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5 min
%Pengham
batan
Penghambatan Proliferasi sel Vero dan sel Raji
Hasil pemisahan ekstrak daun sirsak dengan KLTP diuji daya hambat proliferasinya pada sel Vero dan Raji. Konsentrasi ekstrak yang digunakan ialah 3, 6.25, 12.5, 25, 50, 100, 125, dan 250 µg mL-1. Konsentrasi tertinggi pada 250 µg mL-1 dipilih berdasarkan hasil uji in vitro pada ekstrak kasar terhadap sel Vero. Hasil pada konsentrasi tersebut ialah konsentrasi tertinggi yang minimal toksisitasnya terhadap sel Vero.
100
80
60
40
20
0
‐20
‐40
0 50 100 150 200 250
Konsentrasi (µg/mL)
Sel Vero Sel Raji
Gambar 5 Kurva penghambatan proliferasi ekstrak hasil KLTP daun sirsak terhadap sel Raji (A) dan sel Vero (B).
Dari hasil uji pada sel Vero (Gambar 5), diperoleh bahwa kaempferol sampai dengan konsentrasi 250 µg mL-1 minimal menghambat proliferasi sel sebesar 19.77% sedangkan konsentrasi di bawah 100 µg mL-1 tidak ada penghambatan. Akan tetapi, pada uji sel Raji pada konsentrasi di atas 100 µg mL-1 mengalami peningkatan hambatan proliferasi sampai dengan 76.36% pada konsentrasi 250 µg mL-1 .
A B
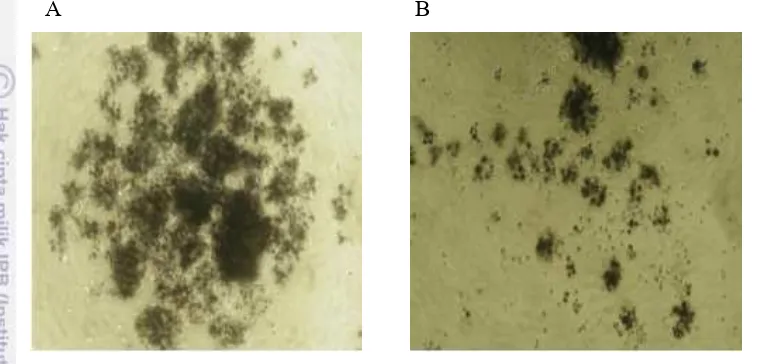
Gambar 6 Sel Raji tanpa pemberian ekstrak (A) dan sel Raji yang diberi ekstrak kaempferol 250 µg mL-1 (B) (Perbesaran 8×10).
Berdasarkan hasil uji MTT, secara makroskopis (Gambar 7) pada sel Vero menghasilkan warna ungu yang hampir sama dengan kontrol sel normal yang tidak diberi ekstrak.
A B
Gambar 7 Sel Vero (kontrol) pada uji MTT (A) dan sel Vero setelah pemberian ekstrak (B).
dibandingkan dengan kontrol, namun tidak dapat dihitung berapa jumlah penurunan sel yang mati, karena metode MTT tidak dapat digunakan untuk menghitung jumlah sel yang mati, hanya dapat menentukan persen penghambatan saja.
A B
Gambar 8 Sel Raji (kontrol) pada uji MTT (A) dan sel raji setelah pemberian ekstrak (B) (perbesaran 8×10).
Berdasarkan hasil perhitungan nilai IC50, hasil uji penghambatan terhadap sel Vero memperlihatkan bahwa ekstrak kasar baru dapat menghambat sel normal di atas 500 µg mL-1 dengan nilai IC50 922.88 µg mL-1.. Dari uji kaempferol hasil fraksinasi dengan KLTP pada sel normal dan sel kanker Raji, terlihat bahwa persen penghambatan pada sel kanker Raji lebih besar daripada sel Vero bahkan pada sel Vero dapat dikatakan tidak memiliki IC50 karena pada konsentrasi 250 µg mL-1 ekstrak kaempferol hanya menghambat proliferasi sel sebesar 19.77%.
Tabel 2. Nilai IC50 dari ekstrak kasar dan ekstrak kaempferol terhadap sel Vero dan sel Raji
Perlakuan Persamaan garis R2 IC50 Ekstrak metanolik pada sel
Vero
Ekstrak kaempferol pada sel Vero
Ekstrak kaempferol pada sel Raji
y=11.13 Ln x-25.99 0.759 922.86
y=7.52 Ln x-29.04 0.763 -
PEMBAHASAN
Uji fitokimia pada serbuk daun dan ekstrak daun sirsak bertujuan mendeteksi keberadaan flavonoid pada sampel awal daun sirsak sebelum tahap ekstraksi, sedangkan uji pada ekstrak kasar dilakukan untuk mengevaluasi efektivitas pelarut dalam mengekstrak flavonoid. Hasil uji fitokimia flavonoid, baik serbuk daun maupun ekstrak metanol, menyatakan kandungan flavonoid pada sampel, hal ini sesuai dengan penelitian Santos & Salatino (2000) yang melaporkan 31 spesies dari famili Annonaceae memiliki kandungan flavonoid di antaranya adalah kaempferol dan kuersetin. Namun, penelitian Pathak et al. (2010) melaporkan bahwa dari uji fitokimia tidak terdeteksi flavonoid dalam daun sirsak. Perbedaan laporan ini kemungkinan disebabkan perbedaan tempat tumbuh sehingga isolat yang dihasilkan juga berbeda-beda.
Proses ekstraksi senyawa flavonoid dilakukan dengan metode maserasi. Ekstraksi awal dilakukan dengan pelarut n-heksana yang bersifat nonpolar. Tujuan penggunaan pelarut ini adalah untuk menghilangkan kandungan lemak yang ada dalam daun sirsak. Selain itu untuk memudahkan perolehan senyawa flavonoid yang pada umumnya bersifat polar. Oleh karena itu dengan menggunakan pelarut n-heksana, ekstrak terbebas dari lemak. Partisi dengan diklorometana yang bersifat semipolar dilakukan untuk memisahkan senyawa- senyawa yang bersifat semipolar, sedangkan campuran metanol-air bertujuan memperoleh senyawa flavonoid yang lebih banyak karena sebagian besar senyawa flavonoid di alam ditemukan dalam bentuk glikosida, yaitu satu unit flavonoid terikat pada suatu gula. Adanya gula yang terikat pada flavonoid cenderung menyebabkan flavonoid lebih mudah larut dalam air, dengan demikian campuran pelarut metanol dengan air merupakan pelarut yang lebih baik untuk melarutkan glikosida (Harborne 1987).
senyawa yang dihasilkan merupakan senyawa kaempferol dengan waktu retensi yang hampir sama antara waktu retensi kaempferol standar dengan kaempferol dari ekstrak hasil KLTP. Bila dibandingkan dengan standar kaempferol dengan konsentrasi 90%, hasil yang diperoleh sedikit sekitar 0.22 µg mL-1 dalam 10 µg mL-1 hasil KLTP. Penelitian Vega et al. (2007) tidak melaporkan rendemen, kaempferol namun dari dosis ekstrak kaempferol yang diberikan pada sel kanker karsinoma Erlich dapat diketahui, kadar kaempferol sebanyak 0.022 µg mL-1. Berdasarkan perbandingan perolehan kaempferol ini dapat disimpulkan bahwa kaempferol yang diperoleh pada daun A.muricata lebih banyak daripada A. dioca.
Berdasarkan pengamatan secara makroskopis, bentuk dan ukuran sel lebih besar daripada sel normal. Kemungkinan senyawa kaempferol masuk ke dalam mitokondria dari sel kanker dan merusak sel sehingga ukuran sel menjadi besar yang menyebabkan sel menjadi mati. Dari Gambar 6 disimpulkan, kemungkinan kematian sel terjadi melalui proses nekrosis. Nekrosis merupakan proses kerusakan sel yang dapat ditandai dengan meningkatnya volume sel (Nursid et al. 2006). Sel yang mengalami nekrosis akan terlihat membengkak untuk kemudian mengalami lisis. Nekrosis disebabkan oleh faktor eksternal di antaranya, yaitu infeksi, toksiksitas, trauma sel, dan kematian prematur pada sel (Prasetyo 2008).
Nilai IC50 akibat pemberian ekstrak kaempferol pada sel kanker Raji sangat berbeda dengan ekstrak kaempferol hasil penelitian Vega et al. (2007) yang diuji pada sel kanker karsinoma Erlich dengan IC50 0.022 µg mL-1. IC50 pada sel kanker Raji sebesar 110.82 µgmL-1. Nilai IC50 ekstrak daun A. dioca yang diperoleh Vega et al. (2007), lebih rendah daripada ekstrak A.muricata yang berarti ekstrak daun A. dioca lebih toksik dibandingkan daun sirsak. Hal tersebut kemungkinan disebabkan beberapa hal diantaranya karena perbedaan sel kanker yang diuji, dan perbedaan sampel tanaman meskipun masih satu genus. Kemungkinan yang lain juga disebabkan flavonoid yang dihasilkan mempunyai aktivitas yang berbeda terhadap berbagai jenis sel kanker.
SIMPULAN
DAN
SARAN
Simpulan
Berdasarkan hasil isolasi senyawa flavonoid dari daun sirsak, dikuatkan dengan spektrum KCKT, diperoleh senyawa flavonoid kaempferol. Ekstrak kaempferol dari daun sirsak memiliki daya hambat proliferasi terhadap sel Raji sekitar 76% pada konsentrasi 250 µg mL-1 dan pada sel Vero mendekati 20% pada konsentrasi yang sama. Kaempferol dari daun sirsak memberi efek toksik yang kecil pada sel normal dibandingkan dengan sel kanker.
Saran
DAFTAR
PUSTAKA
Adewole SO, Ojewole JAO. 2009. Protective effects of Annona muricata Linn. (Annonaceae) leaf aqueous extract on serum lipid profiles and oxidative stress in hepatocytes of streptozotocin-treated diabetic rats. African Journal Traditional CAM 6:30-41.
[AOAC] Association of Official Analytical Chemist. 2006. Official method of
analysis of the association of official analytical chemist. Edisi ke-18.
Washington DC: AOAC.
Coloma AG, Guadano A, Ines CD, Diaz RM, Cortes D. 2002. Selective action of acetogenin mitochondrial complex I inhibitors. Zeitschrift Für Naturforsh 57:1028-1034.
De Sousa OV, Del-Vechio VD, Pinho JRG, Yamamoto CH, Alves MS. 2010. Antinociceptive and anti-inflamatory activities of the ethanol extract of Annona muricata L. leaves in animal models. International Journal Molecules Science 11:2067-2078.
Etcheverry S, Shapaz S, Fall D, Laurens A, Cave A. 1994. Annoglaucin, an acetogenin from Annona glauca. Phytochemistry 38:1423-1426.
Harborne JB. 1987. Metode Fitokimia: Penuntun cara modern menganalisis tumbuhan. Terbitan ke-2. K Padmawinata & I Soediro, penerjemah; Bandung: ITB. Terjemahan dari Phytochemical Methods.
Kim GS, et al. 1998. Muricoreacin and murihexocin C, monotetrahydrofuran acetogenins, from the leaves of Annona muricata. Phytochemstry 49:565- 571.
Liu RH, Liu J, Chen B. 2005. Apples prevent mammary tumors in rats. Journal Agriculture Food Chemistry 53:2342-2343.
Luo H, Daddysman M, Rankin GO, Jiang B, Chen YC. 2010. Kaempferol enhances cisplatin’s effect on ovarians cancer through promoting apoptosis caused by down regulation of cMyc. Cancer Cell International 10:1-9.
Markham KR. 1988. Cara mengidentifikasi flavonoid. Padmawinata K, penerjemah. Bandung: ITB.
Miller AL. 1996. Antioxidant flavonoids: structure, function, and clinical usage. Alternative Medicine Review 1:103-111.
Nursid M, Wikanta T, Fajarningsih ND, Marraskuranto E. 2006. Aktivitas sitotoksik, induksi apoptosis, dan ekspresi gen p53 fraksi metanol spons Petrosia cf.nigricans terhadap sel tumor HeLa. Jurnal Pascapanen dan Bioteknologi Kelautan dan Perikanan 1:103-110.
Olawale AD, Aderibigde KO, Stephen AO, Martins OE, Kehinde AT. 2009. Anti hyperglycemic activities of Annona muricata Linn. African Journal Traditional CAM 6:62-69.
Pathak P, Vora S, Savai J. 2010. In vitro antimicrobial activity and phytochemical analysis of the leaves of Annona muricata. International Journal of Pharma Reseach & Development 2:1-6.
Presetyo AA. 2008. Beda apoptosis dan nekrosis. http://afie.staff.uns.ac.id/2008/12/25/beda-apoptosis-dan-nekrosis/.
Sajuthi D. 2001. Ekstraksi, fraksinasi, dan uji hayati in vitro senyawa bioaktif daun dewa (Gynura pseudochina (Linn.) DC.) sebagai antikanker, tahap II. Buletin Kimia 1:75-79.
Santos DYAC, Salatino MLF. 2000. Foliar flavonoids of annonaceae from Brazil: taxonomic significance. Phytochemistry 55:567-573.
Vega MRG, et al. 2007. Flavonoids from Annona dioica leaves and their effects in Erlich carcinoma cells, DNA-topoisomerase I and II. Journal Brazzil Chemistry Society 18:1554-1559.
Xiao ZP et al. 2006. Kaempferol and quercetin flavonoids from Rosa rugosa. Chemistry of Natural Compounds 42:736-737.
Wang Y et al. 2009. Screening antitumor compounds psoralen and isopsoralen from Psoralea coryfolia L. seeds. eCAM Advance Access 1-7.
Yoshida T et al. 2008. Kaempferol sensitizes colon cancer cells to TRAIL- induceed apoptosis. Biochemistry Biophysics Commun 375:129-133.
Lapisan MeOH : H2O
Lampiran 2 Bagan alir penelitian
Metode ekstraksi kaempferol (Vega et al. 2007)
Serbuk daun sirsak
dimaserasi (n-heksana); disaring Ekstrak n-heksana Residu
CH2Cl2
MeOH : H2O = 2 : 1
diuji flavonoid Lapisan CH2Cl2
Fraksinasi KLTP, eluen HCO2H-H2O-MeOH
Uji aktivitas penghambatan
proliferasi pada sel normal
Fraksi 1
Fraksi 2 Fraksi n
Uji flavonoid
Identifikasi flavonoid UV, KCKT
Lampiran 3 Bagan alir metode MTT
Uji aktivitas antikanker menggunakan metode MTT (Wang et at. 2009)
Penumbuhan sel
Dinkubasi sel pada suhu 37 °C selama 24 jam
Ditambah senyawa flavonoid dengan konsentrasi 3, 6.25, 12.5, 25, 50, 100, 125, 250 ppm
Diinkubasi pada suhu 37 °C selama 48 jam
+ 10 µL MTT 5
Diinkubasi 37 °C selama 4
+ 100 µL HCl 0,1 N dalam isopropanol 10%
Diinkubasi selama 10 menit
k t k ( L ) S
(b) ( b)/ %
Serapan 1 Serapan 2 Serapan 3 Rata-rata
Lampiran 4 Data hasil uji penghambatan ekstrak kasar terhadap sel Vero Konsentrasi 1 Serapan 2 Serapan 3 rata-rata penghambatan Kontrol sel
25000 0.157 0.035 0.154 0.025 0.177 0.036 0.163 0.032 0 0.804 0 80.37 15000 0.029 0.047 0.036 0.037 0.771 77.10 10000 0.027 0.038 0.033 0.033 0.800 79.96 5000 0.031 0.058 0.038 0.042 0.740 74.03 1500 0.031 0.051 0.055 0.046 0.720 71.98 1000 0.048 0.072 0.136 0.085 0.476 47.65 500 0.062 0.109 0.164 0.112 0.315 31.49
Kontrol sel
(a) 0.157 0.154 0.177 0.163
Contoh perhitungan % penghambatan sel
% penghambatan = Rerata serapan kontrol sel-Rerata serapan sampel
Rerata serapan kontrol sel × 100 %
= (0.804-0.163) 0.804 = 80.37%
K ae m pf er ol /3 .4 21 /7 89 45 8 K ae m pfer ol/ 3.3 84/ 790 638 K a em pf e rol /3 .4 21 /7 8 9 4 5 8
Lampiran 5 Kromatogram standar kaempferol pada konsentrasi 10 µg mL-1
mV
45 Detector A Ch2:370nm
40 35 30 25 20 15 10 5 0 -5
0.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5 min
mV
Detector A Ch2:370nm 45 40 35 30 25 20 15 10 5 0 -5 -10
0.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5 min
mV
45 Detector A Ch2:370nm
40 35 30 25 20 15 10 5 0 -5
Ka emp fe rol /3 .395 /171 37 Ka em pf er ol /3 .318 /170 47
Lampiran 6 Kromatogram hasil KLTP daun sirsak
mV
Detector A Ch2:370nm
15.0 12.5 10.0 7.5 5.0 2.5 0.0
0.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5 min
mV
17.5 Detector A Ch2:370nm 15.0 12.5 10.0 7.5 5.0 2.5 0.0
Lampiran 7 Penentuan kadar kaempferol dalam daun sirsak hasil KLTP dengan metode KCKT
A. Standar kaempferol
Ulangan Waktu retensi Luas puncak Konsentrasi (%)
1 3.421 789458 90
2 3.384 790638 90.067
3 3.421 789458 89.955
Rerata 3.408 789851 90.007 % RSD 0.621 0.086 0.063
B. Ekstrak hasil KLTP
Ulangan Waktu retensi Luas puncak Konsentrasi (%)
1 3.395 17137 1.953
2 3.318 17047 1.942
Rerata 3.357 17093 1.948
( L ) S S
(b) ( b)/ %
Lampiran 8 Data hasil penghambatan flavonoid kaempferol dari daun sirsak terhadap proliferasi sel Vero
Konsentrasi
1 2
Serapan 3
Rata-rata
Penghambatan Kontrol sel
250
0.119 0.047
0.118 0.094
0.115 0.14
0.117 0.094
0 0.198
0 19.77 125 0.08 0.091 0.157 0.109 0.064 6.35 100 0.096 0.101 0.132 0.110 0.061 6.07 50 0.131 0.119 0.14 0.130 -0.113 -11.35 25 0.116 0.116 0.148 0.127 -0.085 -8.49 12.5 0.141 0.133 0.101 0.125 -0.071 -7.07 6.25 0.149 0.127 0.098 0.125 -0.068 -6.78 3 0.149 0.167 0.117 0.144 -0.236 -23.63
Kontrol sel
Serapan 1 Serapan 2 Serapan 3 Rata-rata (a) 0.119 0.118 0.115 0.117
Contoh perhitungan % penghambatan sel Vero oleh senyawa falvonoid kaempferol sama seperti perhitungan % penghambatan ekstrak kasar daun sirsak.
( L ) S
(b) ( b)/b %
Lampiran 9 Data hasil penghambatan flavonoid kaempferol dari daun sirsak terhadap proliferasi sel Raji
Konsentrasi 1 Serapan 2 Serapan 3 Rata-rata penghambatan Kontrol media 250 0.109 0.044 0.109 0.04 0.109 0.038 0.109 0.041 0 0.026 0 76.36 125 0.082 0.072 0.062 0.072 0.057 48.18 100 0.077 0.07 0.076 0.074 0.059 46.06 50 0.089 0.102 0.1 0.097 0.082 25.45 25 0.108 0.094 0.097 0.100 0.085 23.03 12.5 0.099 0.1 0.099 0.099 0.084 23.33 6.25 0.111 0.115 0.11 0.112 0.097 11.82 3 0.119 0.118 0.123 0.120 0.105 4.55
Kontrol Media
Serapan 1 Serapan 2 Serapan 3 Rata-rata (a) 0.109 0.109 0.109 0.109
Contoh perhitungan % penghambatan sel
% penghambatan = Rerata serapan kontol media-Rerata serapan sampel
Serapan kontrol media × 100 %
= (0.109-0.026) 0.109 = 76.36%
Lampiran 10 Gambar sel Vero (sel normal)
Sel Lestari Vero Normal
BAIQ AYU A. MUSTARIANI. Potential of Kaempferol Soursop Leaves as
Inhibitor Raji Cancer Cell Proliferation. Under direction of
SUMINAR S.
ACHMADI, IRMA H. SUPARTO, and SILMI MARIYA.
Leaves of soursop (
Annona muricata
) has been widely studied, particularly
as anti-cancer, but research on flavonoids as anticancer partion isolated from the
leaves of the soursop has not been found. Therefore, the purpose of this study is to
determine the effectiveness of flavonoids isolated from leaves of the soursop in
inhibiting cancer cell proliferation using Raji cells (ATCC CCL-86), Extraction
was done by maceration technique using successive solvents, i.e.
n
-hexane,
CH
2Cl
2and MeOH-H
2O. Separation of active extract used preparative thin layer
chromatography. Methanolic activity assay extract was performed on normal cells
to determination initial concentration on cancer cells showed, that the lowest
inhibition was at concentrations of 1000 µg mL
-1−
500 µg mL
-1with percent
inhibition 48% and 31%, respectively. The flavonoids produced a single spot on
thin layer chromatograph with Rf value of 0.87. Identification of flavonoids by
UV-Vis spectrometer and high performance liquid chromatography confirmed
that the flavonoid was kaempferol. Kaempferol extract obtained wastested on Raji
cells and Vero cells. For Raji cells the methanolic extract inhibited 76% of the
cells at concentration of 250 µg mL
-1but for the normal cells it only inhibited
20%. These results suggest that kaempferol from the soursop leaf can inhibit cell
proliferation of Raji cells but gives minimal toxic effect on Vero cells.
Latar Belakang
Sirsak (
Annona
muricata
) merupakan salah satu tanaman famili dari
Annonaceae yang sangat potensial dalam mengobati penyakit kanker. Biji dan
daun sirsak sebagai antikanker secara empiris telah banyak digunakan, akan tetapi
senyawa yang lebih banyak diteliti sebagai agen antikanker pada sirsak adalah
senyawa
annonaceous
asetogenin yang merupakan suatu poliketida, salah satu
metabolit sekunder dari famili Annonaceae (Etcheverry
et al.
1994, Coloma
et al.
2002). Penelitian tentang senyawa-senyawa lain dalam tanaman ini yang
diperkirakan aktif sebagai antikanker belum banyak ditelusuri di antaranya ialah
senyawa flavonoid.
Hasil penelitian Vega
et al
. (2007) menunjukkan bahwa golongan flavonoid
daun
A
.
dioca,
salah satu genus dari sirsak memiliki aktivitas dalam menghambat
pertumbuhan sel kanker karsinoma Ehrlich. Hasil ini membuktikan bahwa
senyawa flavonoid famili Annonaceae memiliki aktivitas farmakologis sebagai
antikanker. Penelitian yang dilakukan oleh Santos & Salatino (2000)
menunjukkan bahwa kandungan golongan flavonoid daun genus Annona di
antaranya adalah kuersetin dan kaempferol. Kedua senyawa ini diduga berpotensi
sebagai antikanker sebagaimana diindikasikan oleh Liu
et al.
(2005), Vega
et al
.
(2007), Yoshida
et al.
(2008), dan, Luo
et al.
(2010).
Penelitian ini bertujuan menguji efektivitas isolat flavonoid dari daun sirsak
dalam menghambat pertumbuhan sel kanker Raji secara
in vitro
.
Manfaat Penelitian
Tempat Penelitian
Penelitian dilakukan di Laboratorium Kimia Organik, Departemen Kimia,
Fakultas Matematika dan Ilmu Pengetahun Alam, Institut Pertanian Bogor (IPB).
Uji penghambatan proliferasi terhadap sel secara
in vitro
dilakukan di Pusat Studi
Satwa Primata (PSSP) IPB.
Bahan Tumbuhan dan Subjek Uji
Bahan yang digunakan adalah daun sirsak tua yang diperoleh dari kebun
Pusat Studi Biofarmaka IPB. Untuk keperluan identifikasi tumbuhan, sampel
dikirim ke Herbarium Bogoriense, Bogor. Pada tahap awal daun sirsak
dibersihkan dengan air. Selanjutnya daun dikeringkan dalam oven dengan suhu
40 ºC selama 72 jam, lalu dijadikan serbuk untuk kemudian diekstraksi. Subjek uji
yang digunakan adalah penghambatan aktivitas sel Vero (ATCC CCL-81) dan sel
Raji (ATCC CCL-86). Kedua jenis sel ini diperoleh dari PSSP
Penentuan Kadar Air
Cawan porselin dikeringkan pada suhu 105 °C dalam oven selama 30 menit,
kemudian didinginkan dalam eksikator dan ditimbang. Sebanyak 5 g serbuk daun
sirsak dimasukkan ke dalam cawan dan dipanaskan dalam oven pada suhu 105 °C
selama 3 jam, kemudian cawan diangkat dan didinginkan dalam eksikator selama
30 menit. Cawan dengan sampel ditimbang hingga diperoleh bobot konstan
(AOAC 2006). Persen kadar air dihitung dengan persamaan:
% Kadar air =
×
100%
Dengan:
Uji kualitatif flavonoid dilakukan mengacu pada Harborne (1987).
Sebanyak 1 g sampel berupa serbuk kering ditambahkan 10 mL air panas
kemudian dididihkan selama 5 menit dan disaring. Sebanyak 10 mL filtrat
ditambahkan 0.5 gram serbuk Mg, 1 mL HCl pekat, dan 1 mL amil alkohol
kemudian dikocok dengan kuat. Uji positif ditandai dengan munculnya warna
merah, kuning, atau jingga pada lapisan amil alkohol.
Ekstraksi Flavonoid Kaempferol
Ekstraksi flavonoid (Lampiran 1) mengacu pada Vega
et al
. (2007). Serbuk
daun sirsak kering diekstraksi dengan maserasi menggunakan pelarut
n
-heksana
dan metanol. Ekstraksi diawali dengan menggunakan pelarut
n
-heksana untuk
menghilangkan kandungan lemak, selanjutnya sampel disaring dan dipisahkan.
Ekstrak
n
-heksana dibuang dan residu dari hasil maserasi dengan
n
-heksana
dikeringkan dengan diangin-anginkan di udara terbuka. Ekstraksi dilanjutkan
dengan menggunakan pelarut metanol. Residu dari pelarut
n
-heksana dimaserasi
dengan metanol dan selanjutnya ekstrak metanol dipartisi dengan diklorometana
dan campuran metaol air dengan nisbah 2:1 untuk memberikan fraksi
hidroalkohol dan diklorometana. Fraksi diklorometana
dibuang dan yang
digunakan adalah fraksi metanolik. Sebagian fraksi metanolik dipisahkan untuk
uji hayati dan uji flavonoid, dan sebagian lain dihidrolisis dengan HCl 1.8 N.
Larutan yang dihasilkan diekstraksi dengan amil alkohol. Selanjutnya fase organik
diambil dan dicuci dengan air sampai pH fase organik konstan. Hasil hidrolisis
diuapkan dengan penguap putar pada suhu 40 ºC dan dilakukan uji flavonoid dan
uji penghambatannya terhadap sel kanker. Rendemen ekstrak dihitung dengan
persamaan:
% Rendemen ekstrak =
× 100 %
dengan
Eluen terbaik untuk mengisolasi senyawa kaempferol dipilih dengan
menggunakan kromatografi lapis tipis (KLT). Pelat KLT yang digunakan adalah
jenis silika G
60F
254. Ekstrak pekat ditotolkan pada pelat KLT, setelah kering,
langsung dielusi dalam ruang elusi yang telah dijenuhkan oleh uap eluen
pengembang. Eluen yang digunakan yaitu HCO
2H-H
2O-MeOH. Noda hasil elusi
diamati di bawah lampu UV pada panjang gelombang 254 dan 366 nm.
Fraksionasi Menggunakan Kromatografi Lapis Tipis Preparatif
Ekstrak metanol hasil hidrolisis dipisahkan dengan menggunakan
kromatografi lapis tipis preparatif (KLTP). Fraksi yang diperoleh selanjutnya
dikerok, dilarutkan, dan didekantasi dengan pelarut awalnya, yaitu metanol,
kemudian disaring lalu diuapkan. Hasil fraksinasi dengan KLTP kemudian
diidentifikasi kandungan senyawa flavonoidnya dengan spekrofotometer
kromatografi cair kinerja tinggi (KCKT) dan diuji aktivitas antikankernya pada sel
kanker secara
in vitro
.
Uji aktivitas Penghambatan Proliferasi terhadap Sel Vero dan Sel Raji
Uji aktivitas penghambatan kanker dari sel Raji dilakukan merujuk pada Sajuthi
(2001) dan Wang
et al
. (2009). Sel Vero dan sel Raji ditumbuhkan terlebih
dahulu. Media tumbuh yang digunakan ialah DMEM (Dulbecco’s Modified
Eagle’s Medium) untuk sel Vero dan RPMI (Roswell Park Memorial
Institute)-1640 untuk sel Raji dengan penambahan masing-masing 10% FBS dan 1%
penisilin-streptomisin. Sel didistribusikan ke dalam pelat kultur jaringan 96 sumur
dengan konsentrasi sel yang digunakan ialah 2×10
3sel/mL per sumur. Selanjutnya
sel diinkubasi selama 24 jam dalam inkubator CO
2dengan konsentrasi 5% pada
berwarna ungu pada sel hidup. Selanjutnya ditambahkan HCl ke dalam
isopropanol 0.1 N sebanyak 100 µL/sumur kemudian diinkubasi kembali selama
10 menit dan dibaca serapannya dengan menggunakan spektrofotometer ELISA
reader
dengan panjang gelombang 595 nm. Penghambatan pertumbuhan sel
kanker dihitung menggunakan rumus berikut:
% penghambatan = Serapan kontrol – serapan perlakuan
× 100 %
× 100 %
Serapan
kontrol
Dari % penghambatan yang diperoleh selanjutnya ditentukan penghambatan
sel kanker dari setiap konsentrasi senyawa flavonoid yang diujikan dan ditentukan
aktivitas penghambatan yang terbesar dari senyawa flavonoid yang diperoleh.
Nilai IC
50ditentukan dari grafik persen sel hidup vs log konsentrasi sampel
uji (Wang
et al.
2009). Nilai IC
50ditentukan dengan menggunakan persamaan
Kadar Air
Kadar air sampel daun sirsak adalah, 5.24 %. Kadar air dalam suatu bahan yang
dapat mengurangi aktivitas mikrob 3-7%. Kadar air pada kisaran tersebut juga
lebih stabil dan terhindar dari enzim oksidasi.
Kandungan Flavonoid
Kandungan flavonoid ditentukan dalam dua tahap, yaitu pada serbuk daun
dan ekstrak metanolik daun. Berdasarkan uji flavonoid dengan uji fitokimia secara
kualitatif, serbuk daun dan ekstrak metanolik daun sirsak positif mengandung
flavonoid. Secara kualitatif dapat dilihat dari intensitas warna ekstrak metanolik
dan serbuk yang tidak berbeda dari intensitas warna serbuk daun. Hal ini
menunjukkan bahwa pelarut metanol yang telah dipartisi dengan diklorometana
dan air efektif dalam mengekstrak flavonoid dari daun sirsak. Intensitas warna
flavonoid yang terkandung dalam daun sirsak dapat dilihat pada Gambar 1.
A
B
Gambar 1 Hasil uji fitokimia flavonoid pada serbuk daun (A) dan ekstrak
metanol (B).
Ekstrak Flavonoid
Ekstrak metanolik diujikan terlebih dahulu pada sel normal. Uji
pendahuluan ini dilakukan untuk menentukan konsentrasi yang diperlukan guna
diujicobakan pada sel kanker yang tidak merusak sel normal.
Uji pendahuluan dari ekstrak metanolik pada sel Vero menggunakan
berbagai konsentrasi, mulai dari 25000 µg mL
-1sampai 500 µg mL
-1. Hasilnya
dapat dilihat pada Tabel 1. Semakin tinggi konsentrasi ekstrak semakin besar pula
penghambatannya pada proliferasi sel Vero. Penghambatan ekstrak metanolik
daun sirsak menurun pada konsentrasi 1000 µg mL
-1dan 500 µg mL
-1dengan
penghambatan masing-masing 47.65% dan 31.49%. Berdasarkan hasil ini, ekstrak
hasil fraksinasi daun sirsak yang diujikan adalah di bawah 500 µg mL
-1agar tidak
menghambat proliferasi sel normal.
Tabel 1 Penghambatan proliferasi ekstrak kasar daun sirsak terhadap sel Vero.
Konsentrasi ekstrak
µg mL-1
Rata-rata
serapan
% Penghambatan
proliferasi
25000 0.032
80.37
15000 0.037
77.1
10000 0.033
79.96
5000 0.042
74.03
1500 0.046
71.98
1000 0.085
47.65
500 0.112
31.49
Kaempferol Hasil Kromatografi Lapis Tipis Preparatif
Gambar 2
Eks
KLT, yait
pemisahan
rendemen
Flav
gambaran
flavonoid
spektrome
C18, pada
asam fosf
satu punca
(Gambar 3
Profil KL
eluen HC
strak kasar
tu HCO
2H:
n dengan K
sebanyak 2
vonoid yang
yang jela
yang terka
eter UV-Vis
a laju alir 1
fat 0.5%. H
ak serapan m
3).
A
LT eluen te
CO
2H:H
2O
dipisahkan
H
2O:MeOH
KLTP sela
23.45%.
Id
g dicari, yai
as tentang
andung di d
s dan KCKT
1ml/menit,
Hasil identif
maksimum
rbaik ekstra
:MeOH dan
n menggun
H untuk me
anjutnya di
dentitas Fla
itu kaempfe
struktur
dalam daun
T. Kondisi
detektor UV
fikasi denga
di daerah p
ak kasar dau
n profil KLT
nakan KLTP
emperoleh
iuapkan hin
avonoid
erol, diiden
senyawa y
sirsak dide
untuk KCK
V 370 nm,
an spektrom
panjang gelo
B
un sirsak (A
T setelah hi
A) menggun
drolisis (B)
nakan
.
P dengan
senyawa ka
ngga pekat
eluen dari
aempferol.
t dan dipe
hasil
Hasil
eroleh
ntifikasi unt
yang diingi
eteksi denga
KT dilakuka
dengan elu
meter Uv-V
ombang 250
tuk mendap
inkan. Sen
an menggun
an dengan k
uen MeOH
Vis menunju
0 sampai 30
Gambar 3 Spektrum UV-Vis ekstrak daun sirsak dalam metanol.
Hasil analisis menunjukkan bahwa ekstrak yang diperoleh memiliki waktu
retensi yang hampir sama dengan standar kaempferol (
≥
90%) yang diperoleh dari
Sigma-Aldrich, USA, sehingga diyakini bahwa senyawa yang diperoleh
merupakan senyawa kaempferol (Gambar 4). Gambar hasil KCKT menunjukkan
bahwa waktu retensi yang diperoleh dari ekstrak hasil KLTP ialah 3.395 dan
standar kaempferol memiliki waktu retensi 3.384.
A B
0.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5 min -10 -5 0 5 10 15 20 25 30 35 40 45 mV
Detector A Ch2:370nm
K ae m pf er o l/ 3. 38 4 /79 0 6 3 8
0.0 0.5 1.0 1.5 2.0 2.5 3.0 3.5 4.0 4.5 5.0 5.5 min 0.0 2.5 5.0 7.5 10.0 12.5 15.0 mV
Detector A Ch2:370nm
K a em p fe ro l/ 3 .3 95 /1 71 3 7
[image:55.595.176.385.87.314.2]Hasil pemisahan ekstrak daun sirsak dengan KLTP diuji daya hambat
proliferasinya pada sel Vero dan Raji. Konsentrasi ekstrak yang digunakan ialah
3, 6.25, 12.5, 25, 50, 100, 125, dan 250 µg mL
-1. Konsentrasi tertinggi pada 250
µg mL
-1dipilih berdasarkan hasil uji
in vitro
pada ekstrak kasar terhadap sel Vero.
Hasil pada konsentrasi tersebut ialah konsentrasi tertinggi yang minimal
toksisitasnya terhadap sel Vero.
‐40
‐20 0 20 40 60 80 100
0 50 100 150 200 250
%
Penghambatan
Konsentrasi (µg/mL)
Sel Vero
Sel Raji
Gambar 5 Kurva penghambatan proliferasi ekstrak hasil KLTP daun sirsak
terhadap sel Raji (A) dan sel Vero (B).
Dari hasil uji pada sel Vero (Gambar 5), diperoleh bahwa kaempferol
sampai dengan konsentrasi 250 µg mL
-1minimal menghambat proliferasi sel
sebesar 19.77% sedangkan konsentrasi di bawah 100 µg mL
-1tidak ada
penghambatan. Akan tetapi, pada uji sel Raji pada konsentrasi di atas 100 µg mL
-1mengalami peningkatan hambatan proliferasi sampai dengan 76.36% pada
konsentrasi 250 µg mL
-1.
Gambar 6 Sel Raji tanpa pemberian ekstrak (A) dan sel Raji yang diberi ekstrak
kaempferol 250 µg mL
-1(B) (Perbesaran 8×10).
Berdasarkan hasil uji MTT, secara makroskopis (Gambar 7) pada sel Vero
menghasilkan warna ungu yang hampir sama dengan kontrol sel normal yang
tidak diberi ekstrak.
A B
Gambar 7 Sel Vero (kontrol) pada uji MTT (A) dan sel Vero setelah
pemberian ekstrak (B).
penurunan sel yang mati, karena metode MTT tidak dapat digunakan untuk
menghitung jumlah sel yang mati, hanya dapat menentukan persen penghambatan
saja.
A
B
[image:58.595.117.511.171.362.2]Gambar 8 Sel Raji (kontrol) pada uji MTT (A) dan sel raji setelah
pemberian ekstrak (B) (perbesaran 8×10).
Berdasarkan hasil perhitungan nilai IC
50, hasil uji penghambatan terhadap
sel Vero memperlihatkan bahwa ekstrak kasar baru dapat menghambat sel normal
di atas 500 µg mL
-1dengan nilai IC
50922.88 µg mL
-1.. Dari uji kaempferol hasil
fraksinasi dengan KLTP pada sel normal dan sel kanker Raji, terlihat bahwa
persen penghambatan pada sel kanker Raji lebih besar daripada sel Vero bahkan
pada sel Vero dapat dikatakan