PEMBUATAN BIOETANOL DARI ECENG GONDOK DENGAN
PROSES HIDROLISIS, FERMENTASI, DAN EKSTRAKSI
SECARA TERPADU
TESIS
Oleh
OKTA BANI
117022004/TK
FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA
MEDAN
PEMBUATAN BIOETANOL DARI ECENG GONDOK DENGAN
PROSES HIDROLISIS, FERMENTASI, DAN EKSTRAKSI
SECARA TERPADU
TESIS
Untuk Memperoleh Gelar Magister Teknik
Pada Program Studi Teknik Kimia
Fakultas Teknik Universitas Sumatera Utara
OLEH
OKTA BANI
117022004/TK
FAKULTAS TEKNIK
UNIVERSITAS SUMATERA UTARA
MEDAN
PANITIA PENGUJI TESIS
Ketua : Dr. Ir. Taslim, M.Si
Anggota : - Dr. Eng. Ir. Irvan, M.Si
- Prof. Dr. Ir. Rosdanelli Hsb, MT
ABSTRAK
Eceng gondok merupakan gulma air yang dianggap merusak dan susah diberantas. Salah satu cara pengendalian yang cukup menjanjikan adalah memanfaatkannya untuk produksi bioetanol. Penelitian terdahulu telah berhasil menghasilkan etanol dari eceng gondok, tetapi teknologi ini masih belum menguntungkan. Pemilihan tekonologi praperlakuan yang tepat dan produksi enzim secara on-site dianggap penting untuk menurunkan biaya produksi. Selain itu, penerapan proses daur-ulang dan ekstraksi secara simultan juga menjanjikan sebagai pengganti teknologi pemurnian yang banyak digunakan saat ini yaitu distilasi. Oleh karena itu, penelitian ini ditujukan untuk mengevaluasi kompatibilitas proses-proses tersebut dalam produksi bioetanol. Dalam penelitian ini, eceng gondok yang telah dihaluskan dihadapkan pada 4 jenis praperlakuan: dilute acid pretreatment (DAP), liquid hot water (LHW), praperlakuan biologis, and tanpa praperlakuan. Kemudian, eceng gondok dihidrolisis dengan campuran selulase dari Tricoderma reesei dan
Aspergillus niger, dan difermentasi dengan Saccharomyces cerevisiae dan Candida utilis. Kaldu fermentasi didaur-ulang langsung setelah penyaringan, dan biodiesel sawit digunakan sebagai pengekstrak. Magnesium sulfat ditambahkan untuk meningkatkan kualitas proses. Hasil penelitian menunjukkan bahwa penggunaan DAP, penambahan inokulum C. utilis dan magnesium sulfat, serta ekstraksi dengan biodiesel sawit memberikan hasil positif. Daur ulang kaldu meningkatkan kadar etanol yang dicapai, tetapi menurunkan yield etanol yang dihasilkan.
ABSTRACT
Water hyacinth is an aquatic weed that is considered damaging and difficult to eradicate. One promising way to control it is by utilizing it for bioethanol production. Previous researches have successfully yielded ethanol from water hyacinth, but this technology is yet to be profitable. Correct choice of pretreatment and on-site enzyme production are considered important to cut the production cost. In addition, integration of recycling process along with simultaneous extraction seems promising as a substitute for existing purification technology (distillation). Therefore, this study aimed to evaluate compatibility of these processes in the production of bioethanol. In this study, pre-blended water hyacinth was subjected to 4 types of pretreatment: dilute acid pretreatment (DAP), liquid hot water (LHW), biological, and without pretreatment. Afterwards, water hyacinth was hydrolyzed by cellulase mixture from Tricoderma reesei and Aspergillus niger, and subsequently fermented by Saccharomyces cerevisiae and Candida utilis. Fermentation broth was directly recycled after filtration, and palm biodiesel was used as extractor. Magnesium sulfate was added to enhance the process. Result favors the use of DAP as pretreatment, addition of C. utilis inoculums and magnesium sulfate in fermentation broth, as well as extraction by palm biodiesel. Broth recycling increase ethanol level, but lowers ethanol yield.
KATA PENGANTAR
Puji syukur Penulis panjatkan ke hadirat Tuhan Yang Maha Esa atas berkat
dan karunia-Nya Penulis dapat menyelesaikan Tesis yang berjudul:
PEMBUATAN BIOETANOL DARI ECENG GONDOK DENGAN PROSES
HIDROLISIS, FERMENTASI, DAN EKSTRAKSI SECARA TERPADU
Dalam penyusunan tesis ini, Penulis mendapatkan bimbingan serta bantuan
dari berbagai pihak. Pada kesempatan ini juga, Penulis ingin mengucapkan terima
kasih kepada Bapak Dr. Ir. Taslim, M.Si selaku Ketua Komisi Pembimbing dan
Ketua Program Studi Magister Teknik Kimia yang telah memberikan bimbingan,
arahan dan bantuan dalam penyusunan Tesis ini; Bapak Dr. Eng. Ir. Irvan, M.Si
selaku Anggota Komisi Pembimbing yang telah memberikan bimbingan dan arahan
dalam penyusunan Tesis ini; Ibu Dr. Ir. Iriany, M.Si atas kesediaannya sebagai
penguji Tesis ini; Ibu Prof. Dr. Ir. Rosdanelli Hsb, MT atas kesediaannya sebagai
penguji Tesis ini; Ibu Feni Amriani, ST, MT atas bantuannya selama penelitian;
Lembaga Pengelolaan Dana Pendidikan (LPDP) yang telah mendanai penelitian ini;
dan rekan-rekan di Magister Teknik Kimia USU serta seluruh pihak yang telah
membantu dan memberi dukungan dalam penyelesaian Tesis ini.
Terima kasih sebesar-besarnya disampaikan secara khusus kepada kedua
orang tua Penulis yang telah memberikan dukungan moral dan spiritual karena
Dalam penyusunan Tesis ini, Penulis menyadari masih banyak terdapat
kekurangan. Oleh karena itu, Penulis sangat mengharapkan saran dan kritik dari
pembaca yang bersifat konstruktif demi kesempurnaan penulisan ini. Akhir kata,
Penulis mengucapkan terima kasih.
Medan, 24 Februari 2014
Penulis
RIWAYAT HIDUP
Penulis lahir di Medan pada tanggal 1 Nopember 1988, merupakan anak
kedua dari tiga bersaudara dari pasangan Bapak Darmadi dan Ibu Jang King.
Pendidikan TK ditempuh di TK SUTOMO I MEDAN pada tahun 1992 -
1994, kemudian melanjutkan ke pendidikan sekolah dasar di SD SUTOMO I pada
tahun 1994 – 2000, kemudian melanjutkan ke SLTP SUTOMO I pada tahun 2000 –
2003, dan SMA SUTOMO I pada tahun 2003 – 2006.
Pada tahun 2006 Penulis melanjutkan pendidikan di Program Sarjana Teknik
Kimia di Fakultas Teknik Universitas Sumatera Utara dan lulus pada tahun 2011.
Setelah itu Penulis mengambil program Magister Teknik Kimia di Fakultas Teknik
DAFTAR ISI
Judul Halaman
ABSTRAK ... i
ABSTRACT ... ii
KATA PENGANTAR ... iii
RIWAYAT HIDUP ... v
DAFTAR ISI ... vi
DAFTAR GAMBAR ... xii
DAFTAR TABEL ... xv
DAFTAR SINGKATAN ... xvii
BAB I PENDAHULUAN ... 1
1.1. Latar Belakang Penelitian ... 1
1.2. Perumusan Masalah ... 4
1.3. Tujuan Penelitian ... 5
1.4. Manfaat Penelitian ... 5
1.5. Lingkup Penelitian ... 5
BAB II TINJAUAN PUSTAKA ... 8
2.1. Eceng Gondok dalam Produksi Bioetanol ... 8
2.2. Karakteristik dan Pola Perkembangbiakan Eceng Gondok ... 9
2.4. Danau Toba dan Masalah Eceng Gondok ... 13
2.5. Ulasan Teknologi Produksi Bioetanol ... 14
2.5.1. Metode Praperlakuan ... 16
2.5.2. Metode Hidrolisis ... 18
2.5.3. Fermentasi dan Skema Proses Terpadu ... 23
2.5.4. Strategi – Strategi yang Diterapkan untuk Meningkatkan Tiap Proses ... 24
2.6. Produksi Bioetanol dari Eceng Gondok dan Perkembangannya . 25 2.7. Komponen – Komponen dalam Produksi Bioetanol ... 26
2.7.1. Selulosa ... 26
2.7.2. Hemiselulosa ... 35
2.7.3. Lignin ... 36
2.7.4. Struktur Mikrofibril Lignoselulosa ... 37
2.8. Mikroorganisme dalam Produksi Bioetanol ... 38
2.8.1. Trichoderma reesei ... 38
2.8.2. Aspergillus niger ... 39
2.8.3. Saccharomyces cerevisiae ... 39
2.8.4. Candida utilis ... 39
2.8.5. Jamur Akar Putih... 40
2.9. Modifikasi Proses dalam Produksi Bioetanol ... 40
2.9.2. Co-Fermentasi Hemiselulosa ... 43
2.9.3. Sistem Fermentasi Non-Steril ... 43
2.9.4. Daur Ulang dalam Produksi Bioetanol ... 44
BAB III METODOLOGI PENELITIAN ... 45
3.1. Lokasi Penelitian ... 45
3.2. Bahan dan Peralatan ... 45
3.3. Prosedur... 47
3.3.1. Prosedur Pembenihan Isolat... 48
3.3.2. Prosedur Persiapan Inokulum ... 49
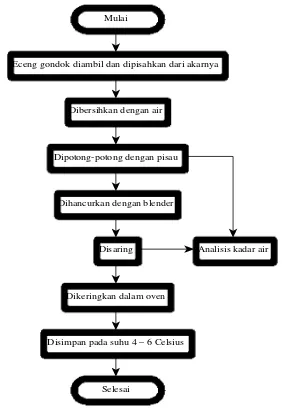
3.3.3. Prosedur Persiapan Eceng Gondok ... 49
3.3.4. Prosedur Pembuatan Enzim ... 50
3.3.5. Prosedur Praperlakuan Eceng Gondok ... 50
3.3.6. Prosedur Fermentasi Eceng Gondok ... 52
3.3.7. Prosedur Daur Ulang Hidrolisat ... 52
3.3.8. Prosedur Analisis Densitas ... 53
3.3.9. Prosedur Analisis Viskositas ... 53
3.3.10. Prosedur Analisis pH ... 54
3.3.11. Prosedur Analisis Kadar Hemiselulosa, Selulosa dan Lignin ... 54
3.3.12. Prosedur Analisis Kadar Air ... 55
3.3.14. Prosedur Assay Enzim ... 56
3.3.15. Prosedur Analisis Kadar Etanol ... 57
3.4. Flowchart ... 59
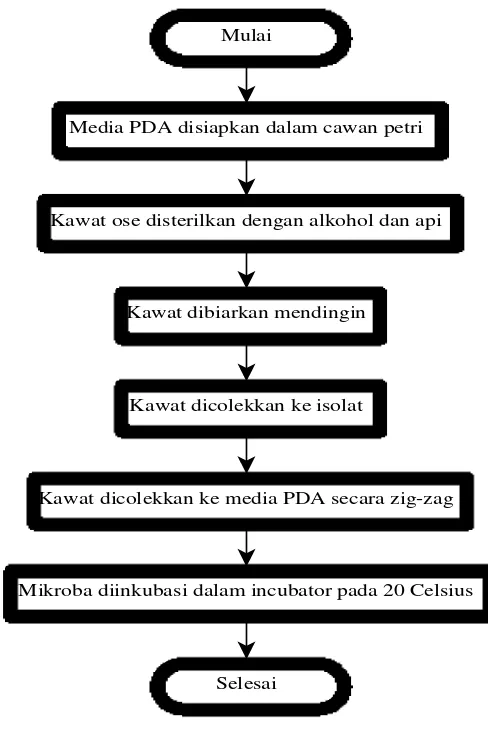
3.4.1. Flowchart Pembenihan Isolat ... 59
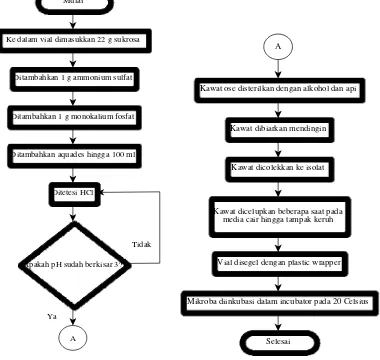
3.4.2. Flowchart Persiapan Inokulum ... 60
3.4.3. Flowchart Persiapan Eceng Gondok ... 61
3.4.4. Flowchart Pembuatan Enzim ... 62
3.4.5. Flowchart Praperlakuan Eceng Gondok ... 63
3.4.6. Flowchart Fermentasi Eceng Gondok ... 64
3.4.7. Flowchart Daur Ulang Hidrolisat ... 66
3.4.8. Flowchart Analisis Densitas ... 68
3.4.9. Flowchart Analisis Viskositas... 69
3.4.10. Flowchart Analisis pH ... 70
3.4.11. Flowchart Analisis Kadar Hemiselulosa, Selulosa dan Lignin ... 71
3.4.12. Flowchart Analisis Kadar Air ... 74
3.4.13. Flowchart Analisis Kadar Gula ... 75
3.4.14. Flowchart Assay Enzim ... 76
3.4.15. Flowchart Analisis Kadar Etanol ... 77
BAB IV HASIL DAN PEMBAHASAN ... 78
4.2. Pengaruh Metode Praperlakuan pada Fermentasi ... 79
4.3. Pengaruh Kadar Magnesium Sulfat pada Fermentasi ... 81
4.4. Pengaruh Durasi Fermentasi pada Fermentasi ... 82
4.5. Pengaruh Pemilihan Mikroorganisme pada Fermentasi ... 83
4.6. Pengaruh Perbandingan Pelarut pada Fermentasi ... 85
4.7. Pengaruh Daur Ulang pada Fermentasi ... 87
4.8. Data Densitas dan Viskositas Kaldu Fermentasi dan Pelarut ... 89
BAB V KESIMPULAN DAN SARAN ... 92
5.1. Kesimpulan ... 92
5.2. Saran ... 93
DAFTAR PUSTAKA ... 95
LAMPIRAN A DATA PENELITIAN ... 105
A.1. Hasil Analisis Kadar Air Eceng Gondok ... 105
A.2. Hasil Analisis Kandungan Hemiselulosa-Selulosa-Lignin Eceng Gondok ... 105
A.3. Data dan Kurva Kalibrasi Larutan Etanol Standar ... 106
A.4. Data dan Kurva Kalibrasi Etanol-Biodiesel Sawit ... 106
A.5. Data Analisis GC Sampel ... 107
A.6. Data dan Kurva Kalibrasi Larutan Gula Standar ... 108
A.7. Data Analisis Spektrofotometer UV-Vis (λ = 540 nm) ... 109
A.9. Data Densitas Pelarut ... 111
A.10. Data Viskositas Kaldu Fermentasi ... 112
A.11. Data Viskositas Pelarut ... 113
LAMPIRAN B IDENTITAS DATA ... 114
B.1. Identitas Data ... 114
LAMPIRAN C CONTOH PERHITUNGAN ... 115
C.1. Contoh Perhitungan Kadar Air ... 115
C.2. Contoh Perhitungan Aktivitas Enzim ... 115
C.3. Contoh Perhitungan Densitas Run 5 ... 115
C.4. Contoh Perhitungan Viskositas Sampel Run 5 ... 116
C.5. Contoh Perhitungan Total Etanol per 50 ml Run 22 (dalam g/L) ... 116
C.6. Contoh Perhitungan Yield Etanol Run 22 (tanpa daur ulang)... 117
C.7. Contoh Perhitungan Yield Etanol Run 23 (dengan daur ulang) .. 117
LAMPIRAN D DOKUMENTASI ... 118
D.1. Eceng Gondok ... 118
D.2. Isolat Mikroorganisme ... 118
DAFTAR GAMBAR
Nomor Judul Halaman
2.1. Spesies Eceng Gondok Umum ... 9
2.2. Tahapan dalam Produksi Bioetanol Secara Umum ... 15
2.3. Perubahan Struktur Mikro Akibat Praperlakuan ... 18
2.4. Aktivitas Enzim dalam Hidrolisis Selulosa ... 21
2.5. Berbagai Senyawa Turunan Hidrolisis Asam ... 22
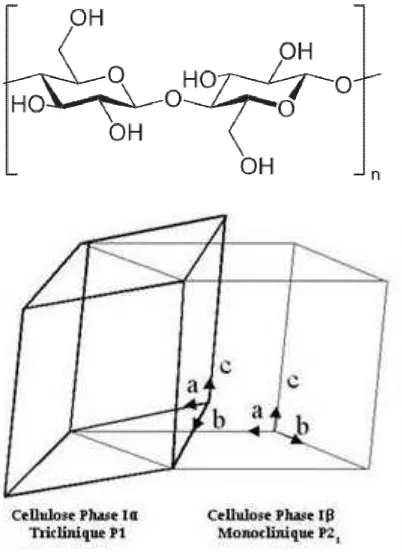
2.6. Kiri: Unit Penyusun Selulosa, Selobiosa; Kanan: Fasa Selulosa Monoklinik Iα dan Triklinik Iβ ... 34
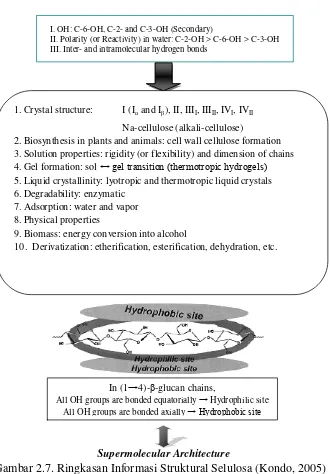
2.7. Ringkasan Informasi Struktural Selulosa ... 35
2.8. Representasi Struktur Hemiselulosa ... 36
2.9. Representasi Struktur Lignin dan Lignols ... 37
2.10. Matriks Selulosa – Hemiselulosa – Lignin ... 38
2.11. Ekstraksi Etanol dengan Minyak dan Turunannya ... 41
3.1. Flowchart Pembenihan Isolat ... 59
3.2. Flowchart Persiapan Inokulum ... 60
3.3. Flowchart Persiapan Eceng Gondok ... 61
3.4. Flowchart Pembuatan Enzim ... 62
3.5. Flowchart Praperlakuan Eceng Gondok ... 63
3.7. Flowchart Daur Ulang Hidrolisat ... 66
3.8. Flowchart Analisis Densitas ... 68
3.9. Flowchart Analisis Viskositas... 69
3.10. Flowchart Analisis pH ... 70
3.11. Flowchart Analisis Kadar Hemiselulosa, Selulosa dan Lignin ... 71
3.12. Flowchart Analisis Kadar Air ... 74
3.13. Flowchart Analisis Kadar Gula ... 75
3.14. Flowchart Assay Enzim ... 76
3.15. Flowchart Analisis Kadar Etanol ... 77
4.1. Perbandingan berbagai metode praperlakuan dalam fermentasi selama 24 jam dalam inkubator pada 20 oC ... 79
4.2. Pengaruh kadar magnesium pada fermentasi... 81
4.3. Endapan pada sampel sewaktu dianalisa dengan metode DNS ... 82
4.4. Pengaruh durasi fermentasi pada fermentasi ... 83
4.5. Pengaruh pemilihan mikroorganisme pada fermentasi ... 84
4.6. Pengaruh rasio pelarut pada fermentasi ... 86
4.7. Pengumpulan substrat di atas lapisan kaldu, baik disertai pelarut maupun tanpa pelarut ... 87
4.8. Pengaruh daur ulang pada fermentasi ... 88
4.10. Data viskositas kaldu fermentasi (kiri) dan pelarut (kanan) ... 91
A.1. Kurva Kalibrasi Larutan Etanol Standar ... 106
A.2. Kurva Kalibrasi Etanol-Biodiesel Sawit ... 107
A.3. Kurva Kalibrasi Larutan Gula Standar ... 109
D.1. Eceng Gondok ... 118
D.2. Isolat Aspergillus niger ... 118
D.3. Isolat Trichoderma reesei ... 119
D.4. Isolat Candida utilis ... 119
D.5. Isolat Ganoderma boninense ... 119
DAFTAR TABEL
Nomor Judul Halaman
1.1. Ringkasan Penelitian Terdahulu ... 2
2.1. Kandungan Hemiselulosa, Selulosa dan Lignin Eceng Gondok (basis kering) ... 12
2.2. Berbagai Metode Praperlakuan ... 19
2.3. Skema Proses Terpadu dalam Produksi Bioetanol... 24
2.4. Berbagai Penelitian mengenai Bioetanol dari Eceng Gondok ... 27
4.1. Rangkuman Hasil Analisis Kondisi Awal ... 78
A.1. Hasil Analisis Kadar Air Batang Eceng Gondok ... 105
A.2. Hasil Analisis Kadar Air Daun Eceng Gondok ... 105
A.3. Hasil Analisis Kadar Air Bubur Eceng Gondok ... 105
A.4. Hasil Analisis Kandungan Hemiselulosa-Selulosa-Lignin Eceng Gondok ... 105
A.5. Data Kurva Kalibrasi Larutan Etanol Standar ... 106
A.6. Data Kurva Kalibrasi Etanol-Biodiesel Sawit ... 106
A.7. Data Analisis GC Sampel ... 107
A.8. Data Kurva Kalibrasi Larutan Gula Standar (λ = 540 nm) ... 108
A.9. Data Analisis Spektrofotometer Enzim ... 109
A.11. Data Densitas Kaldu Fermentasi ... 110
A.12. Data Densitas Pelarut ... 111
A.13. Data Viskositas Kaldu Fermentasi ... 112
A.14. Data Viskositas Pelarut ... 113
DAFTAR SINGKATAN
DAP : Dilute Acid Pretreatment
LHW : Liquid Hot Water
HMF : Hidroksimetil Furfural
SHF : Separated Hydrolysis and Fermentation
SSF : Simultaneous Saccharification and Fermentation
HHF : Hybird Hydrolysis and Fermentation
SSCF : Simultaneous Saccharification and Cofermentation
CBP : Consolidated Bioprocessing
DMC : Direct Microbial Conversion
PEG : Polietilen glikol
BSA : Bovine serum albumin
CG : Crude glycerol
IL : Ionic Liquid
IU : International Unit
FPU : Filter Paper Unit
FDA : Food and Drug Administration
CMC : Karboksimetil selulosa
DNS : Dinitro salisilat
ABSTRAK
Eceng gondok merupakan gulma air yang dianggap merusak dan susah diberantas. Salah satu cara pengendalian yang cukup menjanjikan adalah memanfaatkannya untuk produksi bioetanol. Penelitian terdahulu telah berhasil menghasilkan etanol dari eceng gondok, tetapi teknologi ini masih belum menguntungkan. Pemilihan tekonologi praperlakuan yang tepat dan produksi enzim secara on-site dianggap penting untuk menurunkan biaya produksi. Selain itu, penerapan proses daur-ulang dan ekstraksi secara simultan juga menjanjikan sebagai pengganti teknologi pemurnian yang banyak digunakan saat ini yaitu distilasi. Oleh karena itu, penelitian ini ditujukan untuk mengevaluasi kompatibilitas proses-proses tersebut dalam produksi bioetanol. Dalam penelitian ini, eceng gondok yang telah dihaluskan dihadapkan pada 4 jenis praperlakuan: dilute acid pretreatment (DAP), liquid hot water (LHW), praperlakuan biologis, and tanpa praperlakuan. Kemudian, eceng gondok dihidrolisis dengan campuran selulase dari Tricoderma reesei dan
Aspergillus niger, dan difermentasi dengan Saccharomyces cerevisiae dan Candida utilis. Kaldu fermentasi didaur-ulang langsung setelah penyaringan, dan biodiesel sawit digunakan sebagai pengekstrak. Magnesium sulfat ditambahkan untuk meningkatkan kualitas proses. Hasil penelitian menunjukkan bahwa penggunaan DAP, penambahan inokulum C. utilis dan magnesium sulfat, serta ekstraksi dengan biodiesel sawit memberikan hasil positif. Daur ulang kaldu meningkatkan kadar etanol yang dicapai, tetapi menurunkan yield etanol yang dihasilkan.
ABSTRACT
Water hyacinth is an aquatic weed that is considered damaging and difficult to eradicate. One promising way to control it is by utilizing it for bioethanol production. Previous researches have successfully yielded ethanol from water hyacinth, but this technology is yet to be profitable. Correct choice of pretreatment and on-site enzyme production are considered important to cut the production cost. In addition, integration of recycling process along with simultaneous extraction seems promising as a substitute for existing purification technology (distillation). Therefore, this study aimed to evaluate compatibility of these processes in the production of bioethanol. In this study, pre-blended water hyacinth was subjected to 4 types of pretreatment: dilute acid pretreatment (DAP), liquid hot water (LHW), biological, and without pretreatment. Afterwards, water hyacinth was hydrolyzed by cellulase mixture from Tricoderma reesei and Aspergillus niger, and subsequently fermented by Saccharomyces cerevisiae and Candida utilis. Fermentation broth was directly recycled after filtration, and palm biodiesel was used as extractor. Magnesium sulfate was added to enhance the process. Result favors the use of DAP as pretreatment, addition of C. utilis inoculums and magnesium sulfate in fermentation broth, as well as extraction by palm biodiesel. Broth recycling increase ethanol level, but lowers ethanol yield.
BAB I
PENDAHULUAN
1.1. Latar Belakang Penelitian
Tumbuhnya eceng gondok dalam suatu ekosistem dapat menyebabkan
penurunan kualitas lingkungan ekosistem tersebut. Di beberapa danau di dunia,
seperti Danau Victoria, Danau Toba dan danau lain, eceng gondok tumbuh
melampaui spesies alami, sehingga mengurangi biodiversitas ekosistem tersebut
(Moedjojo et al. 2006; Rutashobya, 1996 dalam Katima, 2001). Eceng gondok
mampu memurnikan suatu badan air tetapi ketika tumbuh di luar kendali, tumbuhan
ini menyebabkan banyak masalah (Flacker, 2004; Jafari, 2010; Mahamadi, 2011).
Karena usaha mengontrol populasi eceng gondok telah mengalami banyak
kegagalan, studi baru-baru ini lebih ditekankan pada pemanfaatannya (Abdel-sabour,
2010; Malik, 2007). Salah satu pemanfaatan yang ramah lingkungan adalah dengan
mengubah eceng gondok ke etanol (Mukhopadhyay dan Chatterjee, 2010).
Penelitian-penelitian terdahulu mengenai produksi bioetanol dari eceng gondok
beserta penelitian lain yang dijadikan sebagai acuan dalam modifikasi proses,
diringkas dalam Tabel 1.1.
Dari penelitian-penelitian yang telah dilakukan, alur proses secara umum
meliputi praperlakuan (pretreatment) dengan/tanpa detoksifikasi, diikuti hidrolisis
Fermentation) ataupun bersamaan seperti Simultaneous Saccharification and
Fermentation / Simultaneous Saccharification, Co-Fermentation and Fermentation /
Consolidated BioProcessing).
Tabel 1.1. Ringkasan Penelitian Terdahulu Lingkup studi Peneliti Hasil
Metode dan
Tiap metode praperlakuan memiliki kelemahan dan kekurangan masing-masing. Praperlakuan yang lebih intensif biasanya memungkinkan konversi selulosa yang lebih tinggi dan lebih cepat, namun menyebabkan terbentuknya inhibitor.
Praperlakuan yang terlalu lama dianggap tidak efektif dan menyebabkan degradasi gula.
Terdapat literatur yang menyebutkan bahwa penggilingan saja merupakan praperlakuan yang memadai.
Dari berbagai metode yang pernah dicoba, hanya praperlakuan biologis dengan jamur akar putih yang tidak menghasilkan inhibitor.
Penggunaan campuran enzim selulase memberikan efek sinergis. Semakin tinggi konsentrasi enzim, konversi yang lebih tinggi dan lebih cepat diperoleh.
Akan tetapi, dalam banyak studi disampaikan bahwa peningkatan hasil tidak sebanding dengan biaya tambahannya.
Selain selulase, penggunaan jenis enzim lain seperti pektinase, hemiselulase, arabinose, ligninase, dan xilanase juga memberikan kontribusi positif dalam produksi bioetanol.
Loading
Studi-studi yang ada menunjukkan bahwa ketika
loading biomassa ditingkatkan, konsentrasi
Tabel 1.1. Ringkasan Penelitian Terdahulu Lingkup studi Peneliti Hasil
Mikroba
Beragam strain dan spesies ragi dan bakteri telah dicoba. Parameter utama perbandingan biasanya adalah yield etanol yang dicapai masing-masing organisme. Strain baru dan rekombinan masih terus diisolasi dan dikembangkan.
Penggunaan surfaktan mengurangi ikatan non efektif selulase pada lignin sehingga mengurangi konsumsi enzim.
Mode proses yang menggabungkan fermentasi dan hidrolisis memberikan hasil yang lebih baik.
Ekstraksi etanol Offeman et al. 2010; 2008; 2006
Stang et al. 2001 Kim et al. 1999 Munson dan King, 1984
Berbagai jenis pelarut diuji. Tiap pelarut memberikan harga koefisien distribusi dan faktor separasi yang sangat beragam. Beberapa karakteristik pelarut menentukan toksisitas pelarut. Penerapan ekstraksi simultan meningkatkan produksi bioetanol.
Peningkatan toleransi ragi
Hu et al. 2003 Ion Mg2+ mengurangi permeabilitas membran
plasma dan meningkatkan toleransi etanol ragi.
Fermentasi non-steril (bioetanol / non-eceng gondok)
Larsen, 2012 Pada konsentrasi yang tidak terlalu tinggi, efek inhibisi dari inhibitor dalam larutan fermentasi tidak terlalu mengganggu ragi, tetapi sangat menghambat pertumbuhan bakteri asam laktat
Pergeseran hidrofobik. Heterogenitas dan zona separasi juga meningkat.
Kebanyakan penelitian-penelitian tersebut berfokus pada evaluasi metode
proses, pengembangan mikroba fermentasi, ataupun optimisasi kondisi operasi.
Perkembangan aspek-aspek tersebut sangat dipengaruhi rekayasa genetika dimana
mikroorganisme rekombinan dan enzim-enzim chimera telah dikembangkan.
Sementara aspek-aspek tersebut terus berkembang pesat, aspek-aspek lain seperti
pemurnian etanol, peluang daur ulang total proses, dan peluang fermentasi non-steril
yang dapat mempengaruhi biaya operasi tampaknya masih kurang diteliti. Oleh
karena itulah, penelitian ini lebih diarahkan pada aspek-aspek tersebut dengan
mengadaptasikan beberapa modifikasi dalam produksi bioetanol dari eceng gondok.
Adapun modifikasi yang dimaksud meliputi:
1. Penggunaan produksi enzim on-site,
2. Perlakuan hidrolisis, fermentasi, dan ekstraksi secara simultan,
3. Penambahan magnesium sulfat (mempengaruhi fermentasi dan ekstraksi),
4. Penerapan daur ulang hidrolisat fermentasi, dan
5. Dilangsungkannya daur ulang fermentasi secara non-steril.
1.2. Perumusan Masalah
Permasalahan utama dalam penelitian ini adalah merumuskan suatu konsep
produksi bioetanol dari eceng gondok yang aman, ekonomis, sederhana, dan ramah
lingkungan sehingga dapat diaplikasikan ke masyarakat yang berdomisili di daerah
1.3. Tujuan Penelitian
Tujuan penelitian ini adalah:
1. Mendesainkan suatu alur proses produksi etanol yang aman, ekonomis,
sederhana dan ramah lingkungan dari eceng gondok,
2. Mengevaluasi keberhasilan penerapan metode fermentasi non-steril, ekstraksi
in-situ dan sistem daur ulang dalam proses fermentasi,
3. Mengidentifikasi kendala dan faktor yang mempengaruhi proses produksi
bioetanol akibat modifikasi tersebut, dan
4. Mencoba memecahkan masalah-masalah terkait kendala-kendala tersebut.
1.4. Manfaat Penelitian
Secara umum, penelitian ini akan memberikan informasi mengenai produksi
bioetanol dari eceng gondok, terutama dari sisi modifikasi prosesnya. Jika penelitian
berhasil, maka hasilnya akan membantu mengatasi salah satu masalah utama
lingkungan di Danau Toba, dan meningkatkan perekonomian daerah tersebut.
1.5. Lingkup Penelitian
Penelitian ini difokuskan pada trial integrasi metode ekstraksi in-situ secara
simultan ke fermentasi hidrolisat eceng gondok non-steril dan analisis variable
terkait seperti perbandingan pelarut dan kaldu, pengujian teknik-teknik daur ulang
dalam sistem daur ulang, pengumpulan data-data reologi proses dan peninjauan
Penelitian ini dilaksanakan di Laboratorium Mikrobiologi Farmasi, Fakultas
Farmasi, Universitas Sumatera Utara, Medan. Bahan-bahan utama yang digunakan
antara lain eceng gondok, ekstrak enzim selulase kasar, magnesium sulfat hepta
hidrat, asam sulfat, natrium hidroksida dan biodiesel sawit. Organisme yang
digunakan dalam penelitian ini adalah ragi Saccharomyces cerevisiae, ragi Candida
utilis, jamur Trichoderma reesei, jamur Aspergillus niger, dan jamur akar putih /
Ganoderma boninense. Peralatan utama dalam penelitian ini adalah autoklaf,
inkubator, sentrifugator, lemari aseptik, oven, freezer, spektrofotometer, GC,
pHmeter, viskometer Oswald, piknometer, refluks kondensor, vial, dan cuvet.
Variabel yang diuji dalam penelitian ini meliputi:
1. Metode praperlakuan (pretreatment):
a. Tanpa praperlakuan (sterilisasi),
b. Dilute Acid Pretreatment (DAP),
c. Liquid Hot Water (LHW), dan
d. Praperlakuan biologis dengan jamur akar putih.
2. Konsentrasi magnesium sulfat(mM) : 0, 25, 50, 75, dan 100
3. Lama fermentasi : 1, 2, dan 4 hari
4. Mikroorganisme fermentasi: Saccharomyces cerevisiae, dan Candida utilis
5. Perbandingan pelarut terhadap kaldu: 0; 0,4; 0,5; 0,66; 1
Variabel diuji dengan memvariasikan hanya 1 jenis variabel pada satu kondisi
tetap. Kondisi tetap yang digunakan adalah kondisi dengan variabel yang ditetapkan
di awal apabila kondisi terbaik belum diketahui atau kondisi terbaik bila sudah
diketahui, yaitu konsentrasi magnesium sulfat 0 mM, fermentasi 1 hari, monokultur
Saccharomyces cerevisiae, volum pelarut 0 ml, dan persentase daur ulang 0%.
Parameter yang diukur adalah kadar hemiselulosa, kadar selulosa, kadar lignin,
aktivitas enzim, kadar gula tereduksi, kadar etanol, kadar air, pH, densitas, dan
viskositas. Kadar hemiselulosa, selulosa, dan lignin dianalisis dengan metode
Chesson, aktivitas enzim dianalisis dengan assay CMC, kadar gula tereduksi
dianalisis dengan metode DNS, kadar etanol diukur menggunakan GC dengan
metode static head space, kadar air diukur secara gravimetri, pH diukur
menggunakan pHmeter, densitas diukur menggunakan piknometer, dan viskositas
diukur menggunakan viskometer. Sampel yang tidak dianalisis langsung disimpan
BAB II
TINJAUAN PUSTAKA
2.1. Eceng Gondok dalam Produksi Bioetanol
Konversi biomassa lignoselulosa ke bahan bakar bio berpotensi
mengamankan sekuritas energi dan mengurangi emisi gas rumah kaca demi
keberlangsungan lingkungan (Wyman, 1999 dalam Kumar et al. 2009; Joshi et al.
2011). Eceng gondok, tersedia dalam jumlah banyak dan tidak diinginkan, cocok
digunakan sebagai tanaman penghasil bioenergi karena bereproduksi dengan cepat,
memiliki kandungan lignin rendah, resistan terhadap zat kimia, tidak kompetitif
dengan tanaman pangan, dan memiliki kecenderungan polusi genetik yang rendah
melalui penyerbukan silang antar tanaman pangan terkultivasi (Patel, 2012;
Bhattacharya dan Kumar, 2010; Mukhopadhyay dan Chatterjee, 2010).
Kapabilitasnya menghasilkan etanol menyamai limbah pertanian, sesuai untuk
produksi bahan bakar bio dan juga sebagai kandidat bahan baku industri penghasil
lapangan kerja (Mashima et al. 2008). Hronich et al. (2008) menyatakan bahwa
penggunaan eceng gondok menjadi ekonomis pada biaya produksi sekitar $40 per
ton massa kering.
Produksi etanol sendiri diperkirakan meningkat tajam di masa depan, karena
kemungkinan naiknya harga minyak, meningkatnya permintaan bahan bakar cair,
E-10), dan produksi bahan bioplastik dari etanol (Nag, 2008; Neves et al. 2007). Di
samping alasan-alasan di atas, mencampurkan etanol ke dalam bensin juga
meningkatkan bilangan oktan bensin, dan memungkinkan pembakaran yang lebih
sempurna (Wyman 1994).
2.2. Karakteristik dan Pola Perkembangbiakan Eceng Gondok
Eceng gondok adalah tanaman akuatis terapung perenial yang berasal dari
Brazil, basin Amazon, daerah ekuator, daerah tropis dan sub-tropis Amerika Selatan.
Dengan daun yang lebar dan mengkilap, eceng gondok dapat mencapai tinggi 1
meter di atas permukaan air. Batangnya panjang, menggelembung dan berongga.
Akarnya yang berbulu dan bebas bergantung berwarna ungu kehitaman. Satu tangkai
tegak menyokong segerombol 8 – 15 bunga yang atraktif, kebanyakan berwarna
lavender sampai merah jambu dengan enam kelopak seperti dalam Gambar 2.1
(Patel, 2012; Flacker, 2004).
Sebagai salah satu tanaman dengan laju pertumbuhan tercepat, eceng gondok
berproduksi terutama melalui stolon yang membentuk anak tanaman. Eceng gondok
juga dapat menghasilkan tanaman baru melalui fragmentasi (pecah menjadi bagian
kecil), membentuk tunas daun di pucuk dasar batang, dan memproduksi sejumlah
besar bibit yang tahan hingga tiga puluh tahun. Eceng gondok umum (Eichhornia
crassipes) tumbuh secara agresif, dan diketahui dapat melipat-gandakan populasinya
dalam dua minggu (Flacker, 2004). Dalam suatu studi, dua tanaman menghasilkan
1.200 anak tanaman dalam empat bulan. Satu tanaman dapat memproduksi 5.000
bibit dan unggas air memakan dan memindahkan bibit ke lokasi baru (Anonim,
2012). Tanaman tropis ini menyebar ke berbagai bagian bumi di akhir abad ke-19
dan awal abad-20 (Wilson et al. 2005). Semua usaha ilmuwan dan teknokrat di
seluruh dunia untuk memberantas tanaman ini secara kimiawi dan biologis hanya
membuahkan sedikit hasil (Jafari, 2010).
Adapun mudahnya adaptasi eceng gondok di habitat barunya dapat dilacak ke
beberapa sifat (Flacker, 2004; Soltan dan Rashed, 2003):
1. Eceng gondok berkembang-biak secara efektif melalui dua metode vegetatif.
2. Batangnya yang berongga dan terisi udara memudahkannya tetap terapung.
3. Daunnya yang menyerupai kipas mempermudah penyebarannya ke badan air
ketika angin bertiup.
5. Eceng gondok dapat bertahan hidup di campuran logam berat dengan
konsentrasi sampai 3 mg/l.
2.3. Dampak Ekologi, Kimia – Fisik dan Utilisasi Eceng Gondok
Keberadaan eceng gondok pada ekosistem yang dimasukinya bersifat
merusak. Eceng gondok dapat merubah struktur dan fungsi ekosistem dengan
mengganggu rantai makanan dan siklus nutrisi. Eceng gondok juga menutupi
permukaan air dan menghalangi cahaya matahari. Ketika eceng gondok ataupun
tumbuhan yang diganggunya membusuk, pembusukannya menghabiskan oksigen
terlarut dalam air (Patel, 2012; Flacker, 2004).
Pertumbuhan eceng gondok yang masif dan invasif juga berpengaruh pada
kehidupan manusia. Terganggunya aktivitas pelayaran dan nelayan, sistem drainasi
yang tersumbat, serta menurunnya estetika dan nilai rekreasional lingkungan
merupakan contoh gangguan yang disebabkan gulma ini (Patel, 2012; Flacker, 2004).
Ketika tumbuh di luar kendali, eceng gondok merupakan gangguan, tetapi
beberapa peneliti menyarankan penggunaan tanaman eksotis ini sebagai sumber daya
dapat dipanen, misalnya sebagai makanan hewan, sumber antioksidan, sumber
antibiotik, biosorben, agen fitoremediasi, bahan pulp, pupuk organik, bahan
kerajinan tangan dan perabotan, bahan biofuel, dan untuk memproduksi enzim
selulase (Bhattacharya dan Kumar, 2010; Calvert, 2001; Patel, 2012; Chen et al.
dan Saikia, 1994; Hasan et al. 2007; Ibrahim et al. 2012; Jianbao et al. 2008; Ma et
al. 2010; Mahamadi, 2011; Mishima et al. 2008; Orth dan Sapkota, 1988; Yerima et
al. 2009; Yi et al. 2009). Akan tetapi, bahkan dengan banyaknya pemanfaatannya,
sejauh ini dampak negatif tanaman ini ke habitat adopsinya masih jauh melampaui
kontribusinya ke lingkungan barunya (Flacker, 2004).
Dari segi komposisi kimianya, tanaman ini memiliki flavanoid, asam amino,
protein kasar, sianida, fosfat, zat organik dan karbon organik tinggi (Nyananyo et al.
2007). Tanaman segar mengandung 95,5% kelembapan, 0,04% N, 1,0% abu, 0,06%
P2O5, 0,20% K2O, 3,5% bahan organik. Pada basis kelembapan nol, terdapat 75,8%
bahan organik, 1,5% N, dan 24,2% abu. Abu mengandung 28,7% K2O, 1,8% Na2O,
12,8% CaO, 21,0% Cl, dan 7,0% P2O5. Protein mentah mengandung, per 100 g, 0,72
g metionin, 4,72 g fenilalanin, 4,32 g treonin, 5,34 g lisin, 4,32 g isoleusin, 0,27 g
valin, dan 7,2 g leusin (Matai dan Bagchi, 1980 dalam Jafari, 2010). Kuantitas
hemiselulosa, selulosa dan lignin dari berbagai sumber ditunjukkan dalam Tabel 2.1.
Tabel 2.1. Kandungan Hemiselulosa, Selulosa dan Lignin Eceng Gondok (Basis Kering)
(Sornvoraweat dan Kongkiattikajorn, 2010; Hasan dan Chakrabati, 2009)
Hasan dan Chakrabarti (2009) juga menyampaikan bahwa hanya ada sedikit
Akan tetapi, eceng gondok yang hidup di kondisi yang berbeda mungkin memiliki
variasi komposisi karena akar mereka menyerap polutan secara alami (Jafari, 2010).
Lebih jauh lagi, sebuah studi oleh Mahmood et al. (2005) menunjukkan bahwa di
bawah pengaruh limbah tekstil, eceng gondok mengalami penurunan ukuran secara
anatomis. Kondisi yang sama kemungkinan besar juga dialami eceng gondok di
perairan Danau Toba yang tercemar. Namun, besar pengaruh hal tersebut dalam
produksi bioetanol masih belum dapat dipastikan.
2.4. Danau Toba dan Masalah Eceng Gondok
Danau Toba merupakan danau terbesar Indonesia dan terletak di provinsi
Sumatera Utara, 176 km ke barat ibukota provinsi, Medan. Danau Toba memiliki
panjang 87 km dari barat laut ke Tenggara dan lebar 27 km, dan berada 904 meter di
atas permukaan laut dengan kedalaman 505 meter. Danau tersebut merupakan salah
satu tujuan wisata penting. Daerah resapannya seluas 3.704 km2, meliputi sebagian
area dari lima kabupaten. Kualitas air di danau ini telah terpengaruh secara negatif
oleh buangan air domestik, peternakan ikan, polusi minyak dan polusi biologis
(Moedjodo et al. 2006; Worldlake, 2012).
Sejak 1990, eceng gondok telah tampak mengambang di daerah Parapat,
menandakan dimulainya eutrofikasi danau tersebut (Moedjodo et al. 2006). Setelah
itu, berbagai masalah mulai bermunculan, mulai dari terganggunya penangkapan
2004). Walaupun sejumlah konsep sudah diberikan untuk mengatasi masalah
lingkungan tersebut, merealisasikan konsep ini terbukti susah karena perbedaan
persepsi dan konflik kepentingan antara pemegang saham (Moedjodo et al. 2006).
Ledakan pertumbuhan eceng gondok dalam danau ini telah dihubungkan
dengan polusi fosfor dan nitrogen. Idealnya, jalan terbaiknya adalah menekan
masukan limbah. Akan tetapi, terbatasnya limbah yang bisa dikurangi dan lamanya
waktu operasi telah menyebabkan cara ini tidak efektif. Jelas kiranya bahwa populasi
eceng gondok harus dikendalikan. Mukhopadhyay dan Chatterjee (2010)
mengusulkan cara pengendalian yang ramah lingkungan dengan menggunakannya
sebagai bahan baku murah dalam proses inovatif biokonversi ke etanol.
2.5. Ulasan Teknologi Produksi Bioetanol
Teknologi produksi bioetanol saat ini (proses generasi pertama)
menggunakan gula tebu dan/atau biji-bijian dan umbi – umbian berbasis tepung
(terutama jagung dan kentang) sebagai substrat utama. Akan tetapi oleh karena
dampak negatifnya pada harga makanan dan sekuritas makanan, trend saat ini sedang
bergeser ke biomassa lignoselulosa. Ada dua proses lignoselulosa yang tersedia,
proses enzimatis dan proses termokimia. Proses enzimatis umumnya melibatkan
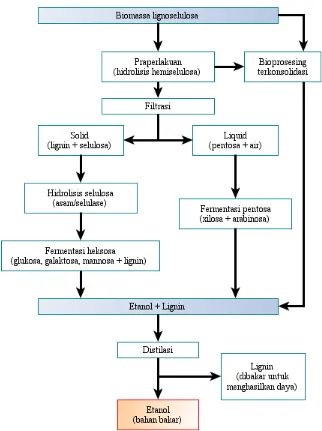
hidrolisis biomassa lignoselulosa ke gula diikuti fermentasi gula ke etanol (lihat
Gambar 2.2). Proses termokimia menggunakan jalur gasifikasi dan jalur pirolisis
Gambar 2.2. Tahapan dalam Produksi Bioetanol Secara Umum (Joshi et al. 2011)
Untuk biomassa lignoselulosa herbal, proses enzimatis lebih cocok (Foust et
al. 2009). Penjelasan lengkap tentang praperlakuan, hidrolisis/sakarifikasi,
Untuk saat ini, etanol selulosa masih kurang diminati karena keuntungannya yang
marginal. Beberapa alasan yang menyebabkannya antara lain:
a. Teknologi praperlakuan yang ada kurang efisien atau terlalu mahal dan
banyak kelemahan yang menyertainya.
b. Harga enzim terlalu tinggi.
c. Konversi oleh mikroba masih terbatas. Sebagai contoh, Zymmomonas
mobilus yang lebih toleran dari ragi hanya mampu mentolerir konsentrasi
etanol sampai 16% saja.
Teknologi ini diperumit lagi oleh masalah-masalah umum bioreaktor seperti
kontaminasi mikroba, tidak stabilnya proses, problematika daur ulang dan washout
mikroba, serta pemrosesan akhir yang sukar. Khusus untuk proses fermentasi
lignoselulosa, tingginya kekentalan pada loading padatan tinggi menyebabkan
masalah pengadukan (Huang et al. 2011). Walau begitu, teknik-teknik untuk
mengatasi masalah – masalah ini telah banyak dikembangkan.
2.5.1. Metode Praperlakuan
Salah satu rintangan utama dalam hidrolisis selulosa adalah karakteristik
substrat yang tidak mendukung hidrolisis selulosa. Karakteristik ini kemudian
dimodifikasi agar hidrolisis berlangsung lebih efisien (Huang et al. 2011). Sebab
itulah, praperlakuan memiliki dampak besar pada seluruh operasi dan biasanya
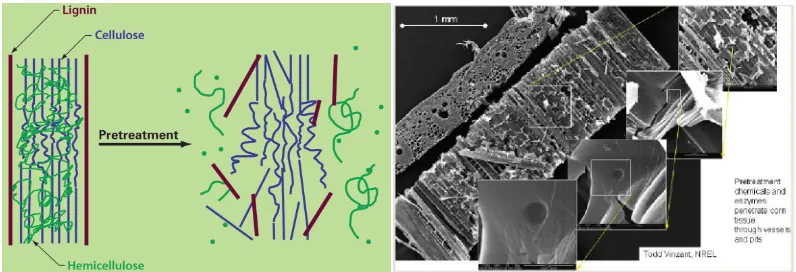
untuk membuka struktur lignoselulosa agar dapat diakses enzim seperti dalam
Gambar 2.3 (Huang et al. 2011; Sanderson, 2006 dalam Neves et al. 2007). Beberapa
masalah umum dalam praperlakuan adalah terbentuknya produk penghambat,
pembukaan struktur lignin – hemiselulosa – selulosa kurang efektif, terlalu banyak
selulosa terdegradasi, perlunya biaya kapital (peralatan) atau operasi yang mahal,
daur ulang senyawa kimianya mahal, terbentuknya limbah, ataupun kondisi operasi
yang tidak aman (Geddes et al. 2011; Huang et al. 2011; Menon dan Rao, 2012;
Neves et al. 2007). Sejumlah cara praperlakuan dijabarkan dalam Tabel 2.2.
Praperlakuan yang telah dilakukan biasanya bertujuan untuk meningkatkan akses
enzim, menghilangkan lignin, dan mengganggu kristalinitas selulosa. Dalam banyak
studi, meningkatkan akses enzim dianggap lebih penting daripada menghilangkan
lignin (Zhu, 2011; Huang et al. 2011). Ahn et al. (2012) juga menunjukkan bahwa
praperlakuan yang menghasilkan konten selulosa tinggi lebih penting dibanding
dengan yang menghasilkan konten lignin rendah. Selain hal-hal di atas, hal yang
perlu diperhatikan adalah terbentuknya pseudo-lignin dalam metode pretreatment
tertentu (Hu et al. 2003).
Praperlakuan yang ada dikembangkan untuk mengurangi limbah, kerusakan,
inhibitor, gula nonfermentable, meningkatkan hasil gula, dan mengurangi biaya
praperlakuan (Kumar et al. 2009; Houghton et al. 2006). Secara garis besar,
praperlakuan fisik biasanya memerlukan energi besar, sedangkan praperlakuan
dan peralatan yang mahal (Taherzadeh dan Karimi, 2008). Dalam penelitian ini,
beberapa jenis praperlakuan dipilih dan dibandingkan untuk mengetahui metode
yang paling sesuai dengan prioritas kesederhanaan, keamanan, dan ramah
lingkungan.
Gambar 2.3. Perubahan Struktur Mikro Akibat Praperlakuan (Houghton et al. 2006)
2.5.2. Metode Hidrolisis
Tahap hidrolisis mentransformasi selulosa ke gula terfermentasi. Dua metode
umum hidrolisis adalah hidrolisis asam dan hidrolisis enzimatis. Metode hidrolisis
lain adalah hidrolisis termal yang sangat jarang digunakan. Hidrolisis enzimatis lebih
dipilih karena bekerja pada suhu wajar, menghasilkan yield tinggi dengan jumlah
yang sedikit, merupakan senyawa alami yang dapat terbiodegradasi dan ramah
Tabel 2.2. Berbagai Metode Praperlakuan
Metode Praperlakuan Keterangan Literatur
Praperlakuan asam: asam encer, dan asam pekat
Menghidrolisa hemiselulosa dan merusak struktur kristal selulosa, tapi menghasilkan produk samping inhibitor, dan memerlukan peralatan tahan korosi. Biasanya menggunakan H2SO4, tetapi asam fosfat
dikatakan menghasilkan lebih sedikit produk samping beracun dan dapat digunakan pada reaktor baja antikarat. Jenis asam encer memberi yield rendah sedangkan jenis asam pekat menghasilkan produk samping, mendegradasi selulosa dan memerlukan biaya daur ulang mahal.
Eshtiaghi et al. 2012 Merina dan Trihadinigrum, 2011
Satyanagalakshmi et al. 2011
Sornvoraweat dan Kongkiattikajorn, 2010 Sassner et al. 2008
Praperlakuan alkali/basa Memisahkan lignin dan sebagian hemiselulosa, dan meningkatkan reaktivitas selulosa. Biasanya menggunakan NaOH, Ca(OH)2, urea
atau Ammonia (SAA, ARP). NaOH juga meningkatkan derajat polimerisasi dan kristalinitas selulosa. Ammonia juga mengembangkan substrat yang tersisa.
Praperlakuan dengan agen pengoksidasi: hidrogen per-oksida, asam per asetat
Yield setinggi 98% berhasil dicapai. Saha dan Cotta, 2007
Teixeira et al. 1999 Gould, 1984
Praperlakuan dengan pelarut organik
Melarutkan lignin dan sebagian hemiselulosa tapi memerlukan peralatan dengan tekanan tinggi. Pelarut organik yang sudah digunakan misalnya metanol, etanol, aseton, etilen glikol, trietilen glikol, dan alkohol tetrahidrofurfuril.
Yamashita et al. 2010 Pan et al. 2005
Steam explosion, ammonia fiber expansion/explosion,
acid catalyzed steam
explosion
Bahan dipanaskan pada suhu dan tekanan tinggi kemudian didekompresi ke tekanan atmosfir secara tiba-tiba. Masih belum praktis karena butuh energi besar dan peralatan mahal.
Tabel 2.2. Berbagai Metode Praperlakuan (lanjutan)
Metode Praperlakuan Keterangan Literatur
Liquid Hot Water
(LHW)
Menghidrolisa hemiselulosa menggunakan air bersuhu tinggi (160 – 190oC) dan tekanan tinggi (30 bar). selulosa, ataupun lignin. Substrat dilarutkan dalam cairan ionik dan dipanaskan kemudian dipresipitasi dengan antisolven. Proses ini merupakan teknologi baru dan lebih cocok untuk biomassa berkayu.
Muhammad et al. 2012 Sathitsuksanoh et al. 2012
Guragain et al. 2011 Lee et al. 2009 Granstorm et al. 2008 Kosan et al. 2008
Praperlakuan mikrobial Jamur akar putih, coklat, dan lunak (Basidiomycetes) telah banyak digunakan untuk mendepolimerisasi substrat lignoselulosa tanpa banyak produk samping inhibitor
Chandel et al. 2011b Zhong et al. 2011 Cardona et al. 2007
Penggilingan Ekstrusi
Tanpa mempengaruhi lignin dan hemiselulosa, meningkatkan aksesibilitas dan merubah kristalinitas selulosa. Merupakan salah satu metode paling efektif tetapi kurang cocok diterapkan di industri. Penggilingan dilakukan dalam hampir semua proses di laboratorium.
Harun et al. 2011 Merina dan
trihadinigrum, 2011 Satyanagalakshmi et al. 2011
Hidrolisis asam menggunakan berbagai asam mineral pada suhu tinggi,
walaupun proses sering mendegradasi glukosa ke hidroksimetil furfural (HMF) dan
produk samping beracun lain, atau mencapai yield rendah. Harga asam, daur ulang,
dan pengolahan limbahnya masih menjadi masalah dalam hidrolisis asam.
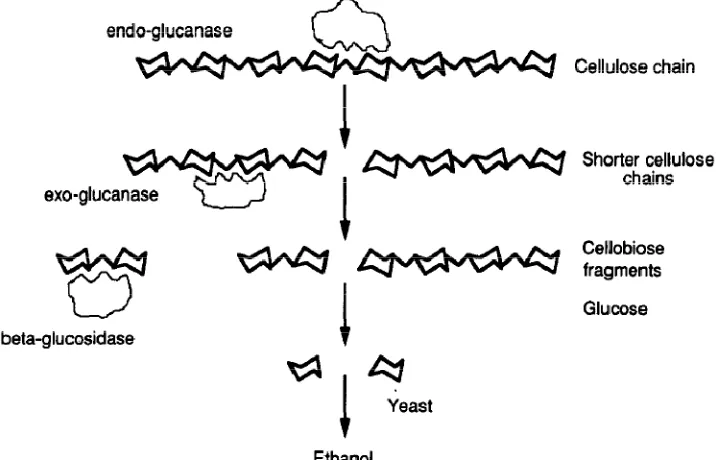
Gambar 2.4. Aktivitas Enzim dalam Hidrolisis Selulosa (Wyman, 1994)
Hidrolisis enzimatis memanfaatkan 3 kelompok enzim untuk berfungsi
dengan baik (Lihat Gambar 2.4). Pertama, 1,4--D-glukan glukanohidrolase (EC
3.2.1.3) dan 1,4--D-glukan 4-glukanohidrolase (EC 3.2.1.4), dikenal sebagai
endo-1,4--glukanase, memotong rantai selulosa secara acak. Kemudian, 1,4--D-glukan
glukohidroliase (EC 3.2.1.74) dan 1,4--D-glukan selobiohidroliase (EC 3.2.1.91),
dikenal sebagai ekso-1,4--glukanase berturut-turut membebaskan glukosa dan
juga sebagai selobiase, mengubah selobiosa menjadi D-glukosa (Joshi et al. 2011;
Geddes et al. 2011; Neves et al. 2007; Wyman, 1994).
Selulase komersial dan produksi on-site selulase dapat digunakan.
Kebanyakan glukanase diproduksi Trichoderma ressei (jamur akar halus) sedangkan
selobiase dari Aspergillus niger (Barta et al. 2010 dalam Geddes et al. 2011; Kaur et
al. 2007 dalam Joshi et al. 2011).
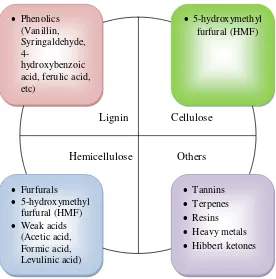
Gambar 2.5. Berbagai Senyawa Turunan Hidrolisis Asam (Chandel et al. 2011b)
Salah satu perbedaan terbesar hidrolisis asam dan enzim adalah produk
samping hidrolisis asam yang sangat beragam dan bersifat menginhibisi Lignin Cellulose
Hemicellulose Others
pertumbuhan. Selain itu, jenis hidrolisis asam menghasilkan limbah dan memerlukan
penanganan khusus. Oleh sebab itulah, proses hidrolisis yang digunakan dalam
penelitian ini menggunakan jenis hidrolisis enzim. Berbagai jenis produk samping
hasil hidrolisis asam dapat dilihat pada Gambar 2.5.
2.5.3. Fermentasi dan Skema Proses Terpadu
Ragi Saccharomyces cerevisiae merupakan mikroorganisme yang paling
disukai dalam fermentasi heksosa. Selain ragi, Pichia stipitis dan Candida shehatae
juga mampu memfermentasi heksosa dan pentosa ke etanol (Parekh et al. 1986
dalam Joshi et al. 2011). Gorsek dan Zajsek (2010) menemukan bahwa dalam
jangkauan suhu 16oC sampai 30oC, produksi etanol oleh ragi meningkat.
Di samping intensifikasi proses, penggembangan juga dilakukan dalam
sistem bioreaktor misalnya external loop liquid-lift bioreactor, circulating loop
bioreactor, bioreaktor membran, ultrasonic airlift reactors, fluidized bed reactor
(Stang et al. 2001; Roble et al. 2003; Huang et al. 2011). Sistem bioreaktor yang
dikembangkan biasanya mengangkat isu-isu mengenai masalah viskositas campuran
yang tinggi sehingga mengurangi transfer massa ataupun merujuk pada upaya
integrasi proses ekstraksi etanol secara simultan dalam proses kontiniu sehingga
mengurangi inhibisi produk. Beberapa skema proses yang sering digunakan dalam
Tabel 2.3. Skema Proses Terpadu dalam Produksi Bioetanol
Tahap hidrolisis selulosa dan fermentasi dipisah sehingga mengurangi interaksi antar tahap.
Kelemahan: sering kali produk akhir hidrolisis menghambat kerja enzimnya dan membatasi kinerjanya.
Tahap hidrolisis selulosa dan fermentasi digabung. Secara umum meningkatkan kinetika fermentasi dan ekonomi karena mengurangi akumulasi gula yang menginhibisi enzim dan adanya etanol mengurangi kontaminasi mikroba.
Kelemahan: kondisi optimal enzim dan mikroba mungkin berbeda dan banyak gula dipakai untuk pertumbuhan ragi.
Simultaneous saccharification and cofermentation (SSCF)
Sama seperti SSF tetapi fermentasi pentose juga diintegrasikan ke dalam proses. Kelemahan: sama seperti SSF tapi
lebih rumit lagi.
Consolidated
BioProcessing (CBP)
atau Direct Microbial
Conversion (DMC)
Produksi selulase, hidrolisis substrat, dan fermentasi dilakukan dalam satu tahapan. Kelemahan CBP/DMC: tidak ada mikroba alami yang mampu memproduksi selulase sekaligus memfermentasi hidrolisat (harus menggunakan mikroba hasil rekayasa genetik) dan proses terbentur oleh wujud alami suspensi yang berserat (rheologi aliran).
(Joshi et al. 2011; Geddes et al. 2011; Neves et al. 2007)
2.5.4. Strategi-strategi yang Diterapkan untuk Meningkatkan Tiap Proses
Selain pengembangan teknologi dan mikroorganisme dalam proses itu
sendiri, beberapa strategi juga telah dikembangkan untuk meningkatkan efisiensi tiap
proses. Beberapa di antara strategi-strategi tersebut adalah detoksifikasi hidrolisat,
penambahan additif, immobilisasi sel dan enzim, penambahan antibiotik/agen
anaerob penghasil selulosom dan/atau strain flokulen (Chandel et al. 2011b; Huang
et al. 2011; Najafpour et al. 2004; Rakin et al. 2009; Maye, 2011).
Berbagai cara detoksifikasi telah tersedia misalnya evaporasi vacuum,
separasi membran, netralisasi, overliming, activated charcoal pretreatment, resin
penukar ion, ekstraksi dengan etil asetat, aklimatisasi mikrobial, detoksifikasi
mikrobial in-situ, dan detoksifikasi enzimatis. Dari cara-cara yang ada, detoksifikasi
biologislah yang paling menguntungkan (Chandel et al. 2011b). Detoksifikasi
biologis dapat dilakukan dengan simultaneous detoxification and enzymatic
production, simultaneous detoxification andfermentation, dan cara lainnya.
Penggunaan aditif seperti Tween 20, Tween 80, polietilen glikol (PEG),
bovine serum albumin (BSA), dapat mengurangi adsorpsi selulase ke lignin dan
menjaga kestabilan enzim. Sebuah kelas protein non katalitik seperti ekspansin,
protein mirip ekspansin, dan swollenins, diketahui dapat mengubah struktur selulosa
walau penjelasan mengenai cara kerja protein ini masih sebatas spekulasi (Huang et
al. 2011). Aditif lain seperti ion Mg2+dapat meningkatkan toleransi ragi S. cerevisiae
terhadap etanol melalui penurunan permeabilitas membran plasma (Hu et al. 2003).
2.6. Produksi Bioetanol dari Eceng Gondok dan Perkembangannya
Penelitian mengenai pembuatan bioetanol dari eceng gondok dapat dilihat di
Tabel 2.4. Dari tabel tersebut dapat dilihat bahwa hampir semua penelitian berkutat
berbagai studi telah dilakukan, hasil-hasil tersebut belum diterapkan di industri
karena sebab-sebab seperti: yield etanol yang rendah; teknik pemrosesan yang
kompleks dan lama; penggunaan bahan kimia, peralatan, ataupun alur proses yang
mahal; dan teknik yang tidak ramah lingkungan. Dalam penelitian ini akan dicoba
teknik pemrosesan yang berbeda yaitu fermentasi non-steril yang dilangsungkan
bersamaan dengan hidrolisis hemiselulosa-selulosa, isomerisasi xilosa dan ekstraksi
etanol serta sistem daur-ulang larutan fermentasi.
2.7. Komponen – Komponen dalam Produksi Bioetanol
2.7.1. Selulosa
Selulosa merupakan glukan paling penting yang tersusun oleh sakarida
homopolimer selobiosa yang terdiri dari dua molekul -D-glukosa yang terikat
dalam ikatan -(1–4)- glikosidik dan dapat berputar untuk membentuk ikatan
intramolekul dan intermolekul (Bobleter, 2005). Dalam banyak penelitian, eceng
gondok dikeringkan untuk mempermudah penanganannya, tetapi selulosa mengalami
modifikasi fisik berupa penciutan (disebut juga hornifikasi) yang dapat menghambat
sakarifikasi saat didehidrasi (Arantes dan Saddler, 2011; Zhu, 2011; Houghton et al.
Tabel 2.4. Berbagai Penelitian mengenai Bioetanol dari Eceng Gondok
Judul Penelitian Metodologi Hasil
Abdel-Fattah dan
- Praperlakuan: NaOH, alkalin H2O2, asam perasetat, NaClO2, kombinasi NaClO2 dengan NaOH, alkalin H2O2, atau asam perasetat.
- Hidrolisis: enzimatis dengan selulase
- Variasi: metode praperlakuan, penambahan gula dan etanol, penambahan selobiase, dan waktu sakarifikasi (hidrolisis)
Hasil terbaik dicapai dengan
kombinasi praperlakuan
NaClO2 selama 1 jam dan asam perasetat selama 15
menit pada 100 oC.
Penambahan 8% glukosa
ataupun 8% etanol
- Praperlakuan: dicuci, akar dibuang, dikeringkan, ditepungkan, kemudian diolah
dalam larutan NaOH 1, 3, 5, 7, 10% w/v pada suhu 60 oC (24 jam) atau 100 oC (2 jam).
Lalu didinginkan dan diolah dengan H2O2 0,1; 0,5; 1; 2; 3; dan 6% v/v selama 24 jam. - Hidrolisis: enzimatis dengan Cellulast 1.5 L and Viscozyme L dengan konsentrasi 1, 5, 10, 15, 20–25% v/v dan rasio 1:9, 3:7, 5:5, 7:3, dan 9:1 selama 112 jam.
- Mikroba fermentasi: Saccharomyces cerevisiae KCTC 7928
- Mode: SHF
- Variasi: konsentrasi NaOH, suhu dan waktu praperlakuan dengan NaOH, konsentrasi H2O2, konsentrasi enzim, rasio enzim, konsentrasi eceng gondok (mula-mula 2,5% dikonsentrasikan dengan faktor 2, 5, 7, 10 dan 15).
Konversi glukosa 71,42% dicapai untuk NaOH 7%
pada 100 oC dan H2O2 2%.
Tabel 2.4. Berbagai Penelitian mengenai Bioetanol dari Eceng Gondok (lanjutan)
Judul Penelitian Metodologi Hasil
Eshtiaghi et al. 2012.
Preliminary study for
bioconversion of
water hyacinth
(Eichhornia
crassipes) to bioethanol
- Praperlakuan: dibersihkan, dipotong-potong dan dikeringkan. Selanjutnya:
i. 10 g tepung dicampur ke 1, 3, 5, 7 dan 9% w/w larutan asam sulfat sampai 100 ml
dan diautoklafpada 121 oC selama 15 menit
ii. 10 g tepung dicampur ke 1, 2, 3, 4, dan 5% w/w larutan NaOH sampai 100 ml dan
dipanaskan pada 85 oC selama 1 jam
iii. 2 g tepung dicampur ke 20 ml air dan dipanaskan pada 160 oC dan 200 oC selama
10 menit
- Hidrolisis: enzimatis dengan Crystalzyme 200 XL, Cellulast 1.5 L FG, Alcalase 2.5 L DX, Validase ANC-L dan Xylanase (rasio 1:1:1:1:1) dengan konsentrasi 0,8% w/w
pada 55 oC selama 12 jam
- Mikroba fermentasi: Saccharomyces cerevisiae 0,2 g/ 50 ml sampel
- Mode: SHF
- Variasi: metode praperlakuan, konsentrasi asam, konsentrasi alkali, suhu pemanasan air, konsentrasi enzim (0,8% w/w dan 4% w/w) dan lama fermentasi
Konversi gula optimum
mencapai 50,5% dengan
Hidrolisat kemudian dinetralkan dengan Ba(OH)2 sampai pH 4,5.
- Hidrolisis: enzimatis dengan selulase GC220 0 – 1000 IU pada 50 oC selama 24 jam,
diikuti evaporasi vakum pada 70 oC untuk pengentalan.
- Mikroba fermentasi: (masing – masing) 0,1 g per 100 ml
Saccharomyces cerevisiae NBRC10217
Saccharomyces cerevisiae sake yeast No.7
Saccharomyces cerevisiae brewers’ yeast BSRIYB23-3
Saccharomyces cerevisiae TY2
Pichia stipitis NBRC1689 - Mode: SHF
- Variasi: loading eceng gondok, konsentrasi selulase, dan jenis mikroba fermentasi
Kadar etanol setinggi 9,6 1,1 g/l berhasil dicapai untuk larutan terkonsentrasi.
Konsentrasi selulase
optimum 400 IU. Loading
eceng gondok di atas 3 g
tidak memberi dampak
positif. Jenis mikroba yang memberikan hasil maksimum
Tabel 2.4. Berbagai Penelitian mengenai Bioetanol dari Eceng Gondok (lanjutan)
Judul Penelitian Metodologi Hasil
Guragain et al.
- Hidrolisis: enzimatis dengan selulase dari T. reesei
- Mikroba fermentasi: Saccharomyces cerevisiae
- Mode: -
- Hidrolisis: asam sulfat 5% pada suhu 121 3 o
C, 60 menit
- Variasi: metode praperlakuan, besar daya ultrasonication, dan lama ultrasonication
Produksi gula tertinggi
(155,13 mg gula/g massa
surface structure and crystallinity of water
hyacinth (Eichhornia
crassipes) following
recombinant α
-L-arabinofuranosidase (abfa) treatment
- Praperlakuan: dipotong, dibersihkan, dikeringkan, dan ditepungkan.
- Hidrolisis: enzimatis dengan α-L-arabinofuranosidase dengan rasio enzim intraselular
dan ekstraselular 1:10, 1:8, 1:4, 1:2, 1:1 pada 70 oC selama 1, 2, 4, 8, 12, dan 24 jam.
- Variasi: perbandingan enzim intraselular (P) dan enzim ekstraselular (S) (analisa aktivitas), perbandingan enzim intraselular (P) dan enzim ekstraselular (S) (konsentrasi gula pereduksi), lama hidrolisis
Aktivitas enzim terbaik pada rasio P:S = 1:10 sampai 1:0.
Rasio P:S = 1:2
menghasilkan konsentrasi
gula pereduksi terbesar.
Tabel 2.4. Berbagai Penelitian mengenai Bioetanol dari Eceng Gondok (lanjutan)
Judul Penelitian Metodologi Hasil
Merina dan
- Praperlakuan: dibersihkan, dikeringkan, dan ditepungkan. Selanjutnya:
i. 25 g tepung dicampur ke 420 ml asam sulfat 2% v/v disetir 7 jam diikuti netralisasi dan penambahan buffer
ii. pemanasan (121 oC, 30 menit) diikuti penambahan air dan buffer
- Hidrolisis: likuifikasi (A. niger) dan pemanasan diikuti (atau tanpa) sakarifikasi (S. tidaknya sakarifikasi, dan jenis mikroba fermentasi.
Kadar etanol tertinggi 0,27% dicapai dengan pemanasan, likuifikasi dengan seeding ratio 8/40 v/v dan sakarifikasi diikuti fermentasi 3 hari oleh
- Praperlakuan: dipotong, dikeringkan, ditepungkan, lalu 15 g tepung dicampur air
dengan perbandingan 1:3 dan diautoklafselama 20 menit pada 121 oC.
- Delignifikasi:
i. Dengan jamur akar putih (Phanerochaete chrysosporium) selama 8 minggu
ii. Dengan gabungan Pleurotus osterotus dan Phanerochaete chrysosporium selama 8
minggu
- Variasi: metode delignifikasi
Delignifikasi sampai 67,23% berhasil dicapai pada minggu
ke 8. Selulosa dan
Tabel 2.4. Berbagai Penelitian mengenai Bioetanol dari Eceng Gondok (lanjutan)
Judul Penelitian Metodologi Hasil
Satyanagalakshmi et
al. 2011.
Bioethanol
production from acid
pretreated water
hyacinth by separate
hydrolysis and
fermentation.
- Praperlakuan: dibersihkan, dikeringkan, digiling dengan knife mill, kemudian 10 g
biomassa dicampur ke: (i) HCl 2% v/v; (ii) H2SO4 2% v/v; (iii) asam asetat 30% v/v;
(iv) asam formiat 30% v/v dan diautoklaf (121 oC, 1 jam) diikuti netralisasi dengan
NaOH, pencucian dan pengeringan.
- Hidrolisis: enzimatis dengan selulase komersial Zytex
- Mikroba fermentasi: Saccharomyces cerevisiae
- Mode: SHF
- Variasi: konsentrasi asam (1-7% w/v), loading biomassa (5; 7,5; 10; 12,5; 15 dan
17,5% w/w), jenis surfaktan (Tween 80, Triton X-100, dan PEG), konsentrasi surfaktan (0,01; 0,02; 0,05; 0,1 dan 0,2), konsentrasi selulase (10, 30, 50, 70 FPU/g biomassa),
suhu (80 o, 100 o & 121 oC), dan waktu inkubasi (15 – 90 menit)
Hasil terbaik (0,292% w/v etanol) untuk waktu inkubasi 24 jam, loading biomassa
sulfat pada loading padatan
10% w/w pada suhu 121 oC
- Praperlakuan: pencucian, pengecilan ukuran, dan pengeringan pada 80 oC selama 24
jam, diikuti sterilisasi dengan autoklafpada 121 oC selama 15 menit.
- Hidrolisis: termal pada 175 oC dan tekanan 8 – 10 bar (10 g eceng gondok per 200 ml
aquades)
- Mikroba fermentasi: Pichia stipitis NRRL Y-7124
- Mode: SHF
- Variasi: suhu (25 dan 30 oC), dan laju pengadukan (75 dan 150 rpm)
Yield etanol tertinggi (58,356 ge/gs) diperoleh pada variasi
suhu 25 oC dan pengadukan
i. Dengan asam sulfat 0,25% saja
ii. Dengan asam sulfat 0,25% dan jamur akar putih Echinodontium taxodii
iii. Dengan asam sulfat 0,25% dan jamus akar coklat Antrodia sp. 5898
- Hidrolisis: enzimatis
- Mikroba fermentasi: Saccharomyces cerevisiae
- Mode: SHF
- Variasi: metode praperlakuan, suhu praperlakuan dan lama praperlakuan
Yield etanol tertinggi 0,192 g/g massa kering dicapai untuk copraperlakuan asam
sulfat dan E. taxodii selama
Tabel 2.4. Berbagai Penelitian mengenai Bioetanol dari Eceng Gondok (lanjutan)
Judul Penelitian Metodologi Hasil
Mukhopadhyah dan
- Hidrolisis: enzimatis dengan selulase dari Trichoderma reesei ATCC 26921 dan
-glukosidase dari Aspergillus phoenicis ATCC 52007
- Mikroba fermentasi: Saccharomyces cerevisiae MTCC 171 (tahap 1) diikuti
Pachysolen tannophilus MTCC 1077 (tahap 2) - Mode: SHF, SSF, SBB, PH-SSF
- Praperlakuan: dibersihkan, dikeringkan, digiling, kemudian 1,5 g bubuk diautoklaf
dalam 100 ml asam sulfat 0,1 M selama 10 – 90 menit, suhu 120 – 135 oC.
- Hidrolisis: enzimatis dengan selulase, -amilase, xilanase, amiloglukosidasie, dan
pektinase dalam 0,1 M Na3PO4, 48 jam, 50 oC.
- Mikroba fermentasi: (monokultur dan co-kultur)
Saccharomyces cerevisiae TISTR 5048
Saccharomyces cerevisiae KM 1195
Saccharomyces cerevisiae KM 7253
Candida tropicalis TISTR 5045 - Mode: SHF
- Variasi: waktu praperlakuan, suhu praperlakuaan, dan jenis mikroba fermentasi
Yield 0,27 g/g biomassa dan
5045. Kondisi optimum
praperlakuan dicapai pada
135 oC dan 30 menit, dan isolated from various hydrospheres
- Praperlakuan: dibersihkan, dikeringkan, lalu digiling
- Hidrolisis: 3 g bubuk ditambah ke 50 ml asam sulfat encer 0,5 – 4% v/v suhu 121 oC,
waktu 0,5 – 1,5 jam kemudian dinetralkan dan disaring. - Mikroba fermentasi:
Saccharomyces cerevisiae 484 dari Sungai Katsuragawa
Saccharomyces cerevisiae K7 dan 11 strain lain - Mode: SHF
- Variasi: konsentrasi asam sulfat, waktu hidrolisis
Hasil terbaik (1,77 0,4 g/l
etanol) diperoleh untuk
hidrolisis dengan asam sulfat
encer 1% v/v suhu 121 oC
Tabel 2.4. Berbagai Penelitian mengenai Bioetanol dari Eceng Gondok (lanjutan)
Judul Penelitian Metodologi Hasil
Mishima et al. 2008.*
Saccharomyces cerevisiae NBRC 2346
Escherichia coli KO11 (strain rekombinan) - Mode: SHF, SSF
- Variasi: Jenis biomassa (eceng gondok dan water lettuce), jenis mikroba fermentasi,
dan mode proses.
Hasil terbaik (16,9 g/l etanol) dicapai untuk substrat eceng gondok dengan proses SSF
- Praperlakuan: dibersihkan, dipotong-potong, dihancurkan, lalu dikeringkan
- Hidrolisis: 100 g tepung eceng gondok dicampur dengan 1% atau 10% H2SO4 sampai
1000 ml, lalu diautoklafpada 121oC selama 15 menit. Kemudian didinginkan, disaring,
dipanaskan ke 60 oC, ditambah NaOH dan Ca(OH)2 sampai pH 10, ditambah 10 g
neopepton, pH disesuaikan ke 5,6, lalu ditambah air sampai 1000 ml.
- Mikroba fermentasi: Candida shehatae TISTR 5843
- Mode: SHF
- Variasi: jenis substart (sabouraud dextrose broth, sabouraud xylose broth, hidrolisat
eceng gondok), dan konsentrasi asam sulfat
Yield etanol tertinggi 0,19 g/g atau 1,01 g/l pada konsentrasi asam sulfat 10%.
Walaupun kebanyakan polisakarida larut dalam air, selulosa tidak larut dalam
air karena ikatan hidrogen intra dan intermolekuler (Kajiwara dan Miyamoto, 2005).
Alomorf selulosa ada 4: selulosa I, selulosa II, selulosa III, dan selulosa IV. Dari
alomorf ini, selulosa I lah yang paling banyak ditemukan di alam. Selulosa I sendiri
tersusun oleh kombinasi fasa triklinik Idan fasa monoklinik I(Perez dan Mazeau,
2005). Polimerasi dan kristalinitas selulosa bervariasi dan mempengaruhi sifat
hidrolitiknya (Lihat Gambar 2.6 dan 2.7).