PEMBUATAN BAHAN SURFAKTAN KOSMETIKA
MELALUI MODIFIKASI KIMIA DARI KITOSAN
MENJADI KITOSAN PALMITAT
TESIS
Oleh
NURMARIANA OKTO DELIMA SINAGA 087006021/KM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PEMBUATAN BAHAN SURFAKTAN KOSMETIKA MELALUI
MODIFIKASI KIMIA DARI KITOSAN
MENJADI KITOSAN PALMITAT
TESIS
Diajukan Sebagai Salah Satu Syarat untuk
Memperoleh Gelar Magister Sains dalam Program Studi Magister Kimia pada Fakultas Matematika dan Ilmu Pengetahuan Alam
Universitas Sumatera Utara
Oleh
NURMARIANA OKTO DELIMA SINAGA 087006021/KM
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
Judul Tesis : PEMBUATAN BAHAN SURFAKTAN KOSMETIKA MELALUI MODIFIKASI KIMIA DARI KITOSAN MENJADI KITOSAN PALMITAT
Nama : Nurmariana Okto Delima Sinaga
Nomor Pokok : 087006021
Program Studi : Ilmu Kimia
Menyetujui
Komisi Pembimbing
(Prof. Dr. Jamaran Kaban, MSc) (Dr. Mimpin Ginting, MS)
Ketua Anggota
Ketua Program Studi Dekan
(Prof. Basuki Wirjosentono, MS.PhD) (Prof. Dr. Eddy Marlianto, MSc)
Telah diuji pada
Tanggal 10 Mei 2010
PANITIA PENGUJI TESIS
Ketua : Prof. Dr. Jamaran Kaban, MSc
Anggota : 1. Dr. Mimpin Ginting, MS
2. Prof. Basuki Wirjosentono, MS, Ph.D
3. Prof. Dr. Harry Agusnar, MSc, M.Phil
Abstrak
Senyawa kitosan telah banyak dimanfaatkan dalam kehidupan melalui modifikasi kimia. Dalam penelitian ini kitosan ditransformasi menjadi kitosan palmitat sebagai bahan surfaktan kosmetik.
Metodologi pembuatan kitosan palmitat dilakukan melalui reaksi transesterifikasi antara metil palmitat dengan kitosan asetat menggunakan katalis natrium metoksida. Sedangkan kitosan asetat diperoleh melalui pembentukan aldimin kitosan melalui reaksi antara kitosan dan asetaldehid yang diikuti reaksi asetilasi dengan asam asetat anhidrid. Kitosan palmitat yang terbentuk dianalisa dengan FT-IR dan dilakukan uji HLB.
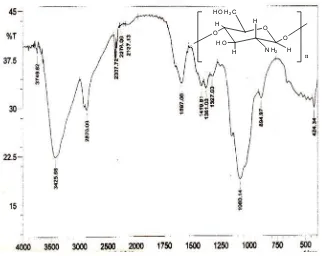
Hasil analisa FT-IR kitosan palmitat memberikan puncak-puncak serapan
pada daerah bilangan gelombang (cm-1) 3387 dan 3371 yang menunjukkan gugus
-NH dan -OH, 1720 yang menunjukkan gugus C=O ester, 1562 yang menunjukkan gugus fungsi C-O-C serta 717 yang menunjukkan alkil rantai panjang.Hasil uji HLB memberikan nilai 12,3 yang menunjukkan bahwa kitosan palmitat sebagai bahan surfaktan kosmetik merupakan zat pengemulsi O/W.
Abstract
Kitosan compound what does our life benefit via chemical modification. In this research the kitosan is transformation to kitosan palmitat as material as surfaktan cosmetics.
Kitosan palmitat makings is done with transesterifikasi reaction among palmitat methyl with kitosan acetic in natrium metoksida is catalis. On the contrary kitosan asetic is produced through formation of aldimin kitosan with reaction kitosan and acetaldehyda followed by acetilasi reaction with acetic anhidryda. Kitosan palmitat that molded being analysed by FT-IR and done by HLB quiz.
FT-IR Kitosan Palmitat morphological result give uptake top on wave
number region (cm-1) 3387 and 3371 one points out NH bunches and OH, 1720 one
points out C=O bunches esters, 1562 one point out function bunch C-O-C and 717 one point out elongated chain alkyls. Result tests HLB assigns value 12,3 one point out that kitosan palmitat as material as surfaktan cosmetics constitutes emulsifier substance o/w.
KATA PENGANTAR
Segala pujian dan rasa syukur yang begitu besar saya naikkan ke hadirat Tuhan yang begitu mengasihi hidup saya, karena berkat-Nya sangat saya rasakan menyertai dan menolong hidup saya sehingga dapat menyelesaikan tesis ini.
Terima kasih yang begitu besar saya sampaikan kepada Bapak Prof. Dr Jamaran Kaban, MSc sebagai komisi pembimbing utama dan Bapak Dr. Mimpin Ginting, MS sebagai anggota komisi pembimbing yang sangat banyak menolong dan membimbing saya dalam menyelesaikan tesis ini.
Ucapan terima kasih juga tak lupa saya sampaikan kepada Bapak Prof. Dr. Eddy Marlianto, MSc sebagai Dekan FMIPA USU dan kepada Bapak Prof. Basuki Wirjosentono, MS, PhD sebagai Ketua Program Pasca Sarjana Kimia USU yang juga sebagai komisi penguji serta Bapak Prof. Dr. Harry Agusnar, MSc, M. Phil sebagai Sekretaris Program Pasca Sarjana Kimia USU yang juga sebagai komisi penguji, yang telah banyak memberikan dorongan semangat dan masukan-masukan yang sangat menolong saya dalam menyelesaikan tesis ini.
Saya juga berterima kasih kepada Bapak Prof. Dr. Tonel Barus sebagai komisi penguji yang telah memberikan arahan dan masukan yang begitu bermanfaat bagi saya dalam menyelesaikan tesis ini. Begitu juga kepada Bapak Prof. Dr. Yunazar Manjang sebagai komisi penguji dari luar yang telah memberikan masukan
positif bagi saya dalam merampungkan tesis ini. Kepada Bapak Drs. Adil Ginting, MSc sebagai Kepala Laboratorium Kimia Organik, saya ucapkan terima kasih karena telah memberikan penggunaan laboratorium dengan semestinya selama saya melaksanakan penelitian. Terima kasih juga saya sampaikan kepada Bapak Drs. M. Hutapea sebagai kepala sekolah SMA N 1 Sibolga tempat saya bertugas. Juga kepada asisten yang ada di laboratorium kimia organik FMIPA USU yaitu : Robby, Aspriadi, Yemima, Mery, Maria, beserta kawan-kawan yang telah membantu saya selama mengadakan penelitian di laboratorium kimia organik FMIPA USU Medan.
juga kepada mertua saya St. A. Butarbutar (alm) dan R. Situmorang yang selalu mendoakan saya, sehingga saya dapat menyelesaikan tesis ini dengan baik.
Akhirnya rasa terimaksih saya yang begitu besar dan tidak dapat saya gambarkan saya ucapkan kepada suami tercinta Drs. Rudolf S. Butarbutar, MPd yang selalu memberikan perhatian dan kasih sayang yang sangat besar kepada saya selama perkuliahan sampai dengan penulisan tesis ini, juga kepada anak-anak kami Wilbert Ramonray Butarbutar, Jonhard Ariady Butarbutar, Gideon Apriely Butarbutar dan anak bungsu kami Harry Eligusty Butarbutar yang selalu sabar selama saya mengikuti pendidikan sampai selesainya penyusunan tesis ini.
Medan, Mei 2010
(Nurmariana Okto Delima Sinaga)
DAFTAR ISI
Halaman
ABSTRAK... i
ABSTRACT... ii
KATA PENGANTAR ... iii
DAFTAR ISI ... v
DAFTAR GAMBAR ... ix
DAFTAR TABEL ... x
DAFTAR LAMPIRAN ... xi
BAB 1 : PENDAHULUAN ... 1
1.1.Latar Belakang ... 1
1.2.Permasalahan ... 3
1.3 Pembatasan Masalah ... 3
1.4 Tujuan Penelitian ... 3
1.5 Manfaat Penelitian ... 4
1.6 Lokasi Penelitian ... 4
1.7 Metodologi Penelitian... 4
BAB 2 : TINJAUAN PUSTAKA ... 5
2.1 Kitosan ... 5
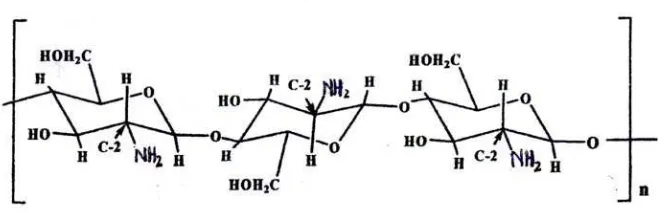
2.1.1Struktur Kitosan... 5
2.1.2Sifat-sifat Fisika dan Kimia Kitosan... 6
2.1.2.1Sifat Fisika ... 6
2.1.2.2Sifat Kimia ... 9
2.1.3Kegunaan Kitosan... 12
2.2 Kosmetik... 13
2.2.1 Bahan Kosmetik... 13
2.2.2 Pemanfaatan Kitosan dalam Bidang Kosmetik 14 2.3 Reaksi Interesterifikasi... 16
2.4 Gugus Pelindung... 17
2.5 Surfaktan dan Pengujian HLB ... 18
2.5.2 Penentuan Uji HLB
(Hydrophilic Lipophilic Balance)... 19
BAB 3 METODE PENELITIAN ... 22
3.1 Alat dan Bahan... 22
3.2 Prosedur Penelitian ... 22
3.2.1 Pembuatan Reagen dan Standarisasi ... 22
3.2.1.1 Pembuatan Larutan Indikator pp... 22
3.2.1.2 Pembuatan Larutan H2C2O4 0,1 N... 23
3.2.1.3 Pembuatan Larutan KOH-Alkohol 0,5N 23 3.2.1.4 Pembuatan Larutan KOH 0,1N... 23
3.2.1.5 Pembuatan larutan HCl 0,5 N... 23
3.2.1.6 Pembuatan larutan KOH 0,02N... 23
3.2.1.7 Pembuatan Alkohol Netral... 23
3.2.2 Pembuatan Metil Palmitat... 23
3.2.3 Pembuatan Aldimin Kitosan... 24
3.2.4 Pembuatan Kitosan Asetat... 24
3.2.5 Pembuatan Kitosan Palmitat... 25
3.2.6. Uji HLB dengan Metode Titrasi... 25
3.2.6.1 Analisis Bilangan Penyabunan... 25
3.2.6.2 Analisis Bilangan Asam... 25
3.3 Bagan Penelitian ... 26
3.3.1 Pembuatan Metil Palmitat ... 26
3.3.2 Pembuatan Aldimin Kitosan ... 27
3.3.3 Pembuatan Kitosan Asetat... 28
3.3.4 Pembuatan Kitosan Palmitat... 29
3.3.5 Bagan Analisis... 30
3.3.5.1 Analisis Bilangan Penyabunan... 30
3.3.5.2 Analisis Bilangan Asam ... 30
BAB 4 HASIL DAN PEMBAHASAN ... 31
4.1 Hasil ………. ... 31
4.1.2 Metil Palmitat ... 32
4.1.3 Kitosan Asetat ... 32
4.1.4 Kitosan Palmitat ... 34
4.1.5 Nilai HLB ... 35
4.2 Pembahasan ... 36
4.2.1 Pembuatan Metil Palmitat... 36
4.2.2 Reaksi Kitosan dengan Asetat Anhidrida 37 4.2.3 Reaksi Kitosan Asetat dengan Metil Metil Palmitat... 40
4.2.4 Pengujian Nilai HLB ... 42
BAB 5 KESIMPULAN DAN SARAN ... 45
5.1 Kesimpulan ... 45
5.2 Saran ……. ... 46
DAFTAR GAMBAR
Nomor Judul Halaman
1.1 Struktur Turunan Kitosan... 2
2.1. Struktur Kitosan ... 5
2.2. Struktur Kitin... 6
2.3. Struktur Selulosa... 6
2.4. Penggunaan Beberapa Turunan Kitosan dalam Bidang Kosmetik... 15
2.5 Skala Penunjuk Nilai HLB Surfaktan... 23
4.1 Spektrum FT-IR Kitosan ... 31
4.2 Spektrum FT-IR Metil Palmitat ... 32
4.3 Spektrum FT-IR Aldimin Kitosan ... 33
4.4 Spektrum FT-IR Kitosan asetat ... 34
4.5 Spektrum FT-IR Kitosan Palmitat ... 35
4.6 Mekanisme Reaksi Pembuatan Metil Palmitat... 37
4.7 Mekanisme Reaksi Pembuatan Kitosan Asetat... 39
DAFTAR TABEL
Nomor Judul Halaman
2.1 Sifat-sifat dan Pemanfaatan Kitosan... 14
2.2 Nilai HLB Beberapa Surfaktan... 23
2.3 Nilai HLB Gugus Fungsi... 24
4.1 Penentuan Bilangan Penyabunan ... 40
Abstrak
Senyawa kitosan telah banyak dimanfaatkan dalam kehidupan melalui modifikasi kimia. Dalam penelitian ini kitosan ditransformasi menjadi kitosan palmitat sebagai bahan surfaktan kosmetik.
Metodologi pembuatan kitosan palmitat dilakukan melalui reaksi transesterifikasi antara metil palmitat dengan kitosan asetat menggunakan katalis natrium metoksida. Sedangkan kitosan asetat diperoleh melalui pembentukan aldimin kitosan melalui reaksi antara kitosan dan asetaldehid yang diikuti reaksi asetilasi dengan asam asetat anhidrid. Kitosan palmitat yang terbentuk dianalisa dengan FT-IR dan dilakukan uji HLB.
Hasil analisa FT-IR kitosan palmitat memberikan puncak-puncak serapan
pada daerah bilangan gelombang (cm-1) 3387 dan 3371 yang menunjukkan gugus
-NH dan -OH, 1720 yang menunjukkan gugus C=O ester, 1562 yang menunjukkan gugus fungsi C-O-C serta 717 yang menunjukkan alkil rantai panjang.Hasil uji HLB memberikan nilai 12,3 yang menunjukkan bahwa kitosan palmitat sebagai bahan surfaktan kosmetik merupakan zat pengemulsi O/W.
Abstract
Kitosan compound what does our life benefit via chemical modification. In this research the kitosan is transformation to kitosan palmitat as material as surfaktan cosmetics.
Kitosan palmitat makings is done with transesterifikasi reaction among palmitat methyl with kitosan acetic in natrium metoksida is catalis. On the contrary kitosan asetic is produced through formation of aldimin kitosan with reaction kitosan and acetaldehyda followed by acetilasi reaction with acetic anhidryda. Kitosan palmitat that molded being analysed by FT-IR and done by HLB quiz.
FT-IR Kitosan Palmitat morphological result give uptake top on wave
number region (cm-1) 3387 and 3371 one points out NH bunches and OH, 1720 one
points out C=O bunches esters, 1562 one point out function bunch C-O-C and 717 one point out elongated chain alkyls. Result tests HLB assigns value 12,3 one point out that kitosan palmitat as material as surfaktan cosmetics constitutes emulsifier substance o/w.
BAB 1
PENDAHULUAN
1.1
Latar Belakang
Salah satu terobosan yang dapat dilakukan dalam kimia dan teknologi adalah
pengembangan modifikasi kimianya. Dalam hal ini kitosan telah banyak menarik
perhatian peneliti dalam penelitian dasar maupun penelitian aplikasi yang meliputi
bidang biologi, biokimia, kimia organik, polimer, farmakologi dan obat-obatan
(Kaban, 2009).
Kitosan adalah polisakarida alam yang diperoleh dari deasetilasi kitin, dengan
derajat deasetilasi antara 80-90% (Uragami, 2006). Kitosan mempunyai rumus
umum (C6H9NO3)n atau disebut poli (β(1,4)-2-amino-2-deoksi-D-Glukopiranosa).
Sifat kimia dari kitosan antara lain merupakan poliamin linear, mempunyai gugus
amina dan gugus hidroksil yang reaktif, dapat membentuk kelat dengan ion logam
transisi. Sedangkan sifat biologisnya, kitosan mudah mengalami biodegradasi, tidak
beracun, dan bersifat biokompatibel. Adanya gugus amina (-NH2) dan gugus
hidroksil (-OH) menyebabkan kitosan mempunyai reaktifitas kimia yang tinggi dan
mudah dimodifikasi secara kimia (Skjak-Braek, et al., 1989).
Kitosan merupakan turunan kitin yang sangat bermanfaat. Hal ini karena
kitosan memiliki berat molekul yang tinggi, sifat polielektrolit, keberadaan gugus
fungsional, kemampuan untuk membentuk gel, dan kemampuan mengadsorbsi.
Kitosan dapat dimodifikasi secara kimia dan enzimatik dan bersifat biodegradable
dan biokompatibel dengan sel dan jaringan manusia. (Synowiecki and Al-Kateeb,
Berdasarkan sifat fisika maupun kimianya, kitosan dan turunannya dapat
digunakan dalam berbagai aplikasi misalnya dalam pembuatan produk kosmetik.
Kitosan dan turunannya dapat digunakan sebagai bahan kosmetik seperti krim badan,
perawatan rambut dan cat kuku (Dutta, 2006).
Salah satu turunan kitosan yang digunakan sebagai bahan kosmetik untuk
kuku adalah ester dari kitosan yang memiliki struktur berikut:
O H
O H O H2C
H O
H N H2
O H H
n
O
1 ⁄ ⁄
CH2-O-C(CH2)n-CH3
1
Gambar 1.1 Struktur Turunan Kitosan (Skajak-Break, et al., 1989).
Penelitian yang berhubungan dengan struktur tersebut telah dilakukan
terhadap kitosan laurat secara transesterifikasi (Sanni, 2008).
Asam palmitat adalah asam lemak jenuh yang tersusun dari 16 atom karbon
dengan rumus CH3(CH2)14COOH. Pada suhu kamar asam palmitat berwujud padat
berwarna putih dan memiliki titik lebur 640C. (Poedjiadi, A., Supriyati, T. 2007).
Minyak kelapa sawit kaya akan kandungan asam palmitat (14-47%) dan asam
oleat (37-40%), sedangkan minyak inti sawit relatif kaya dengan kandungan asam
laurat (40-55%) dan asam miristat (14-18%) yang mendekati komposisi asam lemak
yang dikandung minyak kelapa (Bhat, 1990).
Komposisi kandungan asam lemak yang berbeda antara berbagai minyak dan
lemak alami menyebabkan penggunaan asam lemak berbeda dalam industri kimia
oleo. Kimia oleo dihasilkan melalui pemecahan dan reaksi lanjutan dari minyak dan
lemak, asam lemak dan amina, misalnya turunan asam lemak dan metil esternya
(Ang , 1989).
Asam palmitat(C15H 31COOH), asam stearat (C17H35COOH), dan asam oleat
miristat (C13H27COOH), memiliki kedudukan sebagai bahan detergen pemantap,
maupun penggunaannya sebagai bahan kosmetika (Shoog and Leary, 1992).
Peneliti sebelumnya telah mensintesis ester kitosan dengan mereaksikan
klorokitosan dengan natrium oleat (Kemit, 1995), dan kitosan laurat melalui
transesterifikasi metil laurat dengan kitosan asetat (Sanni, 2008).
Dari hal di atas, peneliti tertarik untuk membuat kitosan palmitat yang dapat
digunakan sebagai bahan formulasi kosmetik (Skjak-Break, et al., 1989). Kitosan
palmitat dapat dibuat melalui tahap reaksi pembentukan metil palmitat dan
pembentukan kitosan asetat, dimana kitosan direaksikan lebih dahulu dengan
asetaldehida untuk melindungi gugus amina dalam kitosan. Setelah itu akan
dilakukan reaksi transesterifikasi antara kitosan asetat dan metil palmitat yang
menghasilkan kitosan palmitat. Kitosan palmitat yang diperoleh akan dianalisis
dengan spektroskopi infra merah.
1.2
Permasalahan
Apakah kitosan palmitat sebagai bahan surfaktan kosmetik dapat dibuat
melalui reaksi taransesterifikasi antara kitosan asetat dengan metil palmitat?
1.3
Pembatasan Masalah
Penelitian ini hanya dibatasi pada pembuatan kitosan palmitat melalui reaksi
transesterifikasi antara metil palmitat dengan kitosan asetat.
Untuk membuat bahan surfaktan kosmetik dari kitosan menjadi kitosan
palmitat melalui reaksi transesterifikasi antara metil palmitat dengan kitosan asetat,
dimana kitosan terlebih dahulu direaksikan dengan asetaldehida membentuk aldimin
dan kemudian diasetilasi dengan asetat anhidrida.
1.5
Manfaat Penelitian
Pengembangan kimia organik sintesa pada pembuatan senyawa kitosan
palmitat yang diharapkan dapat digunakan sebagai bahan surfaktan untuk formulasi
kosmetik.
1.6
Lokasi Penelitian
Penelitian dilakukan di laboratorium Kimia Organik FMIPA-USU Medan
dan analisa FT-IR dilakukan di laboratorium KIMIA Organik FMIPA-UGM
Yogyakarta.
1.7
Metodologi Penelitian
Kitosan palmitat diperoleh dari reaksi transesterifiksi antara metil palmitat
dan kitosan asetat. Pembuatan metil palmitat dilakukan dengan cara mereaksikan
asam palmitat dengan metanol dalam pelarut benzena dengan bantuan katalis asam
sulfat dalam kondisi refluks. Selanjutnya dilakukan pembuatan kitosan asetat dengan
cara mereaksikan aldimin kitosan dengan asetat anhidrida dalam pelarut
diklorometan. Sebelum diasetilasi, kitosan direaksikan terlebih dahulu dengan
BAB 2
TINJAUAN PUSTAKA
2.1 Kitosan
2.1.1 Struktur Kitosan
Kitosan adalah polisakarida alam yang diperoleh dari deasetilasi kitin. Jika
sebagian besar gugus asetil pada kitin disubstitusikan oleh atom hidrogen menjadi
gugus amino dengan penambahan larutan basa kuat berkonsentrasi tinggi, hasilnya
dinamakan kitosan atau kitin terdeasetilasi (Bastaman, 1989).
Kitosan mempunyai rumus umum (C6H9NO3)n atau disebut sebagai poli (β
-(1,4)-2-amino-2-Deoksi-D-Glukopiranosa). Kitosan bukan merupakan senyawa
tunggal, tetapi merupakan kelompok yang terdeasetilasi sebagian dengan derajat
polimerisasi yang berbeda. Kitin dan kitosan adalah nama untuk dua kelompok
senyawa yang dibatasi dengan stoikiometri, kitin adalah poli N-asetilglukosamin
yang terdeasetilasi sedikit. Derajat deasetilasi biasanya bervariasi diantara 8-15%,
tetapi tergantung pada sumber yang digunakan untuk memperoleh kitin, dan metode
yang digunakan untuk isolasi dan pemurnian. Sedangkan kitosan adalah kitin yang
terdeasetilasi sebanyak mungkin dengan derajat deasetilasi antara 80-90% (Uragami,
2006). Struktur kitosan yang terlihat pada gambar 2.1 tidak mengandung gugus asetat
bukan berarti merupakan kitin yang terdeasetilasi 100%.
5
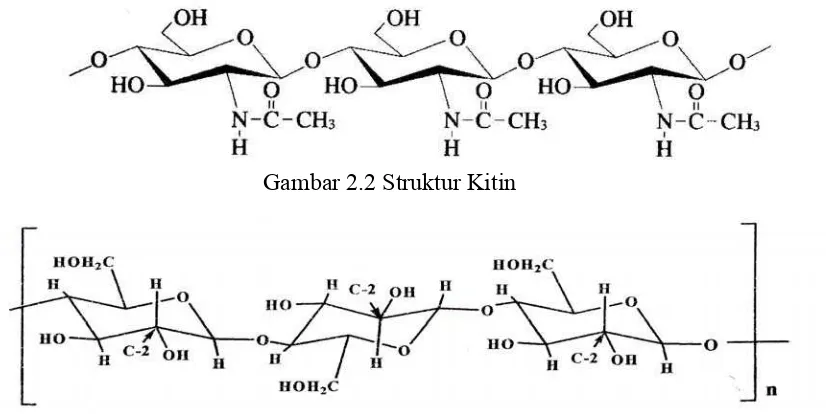
Struktur kimia dari kitin mirip dengan struktur kimia dari selulosa. Residu
monosakarida pada selulosa adalah β-D-glukosa sedangkan pada kitin adalah
N-asetil-β-D-glukosa dimana gugus hidroksil (-OH) pada posisi C-2 digantikan oleh
gugus asetamido (-NHCOCH3), dimana monosakaridanya dihubungkan melalui
ikatan β(1,4) (Kumar, 2000;Taranathan & Kittur, 2003).
Gambar 2.2 Struktur Kitin
Gambar 2.3 Struktur Selulosa
2.1.2 Sifat-sifat Fisika dan Kimia Kitosan
2.1.2.1 Sifat Fisika
Pada umumnya polisakarida alami seperti selulosa, dekstrin, pektin, alginat,
agar-agar, karagenan bersifat netral atau sedikit asam, sedangkan kitin dan kitosan
bersifat basa (Kumar, 2000).
Kitosan merupakan padatan amorf putih yang tidak larut dalam alkali dan
asam mineral kecuali pada keadaan tertentu. Kitosan merupakan molekul polimer
yang mempunyai berat molekul tinggi. Kitosan dengan berat molekul tinggi didapati
mempunyai viskositas yang baik dalam suasana asam (Onsoyen and Skaugrud,
Kitin merupakan bahan organik kedua yang melimpah sesudah selulosa.
Produksi kitin dan kitosan berkisar 700 metrik ton per tahun, dan pemasarannya
diperkirakan sekitar 5 triliun yen. Sekitar 85% kitosan yang diproduksi di Jepang
digunakan untuk pengolahan air limbah industri pangan (Alasalvar and Taylor,
2002).
Kitin sebagai prekursor kitosan pertama sekali ditemukan oleh Henri
Braconnot yang diisolasi dari jamur, dan 10 tahun kemudian ditemukan kitin dari
kulit serangga. Pada umumnya keberadaan kitin di alam tidak terdapat dalam
keadaan bebas, akan tetapi berikatan dengan protein, mineral, dan berbagai macam
pigmen.
Walaupun kitin tersebar secara luas di alam, sumber utama yang dapat
digunakan memproduksi kitin dalam skala besar dan dijadikan untuk pengembangan
lebih lanjut adalah kitin yang terdapat pada Crustaceae yang dipanen secara komersil
seperti kepiting, udang dan lobster. Kitin dari jenis Crustaceae ini banyak tersedia
dalam jumlah besar sebagai limbah industri pangan (Kaban, 2009).
Pada saat ini, hanya sedikit jumlah limbah cangkang yang dimanfaatkan
sebagai pakan ternak dan bahan sumber kitin, sehingga pengolahan cangkang
menimbulkan pencemaran lingkungan. Akhir-akhir ini, nilai komersial dari kitin
meningkat karena sifat-sifat yang menguntungkan dari turunannya yang sangat sulit
larut dalam air sehingga cocok digunakan dalam industri kimia, bioteknologi, bidang
pertanian, pengolahan pangan, kosmetik, peternakan, kedokteran, proteksi
lingkungan, industri pembuatan kertas dan tekstil (Kumar, 2000).
Di negara-negara maju seperti Jepang dan Amerika Serikat, produk kitin,
kitosan dan turunannya telah diproduksi secara komersil, maka pemanfaatan limbah
Kitin mempunyai sifat utama sangat sulit larut dalam air dan beberapa pelarut
organik sehingga kelarutan dan reaktifitas kimianya rendah. Kitin berwarna putih,
keras, tidak elastis, polisakarida yang mengandung nitrogen. Kitin dapat larut di
dalam HCl, H2SO4, H3PO4, dikloroasetat, trikloroasetat, dan asam formiat. Kitin juga
larut di dalam larutan pekat garam netral yang panas (Synowiecki and Al-Kateeb,
2003).
Molekul kitin cenderung bergabung dengan makro molekul lain karena
adanya gugus nitrogen dan menyebabkan jenis struktur dan sifat fisikokimia baru.
Misalnya ikatan kovalen antara kitin dan protein yang terbentuk antara N-asetil dari
kitin bereaksi dengan α-asam amino (terutama tirosin), dan protein kutikular akan
membentuk kompleks stabil namun mudah terdisosiasi setelah pH berubah. Kitin
dapat dianggap sebagai basa lemah, oleh karena itu dapat mengalami reaksi
netralisasi sebagai senyawa yang bersifat alkali (Taranathan and Kittur, 2003).
Kitin mempunyai sifat-sifat yaitu : (1) berasal dari alam (renewable), (2)
biodegradable dan tidak mencemari lingkungan, (3) biokompatibel tidak hanya pada
hewan juga dengan jaringan tanaman, (4) tidak bersifat toksis, (5) struktur
molekulnya dapat dan mudah dimodifikasi. Sifat-sifat inilah yang menjadi
pendorong untuk digunakan dalam industri yaitu modifikasi metode sehingga
biopolimer yang bernilai ini digunakan sebagai bahan yang multiguna (Taranathan
and Kittur, 2003). Pemanfaatan kitin dan turunannya di bidang industri adalah untuk
pangan yang berserat, kosmetik, alat pembalut dan untuk toilet.
Kitosan hasil deasetilasi kitin larut dalam asam encer seperti asam asetat dan
asam formiat. Kitosan dapat membentuk gel dalam N-metilmorpholin N-Oksida
yang dapat digunakan dalam formulasi pelepasan obat terkendali. Kandungan
nitrogen dalam kitin berkisar 5-8% tergantung pada tingkat deasetilasi sedangkan
nitrogen pada kitosan kebanyakan dalam bentuk gugus amino. Maka kitosan
bereaksi melalui gugus amino dalam pembentukan N-asilasi dan reaksi basa schiff,
Sifat fisik yang khas dari kitosan yaitu mudah dibentuk menjadi spons,
larutan, gel, pasta, membran dan serat yang sangat berperan dalam aplikasinya
(Kaban, 2009).
2.1.2.2 Sifat Kimia
Sifat kimia kitosan antara lain adalah polimer poliamin berbentuk linear,
mempunyai gugus amino dan hidroksil yang aktif dan mempunyai kemampuan
mengkelat beberapa jenis logam.
Adanya gugus amino dan hidroksil dari kitosan juga menyebabkan kitosan
mudah dimodifikasi secara kimia antara lain dalam reaksi pembentukan:
a. N-Asil
Metode yang paling sederhana adalah dengan mereaksikan asam karboksilat
dengan kitosan, pemanasan larutan kitosan dalam asam formiat 100% pada suhu
90-o
C dengan penambahan piridin sedikit demi sedikit untuk menghasilkan
N-formilkitosan, serta N-Asetil dalam asam asetat 20%.
b. O-Asilasi
Gugus amino kitosan lebih reaktif daripada gugus hidroksilnya. Karenanya
gugus amino perlu di proteksi selama proses asilasi untuk menghasilkan
O-Asilkitosan. Metode proteksi yang dilakukan antara lain melalui pembuatan basa
schiff disusul O-Asetilasi menggunakan larutan asetat anhidrida-piridin untuk
Pembuatan O-Asetil kitosan dapat juga dilakukan dengan melarutkan kitosan
terasetilasi dalam asam formiat 90% yang mengandung asetat anhidrida dan HClO4,
dengan asumsi protonasi gugus amino akan mencegah terjadinya N-Asetilasi.
c. Basa Schiff
Basa schiff turunan kitosan belum dibahas seluas N-Asil kitosan atau eter
kitosan karena rendahnya kestabilan basa schiff yang menyebabkan basa schiff
mudah mengalami hidrolisis asam dan telah digunakan sebagai proteksi terhadap
gugus amina.
Turunan basa schiff dapat diperoleh dari reaksi film kitosan dengan aldehid
alifatik, bukan saja yang linier-asetaldehid ke dekanal juga yang bercabang dan
aldehid aromatrik.
d. N- dan O-Asilasi
N- dan O-Asilasi kitosan juga dapat diperoleh bersamaan dengan
menggunakan asil klorida. Caranya dengan merefluks kitosan dalam campuran
dodekanoil klorida berlebih-piridin-kloroform dan ditambah asam klorida sesudah
direfluks 5 jam. Produk yang diperoleh sesudah 9 jam larut dalam kloroform, benzen,
dietil eter dan piridin.
e. Eter Kitosan
Pembuatan derivat Alkil kitosan dapat dilakukan dengan dua cara yaitu
O-alkilasi kitin disusul pengurangan N-Asetilasi dan O-O-alkilasi derivat kitosan, dimana
gugus amino diproteksi selama reaksi alkilasi.
Karboksimetil kitosan yang diperoleh melalui prosedur pertama
garam hidroklorida dari amino dengan gugus karboksimetil dalam bentuk asam.
Sensitifitas terhadap penambahan elektrolit meningkat dengan bertambahnya
karboksimetilasi. Perlakuan alkali kitin dengan epiklorohidrin pada 0-15oC disusul
deasetilasi menghasilkan O-hidroksialkil kitosan (Kaban, 2007).
f. N-Alkil
Metode yang paling mudah untuk N-alkilasi kitosan adalah reaksi antara
kitosan dan alkil halida yaitu metode yang menyelidiki reaksi kitosan dengan
metil-etil iodida dalam keberadaan beberapa amina tersier, piridin, dimmetil-etilpiridin, trimmetil-etil
piridin dan trietilamin.
g. Kitosan nitrat
Penyelidikan kitosan nitrat dilakukandengan dua cara yaitu, petama
melarutkan kitosan dalam HNO3 absolut, kemudian yang kedua kitosan ditambahkan
dalam campuran 1:1:1 dari asam asetat glasial; asetat anhidrid; asam nitrit absolut
selama 5,5 jam pada suhu <5oC.
h. Kitosan pospat
Tehnik penyiapan kitosan pospat yang dikembangkan ada dua cara yaitu,
pertama berdasarkan pada metode penyiapan selulosa pospat, dimana mula-mula
seluruh campuran asam posporat dan urea dipanaskan kemudian diubah dengan
menggunakan cairan inert sebagai perantara reaksi. Metode yang kedua adalah reaksi
poaporus pentoksida dengan kitosan yang dilarutkan dalam asam metanasulponat.
i. Kitosan sulpat
Kitosan sulpat diperoleh dengan menggunakan ClSO3H-piridin yang
gugus sulpat setiap satu D-glukosamin anhidra. Perlakuan lain adalah menggantikan
piridin dengan DMF, karena komleks SO3-DMF melebihi DMF maka reaksi dibuat
pada suhu kamar. Hasil yang diberikan mengandung satu gugus N-sulfat dan satu
gugus O-sulfat setiap D-glukosamin anhidra (March, 1984).
2.1.3 Kegunaan Kitosan
Kitosan merupakan turunan kitin yang paling bermanfaat. Ini disebabkan
karena berat molekul yang tinggi, sifat polielektrolit, keberadaan gugus fungsional,
kemampuan untuk membentuk gel, dan kemampuan mengadsorbsi. Selanjutnya
kitosan dapat dimodifikasi secara kimia dan enzimatik dan bersifat biodegradable
dan biokompatibel dengan sel dan jaringan manusia. Untuk pemanfaatannya, berat
molekul dan tingkat deasetilasi sangat berperan, karena kedua parameter ini
mempengaruhi kelarutan, sifat-sifat fisikokimia, dan sifat biokompatibilitas serta
aktivitas immunitas. Kapasitas mengadsorbsi kitin dan kitosan meningkat dengan
bertambahnya kandungan gugus amino yang bebas (Syanowiecki and Al-Kateeb,
2003).
Kitosan banyak digunakan dalam berbagai industri antara lain industri
farmasi, kesehatan, biokimia, bioteknologi, pangan, pengolahan limbah, kosmetik,
agroindustri, industri tekstil, industri perkayuan, dan industri kertas (Kaban, 2009).
Sifat-sifat dan pemanfaatan kitosan antara lain dapat dilihat pada tabel berikut :
Tabel 2.1 Sifat-sifat dan Pemanfaatan Kitosan
Sifat-sifat Pemanfaatan
Kationik : Polielektrolit linier bermuatan tinggi
Mengkelat ion logam beracun
Pemurnian air
Flokulan yang baik
Kimiawi : Berat Molekul tinggi Gugus amino dan hidroksil
Viskositas tinggi, film Modifikasi kimia
Bioaktivitas Antimikroba, antitumor
Farmasi : Biokompatible, biodegradable Penyembuh luka, pelepasan obat, kulit sintesis, kontak lensa
Sifat-sifat Pemanfaatan
Umum-kosmetik :
Pelembab, pakan, penyalut, pelindung
Produk perawatan kulit, perawatan/pemeliharaan rambut
Makanan dan Pertanian: Pengikat ion (asam empedu atau asam lemak)
Fungistatik Bakteriologis: Penjerat dan Adsorben
Penurun kolesterol, antikanker, serat pangan, anti luka
Meningkatkan produksi, bahan penjerat
Sumber : Taranathan and Kittur (2003).
2.2 Kosmetik
2.2.3 Bahan Kosmetik
Kosmetik berasal dari kata Yunani ”Kosmetikos” yang berarti keterampilan
menghias (Trenggono, 2007). Sedangkan menurut Badan Pengawas Obat dan
Makanan Republik Indonesia, kosmetik adalah setiap bahan atau sediaan yang
dimaksudkan untuk digunakan pada seluruh bagian luar tubuh manusia (epidermis,
rambut, kuku, bibir dan organ genital bagian luar) atau gigi dan membran mukosa
disekitar mulut terutama untuk membersihkan, mewangikan, mengubah penampilan
dan atau memperbaiki bau badan dan atau melindungi serta memelihara tubuh pada
kondisi baik.
Bahan kosmetik merupakan bahan-bahan yang termasuk di dalam kosmetik
tertentu, misalnya cat kuku secara garis besar memiliki bahan-bahan pembentuk
lapisan film yang tidak tembus air dan udara seperti selulosa asetat, selulosa aseto
butirat, etil selulosa, nitroselulosa, bahan plasticizer supaya cat kuku tidak mudah
supaya cat kuku lebih rekat dan lebih tebal seperti sulfonamida-formaldehid dan
bahan pelarut serta bahan pewarna (Trenggono, 2007).
Bahan kosmetik lain seperti kosmetik lotion dibuat dari bahan yang
menggunakan turunan karboksil kitosan, asam hialuronik, etanol, gliserin, metil
paraben, sodium adetat dan air. Kosmetik tersebut menunjukkan pengaruh
pelembaban kulit yang sangat baik (Tabloid Nova, 2008).
2.2.4
Pemanfaatan Kitosan dalam Bidang Kosmetik
Pada tahun 1976, Gross, Konrad dan Mager telah menemukan bahwa
beberapa garam-garam kitosan sangat efektif digunakan dalam bahan perawatan
rambut, kulit dan mulut. Garam-garam kitosan tidak larut dalam larutan netral dan
basa serta dalam bahan yang mengandung deterjen yang bermuatan negatif. Sifat ini
menjadikan adanya batasan penggunaan kitosan dalam bidang kosmetik, namun
beberapa penelitian tentang sintesis kitosan telah menghasilkan turunan kitosan yang
sesuai dengan deterjen yang bermuatan negatif sehingga dapat digunakan untuk
semua jenis kosmetik(Skjak-Braek, et al., 1989).
Kitosan dapat mempengaruhi kelembaban kulit serta memberi perlindungan
terhadap kerusakan mekanik serta efek anti elektrostatik pada rambut, tergantung
pada berat molekul dan derajat deasetilasinya. Kitosan dengan berat molekul tinggi
akan meningkatkan resistansi air terhadap emulsi, sehingga memberi perlindungan
terhadap irradiasi dan meningkatkan kemampuan membentuk film. Krim kosmetik
yang ditambahkan 1,0% kitosan akan meningkatkan bioaktivasi unsur-unsur lipofilik
seperti vitamin, sehingga dapat meresap lebih baik pada permukaan kulit. Kapasitas
pembentukan film dan sifat antiseptik kitosan melindungi dari kemungkinan infeksi
mikroba (Synowiecki and Al-Kateeb, 2003).
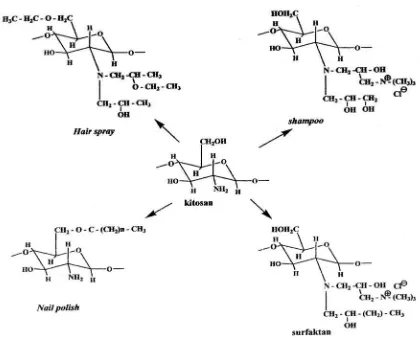
1. Reaksi antara kitosan dengan senyawa epoksida, yaitu reaksi kitosan dengan
etilena oksida, butilena oksida dan glisidol menghasilkan turunan kitosan
Turunan kitosan ini dapat dibuat membran dan digunakan dalam
produk-produk kosmetik seperti sampo, pelembab dan sabun.
2. Reaksi antara kitosan dan gabungan senyawa epoksida yang bermuatan
positif dan negatif, yaitu reaksi antara glisidiltrimetilamonium klorida dan
etilena oksida, propilena oksida dan glisidol dengan kitosan yang bermuatan
menghasilkan polimer yang dapat digunakan pada hampir seluruh produk
kosmetik. Hasil reaksi ini terbukti dapat digunakan dalam perawatan kulit dan
rambut.
3. Reaksi dengan senyawa epoksida dan alkilhalogenida, yaitu reaksi
N-Hidroksilpropil kitosan dengan senyawa alkilhalogenida (misalnya etil
bromida dan etil klorida). Hasil reaksi ini larut dalam dalam berbagai pelarut
organik. Apabila kitosan dimodifikasi dengan senyawa yang sesuai dapat
digunakan sebagai resin pada hair spray.
4. Asil kitin, yaitu telah dibuktikannya oleh peneliti terdahulu bahwa senyawa
asil kitin tidak dapat digunakan untuk hair spray tetapi asil kitin dan kitosan
ini dapat digunakan dalam pembentuk membran atau senyawa resin dalam
nail polish.
5. Sulfoalkil Kitosan, yaitu reaksi antara kitin atau kitosan yang bersifat basa
dengan 1,3 propana sulfonat akan menghasilkan ampholitik dimana gugus
sulfopropil akan mesubstitusi atom yang tidak bernuatan, yang dapat
Gambar 2.4 Penggunaan beberapa turunan kitosan dalam bidang kosmetik
2.3
Reaksi Interesterifikasi
Interesterifikasi adalah reaksi perubahan dari statu ester menjadi ester yang
lain, dimana terjadi pertukaran antara gugus asil ester yang satu dengan gugus
alkoksi dari ester yang lain, demikian juga sebaliknya gugus asil dari ester menerima
gugus alkoksi dari ester yang lainnya sehingga terbentuk dua senyawa ester yang
baru.
Reaksi interesterifikasi terbagi atas 3, yaitu : transesterifikasi, alkoholisis dan
asidolisis (Moran, 1994).
Transesterifikasi adalah istilah umum yang digunakan untuk menjabarkan
interchange alkoxy. Reaksi transesterifikasi adalah reaksi setimbang dan transformasi
yang terjadi oleh adanya pencampuran reaktan (Hendartomo, 2004).
Reaksinya sebagai berikut:
R─COOR1 + R2─COOR3 R─COOR3 + R2─COOR1
Ester 1 Ester 2 Ester baru 1 Ester baru 2
Alkoholisis adalah : reaksi suatu asam karboksilat dengan alkohol untuk
membentuk suatu ester, reaksi ini merupakan reaksi bolak balik yang pada suhu
kamar akan berlangsung sangat lambat namun dapat dipercepat
dengan bantuan suatu katalis yang biasa dipergunakan seperti HCl dan H2SO4
demikian juga penggunaan alkohol yang berlebih (Hendartomo,2004).
Reaksinya sebagai berikut:
R – C – OOR’ + R” – OH R – C –OOR” + R’OH
Asam karboksilat Alkohol Ester
Asidolisis adalah : reaksi pembentukan suatu ester antara asam lemak dengan
ester yang lain. Disini terjadi pertukaran gugus alkil pada ester dengan atom hidrogen
dari asam yang digunakan.
Reaksinya sebagai berikut :
R–COOR’ + R”–COOH R”–COOR’ + R−COOH
ester 1 asam ester 2 asam
2.4 Gugus Pelindung
Reaksi kimia yang memiliki gugus fungsi lebih dari satu memerlukan reaksi
selektif untuk menghindarkan terjadinya reaksi terhadap seluruh gugus fungsi yang
Dalam mendapatkan reaksi yang selektif terhadap gugus fungsi yang
menjadi sasaran perubahan reaksi, maka gugus fungsi lain yang memiliki potensi
untuk terserang diberi perlindungan. Perlindungan terhadap gugus fungsi yang
diharapkan tidak mengalami perubahan tersebut dilakukan dengan cara melindungi
gugus fungsi itu terlebih dahulu secara selektif agar tidak terserang oleh pereaksi
yang diberikan. Semua gugus fungsi memiliki cara tertentu melalui penggunaan
pereaksi untuk melindunginya, baik gugus karbonil, hidroksil, amino, ikatan rangkap
dan gugus lainnya (Greene, 1991).
Gugus amino mempunyai pereaksi tertentu untuk melindunginya misalnya
dengan AcOC6H4-p-NO2, pH 11. Perlindungan gugus amina dengan AcOC6H4-p
-NO2 akan membentuk –NHAc. Sebagai contoh :
CO2H O2N OAc CO2H
│ NH2 │ NHAc
H2N pH 11 H2N
Pereaksi lain yang digunakan untuk melindungi gugus amino adalah
asetaldehida, ionCu(II), dan asam perklorat. Pereaksi yang menggunakan
R2NCOCH2Cl dengan contoh reaksi sebagai berikut:
H2N R2N
R2NCOCH2Cl + LiOH, H2O NH
H2N 100oC, 1jam O NH2
Deproteksi terhadap gugus amino dapat dilakukan antara lain dengan menggunakan
asetat anhidrida, K2CO3, Hog kidney asilasi dan bromokatekolboran.
Molekul-molekul atau ion-ion yang teradsorbsi pada perbatasan (interfasa)
disebut dengan bahan aktif permukaan (surface active agents) atau surfaktan.
Surfaktan mempunyai peran penting untuk menurunkan tegangan permukaan bahan
yang dikenai. Penggunaan surfaktan terbagi atas tiga golongan, yaitu sebagai bahan
pembasah (wetting agents), bahan pengemulsi (emulsifying agents), dan sebagai
bahan penglarut (solubilizing agents). Aktifitas kerja suatu surfaktan karena sifat
ganda dari molekul tersebut (Pavia, 1976).
Secara umum gugus hidrofob memiliki lebih banyak variasi dibandingkan
gugus hidrofil. Selain gugus hidrokarbon berantai panjang, di bawah ini merupakan
variasi struktur gugus hidrofob lainnya, yaitu:
1. Gugus alkil rantai panjang lurus (n = C8-C22 dengan substitusi dari kulit kepala)
CH3(CH2)n-S.
2. Gugus alkil rantai panjang bercabang (n=C8-C22, substitusi internal)
CH3(CH2)nC(CH3)H(CH2)mCH2-S.
3. Rantai alkena tidak jenuh, contohnya turunan dari minyak nabati
CH3(CH2)nCH=CH(CH2)m-S.
4. Alkil benzena (C8-C15C6H4 dengan bentuk substitusi yang berbeda-beda)
C9H19(C6H4)-S.
5. Alkil naftalena (alkil R biasanya C3 atau lebih besar) Rn-C10H(7-n)-S.
6. Gugus Fluroalkil (n>4, sebagian atau seluruhnya terfluoronasi) CF3(CF2)2-S.
7. Polidimetilsiloksan, CH3-(Osi[CH3]2O)n-S.
8. Turunan polioksipropilena glikol CH3CH(OH)-CH2-O(-CH(CH3)CH2O)n-S.
9. Biosurfaktan.
10.Turunan polimer alami dan sintetik.
Dengan banyaknya variasi struktur senyawa yang dapat digunakan sebagai
surfaktan maka akan memberikan banyak aplikasi surfaktan yang dihasilkan
tergantung kepada kegunannya (Myers, 2006).
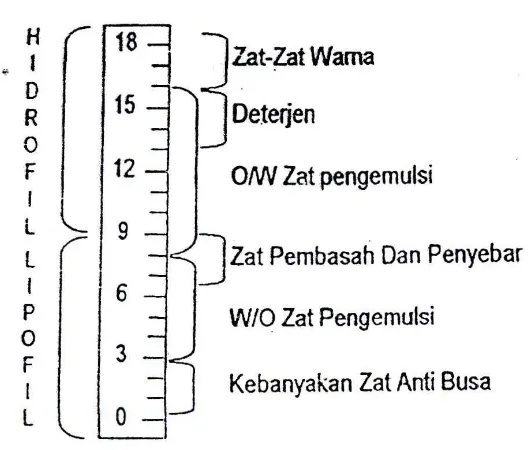
Griffin merancang suatu skala sembarang dari berbagai angka untuk dipakai sebagai
suatu ukuran keseimbangan hidrofilik-lipofilik (HLB) dari zat-zat aktif permukaan
(surfaktan). Dengan bantuan angka ini, adalah mungkin untuk membentuk suatu
jarak HLB untuk efisiensi optimum atau terbaik dari masing-masing golongan
surfaktan seperti terlihat pada gambar 2.5. HLB dari sejumlah senyawa dapat
dihitung dengan menggunakan rumus sebagai berikut:
HLB = 20 (1-S/A), dimana S adalah bilangan penyabunan senyawa dan A adalah
[image:35.595.130.396.279.504.2]bilangan asam senyawa.
Gambar 2.5 Skala Penunjuk Nilai HLB Surfaktan
Nilai HLB beberapa surfaktan dapat dilihat pada tabel 2.2 berikut :
Tabel 2.2 Nilai HLB Beberapa Surfaktan *)
Zat HLB
Asam oleat
Gliseril Monostearat
1
[image:35.595.104.347.686.751.2]Sorbitan mono-oleat
Sorbitan monolaurat
Trietanolamin oleat
Poliositilena sorbitan mono-oleat
Poliositilena sorbitan monolaurat
Natrium oleat
Natrium lauril sulfat
4,3
8,6
12
15
16,7
18
40
*) ( Martin, 1993).
Davies telah menghitung nilai HLB untuk zat aktif permukaan dengan
memecah berbagai molekul surfaktan ke dalam gugus-gugus penyusunnya, yang
masing-masing diberi suatu angka gugus. Penjumlahan dari angka-angka gugus
untuk suatu surfaktan tertentu memungkinkan perhitungan nilai HLB nya menurut
persamaan berikut :
HLB = ∑(angka-angka gugus hidrofilik) - ∑ (angka-angka gugus lipofilik) + 7
[image:36.595.105.349.80.245.2]Harga HLB beberapa gugus fungsi dapat dilihat pada tabel 2.3 berikut :
Tabel 2.3 Harga HLB Gugus Fungsi *)
Gugusan senyawa Angka gugus
Grup hidrofilik
-SO4-Na+
-COO-Na+
38,7
Ester (cincin sorbitan)
Ester (bebas)
Hidroksil (bebas)
Hidroksil (cincin sorbital)
Grup lipofilik
H
- C -
-CH2
-CH3
-=CH-
6,8
2,4
1,9
0,5
0,475
0,475
0,475
0,475
BAB 3
METODE PENELITIAN
3.1 Alat dan Bahan
Alat-alat yang digunakan dalam penelitian ini adalah Laba leher dua (Pyrex),
termometer 2100C ( Fisons), kondensor bola (Pyrex), rotarievaporator (Heidolph),
hotplate strirrer (Fisons), oven, Botol akuades, magnetik bar, corong pisah (Pyrex),
tabung CaCl2 (Pyrex), spektrofotometer IR (Shimadzu), alat vakum (Fisons),
kertas saring (Whatman), neraca analitis (Mettler PM 480), gelas ukur (Pyrex),
gelas Beaker (Pyrex), gelas Erlenmeyer (Pyrex), statif dan klem, dan buret (Pyrex).
Sedangkan bahan-bahan yang digunakan dalam penelitian ini adalah kitosan
powder, metanol (p.a. E. Merck), benzena (p.a. E. Merck), n-heksana (p.a. E.
Merck), asam sulfat 98% (p.a. E. Merck), akuades (p.a. E. Merck), asam asetat
anhidrida (p.a. E. Merck), asam palmitat padat (p.a. E. Merck), asam asetat glatsial
(p.a. E. Merck), kalsium klorida anhidrous (p.a. E. Merck), asam sitrat padat (p.a. E.
Merck), natrium metoksida padat (p.a. E. Merck), natrium bikarbonat padat (p.a. E.
Merck), asetaldehida (p.a. E. Merck), diklorometana (p.a. E. Merck), natrium sulfat
anhidrous (p.a. E. Merck), kalium hidroksida padat (p.a. E. Merck), alkohol 96%
(teknis), fenolftalein (p.a. E. Merck), asam oksalat padat (p.a. E. Merck), asam
klorida 37% (p.a. E. Merck), dan brom timol biru (p.a. E. Merck).
3.2 Prosedur Penelitian
3.2.1 Pembuatan reagen dan standarisasi
3.2.1.1 Pembuatan larutan indikator penolftalen
Sebanyak 1 gram fenolftalein dilarutkan dengan alkohol dalam labu takar 100
3.2.1.2 Pembuatan larutan H2C2O4 0.1 N
Sebanyak 1,575 gram H2C2O4.2H2O dilarutkan dalam labu takar 250 ml dan
kemudian diencerkan dengan akuades sampai garis batas.
3.2.1.3 Pembuatan larutan KOH-Alkohol 0,5 N
Sebanyak 7,0125 gram KOH dilarutkan dengan alkohol dalam labu takar 250
ml sampai garis batas dan distandarisasi dengan larutan H2C2O4 0,1 N dan
indikator fenolftalein.
25
3.2.1.4 Pembuatan larutan KOH 0,1 N
Sebanyak 1,4 gram KOH dilarutkan dengan akuades dalam labu takar 250 ml
sampai garis batas dan distandarisasi dengan larutan H2C2O4 0,1 N dan
indikator fenolftaalein.
3.2.1.5 Pembuatan larutan HCl 0,5 N
Sebanyak 11,92 ml HCl 37% diencerkan dengan akuades dalam labu takar
250 ml sampai garis batas dan distandarisasi dengan larutan KOH 0,1 N dan
indikator Brom Timol Blue.
3.2.1.6Pembuatan larutan KOH 0,02N
Sebanyak 50 ml larutan KOH 0,1 N diencerkan dalam labu takar 250 ml
dengan akuades dan distandarisasi dengan larutan H2C2O4 0,1 N dan
indikator fenolftalein.
3.2.1.7Pembuatan alkohol netral
Sebanyak 200 ml alkohol 96% ditambahkan 4 tetes indikator fenolftalein dan
ditetesi dengan larutan KOH 0,1 N hingga menjadi merah muda.
3.2.2 Pembuatan Metil Palmitat
Sebanyak 12,8 gram (0,05 mol) asam palmitat dimasukkan ke dalam labu
leher dua berisi magnet stirer yang dilengkapi dengan kondensor yang dialiri air dan
ujungnya dihubungkan dengan tabung yang berisi CaCl2 anhidrous dalam kapas.
Selanjutnya ditambahkan 50 ml metanol dan 100 ml benzena. Melalui corong
penetes sambil diaduk dalam keadaan dingin diteteskan sebanyak 2 ml H2 SO4 (p).
Campuran direfluks selama 5 jam. Hasil reaksi yang diperoleh diuapkan untuk
dimasukkan ke dalam corong pisah dan diekstraksi dengan 200 ml n-Heksana.
Lapisan atas dicuci dengan akuades sebanyak dua kali masing-masing sebanyak 25
ml, ditambahkan Na2SO4 anhidrous secukupnya dan didiamkan selama 30 menit,
kemudian disaring. Filtrat hasil saringan diuapkan dan residu yang diperoleh adalah
metil palmitat, kemudian dianalisis dengan spektroskopi infra merah.
3.2.3 Pembuatan senyawa aldimin kitosan
Sebanyak 1 gram (~0,000001 mol) kitosan dilarutkan dalam 100 ml asam
asetat 1% dimasukkan dalam labu leher dua yang dihubungkan dengan kendensor
yang dialiri air. Melalui corong penetes ditetaskan 3 ml asam asetat glasial sambil
diaduk dengan pengaduk magnet. Setelah 1 jam, ditambahkan 2 ml asetaldehida lalu
diaduk pada suhu kamar selama 6 jam. Hasil yang diperoleh dianalisis dengan
spektroskopi infra merah.
3.2.4 Pembuatan Kitosan Asetat
Sebanyak 2 gram (~0,000001 mol) aldimin kitosan dimasukkan kedalam
labu leher dua, ditambahkan pelarut diklorometana 100 ml. kemudian, dihubungkan
dengan kendensor yang ujungnya dihubungkan dengan tabung yang berisi CaCl2
anhidrous dalam kapas. Melalui corong penetes, kemudian ditetesi asetat anhidrida
sebanyak 2 ml sambil diaduk dengan pengaduk magnet, setelah itu direfluks pada
suhu 60o selama 6 jam. Hasil yang diperoleh, dimasukkan dalam corong pisah.
Lapisan bawah ditampung dari dicuci dengan akuades sebanyak dua kali, lalu
disaring. Residu yang diperoleh dikeringkan, kemudian dianalisis dengan
3.2.5 Pembuatan Kitosan Palmitat
Sebanyak 2 gram (~0,000001 mol) kitosan asetat dan 2,16 gram (0,01 mol)
metil palmitat dimasukkan kedalam labu leher dua, ditambahkan 0,5 gram natrium
metoksida sebagai katalis. Campuran direfluks selama 6 jam pada suhu 130-1400C.
Hasil yang diperoleh, dimasukkan ke dalam corong pisah. Lapisan bawah ditampung
dan dicuci dengan larutan asam sitrat 20%, kemudian disaring dan kelebihan asam
sitrat dicuci dengan akuades sebanyak dua kali lalu disaring. Residu yang diperoleh
ditambahkan natrium bikarbonat yang diikuti pencucian dengan akuades lalu
dikeringkan. Kitosan palmitat yang diperoleh dianalisis dengan spektroskopi infra
merah.
3.2.6 Uji HLB dengan Metode Titrasi
3.2.6.1Analisis Bilangan Penyabunan
Ditimbang ± 0,1 gram kitosan palmitat dan dimasukkan ke dalam gelas
Erlenmeyer. Kemudian ditambahkan 25 ml larutan KOH-Alkohol 0,5 N dan
dipanaskan hingga mendidih. Didinginkan dan ditambah 3 tetes indikator fenolftalein
kemudian dititrasi dengan larutan HCl 0,5 N hingga warna merah muda hilang.
Volume HCl yang terpakai dicatat dan dihitung bilangan penyabunan dengan rumus :
Bilangan Penyabunan =
(
)
sampel Massa
56,1 x NHCl x V Vblanko− titrasi
3.2.6.2Analisis Bilangan Asam
Ditimbang ± 0,1 gram kitosan palmitat dimasukkan ke dalam gelas
Erlenmeyer. Kemudian ditambah 10 ml larutan alkohol netral. Erlenmeyer tersebut
ditutup dengan plastik dan dipanaskan selama 30 menit. Larutan teersebut
larutan KOH 0,02 N sampai terbentuk larutan warna merah muda. Volume KOH
yang dipakai dicatat dan dihitung bilangan asam dengan menggunakan rumus :
Bilangan Asam =
Sampel Massa
56,1 x N x
VKOH KOH
3.3 Bagan Penelitian
3.3.1 Pembuatan Metil Palmitat
12,8 gram asam palmitat (dalam labu leher dua)
Campuran
Å Ditambah 50 ml metanol
Residu Pelarut
Lapisan bawah Lapisan atas
Filtrat
Residu Å Ditambah 100 ml benzena
Å Diaduk dan diteteskan 2 ml H2SO4 (p)
Å Direfluks pada suhu 800C selama 5 jam Å Dirotarievaporasi
Å Diekstraksi dengan 200 ml n-Heksana Å Dicuci dengan akuades
Å Ditambah Na2SO4 anhidrous dan didiamkan selama 30 menit
Å Disaring
Metil Palmitat
Pelarut
Analisis FT-IR
3.3.2 Pembuatan aldimin kitosan
1 gram kitosan (dalam labu leher dua)
Å Ditambah 100 ml CH3 COOH 1 %
Campuran
Å Diteteskan 2 ml asetal dehida Å Distirrer pada suhu kamar selama 6
jam
Aldimin kitosan
3.3.3 Pembuatan Kitosan Asetat
2 gram Aldimin kitosan (dalam labu leher dua)
Campuran
Å Ditambah 100 ml diklorometana Å Diaduk dan ditetesi 2,16 g asetat anhidrida
Lapisan bawah Lapisan atas
Filtrat Residu
Kitosan asetat
Analisis FT-IR
Å Direfluks pada suhu 600C selama 6 Jam
Å Dimasukkan dalam corong pisah
Å Dicuci dengan akuades Å Disaring
3.3.4 Pembuatan Kitosan Palmitat
2 gram kitosan asetat (dalam labu leher dua)
Campuran
Lapisan bawah Lapisan atas
Filtrat Residu
Filtrat Residu
Filtrat Residu
Kitosan palmitat
Å Dicuci dengan larutan asam sitrat 20% Å Disaring
Å Ditambahkan natrium bikarbonat dan akuades Å Disaring
Å Dikeringkan
Å Dicuci dengan akuades
ÅDirefluks pada suhu 130-1400C selama 6 jam
Å Dimasukkan kedalam corong pisah.
Å ditambah 0.5 gram natrium metoksida Å Diaduk dan diteteskan 19 gram metil
3.3.5 Bagan Analisis
3.3.5.1 Analisis Bilangan Penyabunan
Sampel (±0,1 gram)
Sampel (±0,1 gram) 3.3.5.2 Analisis Bilangan Asam
Å Dimasukkan ke dalam gelas Erlenmeyer Å Ditambah 25 ml KOH – Alkohol 0,5 N Å Dipanaskan sampai mendidih
Å Didinginkan
Å Ditambah 3 tetes indikator fenolftalein
Larutan merah muda
Å Dititrasi dengan HCl 0,5 N
Larutan Bening
Hasil
Å Dicatat volume HCl 0,5 N
Å Dimasukkan ke dalam gelas Erlenmeyer Å Ditambah 10 ml Alkohol netral
Å Dipanaskan salama 30 menit Å Didinginkan
Å Dititrasi dengan KOH 0,02 N
Larutan Merah muda
Hasil
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil
4.1.1 Kitosan
Kitosan yang digunakan dalam penelitian ini adalah kitosan Fluka yang
diperoleh dari kulit udang dengan derajat deasetilasi 87,4%. Spektrum FT-IR kitosan
yang digunakan memberikan puncak-puncak serapan pada daerah bilangan
gelombang (cm-1) 3425,58; 2870,08; 2337,72; 2137,13; 1597,06; 1419,61; 1381,03;
1327,03; 1080,14; 894,97 (gambar 4.1).
O H
O H O H2C
H O
H N H2
O H H
[image:48.595.151.473.390.646.2]n
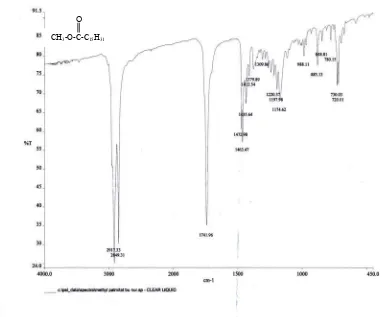
4.1.2 Metil Palmitat
Metil palmitat diperoleh dari hasil reaksi esterifikasi antara asam palmitat
dengan metanol. Asam palmitat yang digunakan memiliki derajar kemurnian 95%.
Metil palmitat yang diperoleh dari reaksi esterifikasi 12,8 g (0,05 mol) asam palmitat
dengan 50 ml metanol diperoleh metil palmitat 10,24 g, spektrum FT-IR metil
palmitat memberikan puncak-puncak serapan pada daerah bilangan gelombang (cm
-1
) 2917,33; 2849,31; 1741,96; 1435,64; 1174,62; 730,03 (gambar 4.2).
35
[image:49.595.117.505.261.578.2]CH3-O-C-C15H31 O
Gambar 4.2 Spektrum FT-IR Metil Palmitat
4.1.3 Kitosan Asetat
Kitosan asetat merupakan hasil reaksi antara kitosan dengan asetat anhidrida.
Dimana gugus NH2 pada kitosan terlebih dahulu diproteksi dengan cara mereaksikan
kitosan dengan asetaldehida membentuk aldimin. Kemudian aldimin kitosan ini
jam pada suhu 60oC. Hasil refluks kemudian dipisahkan antara residu dan pelarut.
Residu dicuci dua kali dengan akuades. Residu yang diperoleh merupakan kitosan
asetat dikeringkan dan diperoleh 1,55 g yang kemudian dianalisis secara
spektroskopi FT-IR. Dari data spektroskopi FT-IR, spektrum aldimin kitosan
memberikan puncak-puncak serapan pada daerah bilangan gelombang (cm-1)
3446,72; 2075,41; 1635,64; 1087,85 (gambar 4.3).
O H
O H O H2C
H O
H N
O H H
n
[image:50.595.109.497.197.475.2]C H C H3
Gambar 4.3 Spektrum FT-IR Aldimin Kitosan
Sedangkan spektrum dari FT-IR kitosan asetat memberikan puncak-puncak
serapan pada daerah bilangan gelombang (cm-1) 3441,01; 2885,51; 1635,64;
O H
O H2C
HO
H N
O
H H
n
CH
CH3 O C
O
[image:51.595.133.490.87.372.2]CH3
Gambar 4.4 Spektrum FT-IR Kitosan Asetat
4.1.4 Kitosan Palmitat
Senyawa kitosan palmitat merupakan senyawa ester yang dibuat dengan
mereaksikan kitosan asetat dan metil palmitat dengan bantuan katalis natrium
metoksida, direfluks selama 6 jam pada suhu 130-140oC. Residu yang diperoleh
dicuci dengan natrium sitrat 20% dan diikuti penambahan natrium bikarbonat dan
akuades lalu disaring dan dikeringkan. Residu yang diperoleh berupa kitosan
palmitat sebesar 1,45 g yang selanjutnya dianalisis secara spektroskopi FT-IR. Hasil
analisis secara spektroskopi FT-IR memberikan puncak-puncak serapan pada daerah
bilangan gelombang (cm-1) 3387,0; 2916,37; 2850,79; 1720,50; 1627,92; 1562,34;
O H
O H2C
HO
H NH2
O H H
n
O C O
C15H31
4.1.5 Nilai HLB
Nilai HLB Kitosan Palmitat diperoleh dari analisis bilangan penyabunan
dan analisis bilangan asam dengan cara titrasi. Hasil yang diperoleh dari analisis
bilangan penyabunan dan hasil analisis bilangan asam digunakan dalam penentuan
bilangan penyabunan dan penentuan bilangan asam yang dapat dilihat pada tabel
[image:52.595.116.503.82.383.2]4.1 dan 4.2 berikut :
Tabel 4.1 Penentuan Bilangan Penyabunan
Massa sampel (gram) Volume titrasi (ml) Sampel
M1 M2 M3 M V1 V2 V3 V
Blanko _ _ _ _ 32,27 32,26 32,27 32,27
[image:52.595.105.509.644.728.2]Tabel 4.1 Penentuan Bilangan Penyabunan
Massa sampel (gram) Volume titrasi (ml) Sampel
M1 M2 M3 M V1 V2 V3 V
Blanko _ _ _ _ 32,27 32,26 32,27 32,27
Kirosan Palmitat 0,101 0,102 0,101 0,101 32,18 32,19 32,19 32,19
Tabel 4.2 Penentuan Bilangan Asam
Massa sampel (gram) Volume titrasi (ml) Sampel
M1 M2 M3 M V1 V2 V3 V
Kirosan Palmitat 0,101 0,101 0,102 0,101 5,24 5,25 5,25 32,19
4.2 Pembahasan
4.2.1 Pembuatan Metil Palmitat
Reaksi asam palmitat dengan metanol menghasilkan metil palmitat
merupakan reaksi esterifikasi. Reaksinya adalah :
+ CH3OH + H2O
Asam Palmitat Metanol Metil Palmitat C15H31C-OH
O
C15H31C-OCH3 O H2SO4
Reaksi esterifikasi asam palmitat dan metanol terjadi dengan adanya katalis asam
sulfat. Adisi nukleofil oleh metanol terhadap asam palmitat akan membentuk ikatan
ester. Kesetimbangan berlangsung dalam suasana asam dimana protonasi terjadi
terhadap salah satu gugus hidroksil yng mengakibatkan lepasnya air. Pada akhir
reaksi ester yang berproton melepaskan protonnya (Hart, 1990). Mekanisme
[image:53.595.138.500.545.599.2]
O O−H -HSO4 OH
║ ║ ║
+
C15H31C─OH + H-HSO4 C15H31C─OH + CH3−OH C15H31C─OH
metanol │
asam palmitat CH3O−H
O−H -HSO4 O
║ +
C15H31C─O−H C15H31C=O−H + H2O C15H31C─OCH3 + H2SO4
│ H │ metil palmitat
[image:54.595.105.502.121.306.2]CH3O CH3O
Gambar 4.6 Mekanisme Reaksi Pembuatan Metil Palmitat
Spektrum hasil analisis spektroskopi FT-IR, spektrum metil palmitat (gambar
4.2) memberikan puncak-puncak serapan pada daerah bilangan gelombang
2917,3cm-1; 2849,31 cm-1 yang menunjukkan gugus C-H sp3, dan serapan pada daerah bilangan gelombang 1741,96 cm-1 menunjukkan gugus karbonil C=O dari ester yang didukung oleh puncak serapan pada daerah bilangan gelombang 1111,0
cm-1 menunjukkan gugus C-O-C serta serapan pada daerah bilangan gelombang
1220,37 cm-1; 1197,98 cm-1; 1174,6 cm-1 yang menunjukkan gugus C-O, juga
dengan adanya serapan pada daerah bilangan gelombang 730,03 cm-1 menunjukkan
gugus alkil rantai panjang atau (CH2)n. Asam palmitat yang digunakan untuk
pembuatan metil palmitat memiliki gugus hidroksil sebagai karboksilat (-COOH)
yang pada pemeriksaan secara analisis spektroskopi gugus –OH akan memberikan
vibrasi pada daerah bilangan gelombang 3500-3300 cm-1 dan tidak dijumpainya
vibrasi pada daerah tersebut menunjukkan bahwa asam palmitat telah sempurna
membentuk metil palmitat.
Reaksi antara kitosan dan asetat anhidrida menghasilkan senyawa ester yang
merupakan kitosan asetat. Dalam hal ini kitosan terlebih dahulu direaksikan dengan
asetaldehida membentuk aldimin. Reaksinya adalah :
+ CH3COOH
Aldimin kitosan yang dihasilkan direaksikan dengan asetat anhidrida dengan
pelarut diklorometana pada kondisi refluks. Senyawa asetat anhidrida termasuk ke
dalam elektron sink yang baik dan bersifat reaktif apabila adanya serangan suatu
nukleofil yang menyebabkan pecahnya ikatan pada C-O-C anhidrida. Dari reaksi
aldimin kitosan dan asetat anhidrida, pasangan elektron bebas dari oksigen pada
gugus alkohol posisi C-6 yang bersifat nukleofil dari aldimin kitosan akan bereaksi
dengan gugus asil pada senyawa asetat anhidrida dalam pelarut diklorometana akan
menghasilkan senyawa kitosan O-asetat. Mekanisme reaksinya adalah :
O O─H
║ ║
CH3─C─H CH3COO─H CH3─C─H +
CH3COO- CH3COO−H
CH3-C-O-C-CH3
O O
H O H2C
O H
O H2C
HO H N O H H n CH CH3 O C O CH3 kitosan Kitosan asetat aldimin kitosan O H O H O
H N H2
O H
H H O H2C
n O H O H O H N O H H n C H C H3 CH3CHO
+
O H
O H O H2C
H O
H N H2
O H H
n
N─H
H
O H
O H O H2C
H O H
O H
O H O H2C
H O H N H2
O H
H H
n
NH─H
CH─OH
CH3
+
O N H2 H
n
NH
CH─OH
CH3COO -O
H O H O H2C
H O H
CH3CO−
+ H2O + CH3COOH
O O
║ ║ + CH3−C−O−C−CH3
+ CH3COOH
[image:56.595.101.487.88.583.2]CH3COO-
Gambar 4.7 Mekanisme Reaksi Pembuatan Kitosan Asetat
Terbentuknya aldimin kitosan dan kitosan asetat diidentifikasi dengan
spetroskopi FT-IR. Dari hasil analisis spektroskopi FT-IR, spektrum aldimin kitosan
(gambar 4.3) memberikan puncak-ouncak serapan pada daerah bilangan gelombang
3448,72 cm-1 menunjukkan gugus O-H, serapan pada daerah bilangan gelombang
1404,16 cm-1 menunjukkan gugus C-H, dan serapan pada daerah bilangan
gelombang 1087,85 cm-1 menunjukkan gugus C-O-C, selanjutnya serapan pada
N H2
O H
O H
O H O H2C
H O H H
n
NH
CH─OH2
CH3
+ N H2
O H
H
N─H
CH CH3 n O H O H O H2C
H O H
H
N H2
O H N ║ CH │
CH3 n
O H
O H O H2C
H O
H N H2
O H H n N ║ CH │ CH3 O H O H O H2C
H O
H N H2
O H H
H O- O │ │ ║ CH2O─C─O─C─CH3
+ │ CH3 n N ║ CH │ CH3 O H O H O H2C
H O
H N H2
O H H n N ║ CH │ CH3 H O │ ║ CH2O─C
+ │
CH3 H O
O H O H2C
H O H
H
N H2
O H
O CH2─O─C─CH3
daerah bilangan gelombang 1635,64 cm-1 yang menunjukkan adanya gugus C=N
yang menggambarkan bahwa telah terbentuk aldimin kitosan (Silverstein, 1981).
Sedangkan apektrum FT-IR (gambar 4.4) memberikan puncak serapan pada daerah
bilangan gelombang 3271 cm-1 yang menunjukkan gugus O-H, serapan pada daerah
bilangan gelombang 2885,51 yang menunjukkan gugus C-H sp3 dan serapan pada
daerah bilangan gelombang 1157,28 cm-1 yang masih menunjukkan gugus C-O-C,
serta daerah bilangan gelombang 1635,64 dan 1558 cm-1 menunjukkan adanya
gugus C=N dan C=O dari ester asetat.
Adanya puncak serapan pada daerah bilangan gelombang yang menunjukkan
gugus-gugus fungsi tersebut dapat mengidentifikasikan terbentuknya kitosan asetat.
4.2.3 Reaksi Kitosan Asetat dengan Metil Palmitat
Reaksi antara kitosan asetat dan metil palmitat menghasilkan kitosan
palmitat. Reaksinya adalah :
O
O
CH3ONa
+ C15H31COOCH3
Kitosan asetat Kitosan palmitat metil palmitat O H O H2C
HO H N O H H n CH CH3 O C CH3
O H
O H2C
HO
H NH2
O H H n O C O
C15H31
refluks
O H
O H2C
HO
H NH2
O H H
n
O C C15H31
Senyawa kitosan palmitat yang diperoleh merupakan hasil dari reaksi
transesterifikasi antara kitosan asetat dan metil palmitat dengan bantuan katalis
natrium metoksida dalam kondisi refluks.
Reaksi transesterifikasi yang terjadi didukung oleh teori HSAB yang
memperlihatkan C15H31C+O dari metil palmitat merupakan elektrofilik yang hard
acid, akan tetapi lebih lunak daripada CH3C+O kitosan asetat. Begitu pula dengan
CH3O- dari metil palmitat merupakan nukleofilik yang hard base akan tetapi lebih
keras bila dibandingkan dengan RCH2O- dari kitosan asetat. Sehingga gugus asil
C15H31C+O dari metil palmitat akan bereaksi dengan RCH2O- dari kitosan asetat
membentuk kitosan palmitat dan CH3C+O dari kitosan asetat akan bereaksi dengan
CH3O- dari metil palmitat membentuk metil asetat (Brahmana, 1994). Mekasnisme
reaksinya adalah : CH2
-OCH3 H
- OCH3 O O O ║ + C15H31─C─OCH3
-OCH3
H O
H2C
HO H N O H H n CH CH3 O C O
CHCH32 \ H
O H
O H2C
HO H N O H H n CH CH3 O C O CH3 - + O H O H2C
HO H N O H H n CH CH3 O C O CH3 - CH2 O H O H2C
HO H N O H H n CH CH3 O C O CH3 O- │ CH2─C─C15H31 │
OCH3
O H
O H2C
HO H N O H H n CH CH3 O C O CH3
O O ║ ║
C─CH2─C-C15H31 + H O H O H2C
HO H N O H H n CH CH3 O C O CH3 O - O │ ║ CH2─O─C─CH2─C-C15H31 │
OCH3
O H
O H2C
HO H N O H H n CH CH3 O C O CH3
O O ║ ║ C─CH2─C-C15H31 │
OCH3
CH2 ─ O-
O H
O H2C
HO H N O H H n CH CH3 O C O CH3 O - │ CH2 ─O─ C─C15H31 │ CH2─C=O
OCH3
H2C O C O
CH3 O ║
CH2 ─O─ C─C15H31 H2C H O C O CH3 O ║ CH2 ─O─ C─C15H31 O
H O
H2C
+H –OCH 3
O
║
+ CH3─C─CH3 + -OCH3
O +H-OH
║
O H
O H2C
+ Na─O─C─O─H
[image:59.595.101.506.76.497.2]
(Smith, 1994).
Gambar 4.8 Mekanisme Reaksi Pembuatan Kitosan Palmitat
Dari hasil analisis spektroskopi FT-IR, spektrum kitosan palmitat (gambar
4.5), memberikan puncak-puncak serapan pada daerah bilangan gelombang 3380,0
cm-1; 3371,57 cm-1 menunjukkan gugus O-H dan gugus N-H yang saling tumpang
tindih dari kitosan dan munculnya serapan pada daerah bilangan gelombang 1720,50
cm-1 menunjukkan adanya gugus karbonil C=O yang didukung oleh serapan pada
daerah bilangan gelombang 1068,56 cm-1 yang menunjukkan gugus C-O-C, serta
adanya serapan pada daerah bilangan gelombang 1562,34 cm-1 menunjukkan tetap
adanya gugus C-N dan tidak ditemukannya lagi serapan pada daerah bilangan
gelombang 1635,64 cm-1 yang menunjukkan gugus C=N hal ini disebabkan oleh O
H O
H2C
HO H N O H H n CH CH3 O C O CH3 O ║ CH2 ─O─ C─C15H31 HO H N O H H O C O CH3 O ║ CH2 ─O─ C─C15H31 n CH CH3 │ CH─CH3 │ O─C─OH ║ O O H O H2C
HO H N O H H n CH CH3 O C O CH3 CH2 ─O
O ║ ─ C─C15H31
O H
O H2C
HO H N O H H n CH CH3 O C O CH3 O ║ O H O H2C CH2 ─O─ C─C15H31
NH │ CH─CH3 ║ O NH │ CH─CH3
│ OH O─C─OH │ O - O ║ H─O─C─O─H HO H N O H H O C O CH3 O ║ CH2 ─O─ C─C15H31 n CH CH3 Kitosan palmitat
O O ║ ║ + CH3 ─C─H + Na─O─C─O─H
dibukanya selubung yang telah memberikan proteksi terhadap gugus amina (-NH2),
serta adanya gugus alkil rantai panjang (CH2)n dari rantai karbon palmitat yang
ditunjukkan oleh serapan pada daerah bilangan gelombang 717,52 cm-1 sehingga
dapat diidentifikasikan telah terbentuknya kitosan palmitat.
4.2.4 Pengujian Nilai HLB
Dari data penentuan bilangan penyabunan Kitosan Palmitat dapat dihitung nilai
bilangan pernyabunan Kitosan Palmitat dengan menggunakan persamaan:
Bilangan Penyabunan =
) ( 1 , 56 . ) ( gram sampel Massa N V
Vblanko − titrasi HCl
= 101 , 0 1 , 56 . 501 , 0 ) 19 , 32 27 , 32 (
= 22,26
Dari data penentuan bilangan asam Kitosan Palmitat dapat dihitung nilai
bilangan asam Kitosan Palmitat dengan menggunakan persamaan:
) ( 1 , 56 . gram l MassaSampe N V Asam
Bilangan = KOH KOH
73
,
57