i
SIMULASI NUMERIK UNTUK MEMPREDIKSI KINERJA
REAKTOR GASIFIKASI SABUT KELAPA TIPE
DOWNDRAFT
DZIYAD DZULFANSYAH
DEPARTEMEN TEKNIK MESIN DAN BIOSISTEM FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
iii
PERNYATAAN MENGENAI SKRIPSI DAN
SUMBER INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi berjudul Simulasi Numerik untuk Memprediksi Kinerja Reaktor Gasifikasi Sabut Kelapa Tipe Downdraft
adalah benar karya saya dengan arahan dari dosen pembimbing dan belum diajukan dalam bentuk apa pun kepada perguruan tinggi mana pun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis saya kepada Institut Pertanian Bogor.
Bogor, Juli 2013
Dziyad Dzulfansyah
ABSTRAK
DZIYAD DZULFANSYAH. Simulasi Numerik untuk Memprediksi Kinerja Reaktor Gasifikasi Sabut Kelapa Tipe Downdraft. Dibimbing oleh LEOPOLD OSCAR NELWAN.
Sabut kelapa merupakan limbah pertanian (perkebunan kelapa) yang belum banyak digunakan dalam bidang energi terbarukan. Sabut kelapa berpotensi untuk digunakan sebagai bahan gasifikasi untuk menghasilkan gas mampu bakar (CO, H2, dan CH4). Pemodelan matematika dan simulasi numerik pada model kesetimbangan termodinamika dikembangkan untuk memprediksi komposisi gas yang dihasilkan pada beragam kadar air dan equivalence ratio (ER). Hasil model kemudian dibandingkan dengan hasil percobaan yang dilakukan. Hasil perbandingan cukup dekat dan memuaskan dengan nilai eror RMS 2.44% dan nilai R2 0.885. Hasil simulasi menunjukkan bahwa pada peningkatan kadar air setiap 5% rata – rata akan terjadi peningkatan persentase gas H2 0.67%, CO2 0.79%, dan CH4 0.04%, dan penurunan suhu 68.62 K, persentase gas CO 2.00%, dan N2 0.33%. Hasil simulasi juga menunjukkan bahwa pada peningkatan ER setiap 0.05 rata – rata akan terjadi penurunan persentase gas H2 2.03%, CO 2.31%, dan CH4 0.68%, dan peningkatan suhu 165.74 K, persentase gas CO2 0.52%, dan N2 4.56%.
Kata kunci: Sabut kelapa, gasifikasi, gas mampu bakar, model kesetimbangan termodinamika
ABSTRACT
DZIYAD DZULFANSYAH. Numerical Simulation for Predicting Performance of Downdraft - Coconut Husk/Coir Gasifier. Supervised by LEOPOLD OSCAR NELWAN.
Coconut husk/coir is a waste of agriculture field (coconut plantation) which rarely utilized in renewable energy. Coconut husk/coir is potential for used as gasification material/feedstock for generating combustible gas (CO, H2, and CH4). Mathematical modeling and numerical simulation on thermodynamic equilibrium model is developed for predicting gas composition generated in various moisture content and equivalence ratio (ER). Results of model are compared with experimental results. Results of comparison is quite close and satisfactory with RMS error 2.44% and R2 0.885. Results of simulation show that on increasing of moisture content each 5% will take effect average increasing of percentage of H2 0.67%, CO2 0.79%, and CH4 0.04%, and average decreasing of temperature 68.62 K, percentage of CO 2.00%, and N2 0.33%. Results of simulation also show that on increasing of ER will take effect average decreasing of H2 2.03%, CO 2.31%, and CH4 0.68%, and average increasing of temperature 165.74 K, percentage of CO2 0.52%, dan N2 4.56%.
iii
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Teknologi Pertanian
pada
Departemen Teknik Mesin dan Biosistem
SIMULASI NUMERIK UNTUK MEMPREDIKSI KINERJA
REAKTOR GASIFIKASI SABUT KELAPA TIPE
DOWNDRAFT
DZIYAD DZULFANSYAH
DEPARTEMEN TEKNIK MESIN DAN BIOSISTEM FAKULTAS TEKNOLOGI PERTANIAN
INSTITUT PERTANIAN BOGOR BOGOR
v
Judul Skripsi : Simulasi Numerik untuk Memprediksi Kinerja Reaktor Gasifikasi Sabut Kelapa Tipe Downdraft
Nama : Dziyad Dzulfansyah NIM : F14090012
Disetujui oleh
Dr. Leopold Oscar Nelwan, STP, MSi Pembimbing
Diketahui oleh
Dr. Ir. Desrial, MEng Ketua Departemen
PRAKATA
Puji dan syukur penulis panjatkan kepada Allah subhanahu wa ta’ala atas segala karunia-Nya sehingga karya ilmiah ini berhasil diselesaikan. Tema yang dipilih dalam penelitian yang dilaksanakan sejak bulan Maret 2013 ini ialah gasifikasi, dengan judul Simulasi Numerik untuk Memprediksi Kinerja Reaktor Gasifikasi Sabut Kelapa Tipe Downdraft.
Terima kasih penulis ucapkan kepada Bapak Dr. Leopold Oscar Nelwan, STP, MSi selaku dosen pembimbing, Bapak Dr. Ir. Desrial, MEng dan Ibu Ir. Sri Endah Agustina, MS selaku dosen penguji, dan Program Hi-Link selaku pemberi dana untuk penelitian ini. Di samping itu, penghargaan penulis sampaikan kepada ayah, ibu, serta seluruh keluarga, atas segala doa dan kasih sayang yang telah diberikan. Ucapan terima kasih juga disampaikan kepada teknisi Laboratorium Energi dan Elektrifikasi Pertanian (Pak Harto) dan teknisi Laboratorium Lapang Siswadhi Supardjo (Pak Darma dan Mas Firman) yang telah banyak membantu penulis dalam melakukan penelitian, juga teman – teman Teknik Pertanian angkatan 46 (Orion) yang telah menjadi rekan seperjuangan penulis hingga dapat menyelesaikan skripsi ini.
Semoga karya ilmiah ini bermanfaat.
Bogor, Juli 2013
vii
DAFTAR ISI
DAFTAR TABEL viii
DAFTAR GAMBAR viii
DAFTAR LAMPIRAN ix
DAFTAR SIMBOL ix
PENDAHULUAN 1
Latar Belakang 1
Tujuan 2
TINJAUAN PUSTAKA 3
Gasifikasi 3
Model Kesetimbangan Termodinamika 7
Pengukuran Laju Aliran Udara 10
METODE 12
Waktu dan Tempat Pelaksanaan 12
Alat dan Bahan 12
Prosedur 15
HASIL DAN PEMBAHASAN 21
Model Kesetimbangan Termodinamika 21
Percobaan dan Validasi Model 23
Simulasi 29
SIMPULAN DAN SARAN 39
Simpulan 39
Saran 40
DAFTAR PUSTAKA 40
LAMPIRAN 41
DAFTAR TABEL
1. Karakteristik beberapa jenis biomassa (Raveendran et al 1994) 3 2. Kelebihan dan kekurangan setiap reaktor gasifikasi (Rajvanshi 1986) 6 3. Reaksi kimia utama pada proses gasifikasi (Mhilu 2012) 8 4. Entalpi pembentukan beragam jenis produk (Perry dan Green 1984
dalam Zainal et al 2001) 9
5. Nilai koefisien pada persamaan ∆gf,T0 (Probstein et al 1982 dalam
Jarungthammachote dan Dutta 2006) 10
6. Nilai koefisien persamaan panas jenis (Cengel et al 2002 dalam
Jarungthammachote dan Dutta 2006) 10
7. Data pengujian kadar air sampel sabut kelapa 24
8. Data komposisi gas rata - rata 27
9. Nilai eror RMS hasil model terhadap hasil percobaan 27 10. Pengaruh peningkatan kadar air terhadap perubahan komposisi gas 29 11. Pengaruh peningkatan ER terhadap perubahan komposisi gas 34
DAFTAR GAMBAR
1. Skema reaktor gasifikasi tipe crossdraft (Foley dan Barnard 1983 dalam
Rajvanshi 1986) 4
2. Skema reaktor gasifikasi tipe updraft (Foley dan Barnard 1983 dalam
Rajvanshi 1986) 5
3. Skema reaktor gasifikasi tipe downdraft (Foley dan Barnard 1983 dalam
Rajvanshi 1986) 5
4. Tampilan Microsoft Excel dengan developer Visual Basic 12 5. Reaktor gasifikasi tipe downdraft yang digunakan 13
6. Drying oven 13
7. Timbangan gantung 13
8. Gas analyzer 13
9. Skema reaktor gasifikasi tipe downdraft yang digunakan 14
10. Penjemuran sabut kelapa 15
11. Sabut kelapa yang telah dipotong 15
12. Diagran alir proses pembuatan model kesetimbangan 16
13. Sampel sabut kelapa 17
14. Peletakkan sampel sabut kelapa yang akan dikeringkan di dalam oven 17 15. Penimbangan bobot akhir sampel sabut kelapa setelah dikeringkan 17
16. Perbedaan tinggi muka air pada manometer 18
17. Penimbangan sabut kelapa 18
18. Pemasukan sabut kelapa ke dalam reaktor 18
ix
25. Perubahan suhu dan komposisi gas selama percobaan 26 26. Lidah api pada ujung pipa pengeluaran gas yang disulut api 27 27. Perbandingan hasil model dengan hasil percobaan 28
28. Validasi model 28
29. Pengaruh kadar air terhadap komposisi gas pada equivalence ratio (ER)
0.15 30
30. Pengaruh kadar air terhadap komposisi gas pada equivalence ratio (ER)
0.20 30
31. Pengaruh kadar air terhadap komposisi gas pada equivalence ratio (ER)
0.25 31
32. Pengaruh kadar air terhadap komposisi gas pada equivalence ratio (ER)
0.30 31
33. Pengaruh kadar air terhadap komposisi gas pada equivalence ratio (ER)
0.35 32
34. Pengaruh kadar air terhadap komposisi gas pada equivalence ratio (ER)
0.40 32
35. Pengaruh kadar air terhadap komposisi gas pada equivalence ratio (ER)
0.45 33
36. Pengaruh kadar air terhadap suhu gasifikasi pada berbagai nilai
equivalence ratio (ER) 33
37. Pengaruh equivalence ratio (ER) terhadap komposisi gas pada kadar air
(mc) 5% 35
38. Pengaruh equivalence ratio (ER) terhadap komposisi gas pada kadar air
(mc) 10% 35
39. Pengaruh equivalence ratio (ER) terhadap komposisi gas pada kadar air
(mc) 15% 36
40. Pengaruh equivalence ratio (ER) terhadap komposisi gas pada kadar air
(mc) 20% 36
41. Pengaruh equivalence ratio (ER) terhadap komposisi gas pada kadar air
(mc) 25% 37
42. Pengaruh equivalence ratio (ER) terhadap komposisi gas pada kadar air
(mc) 30% 37
43. Pengaruh equivalence ratio (ER) terhadap komposisi gas pada kadar air
(mc) 35% 38
44. Pengaruh equivalence ratio (ER) terhadap suhu gasifikasi pada berbagai
tingkat kadar air (mc) 38
DAFTAR LAMPIRAN
1. Pemrograman untuk simulasi numerik menggunakan Microsoft Office
Excel dengan developer Visual Basic 41
DAFTAR SIMBOL
A luas penampang, m2
Ar massa atom relatif, kg/kmol
A/F air to fuel ratio
C koefisien aliran orifice
Cp panas jenis pada tekanan tetap, kJ/kmol K
ER equivalence ratio
g percepatan gravitasi, m/s2
∆gf0 fungsi Gibbs untuk reaksi pembentukan standar ∆GT0 fungsi energi bebas Gibbs untuk reaksi standar hf
0
entalpi pembentukan, kJ/kmol
ΔhT perbedaan entalpi pada suhu T dan pada suhu 298 K pada tekanan 1 atm, kJ/kmol
HHV higher heating value, kJ/kmol k konstanta kesetimbangan reaksi LHV lower heating value, kJ/kmol
m jumlah oksigen yang terkandung dalam udara per kmol biomassa
mc kadar air, %
Mr massa molekul relatif, kg/kmol
n mol
p tekanan, atm
Q debit, m3/detik
R konstanta gas universal, kJ/kmol RMSE root mean square error
T suhu, K
v kecepatan aliran fluida, m/s
w jumlah air yang terkandung dalam biomassa per kmol biomassa
Huruf Yunani
ρ densitas, kg/m3
ν bilangan stokiometri
Υ faktor ekspansi
Subskrip
PENDAHULUAN
Latar Belakang
Gasifikasi adalah proses konversi bahan bakar dalam bentuk padat ke dalam bentuk gas mampu bakar melalui proses termal. Gas mampu bakar ini sebagian besar tersusun atas gas karbon monoksida (CO), hidrogen (H2) dan sedikit metana (CH4). Gas mampu bakar ini dapat digunakan secara langsung untuk pembakaran, misalnya untuk keperluan rumah tangga atau pengeringan, ataupun juga dapat digunakan sebagai bahan bakar motor bakar yang dapat digunakan untuk pembangkit listrik ataupun keperluan lainnya. Pemahaman interaksi antara mekanisme kimia dan fisika selama proses gasifikasi merupakan dasar yang sangat penting untuk desain yang optimum dari reaktor gasifikasi.
Ada beberapa tipe reaktor gasifikasi, tetapi yang umum digunakan untuk menghasilkan gas yang dapat digunakan sebagai bahan bakar engine adalah tipe
downdraft. Tipe ini dapat menghasilkan gas yang lebih bersih karena tar hasil dari
proses pirolisis akan ikut terbakar sehingga sedikit yang akan terikut di dalam gas mampu bakar yang dihasilkan. Kadar tar yang masih terikut pada gasifikasi tipe
downdraft biasanya sekitar 50 mg/m3 – 2 g/m3 (Neeft et al 2002 dalam Surjosatyo
dan Vidian 2012).
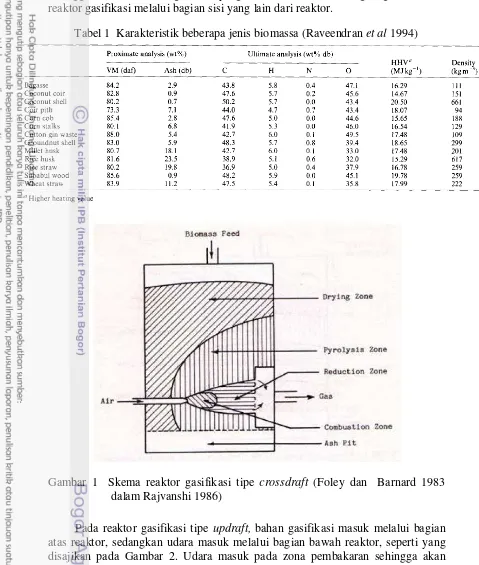
Bahan yang dapat digunakan untuk gasifikasi adalah semua jenis bahan yang mengandung kadar karbon cukup tinggi. Salah satu bahan yang dapat digunakan adalah biomassa. Biomassa yang digunakan sebaiknya adalah biomassa yang tidak memiliki kegunaan lain atau lebih ekonomis jika digunakan sebagai bahan gasifikasi dibandingkan jika digunakan untuk yang lain. Sabut kelapa merupakan salah satu bahan yang memenuhi kriteria tersebut karena menurut Raveendran et al (1995) sabut kelapa mengandung karbon sebesar 47.6%, hidrogen sebesar 5.7%, nitrogen sebesar 0.2%, dan oksigen sebesar 45.6%.
Sabut kelapa merupakan limbah hasil dari perkebunan kelapa yang belum banyak dimanfaatkan di bidang energi terbarukan. Sabut kelapa menjadi potensial untuk dimanfaatkan sebagai sumber energi terbarukan di Indonesia karena Indonesia memiliki perkebunan kelapa yang cukup luas. Selain itu, sabut kelapa juga masih jarang dimanfaatkan dan dianggap memiliki nilai ekonomi yang rendah oleh masyarakat. Metode gasifikasi untuk memanfaatkan limbah sabut kelapa dipilih dibandingkan dengan metode lain, seperti pembakaran langsung pada insenerator karena sabut kelapa sulit untuk dibakar. Selain itu, sabut kelapa yang dibakar akan menghasilkan banyak asap. Dengan metode gasifikasi, asap yang dihasilkan tidak dibuang ke lingkungan tetapi dapat diubah menjadi gas mampu bakar yang lebih bermanfaat.
2
dihasilkan akan sedikit, tetapi jika kadar air terlalu tinggi maka akan menurunkan efisiensi pemanasan reaktor gasifikasi karena panas yang ada digunakan untuk menguapkan air.
Kadar air merupakan salah satu karakteristik biomassa yang paling signifikan yang mempengaruhi proses gasifikasi. Has dan Groeneveld (1987) dalam Ramanan et al (2008) menjelaskan bahwa adanya pengaruh kadar air bahan terhadap komposisi gas yang dihasilkan. Menurut Bridgewater et al (1986) dalam Ramanan et al (2008), bahan dengan kadar air tinggi masih dapat digunakan pada reaktor gasifikasi tipe updraft, tetapi batasan kadar air tertinggi yang diterima untuk tipe downdraft umumnya sekitar 40% (basis kering). Reed dan Das (1988) dalam Ramanan (2008) menjelaskan bahwa kadar air bahan harus di bawah 33% (basis basah) untuk menghasilkan gas mampu bakar dengan kualitas yang baik.
Sebuah reaktor gasifikasi untuk sabut kelapa telah dirancang dan dibuat oleh Nelwan dkk pada program Hi-Link 2012 (Tooy et al 2013). Gas mampu bakar yang dihasilkan dari reaktor gasifikasi sabut kelapa ini akan digunakan sebagai bahan bakar motor bakar untuk menggerakkan generator listrik. Reaktor gasifikasi biomassa merupakan suatu peralatan yang cukup kompleks yang membutuhkan banyak waktu untuk perancangan dan pengoperasian sehingga sulit untuk mengeksplorasi beragam kondisi kerja. Oleh sebab itu, pemodelan matematika dibuat untuk memprediksi kinerja reaktor gasifikasi. Studi teoritis baru – baru ini mencakup pemodelan kinetik atau nonekuilibrium reaksi reduksi pada reaktor gasifikasi biomassa tipe downdraft. Model ini menggambarkan proses reduksi arang menggunakan pernyataan laju kinetik yang diperoleh dari eksperimen dan simulasi data eksperimen di mana waktu tinggal gas dan biomassa relatif singkat.
Meskipun kesetimbangan termodinamika pada kenyataannya tidak pernah terjadi selama proses gasifikasi, perhitungan kesetimbangan termodinamika telah digunakan secara luas untuk memprediksi batasan termodinamika pada reaksi proses gasifikasi. Karena tidak bergantung pada desain reaktor gasifikasi, pendekatan ini sering digunakan dalam studi pengaruh parameter bahan atau parameter penting lainnya terhadap kinerja proses gasifikasi. Syed et al (2012) mengembangkan model untuk gasifikasi biomassa yang menggunakan persamaan energi bebas Gibbs (Gibbs free energy) dari reaksi dan mengembangkan model kesetimbangan. Zainal et al (2001) juga mengembangkan model kesetimbangan reaksi gasifikasi yang menggambarkan komposisi kesetimbangan menggunakan reaksi water-gas shift dan metana (hydrogenating gasification). Prediksi ini menyoroti pengaruh dari kadar air potongan kayu dan suhu reaksi terhadap komposisi gas mampu bakar yang dihasilkan.
Tujuan
3
TINJAUAN PUSTAKA
Gasifikasi
Gasifikasi merupakan proses untuk mengkonversi bahan bakar dalam bentuk padat ke dalam bentuk gas. Energi kimia bahan bakar dalam bentuk padat dikonversi ke dalam bentuk energi panas dan energi kimia gas. Energi kimia yang terkandung dalam gas adalah fungsi dari komposisi kimianya. Hal tersebut membuat komposisi gas yang dihasilkan menentukan kualitasnya sebagai bahan bakar. Konsentrasi tinggi dari gas mampu bakar seperti H2, CO, dan CH4 meningkatkan energi pembakaran dari gas yang dihasilkan (Iyer et al 2002 dalam Kumar SS et al 2008). Gas dapat dibakar sehingga menghasilkan panas untuk keperluan industri atau suatu wilayah tertentu, untuk menjalankan motor bakar untuk keperluan tenaga mekanik maupun listrik, atau untuk membuat bahan bakar sintetik (Reed dan Das 1988).
Menurut Gumz (1950) dalam Pitchandi (2012), selama proses gasifikasi, material organik yang terkandung dalam bahan bakar keluar karena proses panas dan dengan cepat mendorong terbentuknya susunan arang yang utamanya tersusun atas karbon dan abu. Partikel arang mengalami reaksi lebih jauh dengan beberapa gas untuk menghasilkan gas yang diinginkan. Oleh karena itu, karakteristik termokimia dari biomassa memainkan peranan penting dalam pemilihan sistem dan kinerja sistem gasifikasi.
Untuk pembakaran lengkap terhadap biomassa, secara teoritis (stokiometri) udara yang dibutuhkan adalah 6 hingga 6.5 kg udara per kg biomassa. Produk yang dihasilkan pada pembakaran tersebut adalah CO2 dan H2O. Dalam proses gasifikasi, reaksi diperlakukan di bawah kondisi stokiometri dengan jumlah udara yang dibatasi pada kisaran 1.5 hingga 1.8 kg udara per kg biomassa (Vaezi et al
2008). Nilai equivalence ratio (ER) merupakan perbandingan air-fuel ratio aktual dengan air-fuel ratio stokiometri. Secara teoritis, nilai ER untuk pembakaran lengkap adalah 1 (Ramanan et al 2008), sedangkan nilai ER untuk gasifikasi adalah antara 0.15 – 0.4 (Ramanan et al 2008), 0.19 – 0.43 (Zainal et al 2002 dalam Gunarathne 2012), atau 0.3 – 0.6 (Vaezi et al 2008).
Sabut kelapa merupakan salah satu biomassa yang dapat digunakan sebagai bahan gasifikasi. Hal ini karena sabut kelapa memiliki kandungan karbon yang cukup tinggi, seperti yang tersaji pada Tabel 1 bahwa sabut kelapa memiliki kadar karbon 47.6%, sedangkan kadar material lain yaitu hidrogen, nitrogen, dan oksigen secara berturut – turut adalah 5.7%, 0.2%, dan 45.6%. Kadar karbon sabut kelapa hampir sama dengan kadar karbon kayu yang biasa digunakan sebagai bahan gasifikasi di mana kadar karbon kayu adalah 48.2%, sedangkan komposisi unsur yang lain adalah kadar hidrogen 5.9%, kadar nitrogen 0%, dan kadar oksigen 45.1%.
Secara umum, terdapat tiga tipe reaktor gasifikasi, yaitu crossdraft, updraft,
dan downdraft. Pada reaktor gasifikasi tipe crossdraft, bahan gasifikasi masuk
4
sehingga akan dihasilkan gas. Gas yang dihasilkan dialirkan langsung keluar dari reaktor gasifikasi melalui bagian sisi yang lain dari reaktor.
Tabel 1 Karakteristik beberapa jenis biomassa (Raveendran et al 1994)
Gambar 1 Skema reaktor gasifikasi tipe crossdraft (Foley dan Barnard 1983 dalam Rajvanshi 1986)
5
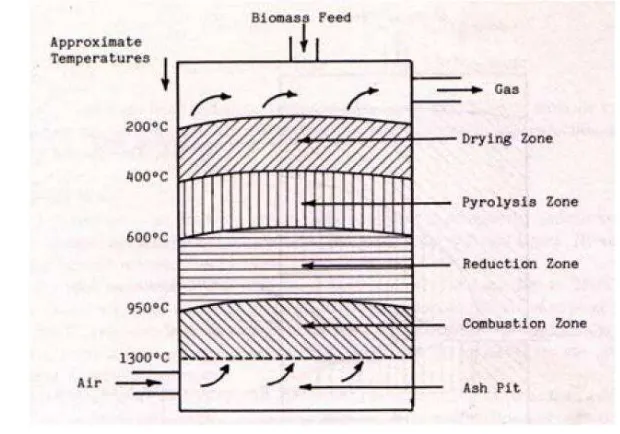
Gambar 2 Skema reaktor gasifikasi tipe updraft (Foley dan Barnard 1983 dalam Rajvanshi 1986)
Pada reaktor gasifikasi tipe downdraft, bahan gasifikasi masuk melalui bagian atas reaktor, sedangkan udara masuk melalui bagian tengah reaktor, seperti yang disajikan pada Gambar 3. Udara masuk pada zona pembakaran sehingga akan membakar bahan gasifikasi. Panas yang dihasilkan akan digunakan untuk proses lain, yaitu pengeringan, pirolisis, dan reduksi sehingga akan dihasilkan gas. Gas yang dihasilkan akan mengalir mengikuti aliran udara dan keluar pada bagian bawah reaktor. Tar hasil dari proses pirolisis terbakar pada zona pembakaran sehingga sedikit yang terikut bersama aliran gas yang dihasilkan.
6
Berdasarkan Tabel 2, diketahui bahwa reaktor gasifikasi tipe downdraft
dapat menghasilkan gas mampu bakar dengan kadar debu dan tar yang rendah serta fleksibel terhadap variasi beban kerja.
Tabel 2 Kelebihan dan kekurangan setiap reaktor gasifikasi (Rajvanshi 1986) No yang dibutuhkan untuk menyalakan motor bakar internal
2 Downdraft Penyesuaian yang fleksibel
dari produksi gas terhadap beban
Kurang sensitif terhadap kandungan debu dan tar dari bahan
3 Crossdraft Rancangan memiliki ukuran
dan bentuk yang relatif kecil Respon sangat cepat
terhadap beban Produksi gas fleksibel
Sangat sensitif terhadap pembentukan kerak
Pressure drop tinggi
Di dalam reaktor gasifikasi, terjadi reaksi kimia pada zona pembakaran dan reduksi. Uraian tentang proses kimia tersebut adalah sebagai berikut (Gaos 2008):
1. Zona pengeringan
Bahan baku terkena panas antara 100 – 250 oC sehingga bahan baku mulai mengering. Dengan demikian air yang terkandung di dalam bahan akan menguap, seperti pada persamaan reaksi berikut:
H2O (cair) H2O (uap) (1) 2. Zona pirolisis
Setelah proses pengeringan dilakukan, bahan baku umpan akan turun dan menerima panas pada suhu antara 250 – 500 oC dalam kondisi tanpa udara. Bahan baku mulai terurai dan menjadi arang, uap air, dan gas. Proses pirolisis dimulai dengan dekomposisi hemiselulosa pada suhu antara 200 – 250 oC, dekomposisi selulosa sampai dengan suhu 350 oC, dan proses pirolisis berakhir pada suhu 500 o
C. Selanjutnya proses pengarangan yang berlangsung pada suhu 500 – 900 oC terjadi di daerah batas zona pirolisis dan oksidasi. Proses kimia pirolisis adalah sebagai berikut:
7 3. Zona oksidasi
Arang yang terbentuk dari ujung zona pirolisis masuk ke daerah oksidasi, selanjutnya dibakar dengan udara yang dimasukkan dari luar melalui lubang pemasukan udara, akan tetapi dengan jumlah yang tidak memadai sehingga terjadi pembakaran tidak sempurna. Suhu oksidasi berkisar antara 900 – 1400 oC terjadi di daerah cekikan (throat section) yang merupakan zona pembakaran.
2C + O2 2CO + energi termal (3) 2CO + O2 2CO2 + energi termal (4) Tar, minyak, metana, dll CO, CO2, H2O, CH4 + energi termal (5) 4. Zona reduksi
Proses ini dimaksudkan untuk mereduksi gas CO2 hasil proses oksidasi dengan arang menjadi gas CO. Proses ini berlangsung pada kisaran suhu 900 oC, dengan mengambil panas dari zona oksidasi. Arang bereaksi dengan gas CO2 membentuk gas CO, dan arang bereaksi dengan uap air membentuk gas CO dan gas H2. Proses kimia reduksi adalah sebagai berikut:
C + H2O CO + H2 – energi temal (6) CO2 + C 2CO – energi termal (7) Model Kesetimbangan Termodinamika
Model kesetimbangan termodinamika secara keseluruhan terdiri dari persamaan neraca massa dan neraca energi. Neraca massa yang digunakan adalah neraca massa dari reaksi total gasifikasi. Persamaan umum reaksi total gasifikasi adalah sebagai berikut (Jarungthammachote dan Dutta 2006):
CHxOyNz + wH2O + m(O2 + 3.76N2) = x1H2 + x2CO + x3CO2 + x4H2O + x5CH4 + (3.76m + z/2) N2 (8) di mana x, y, dan z adalah jumlah atom hidrogen, oksigen, dan nitrogen per satu atom karbon di dalam biomassa, w adalah jumlah air yang terkandung dalam biomassa per kmol biomassa, m adalah jumlah oksigen yang terkandung dalam udara per kmol biomassa, dan x1, x2, x3, x4, dan x5, adalah koefisien konstituen masing – masing produk.
Nilai m dapat dihitung dengan mengalikan laju aliran udara dengan lama waktu proses gasifikasi. Nilai w dapat dihitung berdasarkan kadar air biomassa dengan rumus sebagai berikut (Vaezi et al 2008):
w = Mr biomassa × mc Mr H2O × (1 - mc)
di mana Mr biomassa dan Mr H2O adalah massa molekul relatif biomassa dan air,
sedangkan mc adalah kadar air biomassa.
Persamaan reaksi kimia secara spesifik yang terjadi selama proses gasifikasi disajikan pada Tabel 3. Dari beberapa reaksi kimia yang terjadi, hanya ada empat reaksi yang merupakan reaksi independen, yaitu oksidasi (R1), Boudouard (R2),
water-gas (R3), dan pembentukan metana (R4). Reaksi water-gas shift dapat
8
dianggap sebagai pengurangan reaksi steam gasification dan Boudouard. Reaksi oksidasi diasumsikan terjadi sangat cepat dan lengkap.
Tabel 3 Reaksi kimia utama pada proses gasifikasi (Mhilu 2012)
Reaction no Reaction scheme Chemical reaction
R1 (a) C + O2 → CO2 Nilai konstanta kesetimbangan reaksi yang merupakan fungsi dari suhu dapat dihitung menggunakan persamaan perubahan energi bebas Gibbs (Gibbs
free energy) untuk reaksi standar pada suhu dan tekanan konstan (Perry dan Green
1984 dalam Zainal et al 2001):
dimana R adalah konstanta gas universal (8.314 kJ/kmole) dan ∆GT 0
adalah fungsi perubahan energi bebas Gibbs untuk reaksi standar. Fungsi ∆GT0 terhadap suhu dapat dinyatakan sebagai berikut (Jarungthammachote dan Dutta 2006):
∆GT0 = vi∆gf,T,i0 i
Nilai ∆GT 0
untuk water-gas shift reaction adalah sebagai berikut: ∆GT, 10 = ∆gf,CO
Nilai ∆GT0 untuk methanation reaction adalah sebagai berikut: ∆GT, 20 = ∆gf,CH suhu tertentu dari gas i yang dinyatakan dengan persamaan di bawah ini.
9 Nilai a, b, c, d, e, f, dan g adalah koefisien persamaan fungsi pembentukan Gibbs untuk reaksi standar yang nilainya disajikan pada Tabel 5.
Dalam tujuan untuk menentukan suhu gasifikasi, digunakan persamaan neraca energi antara reaktan dan produk. Persamaannya adalah sebagai berikut (Syed et al 2012):
adalah entalpi pembentukan reaktan i, xj jumlah mol produk j, hf,j
0
adalah entalpi pembentukan produk j, ∆hT adalah perbedaan entalpi produk j pada suhu T dan pada suhu 298 K, Cp, j adalah panas jenis produk j pada tekanan konstan, dan ∆T adalah selisih suhu gasifikasi (T) dengan suhu referensi (298 K).
Entalpi pembentukan untuk masing – masing produk disajikan pada Tabel 4 sedangkan higher heating value (HHV) dan entalpi pembentukan biomassa (hf) berturut – turut dihitung menggunakan rumus sebagai berikut (Syed et al 2012):
HHV = 418920 + 117830 x - 166880 y kJ
Tabel 4 Entalpi pembentukan beragam jenis produk (Perry dan Green 1984 dalam Zainal et al 2001)
Panas jenis rata – rata pada selang suhu tertentu yang digunakan pada persamaan (17) dihitung dengan menggunakan rumus sebagai berikut (Jarungthammachote dan Dutta 2006):
Cp,i(T)=a+bT+cT2+dT3
10
CO -110.5 5.619 -11.90 6.383 -1.846 -4.891 8.684 -6.131
CO2 -393.5 -19.49 31.22 -24.48 6.946 -4.891 52.70 -12.07
H2O -241.8 -8.950 -3.672 5.209 -1.478 0.0 28.68 -1.722
CH4 -74.8 -46.20 11.30 13.19 -6.647 -4.891 141.1 -22.34
Pengukuran laju aliran udara yang melalui pipa dapat dilakukan dengan menggunakan celah orifice (orifice plate) yang dihubungkan dengan manometer. Data yang perlu diambil dari percobaan adalah perbedaan tinggi muka air pada kolom manometer. Persamaan yang digunakan pada pengukuran laju aliran udara adalah sebagai berikut (http://www.engineeringtoolbox.com):
Dengan mengkombinasikan persamaan Bernoulli dan persamaan kontinuitas, didapatkan persamaan untuk menghitung laju aliran udara sebagai berikut:
Q = CY A2 2ρ(p1 - p2) /ρ
di mana p1 – p2 adalah perbedaan tekanan aliran sebelum dan setelah melewati celah orifice, Y adalah faktor ekspansi, A2 adalah luas celah orifice, dan C adalah koefisien aliran orifice.
(21)
(22)
11 Perbedaan tekanan aliran sebelum dan setelah celah orifice dapat dihitung menggunakan rumus sebagai berikut:
p1- p2 = ρ g ∆h
di mana ρ adalah densitas udara (kg/m3), g adalah percepatan gravitasi (m/s2), dan ∆h adalah perbedaan tinggi muka air dalam kolom manometer.
Nilai faktor ekspansi (Y) dapat dihitung menggunakan rumus sebagai berikut:
Y=1– 1-r
k 0.41+0.35 β 4
di mana r adalah perbandingan tekanan aliran udara setelah melewati celah orifice dengan sebelum melewati celah orifice (p2/p1), k adalah ratio panas jenis pada
tekanan tetap dengan panas jenis pada volume tetap (cp/cv), β adalah perbandingan diameter celah orifice dengan diameter pipa (d2/d1).
Laju aliran oksigen dihitung menggunakan rumus sebagai berikut: QO
2 = Qudara (m
3
/detik) * 21% (26)
Laju aliran massa oksigen dihitung menggunakan rumus sebagai berikut: ṁO2 = QO
2* (m
3
/detik) * ρO
2(kg/m
3
) (27)
Mol oksigen dihitung menggunakan rumus sebagai berikut:
m = ṁO2(kg/detik) * waktu (jam) * 3600 detik/jam / Mr O2 (kg/kmol) (28) Nilai air to fuel ratio (A/F ratio) dihitung menggunakan rumus sebagai berikut: (A/F) = [m (kmol) * (Mr O2 + 3.76 * Mr N2) (kg/kmol)] / (massa sabut (kg)) (29) Pada kondisi stokiometri, jumlah mol O2 sama dengan jumlah mol sabut kelapa pada persamaan (8), sehingga nilai m = 1.
Dengan menggunakan nilai (A/F) aktual dan nilai (A/F) stokiometri, maka dapat dihitung nilai equivalence ratio. Perhitungannya adalah sebagai berikut:
Nilai equivalence ratio = (A/F) aktual / (A/F) stokiometri (30) (24)
12
METODE
Waktu dan Tempat Pelaksanaaan
Penelitian ini dilaksanakan dari bulan Maret 2013 sampai dengan bulan Juni 2013. Tempat pelaksanaan penelitian ini adalah Laboratorium Energi dan Elektrifikasi Pertanian, dan Laboratorium Lapang Siswadhi Supardjo Leuwikopo Gedung Metatron.
Alat dan Bahan
Rincian alat dan bahan yang digunakan pada penelitian ini adalah sebagai berikut: Pembuatan model kesetimbangan dan simulasi
Alat: Komputer dan software Microsoft excel dengan developer Visual
Basic (Gambar 4).
Bahan: Data karakteristik sabut kelapa berdasarkan data ultimate analysis
sabut kelapa.
Percobaan dan validasi model
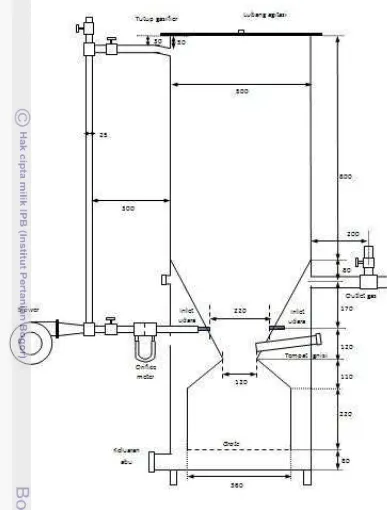
Alat: Reaktor gasifikasi tipe downdraft - batch (Gambar 5 dan Gambar 9), termokopel batang tipe K merk Chino K/G385, termokopel tipe K (kawat),
hybrid recorder merk yokogawa 3081, drying oven SS 204D (Gambar 6),
timbangan digital merk DJ1000, penggaris dengan nilai skala terkecil 1 mm, timbangan gantung tipe jarum merk Salter (Gambar 7), dan gas analyzer
merk Lancom 4 (Gambar 8).
Bahan: Sabut kelapa dari buah kelapa tua berumur sekitar 11 – 13 bulan. Sabut kelapa terlebih dahulu dijemur di bawah sinar matahari langsung (Gambar 10) agar didapatkan sabut kelapa yang cukup kering untuk proses gasifikasi. Selanjutnya sabut kelapa dipotong menjadi berukuran relatif kecil (Gambar 11).
13
Gambar 5 Reaktor gasifikasi tipe downdraft yang digunakan
Gambar 6 Drying oven Gambar 7 Timbangan gantung
Gambar 8 Gas analyzer Kran
pemasukan udara Kran
pembuangan
kelebihan udara Pipa
pengeluaran gas
Lubang ignisi
Blower
14
15
Gambar 10 Penjemuran sabut kelapa Gambar 11 Sabut kelapa yang telah dipotong
Prosedur
Prosedur yang digunakan pada penelitian ini secara umum terbagi dalam dua prosedur, yaitu pembuatan model kesetimbangan & simulasi dan percobaan & validasi model. Penjelasan untuk masing – masing prosedur adalah sebagai berikut:
Pembuatan model kesetimbangan dan simulasi
Asumsi yang digunakan pada pembuatan model kesetimbangan ini adalah sebagai berikut:
1. Sabut kelapa direpresentasikan dengan rumus molekul CHxOyNz.
2. Reaksi di dalam reaktor berada pada kesetimbangan termodinamika dan berlangsung pada tekanan 1 (satu) atmosfir.
3. Reaktor gasifikasi bersifat adiabatik (tidak ada panas yang hilang ke lingkungan).
4. Semua gas bersifat gas ideal.
5. Semua karbon di dalam biomassa tergasifikasi sehingga pembentukan arang diabaikan.
6. Abu di dalam biomassa inert sehingga tidak ikut dalam reaksi kimia. 7. Gas yang dihasilkan terdiri dari H2, CO, CO2, H2O, CH4, dan N2. 8. Tar tidak diperhitungkan di dalam simulasi.
9. Gas N2 inert selama proses gasifikasi.
Langkah – langkah dalam pembuatan model kesetimbangan disajikan pada Gambar 12. Berikut merupakan penjelasan langkah – langkah tersebut disertai dengan langkah – langkah perhitungan komposisi gas serta suhu gasifikasi: 1. Rumus molekul bahan reaktan pada reaksi gasifikasi dibentuk dengan
berdasarkan karakteristik sabut kelapa yang diperoleh dari data ultimate
analysis sabut kelapa (Tabel 1). Reaksi total gasifikasi sabut kelapa kemudian
dibentuk mengikuti persamaan (8).
16
3. Komposisi gas yang dihasilkan dari proses gasifikasi diperoleh dengan melakukan iterasi menggunakan Newton-Raphson method terhadap fungsi kesetimbangan yang dibentuk dengan memasukkan suhu dan komposisi gas sebagai dugaan awal, serta nilai kadar air dan equivalence ratio (ER) sebagai nilai yang telah ditetapkan. Iterasi dilakukan hingga perubahan nilai mol masing – masing gas kurang dari nilai mutlak 1 x 10-10.
4. Dengan memasukkan nilai mol masing – masing gas yang diperoleh dari langkah (3), nilai mol oksigen (m), entalpi pembentukan (hf) dan fungsi Cp untuk masing – masing produk dan reaktan ke dalam persamaan (16), maka terbentuk fungsi neraca energi dengan satu variabel yaitu variabel T (suhu). Dengan memasukkan suhu dugaan awal, iterasi menggunakan
Newton-Raphson method dilakukan terhadap persamaan neraca energi hingga
perubahan suhu di dalam iterasi kurang dari nilai mutlak 1 x 10-5 sehingga diperoleh suhu gasifikasi yang baru.
5. Komposisi gas dan suhu gasifikasi yang baru digunakan untuk melakukan kembali langkah (3) dan seterusnya hingga suhu gasifikasi relatif tidak berubah (perubahan kurang dari nilai mutlak 1 x 10-2).
Gambar 12 Diagram alir proses pembuatan model kesetimbangan
Mulai
Pembentukan persamaan reaksi total untuk gasifikasi sabut kelapa
Pembentukan persamaan neraca massa karbon, neraca massa hidrogen, neraca massa oksigen, konstanta kesetimbangan untuk water-gas shift reaction, dan konstanta kesetimbangan methanation reaction
Pembentukan persamaan neraca energi pada reaksi gasifikasi
Selesai Data ultimate analysis
sabut kelapa dari literatur
17 Percobaan dan validasi model
Percobaan digunakan untuk memvalidasi model yang telah dibuat. Percobaan dilakukan setelah model kesetimbangan dibentuk. Penjelasan langkah – langkah percobaan adalah sebagai berikut:
1. Kadar air sabut kelapa (basis basah) diukur dengan langkah – langkah berikut ini:
1) Sampel sabut kelapa diambil sebanyak 3 sampel dengan masing – masing sekitar 100 gram per sampel (Gambar 13).
2) Bobot sampel sabut kelapa diukur menggunakan timbangan digital.
3) Sampel sabut kelapa diletakkan pada wadah lalu diletakkan di dalam oven (Gambar 14) untuk dipanaskan selama 40 jam pada suhu konstan 105 oC. 4) Bobot akhir sabut kelapa diukur kembali menggunakan timbangan digital
(Gambar 15).
5) Kadar air sabut kelapa basis basah dihitung dengan membandingkan bobot sabut kelapa kering dengan bobot sabut kelapa awal (sebelum dikeringkan) 6) Kadar air dari ketiga sampel dirata - ratakan. Nilai kadar air rata – rata
dijadikan sebagai kadar air sabut kelapa.
Gambar 13 Sampel sabut kelapa
Gambar 14 Peletakkan sampel sabut kelapa yang akan dikeringkan di dalam oven
18
2. Laju aliran udara diatur dengan menggunakan kran yang ada di pipa pemasukan udara. Laju aliran udara diukur menggunakan orifice meter yang dilengkapi dengan manometer. Pada manometer akan terbaca perbedaan tinggi muka air di dalam manometer (Gambar 16) yang selanjutnya digunakan untuk mencari laju aliran udara menggunakan persamaan laju aliran udara pada
orifice meter.
Gambar 16 Perbedaan tinggi muka air pada manometer
3. Sabut kelapa ditimbang dengan menggunakan timbangan gantung (Gambar 17) sebelum dimasukkan ke dalam reaktor. Arang dimasukkan terlebih dahulu hingga ruang di bawah daerah cekikan reaktor terpenuhi oleh arang, lalu sabut kelapa dimasukkan sedikit demi sedikit (Gambar 18) ke dalam reaktor hingga penuh (Gambar 19).
Gambar 17 Penimbangan Gambar 18 Pemasukan sabut kelapa sabut kelapa ke dalam reaktor
19 4. Suhu gasifikasi diukur dengan menggunakan termokopel tipe K. Termokopel
tipe K dipilih sebagai instrumen pengukuran karena dapat mengukur suhu hingga 1370 oC. Titik pengukuran suhu pada penelitian ini disajikan pada Gambar 20, yaitu pada zona oksidasi menggunakan termokopel batang dan bagian paling bawah zona reduksi menggunakan termokopel kawat.
Gambar 20 Titik pengukuran suhu zona oksidasi dan bagian bawah zona reduksi
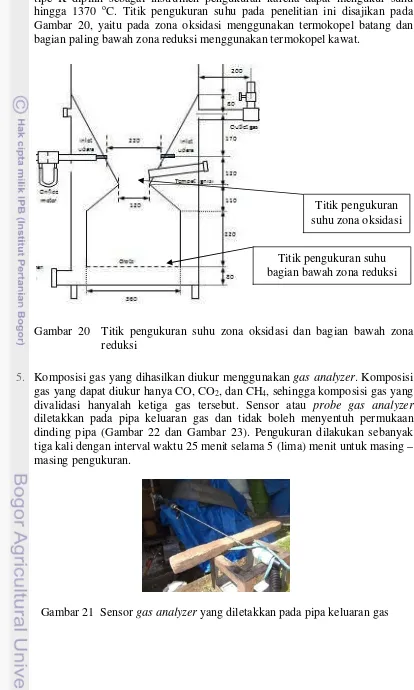
5. Komposisi gas yang dihasilkan diukur menggunakan gas analyzer. Komposisi gas yang dapat diukur hanya CO, CO2, dan CH4, sehingga komposisi gas yang divalidasi hanyalah ketiga gas tersebut. Sensor atau probe gas analyzer
diletakkan pada pipa keluaran gas dan tidak boleh menyentuh permukaan dinding pipa (Gambar 22 dan Gambar 23). Pengukuran dilakukan sebanyak tiga kali dengan interval waktu 25 menit selama 5 (lima) menit untuk masing – masing pengukuran.
Gambar 21 Sensor gas analyzer yang diletakkan pada pipa keluaran gas Titik pengukuran suhu bagian bawah zona reduksi
20
Gambar 22 Sensor yang tidak menyentuh permukaan dinding pipa
6. Data komposisi gas yang dihasilkan dari percobaan dan hasil model dibuat perbandingannya lalu dianalisis dengan metode root mean square error
(RMSE) dan koefisien penentuan (R2). Rumus perhitungan metode root mean
square error (RMSE) adalah sebagai berikut:
RMSE = ∑ (percobaani-modeli) 2 N
i=1
Jumlah data
Simulasi
Simulasi dilakukan setelah percobaan dan validasi model dilakukan. Simulasi dilakukan untuk mengetahui perubahan komposisi gas dan suhu gasifikasi akibat dari perubahan kadar air sabut kelapa dan terhadap perubahan
equivalence ratio (ER). Kadar air sabut kelapa yang disimulasikan adalah 5%,
10%, 15%, 20%, 25%, 30%, dan 35%, sedangkan equivalence ratio (ER) yang disimulasikan adalah 0.15, 0.20, 0.25, 0.30, 0.35, 0.40, dan 0.45. Pemrograman untuk simulasi disajikan pada Lampiran 1.
21
HASIL DAN PEMBAHASAN
Model Kesetimbangan Termodinamika
Berdasarkan data ultimate analysis sabut kelapa, diketahui bahwa kandungan karbon, hidrogen, oksigen, dan nitrogen di dalam sabut kelapa berturut – turut adalah 47.6%, 5.7%, 45.6%, dan 0.2%, sehingga rumus molekul sabut kelapa dapat ditentukan dengan perhitungan sebagai berikut:
Karbon (C) = 47.6 * 1 / ArC = 47.6 * 1 / 12 = 3.97 Hidrogen (H) = 5.7 * 1 / ArH = 5.7 * 1 / 1 = 5.70 Oksigen (O) = 45.6 * 1 / ArO = 45.6 * 1 / 16 = 2.85 Nitrogen (N) = 0.2 * 1 / ArN = 0.2 * 1 / 14 = 0.0143
Sehingga, rumus molekul sabut kelapa dapat dinyatakan C3.97H5.7O2.85N0.0143 dan rumus molekul tiap 1 mol atom karbon = CH1.44O0.72N0.0035
Reaksi total gasifikasi untuk sabut kelapa mengikuti persamaan (8), sehingga reaksi total gasifikasi adalah sebagai berikut:
CH1.44O0.72N0.0035 + wH2O + m(O2 + 3.76N2) = x1H2 + x2CO + x3CO2 + x4H2O + x5CH4 + (3.76m + z/2) N2 (32) Dari persamaan reaksi gasifikasi di atas, diketahui bahwa terdapat lima variabel yang tidak diketahui, yaitu x1, x2, x3, x4, dan x5, sedangkan w dapat diketahui berdasarkan kadar air sabut kelapa dengan menggunakan persamaan (9), dan m dapat diketahui dari laju aliran udara menggunakan perhitungan mol oksigen pada persamaan (28). Oleh karena itu, diperlukan lima persamaan untuk mengetahui nilai variabel yang belum diketahui.
Neraca massa
22
Neraca massa oksigen:
0.72 + w + 2m = x2 + 2x3 + x4 Konstanta kesetimbangan reaksi
Konstanta kesetimbangan reaksi yang digunakan untuk reaksi gasifikasi adalah konstanta kesetimbangan water-gas shift reaction dan methanation
reaction (Jarungthammachote dan Dutta 2006). Persamaan water-gas shift
reaction dan methanation reaction disajikan pada Tabel 3.
Persamaan konstanta kesetimbangan water-gas shift reaction: k1 =
nCO2 nH2
nCO nH2O
= x3 x1 x2 x4 Persamaan konstanta kesetimbangan methanation reacton:
k2 = nCH4 ntotal persamaan (37) berturut – turut diubah bentuknya menjadi persamaan berikut ini:
f1 = 1 - x2 - x3 - x5 = 0 (38) f2 = 1.44 + 2w - 2x1 - 2x4 - 4x5 = 0 (39) f3 = 0.72 + w + 2m - x2 - 2x3 - x4 = 0 (40) f4 = k1 (x2 x4) - (x3 x1) = 0 (41) f5 = k2 (x1)2 - x5 xtotal = 0 (42) Iterasi menggunakan Newton-Raphson method dilakukan terhadap persamaan (38) hingga persamaan (42). Dalam penentuan nilai perubahan komposisi gas (∆x1, ∆x2, ∆x3, ∆x4, dan ∆x5), digunakan metode Gauss dengan terlebih dahulu menyusun turunan parsial persamaan (38) hingga persamaan (42) ke dalam matriks, seperti yang disajikan pada persamaan (43). Iterasi dilakukan dengan mengambil nilai dugaan awal terhadap suhu, x1, x2, x3, x4, dan x5.Fungsi neraca energi (persamaan (44)) dibentuk mengikuti persamaan (16) dengan menggunakan persamaan (17) hingga persamaan (20). Secara ringkas tahapan perhitungan komposisi gas dan suhu gasifikasi disajikan pada Gambar 24.
23
Percobaan dan Validasi Model Kadar air sabut kelapa
Sabut kelapa yang telah dijemur, dipotong menjadi ukuran yang relatif kecil. Dimensi sabut kelapa rata – rata dari 10 sampel yang diambil adalah panjang 5.75 cm, lebar 4.35 cm, dan tebal 2.5 cm. Proses pengukuran dimensi sabut kelapa
Mulai
Suhu (T) dugaan awal, x1, x2, x3, x4, dan x5 dugaan awal, dan m
Perhitungan nilai konstanta kesetimbangan
Perhitungan komposisi gas yang dihasilkan dengan melakukan iterasi Newton-Raphson method terhadap persamaan neraca massa dan konstanta kesetimbangan
Perhitungan suhu gasifikasi dengan melakukan iterasi
Newton-Raphson method terhadap persamaan neraca energi
|Tbaru – T| < 0.01
x1, x2, x3, x4, x5, T T = Tbaru,
x1 = x1 baru, x2 = x2 baru, x3 = x3 baru, x4 = x4 baru, x5 = x5baru
Selesai
x1 baru, x2 baru, x3 baru, x4 baru, dan x5 baru
Tbaru
Tidak
Ya
24
disajikan pada Gambar 25. Sabut kelapa yang telah dipotong dimasukkan ke dalam karung lalu diukur kadar airnya dengan mengambil 1 (satu) sampel sebanyak sekitar 100 gram sabut kelapa dari masing - masing karung. Kadar air rata – rata sabut kelapa yang yang terukur dan digunakan untuk percobaan adalah 15.93 %. Data pengujian kadar air sampel sabut kelapa disajikan pada Tabel 7. Kadar air sabut kelapa ini cukup baik untuk proses gasifikasi karena Jayah et al
(2003) dalam Jarungthammachote dan Dutta (2006) melakukan percobaan gasifkasi pada kadar air kayu 14% dan 16%, Altafini et al (2003) dalam Jarungthammachote dan Dutta (2006) melakukan percobaan gasifikasi pada kadar air kayu 10%, dan Alauddin (1996) dalam Vaezi et al (2008) melakukan percobaan gasifikasi pada kadar air kayu 20%.
(a) (b) (c)
Gambar 24 Pengukuran dimensi sabut kelapa yang telah dipotong; (a) panjang, (b) lebar, dan (c) tebal
Tabel 7 Data pengujian kadar air sampel sabut kelapa Sampel Bobot awal (gram) Bobot akhir (gram) Kadar air (%)
1 101.65 85.93 15.46%
2 101.57 84.56 16.75%
3 101.00 85.27 15.57%
Rata – rata 15.93%
Laju aliran udara
Laju aliran udara yang digunakan adalah 7.96 m3 / jam dengan equivalence
ratio (ER) adalah 0.38. Hal ini didapatkan dari perhitungan di mana perbedaan
tinggi muka air pada kolom manometer adalah 1 cm. Data – data yang digunakan dalam perhitungan adalah jumlah sabut kelapa yang dimasukkan ke dalam reaktor adalah 12 kg (kadar air 15.93%), sisa arang sabut kelapa adalah 3.9 kg, waktu proses adalah 77 menit (1.28 jam), diameter dalam pipa (d1) adalah 3 cm (0.03 m), diameter celah orifice (d2) adalah 1.5 cm (0.015 m), koefisien orifice yang digunakan (Cd) adalah 0.97 (http://www.Buschusa.com), dan persentase oksigen terhadap udara adalah 21%. Berikut merupakan tahapan perhitungan yang dilakukan:
a. Perbedaan tekanan udara sebelum dan setelah melewati celah orifice: ∆p = ρair (kg.m3) * g (m/s2) * ∆h (m)
= 1000 * 9.81 * 1 cm / (100 cm/m) = 98.10 Pa b. Konstanta persamaan laju aliran udara:
25 = 0.97 / ((1 – (0.015/0.03)4)0.5) = 1.0018
c. Luas penampang celah orifice:
A2 = 0.25 * π * d22 (m2) = 0.25 * π * 0.0152 = 0.0001767 m2 f. Laju aliran massa oksigen
ṁO2 = QO2* (m
h. Nilai equivalence ratio:
Jumlah sabut kelapa yang dimasukkan ke dalam reaktor = 12 kg.
Dengan kadar air sabut kelapa 15.93%, maka bobot kering sabut kelapa adalah 12 kg * (100% - 15.93%) = 10.1 kg.
Jumlah arang sabut kelapa yang tersisa adalah 3.9 kg.
Jumlah sabut kelapa yang digunakan selama gasifikasi adalah 10.1 kg – 3.9 kg = 6.2 kg. Nilai (A/F) aktual adalah sebagai berikut:
(A/F) aktual = [m (kmol) * (Mr O2 + 3.76 * Mr N2) (kg/kmol)] / (massa sabut Sehingga nilai (A/F) stokiometri adalah sebagai berikut:
(A/F) stokiometri = 1 kmol * (Mr O2 + 3.76 * Mr N2) (kg/kmol) / (massa sabut kelapa (kg))
= [1 * (32 + 3.76 * 28)] / [1 * (12 + 1.44 + 0.72 * 16 + 0.0035 * 14] = 5.49
Dengan menggunakan nilai (A/F) aktual dan nilai (A/F) stokiometri, maka dapat dihitung nilai equivalence ratio. Perhitungannya adalah sebagai berikut:
Nilai equivalence ratio = (A/F) aktual / (A/F)stokiometri = 2.11 / 5.49 = 0.38
Nilai equivalence ratio (ER) berdasarkan hasil perhitungan adalah 0.38. Nilai ini masih termasuk dalam range ER untuk proses gasifikasi, yaitu 0.15 – 0.4 (Ramanan et al 2008).
26
(data 3) selama masing – masing lima menit untuk setiap pengambilan data. Berikut merupakan data pengukuran suhu dan komposisi gas hasil dari percobaan yang dilakukan:
Suhu gasifikasi
Suhu gasifikasi yang terjadi pada zona oksidasi berkisar antara 917.7 - 1012.6 oC. Hal ini sesuai dengan literatur yang ada, yaitu menurut Gaos (2008) bahwa suhu zona oksidasi pada reaktor gasifikasi tipe downdraft adalah berkisar antara 900 – 1400 oC. Data mengenai pengukuran suhu gasifikasi disajikan pada Gambar 26. Meskipun demikian, suhu maksimum zona oksidasi yang terukur hanya sampai pada 1012.6 oC. Hal ini karena reaktor gasifikasi pada kenyataannya tidak adiabatik. Selain itu, reaktor gasifikasi tidak dilapisi insulator sehingga panas yang dihasilkan dari proses oksidasi mudah keluar ke lingkungan. Hal ini membuat suhu hasil percobaan yang diukur lebih rendah dari data yang terdapat pada literatur.
Suhu yang terukur pada bagian paling bawah zona reduksi berkisar antara 104.6 – 108.2 oC. Hasil ini tidak sesuai dengan literatur yang ada. Suhu pada zona reduksi seharusnya berkisar 900 oC (Gaos 2008). Perbedaan ini dapat terjadi karena posisi ujung kawat termokopel hanya terletak beberapa sentimeter dari bagian dasar zona reduksi. Padahal zona reduksi merupakan zona yang terletak beberapa sentimeter di bawah zona oksidasi hingga bagian dasar zona reduksi. Oleh karena itu, suhu yang terukur pada zona reduksi pada bagian paling bawah tidak dapat mewakili suhu zona reduksi secara keseluruhan.
Komposisi gas yang dihasilkan
Komposisi gas yang dihasilkan adalah 14.03% CO, 16.59% CO2, dan 1.38% CH4 (% volume). Data pengukuran komposisi gas rata – rata disajikan pada Tabel 8, sedangkan data keseluruhan pengukuran disajikan pada Lampiran 2.
Gambar 25 Perubahan suhu dan komposisi gas selama percobaan
27 Tabel 8 Data komposisi gas rata – rata
Jenis Gas Persentase rata – rata (% volume)
CO 14.03%
CO2 16.59%
CH4 1.38%
Komposisi CO dan CH4 menurun dari pengambilan data pertama hingga data ketiga. Hal ini karena sabut kelapa dan arang yang ada jumlahnya semakin sedikit, sehingga gas CO dan CH4 yang dihasilkan semakin sedikit. Hal ini berkesesuaian dengan suhu gasifikasi. Suhu gasifikasi menurun dari pengambilan data pertama hingga data ketiga. Hal ini menunjukkan bahwa komposisi gas CO dan CH4 dipengaruhi oleh suhu gasifikasi yang terjadi di mana suhu gasifikasi yang terjadi dipengaruhi oleh suplai oksigen dan biomassa. Pengujian dengan menyulut api pada ujung pipa pengeluaran gas juga dilakukan untuk membuktikan adanya gas mampu bakar yang dihasilkan, seperti yang disajikan pada Gambar 27.
Gambar 26 Lidah api pada ujung pipa pengeluaran gas yang disulut api Validasi model
Validasi model dilakukan dengan membandingkan hasil model dengan hasil percobaan pada kadar air dan laju aliran udara yang sama, yaitu pada kadar air 15.93% dan laju aliran udara 7.96 m3/jam (equivalence ratio (ER) 0.38). Nilai eror RMS disajikan pada Tabel 9, perbandingan hasil model dengan hasil percobaan disajikan pada dan Gambar 28 dan nilai R2 disajikan pada Gambar 29.
Tabel 9 Nilai eror RMS hasil model terhadap hasil percobaan Jenis Gas
Model Percobaan
Eror RMS Komposisi
(% volume)
Komposisi (% volume)
CO 17.65% 14.03%
2.44%
CO2 14.61% 16.59%
28
Gambar 27 Perbandingan hasil model dengan hasil percobaan
Gambar 28 Validasi model
Hasil validasi menunjukkan bahwa komposisi gas hasil model memiliki hasil yang cukup dekat dengan gas hasil percobaan. Hal ini ditunjukkan dengan angka eror RMS yang cukup rendah yaitu 2.44% serta nilai R2 yang cukup tinggi yaitu 0.885 (Gambar 29). Sebagai perbandingannya adalah bahwa Jarungthammachote dan Dutta (2006) melakukan validasi model untuk gasifikasi limbah pertanian dengan eror RMS 0.7%, 3.65%, dan 2.845%. Selain itu, Vaezi et al (2008) juga melakukan validasi model untuk gasifikasi kayu dengan eror RMS 0.56%, 1.62%, 3.32%, dan 3.74% (adanya beberapa nilai eror RMS dari masing – masing peneliti karena validasi dilakukan terhadap beberapa literatur yang berbeda). Berdasarkan nilai eror RMS dan R2 dari validasi yang dilakukan, model dapat diterima untuk memprediksi komposisi gas hasil gasifikasi sabut kelapa.
0.00%
Komposisi gas hasil model (% volume)
Validasi
29 Simulasi
Gambar 30 hingga Gambar 36 menyajikan grafik hasil simulasi perubahan komposisi gas (% volume) yang dihasilkan terhadap perubahan kadar air basis basah sabut kelapa pada nilai equivalence ratio (ER) tertentu. Berdasarkan grafik, dapat diketahui bahwa persentase gas H2, dan CO2 meningkat jika kadar air sabut kelapa meningkat, persentase gas CO menurun jika kadar air sabut kelapa meningkat, serta persentase gas CH4 dan N2 relatif stabil tetapi sedikit meningkat untuk gas CH4 dan sedikit menurun untuk gas N2 jika kadar air sabut kelapa meningkat. Hal yang sama juga didapatkan dalam penelitian Zainal et al (2001), dan Jarungthammachote dan Dutta (2006).
Persentase gas H2 dan CO2 meningkat karena gas H2 dan CO2 dihasilkan dari reaksi antara air dengan gas CO (water-gas shift reaction), di mana pada saat yang bersamaan persentase gas CO menurun jika kadar air sabut kelapa meningkat. Persentase gas CH4 meningkat karena gas CH4 dihasilkan dari reaksi antara karbon dengan gas H2 (methanation reaction) sehingga jika persentase gas H2 meningkat maka persentase gas CH4 juga akan meningkat. Persentase gas N2 Tabel 10. Hasil ini menunjukkan bahwa pengaruh terbesar peningkatan kadar air sabut kelapa terjadi terhadap penurunan rata – rata persentase gas CO.
34
Gambar 38 hingga Gambar 44 menyajikan grafik hasil simulasi perubahan komposisi gas (% volume) yang dihasilkan terhadap perubahan equivalence ratio
(ER) pada kadar air (mc) tertentu. Berdasarkan grafik, dapat diketahui bahwa persentase gas mampu bakar, yaitu gas H2, gas CO, dan gas CH4 menurun jika nilai ER meningkat, persentase gas CO2 meningkat jika nilai ER meningkat dan persentase gas N2 meningkat jika nilai ER meningkat. Hal yang sama juga didapatkan dalam penelitian Ramanan et al (2008) dan Pitchandi (2012).
Hal ini karena meningkatnya nilai ER akan menyebabkan lebih banyak reaksi oksidasi yang terjadi terhadap sabut kelapa sehingga sabut kelapa lebih banyak terkonversi menjadi gas CO2 dan H2O di zona oksidasi. Pada range ER 0.15 – 0.45 untuk setiap kenaikan 0.5 nilai ER, penurunan rata – rata persentase gas H2, CO, dan CH4, serta peningkatan rata – rata persentase gas CO2 dan N2 berturut – turut adalah 2.03%, 2.31%, 0.68%, 0.52%, dan 4.56%, seperti yang disajikan pada Tabel 12. Hasil ini menujukkan bahwa pengaruh terbesar peningkatan ER terjadi terhadap gas CO untuk kelompok gas mampu bakar, dan gas N2 untuk keseluruhan gas. Persentase gas CO lebih besar dari gas CO2 pada ER kurang dari 0.45 untuk kadar air sabut kelapa di bawah 15%. Pada kadar air sabut kelapa 20% persentase gas CO lebih besar dari gas CO2 terjadi pada ER kurang dari 0.40, pada kadar air 25% persentase gas CO lebih besar dari gas CO2 terjadi pada ER kurang dari 0.35, pada kadar air 30% persentase gas CO lebih besar dari gas CO2 terjadi pada ER kurang dari 0.30, dan pada kadar air 35% persentase gas CO lebih besar dari gas CO2 terjadi pada ER kurang dari 0.20.
Gambar 45 menyajikan pengaruh ER terhadap suhu gasifikasi. Peningkatan nilai ER akan menyebabkan peningkatan suhu gasifikasi yang terjadi. Hal ini karena proses oksidasi akan lebih sempurna dan lebih banyak sabut kelapa yang dioksidasi seiring dengan meningkatnya nilai ER, sehingga lebih banyak panas yang dihasilkan. Suhu tertinggi yang dapat dicapai pada ER 0.15 adalah sekitar 721 K (448 oC). Hal ini dikhawatirkan suhu gasifikasi tidak tercapai. Suhu gasifikasi dapat tercapai pada ER di atas 0.2. Pada range ER 0.15 – 0.45 untuk setiap kenaikan 0.5 nilai ER, peningkatan rata – rata suhu adalah 165.74 K, seperti yang disajikan pada Tabel 11.
35 Tabel 11 Pengaruh peningkatan ER terhadap perubahan rata - rata komposisi gas
dan suhu
36
Gambar 38 Pengaruh equivalence ratio (ER) terhadap komposisi gas pada kadar air (mc) 10%
37
Gambar 40 Pengaruh equivalence ratio (ER) terhadap komposisi gas pada kadar air (mc) 20%
38
Gambar 42 Pengaruh equivalence ratio (ER) terhadap komposisi gas pada kadar air (mc) 30%
39
Gambar 44 Pengaruh equivalence ratio (ER) terhadap suhu gasifikasi pada berbagai tingkat kadar air (mc)
SIMPULAN DAN SARAN
Simpulan
Model kesetimbangan termodinamika dan simulasi numerik proses gasifikasi sabut kelapa telah berhasil dibuat untuk memprediksi kinerja reaktor gasifikasi sabut kelapa tipe downdraft. Hasil validasi menunjukkan bahwa hasil model cukup dekat dengan hasil percobaan. Hal ini dibuktikan dengan nilai eror RMS yang rendah (2.44%) dan nilai R2 yang tinggi (0.885). Hasil simulasi menunjukkan bahwa pada peningkatan kadar air setiap 5% rata - rata akan terjadi peningkatan persentase gas H2 0.67%, CO2 0.79%, dan CH4 0.04%, dan penurunan suhu 68.62 K, persentase gas CO 2.00%, dan N2 0.33%. Hasil simulasi juga menunjukkan bahwa pada peningkatan ER setiap 0.05 rata - rata akan terjadi penurunan persentase gas H2 2.03%, CO 2.31%, dan CH4 0.68%, dan peningkatan suhu 165.74 K, persentase gas CO2 0.52%, dan N2 4.56%. Dengan demikian, peningkatan kadar air sabut kelapa akan menurunkan suhu gasifikasi dan konsentrasi gas CO tetapi menaikkan konsentrasi gas H2 dan CH4, dan peningkatan laju aliran udara akan menaikkan suhu gasifikasi yang terjadi dan menurunkan konsentrasi gas – gas mampu bakar, yaitu H2, CO, dan CH4. Kualitas gas mampu bakar terbaik dari proses gasifikasi sabut kelapa berdasarkan hasil simulasi adalah kadar air sabut kelapa harus serendah mungkin dengan nilai
equivalence ratio 0.20 karena suhu gasifikasi dapat tercapai dan komposisi gas
yang dihasilkan baik. Nilai equivalenceratio dapat diambil lebih tinggi jika terjadi kehilangan cukup banyak panas dari reaktor gasifikasi.
40
Saran
Saran untuk penelitian berikutnya adalah perlu penelitian lebih lanjut tentang pengukuran laju aliran gas yang dihasilkan agar diketahui laju dan lower heating
value (LHV) gas mampu bakar yang dihasilkan. Selain itu, diberikan adanya
sistem insulasi pada reaktor gasifikasi agar tidak terlalu banyak panas yang hilang dan keluar ke lingkungan, serta titik - titik pengukuran suhu perlu diperbanyak agar lebih dapat mewakili secara keseluruhan suhu pada zona gasifikasi, khususnya zona oksidasi dan reduksi.
DAFTAR PUSTAKA
Gaos YS. 2008. Gasifikasi biomassa untuk pembangkit listrik dan pemanfaatan gas buang sebagai pemasok panas bagi pendingin adsorpsi [disertasi]. Bogor (ID): Institut Pertanian Bogor.
Gunarathne D. 2012. Optimization of the performance of downdraft biomass gasifier installed at National Engineering Research & Development (NERD) Center of Srilangka [thesis]. Stockholm (SE): KTH School of Industrial Engineering and Management.
Jarungthammachote S, Dutta A. 2006. Thermodynamic equilibrium model and second law analysis of a downdraft waste gasifier. Energy. 32(9): 1660 - 1669
Kumar SS, Pitchandi K, Natarajan E. 2008. Modeling and simulation of downdraft wood gasifier. Journal of Applied Science. 8(2): 271 – 279. Mhilu, CF. 2012. Modelling performance of high - temperature biomass
gasification process. International Scholarly Research Network. Doi: 10.5402/2012/437186.
Pitchandi K. 2012. Analysis of biomass based downdraft gasifier using equilibrium model. International Journal of Mechanical Engineering.1 (1): 26 – 34.
Rajvanshi AK. 1986. Biomass gasification. Alternative Energy in Agriculture. 2: 83 – 102.
Ramanan MV, Lakshmanan E, Sethumadhavan R, Renganarayanan S. 2008. Performance prediction and validation of equilibrium modeling for gasification of cashew nut shell char. Brazilian Journal of Chemical
Engineering. 25(03): 585 – 601.
Raveendran K, Ganesh A, Khilart KC. 1995. Influence of mineral matter on biomass pyrolysis characteristic. Fuel. 74 (12): 1812 – 1822.
Reed TB, Das A. 1988. Handbook of Biomass Downdraft Gasifier Engine
41 Surjosatyo A, Vidian F. 2012. Tar content evaluation of produced gas in
downdraft biomass gasifier. Iranica Journal of Energy & Environment. 3 (3): 210 – 212. Doi: 10.5829/idosi.ijee.2012.03.03.1588.
Syed S, Janajreh I, Ghenai C. 2012. Thermodynamics equilibrium analysis within the entrained flow gasifier environment. International Journal of Thermal
& Environmental Engineering. 4(1): 47 – 54.
Tooy D, Nelwan LO, Longdong IA. Gaos YS. 2013. Pengembangan Pembangkit Listrik Gasifikasi Skala Kecil dengan Bahan Baku Sabut Kelapa di Kabupaten Minahasa Utara, Provinsi Sulawesi Utara. Laporan Program
Hi-Link Universitas Sam Ratulangi.
Vaezi M, Passandideh-Fard M, Moghiman M, Charmchi M. 2008. Modelling biomass gasification: A new approach to utilize renewable sources of energy. Di dalam: Vaezi M, editor. International Mechanical Engineering
Congress and Exposition; 2008 Okt 31 – Nov 6; Boston, Massachussetts,
Amerika Serikat. Boston (US): IMECE. hlm 1 – 9.
Zainal ZA, Ali R, Lean CH, Seetharamu KN. 2001. Prediction of performance of a downdraft gasifier using equilibrium modeling for different biomass materials. Energy Conversion and Management. 42(12): 1499-1515.
LAMPIRAN
Lampiran 1 Pemrograman untuk simulasi numerik menggunakan Microsoft
Office Excel dengan developer Visual Basic
Public x(10) Public A(10, 10) Function k1(T)
k1 = Exp(((((393.5 + (-1.949 * (10 ^ -2)) * T * Log(T) + (3.122 * (10 ^ -5)) * (T ^ 2) + (-2.448 * (10 ^ -8) / 2) * (T ^ 3) + (6.946 * (10 ^ -12) / 3) * (T ^ 4) - (-4.891 * (10 ^ 2) / (2 * T)) - 5.27 - (-1.207 * (10 ^ -1) * T))) + ((-110.5 - 5.619 * (10 ^ -3) * T * Log(T) - 1.19 * (10 ^ -5)) * (T ^ 2) - (6.383 * (10 ^ -9) / 2) * (T ^ 3) - (-1.846 * (10 ^ -12) / 3) * (T ^ 4) + (-4.891 * (10 ^ 2)) / (2 * T) + 8.684 * (10 ^ (-1)) + -6.131 * (10 ^ -2) * T)) + ((-241.8 - (-8.95 * (10 ^ -3)) * T * Log(T) - (-3.672 * (10 ^ -6)) * (T ^ 2) - (5.209 * (10 ^ -9) / 2) * (T ^ 3) - (-1.478 * (10 ^ -12) / 3) * (T ^ 4) + (0 * (10 ^ 2)) / (2 * T) + 2.868 + -1.722 * (10 ^ -2) * T)))) / (8.314 * T)) End Function
Function k2(T)
42
Sub palingbarubuatvalidasi() m = Sheet37.Cells(13, 14) T = Sheet37.Cells(1, 14) x1 = Sheet37.Cells(2, 14) x2 = Sheet37.Cells(3, 14) x3 = Sheet37.Cells(4, 14) x4 = Sheet37.Cells(2, 12) x5 = Sheet37.Cells(3, 12) p = Sheet37.Cells(5, 14) q = Sheet37.Cells(6, 14) r = Sheet37.Cells(7, 14) mc = Sheet37.Cells(8, 14) C = Sheet37.Cells(9, 14) H = Sheet37.Cells(10, 14) O = Sheet37.Cells(11, 14) N = Sheet37.Cells(12, 14)
HHV = 418920 + 117830 * p - 166880 * q hfbiomass = HHV - (p / 2) * 285830 - 393546 10
Sheet37.Cells(14, 20) = mc
wt = (12 + p * 1 + q * 16 + r * 14) * mc / (18 * (1 - mc)) f1 = x2 + x3 + x5 - 1
f2 = 2 * x1 + 2 * x4 + 4 * x5 - p - 2 * wt f3 = x2 + 2 * x3 + x4 - wt - 2 * m - q f4 = k1(T) * x2 * x4 - x3 * x1
f5 = k2(T) * (x1 ^ 2) - x5 * (x1 + x2 + x3 + x4 + x5 + r / 2 + 3.76 * m) df1x1 = 0
46
bCO + x3 * bCO2 + x4 * bH2O + x5 * bCH4 + (r / 2 + 3.76 * m) * bN2) * ((T - 298) ^ 2) + (x1 * cH2 + x2 * cCO + x3 * cCO2 + x4 * cH2O + x5 * cCH4 + (r / 2 + 3.76 * m) * cN2) * ((T - 298) ^ 3) + (x1 * dH2 + x2 * dCO + x3 * dCO2 + x4 * dH2O + x5 * dCH4 + (r / 2 + 3.76 * m) * dN2) * ((T - 298) ^ 4)
faksen = (x1 * aH2 + x2 * aCO + x3 * aCO2 + x4 * aH2O + x5 * aCH4 + (r / 2 + 3.76 * m) * aN2) + 2 * (x1 * bH2 + x2 * bCO + x3 * bCO2 + x4 * bH2O + x5 * bCH4 + (r / 2 + 3.76 * m) * bN2) * ((T - 298)) + 3 * (x1 * cH2 + x2 * cCO + x3 * cCO2 + x4 * cH2O + x5 * cCH4 + (r / 2 + 3.76 * m) * cN2) * ((T - 298) ^ 2) + 4 * (x1 * dH2 + x2 * dCO + x3 * dCO2 + x4 * dH2O + x5 * dCH4 + (r / 2 + 3.76 * m) * dN2) * ((T - 298) ^ 3)
Tbaru = T - f / faksen T = Tbaru
If Abs(f / faksen) > 0.00001 Then GoTo 20 Tnplus1 = T
Sheet37.Cells(21, 20) = T
If Abs(Tnplus1 - Tlama) > 0.01 Then GoTo 10 Else GoTo 200 200
End Sub Sub Gauss() Dim BB(10) N = 6
' For i = 1 To N - 1 ' Masukkan b(i) sebagai A(i,N) ' A(i, N) = Sheet1.Cells(i + 1, 7)
' sdf = sdf 'Next i 'sdf = sdf 'Elimination
For k = 1 To N - 1 For i = k + 1 To N If A(k, k) = 0 Then For m = k + 1 To N If A(m, k) <> 0 Then
For S = 1 To N ' Menukar baris BB(S) = A(m, S)
47 End If
Next m: 'GoTo 100 Else
5
koef = A(i, k) / A(k, k) sdf = sdf
End If
For L = k To N ' Untuk seluruh kolom pada baris p A(i, L) = A(i, L) - koef * A(k, L)
Next L Next i Next k
'Backward Substitution 'N = 7
x(N) = 0
For j = 1 To N ' menolkan X(t) x(j) = 0
Next j
For j = N - 1 To 1 Step -1 Suma = 0
For L = N To j Step -1
Suma = Suma + A(j, L) * x(L) Next L
x(j) = 1 / A(j, j) * (A(j, N) - Suma) Next j
sdf = sdf GoTo 200 100
Form1.Print "Matriks tak terselesaikan" 200
48
Lampiran 2 Data komposisi gas
Data 1 Data 2 Data 3
Waktu (detik ke -)
Komposisi (%) Waktu
(detik ke -)
Komposisi (%) Waktu (detik ke -)
Komposisi (%)
CO CO2 CH4 CO CO2 CH4 CO CO2 CH4
5 16.33 16.40 2.07 5 15.98 16.61 1.45 5 11.69 16.66 1.03 10 16.33 16.41 2.07 10 15.93 16.61 1.45 10 11.64 16.66 1.03 15 16.33 16.43 2.07 15 15.88 16.61 1.44 15 11.61 16.66 1.02 20 16.33 16.44 2.06 20 15.83 16.61 1.44 20 11.56 16.67 1.02 25 16.33 16.46 2.05 25 15.80 16.61 1.43 25 11.53 16.67 1.01 30 16.33 16.46 2.04 30 15.76 16.61 1.43 30 11.50 16.68 1.01 35 16.33 16.47 2.04 35 15.69 16.61 1.42 35 11.47 16.68 1.00 40 16.33 16.47 2.03 40 15.64 16.61 1.42 40 11.45 16.69 1.00 45 16.33 16.48 2.02 45 15.59 16.61 1.41 45 11.43 16.69 0.99 50 16.33 16.49 2.01 50 15.53 16.61 1.41 50 11.42 16.69 0.99 55 16.33 16.49 2.00 55 15.48 16.61 1.41 55 11.41 16.69 0.98 60 16.33 16.49 1.99 60 15.44 16.61 1.40 60 11.41 16.69 0.98 65 16.33 16.49 1.97 65 15.38 16.60 1.40 65 11.41 16.69 0.98 70 16.33 16.49 1.96 70 15.32 16.60 1.39 70 11.42 16.70 0.97 75 16.33 16.49 1.95 75 15.23 16.60 1.39 75 11.43 16.70 0.97 80 16.33 16.49 1.94 80 15.16 16.59 1.38 80 11.45 16.70 0.97 85 16.33 16.49 1.92 85 15.10 16.59 1.38 85 11.46 16.70 0.97 90 16.33 16.49 1.91 90 15.00 16.59 1.38 90 11.48 16.71 0.97