POTENSI KULIT BUAH LANGSAT (
Lansium domesticum
)
SEBAGAI ANTIBAKTERI
LEONITA SEJATI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
PERNYATAAN MENGENAI SKRIPSI DAN SUMBER
INFORMASI SERTA PELIMPAHAN HAK CIPTA
Dengan ini saya menyatakan bahwa skripsi Potensi Kulit Buah Langsat (Lansium domesticum) sebagai Antibakteri adalah karya saya dengan arahan dari komisi pembimbing dan belum diajukan dalam bentuk apapun kepada perguruan tinggi manapun. Sumber informasi yang berasal atau dikutip dari karya yang diterbitkan maupun tidak diterbitkan dari penulis lain telah disebutkan dalam teks dan dicantumkan dalam Daftar Pustaka di bagian akhir skripsi ini.
Dengan ini saya melimpahkan hak cipta dari karya tulis kepada Institut Pertanian Bogor.
Bogor, Desember 2013
Leonita Sejati
ABSTRAK
LEONITA SEJATI. Potensi Kulit Buah Langsat (Lansium domesticum) sebagai Antibakteri. Dibimbing oleh IRMA HERAWATI SUPARTO dan TUN TEDJA IRAWADI.
Kulit buah langsat (Lansium domesticum) diketahui memiliki potensi sebagai antibakteri. Penelitian ini bertujuan menentukan senyawa metabolit yang memiliki aktivitas antibakteri pada ekstrak kulit buah langsat. Sampel dimaserasi dengan pelarut etanol 70% dan etil asetat. Aktivitas antibakteri diuji terhadap
Staphylococcus aureus menggunakan metode dilusi. Hasil uji menunjukkan
bahwa ekstrak teraktif adalah ekstrak etanol 70% dengan nilai konsentrasi hambat minimum (KHM) dan nilai konsentrasi bunuh minimum (KBM) sebesar 1.00 mg/mL. Fraksionasi ekstrak etanol 70% menggunakan kromatografi kolom dengan elusi gradien menghasilkan 12 fraksi untuk eluen heksana:asetat dan 9 fraksi untuk eluen etil asetat:metanol. F29 merupakan fraksi teraktif dengan KHM dan KBM 0.50 dan 2.00 mg/mL. Berdasarkan identifikasi menggunakan spektrofotometer inframerah diduga senyawa metabolitnya adalah flavonoid.
Kata kunci : Antibakteri, flavonoid, fraksi, kulit buah langsat
ABSTRACT
LEONITA SEJATI. Potency of Langsat Fruit Peel (Lansium domesticum) as Antibacterial Agent. Supervised by IRMA HERAWATI SUPARTO and TUN TEDJA IRAWADI.
The fruit peels of langsat (Lansium domesticum) have antibacterial activities. However, the active compounds responsible for the activities have not been studied. Therefore, this research was aimed to determine the metabolite compounds with antibacterial activity in the fruit peel of langsat. Some samples was macerated using ethanol 70% and further fractionated using column chromatography with gradient elution from non-polar to polar solvent. Antibacterial activity was tested to Staphylococcus aureus using dilution method. Antibacterial test results showed that the most active extracts was ethanol 70% extract with minimum inhibitory concentration (MIC) and minimum bactericidal concentration (MBC) of 1.00 mg/mL. Fractionation using hexane:ethyl acetate gave 12 fractions and 9 fractions for ethyl acetate:methanol. The most active fraction was F29 with MIC and MBC of 0.5 mg/mL and 2.00 mg/mL, respectively. Based on identification using Fourier transform infrared spectrophotometers, the predicted active compound was flavonoids.
POTENSI KULIT BUAH LANGSAT (
Lansium domesticum
)
SEBAGAI ANTIBAKTERI
LEONITA SEJATI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains
Pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul Skripsi : Potensi Kulit Buah Langsat (Lansium domesticum) sebagai Antibakteri
Nama : Leonita Sejati NIM : G44090075
Disetujui oleh
Dr dr Irma Herawati Suparto,MS Prof Dr Ir Tun Tedja Irawadi,MS Pembimbing I Pembimbing II
Diketahui oleh
Prof Dr Dra Purwantiningsih Sugita, MS Ketua Departemen
PRAKATA
Puji dan syukur kehadirat Allah SWT karena atas rahmat dan karunia-Nya yang berlimpah penulis dapat menyelesaikan laporan hasil penelitian yang berjudul Potensi Kulit Buah Langsat (Lansium domesticum) sebagai Antibakteri merupakan salah satu syarat untuk memperoleh gelar Sarjana Sains pada Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Penulis ingin menyampaikan ucapan terimakasih kepada Dr dr Irma Herawati Suparto, MS dan Prof Dr Ir Tun Tedja Irawadi, MS selaku pembimbing atas bimbingan dan dukungan yang telah diberikan. Ucapan terima kasih juga penulis sampaikan kepada orang tua dan kakak atas doa dan dukungannya baik secara moril dan materil yang menjadi motivasi penulis dalam menyelesaikan karya ilmiah ini. Juga terima kasih disampaikan kepada pihak-pihak yang telah membantu penulis selama penelitian, yaitu teman satu penelitian Syifa, pihak Laboratorium Kimia Anorganik, antara lain Bapak Syawal, Bapak Sunarsa, Bapak Mulyadi dan teman-teman penelitian di Laboratorium Kimia Anorganik, pihak Laboratorium Kimia Organik, antara lain Bapak Sabur, Ibu Yenni, Mbak Nia dan teman-teman penelitian di Laboratorium Kimia Organik, pihak dari komdik, serta teman-teman kimia angkatan 46 atas semangat dan kebersamaannya.
Semoga laporan hasil penelitian ini dapat bermanfaat.
Bogor, Desember 2013
DAFTAR ISI
DAFTAR TABEL vii
DAFTAR GAMBAR vii
DAFTAR LAMPIRAN vii
PENDAHULUAN 1
Latar Belakang 1
METODE 2
Waktu dan Tempat Pelaksanaan 2
Alat dan Bahan 2
Prosedur 2
Penentuan Kadar Air 2
Ekstraksi Kulit Buah Langsat 2
Penentuan Kandungan Fitokimia 3
Pemilihan Eluen Terbaik 3
Pemisahan dengan Kromatografi Kolom 4
Uji Aktivitas Antibakteri 4
Identitas Senyawa 4
HASIL DAN PEMBAHASAN 5
Kadar Air 5
Ekstraksi 5
Fitokimia Ekstrak 6
Penentuan Eluen Terbaik 6
Fraksionasi dengan Kromatografi Kolom 7
Aktivitas Antibakteri 8
Identitas Senyawa 10
SIMPULAN DAN SARAN 10
Simpulan 10
Saran 11
DAFTAR PUSTAKA 11
LAMPIRAN 13
DAFTAR TABEL
1 Rendemen ekstrak kulit buah langsat 5
2 Hasil uji fitokimia ekstrak kulit buah langsat 6 3 Aktivitas antibakteri ekstrak kulit buah langsat 8 4 Aktivitas antibakteri hasil fraksionasi ekstrak etanol 70% 10
DAFTAR LAMPIRAN
1 Diagram alir penelitian 13
2 Perhitungan kadar air bubuk kulit buah langsat 14 3 Perhitungan rendemen ekstrak kulit buah langsat 14 4 Kromatogram ekstrak etanol 70% dengan eluen tunggal pada λ 254 nm 15 5 Kromatogram fraksi gabungan hasil fraksionasi ekstrak etanol 70% 16 eluen heksana:etil asetat
6 Kromatogram fraksi gabungan hasil fraksionasi ekstrak etanol 70% 16 eluen etil asetat:metanol
7 Hasil pemisahan ekstrak etanol 70% dengan kromatografi kolom 17 dari fraksi gabungan
8 Spektrum IR pada F29 18
PENDAHULUAN
Latar Belakang
Indonesia merupakan negara tropis yang memiliki ketersediaan sumber daya alam hayati yang melimpah. Sejak dahulu secara turun-temurun masyarakat Indonesia telah memanfaatkan tanaman yang ada di alam untuk memenuhi berbagai kebutuhan hidup. Salah satunya pemanfaatan tanaman sebagai obat-obatan, yaitu untuk penyakit infeksi yang disebabkan oleh mikroorganisme seperti bakteri, virus, dan jamur. Mikroorganisme tersebut merupakan penyebab penyakit pada manusia terutama di daerah tropis dengan menyebabkan infeksi yang mengganggu berbagai fungsi tubuh. Meskipun adanya keberadaan agen antibiotik, akan tetapi resistensi terhadap mikroorganisme tersebut terus muncul sehingga perlu adanya penelitian berkelanjutan dan pengembangan obat baru.
Antibiotik merupakan substansi atau zat yang bisa membunuh atau melemahkan mikroorganisme jasad renik seperti bakteri. Antibiotik yang diperuntukkan dalam penanganan infeksi bakteri disebut antibakteri. Usaha pengobatan terhadap infeksi bakteri patogen menggunakan obat tradisional juga telah banyak dilaporkan ( Hasnawati dan Prawita 2010, Lense 2011).
Salah satu tumbuhan yang diketahui mempunyai potensi sebagai antibakteri adalah kulit buah langsat (Lansium domesticum). Langsat berkhasiat sebagai obat cacing, demam, dan diare serta kulit buahnya dapat digunakan sebagai penolak nyamuk (Korompis et al. 2010). Selain itu, kulit batang langsat juga memiliki aktivitas antioksidan dan antikanker (Semuel 2008), bijinya digunakan sebagai antimalaria (Saewan 2006), serta daunnya sebagai antifeedant (Omar et al. 2007).
Khasiat ekstrak kulit buah langsat berdasarkan hasil penelitian Lawalata (2012), bahwa semua jenis ekstrak kasar kulit buah langsat dari pelarut heksana, etil asetat, dan etanol dengan berbagai konsentrasi mempunyai kemampuan untuk menghambat bakteri Staphylococcus aureus dan Escherichia coli. Aktivitas tertinggi ekstrak etanol dibandingkan ekstrak lainnya. Nilai Konsentrasi Hambat Minimum (KHM) dan Konsentrasi Bunuh Minimum (KBM) pada bakteri S. aureus lebih baik daripada bakteri E. coli terhadap ekstrak etanol kulit buah langsat. Korompis et al. (2010) melaporkan bahwa ekstrak kulit buah, kulit kayu, dan biji buah langsat memiliki aktivitas antibakteri terhadap Salmonella typhii, E. coli, Vibrio cholera, dan S. aureus. Dong et al. (2011) juga melaporkan ekstraksi kulit buah langsat menggunakan pelarut etanol yang memiliki aktivitas antibakteri terhadap bakteri gram positif.
2
METODE
Waktu dan Tempat Pelaksanaan
Penelitian dilakukan di Laboratorim Kimia Anorganik, Kimia Organik, Departemen Kimia, Institut Pertanian Bogor, Pusat Studi Biofarmaka dan Laboratorium Terpadu, Institut Pertanian Bogor. Penelitian dilakukan dari bulan April hingga September 2013.
Alat dan bahan
Bahan utama yang digunakan dalam penelitian ini adalah serbuk kulit buah langsat (Lansium domesticum) yang diperoleh dari Kabupaten Mamuju Provinsi Sulawesi Barat (sumber dari Dr Lawalata). Bahan kimia untuk ekstraksi terdiri dari etil asetat dan etanol serta pelarut organik. Bakteri uji S. aureus, media
Tryticase Soy Broth (TSB), kloramfenikol, dimetil sulfida (DMSO), pereaksi untuk uji fitokimia, dan silika gel 60 untuk kolom.
Peralatan yang digunakan dalam penelitian ini meliputi seperangkat alat gelas, rotavapor, spektrofotometer infra merah, pelat kromatografi lapis tipis (KLT), plastik silika gel 60 F254 dari Merck, vial, mikropipet, kromatografi kolom,
lampu UV, autoklaf, inkubator, 96 well plates, dan neraca analitik.
Prosedur
Metode penelitian yang dilakukan meliputi beberapa tahap, yaitu penentuan kadar air, ekstraksi kulit buah langsat, uji fitokimia, penentuan eluen terbaik, pemisahan ekstrak aktif dengan kromatografi kolom, uji aktivitas antibakteri serta pencirian senyawa dengan spektrofotometer infra merah (Lampiran 1).
Penentuan Kadar Air (AOAC 2005)
Wadah kosong dikeringkan di dalam oven pada suhu 105 oC selama 3 jam, kemudian didinginkan di dalam eksikator dan ditimbang bobotnya. Sebanyak 3 g sampel ditimbang di dalam wadah yang telah diketahui bobotnya, kemudian dikeringkan di dalam oven suhu 105 oC selama 3 jam.Wadah berisi sampel didinginkan di dalam desikator dan ditimbang bobotnya. Proses pengeringan dilakukan hingga bobot konstan.
Kadar air = W 1−W 2
W 1 x 100%
W1 = bobot sampel sebelum pengeringan (g) W2 = bobot sampel setelah pengeringan (g)
Ekstraksi Kulit Buah Langsat
dilakukan selama 24 jam. Ekstrak disaring lalu ampasnya dimaserasi kembali sebanyak 3 kali. Lalu filtrat dipekatkan dengan rotavapor.
Penentuan Kandungan Fitokimia (Harborne 1987)
Penentuan kandungan fitokimia secara kualitatif dilakukan untuk mengetahui ada tidaknya golongan senyawa aktif yang terdapat pada simplisia dan ekstrak kulit buah langsat, meliputi tanin, flavonoid, saponin, alkaloid, triterpenoid, dan steroid.
Uji tanin. Sebanyak 0.1 g ekstrak ditambahkan 10 mL akuades panas kemudian disaring. Filtrat kemudian ditambahkan 1 tetes FeCl3 1 %. Sampel yang
positif mengandung tanin ditandai dengan terbentuk warna hijau, biru tua atau hitam.
Uji Flavonoid. Sebanyak 0.1 g ekstrak ditambahkan 10 mL akuades panas. Setelah larut sempurna, campuran tersebut disaring kemudian ditambahkan serbuk Mg 0.5 g, 1 mL HCl pekat, dan 1 mL amil alkohol. Campuran tersebut kemudian dikocok. Sampel yang positif akan terbentuk warna kuning, merah atau jingga pada lapisan amil alkohol.
Uji saponin. Sebanyak 0.1 g ekstrak ditambahkan 10 mL akuades panas, kemudian didihkan selama beberapa menit, lalu disaring. Filtrat hasil penyaringan dikocok kuat selama 10 menit. Sampel yang positif akan memunculkan busa yang stabil.
Uji alkaloid. Sebanyak 0.1 g ekstrak dilarutkan dalam 10 mL kloroform, kemudian ditambahkan beberapa tetes NH4OH. Setelah itu campuran disaring.
Filtrat ditambahkan 10 tetes H2SO4, kemudian dikocok hingga membentuk dua
lapisan. Lapisan asam dipisahkan kemudian diuji dengan penambahan perekasi Dragendroff, Mayer, dan Wagner. Sampel positif mengandung alkaloid, jika berturut-turut akan membentuk endapan jingga (pereaksi Dragendorf), putih (pereaksi Mayer), dan cokelat (pereaksi Wagner).
Uji triterpenoid dan steroid. Sebanyak 0.1 g ekstrak dilarutkan dalam 25 mL etanol panas. Setelah larut sempurna, campuran disaring. Filtrat hasil penyaringan kemudian diuapkan sampai kering. Sampel kering kemudian dilarutkan dalam eter sampai larut sempurna dan selanjutnya ditambahkan 3 tetes pereaksi Lieberman-Buchard. Sampel yang positif mengandung senyawa triterpenoid apabila setelah penetesan pereaksi tersebut terbentuk warna merah atau ungu. Sampel yang positif senyawa steroid bila terbentuk warna hijau atau biru.
Pemilihan Eluen Terbaik (Houghton dan Raman 1998)
Eluen terbaik ditentukan pada ekstrak dengan aktivitas antibakteri terbaik. Ekstrak aktif ditotolkan pada pelat KLT selanjutnya dikeringudarakan. Pelat yang sudah kering dimasukkan ke dalam chamber kromatografi berisi eluen yang telah dijenuhkan. Mula-mula digunakan eluen tunggal. Eluen-eluen yang digunakan adalah diklorometana, metanol, etanol, n-heksana, kloroform, dietileter, etil asetat, dan aseton. Setelah proses elusi selesai, pemisahan pada pelat KLT dilihat di bawah paparan UV pada panjang gelombang 254 nm dan 366 nm. Eluen terbaik adalah eluen yang dapat mengelusi sampel hingga menghasilkan banyak spot
4
yang memenuhi kriteria tersebut, maka eluen-eluen tersebut dicampurkan dengan nisbah-nisbah tertentu.
Pemisahan dengan Kromatografi Kolom
Kolom yang digunakan berdiameter 2.5 cm dengan fase diam silika gel 60 dari Merck dan fase gerak n-heksana, etil asetat serta metanol yang digunakan secara gradien dengan nisbah tertentu. Sebanyak 60 g fase diam dikemas dengan n-heksana selama semalam. Ekstrak aktif ditimbang 0.9 g, dimasukkan ke dalam kolom, kemudian dialiri dengan pelarut gradien secara kontinu. Eluat ditampung setiap 1 mL/menit selama 5 menit. Hasil koleksi tampungan diuji dengan KLT menggunakan eluen terbaik dan dideteksi pada lampu UV panjang gelombang 254 dan 366 nm. Elusi dilakukan dengan menggunakan campuran eluen heksana:etil asetat yang meningkat kepolarannya dengan nisbah (10:1), (9:1), (8:2), (7:3),
Uji Aktivitas Antibakteri (Batubara et al. 2009)
Bakteri uji adalah S. aureus dengan medium Tryticase Soy Broth (TSB). Sebanyak 100 µL medium steril dan 40 µL sampel dilarutkan dalam DMSO 20% atau kontrol, serta 5 µL inokulum bakteri dimasukkan ke dalam masing-masing sumur (96-well-plate). Inokulum yang telah disiapkan pada konsentrasi 10-2 CFU/mL. Bakteri diinkubasi dalam medium selama 24 jam pada suhu 37 °C. Konsentrasi sampel yang tidak menunjukkan pertumbuhan bakteri (bening) secara visual dideskripsikan sebagai konsentrasi hambat minimum (KHM).
Sebanyak 10 µL dari medium yang tidak menunjukkan pertumbuhan bakteri diinokulasikan pada 100 µL medium baru dan diinkubasi selama 24 jam pada suhu 37 °C. Konsentrasi yang tidak menunjukkan pertumbuhan bakteri setelah inokulasi kedua dideskripsikan sebagai konsentrasi bunuh minimum (KBM). Kontrol negatif yang digunakan adalah DMSO 20% dan kontrol positifnya adalah kloramfenikol.
Identifikasi Senyawa
tersebut diletakkan dalam wadah sampel spektorfotometer infra merah. Selanjutnya wadah sampel diletakkan dalam kompartemen sampel dan dilakukan pembacaan spektrum yang dimiliki sampel. Spektrum sampel yang diperoleh dibandingkan dengan database untuk mengetahui jenis gugus fungsi sampel tersebut.
HASIL DAN PEMBAHASAN
Kadar Air
Hasil penentuan kadar air menunjukkan bahwa kadar air serbuk kulit buah langsat (Lansium domesticum) adalah 13.35% (Lampiran 2). Penentuan kadar air suatu bahan berhubungan dengan indeks kestabilan khususnya saat penyimpanan serta koreksi rendemen keringnya. Simplisia yang disimpan dengan kadar air diatas 10% akan cepat rusak, karena berpeluang sebagai tempat hidup dan berkembangnya mikroorganisme (Depkes 2000). Simplisia ini berpotensi terkontaminasi mikroorganisme sehingga dilakukan penyimpanan yang baik agar dapat meminimalisir kontaminasi kapang ataupun bakteri. Penelitian Lawalata (2012), kadar air kulit buah langsat yang diperoleh adalah 8.06%. Perbedaan kadar air ini dapat disebabkan sampel yang digunakan telah disimpan dalam jangka waktu kurang lebih 6 bulan walaupun disimpan pada suhu 5-10 oC.
Ekstraksi
Metode ekstraksi yang digunakan adalah maserasi. Teknik ekstraksi maserasi dipilih karena sederhana tanpa pemanasan untuk mencegah rusaknya komponen kimia yang tidak tahan panas. Rendemen ekstrak dari kulit buah langsat terlampir pada Tabel 1.
Tabel 1 Rendemen ekstrak kulit buah langsat
Pelarut Bobot sampel (g) Bobot ekstrak (g) Rendemen (%)
Etanol 70% 25.0077 8.5763 39.58
Etil asetat 25.0010 6.8858 31.79
6
Fitokimia Ekstrak
Uji fitokimia pada ekstrak kulit buah langsat dilakukan untuk memperkirakan kandungan metabolit sekunder pada sampel secara kualitatif (Harbone 1987) (Tabel 2).
Tabel 2 Hasil uji fitokimia ekstrak kulit buah langsat
Uji Simplisia Ekstrak etil asetat Ekstrak etanol 70%
Tanin +++ - +++
Keterangan : (-): tidak terdeteksi, (+): terdeteksi; (++): intensitasnya meningkat; (+++): intensitasnya paling tinggi
Penentuan kandungan metabolit ini berguna untuk memperkirakan metabolit sekunder yang berpengaruh pada bioaktivitas sebagai antibakteri serta penentuan senyawa aktifnya. Hasil uji fitokimia menunjukkan, simplisia kulit buah langsat dan etanol 70% mengandung tanin, flavonoid, triterpenoid, saponin, dan alkaloid dengan intensitas yang berbeda, sedangkan pelarut etil asetat mampu mengekstrak triterpenoid.
Uji fitokimia pada penelitian Lawalata (2012) menunjukkan bahwa pelarut etil asetat mampu mengekstrak senyawa yang bersifat nonpolar (steroid dan triterpenoid) dengan intensitas yang lebih banyak dan senyawa yang bersifat polar (flavonoid) dalam intensitas yang sedikit. Ekstrak etanol mampu mengekstrak senyawa yang bersifat polar (saponin, flavonoid, tanin) lebih banyak daripada senyawa nonpolar (triterpenoid).
Penentuan Eluen Terbaik
semipolar belum menghasilkan keterpisahan noda yang baik. Maka eluen yang dipilih sebagai eluen terbaik adalah n-heksana yang bersifat menahan komponen dan etil asetat yang menggerakkan komponen hingga batas garis pelarut dengan keterpisahan yang baik. Kromatogram pemisahan dengan eluen tunggal pada Lampiran 4.
Eluen n-heksana dan etil asetat kemudian dicampurkan dengan nisbah perbandingan n-heksana : etil asetat dengan elusi peningkatan kepolaran. Sampel yang ditotolkan pada fase diam (silika) akan terelusi dengan kecepatan yang bergantung pada sifat senyawa tersebut (kemampuan terikat pada fase diam dan kemampuan larut dalam fase gerak). Eluen campuran yang memberikan pemisahan yang baik ialah n-heksana : etil asetat (7:3). Eluen ini menghasilkan 3 noda dari ekstrak dengan keterpisahan yang baik pada KLT, yaitu di bagian bawah, tengah, dan atas. Eluen campuran n-heksana : etil asetat (3:7), (4:6), (6:4), dan (9:1) juga menghasilkan 3 noda tetapi keterpisahannya kurang baik karena tidak merata di sepanjang KLT (noda ada yang terpisah di bagian atas saja atau di bagian bawah saja). Eluen n-heksana:etil asetat (5:5) menghasilkan 2 noda pada bagian tengah dan atas. Selanjutnya eluen n-heksana:etil asetat (8:2) menghasilkan lebih banyak noda, yaitu 4 noda tetapi keterpisahannya kurang baik karena terpisah pada bagian bawah dan tengah. Kromatogram pemisahan ini dapat dilihat pada Gambar 1.
Gambar 1 Kromatogram ekstrak etanol 70% perbandingan eluen campuran heksana:etil asetat
Fraksionasi dengan Kromatografi Kolom
8
2:8, 1:9, dan diakhiri dengan metanol 100%. Penambahan metanol 100% dilakukan agar komponen-komponen paling polar dari ekstrak dapat terelusi karena kepolaran metanol lebih tinggi dibandingkan silika gel. Setelah penambahan metanol 100%, pita pada kolom dapat terelusi seluruhnya.
Hasil pemisahan ditampung pada tabung setiap 5 menit dengan kecepatan 1 tetes/detik dan diuji pola pemisahan noda pada plat KLT dengan menggunakan eluen terbaik n-heksana:etil asetat (7:3). Elusi dihentikan ketika tidak terdapat lagi noda pada KLT. Eluat yang memiliki pola pemisahan KLT yang sama digabungkan menjadi satu fraksi. Fraksi-fraksi yang telah digabungkan diuji kembali pemisahannya pada KLT sehingga diperoleh 12 fraksi untuk campuran eluen heksana:etil asetat (Lampiran 5) dan 9 fraksi untuk campuran eluen etil asetat:metanol (Lampiran 6). Rendemen dari fraksi yang diperoleh disampaikan pada Lampiran 7.
Aktivitas Antibakteri
Penentuan aktivitas antibakteri dilakukan dengan metode dilusi menggunakan medium steril TSB. Medium ini umum digunakan karena kaya akan nutrisi untuk pertumbuhan bakteri dan bakteri yang digunakan merupakan jenis gram positif. Metode dilusi memiliki keunggulan dibandingkan dengan metode difusi, diantaranya lebih peka, untuk mikrodilusi membutuhkan sampel relatif sedikit, serta mampu membedakan efek bakteriostatik dan bakteriosidal. Pada metode dilusi aktivitas ditentukan dengan melihat kekeruhan yang terjadi. Medium yang lebih jernih daripada sebelumnya menandakan aktivitas mikrob terhambat (Batubara et al. 2009).
Uji aktivitas antibakteri dilakukan untuk menentukan ekstrak teraktif serta ada tidaknya aktivitas antibakteri pada ekstrak kasar kulit buah langsat dengan pelarut etanol 70% dan etil asetat. Cara untuk mengetahui aktivitas penghambatan sampel terhadap pertumbuhan bakteri adalah dengan menentukan nilai konsentrasi hambat minimum (KHM) dan konsentrasi bunuh minimum (KBM). KHM adalah konsentrasi sampel yang menyebabkan pertumbuhan bakteri terhambat sedangkan KBM adalah konsentrasi sampel untuk membunuh bakteri. Hasil pengujian aktivitas antibakteri ekstrak kulit buah langsat disajikan pada Tabel 3.
Tabel 3 Aktivitas antibakteri ekstrak kulit buah langsat
Berdasarkan Tabel 3 terlihat bahwa ekstrak etanol 70% memiliki aktivitas antibakteri terbaik (KBM 1.00 mg/mL) dibandingkan ekstrak etil asetat. Kloramfenikol sebagai kontrol positif mampu menghambat bakteri S. aureus pada konsentrasi yang lebih rendah, yaitu 0.03 mg/mL dan mampu membunuh bakteri pada konsentrasi 0.06 mg/mL. Hal ini disebabkan karena kloramfenikol merupakan senyawa kimia sintesis yang mengandung senyawa tunggal, sehingga memiliki mekanisme penghambatan terhadap bakteri lebih spesifik (Lawalata
Sampel KHM (mg/mL) KBM (mg/mL)
Ekstrak etanol 70% 1.00 1.00
Ekstrak etil asetat 1.00 2.00
Kloramfenikol 0.03 0.06
2012). Antibiotik kloramfenikol menghambat pertumbuhan bakteri dengan menyerang sintesis protein. Kloramfenikol menghambat tahap elongasi dengan cara berikatan pada subunit ribosom 50S untuk mencegah sintesis protein sehingga menyebabkan kesalahan pembacaan kode oleh mRNA (Madigan et al.
2003). Larutan DMSO 20% sebagai blangko tidak memiliki aktivitas antibakteri. Hasil penelitian ini sejalan dengan penelitian Lawalata (2012) yang mendapatkan bahwa ekstrak etanol kulit buah langsat memiliki aktivitas antibakteri dengan daya hambat yang lebih besar pada bakteri S. aureus (3.44 – didapatkan dari penelitian sebelumnya lebih baik. Hal ini dapat disebabkan karena waktu penyimpanan dari sampel yang berpengaruh terhadap penurunan aktivitas antibakteri.
Penelitian antibakteri lainnya pada ekstrak etanol 50% kulit kayu ketapang menghasilkan KHM dan KBM sebesar 1 mg/mL dan 2 mg/mL terhadap bakteri
Propionibacterium acnes, serta pada ekstrak etanol 50% daun jambu biji menghasilkan nilai KHM dan KBM sebesar 1 mg/mL terhadap Propionibacterium acnes (Batubara et al. 2009). Hasil penelitian menunjukkan bahwa ekstrak etanol 70% pada kulit langsat berpotensi sebagai antibakteri, hal ini sesuai jika dibandingkan pada penelitian Batubara et al. 2009.
Kemampuan ekstrak etanol 70% kulit buah langsat dalam menghambat bakteri uji diduga terkandungnya beberapa metabolit sekunder yang bersifat antibakteri, antara lain saponin, flavonoid, tanin, dan terpenoid. Senyawa saponin merupakan zat aktif yang dapat meningkatkan permeabilitas membran, sehingga terjadi hemolisis sel. Senyawa flavonoid dapat berfungsi sebagai bahan antibakteri dengan membentuk ikatan kompleks dengan dinding sel bakteri dan merusak membran sel bakteri. Kemampuan tanin sebagai bahan antibakteri diduga karena tanin akan berikatan dengan dinding sel bakteri, sehingga akan inaktivasi kemampuan menempel bakteri dan menghambat pertumbuhan bakteri. Mekanisme penghambatan pertumbuhan bakteri oleh senyawa terpenoid diduga bereaksi dengan porin pada membran luar dinding sel bakteri sehingga mengakibatkan rusaknya porin. Porin merupakan pintu keluar masuknya substansi, dengan rusaknya porin, mengakibatkan sel bakteri kekurangan nutrisi sehingga pertumbuhan bakteri terhambat atau mati (Cowan 1999).
10
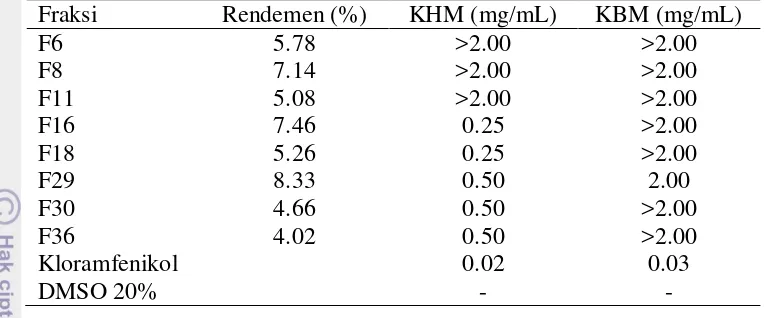
Tabel 4 Aktivitas antibakteri hasil fraksionasi ekstrak etanol 70%
Keterangan : KHM : konsentrasi hambat minimum; KBM : konsentrasi bunuh minimum
Penentuan aktivitas antibakteri terbaik ditunjukkan oleh F29 terhadap bakteri S. aureus (KHM 0.50 mg/mL dan KBM 2.00 mg/mL). Aktivitas antibakteri kloramfenikol lebih baik dengan KHM 0.02 mg/mL dan KBM 0.03 mg/mL.
Identitas Senyawa
Analisis menggunakan spektrofotometer infra merah pada F29 sebagai fraksi teraktif yang memiliki aktivitas antibakteri menunjukkan bahwa senyawa metabolit yang diduga adalah golongan flavonoid (Lampiran 9). Hasil analisis gugus fungsi senyawa diduga flavonoid menunjukkan bahwa isolat memiliki pita serapan pada bilangan gelombang 3356.14 cm-1 yang merupakan serapan gugus hidroksil membentuk ikatan hidrogen (OH). Keberadaan pita serapan pada bilangan gelombang 891.11 cm-1 mengindikasikan adanya gugus aromatik benzena posisi orto, serapan pada bilangan gelombang 2927.94 cm-1 diduga adanya gugus CH2. Serapan pita tajam pada bilangan gelombang 1705.07 cm-1
menunjukkan adanya gugus karbonil (C=O) dan adanya serapan pada bilangan gelombang 2854.65 cm-1 mengindikasikan regang C-H, serta pita serapan pada bilangan gelombang 1049.28 hingga 1257.59 cm-1 menunjukkan adanya gugus C-O (Pavia et al. 2001).
SIMPULAN DAN SARAN
Simpulan
Ekstrak etanol 70% merupakan ekstrak teraktif dibandingkan etil asetat karena memiliki aktivitas antibakteri terbaik dengan nilai konsentrasi hambat minimum (KHM) dan konsentrasi bunuh minimum (KBM) sebesar 1.00 mg/mL. Pemisahan dengan kromatografi kolom menghasilkan F29 sebagai fraksi teraktif
terhadap bakteri S. aureus yang menghasilkan KHM sebesar 0.50 mg/mL dan KBM 2.00 mg/mL. Hasil identifikasi senyawa metabolit F29 menggunakan spektrofotometer infra merah menunjukkan senyawa metabolit aktif diduga golongan flavonoid. Senyawa flavonoid dapat berfungsi sebagai bahan antibakteri dengan membentuk ikatan kompleks dengan dinding sel bakteri dan merusak membran sel bakteri.
Saran
Karakterisasi senyawa aktif dapat didukung pula menggunakan resonansi magnetik inti (NMR) dan spektrometer massa (MS) setelah dilakukan pemurnian lebih lanjut.
DAFTAR PUSTAKA
[AOAC] Association of Official Analytical Chemist. 2005. Official Method
ofAnalysis of The Association of Official Analyticalof Chemist.
Arlington(US): Association of Official Analytical Chemist, Inc.
[DEPKES RI] Departemen Kesehatan Republik Indonesia. 2000. Parameter
Standar Umum Ekstrak Tumbuhan Obat Edisi I. Jakarta: Direktorat Jenderal
Pengawasan Obat dan Makanan, Direktorat Pengawasan Obat Tradisional. Batubara I, Mitsunaga T, Ohasi H. 2009. Screening antiacne potency of
Indonesian medicinal plants: antibacterial, lipase inhibition, and antioxidant activities. J Wood Sci. 55:230–235. doi:10.1007/s10086-008-1021-1.
Cowan MM. 1999. Plant products as antimicrobial agents. Clin Microbiol Rev. penerjemah. Bandung (ID): Penerbit ITB. Terjemahan dari: Phytochemical Method.
Hasnawati, Prawita E. 2010. Isolasi dan identifikasi senyawa antibakteri dari daun
Eupatorium odoratum L. terhadap bakteri Staphylococcus aureus. Majalah Obat Tradisional. 15(1): 41-50.
Houghton PJ, Raman A. 1998. Laboratory Handbook for the Fractionation of Natural Extract. London(GB): Chapman & Hall.
Korompis GEC, Vennetia RD, Oksfriani JS. 2010. Uji in vitro aktivitas antibakteri Lansium domesticum Correa (langsat). Chem Prog. 3(1): 13-19. Lawalata VN. 2012. Rekayasa proses ekstraksi kulit buah langsat (Lansium
domesticum var. langsat) sebagai bahan antibakteri dan antioksidan [disertasi]. Bogor (ID): Institut Pertanian Bogor.
12
Madigan MT, Martinko JM, Parker J. 2003. Biology of Microorganisms. Edisi ke- 9. USA: Pearson Education, Inc.
Omar S, Marcotte M, Fields P, Sanchez PE, Poveda L, Mata R, Jimenez A, Durst T, Zhang J, MacKinnon S et al. 2007. Antifeedant activities of terpenoids isolated from tropical Rutales. J Stor Prod. 43:92-96. doi:10.1016/j.jspr.2005.11.005.
Pavia DL, Lampman GM, Kriz GS. 2001. Introduction to Spectroscopy. Washington (US): Thomson Learning, Inc.
Saewan N, John DS, Kan C. 2006.Antimalaria tetranortriterpenoids from the seeds of Lansium domesticum Corr. Phytochem. 67: 2288-2293.
LAMPIRAN
Lampiran 1 Diagram alir penelitian
Ekstrak etanol 70% Ekstrak etil asetat
Ekstrak etanol 70% Ekstraksi menggunakan pelarut etanol dan etil asetat secara maserasi
Uji aktivitas antibakteri Identifikasi fitokimia
Penentuan kadar air
Pemilihan eluen terbaik dengan KLT Bubuk kulit buah
langsat
Eluen heksana :etil asetat
12 fraksi
F6
Eluen etil asetat : metanol
9 fraksi
Fraksi teraktif F29
F8 F11 F16 F18 F30 F34
FTIR fraksionasi
Uji antibakteri Heksana : etil asetat
14
Lampiran 2 Perhitungan kadar air bubuk kulit langsat
Ulangan Bobot
Lampiran 3 Perhitungan rendemen ekstrak kulit buah langsat
Pelarut Bobot
Rendemen kering etanol 70% = bobot ekstrak
bobot sampel ×1−kadar air × 100%
= 8.5763
25.0077 × 1−0.1335 × 100%
Lampiran 4 Kromatogram ekstrak etanol 70% dengan eluen tunggal pada λ 254 nm
16
Lampiran 5 Kromatogram fraksi gabungan hasil fraksionasi ekstrak etanol 70% eluen heksana : etil asetat
18
Lampiran 8 Spektrum IR pada F29
OH
CH2
C-H
C=O
C-O
Lampiran 9 Data spektrum IR dari F29
No Bilangan gelombang (cm-1) Bentuk pita
Gugus fungsi Gugus fungsi flavonoid
(Cowan 1999) Isolat (Pavia et al. 2001)
1 621.08 2 655.80
3 891.11 690-900 Tajam Aromatik
4 933.55
5 1049.28 1000-1300 Tajam C-O C-O
6 1072.42 1000-1300 Melebar C-O C-O
7 1168.86 1000-1300 Tajam C-O C-O
8 1203.58 1000-1300 Tajam C-O C-O
9 1257.59 1000-1300 Melebar C-O C-O
10 1384.89 1220-1440 Tajam C-O-H
11 1411.89 1220-1440 Tajam C-O-H
12 1566.20 1550-1640 Tajam Tekuk N-H
13 1705.07 1705-1725 Tajam C=O C=O
14 2164.13 2100-2250 Melebar
15 2854.65 2850-3000 Tajam Regang C-H C-H
16 2927.94 2910-2940 Melebar CH2 CH2
20
RIWAYAT HIDUP
Penulis lahir di Tanjungpandan, Belitung pada 5 Agustus 1991. Penulis merupakan anak kedua dari dua bersaudara pasangan M.Taufik dan Yusmawati. Pada tahun 2009, penulis lulus dari SMAN 1 Tanjungpandan dan melanjutkan studi di Departemen Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor melalui jalur undangan seleksi masuk IPB (USMI). Penulis juga pernah mengikuti kepanitiaan dan pelatihan yang ada di lingkungan kampus. Penulis pernah melakukan praktik lapangan di Balai Pengujian Mutu Hasil Tanaman Pangan dan Hortikultura dengan judul laporan Verifikasi Metode Penentuan Logam Berat Kadmium dalam Bawang Merah Menggunakan