ABSTRAK
ANALISIS KUALITAS SEMEN BEKU SAPI SIMMENTAL
MENGGUNAKAN PENGENCER ANDROMED®DENGAN VARIASI
WAKTU PRE FREEZING Oleh
Rizki Indah Pratiwi
Penelitian ini bertujuan untuk: 1) mengetahui pengaruh waktu pre freezing terhadap kualitas semen beku Sapi Simmental yang menggunakan pengencer Andromed®; 2) mencari waktu pre freezing terbaik yang dapat mempertahankan kualitas semen beku Sapi Simmental. Rancangan yang digunakan adalah
Rancangan Acak Lengkap dengan 5 perlakuan waktu pre freezing (5 menit, 6 menit, 7 menit, 8 menit, 9 menit) dan 4 kali ulangan. Peubah yang diamati adalah persentase motilitas spermatozoa dan persentase spermatozoa hidup. Data yang diperoleh dianalisis menggunakan analisis ragam pada taraf nyata 5 atau 1% dan dilanjutkan dengan uji Polinomial Ortogonal pada taraf nyata 5 atau 1%. Hasil penelitian menunjukkan bahwa variasi waktu pre freezing tidak memberikan pengaruh yang nyata (P>0,05) terhadap persentase motilitas spermatozoa dan persentase spermatozoa hidup setelah pre freezing, tetapi memberikan pengaruh yang sangat nyata (P<0,01) terhadap persentase motilitas spermatozoa dan persentase spermatozoa hidup post thawing. Uji polinomial ortogonal juga menunjukkan bahwa variasi waktu pre freezing memberikan pengaruh yang sangat nyata (P<0,01) terhadap persentase motilitas spermatozoa dan persentase spermatozoa hidup post thawing. Pengaruh variasi waktu pre freezing terhadap persentase motilitas spermatozoa dan persentase spermatozoa hidup post thawing berpola linier dengan persamaan masing-masing adalah Ŷ = -28,88 + 7,38X dan Ŷ = -24,97 + 8,09X. Berdasarkan hasil penelitian diketahui bahwa pre freezing selama 9 menit merupakan waktu terbaik dalam mempertahankan persentase motilitas dan persentase spermatozoa hidup setelah thawing.
ABSTRACT
ANALYSIS QUALITY OF SIMMENTAL SEMEN USING ANDROMED® EXTENDER WITH VARIATIONS OF PRE FREEZING TIME
By
Rizki Indah Pratiwi
The goals of research were to know: 1) the effect of pre freezing time to the frozen semen quality of Simmental; 2) the best time of pre freezing that can preserve the frozen semen quality of Simmental. The completely randomized design was used in this research with 5 treatments (5 minutes; 6 minutes; 7 minutes; 8 minutes; 9 minutes) and 4 times of replication. Parameters measured were percentage of sperm motility and percentage of life sperm. The data were analyzed using analysis of variance at significance level of 1% or 5% and then continued with orthogonal polynomial test at significance level of 1% or 5%.
The results showed that the time of pre freezing did not affect significantly (P> 0.05) on the percentage of sperm motility and the percentage of life sperm after pre freezing, but the effect was significant (P <0.01) on percentage of sperm motility and percentage of life sperm post thawing. Orthogonal polynomial test also showed that the time of pre freezing did affect significantly (P< 0.01) on the percentage of sperm motility and the percentage of life sperm after thawing. The effect of pre freezing time on the percentage of sperm motility and percentage of life sperm after thawing had linear pattern with each equation those were Y = -28,88+7,38X and Y = -24,97+8,09X. Pre freezing for 9 minutes was able to show the best percentage of sperm motility and percentage of life sperm after thawing.
RIWAYAT HIDUP
Penulis dilahirkan di Way Jepara, Lampung Timur pada tanggal 19 Maret 1993
sebagai anak pertama dari lima bersaudara pasangan Bapak Muhammad Ihsan dan
Ibu Nurhidayah.
Penulis menyelesaikan pendidikan Sekolah Dasar (SD) di Madrasah Ibtidaiyah
Mamba’ul Ulum (MIMU) Sumberejo pada 2004, pendidikan Sekolah Menengah Pertama (SMP) di SMPN 1 Way Jepara pada 2007, dan Sekolah Menengah Atas
(SMA) di SMAN 1 Way Jepara pada 2010.
Penulis terdaftar sebagai mahasiswa Jurusan Peternakan, Fakultas Pertanian,
Universitas Lampung pada 2010 melalui jalur PKAB. Penulis melakukan Praktik
Umum (PU) pada Juli 2013 di Balai Inseminasi Buatan (BIB) Ungaran, Jawa
Tengah. Selama menjadi mahasiswa penulis pernah menjadi asisten praktikum
Biologi Ternak, aktif sebagai anggota bidang Pendidikan dan Pelatihan di
Himpunan Mahasiswa Peternakan (HIMAPET) Fakultas Pertanian Universitas
Dengan segala rasa syukur kupersembahkan skripsi ini
untuk kedua orang tuaku tercinta, Ayahanda M. Ihsan dan
Ibunda Nurhidayah yang telah membesarkan dan
mendidikku dengan penuh kasih dan keikhlasan hati, semoga
Allah SWT senantiasa menganugerahkan rahmat dan
hidayah-Nya kepada kalian.
Adik-adikku tersayang Fajar Burhanudin, Ahmad Habib
Ismail, Amirul Luthfia, dan M. Faisal Ro’uf, kalianlah
motivasi masa depanku.
Kakanda yang terkasih Kurniawan Hidayah Mahmud,
kaulah yang telah membuatku bersemangat terus melangkah.
“Tidak semua yang kita inginkan harus terjadi seketika. Kita
tidak hidup di dunia dongeng”
(Tere Liye, Eliana)
“
Sesungguhnya bersama kesulitan ada
kemudahan“
(Alam Nashrah: 6)
“Tidak masalah ketika orang lain meragukanmu, tetapi
jangan pernah meragukan dirimu sendiri”
“Filosofi padi, semakin berisi maka padi akan semakin
merunduk, maknanya semakin kita merasa bisa maka kita
harus bisa semakin merasa”
DAFTAR ISI
Halaman
DAFTAR TABEL ... vi
DAFTAR GAMBAR ... viii
I. PENDAHULUAN ... 1
A. Latar Belakang dan Masalah ... 1
B. Tujuan Penelitian ... 4
C. Kegunaan Penelitian ... 4
D. Kerangka Pemikiran ... 4
E. Hipotesis ... 7
II. TINJAUAN PUSTAKA ... 8
A. Sapi Simmental ... 8
B. Semen ... 9
C. Parameter Kualitas Semen ... 10
1. Volume ... 10
2. Warna ... 11
3. Bau ... 12
4. pH ... 12
5. Konsistensi ... 12
7. Motilitas spermatozoa ... 13
III.METODE PENELITIAN ... 24
A. Waktu dan Tempat Penelitian ... 24
B. Alat Penelitian ... 24
C. Bahan Penelitian ... 24
D. Rancangan Penelitian ... 25
E. Pelaksanaan Penelitian ... 25
F. Peubah yang Diamati ... 29
IV.HASIL DAN PEMBAHASAN ... 30
A. Penilaian Kualitas Semen Segar ... 30
B. Penilaian Kualitas Semen setelah Ekuilibrasi ... 32
C. Pengaruh Variasi Waktu Pre Freezing terhadap Persentase Motilitas Spermatozoa ... 34
1. Pengaruh variasi waktu pre freezing terhadap persentase motilitas spermatozoa setelah pre freezing ... 34
2. Pengaruh variasi waktu pre freezing terhadap persentase motilitas spermatozoa setelah thawing ... 35
D. Pengaruh Variasi Waktu Pre Freezing terhadap Persentase Spermatozoa Hidup ... 39
2. Pengaruh variasi waktu pre freezing terhadap persentase
spermatozoa hidup setelah thawing ... 40
V. SIMPULAN DAN SARAN ... 44
A. Simpulan ... 44
B. Saran ... 44
DAFTAR PUSTAKA ... 45
DAFTAR TABEL
Tabel Halaman
1. Hasil evaluasi kualitas semen segar Sapi Simmental ... 30
2. Kualitas semen Sapi Simmental setelah ekuilibrasi ... 32
3. Rataan persentase motilitas spermatozoa semen beku Sapi Simmental
setelah pre freezing ... 34
4. Rataan persentase motilitas spermatozoa semen beku Sapi Simmental setelah thawing ... 36
5. Rataan persentase spermatozoa hidup setelah pre freezing ... 39
6. Rataan persentase spermatozoa hidup setelah thawing ... 40
7. Hasil analisis ragam persentase motilitas spermatozoa setelah pre-
freezing ... 50
8. Analisis ragam persentase motilitas spermatozoa setelah pre freezing pada uji polinomial ortogonal ... 50
9. Analisis ragam persentase motilitas spermatozoa setelah thawing
pada uji polinomial ortogonal ... 50
10.Sidik regresi sederhana persentase motilitas spermatozoa setelah
thawing ... 51
11.Hasil analisis ragam persentase spermatozoa hidup setelah
pre-freezing ... 51
12.Hasil analisis ragam persentase spermatozoa hidup setelah
thawing ... 51
13.Analisis ragam persentase spermatozoa hidup setelah thawing pada
14.Sidik regresi sederhana persentase spermatozoa hidup setelah
DAFTAR GAMBAR
Gambar Halaman
1. Bagan pelaksanaan penelitian ... 26
2. Hubungan antara variasi waktu pre freezing dengan persentase
motilitas spermatozoa setelah thawing ... 37
3. Hubungan antara variasi waktu pre freezing dengan persentase
I. PENDAHULUAN
A. Latar Belakang dan Masalah
Sapi Simmental merupakan salah satu bangsa sapi potong yang mempunyai
pertumbuhan cepat. Sapi jenis ini merupakan sapi dwiguna, yaitu sapi yang
menghasilkan susu dan daging. Secara morfologi, Sapi Simmental memiliki ciri
fisik tidak berpunuk dan tidak bergelambir. Warna bulunya cokelat kemerahan
(merah bata). Bagian wajah dan lutut ke bawah sampai ujung ekor berwarna putih.
Betina dewasa dapat mencapai 800 kg, sedangkan pejantan dewasa mencapai
berat sekitar 1150 kg. Berdasarkan keunggulan tersebut, banyak peternak di
Indonesia yang memelihara Sapi Simmental untuk memenuhi tingginya
kebutuhan daging sapi untuk masyarakat. Bibit Sapi Simmental yang unggul dapat
diperoleh dengan melakukan program pemuliabiakan ternak melalui Inseminasi
Buatan (IB). Menurut Toelihere (1993), teknologi IB dapat mempercepat
perkembangan populasi dan meningkatkan mutu genetik ternak.
IB adalah suatu proses mengawinkan ternak dengan cara buatan yang melibatkan
prosedur kompleks dan petugas pelaksana yang terlatih. Teknologi ini telah lama
diterapkan dengan maksud untuk mempertinggi penggunaan pejantan-pejantan
unggul dan menghindari penyebaran penyakit melalui saluran reproduksi.
2
sehingga semen atau sperma yang dihasilkan oleh seekor pejantan unggul dalam
satu kali ejakulasi dapat digunakan untuk melayani lebih banyak betina setelah
semen tersebut diproses menjadi semen beku.
Semen beku merupakan semen yang berasal dari pejantan sapi terpilih yang telah
melalui proses pengenceran sesuai prosedur produksi sehingga menjadi semen
beku dan disimpan di dalam nitrogen cair pada suhu -196oC pada kontainer. Mutu semen beku sapi merupakan salah satu faktor yang dapat menentukan
keberhasilan program IB, meskipun masih banyak faktor lain yang ikut
memengaruhi seperti keterampilan inseminator, ketepatan deteksi birahi,
kesehatan reproduksi ternak betina, dan tatalaksana pemeliharaan ternak betina.
Oleh sebab itu, mutu semen beku harus selalu terjaga agar fertilitasnya tetap baik.
Untuk menjamin mutu semen beku sapi yang beredar, perlu ditetapkan standar
semen beku sapi yang didukung oleh penanganan yang baik dan benar agar mutu
semen beku sapi dapat dipertahankan hingga siap untuk diinseminasikan.
Tingkat keberhasilan pembuatan semen beku dapat dilihat dari kualitas semen
beku yang dihasilkan. Semen beku yang berkualitas baik mempunyai persentase
motilitas dan spermatozoa hidup yang tinggi. Namun, terdapat banyak faktor yang
dapat menurunkan kualitas semen mulai dari proses pengolahan, penyimpanan
dalam kontainer, dan distribusi semen beku itu sendiri.
Bahan pengencer untuk semen beku harus mengandung zat krioprotektan guna
melindungi spermatozoa. Krioprotektan yang sering digunakan untuk pengencer
semen beku adalah krioprotektan ekstraseluler seperti kuning telur dan intraseluler
3
krioprotektan ekstraselular adalah Andromed®. Media pengencer ini memiliki komposisi kimia yang lebih lengkap dan akan memberikan fungsi yang baik bagi
spermatozoa yang diencerkan. Pengencer komersial ini telah digunakan di beberapa
Balai Inseminasi Buatan dengan hasil yang memuaskan.
Masalah yang sering menyebabkan penurunan kualitas semen adalah pada proses
pembekuan semen. Menurut Parrish (2003), semen akan mengalami penurunan
kualitas sekitar 10 − 40% pada saat pembekuan. Toelihere (1993) menambahkan
bahwa kerusakan spermatozoa sebanyak 20% pada saat pembekuan masih
dianggap memuaskan.
Derajat kecepatan pendinginan untuk mempertahankan fertilitas spermatozoa
belum diketahui dengan pasti. Berbagai percobaan telah dikemukakan, misalnya
pendinginan cepat dalam waktu 2 menit dari -15oC ke -25oC, pendinginan dari 5oC ke -20oC dengan kecepatan 1 sampai 4 derajat per menit. Kecepatan
pendinginan yang sering digunakan saat pembekuan yaitu 1 derajat per menit dari
5oC ke -15oC (Toelihere, 1981). Berdasarkan Peraturan Direktur Jenderal Peternakan Nomor: 12207/Hk.060/F/12/2007 tentang Petunjuk Teknis Produksi
dan Distribusi Semen Beku, proses pembekuan pada tahap pra pembekuan
(pre freezing) dilakukan selama 5 − 9 menit di atas N2 cair.
Waktu pre freezing yang umumnya diterapkan di berbagai Balai Inseminasi
4
B. Tujuan Penelitian
Adapun tujuan dari penelitian ini adalah:
1. mengetahui pengaruh variasi waktu pre freezing terhadap kualitas semen beku
Sapi Simmental menggunakan pengencer Andromed®;
2. mengetahui waktu pre freezing terbaik yang dapat mempertahankan kualitas
semen beku Sapi Simmental menggunakan pengencer Andromed®.
C. Kegunaan Penelitian
Hasil penelitian ini diharapkan dapat memberikan informasi yang bermanfaat
kepada petugas laboratorium Semen Beku di berbagai Balai Inseminasi Buatan
untuk menjadi pedoman pembekuan semen yang baik dalam proses pembuatan
semen beku. Teridentifikasinya waktu pre freezing yang terbaik dalam proses
pembekuan semen dapat memperkecil penurunan kualitas semen beku.
D. Kerangka Pemikiran
Sapi Simmental adalah sapi bangsa Bos taurus yang berasal dari daerah Simme di
Switzerland (Yulianto dan Saparinto, 2010). Namun, sapi ini berkembang lebih
cepat di Benua Eropa dan Benua Amerika. Sapi Simmental merupakan tipe sapi
perah dan pedaging. Sapi Simmental adalah sapi pedaging yang memiliki daging
lunak, sedikit mengandung lemak dan produktivitas daging yang cukup tinggi.
Sapi ini banyak disukai oleh peternak di seluruh dunia termasuk Indonesia karena
5
Untuk meningkatkan populasi Sapi Simmental diperlukan teknologi tepat yang
mudah dan efisien melalui Inseminasi Buatan. IB merupakan salah satu teknologi
pemuliabiakan yang digunakan untuk meningkatkan mutu dan jumlah ternak yang
memanfaatkan penggunaan bibit pejantan unggul dalam upaya perbaikan mutu
genetik ternak. Program IB dilakukan menggunakan semen beku yang diencerkan
dan dibekukan dengan suhu -196oC dalam N2 cair.
Semen beku yang berkualitas baik mempunyai angka konsepsi yang tinggi.
Kualitas semen beku dipengaruhi oleh jenis pengencer yang digunakan dan proses
pembuatan semen beku terutama pada tahap pembekuan. Jenis bahan pengencer
yang banyak digunakan adalah Andromed®. Media pengencer ini memiliki komposisi yang lengkap dan dapat memberikan perlindungan terhadap
spermatozoa sehingga dapat meningkatkan kualitas semen beku yang dihasilkan.
Pembekuan merupakan proses pengeringan fisik yang meliputi dua tahap, yaitu
pre freezing (pembekuan awal) dan freezing (pembekuan). Pada tahap pre-
freezing, straw yang berisi semen diatur pada rak straw dan ditempatkan sekitar
4 cm di atas permukaan N2 cair dengan suhu -110 oC sampai -120oC, kemudian
straw dibekukan pada suhu -196oC dengan cara dimasukkan langsung ke dalam
N2 cair.
Pada proses pembekuan semen akan mengakibatkan terjadinya cold shock dan
perubahan intraseluler yang berkaitan dengan pembentukan kristal-kristal es. Jika
suatu larutan dibekukan maka air sebagai pelarut membeku menjadi kristal-kristal
es, sedangkan bahan terlarut berakumulasi dalam larutan yang masih ada. Pada
6
terlarut lainnya baik di dalam larutan maupun di dalam sel-sel. Konsentrasi
elektrolit yang berlebihan akan melarutkan selubung lipoprotein dinding sel
spermatozoa sehingga pada waktu thawing, permeabilitas membran sel akan
berubah dan menyebabkan kematian sel. Masalah pembekuan ini sebagian dapat
diatasi dengan menggunakan zat-zat pelindung di dalam media pengencer dan
penurunan suhu secara gradual.
Derajat pendinginan merupakan problem penting dalam proses pembekuan semen.
Sperma sapi banyak mengalami kerusakan pada suhu kritik antara -1,5oC dan -30oC, rata-rata pada suhu -17oC. Derajat kecepatan pendinginan pada tahap pembekuan belum diketahui dengan pasti. Berdasarkan Peraturan Direktur
Jenderal Peternakan Nomor: 12207/Hk.060/F/12/2007, proses pre freezing
dilakukan selama 5 − 9 menit. Menurut Nilna (2010), pembekuan berlangsung
selama 9 menit.
Kualitas semen beku dapat dilihat dari besarnya persentase motilitas dan
spermatozoa hidup setelah pembekuan. Motilitas spermatozoa sangat menentukan
keberhasilan spermatozoa dalam menembus cumulus oophorus dan zona pelusida,
yang merupakan lapisan sel telur. Dengan demikian motilitas merupakan faktor
penting yang berperan sebagai penentu keberhasilan proses fertilisasi pada saat
dilakukan IB. Menurut Hunter (1995), gerakan maju yang kuat merupakan indeks
daya hidup yang penting dalam suatu populasi spermatozoa.
Selain motilitas, proses pembekuan semen juga berpengaruh terhadap daya tahan
hidup spermatozoa. Persentase spermatozoa hidup yang tinggi dengan gerakan
7
beku yang dihasilkan memiliki kualitas yang baik. Sebaliknya, apabila persentase
spermatozoa hidup dan motilitas rendah maka semen beku tersebut memiliki
kualitas yang rendah dan tidak layak untuk diinseminasikan.
E. Hipotesis
Hipotesis yang diajukan dalam penelitian ini adalah:
1. terdapat perbedaan kualitas semen beku Sapi Simmental yang menggunakan
pengencer Andromed® dengan variasi waktu pre freezing yang berbeda; 2. terdapat salah satu waktu pre freezing terbaik yang dapat mempertahankan
II. TINJAUAN PUSTAKA
A. Sapi Simmental
Sapi Simmental adalah bangsa Bos taurus yang berasal dari daerah Simme di
Switzerland tetapi sekarang perkembangannya lebih cepat di benua Eropa dan
benua Amerika. Sapi Simmental merupakan tipe sapi dwiguna yaitu perah dan
pedaging (Yulianto dan Saparinto, 2010). Sapi Simmental mempunyai sifat jinak,
tenang, dan mudah dikendalikan (Susilorini, 2008). Sapi Simmental memiliki
badan panjang dan padat, serta dapat menyusui anaknya dengan baik. Sapi
Simmental berukuran besar, baik pada kelahiran, penyapihan maupun saat
mencapai dewasa (Blakely dan Bade, 1991). Berat sapih Sapi Simmental cukup
tinggi demikian pula pertambahan berat badan setelah sapih (Pane, 1993).
Sapi Simmental memiliki ciri-ciri bulu berwarna coklat kemerahan (merah bata),
bagian muka dan lutut ke bawah serta ujung ekor berwarna putih, ukuran tubuh
besar, pertumbuhan otot bagus, penimbunan lemak di bawah kulit rendah dan
ukuran tanduk kecil. Sapi jantan dewasa mampu mencapai berat badan 1150 kg
dan betina dewasa mencapai 800 kg. Sapi Simmental memiliki persentase karkas
yang tinggi. Sapi jenis ini sangat cocok dipelihara di daerah beriklim sedang
9
B. Semen
Semen adalah sekresi kelamin jantan yang diejakulasikan ke dalam saluran
kelamin betina sewaktu kopulasi. Semen terdiri dari spermatozoa yang berada
dalam cairan yang disebut plasma semen (Salisbury dan VanDermark, 1985).
Semen merupakan cairan yang terdiri dari hasil sekresi kelenjar kelamin aksesoris
dan spermatozoa yang sudah masak dari epididimis seekor sapi pejantan dewasa
(Srigandono, 1996). Semen terdiri atas campuran spermatozoa yang dihasilkan
oleh jaringan testis di dalam tubulus seminiferus dan plasma semen yang berasal
dari kelenjar kelamin pelengkap (Hafez, 1993).
Spermatozoa normal memiliki bagian-bagian yang terdiri atas kepala, leher,
badan, dan ekor. Sekitar 2/3 bagian dari dinding depan kepala spermatozoa
tampak tertutup oleh akrosom. Tempat sambungan dasar akrosom dan kepala
disebut cincin nukleus. Di antara kepala dan badan terdapat sambungan pendek
yaitu leher yang berisi sentriol proksimal, terkadang dinyatakan sebagai pusat
kinetik aktifitas spermatozoa. Bagian badan dimulai dari leher dan berlanjut ke
cincin sentriol. Bagian badan dan ekor mampu bergerak bebas meskipun tanpa
kepala. Ekor yang menyerupai cambuk membantu mendorong spermatozoa untuk
bergerak maju (Salisbury dan VanDemark (1985).
Plasma semen merupakan sekresi dari epididimis, vas deferens, kelenjar prostat,
dan vesika seminalis, serta kelenjar cowper, sehingga seminal plasma sangat
berpengaruh terhadap sifat fisik dan kimia semen. Di dalam plasma semen
terdapat berbagai macam zat organik, zat inorganik, dan air. Zat organik tersebut
10
inositol, sorbitol, ergothionine, dan spremine. Zat inorganik meliputi kalium,
kalsium, dan bikarbonat yang relatif tinggi kadarnya dibandingkan dengan yang
terdapat dalam tubuh (Partodihardjo, 1992). Plasma semen berguna sebagai buffer
dan medium bagi spermatozoa agar dapat bertahan lama setelah ejakulasi
(Toelihere, 1993).
C. Parameter Kualitas Semen
Parameter yang digunakan untuk menilai kualitas semen secara umum meliputi:
volume, warna, bau, pH, konsistensi, konsentrasi, motilitas, dan viabilitas.
1. Volume
Volume merupakan salah satu standar minimum untuk evaluasi kualitas semen
yang akan digunakan untuk Inseminasi Buatan (Garner dan Hafez, 2000). Volume
semen dapat diketahui dengan membaca skala yang terdapat pada tabung
penampungan. Volume semen per ejakulat berbeda menurut bangsa, umur, berat
badan, tingkatan makanan, dan frekuensi penampungan. Volume semen akan
menurun sesudah mencapai puncak dewasa (Toelihere, 1993).
Garner dan Hafez (2000) menyatakan bahwa volume semen sapi berkisar antara
5 – 8 ml/ejakulasi. Toelihere (1993) menambahkan bahwa volume semen sapi
jantan berkisar 1 – 15 ml. Menurut Salisbury dan VanDermark (1985), volume
semen yang dihasilkan sapi jantan muda sekitar 1 − 2 ml atau lebih rendah dari
itu, sedangkan sapi jantan yang telah dewasa dapat menghasilkan semen lebih
11
Menurut Feradis (2010), frekuensi ejakulasi sering menyebabkan penurunan
volume dan apabila dua ejakulat diperoleh berturut-turut dalam waktu singkat
maka umumnya ejakulat yang kedua mempunyai volume yang lebih rendah.
Volume semen yang rendah tidak merugikan tetapi apabila disertai dengan
konsentrasi yang rendah pula maka akan membatasi jumlah spermatozoa yang
tersedia.
2. Warna
Semen sapi normal berwarna seperti susu atau krem keputih-putihan dan keruh.
Derajat kekeruhannya tergantung pada konsentrasi spermatozoa. Sekitar 10%
sapi-sapi jantan menghasilkan semen yang normal berwarna kekuning-kuningan
yang disebabkan oleh pigmen riboflavin yang dibawakan oleh satu gen autosom
resesif dan tidak mempunyai pengaruh terhadap fertilitas (Toelihere, 1993).
Adanya kuman-kuman Pseudomonas aeruginosa di dalam semen sapi dapat
menyebabkan warna hijau kekuning-kuningan apabila semen dibiarkan pada suhu
kamar. Gumpalan-gumpalan, bekuan dan kepingan-kepingan di dalam semen
menunjukkan adanya nanah yang umumnya berasal dari kelenjar-kelenjar
pelengkap dari ampula. Semen yang berwarna gelap sampai merah muda
menandakan adanya darah segar dalam jumlah yang berbeda dan berasal dari
saluran kelamin uretra atau penis. Warna kecoklatan menunjukkan adanya darah
yang telah mengalami dekomposisi. Warna coklat muda atau warna
kehijau-hijauan menunjukkan kemungkinan adanya kontaminasi dengan feses
12
3. Bau
Variabel pemeriksaan bau pada semen jarang dilakukan karena tidak berhubungan
dengan kualitas spermatozoa. Umumnya bau semen dikategorikan sebagai bau
khas (Rizal dan Herdis, 2008).
4. pH
Nilai pH dapat dilihat dengan cara mencocokkan warna dari kertas lakmus yang
telah ditetesi semen dengan warna pada tabung kemasan kertas lakmus
(Garner dan Hafez, 2000). Pada umumnya sperma sangat aktif dan tahan hidup
lama pada pH sekitar 7,0. Motilitas partial dapat dipertahankan pada pH antara 5
sampai 10 (Toelihere, 1985).
Feradis (2010) menyatakan bahwa setiap bangsa sapi mempunyai nilai pH semen
segar yang berbeda-beda. Menurut Peraturan Direktur Jendral Peternakan nomor
12207/hk.060/f/12/2007, pH semen segar yang digunakan sebagai semen beku
berkisar antara 6,2 – 6,8. Menurut Garner dan Hafez (2000), pH semen segar
adalah 6,4 – 7,8.
5. Konsistensi
Konsistensi dapat diperiksa dengan menggoyangkan tabung berisi semen secara
perlahan-lahan. Semen sapi mempunyai konsistensi kental krem. Pada sapi, semen
dengan konsistensi krem mempunyai konsentrasi 1000 – 2000 juta atau lebih sel
per ml; konsistensi seperti susu encer memiliki konsentrasi 500 – 600 juta sel per
13
100 juta sel per ml dan yang jernih seperti air kurang dari 50 juta sel per ml
(Toelihere, 1993).
6. Konsentrasi
Penilaian konsentrasi sangat penting karena faktor inilah yang menggambarkan
sifat-sifat semen dan dipakai sebagai salah satu kriteria penentuan kualitas semen
(Toelihere, 1993). Jumlah sel spermatozoa setiap unit volume semen sapi
bervariasi dari nol sampai tiga miliyar (3000×106) sel spermatozoa setiap ml. Konsentrasi spermatozoa yang berderajat tinggi biasanya berkisar dari 2000×106 sampai 2200 × 106 sel spermatozoa (Salisbury dan VanDenmark, 1985).
7. Motilitas spermatozoa
Motilitas umumnya digunakan sebagai parameter kesanggupan spermatozoa untuk
membuahi sel telur (Toelihere, 1985). Sesuai dengan bentuk morfologinya,
spermatozoa hidup dapat mendorong dirinya sendiri maju ke depan di dalam
lingkungan zat cair. Terdapat 3 tipe motilitas spermatozoa mamalia yaitu gerak
progresif, gerak berputar, dan gerak oscillatoris di tempat (Walton dalam
Salisbury dan VanDermark, 1985). Motilitas spermatozoa dipengaruhi oleh
kemampuan metabolisme spermatozoa yang ditunjang oleh lingkungan yaitu suhu
dan komponen-komponen di dalam medium pengencer (Toelihere, 1993).
Tipe gerak normal spermatozoa secara individual bervariasi dari gerakan maju
yang sangat cepat pada spermatozoa yang baru diejakulasikan, ke gerakan maju
yang lebih pelan (gerakan kepala menyerupai baling-baling pada sumbu
14
gerakan sangat lemah dan terkadang tampak ayunan ekor tanpa berpindah tempat
(Salisbury dan VanDermark, 1985).
Menurut Toelihere (1993), penilaian gerakan individu spermatozoa yang terlihat
pada mikroskop adalah sebagai berikut:
0% : spermatozoa tidak bergerak;
0 − 30% : gerakan berputar ditempat, pergerakan progresif;
30 − 50% : gerakan berayun atau melingkar, pergerakan progresif;
50 − 80% : ada gerakan massa, pergerakan progresif;
80 − 90% : ada gelombang, pergerakan progresif;
90 − 100% : gelombang sangat cepat, pergerakan sangat progresif;
Persentase motilitas spermatozoa sapi dibawah 40% menunjukkan nilai semen
yang kurang baik dan sering berhubungan dengan infertilitas. Kebanyakan
pejantan yang fertil mempunyai 50 – 80% spermatozoa yang motil aktif progresif
(Toelihere, 1993).
Menurut Toelihere (1993), pemeriksaan motilitas sperma merupakan satu-satunya
cara penentuan kualitas semen sesudah pengenceran. Penilaian gerakan individual
spermatozoa yang terbaik dilakukan dengan melihat pola pergerakan progresif
atau gerakan aktif maju ke depan. Gerakan melingkar atau gerakan mundur
merupakan tanda bahwa spermatozoa mengalami coldshock. Gerakan berayun
dan berputar-putar di tempat biasanya terlihat pada semen yang sudah tua dan
apabila kebanyakan spermatozoa berhenti bergerak dan dianggap mati.
Menurut Direktorat Jenderal Peternakann (2007), penilaian untuk semen beku sapi
15
mikroskopis minimal 70%. Syarat minimal spermatozoa yang motil progresif
setelah pengenceran adalah 55%. Pada pengujian post thawing motility,
spermatozoa sapi yang motil progresif minimal 40% dan gerak maju individu
spermatozoa minimal 2 (dua).
Menurut Pane (1993), daya gerak spermatozoa sangat penting karena diperlukan
untuk bergerak maju dalam saluran kelamin betina yang selanjutnya membuahi
ovum. Susilawati et al. (2003) menyatakan bahwa proses fertilisasi membutuhkan
spermatozoa motil sekitar sepuluh juta sel, maka syarat spermatozoa sebagai
standar inseminasi adalah 2,5×107 sel spermatozoa per straw dengan motilitas sebesar 40%. Menurut Garner dan Hafez (2000), syarat minimal motilitas individu
spermatozoa postthawing agar dapat digunakan dalam IB adalah 40%.
8. Spermatozoa hidup
Salisbury and VanDemark (1985) menyatakan bahwa persentase hidup
spermatozoa dapat dihitung dengan melihat reaksi spermatozoa terhadap zat
warna tertentu. Spermatozoa yang hidup tidak berwarna sedangkan spermatozoa
yang mati akan menyerap warna. Menurut Hunter (1995), zat warna eosin tidak
dapat menyusup ke dalam sel spermatozoa hidup karena membran plasmanya
masih utuh dan tidak mengalami kerusakan. Menurut Partodihardjo (1992), sel-sel
spermatozoa yang hidup akan sedikit sekali menghisap warna sedangkan sel-sel
yang mati akan mengambil warna karena permeabilitas dinding sel menjadi lebih
tinggi setelah mati.
Suyadi dan Susilawati (1992) mengatakan bahwa kadang-kadang spermatozoa
16
badan. Pengambilan zat warna oleh spermatozoa dapat dipengaruhi oleh
faktor-faktor lain seperti sekresi kelenjar assesoris, pH, suhu, kesalahan teknik pada
waktu pembuatan preparat dan umur semen sesudah pengambilan semen.
Menurut Hafez (2000), persentase hidup semen sapi segar sebesar 60 − 80%.
Toelihere (1993) menyatakan bahwa semen yang baik memiliki persentase
viabilitas diatas 50%. Bearden and Fuquay (2000) menyatakan bahwa persentase
spermatozoa hidup akan selalu lebih tinggi daripada motilitas spermatozoa.
Menurut Partodiharjo (1992), spermatozoa yang tidak bergerak belum tentu mati
sehingga tidak menghisap warna, sedangkan pada penafsiran dengan dasar
bergerak dan tidak bergerak dianggap immotil. Spermatozoa yang hidup dan tidak
bergerak, diiringi defect pada dinding selnya dapat menghisap warna sehingga di
bawah mikroskop dianggap mati, sedangkan penafsiran yang lain dianggap hidup.
Menurut Pangestu (2002), 50% sperma mamalia akan mati setelah pembekuan
dan thawing. Menurut Yudhaningsih (2004), suhu yang rendah akan
mengakibatkan bocornya substansi vital dalam spermatozoa sehingga enzim
intraseluler, lipoprotein, ATP, kalium intraseluler dan lemak berfosfor berkurang
dan menyebabkan kerusakan membran plasma. Menurut Kusuma (1990), matinya
sperma disebabkan berkurangnya cadangan makanan dan tidak seimbangnya
elektrolit larutan akibat metabolisme sperma.
D. Semen Beku
Semen beku adalah semen yang telah diencerkan kemudian dibekukan di bawah
17
spermatozoa dalam waktu yang lama. Pembekuan semen meliputi proses
pengolahan, pengawetan, dan penyimpanan semen sehingga dapat digunakan pada
waktu tertentu sesuai kebutuhan (Graha dalam Wahyu, 2008). Tahapan produksi
semen beku adalah: penampungan semen segar, pemeriksaan semen segar,
pengenceran semen segar, pengujian semen setelah pengenceran, ekuilibrasi,
identifikasi straw, pengemasan (filling dan sealing), proses pembekuan, pengujian
post thawing motility, penyimpanan dan pengujian semen beku setelah
penyimpanan (Direktorat Jenderal Peternakan, 2007).
Menurut Hafez (1993), model pengemasan semen beku yang biasa digunakan
yaitu:
1. straw yang terbuat dari polivinil klorida dengan dua ukuran yaitu ministraw
berisi 0,25 ml dan midistraw berisi 0,5 ml semen;
2. ampul gelas berisi 0,5 − 1 ml semen;
3. pellet berisi 0,1 − 0,2 ml semen.
Toelihere (1985) menyatakan bahwa penyimpanan dalam bentuk straw dapat
menghemat tempat, ringan, dan praktis untuk dibawa kemana-mana sertadapat
dibuat berbagai warna dimana setiap warnanya untuk mengidentifikasipejantan
tertentu.
Menurut Toelihere (1993), penggunaan semen beku memberikan beberapa
keuntungan diantaranya: semen pejantan-pejantan unggul, baik yang masih sehat
maupun yang terluka, cacat, pincang, atau tua, dapat dipakai secara efisien
sepanjang tahun; mengatasi hambatan waktu dan jarak; memungkinkan
18
yang lebih luas; biaya pengangkutan semen dari pusat inseminasi buatan ke
pelaksana inseminasi di daerah sangat dikurangi karena penyediaan semen dan
nitrogen cair hanya dilakukan sekali sebulan dimana semen beku dapat dikirimkan
dengan mobil, kereta api, atau bus ekspres, atau sebagai barang kiriman pos
melalui kapal udara atau kapal laut; pembekuan semen memungkinkan
pengawetan semen pejantan-pejantan muda sebelum mencapai umur yang lebih
tua dimana semennya menjadi relatif infertil.
E. Pengenceran Semen
Salisbury dan VanDenmark (1985) menyatakan bahwa pengenceran semen
memungkinkan IB sapi betina lebih banyak dan mempertahankan daya fertilisasi
sebelum semen disemprotkan ke dalam alat kelamin betina waktu birahi. Menurut
Lindsay et al. (1982), pengenceran semen berfungsi untuk memperbanyak volume
semen, memberi media yang cocok untuk spermatozoa, menjaga pH, tekanan
osmotik, dan sebagai krioprotektan. Dalam melakukan pengenceran semen perlu
menghindari adanya panas yang berlebihan, bahan kimia toxic, berhubungan
dengan udara luar, sinar matahari langsung, dan guncangan.
Menurut Toelihere (1993), syarat-syarat pengencer yang baik sebagai berikut:
1. bahan pengencer hendaknya murah, sederhana dan praktis dibuat, tetapi daya
preservasinya tinggi;
2. pengencer harus mengandung unsur-unsur (fisik dan kimiawi) yang hampir
sama dengan semen dan tidak boleh mengandung zat-zat yang bersifat toksik
19
3. pengencer harus tetap mempertahankan dan tidak membatasi daya fertilisasi
sperma;
4. pengencer harus memberi kemungkinan penilaian sperma sesudah
pengenceran.
Menurut Ridwan (2008), larutan pengencer semen yang memiliki komposisi
kimia lebih lengkap akan memberikan fungsi yang baik bagi spermatozoa yang
diencerkan. Subtrat-subtrat nutrisi dalam bahan pengencer diperlukan
spermatozoa untuk mempertahankan hidupnya, terutama bagi spermatozoa yang
disimpan terlebih dahulu sebelum diinseminasikan.
F. Pengencer Andromed®
Andromed® adalah pengencer komersial dengan bahan dasar bebas protein hewani. Andromed® merupakan bahan pengencer instan berupa cairan yang dapat digunakan dalam proses pembekuan semen. Pengencer Andromed® mengandung gliserolyang berfungsi untuk menghasilkan energi dan membentuk fruktosa,
sehingga menunjukkan spermatozoa yang optimum. Pengencer semen komersial
ini juga mudah digunakan karena telah tersedia dalam paket siap pakai
(Herdis et al., 2008).
Andromed® adalah pengencer yang dapat memberikan pengaruh terbaik terhadap persentase motilitas dan persentase hidup spermatozoa dibandingkan dengan susu
skim (Kuswanto et al., 2007), Andromed® terdiri dari fosfolipid, tris-(hidroksimetil)-aminometan, asam sitrat, fruktosa, gliserol, tilosin tartrat,
20
Menurut Minitub (2001), komposisi kimia bahan pengencer Andromed® tersusun dari beberapa bahan yang dibutuhkan oleh spermatozoa selama proses
pembekuan, diantaranya natrium dan kalium. Kedua bahan tersebut berperan
dalam menjaga integritas fungsional membran plasma spermatozoa. Kalium juga
perperan dalam menginduksi motilitas dan hiperaktivasi spermatozoa, serta dapat
memengaruhi daya tahan hidup spermatozoa.
G. Pembekuan Semen
Menurut Toelihere (1993), pembekuan adalah suatu proses sperma yang telah
mengalami ekuilibrasi dan kemudian dimasukkan dalam kontainer berisi nitrogen
cair dengan suhu -196oC, sehingga sel spermatozoa dapat bertahan hidup dalam waktu yang lama. Menurut Partodiharjo (1992), pembekuan dapat dilakukan
dengan menggunakan es kering, cairan udara, O2 cair, dan N2 cair. N2 cair yang
paling banyak digunakan sebab dapat membekukan pada suhu yang paling rendah
dan dapat menyimpan semen dalam waktu yang lama. Kombinasi es kering dan
kristal CO2 dapat mencapai titik -70oC, cairan N2 suhunya -196oC, sedangkan CO2
cair dan udara cair suhunya -190oC.
Proses pembekuan dilakukan di atas permukaan N2 cair di dalam storage
container dengan suhu -110oC sampai dengan -120oC selama 9 menit. Suhu
tersebut diperoleh bila straw yang disusun di atas rak yang ditempatkan kurang
lebih 4 cm di atas permukaan N2 cair. Setelah pembekuan, semen beku disimpan
di dalam storage container yang berisi N2 cair (Nilna, 2010).
Proses pembekuan semen meliputi tiga tahap yaitu pendinginan (cooling),
21
pendinginan semen setelah diencerkan, dimasukkan dalam gelas ukur tertutup dan
ditempatkan pada beaker glass berisi air (water jacket). Tabung-tabung yang
berisi semen yang telah diencerkan tersebut kemudian dimasukkan dalam
refrigerator (Lindsay et al., 1982).
Proses pendinginan pada suhu 5°C akan menyebabkan penurunan motilitas
spermatozoa akibat adanya asam laktat sisa metabolisme sel yang menyebabkan
kondisi medium menjadi semakin asam karena penurunan pH. Kondisi ini dapat
bersifat racun terhadap spermatozoa yang akhirnya menyebabkan kematian
spermatozoa (Sugiarti et al., 2004).
Pada proses pre freezing, straw yang telah berisi semen diatur pada rak straw dan
ditempatkan sekitar 4,5 cm diatas permukaan nitrogen cair (Toelihere, 1985).
Freezing merupakan proses penghentian sementara kegiatan hidup sel tanpa
mematikan fungsi sel dan proses hidup dapat berlanjut setelah pembekuan
dihentikan (Partodiharjo, 1992).
Berdasarkan Peraturan Direktur Jenderal Peternakan
Nomor:1220/HK.060/F/12/2007 tentang Petunjuk Teknis Produksi dan Distribusi
Semen Beku, proses pembekuan semen dilakukan melalui dua tahap yaitu
pra pembekuan dan pembekuan.
1. Pra pembekuan (pre freezing)
Pre freezing dilakukan di dalam storage container, straw disusun di atas rak
22
2. Pembekuan (freezing)
Freezing dilakukan setelah pre freezing, straw diletakkan pada kontainer
dalam goblet dan canister, kemudian direndam dalam N2 cair dengan suhu
-196oC.
Proses pembekuan dapat menyebabkan perubahan kualitas semen beku yang
dihasilkan. Perubahan kualitas yang sering dihadapi umumnya berkisar pada dua
fenomena yaitu pengaruh cold shock terhadap sel yang dibekukan dan
perubahan-perubahan intraseluler akibat pengeluaran air saat pembentukkan kristal-kristal es.
Kristal-kristal es yang terbentuk saat proses pembekuan semen dapat merusak
spermatozoa. Konsentrasi elektrolit yang berlebihan akan melarutkan selubung
lipoprotein pada dinding sel spermatozoa sehingga permeabilitas membran sel
akan berubah dan menyebabkan kematian sel. Spermatozoa sapi banyak
mengalami kerusakan pada suhu-suhu kritik antara -1,5oC dan -30oC. Kerusakan spermatozoa rata-rata terjadi pada suhu -17oC. Kerusakan sebanyak 20% dari seluruh spermatozoa pada waktu pembekuan masih dianggap memuaskan
(Toelihere, 1993).
Menurut Maxwell dan Watson (1996), pada saat proses pembekuan semen terjadi
kerusakan membran plasma spermatozoa akibat terbentuknya peroksidasi lipid.
Keadaan ini terjadi karena membran plasma spermatozoa banyak mengandung
asam lemak tidak jenuh yang sangat rentan terhadap kerusakan peroksidasi
tersebut.
Menurut Situmorang (2002), penurunan motilitas spermatozoa setelah
23
masing-masing bangsa dan pejantan. Kedua senyawa tersebut merupakan
komponen membran. Phospolipid berfungsi untuk melindungi sel spermatozoa
dari cold shock. Sedangkan kolesterol berperan penting dalam menjaga integritas
sel spermatozoa dari variasi sistem membran yang bertambah selama proses
III. METODE PENELITIAN
A. Waktu dan Tempat Penelitian
Penelitian ini dilaksanakan pada April 2014 di Balai Inseminasi Buatan Daerah
(BIBD) Lampung, Kecamatan Terbanggi Besar, Kabupaten Lampung Tengah,
Provinsi Lampung.
B. Alat Penelitian
Peralatan yang digunakan dalam penelitian ini meliputi peralatan freezing (box
freezing lengkap, kontainer nitrogen cair, rak hitung, timer, pinset panjang),
peralatan thawing (pemanas air, pinset, beaker glass 1000 ml, thermometer,
timer), dan peralatan pemeriksaan kualitas (gunting, kertas label, mikroskop, pipet
tetes, object glass, cover glass, hair dryer, counter number).
C. Bahan Penelitian
Bahan yang digunakan dalam penelitian ini adalah semen Sapi Simmental; NaCl
fisiologis; media pengencer Andromed®; aqua bidestilata; nitrogen cair untuk pembekuan dan penyimpanan semen beku; air hangat (suhu 37oC) untuk thawing; eosin 2% untuk membuat preparat apus dalam menentukan persentase
25
D. Rancangan Penelitian
Rancangan dasar yang digunakan dalam penelitian ini adalah Rancangan Acak
Lengkap (RAL) dengan 5 perlakuan taraf waktu pre freezing dan setiap perlakuan
diulang sebanyak 4 kali. Pengambilan sampel straw dilakukan secara acak. Semen
yang berasal dari satu ekor Sapi Simmental dibagi menjadi lima kelompok
perlakuan waktu pre freezing (5 menit, 6 menit, 7 menit, 8 menit, 9 menit). Data
yang diperoleh dari hasil pengamatan disajikan dalam bentuk tabel dan kemudian
dilakukan analisis secara statistik. Analisis data yang digunakan dalam penelitian
ini adalah analisis sidik ragam dengan taraf nyata 5% atau 1%. Apabila hasilnya
berbeda nyata maka akan dilanjutkan dengan uji polinomial ortogonal pada taraf
5% atau 1% menurut Steel dan Torrie (1991).
E. Pelaksanaan Penelitian
Pelaksanaan penelitian dimulai dengan menampung semen dari pejantan Sapi
Simmental menggunakan vagina buatan (artificial vagina), selanjutnya dilakukan
evaluasi semen segar secara makroskopis (volume, konsistensi, warna, bau) dan
mikroskopis (gerakan massa, gerakan individu, konsentrasi). Semen segar yang
memenuhi syarat kemudian diencerkan dengan pengencer Andromed® secara merata. Selanjutnya dilakukan ekuilibrasi terhadap semen yang telah diencerkan.
Pemeriksaan post ekuilibrasi dilakukan setelah ekuilibrasi selesai. Semen yang
memenuhi standar akan dilanjutkan proses filling, sealing, dan printing. Langkah
selanjutnya yaitu melaksanakan sampling terhadap straw berisi semen sapi
26
pre freezing yang direncanakan (5 menit, 6 menit, 7 menit, 8 menit, dan 9 menit).
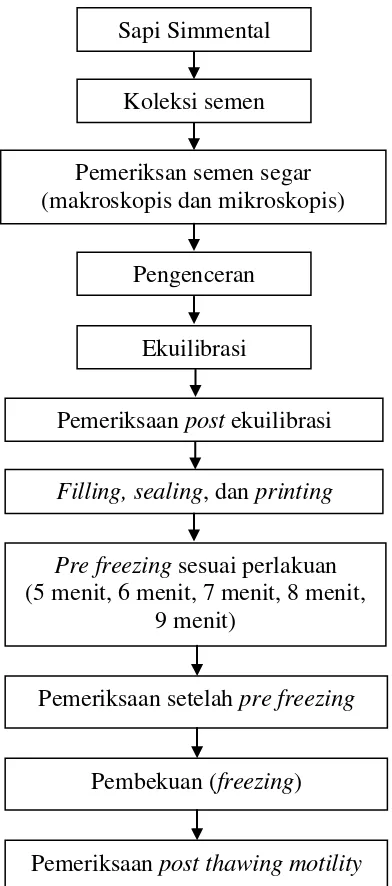
Bagan pelaksanaan penelitian dapat dilihat pada Gambar 1.
Gambar 1. Bagan pelaksanaan penelitian
Proses pembuatan semen beku sebagai berikut:
1. melakukan penampungan semen menggunakan vagina buatan;
2. melakukan evaluasi terhadap semen segar (makroskopis dan mikroskopis); Ekuilibrasi
Sapi Simmental
Koleksi semen
Pengenceran
Filling, sealing, dan printing
Pemeriksaan post ekuilibrasi
Pre freezing sesuai perlakuan
(5 menit, 6 menit, 7 menit, 8 menit, 9 menit)
Pemeriksan semen segar (makroskopis dan mikroskopis)
Pemeriksaan setelah pre freezing
Pembekuan (freezing)
27
3. mencampurkan semen yang memenuhi syarat dengan pengencer Andromed® ke dalam beaker glass;
4. menutup beaker glass yang berisi semen yang telah diencerkan menggunakan
alumunium foil dan memasukkannya ke dalam cool top bersuhu 3 − 5 oC;
5. melakukan proses ekuilibrasi selama 4 jam di dalam cool top;
6. setelah ekuilibrasi selesai dilanjutkan dengan pemeriksaan post ekuilibrasi;
7. proses filling,sealing, dan printing;
8. meletakkan straw yang berisi semen cair di atas rak hitung yang telah diberi
label sesuai perlakuan;
9. memasukkan N2 cair sebanyak 7,5 liter ke dalam box freezing dengan ukuran
panjang 43 cm dan lebar 27 cm;
10.melakukan pre freezing dengan cara memasukkan rak hitung yang berisi straw
semen cair di atas permukaan N2 cair dalam box freezing selama perlakuan
waktu yang diberikan (5 menit, 6 menit, 7 menit, 8 menit, 9 menit);
11.setelah pre freezing selesai dilanjutkan dengan pemeriksaan setelah
pre freezing;
12.mengambil straw menggunakan pinset dan mencelupkannya ke dalam
nitrogen cair sampai terendam;
13.setelah pembekuan selesai, dilanjutkan dengan pemeriksaan post thawing
motility;
14.melakukan pengumpulan data parameter yang diamati yaitu persentase
motilitas spermatozoa dan persentase spermatozoa hidup pada setiap
28
Prosedur yang dilakukan untuk melihat motilitas individu spermatozoa sebagai
berikut:
1. meneteskan sampel semen diatas object glass kemudian ditutup dengan cover
glass;
2. mengamati motilitas spermatozoa menggunakan mikroskop dengan
perbesaran lemah (10 × 10) atau perbesaran sedang (10 × 40);
3. menentukan persentase motilitas spermatozoa sesuai dengan kriteria penilaian
gerakan individu spermatozoa menurut Toelihere (1981) sebagai berikut:
0% : spermatozoa tidak bergerak;
0 − 30% : gerakan berputar ditempat, pergerakan progresif;
30 − 50% : gerakan berayun atau melingkar, pergerakan progresif;
50 − 80% : ada gerakan massa, pergerakan progresif;
80 − 90% : ada gelombang, pergerakan progresif;
90 − 100% : gelombang sangat cepat, pergerakan sangat progresif;
Prosedur yang dilakukan untuk menghitung persentase spermatozoa hidup sebagai
berikut:
1. melakukan thawing;
2. meneteskan semen beku pada salah satu ujung gelas obyek;
3. menambahkan satu tetes eosin 2% pada bagian yang sama;
4. menempelkan ujung gelas obyek yang lain pada kedua cairan sehingga
keduanya bercampur, kemudian didorong ke ujung gelas obyek;
5. mengeringkan preparat ulas tersebut menggunakan hair dryer;
6. setelah kering, melakukan pemeriksaan spermatozoa yang hidup dan mati
29
(10 × 100), spermatozoa yang hidup tetap tidak berwarna sedangkan
spermatozoa yang mati akan berwarna merah atau merah muda.
7. menghitung persentase spermatozoa hidup dengan rumus berikut.
Spermatozoa hidup (%) =
F. Peubah yang Diamati
Peubah yang diamati pada penelitian ini adalah persentase motilitas spermatozoa
V. SIMPULAN DAN SARAN
A. Simpulan
Berdasarkan hasil penelitian yang telah dilakukan, dapat diambil kesimpulan:
1. variasi waktu pre freezing tidak memberikan pengaruh yang nyata terhadap
persentase motilitas spermatozoa dan persentase spermatozoa hidup setelah
pre freezing, tetapi memberikan pengaruh yang sangat nyata terhadap
persentase motilitas spermatozoa dan persentase spermatozoa hidup post
thawing;
2. waktu pre freezing terbaik yang dapat mempertahankan motilitas individu
spermatozoa dan persentase spermatozoa hidup semen beku Sapi Simmental
yang menggunakan pengencer Andromed® terdapat pada perlakuan pre-
freezing selama 9 menit.
B. Saran
Saran yang diberikan adalah:
1. perlu dilakukan penelitian yang serupa dengan waktu pre freezing yang lebih
lama dari 9 menit sehingga dapat diketahui kualitas spermatozoa maksimum
yang dapat meningkatkan keberhasilan IB;
2. melakukan proses pre freezing selama 9 menit agar diperoleh kualitas terbaik
DAFTAR PUSTAKA
Bearden, H. J., and J. W. Fuquay. 2000. Applied Animal Reproduction 5th Ed. Prentice Hall. Upper Saddle River. New Jersey
Blakely, J. dan D. H. Bade. 1991. Ilmu Peternakan Edisi ke-4. Terjemahan: B. Srigandono. Gadjah Mada University Press. Yogyakarta
Direktorat Jenderal Peternakan. 2007. Petunjuk Teknis Produksi dan Distribusi Semen Beku. Direktorat Jenderal Peternakan. Jakarta
Feradis. 2010. Bioteknologi Reproduksi pada Ternak. Alfabeta. Bandung
Garner, D. L. and E. S. E. Hafez. 2000. Spermatozoa and Seminal Plasma in Reproduction in Farm Animals Edited by E. S. E. Hafez. 7th Ed. Lippincott Wiliams and Wilkins. Philadelphia
Hafez, E. S. E. 1993. Reproduction in Farm Animal 5th Ed. Lea and Febiger, Philadelphia
Hafez, E. S. E. 2000. Semen Evaluation in Reproduction In Farm Animals 7th Ed. Lippincott Wiliams and Wilkins. Philadelphia
Herdis, M. Surachman, Yulnawati, M. Rizal dan H. Maheshwari. 2008. Viabilitas dan keutuhan membran plasma spermatozoa epididimis kerbau belang pada penambahan maltosa dalam pengencer andromed®. Jurnal Pengembangan Peternakan Tropis. http://eprints.undip.ac.id/18998/1/33%282%292008p101-106.pdf. Diakses 14 September 2013. 33(2): 101 – 106
Hunter, R. H. F. 1995. Fisiologi dan Teknologi Reproduksi Hewan Betina Domestik. Alih bahasa oleh D. K. Harya Putra. Institut Teknologi Bandung. Bandung
Kusuma, D. L. 1990. Pengaruh Berbagai Pengencer Susu dan Lahan
46
Kuswanto, S. Suharyati dan P. E. Santoso. 2007. Pengaruh Penggunaan Andromed®, Stock Solution, dan Susu Skim Sebagai Bahan Pengencer Terhadap Kualitas Semen Cair Sapi Limousin Selama Penyimpanan. Kumpulan Abstrak Skripsi. Jurusan Peternakan. Fakultas Pertanian. Universitas Lampung. Bandar Lampung
Lindsay, K. W., Entwistle dan A. Winantea. 1982. Reproduksi Ternak di Indonesia. Fakultas Peternakan dan Perikanan. Universitas Brawijaya. Malang
Maxwell, W. M. C. and P. F. Watson. 1996. Recent progress in the preservation of ram semen. J. Anim. Reprod. Sci. 42: 55 − 65
Minitub. 2001. Certificate Andromed. Minitub Abfullund Labortechnik GmbH and Co KG. Germany
Nilna. 2010. Standar Operasional Pekerjaan Prosesing Semen. Pengawas Mutu Bibit Ternak pada Dinas peternakan. Sumatera Barat
Pane, I. 1993. Pemuliabiakan Ternak Sapi. PT. Gramedia Utama. Jakarta
Pangestu, M. 2002. Preservation of spermatozoa: methods and applications. Indonesian Forum on Reproduction. Journal on Reproduction. 1(2): 55 − 56
Parrish, J. 2003. Techniques in domestic animal reproduction-evaluation and freezing of semen. http://www.wisc.edu/ansci_repro/. Diakses 14 September 2013
Partodiharjo, S. 1992. Ilmu Reproduksi Hewan. Mutiara. Jakarta
Ridwan, 2008. Pengaruh jenis pengecer semen terhadap motilitas, abnormalitas dan daya tahan hidup spermatozoa ayam buras pada penyimpanan suhu 5oC. Jurnal Agroland. 15(3): 229 − 235
Rizal, M. dan Herdis. 2008. Inseminasi Buatan pada Domba. Rineka Cipta. Jakarta
Salisbury, G. W. dan N. L. VanDenmark. 1985. Fisiologi Reproduksi dan
Inseminasi Buatan pada Sapi. Penerjemah R. Januar. Gadjah Mada University Press. Yogyakarta
47
Samsudewa, D. dan A. Suryawijaya. 2008. Pengaruh Berbagai Metode Thawing
Terhadap Kualitas Semen Beku Sapi. Seminar Nasional Teknologi Peternakan dan Veteriner. http://peternakan.litbang.deptan.go.id/fullteks semnaspro08-13.pdf. Diakses 14 September 2013. 1: 88 – 92
Situmorang, P. 2002. Pengaruh penambahan eksogenous phospholipid ke dalam pengencer tris dengan tingkat kuning telur yang berbeda pada daya hidup spermatozoa sapi. http://peternakan.litbang.deptan.go.id/fullteks/jitv/jitv73-7.pdf. Diakses 14 September 2013. JITV 7(3): 181 − 187
Srianto, P., S. Fatimah, R. B. Utomo dan I. N. Triana. 2013. Motilitas dan persentase hidup spermatozoa sapi friesian holstein post thawingdalam pengencer skim kuning telur, tris kuning telur dan andromed®.
http://journal.unair.ac.id/filerPDFVETMED%20EDISI%20%2016%202013-10.pdf. Diakses 14 September 2013. 6(1): 51 – 54
Srigandono, B. 1996. Kamus Istilah Peternakan. Gadjah Mada University Press. Yogyakarta
Steel, R. G. D. dan J. H. Torrie. 1991 . Prinsip dan Prosedur Statistika. Penerjemah B. Sumantri. PT. Gramedia Utama. Jakarta
Sugeng, Y. B. 1998. Beternak Sapi Potong. Penebar Swadaya. Jakarta
Sugiarti, T., E. Triwulanningsih, P. Situmorang, R. G. Sianturi dan D. A.
Kusumaningrum. 2004. Penggunaan Katalase dalam Produksi Semen Dingin Sapi. Puslitbang Peternakan. Bogor
Susilawati, T., P. Srianto, Hermanto dan E. Yuliani. 2003. Inseminasi Buatan dengan Spermatozoa Beku Hasil Sexing pada Sapi Untuk Mendapatkan Anak dengan Jenis Kelamin Sesuai Harapan. Laporan Penelitian. Fakultas
Peternakan Universitas Brawijaya. Malang
Susilorini, E. T. 2008. Budi Daya 22 Ternak Potensial. Penebar Swadaya. Jakarta
Suyadi dan Susilawati. 1992. Pengantar Fisiologi Reproduksi. LUW Animal Husbandry Project Universitas Brawijaya. Malang
Toelihere, M. R. 1985. Fisiologi Reproduksi pada Ternak. Angkasa. Bandung
Toelihere, M. R. 1993. Inseminasi Buatan pada Ternak. Angkasa. Bandung
48
Wahyu, J. 2008. Manajemen Mutu Semen Beku Sapi di Balai Inseminasi Buatan (BIB) Lembang Bandung. Skripsi. Fakultas Peternakan. Institut Pertanian Bogor. Bogor
Yudhaningsih, H. 2004. Kualitas dan Integritas Membran Spermatozoa Sapi Madura Menggunakan Motilitas dan Pengencer yang Berbeda Selama Proses Pembekuan Semen. Skripsi. Fakultas Peternakan. Universitas Brawijaya. Malang