PEMERIKSAAN KADAR SERUM TRANSFERRIN
RECEPTOR (sTfR) UNTUK DIAGNOSTIK ANEMIA
DEFISIENSI BESI
T E S I S
OLEH:
PITA OMAS LUMBAN GAOL
DEPARTEMEN PATOLOGI KLINIK
FAKULTAS KEDOKTERAN USU / RSUP H. ADAM MALIK
MEDAN
PEMERIKSAAN KADAR SERUM TRANSFERRIN
RECEPTOR (sTfR) UNTUK DIAGNOSTIK ANEMIA
DEFISIENSI BESI
T E S I S
Diajukan Untuk Melengkapi Persyaratan Untuk Mencapai Keahlian Dalam Bidang Patologi Klinik Pada Fakultas Kedokteran
Universitas Sumatera Utara
OLEH:
PITA OMAS LUMBAN GAOL
DEPARTEMEN PATOLOGI KLINIK
FAKULTAS KEDOKTERAN USU / RSUP H. ADAM MALIK
MEDAN
2010
KATA PENGANTAR
Puji dan syukur saya ucapkan kepada Bapa yang di Surga oleh
karena kasih karuniaNya, sehingga saya dapat mengikuti Program
Pendidikan Dokter spesialis patologi klinik Fakultas Kedokteran Sumatera
utara dan dapat menyelesaikan Karya tulis (tesis) yang berjudul
Pemeriksaan Kadar Serum Transferrin Receptor (sTfR) untuk Diagnostik
Anemia Defisiensi Besi.
Selama saya mengikuti pendidikan dan proses penyelesaian
penelitian untuk karya tulis ini, saya telah banyak mendapat bimbingan,
petunjuk, bantuan dan pengarahan serta dorongan baik moril dan materil
dari berbagai pihak sehinggan saya dapat menyelesaikan pendidikan dan
karya tulis ini. Untuk semua itu perkenankanlah saya menyampaikan rasa
hormat dan terimakasih yang tiada terhingga kepada :
Yth, Prof. Adi Koesoema Aman, SpPK-KH, FISH, sebagai
pembimbing saya yang telah banyak memberikan bimbingan, petunjuk,
pengarahan, bantuan dan dorongan selama dalam pendidikan dan proses
penyusunan, sampai selesainya tesis ini. Saya juga sangat berterimakasih
kepada beliau selaku Ketua Departemen Patologi Klinik yang memberikan
kesempatan sebagai pesera Program Pendidikan Dokter Spesialis
Patologi Klinik.
Yth, Dr. Soegiarto Gani, SpPD, pembimbing II dari Department
pengarahan dan bantuan mulai dari penyusunsn proposal, selama
dilaksanakan penelitian sampai selesainya tesis ini.
Yth, Prof. DR. Dr. Ratna Akbarie ganie, SPPK-KH, FISH dan Dr.
Ricke Loesnihari SpPK-K, sebagai Ketua dan Sekretaris Program Studi di Departemen Patologi Klinik Fakultas Kedokteran Sumatera utara, yang
telah banyak membimbing, mengarahkan dan memotivasi sejak awal
pendidikan dan menyelesaikannya.
Yth, Prof. Herman Hariman, PhD, SpPk-KH, FISH, yang
memberikan bimbingan, pengarahan dan masukan selama saya mulai
pendidikan sampai menyelesaikan penulisan tesis ini.
Yth, Prof. Burhanuddin Nasution, SpPK-KN, FISH, yang banyak
memberikan bimbingan dan pengarahan selama pendidikan dan
menyelesaikan penulisan tesis ini
Yth, Prof. Dr. Iman Sukiman, SpPk-KH, FISH, Dr. R. Ardjuna M
Burhan, DMM, SpPK-K (Alm), Dr. Muzahar, DMM, SpPK-K, Dr. Zulfikar Lubis, SpPK-K, FISH, dr. Tapisari Tambunan, SpPK-KH, Dr. Ozar Sanuddin SpPK, Dr. Farida Siregar, SpPK, Dr. Ulfah Mahidin, SpPK, Dr. Chairul Rahmah, SpPk, Dr. Lina spPK dan Dr Nelly Elfrida SpPK, semuanya guru-guru saya yang telah banyak memberikan petunjuk,
arahan selama saya mengikuti pendidikan Spesialis Patologi Klinik dan
selama penyelesaian tesis ini. Hormat dan terimakasih saya ucapkan.
Yth, Drs. Abdul jalil Amri Arma, MKes, yang telah memberikan
memulai penelitian sampai selesainya tesis saya, terimakasih banyak
saya ucapkan.
Ucapan terimakasih juga saya ucapkan kepada seluruh
teman-teman sejawat Program Pendidikan Dokter Spesialis Patologi Klinik
Fakultas Kedokteran Universitas Sumatera Utara, para analis dan
pegawai, serta semua pihak yang tidak dapat saya sebutkan satu persatu,
atas bantuan dan kerja sama yang diberikan kepada saya, sejak mulai
pendidikan dan selesainya tesis ini.
Hormat dan terimakasih yang sebesar-besarnya kepada Bupati
Kabupaten Toba Samosir dan Kepala Dinas Kesehatan kabupaten Toba samosir, yang telah member izin kepada saya untuk mengikuti Program Studi Dokter spesialis patologi Klinik di Fakultas Kedokteran
Universitas Sumatera utara. Ucapan terimakasih juga kepada Dekan
Fakultas Kedokteran Universitas Sumatera Utara, Rektor Universitas
Sumatera Utara, Direktur rumah Sakit umum Pusat H. Adam Malik yang
telah memberikan kesempatan dan menerima saya untuk mengikuti
Program Pendidikan Dokter Spesialis Patologi Klinik.
Terimakasih yang setulus-tulusnya saya sampaikan kepada
ayahanda Ir. Osman lumban Gaol dan ibunda Nuri Sibarani, BA, yang
telah membesarkan, mendidik serta memberikan dorongan moril dan
materil kepada ananda selama ini. Begitu juga ucapan terimakasih yang
sebesar-besarnya kepada bapak Drs. BP Simatupang dan ibu mertua
materil kepada saya dan keluarga. Juga terimakasih saya kepada kakek
st W. Sibarani (Alm) yang masih memberangkatkan saya dalam doa sewaktu ujian seleksi masuk PPDS.
Akhirnya terimakasih yang tiada terhingga saya sampaikan kepada
suami tercinta Dr. sabam JMT Simatupang yang telah mendampingi
saya dengan penuh pengertian, perhatian, memberikan motivasi dan
pengorbanan selama saya mengikuti pendidikan sampai saya dapat
menyelesaikan pendidikan ini. Juga untuk anak-anakku yang tersayang
Roni, Aryani, Grace dan Peter yang telah banyak kehilangan perhatian dan kasih sayang selama saya mengikuti pendidikan.
Semoga tesis ini bermanfaat bagi kita semua. Dan semoga Tuhan
Yang Maha Kuasa memberkati kita semua.
Medan, Juli 2010
Penulis,
DAFTAR ISI
Kata pengantar... Daftar isi ……….. Daftar gambar dan tabel... Daftar lampiran ……….. Daftar singkatan ………... Abstrak ... Ringkasan...
BAB I. PENDAHULUAN
1.1. Latar Belakang ………...
1.2. Perumusan Masalah………..
1.3. Hipotesa Penelitian ……… 1.4. Tujuan Penelitian
1.4.1. Tujuan Umum ………... 1.4.2. Tujuan Khusus ……… 1.5. Manfaat Penelitian ………... 1.6. Kerangka konsep………
BAB II. Tinjauan Kepustakaan
2.1. Serum Transferrin Receptor ………...
2.2. Anemia Defisiensi Besi ...
2.3. Mekanisme Transport Besi ...
2.4. Stadium Klinis Defisiensi Besi dan Diagnosis Laboratorium ...
2.5. Perubahan Metabolisme Besi Pada Anemia Penyakit Kronis ...
2.6. Metode pemeriksaan sTfR………
BAB III. Metode Penelitian
3.1. Desain Penelitian ……….
3.2. Tempat dan Waktu Penelitian ………
3.3. Populasi dan Sunyek Penelitian
3.3.1. Populasi Penelitian ……… 3.3.2. Subyek Penelitian ………..
3.4. Perkiraan Besar Sampel ………...
3.5. Bahan dan Cara Kerja
3.5.1. Bahan yang diperlukan……….. 3.5.2. Anamnese dan pemeriksaan fisik……….
3.5.3. Pengambilan dan pengolahan sampel………
3.5.4. Pemeriksaan laboratorium……….
3.5.4.1. Pemeriksaan darah lengkap ……….
3.6. Ethical Clearance dan Informed Consent ……….
3.7. Analisa Data ……… 3.8. Batasan operasional………... 3.11. Kerangka operasional……….
BAB IV. HASIL PENELITIAN………..
BAB V. PEMBAHASAN………
BAB VI. KESIMPULAN DAN SARAN...
DAFTAR PUSTAKA ………. 29 30 33
DAFTAR GAMBAR DAN TABEL
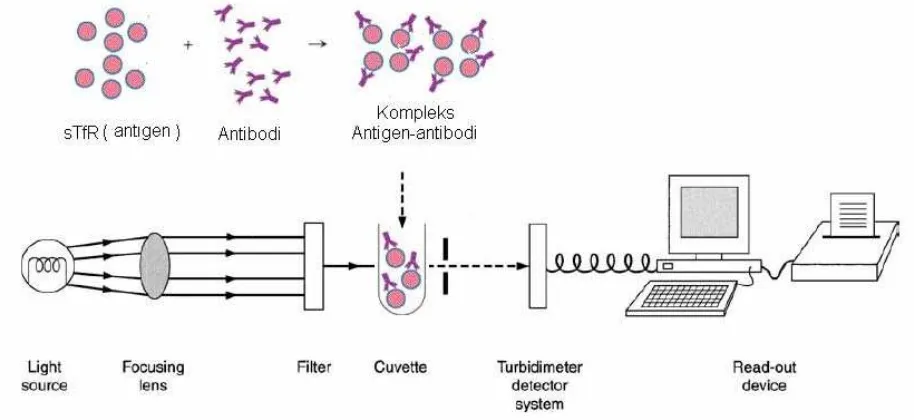
Gambar 2.1. Skema reaksi imunoturbidimetri 19
Grafik 3.1. Grafik kalibrator preciset sTfR 28
Tabel 3.1. Pemantapan kualitas menggunakan sTfR
control set level 1 dan sTfR control set level 2. 29
Tabel 4.1. Karakteristik subjek penelitian kelompok ADB
dan APK
35
Tabel 4.2. Perbandingan parameter hematologi pada
ADB dan APK
36
Tabel 4.3. Perbandingan parameter hematologi pada
APK dengan
indeks sTfR-F < 1,5 (APK murni) dengan indeks sTfR > 1,5 (ADB bersamaan APK).
37
Tabel 4.4. Perbandingan parameter hematologi pada
ADB dan ADB bersamaanAPK
DAFTAR LAMPIRAN
Lampiran 1 Lampiran 2
Formulir persetujuan setelah penjelasan Status penelitian
Lampiran 3 Surat persetujuan Komite Etik Penelitian bidang
Kesehatan FK-USU
Lampiran 4 Data penelitian pasien ADB dan APK.
DAFTAR SINGKATAN
Anemia Defisiensi Besi Serum Iron
Transferrin Saturation Total Iron Binding Capacity Anemia Penyakit Kronis Serum Transferrin Receptor Transferrin receptor
Serum Transferrin Receptor - Ferritin Hemoglobin
Mean Corpuslcular Volume World Health Organization C reactive Protein
Duodenal Cytochrome B Divalent Metal Transporter 1 Mean Corpuscular Hemoglobin
Mean Corpuscular Hemoglobin Consentration
Interferron -
Tumor Necroting Factor - α
ABSTRAK
Latar belakang dan tujuan penelitian: Anemia defisiensi besi (ADB) sering bersamaan dengan anemia penyakit kronis (APK) dan keduanya memberikan gambaran penurunan besi serum. Untuk membedakan ADB dan APK kadang-kadang sulit, khususnya ketika ADB yang bersamaan dengan APK. Pada keadaan kebutuhan besi meningkat dan peningkatan proliferasi sel maka ekspresi transferrin receptor (TfR) pada membran sel meningkat. Penelitian dilakukan bertujuan mengevaluasi kegunaan serum transferrin receptor (sTfR) dan indeks sTfR-Feritin untuk mendiagnosa ADB.
Hasil: Nilai sTfR dan indeks sTfR-F pada ADB murni lebih tinggi dibandingkan total APK. Nilai sTfR dan indeks sTfR-F pada kombinasi APK dengan ADB lebih tinggi dibandingkan APK murni.
Kesimpulan: Pemeriksaan sTfR dan indeks sTfR-F dapat membedakan ADB dengan APK. Pemeriksaan ini juga dapat
RINGKASAN
Anemia defisiensi besi (ADB) merupakan masalah klinis yang
dalam beberapa keadaan relatif mudah didiagnosa dengan menggunakan
pemeriksaan laboratorium status besi konvensional seperti serum iron,
total iron binding capacity (TIBC), saturasi transferin dan serum feritin.
Serum iron mengalami variasi diurnal, nilai TIBC pada keadaan inflamasi
dan hypoalbuminemia menurun, feritin berperan sebagai protein fase akut.
Pewarnaan besi sumsum tulang dengan Prussian blue merupakan marker
pasti, akan tetapi tidak praktis, tidak nyaman dan sulit dilakukan.
Anemia defisiensi besi sering bersamaan dengan APK dan
keduanya memberikan gambaran penurunan besi serum. Untuk
membedakan ADB dan APK kadang-kadang sulit, khususnya pada ADB
awal atau ketika ADB yang bersamaan dengan penyakit kronis. Nilai feritin
serum yang lebih rendah dari 15 ug/L kemungkinan besar merupakan
ADB meskipun bersamaan dengan inflamasi. Dan nilai feritin serum yang
meningkat diatas normal (>150-200 ug/L) kemungkinan besar bukan
ADB meskipun dengan inflamasi. Nilai feritin serum antara kedua level ini
(15-150 ug/L) dan dalam keadaan inflamasi membutuhkan pemeriksaan
lain untuk memastikan apakah dijumpai defisiensi besi. Sebab itu
pemeriksaan parameter besi yang lain diperlukan untuk membedakannya.
Transferrin receptor (TfR) merupakan protein transmembran yang
Transferin receptor (sTfR) yang larut dalam plasma berasal dari
ektodomain yang mengalami proteolisis. Konsentrasi sTfR sebanding
dengan jumlah TfR yang diekspresikan pada membran sel. Pada
keadaan kebutuhan besi meningkat dan peningkatan proliferasi sel maka
ekspresi TfR pada membran sel meningkat.
Penelitian dilakukan bertujuan mengevaluasi kegunaan sTfR dan
indeks sTfR-F untuk mendiagnosa ADB, dilaksanakan dari tanggal 24
Maret 2010 sampai 29 Mei 2010. Subjek penelitian adalah 36 orang
pasien ADB dan 36 orang APK yang berkunjung ke poliklinik Penyakit
Dalam dan yang dirawat di bangsal Penyakit Dalam Rumah Sakit Umum
Pusat H. Adam Malik Medan. Diagnosa ADB menurut kriteria WHO yaitu
laki-laki dewasa: Hb<13 g/dl, perempuan dewasa: Hb<12 g/dl dan nilai
feritin<15ug/L. Diagnosa APK dengan nilai Hb pada laki-laki dewasa <13
g/dl, perempuan dewasa Hb<12 g/dl, nilai feritin>15 ug/Ldan CRP positip.
Pasien yang mendapat terapi Fe, mendapat transfusi dalam 3 bulan
terakhir, anemia hemolitik, anemia megaloblastik, wanita hamil, anemia
dengan penyakit ginjal kronis, pasien dengan keganasan, anemia aplastik
dikeluarkan dari penelitian ini.
Pemeriksaan darah lengkap menggunakan alat cell dyne 3700,dan
morfologi darah tepi dengan pembuatan sediaan apus darah tepi dan
menggunakan pewarnaan giemsa. Pemeriksaan feritin dengan
menggunakan Cobas e 601 dengan prinsip electrochemiluminescence
(CRP) latex reagent set berdasarkan prinsip aglutinasi latex. Pemeriksaan
sTfR dengan menggunakan alat Cobas c 501 menggunakan metode
particle enhanced immunoturbidimetric assay. Nilai indeks sTfR-F dihitung
dengan membagi sTfR terhadap log feritin. Kontrol kualitas untuk feritin
dilakukan dengan elecsys PreciControl Tumor Marker 1 dan 2. Kontrol
kualitas untuk pemeriksaan CRP dengan mengikutkan kontrol CRP positif
dan negatif pada setiap melakukan pemeriksaan. Kontrol kualitas untuk
sTfr dilakukan dengan sTfR Control set, dengan memakai 2 nilai
konsentrasi yaitu sTfR control set level 1 dan sTfR control set level 2 untuk
memantau akurasi assay sTfR.
Pada penelitian ini, nilai sTfR dan indeks sTfR-F kelompok ADB
murni lebih tinggi dibandingkan kelompok total APK . Tetapi pemeriksaan
ini tidak memberi informasi tambahan untuk membedakan ADB murni dari
total APK. Karena parameter lain yaitu Hb, MCV, MCH, dan feritin juga
terdapat perbedaan yang bermakna.
Dengan menggunakan nilai indeks sTfR-F dengan cut-off 1,5, total
APK dibagi menjadi 2 bagian. Kelompok APK yang memiliki nilai indeks
sTfR-F <1,5 merupakan APK murni dan kelompok APK yang memiliki
nilai indeks sTfR-F >1,5 merupakan kombinasi APK dengan ADB. Nilai
sTfR dan nilai indeks sTfR-F kombinasi APK dengan ADB lebih tinggi
dibandingkan APK murni. Tidak dijumpai perbedaan yang bermakna pada
parameter lain yaitu Hb, MCV, MCH, MCHC dan feritin antara kelompok
Nilai sTfR dan indeks sTfR-F kelompok ADB murni lebih tinggi
dibandingkan kelompok kombinasi APK dengan ADB. Dijumpai perbedaan
bermakna pada nilai sTfR dan indeks sTfR-F antara ADB murni
dibandingkan kombinasi APK dengan ADB. Dijumpai juga perbedaan
yang bermakna antara parameter yaitu Hb, MCV, MCH. MCHC dan feritin,
ABSTRAK
Latar belakang dan tujuan penelitian: Anemia defisiensi besi (ADB) sering bersamaan dengan anemia penyakit kronis (APK) dan keduanya memberikan gambaran penurunan besi serum. Untuk membedakan ADB dan APK kadang-kadang sulit, khususnya ketika ADB yang bersamaan dengan APK. Pada keadaan kebutuhan besi meningkat dan peningkatan proliferasi sel maka ekspresi transferrin receptor (TfR) pada membran sel meningkat. Penelitian dilakukan bertujuan mengevaluasi kegunaan serum transferrin receptor (sTfR) dan indeks sTfR-Feritin untuk mendiagnosa ADB.
Hasil: Nilai sTfR dan indeks sTfR-F pada ADB murni lebih tinggi dibandingkan total APK. Nilai sTfR dan indeks sTfR-F pada kombinasi APK dengan ADB lebih tinggi dibandingkan APK murni.
Kesimpulan: Pemeriksaan sTfR dan indeks sTfR-F dapat membedakan ADB dengan APK. Pemeriksaan ini juga dapat
RINGKASAN
Anemia defisiensi besi (ADB) merupakan masalah klinis yang
dalam beberapa keadaan relatif mudah didiagnosa dengan menggunakan
pemeriksaan laboratorium status besi konvensional seperti serum iron,
total iron binding capacity (TIBC), saturasi transferin dan serum feritin.
Serum iron mengalami variasi diurnal, nilai TIBC pada keadaan inflamasi
dan hypoalbuminemia menurun, feritin berperan sebagai protein fase akut.
Pewarnaan besi sumsum tulang dengan Prussian blue merupakan marker
pasti, akan tetapi tidak praktis, tidak nyaman dan sulit dilakukan.
Anemia defisiensi besi sering bersamaan dengan APK dan
keduanya memberikan gambaran penurunan besi serum. Untuk
membedakan ADB dan APK kadang-kadang sulit, khususnya pada ADB
awal atau ketika ADB yang bersamaan dengan penyakit kronis. Nilai feritin
serum yang lebih rendah dari 15 ug/L kemungkinan besar merupakan
ADB meskipun bersamaan dengan inflamasi. Dan nilai feritin serum yang
meningkat diatas normal (>150-200 ug/L) kemungkinan besar bukan
ADB meskipun dengan inflamasi. Nilai feritin serum antara kedua level ini
(15-150 ug/L) dan dalam keadaan inflamasi membutuhkan pemeriksaan
lain untuk memastikan apakah dijumpai defisiensi besi. Sebab itu
pemeriksaan parameter besi yang lain diperlukan untuk membedakannya.
Transferrin receptor (TfR) merupakan protein transmembran yang
Transferin receptor (sTfR) yang larut dalam plasma berasal dari
ektodomain yang mengalami proteolisis. Konsentrasi sTfR sebanding
dengan jumlah TfR yang diekspresikan pada membran sel. Pada
keadaan kebutuhan besi meningkat dan peningkatan proliferasi sel maka
ekspresi TfR pada membran sel meningkat.
Penelitian dilakukan bertujuan mengevaluasi kegunaan sTfR dan
indeks sTfR-F untuk mendiagnosa ADB, dilaksanakan dari tanggal 24
Maret 2010 sampai 29 Mei 2010. Subjek penelitian adalah 36 orang
pasien ADB dan 36 orang APK yang berkunjung ke poliklinik Penyakit
Dalam dan yang dirawat di bangsal Penyakit Dalam Rumah Sakit Umum
Pusat H. Adam Malik Medan. Diagnosa ADB menurut kriteria WHO yaitu
laki-laki dewasa: Hb<13 g/dl, perempuan dewasa: Hb<12 g/dl dan nilai
feritin<15ug/L. Diagnosa APK dengan nilai Hb pada laki-laki dewasa <13
g/dl, perempuan dewasa Hb<12 g/dl, nilai feritin>15 ug/Ldan CRP positip.
Pasien yang mendapat terapi Fe, mendapat transfusi dalam 3 bulan
terakhir, anemia hemolitik, anemia megaloblastik, wanita hamil, anemia
dengan penyakit ginjal kronis, pasien dengan keganasan, anemia aplastik
dikeluarkan dari penelitian ini.
Pemeriksaan darah lengkap menggunakan alat cell dyne 3700,dan
morfologi darah tepi dengan pembuatan sediaan apus darah tepi dan
menggunakan pewarnaan giemsa. Pemeriksaan feritin dengan
menggunakan Cobas e 601 dengan prinsip electrochemiluminescence
(CRP) latex reagent set berdasarkan prinsip aglutinasi latex. Pemeriksaan
sTfR dengan menggunakan alat Cobas c 501 menggunakan metode
particle enhanced immunoturbidimetric assay. Nilai indeks sTfR-F dihitung
dengan membagi sTfR terhadap log feritin. Kontrol kualitas untuk feritin
dilakukan dengan elecsys PreciControl Tumor Marker 1 dan 2. Kontrol
kualitas untuk pemeriksaan CRP dengan mengikutkan kontrol CRP positif
dan negatif pada setiap melakukan pemeriksaan. Kontrol kualitas untuk
sTfr dilakukan dengan sTfR Control set, dengan memakai 2 nilai
konsentrasi yaitu sTfR control set level 1 dan sTfR control set level 2 untuk
memantau akurasi assay sTfR.
Pada penelitian ini, nilai sTfR dan indeks sTfR-F kelompok ADB
murni lebih tinggi dibandingkan kelompok total APK . Tetapi pemeriksaan
ini tidak memberi informasi tambahan untuk membedakan ADB murni dari
total APK. Karena parameter lain yaitu Hb, MCV, MCH, dan feritin juga
terdapat perbedaan yang bermakna.
Dengan menggunakan nilai indeks sTfR-F dengan cut-off 1,5, total
APK dibagi menjadi 2 bagian. Kelompok APK yang memiliki nilai indeks
sTfR-F <1,5 merupakan APK murni dan kelompok APK yang memiliki
nilai indeks sTfR-F >1,5 merupakan kombinasi APK dengan ADB. Nilai
sTfR dan nilai indeks sTfR-F kombinasi APK dengan ADB lebih tinggi
dibandingkan APK murni. Tidak dijumpai perbedaan yang bermakna pada
parameter lain yaitu Hb, MCV, MCH, MCHC dan feritin antara kelompok
Nilai sTfR dan indeks sTfR-F kelompok ADB murni lebih tinggi
dibandingkan kelompok kombinasi APK dengan ADB. Dijumpai perbedaan
bermakna pada nilai sTfR dan indeks sTfR-F antara ADB murni
dibandingkan kombinasi APK dengan ADB. Dijumpai juga perbedaan
yang bermakna antara parameter yaitu Hb, MCV, MCH. MCHC dan feritin,
BAB I PENDAHULUAN
1.1. Latar belakang
Anemia defisiensi besi (ADB) merupakan masalah klinis yang
dalam beberapa keadaan relatif mudah didiagnosa dengan menggunakan
pemeriksaan laboratorium status besi konvensional seperti serum iron
(SI), total iron binding capacity (TIBC), saturasi transferin dan serum
feritin.1 Serum iron menunjukkan variasi diurnal, dengan konsentrasi yang
lebih tinggi pada sore hari dibandingkan pagi hari.2,3 Pemeriksaan serum
feritin sangat efisien untuk menilai cadangan besi tubuh, akan tetapi feritin
berperan sebagai protein fase akut, sehingga sulit dibedakan antara ADB
dengan anemia karena infeksi, inflamasi dan keganasan, yang disebut
anemia penyakit kronis (APK).4,5 Pada ADB nilai TIBC meningkat, tetapi
dapat normal atau menurun pada keadaan inflamasi dan
hypoalbuminemia. 6 Pewarnaan Prussian blue sumsum tulang merupakan
marker pasti untuk defisiensi besi. Akan tetapi pemeriksaan ini tidak
nyaman, tidak praktis dan sulit dilakukan secara rutin. Selain itu,
pemeriksaan ini memerlukan waktu yang lebih lama dan biaya yang lebih
mahal, sehingga dibutuhkan pemeriksaan yang tidak invasif dan sensitif
untuk mendeteksi ADB. 7,8
Gambaran darah tepi ADB adalah mikrositer. Diferensial diagnosa
APK. Anemia defisiensi besi sering bersamaan dengan APK dan
keduanya memberikan gambaran penurunan besi serum. Untuk
membedakan ADB dan APK kadang-kadang sulit, khususnya pada ADB
awal atau ketika ADB yang bersamaan dengan penyakit kronis. 9
Nilai feritin serum yang rendah merupakan diagnosa untuk ADB.
WHO merekomendasikan konsentrasi feritin <12 ug/l mengindikasikan
deplesi cadangan besi pada anak-anak <5 tahun, dan nilai <15 ug/l
mengindikasikan deplesi cadangan besi pada umur >5 tahun.10,11
Penelitian Pasricha dkk mendapatkan dengan pemakaian cut-off feritin
<15 ug/l memberikan sensitivitas 44% dan spesifisitas 80%, dan cut-off
<30% memberikan sensitivitas 72% dan spesifisitas 52%.12 Penelitian di
Bali dengan memakai feritin serum <12 ug/l dan, 20 ug/l memberikan
sensitivitas dan spesifisitas masing-masing 68% dan 98% serta 68% dan
96%.13 Penelitian Mast AE dkk mendapatkan sensitivitas 25% dan
spesivisitas 98% dengan memakai feritin <12 ug/l. Akan tetapi dengan
memakai feritin < 30 ug/l diperoleh sensitivitas 92% dan spesifisitas
98%.14
Nilai feritin serum yang lebih rendah dari 15 ug/L kemungkinan
besar merupakan ADB meskipun bersamaan dengan inflamasi. Dan nilai
feritin serum yang meningkat diatas normal (>150-200 ug/L)
kemungkinan besar bukan ADB meskipun dengan inflamasi. Nilai feritin
serum antara kedua level ini (15-150 ug/L) dan dalam keadaan inflamasi
defisiensi besi. Prosedur diagnostik yang reliabel sangat penting karena
ADB membutuhkan evaluasi dengan seksama. Sebab itu pemeriksaan
parameter besi yang lain diperlukan untuk membedakannya.15
Transferrin receptor (TfR) merupakan protein transmembran yang
berikatan dengan transferin pada proses transportasi besi. Serum
Transferin receptor (sTfR) yang larut dalam plasma berasal dari
ektodomain yang mengalami proteolisis. Konsentrasi sTfR sebanding
dengan jumlah TfR yang diekspresikan pada membran sel. Pada
keadaan kebutuhan besi meningkat dan peningkatan proliferasi sel maka
ekspresi TfR pada membran sel meningkat. Pada beberapa penelitian,
pengukuran sTfR telah terbukti berguna untuk membedakan diagnosa
ADB dengan APK, dan konsentrasi sTfR tidak dipengaruhi respon protein
fase akut, sehingga sTfR lebih baik dibandingkan pengukuran status besi
konvensional. Dalam diferensial diagnosa ADB dan APK, interpretasi sTfR
lebih mudah dibandingkan konsentrasi feritin serum, karena peningkatan
konsentrasi sTfR diatas nilai batas referensi menunjukkan defisiensi besi
sementara pada APK dalam batas referensi.16
Dengan pemeriksaan feritin serum dan sTfR dapat dihasilkan nilai
indeks sTfR-F yaitu rasio sTfR/log feritin. Rasio ini sangat baik untuk
mengestimasi cadangan besi. Cut-off untuk indeks sTfR–F adalah 1,5.
Pada ADB indeks sTfR–F lebih besar dari 1,5 dan pada APK lebih kecil
Kari Punnonen dkk tahun 1996 di Finland meneliti kadar sTfR pada
anemia yang dibagi dalam 3 kelompok yaitu ADB, APK dan kombinasi
ADB dengan APK. sTfR pada ADB dan kombinasi ADB dengan APK lebih
tinggi dibanding APK. Karenanya sTfR indikator yang baik untuk defisiensi
besi.17
Simek M dkk tahun 2002 di Slovakia mendapatkan nilai sTfR pada
ADB lebih tinggi dibandingkan pada APK. Pada ADB kombinasi dengan
APK mempunyai nilai sTfR yang lebih tinggi dibandingkan dengan kontrol
normal dan APK. 18
Jayarenees S dkk tahun 2005 di Kuala Lumpur menilai 91 sampel
darah dengan anemia hipokrom mikrositer, yang dikelompokkan menjadi
ADB, APK dan talasemia. Nilai sTfR pada ADB signifikan lebih tinggi
dibanding kontrol normal, APK dan talasemia.1
1.2. Perumusan masalah
Berdasarkan latar belakang yang telah diuraikan di atas, maka dapat
dirumuskan beberapa masalah yaitu
1. Apakah dengan pemeriksaan sTfR dapat membedakan ADB
dengan APK?
2. Apakah perhitungan indeks sTfR-F dapat membedakan antara
1.3. Hipotesa penelitian
1. Kadar sTfR pada ADB lebih tinggi dibandingkan APK
2. Nilai indeks sTfR-F pada ADB lebih tinggi dibandingkan APK
1.4 Tujuan penelitian
1.4.1. Tujuan umum
Untuk mengevaluasi kegunaan sTfR dan indeks sTfR-F dalam
mendiagnosa ADB.
1.4.2. Tujuan khusus
1. Anemia defisiensi besi dapat dibedakan dari APK dengan
pemeriksaan sTfR.
2. Anemia Penyakit kronis yang bersamaan dengan ADB dapat
ditegakkan dengan pemeriksaan indeks sTfR-F.
1.5. Manfaat penelitian
Dengan pemeriksaan sTfR dan indeks sTfR-F dapat membedakan
ADB MURNI, ADB yang bersamaan APK dan APK MURNI, yang
1.6. Kerangka konsep
ADB MURNI Feritin < 15 ug/L
Feritin > 15 ug/L
Kriteria eksklusi Kriteria inklusi
sTfR & indeks sTfR –F ADB >APK
Indeks sTfR-F pada ADB + APK > APK
Kari Punnonen dkk Simek M dkk
Jayarenees S dkk
Anemia Kriteria WHO
CRP (+)
APK
sTfR &
BAB II
TINJAUAN KEPUSTAKAAN
2.1. Serum Transferrin receptor (sTfR)
Transferrin receptor merupakan transmembran homodimer yang
terdiri dari dua monomer yang identik, berat molekul sekitar 90 kDa,
dimana tiap monomer dihubungkan oleh ikatan 2 sulfida pada Cys89 dan
Cys98. Reseptor ini memiliki region sitoplasmik NH2-terminal (residu
1-67), single transmembrant pass (residu 68-88) dan bagian ektraseluler
yang besar (ektodomain, residu 89-760).19,20,21 Ektodomain larut dan
mengandung satu site yang sensitif trypsin, dan mengandung site untuk
berikatan dengan transferin. sTfR disintesa di retikulum endoplasma.19
Domain ekstraseluler memiliki tiga posisi N-linked glycosilation pada
Asn251, Asn317 dan Asn727 dan posisi O-linked glycosilation pada
Thr104. Posisi ini sangat penting untuk fungsi sTfR.19
Ektodomain merupakan homodimer yang berbentuk seperti
kupu-kupu. Tiap monomer terdiri dari tiga domain globular yang berbeda, yaitu
protease-like, apical dan helical domain, membentuk cleft lateral sehingga
dapat berikatan dengan molekul transferin.19,20,22 Ektodomain dipisahkan
dari membran oleh sebuah tangkai. Transferrin receptor berikatan dengan
dua molekul transferin dengan affinitas yang bervariasi. Protein dalam
bentuk diferik memiliki affinitas yang lebih tinggi dibandingkan bentuk
Transferin receptor diekspresikan pada semua sel yang berinti
seperti sel erytroid, hepatosit, sel intestinal, monosit (makrofag), otak ,
blood brain barrier, tetapi dalam jumlah yang berbeda. Pada sel yang
membelah dengan cepat dapat dijumpai 10.000 sampai 100.000 molekul
per sel, sebaliknya ekspresi TfR pada sel yang tidak berproliferasi sagat
rendah bahkan sering tidak dapat dideteksi.19
Jumlah TfR berbeda selama maturasi seri erytroid, mencapai
puncaknya pada normoblast polikromatofilik. Jumlah paling sedikit
dijumpai pada burst-forming unit-erythroid cells, dan sedikit meningkat
pada colony- forming unit-erythroid cells. Pada setiap sel normoblast
basofilik dijumpai 300.000 reseptor dam meningkat mencapai 800.000
pada tiap sel normoblast polikromatofilik. Tingkat uptake besi secara
langsung berhubungan dengan jumlah reseptor. Jumlah TfR berkurang
pada retikulosit, dimana sel erythroid melepaskan sisa TfR melalui
eksosotosis dan proteolisis. Jumlah reseptor yang lepas dapat dijumpai
pada plasma dalam konsentrasi tertentu yang berhubungan dengan laju
erythropoesis. Peningkatan sTfR merupakan indikator yang sensitif untuk
massa erytroid dan defisiensi besi jaringan.6
Kadar sTfR berubah selama ontogenesis, meningkat pada umur
20-42 minggu kehidupan fetal. Pada saat lahir kadar sTfR dua kali lebih
tinggi dari pada usia dewasa.23 Anak usia satu tahun memiliki nilai sTfR
korelasi dengan usia (19-79 tahun) dan tidak ada perbedaan antara
laki-laki dan perempuan atau perempuan pre dan post menopause.23,24
Pada anemia defisiensi besi nilai sTfR meningkat 3-5 kali lipat
dibandingkan orang normal. Kandungan besi tubuh pada orang yang
dilakukan phlebotomy secara kuantitatif menjadi berkurangnya, tetapi
sTfR masih relatif stabil dalam batas normal sampai cadangan menjadi
kosong. Pada saat kompartemen besi semakin deplesi, nilai sTfR
meningkat secara progresif berbanding terbalik dengan tingkat defisit
besi. Keadan ini mencerminkan peningkatan besar reseptor yang
diekspresikan tiap sel pada defisiensi besi.25
Feritin serum mempunyai keterbatasan dalam menilai status besi
pada anak-anak, masa pertumbuhan, kehamilan dan atlet, karena
cadangan besi biasanya berkurang pada masa ini. Karena faktor-faktor
lain yang mempengaruhi dapat terjadi peningkatan palsu kadar feritin,
sehingga konsentrasi sTfR merupakan penilaian yg baik. Kerusakan lever
akut dan inflamasi tidak mempunyai efek terhadap pengukuran kadar
sTfR. Maka sTfR dapat membedakan anemia karena penyakit kronis dan
inflamasi. Sebelum pemeriksaan sTfR dikembangkan hanya evaluasi
sumsum tulang untuk pewarnaan besi merupakan pemeriksaan yang
reliabel untuk membedakannya ADB dan APK. Pada keadaan dijumpai
kombinasi ADB dan APK, dengan pemeriksaan sTfR diketahui defisit besi
Serum transferrin receptor meningkat pada keadaan aktivitas
erytripoesis sumsum tulang yang meningkat meskipun tidak dijumpai
deplesi besi fungsional yaitu anemia hemolitik atau inefektif eritropoesis
seperti pada anemia megaloblastik, myelodisplasia, dan talasemia mayor.
Pada keadaan yang disebut di atas nilai feritin serum normal atau
meningkat. Pada anemia hemolitik dijumpai retikulositosis dan nilai MCV
normal atau meningkat. Anemia megaloblastik dan myelodisplasia pada
umumnya terjadi peningkatan MCV.19
Konsentrasi sTfR tetap normal pada APK. Ratio sTfR terhadap
feritin merupakan perkiraan kuantitatif jumlah besi di tubuh, dan indeks
sTfR-F secara langsung berbanding dengan jumlah cadangan besi.
Dengan menggunakan indeks sTfR-F, pemeriksaan pewarnaan sumsum
tulang dengan prussian blue besidapat berkurang pada pasien inflamasi
kronik untuk mengetahui apakah terdapat defisiensi.20 Dengan
pemeriksaan feritin dan sTfR dapat dihasilkan nilai indeks sTfR-F yaitu
rasio sTfR/log feritin. Rasio ini sangat baik untuk mengestimasi cadangan
besi. Cut-off untuk indeks sTfR–F adalah 1,5. Pada ADB indeks sTfR–F
lebih besar dari 1,5, dan pada APK lebih kecil dari 1,5.6
2.2. Anemia defisiensi besi
Anemia adalah keadaan dimana massa eritrosit dan/atau massa Hb
yang beredar di sirkulasi tidak dapat memenuhi fungsinya untuk
Menurut WHO, dikatakan anemia bila:27
Laki-laki dewasa Hb < 13 g/dl
Perempuan dewasa tidak hamil Hb < 12 g/dl
Perempuan hamil Hb < 11 g/dl
Anak umur 6-12 tahun Hb < 12 g/dl
Anak umur 6 bulan-6 tahun Hb < 11 g/dl
Anemia defisiensi besi adalah anemia yang timbul akibat
berkurangnya penyediaan besi untuk eritropoiesis, karena cadangan besi
kosong yang akhirnya mengakibatkan pembentukan Hb berkurang.13
Penilaian status besi merupakan tambahan pemeriksaan Hb dan
hematokrit (Ht), dan dapat dinilai dengan beberapa test yang telah
ditetapkan. Hanya saja tidak ada pemeriksaan tunggal yang standart
untuk menilai defisiensi besi tanpa anemia. Penggunaan test yang
beragam hanya sebagian mengatasi keterbatasan test tunggal dan
tidak menjadi pilihan pada keadaan sumber daya yang terbatas. Indikator
yang terbaik untuk deteksi defisiensi besi adalah feritin serum pada saat
tidak dijumpai infeksi.27,28
Feritin serum merupakan indikator yang terbaik untuk menilai
interfensi besi dan deplesi besi. WHO merekomendasikan konsentrasi
konsentrasi feritin < 12 ug/l mengindikasikan deplesi cadangan besi pada
anak-anak < 5 tahun, dan nilai < 15 ug/l mengindikasikan deplesi
cadangan besi pada umur > 5 tahun. Tetapi feritin merupakan protein fase
Pengukuran protein fase akut yang berbeda dapat membantu
menginterpretasi nilai serum feritin, jika konsentrasi protein fase akut ini
meningkat menandakan dijumpai inflamasi. Pemeriksaan protein fase akut
yang sering digunakan adalah CRP, karena meningkat dengan cepat
terhadap inflamasi dan juga turun dengan cepat. 28
2.3. Mekanisme transport besi
Besi merupakan ion yang bermuatan dan tidak dapat berdifusi
bebas melewati membrane sel, sehingga dibutuhkan protein karier spesifik
untuk transfer transmembran. Secara umum ada dua jalan transport
besi. Beberapa sel seperti sel epitel intestinal, hepatosit dan makrofag
dilengkapi keduanya yaitu mekanisme import besi ke dalam sel dan
pelepasan (eksport) besi dari luar sel. Sel-sel ini terlibat dalam
penerimaan, penyimpanan dan mobilisasi besi. Pada sel lain seperti
prekursor eritroid hanya terjadi import besi tetapi tidak melepaskannya
kecuali sel tersebut hancur. 29
Sekitar 25 mg besi dibutuhkan setiap hari untuk mendukung
produksi Hb pada eritrosit yang matur. Jumlah ini sangat besar
dibandingkan dengan 1-2 mg besi yang masuk ke dalam tubuh setiap hari.
Besi untuk eritropoiesis diperoleh dari makrofag retikuloendotelial yang
menjalankan fungsi siklus besi dari eritrosit tua. 29
Besi diabsorbsi dalam lingkungan asam pada mukosa duodenum
ferri (Fe3+) harus direduksi menjadi ferro (Fe2+) oleh ferrireductase, yang
diidentifikasi merupakan duodenal cytochrome b (DCYTB). Ion Fe 2+
melalui divalent metal transporter 1 (DMT1, disebut juga Nramp 2)
memasuki sitoplasma. Besi yang masuk dalam sitoplasma sebagian
disimpan dalam bentuk feritin, sebagian diloloskan melalui basolateral
transporter (ferroportin disebut juga IREG 1) ke dalam kapiler usus. Pada
proses ini terjadi perubahan dari feri menjadi fero oleh enzim ferooksidase,
antara lain hephaestin. 29,30.31
Di dalam plasma, besi berikatan dengan transferin. Transferin
mempunyai tiga fungsi penting. Pertama, menjaga besi dalam bentuk
terlarut. Kedua transferin membuat besi tidak reaktif sehingga menjadi
tidak toksik dalam sirkulasi. Ketiga, transferin memfasilitasi pengiriman
besi menuju sel yang memiliki transferin reseptor di permukaannya.29
Transferin mengirim besi ke normoblast dan sel-sel lain melalui
ikatan dengan transferin reseptor. Setelah interaksi reseptor dengan ligan,
transferin yang mengandung besi mengalami endositosis yang diawali
dengan invaginasi clathrin-coated pits, membentuk endosom. Endosom
mengalami asidifikasi (pH 5-6) melalui influks proton sehingga
memudahkan pelepasan besi dari transferin dan memperkuat interaksi
apotransferin-reseptor. Besi dirubah dari bentuk ferro menjadi ferri dan
keluar dari endosome melalui divalent metal ion transporter 1 (DMT1)
menuju tempat penyimpanan (feritin) dan digunakan dalam sel
eksternalisasi kembali ke permukaan sel dan apotransferin dilepaskan
kembali. 6,31
2.4. Stadium klinis defisiensi besi dan diagnosis laboratorium.
Karakteristik penting dari defisiensi besi adalah pelepasan besi dari
makrofag dan cadangan hepatosit bersama-sama dengan masukan dari
makanan tidak mencukupi kebutuhan besi untuk eritropoiesis. Pada fase
awal yang disebut juga defisiensi besi laten, semua cadangan besi akan
dimobilisasi. Pada keadaan ini semua parameter laboratorium masih
dalam batas normal, meskipun konsentrasi feritin dan cadangan besi di
sumsum tulang (feritin dan hemosiderin) berkurang secara bertahap.16
Reseptor transferin masih stabil.32
Fase kedua yang disebut eritropoesis defisiensi besi, cadangan
besi kosong sehingga jumlah besi tidak cukup untuk produksi Hb dan
protein lain yang mengandung besi. Konsentrasi Hb masih normal, tetapi
feritin serum menurun, SI rendah, transferin serum tinggi (akibatnya
saturasi transferin berkurang) dan terjadi peningkatan sTfR di plasma.16,32
Pada fase ketiga yaitu anemia defisiensi besi, kadar Hb sudah
berkurang. Pada keadaan kronik, dengan berkurangnya Hb lebih lanjut,
MCV dan MCH dapat menjadi rendah, bersamaan dengan munculnya
eritroblast patologis pada sumsum tulang dan morfologi eritrosit yang
patologis pada darah tepi.16 Penurunan feritin lebih berat dan peningkatan
Petunjuk pertama pada defisiensi besi adalah anemia, akan tetapi
penilaian Hb dan Ht memiliki spesifisitas dan sensitivitas yang rendah dan
dibutuhkan pemeriksaan laboratorium tambahan. Selain gambaran
laboratorium untuk erytropoesis defisiensi besi, pemeriksaan lain seperti
saturasi transferin, mean corpuscular hemoglobin consentration (MCHC),
erythrocyte zinc protoporphyrin, konsentrasi hemoglobin eritrosit dan
retikulosit dapat meningkatkan diagnosa. Akan tetapi perubahan dari
parameter ini pada defisiensi besi tidak dapat dibedakan dari APK. Hal ini
karena inflamasi menyebabkan peningkatan hepcidin sehingga
menghalangi pelepasan besi dari enterosit dan sistem retikuloendotelial
dan menghasilkan defisiensi besi eritropoeisis.16
Saturasi transferin memiliki kelebihan yaitu biaya yang murah dan
banyak tersedia, tetapi mengalami variasi diurnal dan dipengaruhi
beberapa kelainan klinis. Pemeriksaan darah tepi dapat dipercaya bila
diperiksa yang berpengalaman. MCV merupakan indikator yang dapat
dipercaya, tetapi parameter ini berubah tergantung onset defisiensi
eritropoeisis. Persentase eritrosit yang hipokrom dapat diukur dengan
hematology analyzer tertentu , tetapi merupakan indikator yang lambat
untuk mendeteksi eritropoeisis defisensi besi.16
Pendekatan diagnostik yang optimal untuk ADB dengan menilai
serum feritin dan sTfR. Pemeriksaan feritin serum tersedia luas dan
telah dibakukan dengan baik dan merupakan indeks status besi yang
WHO merekomendasikan konsentrasi feritin < 12 ug/l mengindikasikan
deplesi cadangan besi pada anak-anak < 5 tahun, dan nilai < 15 ug/l
mengindikasikan deplesi cadangan besi pada umur > 5 tahun.10,11
Penelitian Pasricha dkk mendapatkan dengan pemakaian cut-off feritin
<15 ug/l memberikan sensitivitas 44% dan spesifisitas 80%, dan cut-off <
30% memberikan sensitivitas 72% dan spesifisitas 52%.12 Penelitian di
Bali dengan memakai feritin serum < 12 ug/l dan 20 ug/l memberikan
sensitivitas dan spesifisitas masing-masing 68% dan 98% serta 68% dan
96%. 13 Penelitian Mast AE dkk mendapatkan sensitivitas 25% dan
spesivisitas 98% dengan memakai feritin < 12 ug/l. Akan tetapi dengan
memakai feritin < 30 ug/l diperoleh sensitivitas 92% dan spesifisitas
98%.14
Tetapi feritin merupakan protein fase akut dan pada keadaan
inflamasi akut atau kronis feritin meningkat tidak tergantung pada status
besi. Perbedaan antara APK dan ADB sangat sulit karena konsentrasi
feritin serum yang meningkat tidak mengeksklusi ADB yang bersamaan
dengan inflamasi. Sebaiknya pada negara berkembang dengan frekwensi
infeksi yang tinggi dilakukan pemeriksaan marker inflamasi seperti CRP.16
Dalam waktu relatif singkat (6-8) jam setelah terjadi reaksi radang akut /
kerusakan jaringan, sintesa dan sekresi CRP meningkat dengan tajam,
dan hanya dalam waktu 24-48 jam telah mencapai nilai puncaknya. Kadar
telah mereda. Dalam waktu sekitar 24-48 jam telah dicapai nilai normalnya
kembali.33
2.5. Perubahan metabolisme besi pada anemia penyakit kronis
Anemia penyakit kronis didefinisikan sebagai anemia yang terjadi
pada infeksi kronis, inflamasi atau neoplasma dan bukan oleh karena
adanya tumor pada sumsum tulang, perdarahan atau hemolisis, yang
ditandai dengan hypoferemia dan dijumpai cadangan besi.34
Disregulasi besi pada APK terjadi karena peningkatan hepcidin
sebagai respon terhadap sitokin yang meningkat karena inflamasi dan
juga karena efek langsung sitokin seperti IFN - dan TNF-α yang
merangsang makrofag untuk mengakusisi besi melalui DMT1 dan
menginhibisi feroportin 1 untuk melepaskan besi. Kedua mekanisme ini
menyebabkan sekuestrasi besi dalam fagosit mononuklear, sehingga
ketersediaan besi untuk eritropoesis berkurang.34,35 Gambaran ini tampak
melalui parameter hematologi yaitu, SI berkurang, saturasi transferin
berkurang < 16 %, dan nilai feritin serum normal hingga meningkat.
Pengukuran nilai sTfR dan indeks sTfR-F dapat membedakan ADB
dengan APK.16
2.6. Metode pemeriksaan sTfR
Metode yang umum dipakai untuk mengukur sTfR adalah enzyme
1.
Prinsip ELISA berdasarkan microplate sandwich enzyme
immunoassay menggunakan dua antibodi monoklonal spesifik
untuk sTfR. sTfR sebagai antigen berikatan dengan antibodi
monoklonal yang berada pada microplate. Setelah dicuci kemudian
ditambahkan antibodi monoklonal berkonjugasi dengan enzyme,
sehingga terjadi kompleks antibodi-sTfR-antibodi. Jumlah kompleks
ini sebanding dengan konsentrasi sTfR pada sampel. 37
Pemeriksaan dengan metode ELISA dilakukan secara manual,
sehingga cukup merepotkan , memerlukan banyak waktu dan
memerlukan peralatan khusus. Selain itu belum ada kalibrator yang
sama untuk penetapan nilai sTfR.38
2. Penelitian ini dilakukan dengan menggunakan metode
particle
enhanced immunoturbidimetric assay. sTfR dalam serum sebagai
antigen berikatan dengan antibodi soluble transferrin receptor yang
dilapisi dengan partikel lateks. Komplek antigen antibodi yang
terjadi diukur secara fotometer pada panjang gelombang 583 nm.39
Jumlah analit berbanding terbalik dengan jumlah sinar yang
diteruskan40. Partikel lateks berguna untuk memperbesar kompleks
imun sehingga terjadi amplifikasi reaksi dan sensitivitas reaksi
meningkat secara bermakna.41
Pemeriksaan dengan metode immunoturbidimetry dilakukan secara
dengan metode ELISA. Koefisien variasi intra dan interassay dua
sampai tiga kali lebih rendah dibandingkan dengan metode ELISA.
Akan tetapi metode ini memerlukan analyzer yang tidak dijumpai
pada semua laboratorium klinik. 38
BAB III
METODE PENELITIAN
3.1. Desain penelitian
Penelitian dilakukan dengan observasional analitik dengan cara
cross sectional (potong lintang). Pengambilan sampel dengan cara
consecutive sampling, dimana jumlah sampel dibatasi minimal sesuai
perkiraan jumlah sampel atau sampai batas waktu pengumpulan sampel
yang ditetapkan.
3.2. Tempat dan waktu penelitian
Penelitian dilakukan di Departemen Patologi Klinik FK USU/RSUP.
H. Adam Malik Medan dan Departemen Ilmu Penyakit Dalam FK
USU/RSUP. H. Adam Malik Medan, mulai Maret sampai dengan Mei
2010.
3.3. Populasi dan subyek penelitian
3.3.1. Populasi penelitian
Populasi penelitian adalah pasien-pasien anemia yang berkunjung
ke Poliklinik Penyakit Dalam dan Pasien-pasien anemia yang dirawat di
3.3.2. Subyek penelitian
Pasien dengan diagnosa ADB menurut kriteria WHO yaitu laki-laki
dewasa: Hb<13 g/dl, perempuan dewasa: Hb<12 g/dl dan nilai
feritin<15ug/L .14
Pasien dengan diagnosa APK dengan nilai Hb pada laki-laki
dewasa <13 g/dl, perempuan dewasa Hb<12 g/dl, nilai feritin>15 ug/L14
dan CRP positip.
Kriteria inklusi
Bersedia ikut dalam penelitian.
Pasien umur 19-79 tahun.
Anemia defisiensi besi menurut WHO:
o Anemia :
laki-laki dewasa : Hb < 13 g/dl
Perempuan dewasa: Hb < 12 d/dl
o Feritin < 15 ug/L
Anemia penyakit kronis:
o Anemia menurut kritria WHO:
laki-laki dewasa: Hb< 13 g/dl
Perempuan dewasa: Hb < 12 d/dl
o Feritin > 15 ug/L.
Kriteria eksklusi
Pasien yang mendapat terapi Fe.
Pasien yang menerima transfusi dalam 3 bulan terakhir.
Anemia hemolitik.
Anemia megaloblastik.
Wanita hamil.
Anemia dengan penyakit ginjal kronis .
Pasien dengan keganasan .
Anemia aplastik
3.4. Perkiraan besar sampel
Untuk menentukan sampel yang diteliti dipakai rumus uji hipotesis
terhadap dua rerata dua populasi, dalam hal ini untuk dua kelompok
berpasangan, 43 sebagai berikut:
(Zα + Z) Sd 2
n ≥
d
Dimana:
n = jumlah sampel.
Zα = nilai baku normal dari table Z yang besarnya tergantung pada
nilai α yang ditentukan. Untuk α = 0,05 → Zα = 1,96.
Z = nilai baku normal dari table Z yang besarnya tergantung pada
d = selisih rerata kedua kelompok yang bermakna = 4,0
Sd = simpangan sTfR dari selisih rata-rata, dihitung dari kepustakaan
1.
Sd = (n1-1) Sd1
2
+ ( n2-1) Sd2
n1 + n2 - 2
Dimana : n1 = 47, n2 = 28, Sd1 = 8,76, Sd2 = 3,94
Sd = (47-1) 8,76
2
+ ( 28-1) 3,942
47 + 28 - 2
Sd = 7,355
Jumlah sampel yang dibutuhkan:
(1,96 +1,282) 7,355 2
4,0 n ≥
n ≥ 35,5 ≥ 36
3.5. Bahan dan Cara Kerja
3.5.1. Bahan yang diperlukan
Bahan yang diperlukan dalam penelitian ini adalah darah EDTA dan
darah tanpa anti koagulan.
3.5.2. Anamnese dan Pemeriksaan Fisik
Pemeriksaan fisik dilakukan pada posisi penderita berbaring. Seluruh data
dan hasil pemeriksaan dicatat dalam status khusus penelitian.
3.5.3. Pengambilan dan pengolahan sampel
Sampel darah diambil melalui vena punksi dari vena mediana cubiti
tanpa stasis vena yang berlebihan, Tempat vena terlebih dahulu
dibersihkan dengan alkohol 70% dan dibiarkan kering. Darah diambil
dengan menggunakan spuit disposible sebanyak 5 cc darah, selanjutnya
dibagi menjadi 2 tabung.
Tabung 1 : dimasukkan darah hingga 2 ml dalam tabung yang berisi 3,6
mg EDTA dan dicampurkan secara perlahan. Konsentrasi
EDTA 1,5-2,0 mg/ml darah tidak memberikan efek yang
bermakna terhadap parameter darah lengkap.44
Tabung 2 : dimasukkan darah sebanyak 3 ml (tanpa antikoagulan).
Selanjutnya tabung 2 dibiarkan dalam suhu kamar selama 30
menit, kemudian dilakukan pemutaran dengan sentrifuge
dengan kecepatan 3000 rpm selama 15 menit untuk
mendapatklan serum yang jernih. Serum dipisah secara
hati-hati ke dalam 2 tabung plastik (aliquot). Tabung plastik
pertama untuk pemeriksaan feritin dan CRP. Tabung kedua
segera disimpan dalam freezer (-20OC) - (-70OC) sampai
3.5.4. Pemeriksaan laboratorium
a. Pemeriksaan darah lengkap menggunakan alat cell dyne 3700.
b. Pemeriksaan morfologi darah tepi dengan pembuatan sediaan
apus darah tepi dan menggunakan pewarnaan giemsa.
c. Pemeriksaan feritin dengan menggunakan alat Cobas e 601
d. Pemeriksaan CRP dengan C-Reactive protein (CRP) latex reagent
set.
e. Pemeriksaan sTfR dengan menggunakan alat Cobas c 501.
3.5.4.1. Pemeriksaan darah lengkap
Dengan alat automatic cell counting celldyne 3700 (abbot). Bahan
sampel darah EDTA. Prinsip pemeriksan spectrophotometry berdasarkan
reaksi pembentukan haemoglobin cyanide.
3.5.4.2. Pemeriksaan feritin
Prinsip electrochemiluminescence immunoassay (ECLIA). Feritin
sebagai antigen bereaksi dengan antibodi spesifik feritin monoklonal
biotinylasi, dan antibody spesifik feritin yang dilebel dengan kompleks
ruthenium membentuk kompleks sandwich. Kemudian ditambahkan
mikropartikel yang dilapisi streptavidin, komplek yang terbentuk berikatan
dengan fase solid melalui interaksi biotin dengan streptavidin. Campuran
reaksi diaspirasi dalam cell pengukur dimana mikropartikel secara
berikatan dibuang melalui Procell. Aplikasi voltase (tegangan) pada
elektroda menginduksi emisi chemiluminescent yang diukur oleh
photomultiplier. Dalam reaksi Electro Chemiluminescent (ECL) terjadi
reaksi antara kompleks ruthenium dengan TPA (trypropylamine) yang
distimulasi secara elektrik untuk menghasilkan emisi cahaya. Jumlah
cahaya yang dihasilkan berbanding lurus dengan kadar analit dalam
sampel.45
Sampel darah dari pasien anemia berdasarkan kriteria WHO
dilakukan pemeriksaan feritin. Hasil feritin < 15 ug/l dimasukkan dalam
kelompok ADB. Kemudian pada sampel dengan feritin > 15 ug/l dilakukan
pemeriksaan CRP, dan bila hasil positif dimasukkan dalam kelompok
APK.
3.5.4.3. CRP
Pemeriksaan CRP berdasarkan prinsip aglutinasi latex. Bila serum
mengandung ≥ 0.8 mg/dl CRP maka akan terjadi aglutinasi. Setiap
melakukan pemeriksaan CRP selalu disertakan kontrol positif dan kontrol
negatif. Hasil yang terjadi dikonfirmasi oleh 3 orang untuk menilai apakah
terjadi aglutinasi atau tidak (positif atau negatif).
3.5.4.4. Soluble Transferin Receptor
Pemeriksaan dilakukan secara serentak setelah terkumpul
alat automatic analyzer Cobas Elecsys 601 (Cobas c 601), menggunakan
metode Particle enhanced immunoturbidimetric assay. Sampel yang beku
dari freezer dicairkan pada suhu ruangan. Reagensia, kalibrator dan
kontrol juga disamakan dengan suhu ruangan (20-25 0C). Stabilitas serum
pada temperatur 20-25 0C selama 3 hari, temperature 4-8 0C selama 7
hari, dan temperature (-200C) – (-700C) selama 4 minggu.
Perhitungan indeks sTfR-F dengan menghitung nilai sTfR dengan
membaginya dengan log feritin. Nilai < 1,5 dikatakan APK dan bila > 1,5
dikatakan APK bersamaan ADB.
Indeks sTfR-F = sTfR
log feritin
3.5.5. Pemantapan kualitas
Kontrol kualitas untuk feritin dilakukan dengan elecsys PreciControl
Tumor Marker 1 dan 2, dilakukan setiap melakukan pemeriksaan, setiap
pemakaian reagent kit baru dan setelah selesai kalibrasi. Nilai konsentrasi
kontrol harus masuk dalan range yang ditetapkan untuk menjamin akurasi
assay feritin.
Kontrol kualitas untuk pemeriksaan CRP dengan mengikutkan
3.5.5.1. Kontrol kalibrasi pemeriksaan sTfR
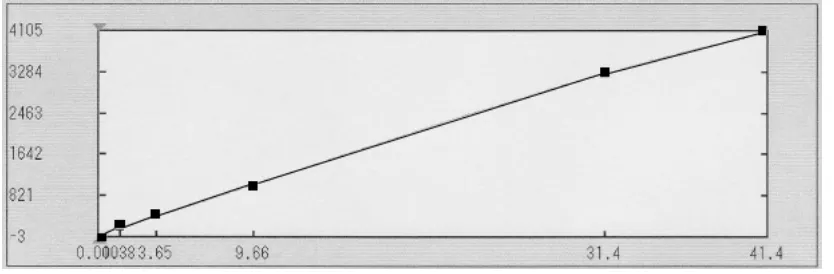
Kontrol kalibrasi menggunakan kalibrator preciset sTfR. Kalibrasi
dilakukan setiap pemakaian lot baru. Grafik yang ditampilkan adalah garis
linier, dengan menggunakan lima titik yaitu 1.60, 3.65, 9.66, 31.4 dan 41.4
Grafik 1. Kalibrator dengan preciset sTfR
3.5.5.1. Kontrol kualitas sTfR
Kontrol kualitas untuk sTfr dilakukan dengan sTfR Control set,
dengan memakai 2 nilai konsentrasi yaitu sTfR control set level 1 dan
sTfR control set level 2 untuk memantau akurasi assay sTfR. Kontrol
dilakukan sesudah kalibrasi dan sebelum dilakukan pemeriksaan terhadap
sampel yang sudah dikumpulkan.
Selama penelitian kontrol kulaitas dilakukan sebanyak 3 kali
bersamaan dengan sampel yang diperiksa. Dalam 3 kali pemeriksaan
sampel, nilai sTfR control set level 1 dan sTfR control set level 2 tidak
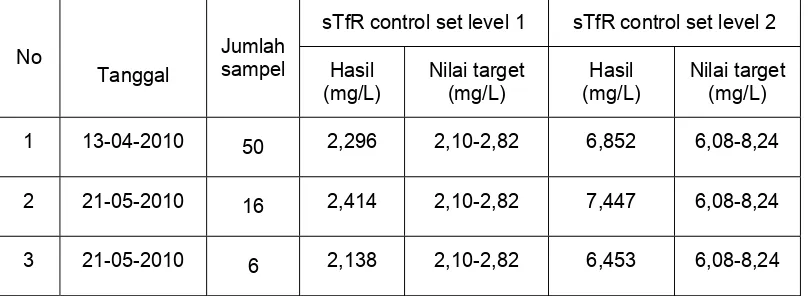
sampel dengan nilai sTfR control set level 1: 2,296 dan sTfR control set
level 2: 6,852. Pemeriksaan kedua sebanyak 16 sampel dengan nilai sTfR
control set level 1: 2,414 dan sTfR control set level 2: 7,447. Pemeriksaan
ketiga menggunakan reagent kit baru dengan lot yang sama sebanyak 6
sampel nilai sTfR control set level 1: 2,138 dan sTfR control set level
2:6,453.
Tabel 3.1. Pemantapan kualitas menggunakan sTfR control set level 1 dan sTfR control set level 2 pada pemeriksaan sTfR.
sTfR control set level 1 sTfR control set level 2 No
3.6. Ethical clearance dan informed consent
Ethical clearance diperoleh dari Komite Penelitian Bidang
Kesehatan Fakultas Kedokteran Universitas Sumatera utara Medan yang
ditanda tangani oleh Prof. Dr Sutomo Kasiman, SpPD, SpJP(K) dengan
nomor surat 118/KOMET/FK USU/2010. Inform consent diminta secara
tertulis dari subjek penelitian atau diwakili oleh keluarganya yang ikut
bersedia dalam penelitian setelah mendapat penjelasan mengenai
3.7. Analisa data
Analisa data dilakukan dengan menggunakan perhitungan statistik.
Untuk melihat perbedaan parameter hematologi dan biokimia pada
anemia defisiensi besi dibandingkan anemia penyakit kronis digunakan
uji T independent jika data pada kedua kelompok yang diamati
berdistribusi normal. Sebaliknya jika tidak berdistribusi normal digunakan
uji Mann-Whitney.
3.8. Batasan Operasional
1. Anemia defisiensi besi
Anemia defisiensi besi adalah anemia yang timbul akibat
berkurangnya penyediaan besi untuk eritropoesis, karena cadangan
besi kosong yang pada akhirnya mengakibatkan pembentukan Hb
berkurang. Anemia defisiensi besi bila dijumpai anemi menurut WHO
dengan feritin serum < 15ug/L.
2. Anemia penyakit kronis
Anemia penyakit kronis adalah anemia yang terjadi karena respon
sistemik penyakit atau inflamasi. Dikatakan anemia penyakit kronis
bila dijumpai anemi menurut kriteria WHO, feritin > 15 ug/L dan
3. Anemia hemolitik
Anemia hemolitik adalah kadar Hb kurang dari normal akibat
kerusakan eritrosit yang lebih cepat dari kemampuan sumsum tulang
untuk menggantikannya.46 Indikator destruksi eritrosit adalah
peningkatan LDH serum dan bilirubin tidak terkonjugasi.47
4. Anemia megaloblastik
Anemia megaloblastik merupakan kelainan yang disebabkan oleh
gangguan sintesis DNA dan ditandai oleh sel megaloblastik.48 Skrening
laboratorium yang digunakan untuk diagnosa adalah dijumpai anemia,
peningkatan MCV dan morfologi darah tepi.49 Peningkatan MCV > 97
fl.50 Morfologi darah tepi berupa makroovalosit dan hipersegmentasi
neutrofil.
5. Anemia dengan penyakit ginjal kronis.
Gagal ginjal ditentukan berdasarkan riwayat penyakit seperti
penderita hemodialisa reguler, pemeriksaan fisik dengan adanya
hipertensi, edema dan pucat dan atau penetapan Estimation
Glomerular Filtration Rate (EGFR) yang direkomendasikan The
National Kidney Foundation, dengan kalkulasi Cocroft-Gault
EGFR (ml/menit) = (140 – umur) X BB (kg)
72 X Scr (mg/dl)
Keterangan: -. Bila perempuan, hasil dikali 0,85
-. Scr adalah kreatinin serum
Penurunan fungsi ginjal ditandai dengan EGFR ≤ 40 ml/menit.
6. Anemia dengan keganasan
Pasien dengan diagnosa keganasan ditetapkan oleh divisi
hematologi Departemen Ilmu Penyakit Dalam FK USU/RSUP. H. Adam
Malik Medan.
7. Wanita hamil
Kehamilan didiagnosa dengan anamnese haid terakhir. Bila pasien
lupa atau tanggal seharusnya haid sudah lewat dilakukan test
kehamilan urine.
8. Pansitopenia
Dikatakan pansitopenia apabila dijumpai penurunan nilai leukosit,
3.11. Kerangka operasional
Pemeriksaan darah lengkap & sediaan hapus darah tepi
HD regular
Hipertensisi, pucat, oedema dan atau EGFR <40 ml/mnt
feritin
Pasien polikliniki dan bangsal devisi hematologi onkologi medik
Riwayat
transfusi < 3 bln eksklusi
BAB IV
HASIL PENELITIAN
Penelitian dilakukan bertujuan mengevaluasi kegunaan sTfR dan indeks sTfR-F untuk mendiagnosa ADB, dilaksanakan dari tanggal 24 Maret 2010 sampai 29 Mei 2010. Subjek penelitian adalah pasien-pasien ADB dan APK yang berkunjung ke poliklinik Penyakit Dalam dan yang dirawat di bangsal Penyakit Dalam Rumah Sakit Umum Pusat H. Adam Malik Medan.
Table 4.1.Data-data laboratorium subjek penelitian
kelompok ADB murni, APK murni dan kombinasi APK dengan ADB.
Jenis
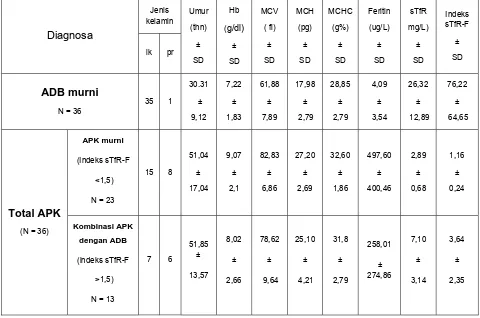
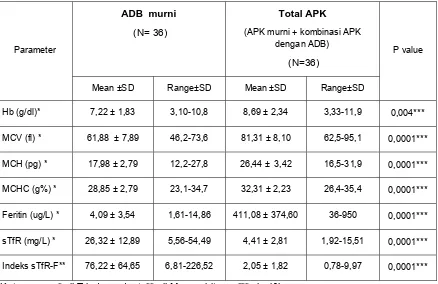
Tabel 4.2. Perbandingan parameter hematologi dan biokimia pada ADB murni dan total APK
ADB murni (N= 36)
Total APK (APK murni + kombinasi APK
dengan ADB)
(N=36) Parameter
Mean ±SD Range±SD Mean ±SD Range±SD
P value
Hb (g/dl)* 7,22 ± 1,83 3,10-10,8 8,69 ± 2,34 3,33-11,9 0,004***
MCV (fl) * 61,88 ± 7,89 46,2-73,6 81,31 ± 8,10 62,5-95,1 0,0001***
MCH (pg) * 17,98 ± 2,79 12,2-27,8 26,44 ± 3,42 16,5-31,9 0,0001***
MCHC (g%) * 28,85 ± 2,79 23,1-34,7 32,31 ± 2,23 26,4-35,4 0,0001***
Feritin (ug/L) * 4,09 ± 3,54 1,61-14,86 411,08 ± 374,60 36-950 0,0001***
sTfR (mg/L) * 26,32 ± 12,89 5,56-54,49 4,41 ± 2,81 1,92-15,51 0,0001***
Indeks sTfR-F** 76,22 ± 64,65 6,81-226,52 2,05 ± 1,82 0,78-9,97 0,0001***
Keterangan: * uji T independent, ** uji Mann-whitney ,*** signifikan
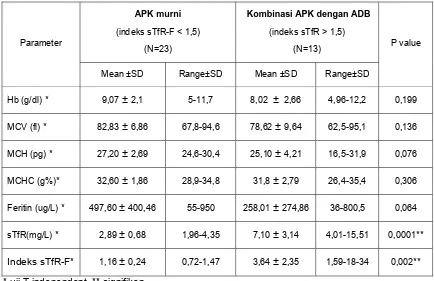
Tabel 4.3. Perbandingan parameter hematologi dan biokimia kelompok APK murni dengan kombinasi APK dengan ADB.
APK murni
(indeks sTfR-F < 1,5)
(N=23)
Kombinasi APK dengan ADB
(indeks sTfR > 1,5) * uji T independent, ** signifikan
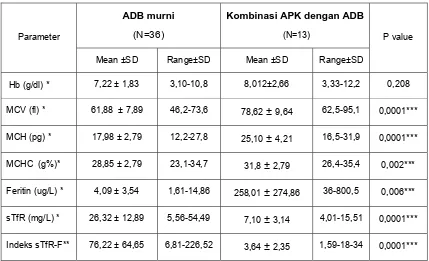
Tabel 4.4. Perbandingan parameter hematologi dan biokimia pada ADB murni dan kombinasi APK dengan ADB.
ADB murni (N=36)
Kombinasi APK dengan ADB (N=13) Keterangan: * uji T independent, ** uji Mann-whitney ,*** signifikan
BAB IV
PEMBAHASAN
Anemia defisiensi besi dalam beberapa keadaan relatif mudah didiagnosa dengan menggunakan pemeriksaan laboratorium status besi konvensional seperti serum iron (SI), total iron binding capacity (TIBC), saturasi transferin dan serum feritin. WHO merekomendasikan konsentrasi feritin < 12 ug/l mengindikasikan deplesi cadangan besi pada anak-anak < 5 tahun, dan nilai < 15 ug/l mengindikasikan deplesi cadangan besi pada umur > 5 tahun.3 Pemeriksaan serum feritin sangat efisien untuk menilai cadangan besi tubuh, akan tetapi feritin berperan sebagai protein fase akut, sehingga sulit dibedakan antara ADB dengan APK. Pada beberapa penelitian, pengukuran sTfR telah terbukti berguna untuk membedakan diagnosa ADB dengan APK, dan konsentrasi sTfR tidak dipengaruhi respon protein fase akut, sehingga sTfR lebih baik dibandingkan pengukuran status besi konvensional. Dengan pemeriksaan feritin dan sTfR dapat dihasilkan nilai indeks sTfR-F.
Punnonen Kari dkk tahun 1997 di Finland membedakan ADB dengan APK berdasarkan pewarnaan besi sumsum tulang. Nilai sTfR pada ADB (6,2 ± 3,5 mg/L) lebih tinggi dibandingkan APK (1,8 ± 0,6 mg/L mg/L). Nilai indeks sTfR-F pada ADB (6,8 ± 6,5) lebih tinggi dibanding indeks sTfR APK ( 0,8 ± 0,3).17
Penelitian Remacha Angel dkk tahun 1998 di Spanyol membedakan ADB dengan APK dengan batasan nilai feritin 13 ug/L. Nilai sTfR pada ADB (8,1 ± 5,4 mg/L) lebih tinggi dibandingkan nilai sTfR pada APK( 3,5 ± 1,2 mg/L).53
Simek M dkk tahun 2002 di Slovakia membedakan ADB dengan APK berdasarkan pewarnaan besi sumsum tulang. Pada pasien ADB nilai sTfR (5,3 ± 1,8 mg/L) lebih tinggi dibandingkan dengan APK (1,6 ± 0,4 mg/L).18
Penelitian Hanif Ejas dkk tahun 2005 di Pakistan membedakan ADB dengan APK dengan pewarnaan besi sumsum tulang. Nilai sTfR pada ADB (9,6± 2,4 mg/L) lebih tinggi dibandingkan nilai sTfR pada APK (2,961,28 ± 1,2 mg/L).54
Jayarenes dkk tahun 2006 di Kuala Lumpur membedakan ADB dengan APK berdasarkan batasan nilai feritin 12 ug/L. Nilai sTfR pada ADB (5,53 ± 8,76 mg/L) lebih tinggi dibandingkan nilai sTfR pada APK (3,32 ± 3,94 mg/L). Nilai indeks sTfR-F pada ADB (2368,98 ± 7236,4) lebih tinggi dibanding indeks sTfR APK ( 71,01± 193,58).1
dkk, 2005 di Dallas juga mendapatkan dijumpai perbedaan yang bermakna pada nilai feritin serum, MCV, MCH dan MCHC pada kelompok ADB dengan APK.55
Dengan menggunakan nilai indeks sTfR-F dengan cut-off 1,5, total APK dibagi menjadi 2 bagian. Kelompok APK yang memiliki nilai indeks sTfR-F <1,5 merupakan APK murni dan kelompok APK yang memiliki nilai indeks sTfR-F >1,5 merupakan kombinasi APK dengan ADB. Nilai sTfR kelompok kombinasi APK dengan ADB (7,10 ± 3,14 mg/L) lebih tinggi dibandingkan kelompok APK murni (2,89 ± 0,68 mg/L). Nilai indeks sTfR-F pada kelompok kombinasi APK dengan ADB (3,64 ± 2,35) lebih tinggi dibandingkan kelompok APK murni (1,16± 0,24).
Punnonen Kari dkk mendapatkan nilai sTfR pada kombinasi APK dengan ADB (2,1±2,0 mg/Lmg/L) lebih tinggi dibandingkan APK (1,8 ± 0,6 mg/Lmg/L). Indeks sTfR-F pada kombinasi APK dengan ADB (3,8 ± 1,9) lebih tinggi dari APK (0,8 ± 0,3).
Penelitian Remacha A dkk mendapatkan nilai sTfR pada kombinasi APK dan ADB (7 ± 5,1 mg/L) lebih tinggi dibandingkan APK (3,54 ± 0,2 mg/L).17
Simek M dkk mendapatkan nilai sTfR pada kombinasi APK dan ADB (6,71 ± 2,58 mg/L) lebih tinggi dibandingkan APK (1,8 ± 0,6 mg/L).53
sTfR-F pada kombinasi APK dengan ADB (176,31 ± 197,12) lebih tinggi dari APK (16,2 ± 28,97).1
Nilai sTfR sangat berguna untuk mendiagnosa ADB, dan indeks sTfR-F merupakan parameter yang baik untuk mengetahui apakah dijumpai defisiensi besi pada pasien-pasien APK. Tidak dijumpai perbedaan yang bermakna pada parameter lain yaitu Hb, MCV, MCH, MCHC dan feritin antara kelompok APK murni dengan APK bersamaan ADB.
BAB VI
KESIMPULAN DAN SARAN
6.1. KESIMPULAN
1. Kadar sTfR dan Indeks sTfR-F pada anemia defisiensi besi lebih
tinggi dibandingkan anemia penyakit kronis sehingga dengan
pemeriksaan sTfR dapat membedakan anemia defisiensi besi
dengan anemia penyakit kronis. Tetapi pemeriksaan sTfR dan
indeks sTfR-F tidak memberi informasi tambahan untuk
membedakan anemia defisiensi besi dengan anemia penyakit
kronis.
2. Kadar sTfr dan indeks sTfR-F pada anemia defisiensi besi lebih
tinggi dibandingkan kombinasi anemia penyakit kronis dengan
anemia defisiensi besi. Tetapi pemeriksaan sTfR dan indeks sTfR-F
tidak memberi informasi tambahan untuk membedakan anemia
defisiensi besi dengan kombinasi anemia penyakit kronis dengan
defisiensi besi.
3. Kadar sTfR dan Indeks sTfR-F pada kombinasi anemia penyakit
kronis dengan anemia defisiensi besi lebih tinggi dibandingkan
anemia penyakit kronis murni. Pemeriksaan ini bermanfaat untuk
6.2. SARAN
Pada anemia penyakit kronis perlu dilakukan pemeriksaan sTfR
disertai feritin untuk mendapatkan indeks sTfR-F sehingga dapat
DAFTAR PUSTAKA
1. Jayaraness S and Sthaneshwar P. Serum soluble transferrin
receptor in hypochromic microcytic anaemia. Singapore Med J,
2006;49(2):38-42.
2. Worwood M, Hoffbrand A.V. Iron metabolisme, Iron deficiency and
disorders of haem synthesis in Postgraduate haematology. 5th ed.
Blackell Publishing, 2005: 26-43.
3. Brugnara C. Iron Deficiency and Erythropoiesis: New diagnostic
approaches. Clin Chem, 2003;49(10):1573-78.
4. Provan D. Iron deficiency anemia in ABC of Clinical haematology.
2nd ed, BMJ Books, 2003:1-4.
5. Beutler E. Disorders of Iron metabolisme in Williams Hematology,
7th ed, McGraw-Hill, 2006:511-53.
6. Andrew NC. Iron deficiency and related disorder in Wintrobe
Clinical Hematology, 11th ed, Lippincott Williams & Wilkins,
2004:979-1009.
7. Wu AC, Lesperance L, Bernstein H. Screening for iron deficiency.
Pediatric in review 2002;23:171-78.
8. Hilman RS, Ault KA, Rinder HM: Iron Deficiency Anemia in
9. Killip S, Bennett JM and Chambers MD. Iron deficiency anemia.
AAFP, 2007;75(5):671-8.
10. Word health organization. Worldwide prevalence of anemia
1993-2005 in WHO Global Database on Anemia, World Health
Organization, 2008.
11. World Health Organization. Methode of assessing iron status in iron
deficiency anemia assessment, prevention and control a guide for
programme managers, WHO, 2001,33-43.
12. Pasricha SR, Casey GJ, Phuc TQ et all. Baseline iron indices as
predictor of hemoglobin improvement in anemic Vietnamese
womwn receiving weekly iron-folic acid supplementation and
deworming. Am.J. Trop. Med. Hyg, 81(6),2009,1114-9.
13. Bakta IM, Suega K, Dharmayuda TG. Anemia defisiensi besi dalam
buku ajar ilmu penyakit dalam, Edisi IV, Pusat Penerbitan Ilmu
Penyakit Dalam FK-UI. Jakarta, 2006:634-40.
14. Mast AE, Blinder ma, Gronowski AM, Chumley C, Scott M. Clinical
utility of the soluble transferring receptor and comparison with
serum feritin in several population. Clinchem,44:1,1998,45-51.
15. Kern WF. Iron deficiency anemia, anemia of chronic disease,
sideroblastic anemias , and megaloblastic anemia in PDQ