PENG ARUH BIOSORPSI RUMPUT LAUT (Sa rg assum)
SETELAH DILAPISI KITOSAN SEBAGAI ADSORBEN
UNTUK MENYERAP ION LOGAM KADMIUM (Cd
2+)
SKRIPSI
WIDAYAN SUCINTA
100822013
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PENG ARUH BIOSORPSI RUMPUT LAUT (Sa rg assum)
SETELAH DILAPISI KITOSAN SEBAGAI ADSORBEN
UNTUK MENYERAP ION LOGAM KADMIUM (Cd
2+)
SKRIPSI
Diajukan untuk melengkapi tugas dan memenuhi syarat mencapai gelar Sarjana Sains
WIDAYAN SUCINTA
100822013
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
UNIVERSITAS SUMATERA UTARA
PERSETUJUAN
Judul : PENGARUH BIOSORPSI RUMPUT LAUT (Sargassum) SETELAH DILAPISI KITOSAN SEBAGAI ADSORBEN UNTUK MENYERAP ION LOGAM KADMIUM Cd2+
Kategori : SKRIPSI
Nama : WIDAYAN SUCINTA
Nomor Induk Mahasiswa : 100822013
Program Studi : SARJANA (S-1) KIMIA
Departemen : KIMIA
Fakultas : MATEMATIKA DAN ILMU PENGETAHUAN
ALAM (FMIPA) UNIVERSITAS SUMATERA UTARA
Disetujui di
Medan, Juli 2012
Komisi Pembimbing :
Pembimbing II Pembimbing I
Drs. Chairuddin, Msc Prof.Dr.Harry Agusnar,M.Sc.,M.Phill NIP. 19593112198701001 NIP. 195308171983031002
Diketahui/Disetujui oleh :
Departemen Kimia FMIPA USU Ketua,
Dr.Rumondang Bulan.,MS NIP. 195408301985032001
PERNYATAAN
PENGARUH BIOSORPSI RUMPUT LAUT (Sargassum) SETELAH DILAPISI KITOSAN SEBAGAI ADSORBEN UNTUK MENYERAP ION LOGAM KADMIUM (Cd2+)
SKRIPSI
Saya mengakui bahwa skripsi ini adalah hasil kerja saya sendiri, kecuali beberapa kutipan dan ringkasan yang masing – masing disebutkan sumbernya.
Medan, Juli 2012
WIDAYAN SUCINTA 100822013
PENGHARGAAN
Puji dan syukur penulis ucapkan pada Allah SWT karena atas rahmat dan karunia-Nya saya dapat menyelesaikan skripsi ini sebagai salah satu persyaratan untuk meraih gelar Sarjana Kimia pada Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara.
Saya sampaikan penghargaan dan cinta kasih yang terdalam dan tulus kepada Ayahanda tercinta dan Ibunda tersayang atas segala doa dan pengorbanan yang telah diberikan kepada saya dan tidak lupa kepada kaka dan adik saya yang telah banyak memberikan semangat kepada saya. Dengan segala kerendahan hati, saya ucapkan terima kasih yang tulus dan sebesar – besarnya kepada :Prof.Dr.Harry Agusnar, M.Sc,M.Phill selaku dosen pembimbing I yang telah memberikan ide dan topik serta tunjuk ajar hingga selesainya skipsi dan Drs. Chairuddin, Msc selaku dosen pembimbing 2 yang telah banyak memberikan bimbingan hingga terselesainya skripsi ini. Dr.Rumondang Bulan Nasution, MS selaku Ketua Departemen Kimia FMIPA USU dan Dr.Darwin Yunus Nasution, MS selaku Koordinator Ekstensi Kimia FMIPA USU serta seluruh staff pegawai Departemen Kimia. Bapak dan Ibu dosen yang telah memberikan ilmunya kepada saya selama perkuliahan. Bapak Sukirman selaku pegawai Laboratorium Peneltian Fakultas Matematika dan Ilmu Pengetahuan Alam (FMIPA) Universitas Sumatera Utara. Yang telah banyak membantu penelitian ini teman saya yang paling saya sayangi Lisma, Khairun nisya, Winny Mustika, Jefri Aldi, Ricky. Terima kasih telah membantu saya dalam menyelesaikan skripsi ini atas dukungan dan motivasinya yang telah diberikan kepada saya.
Saya menyadari bahwa skirpsi ini masih banyak kekurangan, karena keterbatasan pengetahuan saya. Oleh karena itu saya mengharapkan saran dan masukkan yang membangun demi kesempurnaan skripsi ini dan semoga skripsi ini dapat memberikan manfaat bagi kita semua.
Medan, Juli 2012
ABSTRAK
Telah dilakukan penelitian tentang penggunaan rumput laut setelah dilapisi kitosan sebagai adsorben untuk menyerap ion logam kadmium (Cd2+). Rumput laut diaktivasi dengan menggunakan larutan HCl 1,5 M untuk mendapatkan biosorpsi yang optimum. Larutan kitosan 1% digunakan untuk melapisi biosorpsi rumput laut dengan cara di spray hingga basah. Rumput laut yang telah dilapisi kitosan tersebut digunakan sebagai adsorben dengan memasukkan sebanyak 3 gram rumput laut kedalam beaker glass dan digunakan kadmium (Cd2+) 10 mg/L sebagai ion logam yang terserap kemudian diaduk selama 10 menit dan biarkan hingga larutan terpisah. Diambil lapisan bagian atas serta diukur dengan Spektrofotometer Serapan Atom. Hasil penyerapan ion logam (Cd2+) yang didapatkan sebesar 99,997%.
Kata Kunci ; rumput laut, kitosan, biosorpsi, adsorben.
EFFECT OF SEAWEED BIOSORPTION AFTER COATED CHITOSAN AS AN ADSORBEN OF ADSORB METAL ION CADMIUM (Cd2+)
ABSTRACT
The use of seaweed coated chitosan as adsorben to adsorb ion cadmium (Cd2+). The result show that optimum biosorption is with use HCl 1,5 M. The Chitosan 1% used to coat seaweed by sprayed until wet, seaweed which coated by chitosan used to as adsorben with put in 3 gram of seaweed to beakerglass and put on (Cd2+) 10 mg/L, stirred by 10 minutes and leat it. Taken top of layer and measured by Atomic Absorption Spectrophotometry. The result of ion (Cd2+) absorption was 99,997%.
Keyword ; seaweed, chitosan, biosorption, adsorbent.
DAFTAR TABEL
Tabel 2.1 Kondisi Perlakuan dengan NaOH pada Proses Deproteinisasi 11 Tabel.2.2 Kondisi Perlakuan dengan HCl pada Proses Demineralisasi 12 Tabel 4.1 Konsentrasi danAbsorbansi Larutan Standar Kadmium (Cd2+) 33 Tabel 4.2 Kondisi Alat Spektrofotometer Serapan Atom (SSA)
GBC Avanta pada Pengukuran Konsentrasi
Logam Kadmium (Cd2+) 34 Tabel 4.3 Penurunan Persamaan Garis Regresi Logam Kadmium (Cd2+)
Berdasarkan Pengukuran Absorbansi Larutan
Seri Standar Logam Kadmium (Cd2+) 38 Tabel 4.4 Data Persentase (%) Konsentrasi Logam Kadmium (Cd2+)
Dalam Larutan Standar Setelah Penambahan
Rumput Laut Teraktivasi HCl 1,5M 38 Tabel 4.5 Data Persentase (%) Konsentrasi Logam Kadmium (Cd2+)
Dalam Larutan Standar Setelah Penambahan
DAFTAR GAMBAR
Gambar 2.1 Sruktur Alginat 6
Gambar 2.2 Struktur Kitin 8
Gambar 2.3 Struktur Kitosan 9
Gambar 2.4 Struktur Alginat dilapisi kitosan dalam menyerap ion logam Kadmium 10 Gambar 4.1 Kurva Kalibrasi Larutan Standart Kadmium (Cd2+) 34 Gambar 4.2 Kurva Penyerapan Rumput Laut Sargassum
ABSTRAK
Telah dilakukan penelitian tentang penggunaan rumput laut setelah dilapisi kitosan sebagai adsorben untuk menyerap ion logam kadmium (Cd2+). Rumput laut diaktivasi dengan menggunakan larutan HCl 1,5 M untuk mendapatkan biosorpsi yang optimum. Larutan kitosan 1% digunakan untuk melapisi biosorpsi rumput laut dengan cara di spray hingga basah. Rumput laut yang telah dilapisi kitosan tersebut digunakan sebagai adsorben dengan memasukkan sebanyak 3 gram rumput laut kedalam beaker glass dan digunakan kadmium (Cd2+) 10 mg/L sebagai ion logam yang terserap kemudian diaduk selama 10 menit dan biarkan hingga larutan terpisah. Diambil lapisan bagian atas serta diukur dengan Spektrofotometer Serapan Atom. Hasil penyerapan ion logam (Cd2+) yang didapatkan sebesar 99,997%.
Kata Kunci ; rumput laut, kitosan, biosorpsi, adsorben.
EFFECT OF SEAWEED BIOSORPTION AFTER COATED CHITOSAN AS AN ADSORBEN OF ADSORB METAL ION CADMIUM (Cd2+)
ABSTRACT
The use of seaweed coated chitosan as adsorben to adsorb ion cadmium (Cd2+). The result show that optimum biosorption is with use HCl 1,5 M. The Chitosan 1% used to coat seaweed by sprayed until wet, seaweed which coated by chitosan used to as adsorben with put in 3 gram of seaweed to beakerglass and put on (Cd2+) 10 mg/L, stirred by 10 minutes and leat it. Taken top of layer and measured by Atomic Absorption Spectrophotometry. The result of ion (Cd2+) absorption was 99,997%.
Keyword ; seaweed, chitosan, biosorption, adsorbent.
BAB 1
PENDAHULUAN
1.1Latar Belakang
Indonesia merupakan negara kepulauan yang sebagian besar luas wilayahnya adalah lautan, sehingga disebut sebagai negara maritim. Pemanfaatan potensi sumberdaya alam terutama lautan belum dimanfaatkan secara maksimum. Salah satu kekayaan alam yang bisa kita manfaatkan banyak terdapat di perairan. Selain ikan, alternatif hasil laut yang bisa diolah adalah rumput laut. Rumput laut Sargassum atau yang biasa disebut dengan seaweed merupakan tanaman makro alga yang hidup di laut yang tidak memiliki akar, batang dan daun sejati. Rumput laut termasuk dalam anggota alga (tumbuhan memiliki klorofil atau zat hijau daun). Tumbuhan yang hidup diperairan dangkal dan pada umunya hidup di dasar perairan. (Anggadiredja, J.T. 1989)
dengan H+ dari asam dan melarutkan pengotor-pengotor yang terdapat pada biosorben sehingga kapasitas biosorpsinya meningkat.
Salah satu sumber adsorben polimer alam adalah kitosan yang memiliki kapasitas adsorpsi tinggi, juga pemanfaatan kitosan yang cukup luas dalam proses adsorpsi disebabkan karena adanya gugus amina dan hidroksil, yang menyebabkan kitosan mempunyai reaktifitas kimia yang tinggi dan menyebabkan sifat polielektrolit kation sehingga berperan sebagai penukar ion dan dapat berperan sebagai adsorben dalam mengadsorpsi logam berat.
Berdasarkan latar belakang diatas, penulis ingin meneliti tentang penggunaan biosorpsi rumput laut setelah dilapisi kitosan sebagai adsorben untuk menyerap ion logam kadmium (Cd2+).
1.2 Permasalahan
Bagaimana pengaruh rumput laut (Sargassum) yang telah diaktivasi dengan HCl dan dilapisi kitosan terhadap penyerapan ion logam kadmium (Cd2+).
1.3 Pembatasan Masalah
Dalam penelitian ini permasalahan dibatasi pada penentuan kadar optimum ion logam kadmium (Cd2+) sebelum dan sesudah penggunaan rumput laut (Sargassum) setelah dilapisi kitosan.
1.4Tujuan Penelitian
Penelitian ini bertujuan untuk mengetahui pengaruh rumput laut setelah dilapisi kitosan sebagai adsorben untuk menyerap ion logam kadmium (Cd2+) dengan metoda Spektrofotometri Serapan Atom.
1.5 Manfaat Penelitian
Hasil penelitian ini dapat digunakan sebagai sumber informasi yang berguna tentang kemampuan rumput laut setelah dilapisi kitosan dalam mengadsorpsi ion logam kadmium (Cd2+).
1.6 Lokasi Penelitian
Penelitian ini dilakukan di Laboratorium Penelitian Fakultas Matematika dan Ilmu Pengetahuan Alam Universitas Sumatera Utara dan analisa Spektrofotometri Serapan Atom di lakukan di laboratorium Pusat Penelitian Kelapa Sawit (PPKS).
1.7 Metodologi Penelitian
Penelitian ini merupakan eksperimen laboratorium. Pembuatan kitosan berasal dari kulit udang. Rumput laut sargassum diaktivasi dengan HCl 1,5 M. Setelah itu rumput laut dilapisi dengan kitosan dan untuk pengujian logam kadmium (Cd2+), rumput laut sargassum yang sudah dilapisi kitosan dimasukkan kedalam larutan standar kadmium (Cd2+). Diaduk dengan magnetik stirrer selama 10 menit dan disaring. Kemudian hasilnya dianalisa dengan Spektrofotometri Serapan Atom.
BAB 2
TINJAUAN PUSTAKA
2.1 Defenisi dan Morfologi Rumput laut
Ribuan tahun sebelum masehi (SM), bangsa Cina sudah memanfaatkan rumput laut sebagai makanan sehat dan obat-obatan. Kemudian pada 65 SM, bangsa Romawi mulai menggunakannya untuk bahan kosmetik.
Rumput laut tergolong tanaman berderajat rendah, umumnya tumbuh melekat pada substrat tertentu, tidak mempunyai akar, batang maupun daun sejati, tetapi hanya menyerupai batang yang disebut thallus. Rumput laut tumbuh di alam dengan melekatkan dirinya di karang, lumpur pasir, batu, dan benda keras lainnya. Selain benda mati, rumput laut pun dapat melekat pada tumbuhan lain secara epifitik.(Davidson, 1980)
Secara taksonomi, rumput laut dikelompokkan ke dalam divisio Thallophyta. Berdasarkan kandungan pigmennya, rumput laut dikelompokkan menjadi empat kelas :
1. Rhodophyceae (ganggang merah) 2. Phaeophyceae (ganggang coklat) 3. Chlorophyceae (ganggang hijau) 4. Cyanophyceae (ganggang biru-hijau)
Beberapa jenis rumput laut Indonesia yang bernilai ekonomis dan sejak dulu sudah diperdagangkan yaitu : Eucheuma sp, Hypnea sp, Gracilaria sp, Gelidium sp, dari kelas
Rhodophyaceae serta Sargassum sp dari kelas Phaeophyceae.
Eucheuma sp. dan Hypnea sp. menghasilkan metabolit primer senyawa hidrokoloid yang disebut karaginan (carrageenan). Gracilaria sp. dan Gelidium sp. menghasilkan metabolit primer senyawa hidrokoloid yang disebut agar. Sementara Sargassum sp. yang menghasilkan metabolit primer senyawa hidrokoloid yang disebut alginat. Rumput laut yang menghasilkan karaginan disebut pula Carraginophyte (karaginofit), penghasil agar disebut agarophyte
2.2 Deskripsi dan Klasifikasi Sargassum Sp.
Rumput laut jenis Sargassum sp ini umumnya memiliki bentuk thallus silindris atau gepeng. Cabangnya rimbun menyerupai pohon di darat. Bentuk daun melebar, lonjong atau seperti pedang. Mempunyai gelembung udara (bladder) yang umumnya soliter. Warna thallus umumnya coklat . Berikut ini adalah klasifikasi dari Sargassum sp.
Divisio : Rhodophyta
Ciri-ciri khusus yang dimiliki oleh Sargassum sp. antara lain thallus pipih, licin, batang utama bulat agak kasar, dan holdfast (bagian yang digunakan untuk melekat) berbentuk cakram. Cabang pertama timbul pada bagian pangkal sekitar 1 cm dari holdfast. Percabangan berselang-seling secara teratur. Bentuk daun oval dan memanjang berukuran (40x10) mm. Pinggir daun bergerigi jarang, berombak, dan ujung melengkung atau meruncing. Vesicle (gelembung seperti buah) berbentuk lonjong, ujung meruncing berukuran (7x1,5) mm, dan agak pipih. Rumput laut jenis ini mampu tumbuh pada substrat batu karang di daerah berombak. (Othmer, 1986)
2.2.1 Potensi pemanfaatan Sargassum Sp.
Rumput laut sargassum telah lama dimanfaatkan sebagai bahan makanan dan obat. Sebagai sumber gizi, rumput laut memiliki kandungan karbohidrat (gula atau vegetable-gum), protein, sedikit lemak, dan abu yang sebagian besar merupakan senyawa garam natrium dan kalium. Selain itu, rumput laut juga mengandung vitamin-vitamin, seperti A,B1,B2,B6,B12, dan C; betakaroten; serta mineral, seprti kalium, kalsium, fosfor, natrium, zat besi, dan yodium.
maupun industri lainnya seperti cat tekstil, film, makanan ternak, keramik, kertas, fotografi dan lain- lain.
2.2.2. Alginat
Alginat merupakan fikokoloid atau hidrokoloid yang diekstraksi dari alga coklat (phaeophyceae). Senyawa tersebut merupakan suatu polimer linier yang disusun oleh dua unit
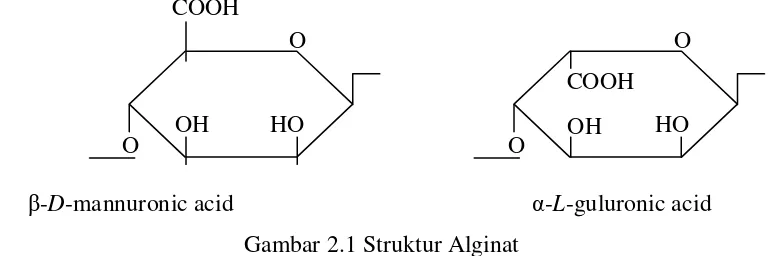
monomerik, yaitu β-D-mannuronic acid dan α-L-guluronic acid. Adapun rumput laut komersil sebagai penghasil alginat yang berasal dari genus-genus Laminaria, Lessonia, Ascophyllum, Sargassum dan Turbinaria.
Alginat menjadi penting karena penggunaanya yang cukup luas untuk dalam industri antara lain sebagai bahan pengental, pensuspensi, penstabil, pembentuk flim, pembentuk gel, disintegrating agent, dan bahan pengemulsi. Sehubungan dengan fungsi tersebut maka alginat banyak dibutuhkan oleh berbagai industri, seperti farmasi (5%), tekstil (50%), makanan dan minuman (30%), kertas (6%), serta industri lainnya (9%). Alginat diekstrak dari rumput laut coklat (Phaeophyceae), misalnya Laminaria dan Sargassum. Asam alginat adalah suatu polisacharida yang terdiri dari D-mannuronic acid dan L-guluronic acid yang merupakan asam-asam karbosiklik (R-COOH) dengan perbandingan mannuronic acid/guluronic acid antara 0,3– 2,35.
β-D-mannuronic acid α-L-guluronic acid Gambar 2.1 Struktur Alginat
alkohol. Di bidang farmasi dan kosmetik, alginat dimanfaatkan dalam bentuk asam alginat atau garam sodium alginat dan kalsium alginat. (Anggadiredja.T.J. 1989)
Mineral esensial yang dikandung rumput laut sangat banyak, antara lain besi dan kalsium. Kandungan kalsium rumput laut sepuluh kali lebih tinggi dibandingkan dengan susu, sehingga rumput laut sangat tepat dikonsumsi untuk mengurangi dan mencegah gejala osteoporosis.
Rumput laut mengandung berbagai vitamin yaitu vitamin A, B kompleks, C, D, dan K. Kandungan vitamin tersebut memberi nutrisi pada kulit sehingga kulit lebih lembab dan kencang. Vitamin C bisa membantu menangkal radikal bebas.
Kandungan protein dan serat rumput laut juga sangat tinggi. Serat pada rumput laut bisa membuat perut terasa lebih kenyang. Selain itu, rumput laut bisa meluruhkan lemak-lemak di perut, sehingga bahan ini banyak dimanfaatkan untuk produk pelangsing.
Manfaat luar biasa rumput laut lainnya adalah kemampuannya untuk membantu proses memperbarui jaringan kulit yang rusak sehingga banyak pula dipakai sebagai produk antikeloid. Selain manfaat diatas juga terdapat manfaat yang lain, yaitu :
• Anti kanker, Penelitian Harvard School of Public Health di Amerika mengungkap, wanita premenopause di Jepang berpeluang tiga kali lebih kecil terkena kanker payudara dibandingkan wanita Amerika. Hal ini disebabkan pola makan wanita Jepang yang selalu menambahkan rumput laut di dalam menu mereka.
• Antioksi dan Klorofil pada gangang laut hijau dapat berfungsi sebagai antioksidan. Zat ini membantu membersihkan tubuh dari reaksi radikal bebas yang sangat berbahaya bagi tubuh.
• Mencegah Kardiovaskular, Para Ilmuwan Jepang mengungkap, ekstrak rumput laut dapat menurunkan tekanan darah pada penderita hipertensi. Bagi pengidap stroke, mengkonsumsi rumput laut juga sangat dianjurkan karena dapat menyerap kelebihan garam pada tubuh.
• Makanan Diet Kandungan serat (dietary fiber) pada rumput laut sangat tinggi. Serat ini bersifat mengenyangkan dan memperlancar proses metabolisme tubuh sehingga sangat baik dikonsumsi penderita obesitas. Karbohidratnya juga sukar dicerna sehingga Anda akan merasa kenyang lebih lama tanpa takut kegemukan.
• Secara tradisional, rumput laut dipercaya dapat mengobati batuk, asma, bronkhitis, TBC, cacingan, sakit perut, demam, influenza, dan artritis.
2.3 Kitosan
2.3.1 Kitin dan Kitosan
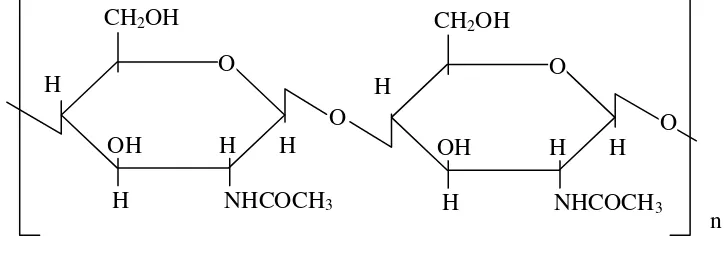
Kitin merupakan polisakarida rantai linier dengan rumus β(1-4)2- asetamida 2-deoksi-D-glucopyranosa (Muzzerelli,R.A.A.1997) dan kitin sebagai precursor kitosan pertama kali ditemukan pada tahun 1811 oleh orang Perancis bernama Henri Braconnot sebagai hasil isolasi dari jamur. Sedangkan kitin dari kulit serangga ditemukan pada tahun 1820. (Rismana,2004)
Gambar 2.2 Struktur Kitin
Kitin murni mengandung gugus asetamida (NH-COCH3), dan kitosan murni mengandung
gugus amino (NH2). Perbedaan gugus ini akan mempengaruhi sifat-sifat kimia senyawa
tersebut.(Roberts,G.A.F,1992)
Kitosan merupakan senyawa turunan dari kitin yang memiliki struktur
(1,4)-2-amino-2-deoksi β-D-Glukosa. Sumber kitosan yang sangat potensial adalah kerangka crustaceae (Muzzerelli,R.A.A.1997).
Kitosan ditemukan oleh C.Rouget pada tahun 1895, dia menemukan bahwa kitin yang telah didihkan pada larutan KOH juga dapat diperlukan dengan NaOH panas maka akan terjadi pelepasan gugus asetil (proses deasetilasi) yang terikat pada atom nitrogen menjadi gugus amino bebas yang disebut dengan kitosan. (Vinvogrado,A.P,1971).
Gambar 2.3 Struktur Kitosan
2.3.2 Kegunaan Kitin dan Kitosan
Dewasa ini aplikasi kitin da kitosan sangat banyak dan meluas. Di bidang industri, kitin, dan kitosan berperan antara lain sebagai koagulan polielektrolit pengolahan limbah cair, pengikat cair, pengikat dan penyerap ion logam, mikroorganisme, mikroalga, pewarna, residu pestisida, lemak tannin, PCB, (poliklorinasi bifenil), mineral dan asam organik, media kromatografi afinitas, gel dan pertukaran ion, penyalut berbagai serat alami dan sintetik, pembentukan film dan membran mulai terurai, meningkatkan kualitas kertas, pulp, dan produk tekstil. Sementara dibidang pertanian dan pangan kitin dan kitosan digunakan sebagai pencampur ransum pakan ternak, antimikrob, antijamur, serat bahan pangan, pestisida, herbisida, virusida, tanaman, dan deasedifikasi buah-buahan, sayuran dan penjernih sari buah. Fungsinya sebagai antimikrob dan anti jamur juga diterapkan dibidang kedokteran kitin dan kitosan dapat mencegah pertumbuhan Candida albican dan Staphvlacoccus aureus. Selain itu bipolimer tersebut juga berguna sebagai antikoagulan, antitumor, antivirus, pembuluh darah-kulit dan ginjal sintetik, bahan pembuat lensa kontak, aditif kosmetik, membran dialis, bahan shampoo, dan kondisioner rambut, zat hemostatik, penstabil liposom, bahan ortoprdik, pembalut luka dan benang bedah yang mudah diserap, serta mempertinggi daya kekebalan, antiinfeksi.(Purwantiningsih,S.,1992)
Kitosan banyak digunakan oleh berbagai industri antara lain industri farmasi, kesehatan, biokimia, bioteknologi, pangan, pengolahan limbah, kosmetik, agroindustri, industri tekstil, industri kertas dan industri elektronika. Aplikasi khusus berdasarkan sifat yang dipunyai antara lain untuk pengolahan limbah cair terutama bahan bersifat resin penukar ion untuk
meminimalisasi logam-logam berat, mengkoagulasi minyak/lemak, serta mengurangi kekeruhan, penstabilan minyak, rasa dan lemak dalam produksi industri pangan. (Rismana,2004)
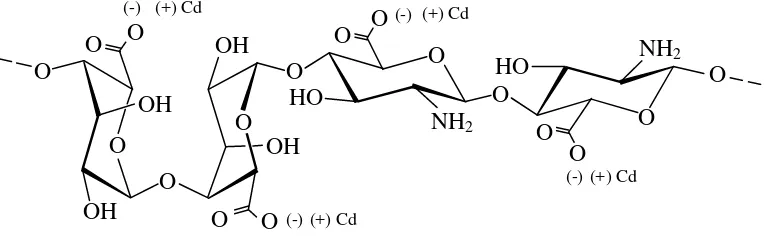
Gambar 2.4 Struktur Alginat dilapisi kitosan dalam menyerap ion logam Kadmium
2.3.3 Pengolahan Kitin dan Kitosan
Kitin yang terdapat padat kulit atau cangkang ini masih terikat dengan protein, CaCO3, pigmen,
dan lemak. Berbagai teknik dilakukan untuk memisahkannya, tetapi pada umumnya ada tiga tahapan yaitu deproteinisasi dengan NaOH encer, demineralisasi dengan HCl encer dan deasitilasi dengan NaOH pekat
Beberapa penelitian menggunakan proses deproteinisasi dan demineralisasi yang berbeda, ada yang demineralisasi dulu kemudian deproteinisasi atau sebaliknya. Pilihan pengolahan tergantung dari tujuan penggunaan kitosan (Brine, 1984).
2.3.4 Deproteinisasi
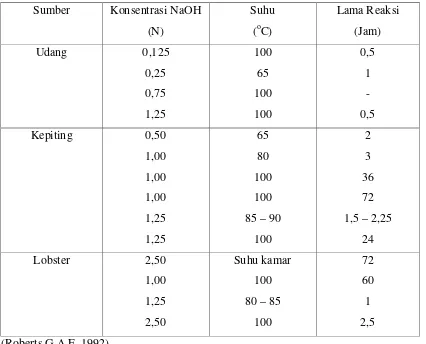
Proses deproteinisasi ini dilakukan untuk menghilangkan protein yang terdapat pada kulit atau cangkang kepiting. Proses deproteinisasi ini menggunakan berbagai pereaksi seperti Na2CO3,
Tabel 2.1 Kondisi Perlakuan dengan NaOH pada Proses Deproteinisasi
Penggunaan enzim untuk memisahkan protein juga dilakukan dalam beberapa penelitian, diantaranya dengan pepsin, setelah didemineralisasi sebelumnya dengan suatu zat. Perlakuan dengan enzim ini masih menyisakan protein sekitar 5 % yang memerlukan proses lanjutan (Roberts,G.A.F, 1992).
2.3.5 Demineralisasi
Proses demineralisasi bertujuan untuk memisahkan kitin dari CaCO3. Proses demineralisasi ini
menggunakan berbagai pereaksi asam seperti HCl, HNO3, H2SO4, CH3COOH dan HCOOH.
Umumnya menggunakan HCl 50 % (Roberts,G.A.F, 1992).
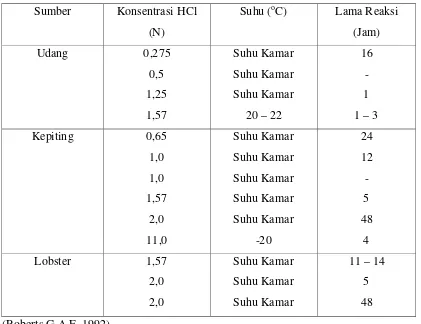
Tabel 2.2 Kondisi Perlakuan dengan HCl pada Proses Demineralisasi
Kitin yang diperoleh dari proses deproteinisasi dan demineralisasi tidak dapat larut dalam sebahagian besar pereaksi kimia. Untuk memudahkan kelarutannya, maka kitin dideasetilasi dengan pelarut alkali menjadi kitosan. Setelah melalui proses deasetilasi maka daya penyerapan kitin akan meningkat dengan bertambahnya gugus amino (NH3) yang terdapat di dalamnya
(Muzzarelli, 1997).
kitosan dengan derajat deasetilasi 92 %. Derajat deasetilasi kitosan tergantung dari konsentrasi alkali yang digunakan, lama reaksi, ukuran partikel kitin dan berat jenis (Hwang dan Shin ,2000) Makin tinggi konsentrasi alkali yang digunakan makin rendah suhu atau makin singkat waktu yang diperlukan dalam proses ini.
2.3.7 Klasifikasi Isoterm Adsorpsi
Terdapat 5 persamaan isoterm yang dapat digunakan untuk mengambil proses adsorpsi, yaitu isoterm adsorpsi Langmuir, Freundlich, Temkin, Brunauer-Emmett-Teller (BET) dan dubirin. Akan tetapi, hanya 2 persamaan pertama yang sering digunakan
a. Isoterm Langmuir
Isoterm Langmuir merupakan isoterm adsorpsi yang pertama dikembangkan secara teoritis sekaligus menjadi dasar bagi banyak persamaan isoterm baru. Isoterm Langmuir ini mengasumsikan bahwa adsorbat hanya membentuk lapisan tunggal diatas permukaan adsorben yang homogen. Isoterm Langmuir juga dapat digunakan untuk mengamati adsorpsi serempak 2 gas pada permukaan adsorben yang sama. Pada kasus ini, kemungkinan terjadinya reaksi antara kedua gas tersebut harus diperhatikan. Markham dan Benton adalah dua peneliti pelopor yang pertama kali mengembangkan isoterm Langmuir untuk campuran gas biner dengan tetap menjaga semua asumsi teori asli, yaitu permukaan adsorben diasumsikan homogen.
Beberapa hasil kemisorpsi menunjukkan bahwa kesahihan persamaan Langmuir hanya terjadi pada kisaran yang pendek dan terbatas. Selain itu, perhitungan kalor adsorpsi pada teori Langmuir tidak mempertimbangkan permukaan yang telah menjerap adsorbat, sedangkan pada kenyataanya kalor adsorpsi akan turun seiring dengan berkurangnya jumlah daerah luasan permukaan yang belum menjerap adsorbat.
b. Isoterm Freundlich
Isoterm Freundlich adalah bentuk terbatas dari isoterm Langmuir dan hanya bisa diterapkan pada tekanan uap sedang. Isoterm Freundlich biasanya berlaku untuk adsorpsi cairan pada permukaan padatan. Isoterm ini biasanya paling umum digunakan, karena dapat mencirikan kebanyakan proses adsorpsi dengan baik (Pope, 2004). Isoterm Freundlich menganggap bahwa pada sisi permukaan adsorben terjadi proses adsorpsi di bawah kondisi yang diberikan. Namun, Isoterm Freundlich tidak memperkirakan keberadaan sisi-sisi permukaan yang dapat mengganggu terjadinya adsorpsi saat kesetimbangan tercapai. Di sisi lain, hanya ada beberapa sisi aktif saja yang mampu mengadsorpsi molekul terlarut (Pope, 2004).
2.3.8 Interaksi Kitosan Dengan Ion Logam
Muzzarelli (1977) menyatakan bahwa kitosan mengikat logam melalui pertukaran ion, penyerapan dan pengkhelatan. Ketiga proses tersebut bergantung pada ion logam masing – masing.
2.3.9 Sifat-sifa Kitosan
Kitosan adalah padatan amorf putih yang tidak larut dalam alkali dan asam mineral kecuali pada keadaan tertentu. Keterlarutan kitosan yang paling baik ialah dalam larutan asam asetat 1%, asam format 10% dan asam sitrat 10%. Kitosan tidak dapat larut dalam asam piruvat, asam laktat, dan asam-asam anorganik pada pH tertenu, walaupun setelah dipanaskan dan diaduk dengan waktu yang agak lama. Keterlarutan kitosan dalam larutan asam format ataupun asam asetat dapat membedakan kitosan dan kitin karena kitin tidak dapat melatut dalam keadaan pelarut asam tersebut.
penyembuhan luka, dan memperbaiki sifat pengikatan warna. Kitosan merupakan penkelat yang kuat untuk ion logam transisi. Kitosan mempunyai kemampuan untuk mengadsorbsi logam dan membentuk kompleks kitosan dengan logam. (Robert,G.A.F,1992)
Kitosan dibedakan dari kitin oleh kelarutannya dalam larutan asam encer. Kitosan bermuatan positif karena kelompok amina pada pH asam, yang besarannya tergantung pada tingkat deasetilasi, dan dengan demikian kitosan diklasifikasikan sebagai polielektronik kationik, sedangkan polisakarida yang lain memberikan muatan netral ataupun anionik.(Hwang dan Shin,2001)
2.3.10 Sifat Fisik-Kimia pada Kitin
Kitin merupakan bahan yang tidak beracun dan bahkan mudah terurai secara hayati (biodegradable). Bentuk fisiknya merupakan padatan amorf yang berwarna putih dengan kalor spesifik 0,373 ± 0,03 kal/g/oC (Knorr,1984).
Kitin hampir tidak larut dalam air, asam encer, dan basa, tetapi larut dalam asam formiat, asam metanasulfonat, N,N-dimetilasemida yang mengandung 5% litium klorida, heksafluoroisopropil alkahol, heksafluoroaseton dan campuran 1,2-diklorotana-asam trikloroasetat dengan nisbah 35:65 (%[V/V]).(Hirano,1986). Asam mineral pekat seperti H2SO4,
HNO3 dan H3PO4 dapat melarutkan kitin sekaligus menyebabkan rantai panjang kitin
terdegradasi menjadi satuan-satuan yang lebih kecil. (Bastaman,1989)
2.4 Pendayagunaan Limbah Udang
Limbah udang yang mencapai 30-40% dari produksi udang beku belum banyak dimanfaatkan. Menurut Moelyanto (1979), limbah udang selain dimanfaatkan sebagai bahan pangan, dapat juga dipergunakan untuk keperluan industri. Pembuatan kitosan dari kulit udang dapat dipakai sebagai bahan kimia untuk industri dan kertas. Kepala udang yang menyatu dengan jengger udang sebagai limbah industri udang beku baru sebagian kecil yang dimanfaatkan, yaitu dibuat tepung
kepala yang dibuat sebagai pencampur bahan dalam pembuatan pellet untuk pakan ternak (Mudjiman, 1982)
Kulit udang mengandung unsur yang bermanfaat yaitu protein kalsium dan kitin yang mempunyai kegunaan dan prospek yang baik dalam industri. Protein dan kalsium dapat digunakan sebagai bahan tambahan dalam pembuatan pakan ternak sedangkan kitin dapat dimanfaatkan sebagai surfaktan, zat pengemulsi, bahan tambahan untuk antibiotik dan kosmetik (Knorr, 1984)
2.5 Pencemaran Logam
Penggunaan logam sebagai bahan baku berbagai jenis industri untuk memenuhi kebutuhan manusia akan mempengaruhi kesehatan manusia melalui 2 jalur, yaitu :
1. Kegiatan industri akan menambah polutan logam dalam lingkungan udara, air, tanah, dan makanan
2. Perubahan biokimia logam sebagai bahan baku berbagai jenis industri biasa mempengaruhi kesehatan manusia.
Dalam kehidupan sehari-hari, manusia tidak terpisahkan dari benda-benda yang berasal dari logam. Logam yang digunakan untuk membuat alat perlengkapan rumah tangga, seperti sendok, garpu, pisau, dan berbagai jenis peralatan rumah tangga lainnya. Pesatnya pembangunan dan penggunaan berbagai bahan baku logam biasanya berdampak negatif yaitu munculnya kasus pencemaran yang melebihi batas sehingga mengakibatkan kerugian dan meresahkan masyarakat yang tinggal di sekitar daerah perindustrian maupun masyarakat pengguna produk industri tersebut. Hal itu terjadi karena sangat besarnya resiko terpapar logam berat maupun logam transisi yang bersifat toksik dalam dosis atau konsentrasi tertentu.
dilingkungan udara, air, dan tanah yang berasal dari proses alami dan kegiatan industri. Proses alami antara lain siklus alamiah sehingga bebatuan gunung berapi biasa memberikan kontribusi ke lingkungan udara, air, dan tanah. Kegiatan manusia yang biasa menambah polutan bagi lingkungan berupa kegiatan industri. Pencemaran logam, baik industri, kegiatan domestik, maupun sumber alami dari batuan akhirnya sampai ke sungai atau laut dan selanjutnya mencemari manusia melalui ikan, air minum, atau air sumber irigasi lahan pertanian sehingga tanaman sebagai sumber pangan manusia tercemar logam.
2.5.1. Logam Kadmium (Cd)
Kadmium (Cd) adalah logam berwarna putih perak, lunak, mengkilap, tidak larut dalam basa, mudah bereaksi, serta menghasilkan kadmium oksida bila dipanaskan. Cd umumnya terdapat dalam kombinasi dengan klor (Cd klorida) atau belerang (Cd sulfit). Kadmium bisa membentuk ion Cd2+ yang bersifat tidak stabil. Cd memiliki nomor atom 40, berat atom 112,4 g/mol, titik leleh 321o C, dan titik didih 767oC.
Kadmium bersifat lentur, tahan terhadap tekanan, serta dapat dimanfaatkan sebagai pencampur logam lain, seperti nikel (Ni), emas (Au), kuprum (Cu), dan besi (Fe). Cd terutama terdapat dalam kerak bumi bersama dengan seng (Zn). Terdapat satu jenis mineral Cd di alam, yaitu green ockite (CdS) yang terdapat dalam lingkungan pada kadar yang rendah berasal dari kegiatan penambangan seng (Zn), timah (Pb), dan kobalt (Co) serta kuprum (Cu). Sementara dalam kadar tinggi, kadmium berasal dari emisi industri, antara lain dari hasil sampingan penambagan, peleburan seng (Zn) dan timbal (Pb). Sumber pencemaran dan paparan Cd berasal dari populasi udara, keramik, rokok, air sumur, makanan yang tumbuh di daerah pertanian yang tercemar Cd, fungisida, pupuk, serta cat. (Widowati,W. 2006)
2.5.2 Logam Berat
(termasuk manusia), karena sifatnya yang meracun dan dapat menyebabkan kematian apabila jumlahnya melewati ambang batas yang ditetapkan. Kandungan logam berat di lingkungan dapat dikurangi dengan cara menyerapnya, salah satunya dengan menggunakan kitosan.
Beberapacontoh logam berat ialah Hg, Zn, Cd, Cu, Co, Pb, dan Cr. Proses penyerapan logam berat pada kitosan dan modifikasinya berlangsung spontan (Karthikeyan et al., 2004) Bahkan, Gotoh et al., (2004) menyatakan bahwa Cu2+, Co2+, dan Cd2+ mencapai kesetimbangan adsorpsi hanya dalam 10 menit. Dalam proses adsorpsi logam berat dari limbah, kompetisi antar-ion logam mungkin saja terjadi. Ion logam dengan afinitas tinggi pada kitosan akan memiliki kapasitas adsorpsi yang tinggi pula. (Gotoh et al., 2004)
2.6 Spektrofotometri Serapan Atom
Spektrofotometer serapan atom adalah metoda pengukuran kuantitatif suatu unsur yang terdapat dalam suatu cuplikan berdasarkan penerapan cahaya pada panjang gelombang tertentu oleh atom – atom bentuk gas dalam keadaan dasar. Telah lama ahli kimia menggunakan pancaran radiasi oleh atom yang dieksitasikan dalam suatu nyala sebagai alat analisis. Fraksi atom – atom yang tereksitasi berubah secara eksponensial dengan temperatur. Teknik ini digunakan untuk penetapan sejumlah unsur, kebanyakan logam dan sampel yang sangat beraneka ragam (Walsh, 1955).
2.6.1. Prinsip Dasar Spektrofotometer Serapan Atom
Jika cahaya dengan panjang gelombang resonansi dilewatkan nyala yang mengandung atom-atom yang bersangkutan, maka sebagian cahaya itu akan diserap, dan jauhnya penyerapan akan berbanding lurus dengan banyaknya atom keadaan dasar yang berada dalam nyala. Hal ini merupakan dasar penentuan kuantitatif logam-logam dengan menggunakan SSA.
Proses terbentuknya uap yang mengandung atom-atom logam dalam nyala, dapat diringkaskan sebagai berikut : bila suatu larutan yang mengandung senyawa yang cocok dari
logam yang akan diselidiki itu dilewatkan ke dalam nyala, terjadilah peristiwa berikut secara berturutan dengan cepat :
1. Penghilangan pelarut atau evaporasi yang meninggalkan residu padat
2. Penguapan zat padat dilanjutkan dengan desosiasi menjadi atom-atom penyusun yang mula-mula akan berada dalam keadaan dasar.
Beberapa atom dapat tereksitasi oleh energi termal dari nyala ke tingkatan-tingkatan energi yang
lebih tinggi dan mencapai kondisi dalam mana mereka akan memancarkan energi. ( Vogel, A.I, 1992)
2.6.2 Cara Kerja Spektrofotometer Serapan Atom
Setiap alat SSA terdiri atas tiga komponen berikut : a. Unit atomisasi
b. Sumber radiasi
c. Sistem pengukur fotometrik
Atomisasi dapat dilakukan baik dengan nyala maupun dengan tungku. Untuk mengubah unsur metalik menjadi uap atau hasil disosiasi diperlukan energi panas. Temperatur harus benar-benar terkendali dengan sangat hati-hati agar proses atomisasinya sempurna. Ionisasi harus dihindarkan dan ini dapat terjadi bila temperatur terlalu tinggi.
Bahan bakar dan gas oksidator dimasukkan dalam kamar pencampur kemudian dilewatkan melalui baffle menuju ke pembakar. Nyala akan dihasilkan. Sampel dihisap masuk ke kamar pencampur. Hanya tetesan kecil yang dapat melalui buffle. Dengan gas asetilen dan oksidator udara tekan, temperatur dapat dikendalikan secara elektris. Biasanya temperatur dinaikkan secara bertahap, untuk menguapkan dan sekaligus mendisosiasikan senyawa yang dianalisis. (Khopkar, S.M, 1990)
2.6.3 Gangguan Pada SSA dan Mengatasinya
Gangguan yang nyata pada SSA adalah seringkali didapatkan suatu harga yang tidak sesuai dengan konsentrasi unsur sampel yang ditentukan. Penyebab dari gangguan ini adalah faktor matriks sampel, faktor kimia adanya gangguan molekuler yang bersifat menyerap radiasi.
Sampel dalam bentuk molekul karena disosiasi yang tidak sempurna akan cendrung mengabsorbsi radiasi dari sumber radiasi. Demikian juga terjadinya ionisasi atom akan menjadi sumber kesalahan pada SSA oleh karena spektrum radiasi oleh ion jauh berbeda dengan spektrum absorbsi atom netral yang memang akan ditentukan. Ada beberapa usaha untuk mengurangi gangguan kimia pada SSA yaitu dengan jalan :
1. Menaikkan temperatur nyala agar mempermudah penguraian untuk itu dipakai gas pembakar campuran C2H2 + N2O yang memberikan nyala dengan temperatur yang
tinggi.
2. Menambahkan elemen pengikat gugus atau atom penyangga, sehingga terikat kuat akan tetapi atom yang ditentukan bebas sebagai atom netral. Misalnya, penentuan logam yang terikat sebagai garam, dengan penambahan logam, yang lainnya akan terjadi ikatan lebih kuat dengan anion penggangu.
3. Pengeluaran unsur penggangu dari matriks sampel dengan cara ekstraksi. (Mulja.M, 1995)
BAB 3
BAHAN DAN METODOLOGI PENELITIAN
3.1. Alat dan Bahan
3.1.1 Alat-alat
-Spektrofotometer Serapan Atom GBC Avanta
-Timbangan analitik Sartorius -Kertas saring
-Pengaduk magnetic stirrer -Desikator
-Pengerus porselen -Ayakan 250 µ m -Corong
-Oven
-Pipet volum Pyrex
-Erlenmeyer Pyrex
-Beaker Glass Pyrex
-Gelas ukur Pyrex
3.1.2 Bahan-bahan
-Rumput laut sagarassum -Aquadest
-HCl 37% p.a (E Merck)
-CH3COOH glasial p.a (E Merck)
-NaOH p.a (E Merck) -Asam pospat 85% p.a (E Merck) -Larutan induk CdCl2 p.a (E Merck)
3.2 Prosedur Penelitian
3.2.1. Pembuatan Larutan Pereaksi
a. Larutan NaOH 0,5%
Sebanyak 100 g NaOH dimasukkan ke tempat pencucian kitin kemudian di tambahkan aquadest sebanyak 20 L.
b. Larutan NaOH 5%
Sebanyak 1 kg NaOH dimasukkan ketempat pencucian kitin kemudian tambahkan aquadest sebanyak 20 L.
c. Larutan HCl 5%
Sebanyak 2,7 L HCl dimasukkan ke tempat pencucian kitin kemudian tambahkan aquadest sebanyak 20 L.
d. Larutan NaOH 50%
Sebanyak 1 kg NaOH dimasukkan ke tempat pencucian kitin kemudian tambahkan aquadest sebanyak 2 L.
e. Larutan Asam Asetat 1%
Sebanyak 10 mL asam asetat glasial dimasukkan ke dalam labu takar 100 mL. Kemudian tambahkan aquadest sampai garis batas, kemudian homogenkan.
f. Larutan HCl 1,5 M
Sebanyak 62 mL H2SO4(p) dimasukkan ke dalam labu takar 1000 mL secara perlahan.
Ditambahkan aquadest secara perlahan-lahan sampai garis batas. Ditunggu sampai larutan benar-benar dingin. Kemudian di homogenkan.
g. Larutan Kitosan 1%
Sebanyak 1 g kitosan dilarutkan dalam 100 mL larutan asam asetat 1%.
3.2.2. Pembuatan Kitin
Udang dikupas dan diambil kulitnya . Lalu dicuci dengan air hingga bersih. Direndam dalam larutan NaOH 0,5% selama 24 jam. Lalu dicuci dengan air hingga pH 6,8. Kemudian dilakukan proses dideproteinisasi dengan merendamkan kulit udang dalam larutan NaOH 5% selama 24 jam. Lalu dicuci dengan air hingga pH 6,8. Selanjutnya dilakukan proses demineralisasi dengan merendamkan kulit udang dalam larutan HCl 5% selama 24 jam. Lalu dicuci dengan air hingga pH 6,8. Dilakukan uji kelarutan dengan asam pospat 85%. Setelah itu dikeringkan pada suhu kamar selama 6 hari.
3.2.3. Pembuatan Kitosan
Kitin Kering direndam dengan NaOH 50% selama 7 hari dan diaduk setiap hari. Diuji kelarutannya dengan asam asetat 1%. Dicuci dengan air hingga bersih. Keringkan pada suhu kamar. Setelah kering, kitosan dihaluskan.
3.2.4. Penyiapan dan aktivasi biosorben rumput laut
Rumput laut Sargassum dicuci hingga bersih dan dibilas dengan aquadest kemudian dikeringkan. Rumput laut yang sudah kering digerus dan diayak. Dimasukkan ke dalam oven dengan suhu 70oC. Disimpan dalam desikator setelah itu diaktivasi dengan HCl 1,5 M. Dimasukkan ke dalam erlenmeyer 500 mL untuk diaktivasi selama 20 menit sambil diaduk. Disaring dengan kertas saring dan dicuci dengan aquadest hingga pH netral. Dikeringakan dengan oven pada suhu 45oC selama 2 hari. Kemudian disimpan dalam desikator.
3.2.5 Larutan Standar Ion Kadmium (Cd2+) 100 mg/L
Sebanyak 10 mL larutan induk ion kadmium (Cd2+) 1000 mg/L dimasukkan kedalam labu takar 100 cc lalu diencerkan dengan larutan pengencer sampai garis batas setelah itu dihomogenkan.
3.2.6 Larutan Seri Standar Ion Kadmium (Cd2+) 10;20;30;40;50 mg/L
Dipipet sebanyak 5;10;15;20;25 mL larutan standar ion kadmium (Cd2+) 100 mg/L dimasukkan kedalam labu takar 50 cc lalu diencerkan dengan larutan pengencer sampai garis batas setelah itu dihomogenkan.
3.2.7 Rumput Laut Dilapisi Kitosan
Sebanyak 20 g rumput laut Sargassum yang telah diaktivasi dispray hingga basah dengan larutan kitosan 1%. Dikeringkan dalam oven pada suhu 45oC kemudian di haluskan.
3.2.8 Penambahan Rumput Laut
Dipipet 30 mL larutan seri standar kadmium 10 mg/L, dimasukkan kedalam beaker glass 100 mL. Ditambahkan 3 g rumput laut yang telah diaktivasi tanpa dilapisi kitosan. Diaduk dengan menggunakan magnetik stirrer selama 10 menit kemudian disaring dan filtratnya dianalisa dengan Spektrofotometer Serapan Atom.
3.2.9 Penambahan Rumput Laut Dilapisi Kitosan
Dipipet 30 mL larutan seri standar kadmium 10 mg/L, dimasukkan kedalam beaker glass 100 mL. Ditambahkan 3 g rumput laut yang telah diaktivasi dan sudah dilapisi kitosan. Diaduk dengan menggunakan magnetik stirrer selama 10 menit kemudian disaring dan filtratnya dianalisa dengan Spektrofotometer Serapan Atom.
3.3 Bagan Penelitian
3.3.1 Proses Penyediaan Kitin (Yang telah dimodifikasi)
Dikupas dan diambil kulitnya
Dicuci dengan air hingga bersih
Direndam dalam larutan NaOH 0,5% selama 24 jam Dicuci dengan air hingga pH 6,8
Dideprotenisasi dengan larutan NaOH 5% selama 24 jam Dicuci dengan air hingga pH 6,8
Didemineralisasi dengan HCl 5% selama 24 jam Dilakukan uji kelarutan dengan asam posfat 98-100% Dicuci dengan air hingga pH 6,8
Dikeringkan pada suhu kamar
udang
kulit udang
Hasil
3.3.2 Proses Penyedian Kitosan Menurut Metode Alimuniar,A dan Zainuddin,R (1992)
Direndam dalam NaOH 50% selama 7 hari
Diuji kelarutannya dengan asam asetat 1%
Dicuci dengan air hingga pH 6,8 Disaring
Dikeringkan diudara terbuka pada suhu kamar Diuji kelarutan
Dihaluskan
Kitin Kering
Kitosan Basah
Kitosan kering
Hasil
3.3.3 Penyiapan dan aktivasi biosorben
Dicuci hingga bersih Dibilas dengan aquadest
Dikeringkan Digerus dan diayak
Dikeringkan dalam oven dengan suhu 70oC Disimpan dalam desikator
Diaktivasi dengan HCl 37% dengan konsentrasi 1,5 M
Dimasukkan ke dalam erlenmeyer Diaktivasi selama 20 menit Diaduk
disaring dengan kertas saring Dicuci dengan aquadest
Dikeringkan dengan oven pada suhu 45oC Disimpan dalam desikator
Rumput Laut Sargassum
Hasil
3.3.4 Pembuatan Larutan Seri Standar Ion Kadmium (Cd2+)
Dipipet sebanyak 10 mL larutan induk ion kadmium (Cd2+) 1000 mg/L
Dimasukkan ke dalam labu takar 100 cc
Diencerkan dengan larutan pengencer sampai garis tanda Diaduk hingga homogen
Dipipet sebanyak 5;10;15;20;25 mL larutan standar ion kadmium (Cd2+) 100 mg/L
Dimasukkan ke dalam labu takar 50 cc
Diencerkan dengan larutan pengencer sampai garis tanda Diaduk hingga homogen
Diukur absorbansinya dengan Spektrofotometer Serapan Atom
Larutan induk ion kadmium (Cd2+) 1000 mg/L
Larutan seri standar ion kadmium (Cd2+) 100
Hasil
3.3.5 Rumput Laut Dilapisi Kitosan
Diambil 20 g rumput laut yang telah diaktivasi
Dispray hingga basah dengan larutan kitosan 1%
Dikeringkan dalam oven
Dihaluskan
Rumput Laut
Rumput laut yang dilapisi kitosan
3.3.6 Penambahan Rumput Laut
Dipipet 30 mL larutan standar kadmium 10 mg/L
Dimasukkan kedalam beaker glass 100 mL
Ditambahkan 3 g rumput laut yang telah diaktivasi
Diaduk dengan menggunakan magnetik stirrer selama 10 menit
Disaring
Dianalisa dengan Spektrofotometri Serapan Atom
Larutan Seri standar Kadmium (Cd2+) 10 mg/L
Filtrat Residu
Hasil
3.3.7 Penambahan Rumput Laut Dilapisi Kitosan
Dipipet 30 mL larutan standar kadmium 10 mg/L
Dimasukkan kedalam beaker glass 100 mL
Ditambahkan 3 g rumput laut yang telah diaktivasi dan sudah dilapisi kitosan
Diaduk dengan menggunakan magnetik stirrer selama 10 menit
Disaring
Dianalisa dengan Spektrofotometri Serapan Atom
Larutan Seri standar Kadmium (Cd2+) 10 mg/L
Filtrat Residu
Hasil
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil Penelitian
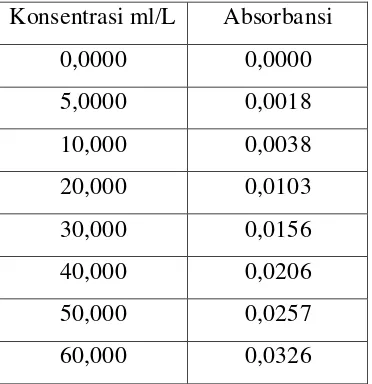
Dari penelitian yang telah dilakukan pada pengukuran konsentrasi logam kadmium dapat dilihat pada tabel 4.1 sebagai berikut :
Tabel 4.1 Konsentrasi dan Absorbansi Larutan Standar Kadmium (Cd2+)
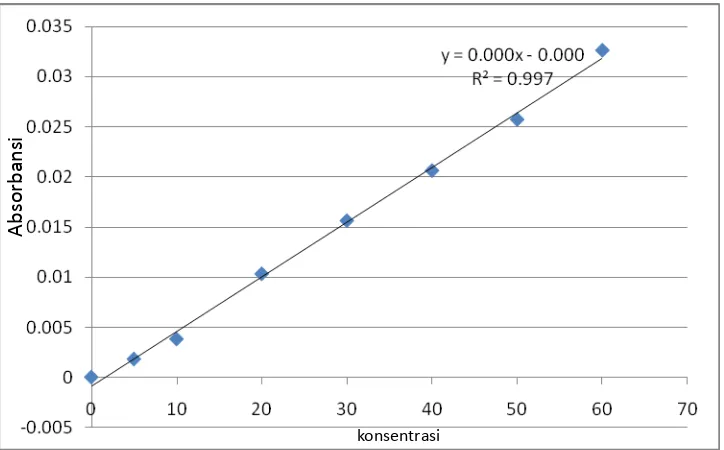
Gambar 4.1 Kurva Kalibrasi Larutan Standart Kadmium (Cd2+)
Kondisi alat Spektrofotometer Serapan Atom (SSA) pada pengukuran konsentrasi logam kadmium (Cd2+) dapat dilihat pada tabel 4.2
Tabel 4.2 Kondisi alat Spektrofotometer Serapan Atom (SSA) GBC Avanta pada pengukuran konsentrasi logam kadmium (Cd2+)
No Parameter Logam Kadmium
1. Panjang gelombang (nm) 326.10 nm 2. Tipe nyala Flame 3. Kecepatan aliran gas pembakar
(L/min)
2.000 L/min
4. Kecepatan aliran udara (L/min) 10.00 L/min 5. Lebar celah (nm) 0.50 nm 6. Ketinggian tungku (mm) 15.10 mm
34
A
bs
o
rba
ns
i
Tabel 4.3 Variasi Konsentrasi dan Absorbansi Terhadap Jumlah (Cd2+) Yang Terserap Pada Rumput Laut Sargassum Teraktivasi HCl
Berat
4.1.1 Pengolahan Data Logam Kadmium (Cd2+)
4.1.1.1 Penurunan Persamaan Garis Regresi dengan Metoda Least Square
Hasil pengukuran absorbansi yang diperoleh dari larutan seri standart logam kadmium (Cd2+) pada tabel 4.1 diplotkan terhadap konsentrasi sehingga diproleh kurva kalibrasi berupa garis linier. Persamaan garis linier untuk kurva kalibrasi ini dapat diturunkan dengan metoda least square dengan data tabel 4.4
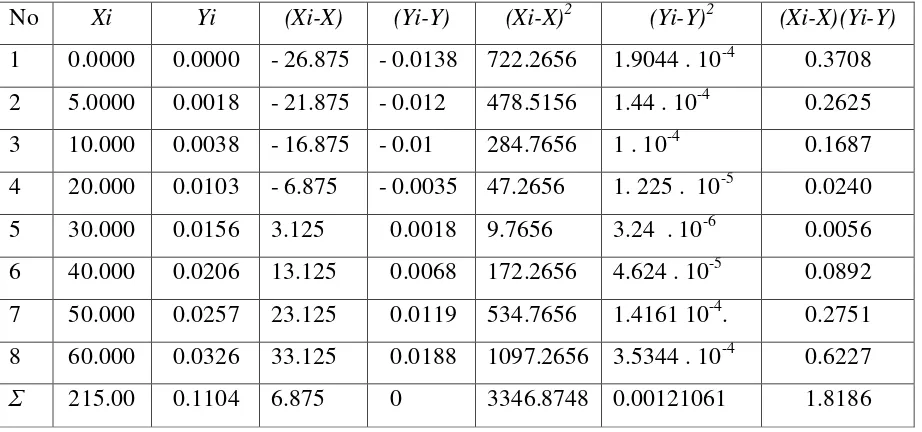
Tabel 4.4 Penurunan persamaan garis regresi logam kadmium (Cd2+) berdasarkan pengukuran absorbansi larutan seri standar logam kadmium (Cd2+)
No Xi Yi (Xi-X) (Yi-Y) (Xi-X)2 (Yi-Y)2 (Xi-X)(Yi-Y)
1 0.0000 0.0000 - 26.875 - 0.0138 722.2656 1.9044 . 10-4 0.3708 2 5.0000 0.0018 - 21.875 - 0.012 478.5156 1.44 . 10-4 0.2625 3 10.000 0.0038 - 16.875 - 0.01 284.7656 1 . 10-4 0.1687 4 20.000 0.0103 - 6.875 - 0.0035 47.2656 1. 225 . 10-5 0.0240 5 30.000 0.0156 3.125 0.0018 9.7656 3.24 . 10-6 0.0056 6 40.000 0.0206 13.125 0.0068 172.2656 4.624 . 10-5 0.0892 7 50.000 0.0257 23.125 0.0119 534.7656 1.4161 10-4. 0.2751 8 60.000 0.0326 33.125 0.0188 1097.2656 3.5344 . 10-4 0.6227
Σ 215.00 0.1104 6.875 0 3346.8748 0.00121061 1.8186
X = = 26,875 Y = = 0,0138
Persamaan garis regresi untuk kurva kalibrasi dapat diturunkan dari persamaan garis : Y = ax + b
Dimana :
a = slope
b = intersept
Selanjutnya harga slope dapat dientukan dengan menggunakan metoda least square sebagai berukut :
Dengan mensubsitusikan harga – harga yang tercantum pada tabel 4.3 pada persamaan ini maka diperoleh :
Maka persamaan garis yang diperoleh adalah
Y = x + 0,0138
4.1.1.2 Koefisien Korelasi
Koefisien korelasi dapat ditentukan dengan menggunakan persamaan sebagai berikut :
{
( (Xi X) )( (Yi Y) )}
Koefisien korelasi untuk logam besi (Cd2+) adalah
{
(3346,874)(0,00121061)}
4.1.1.3 Persentasi (%) Penurunan Konsentrasi Logam Kadmium (Cd2+)
Persentase (%) penurunan konsentrasi logam kadmium (Cd2+) dapat ditentukan dengan menggunakan rumus :
Maka persentasi (%) penurunan konsentrasi logam kadmium (Cd2+) dalam larutan standar setelah penambahan rumput laut teraktivasi adalah
Dengan cara yang sama dapat dihitung persentasi (%) penuruna logam dalam kadmium (Cd2+) larutan standar setelah penambahan kitosan dan rumput laut dilapisi kitosan.
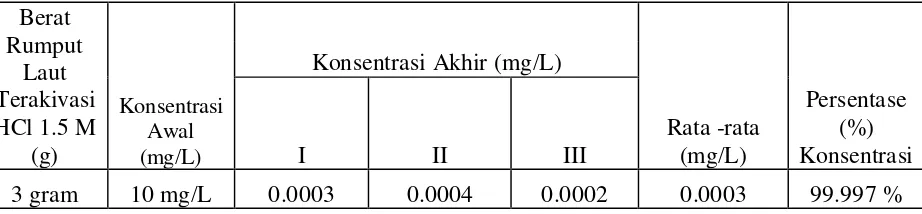
Tabel 4.4 Data Persentase (%) Konsentrasi Logam Kadmium (Cd2+) Dalam Larutan Standar Setelah Penambahan Rumput Laut Teraktivasi HCl 1,5M
Berat
Tabel 4.5 Data Persentase (%) Konsentrasi Logam Kadmium (Cd2+) Dalam Larutan Standar Setelah Penambahan Rumput Laut Dilapisi Kitosan
4.2 Pembahasan
Dari hasil penelitian diperoleh bahwa penyerapan logam kadmium Cd2+ setelah penambahan rumput laut teraktivasi, dan rumput laut dilapisi kitosan berbeda. Dimana penyerapan logam kadmium Cd2+ setelah penambahan rumput laut dilapisi kitosan memiliki penyerapan yang lebih besar dari pada penambahan rumput laut teraktivasi. Ini disebabkan karena rumput laut memilki sifat – sifat yang berbeda satu dengan yang lain sehingga daya penyerapannya berbeda juga. Begitu juga dengan rumput laut dilapisi kitosan yang memiliki sifat perpaduan antara kitosan dengan rumput laut teraktivasi HCl 1.5 M.
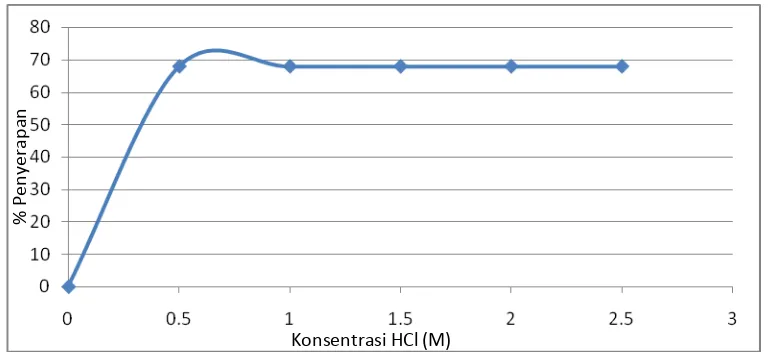
Dimana dilakukan variasi konsentrasi asam klorida 5 M; 1 M; 1,5 M; 2 M; dan 2,5 M untuk mengetahaui jumlah asam optimum yang diperlukan untuk mengaktivasi biosorben secara maksimum, yang ditandai dengan jumlah Cd2+ yang paling banyak terserap. Dari percobaan yang dilakukan bahwa jumlah Cd2+ yang terserap sebanyak 68.966% pada konsentrasi 1,5 M seiring dengan kenaikan rasio asam klorida yang digunakan pada aktivasi rumput laut sampai mencapai titik optimum. Hal ini menunjukkan bahwa sebelum titik optimum tercapai, semakin bertambah jumlah asam klorida yang digunakan pada proses aktivasi semakin bertambah pula jumlah Cd2+ yang terserap. Hal ini disebabkan karena asam (H+) dapat melarutkan logam-logam pengotor, dapat menukar ion logam yang terikat pada biosorben, sehingga jumlah situs aktif menjadi lebih banyak. Konsentrasi biosorben optimum untuk aktivasi biosorben menggunakan asam klorida (HCl) adalah 1,5 M.
Penyerapan kation logam oleh kitosan memanfaatkan keberadaan pasangan elektron bebas pada gugus – OH dan NH2. Oleh karena itu, sebaiknya proses penyerapan dilakukan dalam
lingkungan yang tidak asam agar gugus –NH2 tidak terprotonasi. Pasangan elektron pada gugus –
OH dan – NH2 akan berperan sebagai ligan (basa lewis, donor pasangan elektron) yang dapat
Rumput laut dilapisi kitosan atau juga kitosan-alginat kapasitas adsorpsi hidrogel dengan penaut-silang glutaraldehida terhadap Cd2+ dengan konsentrasi logam 10 ppm. Pola isoterm hidrogel kitosan-alginat dalam menyerap Cd2+ mengikuti pola pola isoterm Langmuir dan Freundlich. Hal ini berarti, bahwa sisi aktif pada permukaan kitosan adalah heterogen dan adsorpsi dapat terjadi secara mono- dan multilapisan. Penyerapan kation logam Cd2+ oleh rumput laut yang dilapisi kitosan dengan keberadaan pasangan elektron bebas pada gugus COO- dan – NH2 akan berperan sebagai ligan yang dapat berinteraksi dengan kation logam melalui
mekanisme pembentukan ikatan kovalen koordinasi.
BAB 5
KESIMPULAN DAN SARAN
5.1 Kesimpulan
Dari data yang diperoleh pada penelitian ini, maka dapat disimpulkan bahwa rumput laut yang telah diaktivasi dengan HCl 1,5 M dilapisi kitosan memiliki daya atau kemampuan yang lebih besar dalam mengadsorpsi logam kadmium (Cd2+) yaitu sebesar (99.997%) dibandingkan dengan rumput laut yang telah teraktivasi saja sebesar (79.61%).
5.2 Saran
Disarankan bagi peneliti selanjutnya agar dilakukan lebih lanjut dengan menggunakan variasi waktu pengadukan, variasi rumput laut teraktivasi, dan menggunakan logam berat lainnya
DAFTAR PUSTAKA
Anggadiredja, J.T. 1996. Potensi dan Manfaat Rumput Laut Indonesia Dalam Bidang Farmasi.Prosiding Seminar Nasional Rumput Laut, APBIRI. Jakarta.
Bastaman, S. 1989. Studies on Degradation and Extraction of Chitin and Chitosan From Prawn Shell (Nephrops Norvegicus) [Tesis]. Belfast : Faculty of Engineering, The Quen’s University of Belfast.
Clark,D.V. 1979. Approach to Atomic Absorption Spectroscopy. Sidney-Autralia : Anal. Chem Consultants Pty. Ltd.
Davidson, R.L. 1980. Handbook of Water Soluble Gums and Resins. New York : Mc. Graw.Hill.Inc
Hwang, J.K. dan Shin, H.H. 2001. Rheological Properties of Chitosan Solutions. Korea Australia
Rheology Journal, vol 12:3/4, 175-179.
Khopkhar, S.M. 1990. Konsep Dasar Kimia Analitik. Jakarta : UI Press. Knorr, D. 1984. Use Chitonous in Food. Food Tech. 38(1):85.
Moelyanto, R. 1979. Udang Sebagai Bahan Makanan. Jakarta : LPTP. Departemen Pertanian. Mudjiman, A. 1982. Budidaya Udang Windu. Jakarta : Penerbit Swadaya.
Mulja, M. 1995. Analisa Instrumen. Surabaya : Airlangga Universitity Press. Muzzarelly, R.A.A. 1977. Chitin. New York. Oxford: Perngamon Press.
Rismana, E. 2004. Serat Kitosan Mengikat Lemak.
Robert, G.A.F. 1992. Chitin Chemistry. London: The Macmillan Press.
Vinvogadro. A.P. 1971. Elementary Chemical Composition of Marine Organism. Moscow: A.V.USSR.
Vogel, A.I. 1992. Kimia Analitik Kuantitatif Anorganik. Terjemahan : Pujaatmaka Setiono. Edisi Keempat. Jakarta : EGC Kedokteran.
Walsh, A. 1955. Application of Absorbation Spectra to Chemical Analysis. Spectrochemica. Acta. Vol 7.
Widowati, W. 2008. Efek Toksit Logam Pencegahan dan Penanggulangan Pencemara.
Yogyakarta : Penerbit Andi Offset.