UIN SYARIF HIDAYATULLAH JAKARTA
UJI STABILITAS FISIK GEL MASKER
PEEL OFF
SERBUK GETAH BUAH PEPAYA (
Carica papaya
L.)
DENGAN BASIS POLIVINIL ALKOHOL DAN
HIDROKSIPROPIL METILSELULOSA
SKRIPSI
HAPPY RAHMA YULIN
1111102000055
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
JAKARTA
UIN SYARIF HIDAYATULLAH JAKARTA
UJI STABILITAS FISIK GEL MASKER
PEEL OFF
SERBUK GETAH BUAH PEPAYA (
Carica papaya
L.)
DENGAN BASIS POLIVINIL ALKOHOL DAN
HIDROKSIPROPIL METILSELULOSA
SKRIPSI
Diajukan sebagai salah satu syarat memperoleh gelar Sarjana Farmasi
HAPPY RAHMA YULIN
1111102000055
FAKULTAS KEDOKTERAN DAN ILMU KESEHATAN
PROGRAM STUDI FARMASI
JAKARTA
vi UIN Syarif Hidayatullah Jakarta
ABSTRAK
Nama : Happy Rahma Yulin
NIM : 1111102000055
Program Studi : Farmasi
Judul : Uji Stabilitas Fisik Gel Masker Peel Off Serbuk Getah Buah Pepaya (Carica papaya L.) dengan Basis Polivinil Alkohol dan Hidroksipropil Metilselulosa
Pepaya merupakan tanaman yang kaya akan manfaat. Seluruh bagian tanaman seperti akar, batang, biji, kulit, daun, dan buah pepaya diketahui dapat digunakan sebagai obat. Buah pepaya muda mengandung getah berwarna putih. Getah tersebut diketahui memiliki kandungan enzim papain yang tinggi. Enzim papain telah banyak digunakan dalam produk kosmetik. Enzim papain bekerja dengan mengangkat sel kulit mati, dan menstimulasi pertumbuhan sel kulit baru yang lebih cerah. Pada penelitian ini, dilakukan pengembangan berupa pembuatan sebanyak 3 formula masker peel off dengan kandungan serbuk getah buah pepaya. Masing-masing formula dibedakan berdasarkan variasi konsentrasi Hidroksipropil Metilselulosa (HPMC) sebanyak 2%, 3%, dan 4%. Evaluasi yang dilakukan terhadap stabilitas fisik masker peel off antara lain uji organoleptis, pH, homogenitas, waktu kering, daya sebar, dan viskositas. Uji stabilitas dilakukan pada suhu 27±2oC dan suhu 40±2oC selama 4 minggu, serta pengujian cycling test sebanyak 6 siklus. Hasil penelitian menunjukkan bahwa masing–masing formula sediaan gel masker peel off serbuk getah buah pepaya yang diformulasikan dengan kombinasi PVA dan HPMC sebagai basis dikatakan tidak stabil selama pengujian karena terjadi perubahan pada parameter uji berupa waktu kering dan viskositas.
vii UIN Syarif Hidayatullah Jakarta
ABSTRACT
Name : Happy Rahma Yulin
NIM : 1111102000055
Major : Pharmacy
Title : Physical Stability Test of Peel Off Mask Gel Formulation Containing Papaya Latex Powder (Carica papaya L.) with Polyvinyl Alcohol and Hydroxypropyl Methylcellulose Base
Papaya is a plant that have many benefits. All parts of the plants such as roots, stems, bark, leaves, and fruit of papaya also known to have medicinal properties. Unripe papaya contains a white latex. The latex of unripe papaya is very rich in papain. Papain enzyme has been widely used in cosmetic products. Papain enzyme works by removing dead skin cells and stimulating the new brighter skin
cell’s growth. In this study, three kinds of formulas were developed to preparate a peel off face mask containing papaya latex powder with varying hidroxypropil metylselullose (HPMC) concentrations which were of 2%, 3%, and 4%. To predict the physical stability of the preparation, stability test was done with a few parameters such as organoleptic, pH, homogenity, drying time, dispersive power, and viscosity. In stability test, each formula is placed at temperature 27±2oC and 40±2oC for 4 weeks. Besides that, cycling test was performed with around 6 cycles. The results showed that each formula has remained unstable during the testing period due to changes in the parameters such as drying time and viscosity.
viii UIN Syarif Hidayatullah Jakarta
KATA PENGANTAR
Puji syukur saya panjatkan atas segala nikmat, karunia, dan ilmu yang bermanfaat yang diberikan oleh Allah Subhanahu wa ta’ala, sehingga penulis dapat menyelesaikan penulisan skripsi ini. Penulisan skripsi ini dilakukan dalam rangka memenuhi salah satu syarat untuk mencapai gelar Sarjana Farmasi pada Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri (UIN) Syarif Hidayatullah Jakarta.
Saya menyadari bahwa tanpa bantuan dan bimbingan dari berbagai pihak dari masa perkuliahan sampai pada penyusunan skripsi ini, sangatlah sulit bagi saya untuk menyelesaikan skripsi ini. Oleh karena itu saya mengucapkan terima kasih kepada :
1. Ibu Nelly Suryani, Ph.D., Apt. dan Bapak Hefriyan Handra, M.Kes., M.Sc., Apt. selaku Pembimbing yang telah meluangkan banyak waktu untuk memberikan bimbingan, motivasi, petunjuk, serta dorongan bagi penulis dari awal hingga skripsi ini dapat terselesaikan.
2. Dr. H. Arif Soemantri, S.KM, M.Kes. selaku Dekan Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta. 3. Bapak Yardi, Ph.D., Apt. selaku Kepala Program Studi Farmasi Fakultas
Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta.
4. Bapak dan Ibu staf pengajar Prodi Farmasi Fakultas Kedokteran dan Ilmu Kesehatan UIN Syarif Hidayatullah Jakarta yang telah memberikan berbagai ilmu pengetahuan, bimbingan, motivasi dan informasi kepada penulis.
5. Kedua orang tua, Ayahanda Masruri dan Ibunda Haryani Yuliyani yang tiada hentinya memberikan kasih sayang, doa yang tak pernah putus, dukungan baik moril maupun materil, dan juga motivasi kepada penulis dalam menyelesaikan skripsi ini.
6. Kedua adik tercinta Febrizio Dwiki Rahmandani dan Kaeza Fairus Azmi atas dukungan dan doa yang diberikan hingga penelitian ini dapat berjalan lancar.
7. Aditya Ramadhan, Ati Maryanti, Euis Chodidjah, dan Elsa Elfrida atas waktu, tenaga, fikiran, semangat, dukungan, doa, dan motivasi kepada penulis selama penelitian hingga terselesaikannya skripsi ini.
8. Teman satu bimbingan, Rosita Pracima yang telah menjadi teman diskusi, dan berbagi keluh kesah selama penelitian.
9. Sahabat selama di bangku perkuliahan, Rachma Ayunda dan Fitri Rahmadani yang telah menemani, berbagi suka maupun duka, dan mengisi cerita selama 4 tahun kebersamaan kita.
10.Seluruh sahabat dan teman Program Studi Farmasi angkatan 2011 sebagai teman seperjuangan yang telah memberikan dukungan dan semangat. 11.Kakak-kakak laboran FKIK, Kak Eris, Kak Rachmadi, Kak Lisna, Kak
Tiwi, dan Kak rani atas dukungan dan kerjasamanya selama kegiatan penelitian.
ix UIN Syarif Hidayatullah Jakarta
Semoga amal baik dan bantuannya mendapat ganjaran dari Allah SWT dan skripsi ini bermanfaat bagi penulis dan pembaca umumnya.
Tidak ada manusia yang luput dari kesalahan dan kekhilafan, demikian pula dengan penulisan skripsi ini. Oleh karena itu, penulis mengharapkan saran dan kritik yang dapat membangun dari semua pihak. Semoga dalam penulisan skripsi ini bermanfaat bagi semua pihak khususnya dalam dunia kefarmasian.
Ciputat, Oktober 2015
xi UIN Syarif Hidayatullah Jakarta
DAFTAR ISI
Halaman
HALAMAN SAMPUL ... i
HALAMAN JUDUL ... ii
HALAMAN PERNYATAAN ORISINALITAS ... iii
HALAMAN PERSETUJUAN PEMBIMBING ... iv
HALAMAN PENGESAHAN ... v
ABSTRAK ... vi
ABSTRACT ... vii
KATA PENGANTAR ... viii
HALAMAN PERSETUJUAN PUBLIKASI ILMIAH ... x
DAFTAR ISI ... xi
DAFTAR GAMBAR ... xiii
DAFTAR TABEL ... xiv
DAFTAR LAMPIRAN ... xv
BAB I. PENDAHULUAN ... 1
1.1 Latar Belakang ... 1
1.2 Rumusan Masalah ... 3
1.3 Tujuan Penelitian ... 3
1.4 Hipotesa ... 3
1.5 Manfaat Penelitian ... 3
BAB 2. TINJAUAN PUSTAKA ... 4
2.1 Tanaman Pepaya (Carica papaya L.) ... 4
2.1.1 Taksonomi ... 4
2.1.2 Deskripsi Tanaman ... 4
2.1.3 Kandungan Buah Pepaya dan Kegunaannya ... 5
2.2 Enzim Papain ... 7
2.2.1 Sifat Fisika Kimia Enzim Papain ... 10
2.3 Kulit ... 11
2.3.1 Anatomi Kulit ... 12
2.3.2 Fungsi Kulit ... 12
2.4 Kosmetika ... 14
2.5 Masker Peel Off... 15
2.5.1 Formulasi Masker Peel Off ... 15
BAB 3. METODE PENELITIAN ... 19
3.1 Waktu dan Tempat Penelitian ... 19
3.2 Alat dan Bahan ... 19
3.2.1 Alat ... 19
3.2.2 Bahan... 19
3.3. Prosedur Kerja ... 19
3.3.1 Formulasi Masker Peel Off Serbuk Getah Pepaya ... 19
3.3.2 Pembuatan Masker Peel Off Serbuk Getah Pepaya ... 20
3.4 Evaluasi ... 21
3.4.1 Uji Stabilitas ... 21
3.4.2 Parameter Uji Stabilitas ... 29
BAB 4. HASIL DAN PEMBAHASAN ... 23
xii UIN Syarif Hidayatullah Jakarta
4.1.1 Hasil Evaluasi Awal Sediaan ... 23
4.1.2 Hasil Organoleptis Sediaan ... 25
4.1.3 Hasil Uji pH Sediaan ... 27
4.1.4 Hasil Uji Waktu Kering ... 28
4.1.5 Hasil Uji Viskositas ... 31
4.1.6 Hasil Uji Daya Sebar ... 33
4.1.7 Hasil Uji Cycling Test ... 38
BAB 5. KESIMPULAN DAN SARAN ... 44
5.1 Kesimpulan ... 44
5.2 Saran ... 44
xiii UIN Syarif Hidayatullah Jakarta
DAFTAR GAMBAR
Halaman
Gambar 2.1 Tanaman Pepaya ... 5
Gambar 2.2 Getah Penghasil Enzim Papain ... 7
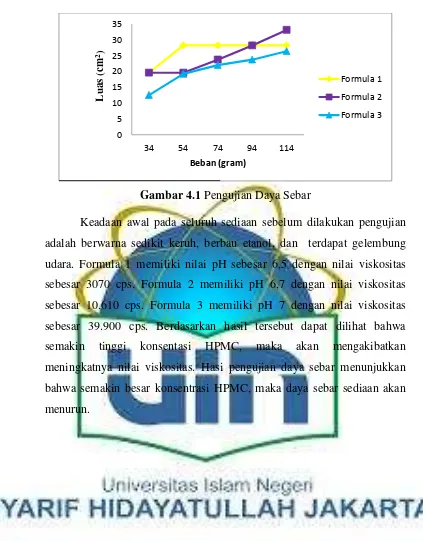
Gambar 4.1 Pengujian Daya Sebar ... 24
Gambar 4.2 Uji pH Sediaan pada Suhu Ruang (27±2oC)... 27
Gambar 4.3 Uji pH Sediaan pada Suhu Tinggi (40±2oC)... 27
Gambar 4.4 Uji Waktu Kering pada Suhu Ruang (27±2oC)... 28
Gambar 4.5 Uji Waktu Kering pada Suhu Tinggi (40±2oC)... 29
Gambar 4.6 Uji Viskositas pada Suhu Ruang (27±2oC)... 31
Gambar 4.7 Uji Viskositas pada Suhu Tinggi (40±2oC)... 31
Gambar 4.8 Uji Daya Sebar pada Suhu Ruang (27±2o) Minggu ke 1... 33
Gambar 4.9 Uji Daya Sebar pada Suhu Ruang (27±2o) Minggu ke 2... 34
Gambar 4.10 Uji Daya Sebar pada Suhu Ruang (27±2o) Minggu ke 3... 34
Gambar 4.11 Uji Daya Sebar pada Suhu Ruang (27±2o) Minggu ke 4... 34
Gambar 4.12 Uji Daya Sebar pada Suhu Tinggi (40±2o) Minggu ke 1... 35
Gambar 4.13 Uji Daya Sebar pada Suhu Tinggi (40±2o) Minggu ke 2... 35
Gambar 4.14 Uji Daya Sebar pada Suhu Tinggi (40±2o) Minggu ke 3... 35
Gambar 4.15 Uji Daya Sebar pada Suhu Tinggi (40±2o) Minggu ke 4... 36
Gambar 4.16 Uji pH pada Cycling Test... 39
Gambar 4.17 Uji Viskositas selama Cycling Test... 40
Gambar 4.18 Uji Daya Sebar Siklus ke 1... 41
Gambar 4.19 Uji Daya Sebar Siklus ke 2... 41
Gambar 4.20 Uji Daya Sebar Siklus ke 3... 42
Gambar 4.21 Uji Daya Sebar Siklus ke 4... 42
Gambar 4.22 Uji Daya Sebar Siklus ke 5... 42
xiv UIN Syarif Hidayatullah Jakarta
DAFTAR TABEL
[image:14.595.84.539.148.614.2]Halaman
Tabel 2.1 Kandungan Buah Pepaya ... 5
Tabel 2.2 Komposisi Asam Amino Penyusun Papain... 8
Tabel 2.3 Sifat Fisik Enzim Papain... 11
Tabel 3.1 Formulasi Sediaan Gel Masker Peel Off... 20
Tabel 4.1 Karakteristik Awal Sediaan ... 23
Tabel 4.2 Hasil Uji Organoleptis Sediaan pada Suhu Ruang (27±2oC)... 25
Tabel 4.3 Hasil Uji Organoleptis Sediaan pada Suhu Tinggi (40±2oC)... 26
Tabel 4.4 Hasil Uji Organoleptis Sediaan pada Cycling Test... 26
xv UIN Syarif Hidayatullah Jakarta
DAFTAR LAMPIRAN
Halaman
Lampiran 1 Bagan Alur Penelitian ... 51
Lampiran 2 Pembuatan Masker Peel Off... 52
Lampiran 3 Data Awal Diameter dan Luas Masker Peel Off... 53
Lampiran 4 Data Hasil Uji pH... 54
Lampiran 5 Data Hasil Uji Waktu Kering... 55
Lampiran 6 Data Hasil Uji Viskositas... 56
Lampiran 7 Data Diameter Masker Peel Off Suhu Ruang (27±2o)... 57
Lampiran 8 Data Luas Masker Peel Off Suhu Ruang (27±2oC)... 58
Lampiran 9 Data Diameter Masker Peel Off Suhu Tinggi (40±2oC)... 59
Lampiran 10 Data Luas Masker Peel Off Suhu Tinggi (40±2oC)... 60
Lampiran 11 Data Diameter selama Cycling Test... 61
Lampiran 12 Data Luas Sebar Sediaan selama Cycling Test... 62
Lampiran 13 Gambar Hasil Penelitian... 63
Lampiran 14 Sertifikat Analisa Serbuk Getah Pepaya... 70
UIN Syarif Hidayatullah Jakarta
BAB 1 PENDAHULUAN
1.1 Latar Belakang
Penggunaan tumbuhan sebagai obat telah lama dikenal secara luas oleh masyarakat Indonesia yang disebut sebagai obat tradisional. Pengobatan dengan menggunakan obat tradisional dewasa ini sangat popular dan semakin disukai oleh masyarakat, hal ini disebabkan karena disamping harganya murah, mudah didapat, juga mempunyai efek samping yang relatif sedikit (Wijaya, 1995 ; Andi, 2000).
Salah satu tanaman obat yang memiliki banyak khasiat yaitu pepaya (Carica papaya L.) (Aravind et al., 2013). Buah pepaya tergolong buah yang popular dan digemari oleh masyarakat. Batang, daun, dan buah pepaya muda mengandung getah berwarna putih. Getah ini mengandung suatu enzim pemecah protein atau enzim proteolitik yang disebut papain (Kalie, 1999 dalam Silaban, 2012).
Enzim papain dilaporkan dapat melembutkan kulit, dan menghilangkan noda pada wajah sehingga dapat digunakan untuk mengobati kerutan pada wajah, bintik matahari, bintik-bintik penuaan, serta masalah jerawat (Reddy et al., 2011). Enzim papain bekerja dengan cara mendegradasi sel kulit mati pada permukaan kulit terluar (kutikula), kemudian secara perlahan akan menstimulasi pertumbuhan jaringan kulit baru. Efek yang ditimbulkan yaitu akan meningkatkan kesehatan, higienitas, dan kecerahan kulit (Hara et al., 2014). Enzim papain lebih tahan terhadap suatu proses, memiliki kisaran pH optimum 5–7,5 dan stabil pada suhu 60–70oC (Fox et al., 1982 dalam Iswanto et al., 2006). Konsentrasi enzim papain yang direkomendasikan dalam penggunaan pada produk kosmetik adalah 0,5–5% (Anonim, 2009).
UIN Syarif Hidayatullah Jakarta
Kualitas fisik sediaan masker peel off dipengaruhi oleh komposisi bahan–bahan yang digunakan, terutama komposisi polivinil alkohol (PVA) serta polimer lain yang digunakan (Beringhs et al., 2013). Polimer yang paling umum digunakan sebagai basis adalah PVA, namun PVA memiliki kelemahan yaitu lapisan film yang dihasilkan cenderung kaku dan memiliki fleksibilitas yang tergolong rendah (Barnard, 2011). Penambahan polimer lain seperti hidroksipropil metilselulosa (HPMC) dapat digunakan untuk meningkatkan kualitas sediaan gel masker peel off. HPMC merupakan polimer yang dapat membentuk lapisan film transparan, kuat, dan fleksibel (Barnard, 2011). Konsentrasi PVA yang dapat digunakan sebagai pembentuk lapisan film yaitu sebesar 5–10% (Harry, 1973), sedangkan konsentrasi HPMC yang digunakan adalah 2–4% (Wade and Waller, 1994 dalam Sukmawati et al., 2013).
Berdasarkan penelitian yang dilakukan oleh Mutiara et al. (2015) tentang formulasi masker wajah peel off ekstrak kulit batang kayu manis dengan perbandingan konsentrasi PVA dan HPMC sebesar 12:1 menunjukkan hasil bahwa sediaan memiliki kestabilan fisik yang baik selama pengujian cycling test. Penelitian yang dilakukan oleh Syarifah et al. (2015) menunjukkan hasil sediaan masker peel off ekstrak daun pepaya dengan perbandingan PVA dan HPMC sebesar 12:1 memiliki kestabilan yang baik pada pengujian stabilitas dalam oven dengan suhu 40oC selama 28 hari. Penelitian yang dilakukan oleh Izzati (2014) pada formula masker
peel off ekstrak kulit buah manggis dengan perbandingan PVA dan HPMC 10:1, 10:2, dan 10:3 menunjukkan hasil bahwa masing–masing formula menunjukkan hasil stabilitas yang baik selama pengujian cycling test.
UIN Syarif Hidayatullah Jakarta
1.2 Rumusan Masalah
Bagaimanakah stabilitas fisik sediaan gel masker peel off serbuk getah buah pepaya yang diformulasikan dengan kombinasi PVA dan HPMC sebagai basis gel?
1.3 Tujuan Penelitian
Mengetahui stabilitas sediaan gel masker peel off serbuk getah buah pepaya dengan kombinasi PVA dan HPMC pada suhu 27±2oC dan suhu 40±2oC selama 28 hari serta pengujian cycling test sebanyak 6 siklus.
1.4 Hipotesa
Kombinasi PVA dengan HPMC sebagai agen pembentuk basis gel tidak berpengaruh terhadap stabilitas fisik sediaan gel masker peel off
serbuk getah buah pepaya.
1.5 Manfaat Penelitian
1.5.1 Memberikan informasi mengenai pemanfaatan serbuk getah buah pepaya dalam bentuk sediaan gel masker peel off.
1.5.2 Memberikan informasi mengenai stabilitas sediaan gel masker peel off
UIN Syarif Hidayatullah Jakarta
BAB 2
TINJAUAN PUSTAKA
2.1 Tanaman Pepaya (Carica papaya L.)
2.1.1 Taksonomi
Klasifikasi tanaman pepaya (Carica papaya L.) adalah sebagai berikut : Divisi : Spermatophyta
Kelas : Angiospermae Subkelas : Dicotyledonae Ordo : Caricales Famili : Caricaceae Genus : Carica
Spesies : Carica papaya L. ( Hutapea, 1991 dalam Ismaya, 2013)
2.1.2 Deskripsi Tanaman
Tanaman pepaya adalah jenis pohon buah-buahan yang berumur pendek dan sifat tumbuhnya cepat sekali. Tanaman ini diperbanyak dengan biji dan mulai tumbuh setelah 6 – 8 minggu (Ariesty, 2010).
UIN Syarif Hidayatullah Jakarta
Gambar 2.1 Tanaman Pepaya [Silaban, 2012]
2.1.3 Kandungan Buah Pepaya dan Kegunaannya
Daging buah pepaya umumnya berwarna kuning dan merah. Perbedaan warna ini disebabkan karena adanya pigmen karoten dan likopen. Karoten adalah suatu kelompok pigmen warna kuning, jingga atau merah jingga yang mudah larut dalam lemak atau pelarut organik, tetapi tidak larut dalam air. Karoten berwarna kuning merupakan provitamin A. Jumlah karoten dalam 100 g daging buah pepaya matang berkisar antara 3,7–4,2 mg (Winarno & Aman, 1981).
Secara lengkap kandungan buah pepaya dengan nilai energi 200 kJ untuk 100 gram buah pepaya dapat ditunjukkan pada tabel berikut :
Tabel 2.1 Kandungan Buah Pepaya
No Komposisi Gizi Pepaya
Matang Pepaya Muda Daun Pepaya 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11.
Kadar air (gram) Energi (Kal) Hidrat arang (gram) Kalsium (miligram) Lemak (gram) Fosfor (miligram) Protein (gram) Vitamin A (SI)
Vitamin B1 (miligram) Vitamin C (miligram) Zat Besi (miligram)
86,7 46 12,2 23 - 12 0,5 365 0,04 78 1,7 92,4 26 4,9 50 0,10 16 2,1 50 0,02 19 0,4 75,4 79 11,9 353 2 63 8,0 18.250 0,15 140 0,8
UIN Syarif Hidayatullah Jakarta
Melihat dari berbagai macam manfaat dan kelebihan buah pepaya, juga terdapat kelebihan lain yang dimiliki buah pepaya, yakni terdapatnya kandungan enzim papain yang ada pada getah pepaya. Getah pepaya yang sering disebut sebagai papain dapat digunakan untuk berbagai macam keperluan, antara lain : penjernih bir, pengempuk daging, bahan bakuindustri penyamak kulit, serta digunakan dalam industri farmasi dan kosmetika (kecantikan). Papain merupakan enzim proteolitik, yaitu enzim yang dapat mengurai dan memecah protein (Warisno, 2003).
Getah pepaya cukup banyak mengandung enzim yang bersifat proteolitik (pengurai protein). Tepung getah pepaya kering banyak digunakan oleh para pengusaha industri maupun ibu-ibu rumah tangga untuk mengolah berbagai macam produk (Warisno, 2003). Enzim proteolitik dianggap penting dalam metabolisme protein dan banyak digunakan dalam industri pangan, misalnya untuk mengempukkan daging. Ada banyak jenis enzim proteolitik yang dikenal seperti enzim papain, bromelin, rennin, protease dan fisin yang mempunyai sifat menghidrolisa protein (Smith, 1993).
UIN Syarif Hidayatullah Jakarta
2.2 Enzim Papain
Enzim papain merupakan salah satu enzim protease atau pemecah protein yang terdapat dalam getah buah pepaya (Carica papaya L.). Enzim papain dapat diperoleh dari getah tanaman pepaya dan buah pepaya muda. Getah pepaya mengandung sebanyak 10% papain, 45% kimopapain dan lisozim sebesar 20% (Winarno, 1986 dalam Silaban et al., 2012). Getah pepaya tersebut terdapat hampir di semua bagian tanaman pepaya, kecuali bagian akar dan biji. Kandungan papain paling banyak terdapat dalam buah pepaya yang masih muda (Warisno, 2003 dalam Silaban et al., 2012).
Gambar 2.2 Getah Penghasil Enzim Papain [Aravind et al., 2013]
Berdasarkan sifat-sifat kimianya, papain digolongkan sebagai protease sulfhidril (Muchtadi et al., 1992 dalam Silaban et al., 2012). Papain mengandung 212 asam amino dalam suatu rantai polipeptida dan berikatan silang dengan tiga jembatan disulfida (Kalk, 1975 dalam Silaban
et al., 2012). Papain memiliki 6 gugus sulfhidril, tetapi hanya dua gugus sulfhidril yang aktif. Gugus sulfhidril ini mengandung unsur sulfur sekitar 1,2 %. Dimana rantai ikatan tersebut tersusun atas arginin, lisin, leusin, dan glisin dengan sistein-25 tempat gugus aktif thiol (-SH) esensial, yang membentuk sebuah rantai peptida tunggal dengan bobot molekul 21.000-23.000 g/mol (Harrison et al., 1997 dalam Silaban et al., 2012).
UIN Syarif Hidayatullah Jakarta
ini mudah larut dalam air, gliserin dan dalam larutan-larutan hidroalkoholik yang berkonsentrasi rendah, tetapi tidak larut dalam pelarut organik dan lemak yang menguap (Sastrodiwiryo, 1971 dalam Ismaya, 2013). Enzim papain relatif tahan terhadap panas dibandingkan enzim proteolitik lainnya, seperti fisin dan bromelin. Papain mempunyai kemampuan menghidrolisis dengan suhu optimum 500-600C, sedangkan pH optimumnya adalah 5,0-7,0 (Winarno, 1997 dalam Ismaya, 2013). Menurut De man (1997) enzim papain juga tidak mengandung karbohidrat seperti pada bromielin dan ficin sehingga mempunyai energi aktivasi yang lebih rendah karena lebih murni dibanding enzim lain (Iswanto et al., 2006).
[image:23.595.90.534.244.656.2]Komposisi asam amino penyusun papain dapat dilihat pada tabel berikut :
Tabel 2.2 Komposisi Asam Amino Penyusun Papain
Asam Amino Jumlah % Relatif
Lisin Histidin Arginin Aspartat Aspargin Glutamat Glutamin Treonin Serin Prolin Glisin Alanin Valin Isoleusin Leusin Tirosin Fenilalanin Triptofan Sistein Sistin 10 2 12 6 13 8 12 8 13 10 28 14 18 11 12 11 4 5 1 6 4,88 0,97 5,86 2,98 6,24 3,88 5,86 3,88 6,34 3,88 13,58 6,58 8,94 5,86 5,36 5,86 1,93 2,44 0,48 2,93
UIN Syarif Hidayatullah Jakarta
Enzim papain stabil pada larutan yang mempunyai pH 5,0. Untuk pH optimal substrat albumin maupun kasein adalah 7,0 dan untuk substrat gelatin adalah 5,0. Enzim papain mempunyai titik isoelektrik pada 8,75. Enzim papain mempunyai daya tahan panas yang lebih tinggi daripada enzim lain. Keaktifan enzim papain hanya menurun 20% pada pemanasan 700C selama 30 menit pada pH 7,0. Disamping keaktifan memecah protein, enzim papain mempunyai kemampuan untuk membentuk protein baru atau senyawa yang menyerupai protein yang disebut plastein (Winarno, 1983 dalam Ismaya, 2013).
Aktivitas enzim papain dapat meningkat dengan adanya penambahan senyawa-senyawa pereduksi seperti sistein, garam sulfit, atau pengkelat seperti EDTA. Aktivitas katalitik enzim papain menurun apabila enzim ini direaksikan dengan senyawa pengganggu gugus tiol yaitu oksidator, senyawa disulfida, ion logam berat dan senyawa pengalkil. Enzim papain stabil terhadap senyawa pendenaturasi (Ismaya, 2013).
Ada beberapa keuntungan dalam penggunaan enzim papain ini, yakni tidak bersifat toksik, tidak ada reaksi samping, tidak ada perubahan tekanan, suhu, dan pH yang derastis, dan pada konsentrasi rendah sudah mampu berfungsi dengan baik. Pada pH, suhu, dan kemurnian enzim papain, daya pemecah protein yang dimiliki papain dapat diintensifkan lebih jauh menjadi kegiatan hidrolisis protein (Ismaya, 2013).
Sebagai enzim proteolitik, papain memiliki nilai ekonomi tinggi dan banyak digunakan dalam industri besar. Meskipun telah diketahui ada beberapa enzim protease yang dihasilkan dari tanaman lain, ternyata papain merupakan enzim yang paling banyak dan sering digunakan. Oleh karenanya, potensi pasar papain dalam perdagangan dunia masih cukup besar (Kalie, 1999 dalam Ismaya, 2013).
UIN Syarif Hidayatullah Jakarta
muka dan sebagai zat antioksidan karena enzim papain dapat melarutkan sel-sel kulit mati yang melekat pada kulit. Noda dan fleks di wajah bisa dikikis oleh enzim papain hingga menjadi mulus dan bersih. Enzim papain juga bisa digunakan sebagai bahan pembuat pasta gigi, sebab bisa membersihkan sisa makanan apa saja yang melekat di gigi (Ismaya, 2013). Manfaat lainnya dari enzim papain adalah sebagai bahan perenyah pada pembuatan kue kering seperti cracker, bahan penggumpal susu pada pembuatan keju, bahan pelarut gelatin, dan bahan pencuci lensa. Pada proses pembuatan bir, enzim papain dapat digunakan sebagai stabilisator untuk menjaga larutan bir tetap jernih dan tidak keruh (Ismaya, 2013).
Enzim papain juga dapat digunakan dalam industri pengolahan daging. Daging dari hewan yang telah berusia tua dan bertekstur keras pun dapat menjadi lunak jika menggunakan papain, sehingga banyak diperdagangkan dalam kemasan kecil sesuai kebutuhan rumah tangga (Kalie, 1999 dalam Silaban et al., 2012).
2.2.1 Sifat Fisika Kimia Enzim Papain
The International Union of Biochemistry mengklasifikasikan enzim papain termasuk dalam kelompok enzim hidrolase yaitu kelompok enzim yang membantu terjadinya hidrolisis suatu senyawa dengan bantuan molekul air. Senyawa yang terhidrolisis dengan enzim papain adalah golongan senyawa peptida termasuk golongan proteinase atau protease (Budiman, 2003 dalam Silaban et al., 2012).
UIN Syarif Hidayatullah Jakarta
Tabel 2.3. Sifat Fisik Enzim Papain
Karakter Fisik Keterangan
Penampakan Warna
Bau Kelarutan Kelembaban Ukuran partikel
Amorf atau granular Putih hingga kecokelatan
Sedikit berbau Larut dalam air Kurang dari 8 %
99% melewati saringan 250 micron 98% melewati saringan 180 micron
[Sumber : Ismaya, 2013]
2.3 Kulit
Kulit merupakan selimut yang menutupi permukaan tubuh dan memiliki fungsi utama sebagai pelindung dari berbagai macam gangguan dan rangsangan dari luar (Tranggono, 2007).
Kulit adalah bagian terluas dari tubuh, terhitung lebih dari 10% dari massa tubuh dan bagian yang paling utama berinteraksi dengan lingkungan (Walters, 2002). Kulit tersusun dari jaringan yang tumbuh, berdiferensiasi, dan beregenerasi (Gregoriadis et al., 1993).
UIN Syarif Hidayatullah Jakarta
2.3.1 Anatomi Kulit
Kulit terbagi menjadi tiga lapisan utama, yaitu : epidermis, dermis, dan subkutan (subkutis) (Seeley et al., 2003). Epidermis merupakan lapisan luar kulit, membentuk perisai fisik dan antimikroba untuk melindungi tubuh dari ancaman lingkungan. Epidermis mengandung keratinosit yang berfungsi sebagai tempat sintesis keratin. Lapisan kulit yang ke dua adalah dermis yang berisi jaringan pembuluh darah, ujung saraf, kelenjar keringat, kelenjar sebasea, folikel rambut, dan otot rambut. Dermis pada dasarnya terdiri dari protein struktural urat saraf yang dikenal sebagai kolagen. Dermis yang paling tebal berada pada bagian punggung, yaitu sekitar 30-40 kali tebal epidermis (James et al., 2006 dalam Izzati, 2014).
Lapisan ke tiga dari kulit adalah lapisan subkutis. Lapisan subkutis merupakan lapisan jaringan ikat longgar dan lemak di bawah dermis. Subkutis terdiri dari kumpulan sel-sel lemak dan di antara kumpulan tersebut terdapat serabut-serabut jaringan dermis. Lapisan lemak ini disebut penikulus adiposus. Tebal jaringan lemak tidak sama, bergantung pada lokasinya. Tebal jaringan lemak pada abdomen adalah 3 cm, sedangkan di daerah kelopak mata dan penis sangat tipis (Wasitaatmadja, 1997 dalam Izzati, 2014).
2.3.2 Fungsi Kulit
Kulit sebagai organ tubuh yang paling utama mempunyai beberapa fungsi, diantaranya sebagai berikut :
1. Fungsi Proteksi
Kulit berperan dalam melindungi organ tubuh dari benturan serta mencegah trauma mekanik langsung ke dalam tubuh..
2. Fungsi Termoregulasi
UIN Syarif Hidayatullah Jakarta
simpatis yang mengeluarkan zat perantara asetilkolin (Langley dan Lenny, 1958).
3. Fungsi Persepsi Sensoris
Kulit bertanggung jawab sebagai indra terhadap rangsangan.Rangsangan dari luar akan diterima oleh reseptor-reseptor tersebut dan diteruskan ke sistem saraf pusat, selanjutnya diinterpretasikan oleh korteks serebri (Langley dan Lenny, 1958). 4. Fungsi Absorbsi
Kulit yang sehat tidak mudah menyerap air, larutan, maupun benda padat. Tetapi cairan yang mudah menguap lebih mungkin diserap kulit, begitu pula zat yang larut dalam minyak. Kemampuan absorbsi kulit dipengaruhi oleh tebal tipisnya kulit, hidrasi, kelembaban udara, metabolisme, dan jenis pembawa zat yang menempel di kulit. Penyerapan dapat melalui celah antar sel, saluran kelenjar atau saluran keluar rambut (Langley dan Lenny, 1958).
5. Fungsi Pembentukan Pigmen (Melanogenesis)
Sel pembentuk pigmen kulit (melanosit) terletak di lapisan basal epidermis. Jumlah melanosit serta besarnya melanin yang terbentuk akan menentukan warna kulit (Langley dan Lenny, 1958).
6. Fungsi Keratinisasi
Proses keratinisasi berlangsung terus-menerus dan berguna untuk fungsi rehabilitasi kulit agar dapat melaksanakan fungsinya secara baik (Langley dan Lenny, 1958).
7. Fungsi Produksi Vitamin D
Kulit juga dapat membuat vitamin D dari bahan baku 7-dihidroksikolesterol dengan bantuan sinar matahari, namun produksi ini masih lebih rendah dari kebutuhan tubuh akan vitamin D dari luar makanan (Langley dan Lenny, 1958).
8. Fungsi Lain
UIN Syarif Hidayatullah Jakarta
2.4 Kosmetika
Kosmetika telah dikenal manusia sejak berabad-abad yang lalu, dan baru pada abad ke-19 mendapat perhatian khusus, yaitu selain untuk kecantikan juga mempunyai fungsi untuk kesehatan. Perkembangan ilmu kosmetik serta industrinya baru dimulai secara besar-besaran pada abad ke-20 dan kosmetik menjadi salah satu bagian dari dunia usaha. Dewasa ini, teknologi kosmetik begitu maju dan merupakan paduan antara kosmetik dan obat (pharmaceutical) atau dikenal dengan istilah kosmetik medik (cosmeceuticals) (Tranggono dan Latifah, 2007) .
Pengertian kosmetik dalam Peraturan Menkes RI No. 445 Tahun 1998 menyebutkan bahwa Kosmetika adalah bahan atau campuran bahan untuk digosokkan, dilekatkan, dituangkan, dipercikkan, atau disemprotkan pada tubuh, dimasukkan, dipergunakan pada badan atau bagian badan manusia dengan maksud untuk membersihkan, memelihara, menambah daya tarik atau mengubah rupa, melindungi supaya tetap dalam keadaan baik, memperbaiki bau badan, tetapi tidak dimaksudkan untuk mengobati atau menyembuhkan penyakit (Tranggono dan Latifah,2007).
Penggolongan menurut Peraturan Menteri Kesehatan RI berdasarkan kegunaan dan lokalisasi pemakaian pada tubuh, kosmetika dibagi menjadi 13 golongan, yaitu :
a. Preparat untuk bayi b. Preparat untuk mandi. c. Preparat untuk mata. d. Preparat wangi-wangian. e. Preparat untuk rambut.
f. Preparat make up (kecuali mata) g. Preparat untuk kebersihan mulut. h. Preparat untuk kebersihan badan. i. Preparat kuku.
j. Preparat perawatan kulit. k. Preparat cukur.
UIN Syarif Hidayatullah Jakarta
2.5 Masker Peel Off
Kosmetika wajah yang umumnya digunakan tersedia dalam berbagai bentuk sediaan, salah satunya dalam bentuk masker wajah peel off. Masker peel off merupakan salah satu jenis sediaan masker yang praktis dan mudah saat penggunaannya. Masker peel off terbuat dari bahan karet, seperti polivinil alkohol atau damar vinil asetat (Evrilia et al., 2014). Masker peel off biasanya digunakan dalam bentuk gel atau pasta, yang dioleskan ke kulit muka. Setelah alkohol yang terkadung dalam masker menguap, terbentuklah lapisan film yang tipis dan transparan pada kulit muka. Setelah berkontak selama 15 – 30 menit, lapisan tersebut diangkat dari permukaan kulit dengan cara dikelupas (Slavtcheff, 2000 dalam Izzati, 2014). Masker peel off memliki beberapa manfaat diantaranya mampu merileksasi otot-otot wajah, membersihkan, menyegarkan, melembabkan, dan melembutkan kulit wajah (Vieira, 2009). Maker berbentuk gel mempunyai beberapa keuntungan diantaranya penggunaan yang mudah, serta mudah untuk dibilas dan dibersihkan. Selain itu, dapat juga diangkat atau dilepaskan seperti membran elastik (Harry, 1973).
2.5.1 Formulasi Masker Peel off a. Polivinil Alkohol (PVA)
Polivinil alkohol adalah polimer sintetis yang larut dalam air dengan rumus (C2H4O)n. Nilai n untuk bahan yang tersedia secara
komersial terletak di antara 500 dan 5000, setara dengan rentang berat molekul sekitar 20.000 – 200.000. Polivinil alkohol berupa bubuk granular berwarna putih hingga krem, dan tidak berbau (Rowe et al., 2009).
UIN Syarif Hidayatullah Jakarta
serta digunakan dalam kosmetik pada konsentrasi hingga 7% (Rowe et al., 2009).
Polivinil alkohol diproduksi dengan cara polimerasi vinil asetat menjadi polivinil asetat, dan diikuti dengan hidrolisis polivinil asetat membentuk polivinil alkohol (Nagar et al., 2011).
Polivinil alkohol dikenal sebagai agen pembentuk lapisan film, pendispersi, lubrikan, pelindung kulit, digunakan pada formulasi gel dan lotion, shampo, tabir surya, masker, serta beberapa aplikasi kosmetik dan perawatan kulit lainnya. Namun salah satu kelemahan dari polivinil alkohol adalah lapisan film yang dihasilkan cenderung lebih kaku dan memiliki fleksibilitas yang tergolong rendah (Barnard, 2011).
b. Hidroksipropil Metilselulosa
Hidroksipropil Metilselulosa (HPMC) atau hipermelosa secara luas digunakan sebagai bahan tambahan dalam formulasi sediaan farmasi oral, mata, hidung, dan topikal. Selain itu, HPMC juga digunakan secara luas dalam kosmetik dan produk makanan. Kegunaan HPMC diantaranya sebagai zat peningkat viskositas, zat pendsipersi, zat pengemulsi, penstabil emulsi, zat penstabil, zat pensuspensi, sustained release agent, pengikat pada sediaan tablet, dan zat pengental (Rowe et al., 2009).
HPMC berbentuk serbuk granul atau serat berwarna putih atau putih-krem. HPMC larut dalam air dingin, membentuk larutan koloid kental, praktis tidak larut dalam air panas, kloroform, etanol (95%), dan eter, tetapi larut dalam campuran etanol dan diklorometana, dan campuran air dan alkohol (Rowe et al., 2009).
UIN Syarif Hidayatullah Jakarta
c. Propilen Glikol
Propilen glikol (C3H8O2) merupakan cairan bening, tidak
berwarna, kental, praktis tidak berbau, manis, dan memiliki rasa yang sedikit tajam menyerupai gliserin. Propilen glikol larut dalam 6 bagian eter, tidak larut dengan minyak mineral ringan atau fixed oil, tetapi akan melarutkan beberapa minyak esensial (Rowe et al., 2009).
Propilen glikol telah banyak digunakan sebagai pelarut, ekstraktan, dan pengawet dalam berbagai formulasi farmasi parenteral dan nonparenteral. Pelarut ini umumnya lebih baik dari gliserin dan melarutkan berbagai macam bahan, seperti kortikosteroid, fenol, obat sulfa, barbiturat, vitamin (A dan D), alkaloid, dan banyak anestesi lokal. Propilen glikol biasa digunakan sebagai pengawet antimikroba, desinfektan, humektan, plasticizer, pelarut, dan zat penstabil. Konsentrasi propilen glikol yang biasa digunakan sebagai humektan adalah 15% (Rowe et al., 2009).
d. Metil Paraben
Metil paraben banyak digunakan sebagai pengawet antimikroba dalam kosmetik, produk makanan, dan formulasi sediaan farmasi. Metil paraben dapat digunakan sendiri atau dikombinasikan dengan paraben lain atau dengan zat antimikroba lainnya. Dalam kosmetik, metilparaben merupakan pengawet yang paling sering digunakan (Rowe et al., 2009).
Metilparaben (C8H8O3) berbentuk kristal tak berwarna atau bubuk
UIN Syarif Hidayatullah Jakarta
e. Propil Paraben
Propil paraben (C10H12O3) berbentuk bubuk putih, kristal, tidak
berbau, dan tidak berasa. Propil paraben banyak digunakan sebagai pengawet antimikroba dalam kosmetik, produk makanan, dan formulasi sediaan farmasi. Propil paraben menunjukkan aktivitas antimikroba antara pH 4–8. Efikasi pengawet menurun dengan meningkatnya pH karena pembentukan anion fenolat. Paraben lebih aktif terhadap ragi dan jamur daripada terhadap bakteri. Mereka juga lebih aktif terhadap positif dibandingkan terhadap bakteri gram-negatif (Rowe et al., 2009).
f. Etanol 96%
Etanol memiliki sinonim alkohol, etil alkohol; etil hydroxide; grainalkohol; methyl carbinol. Etanol jernih, tidak berwarna, sedikit mudah menguap, memiliki bau yang khas dan rasa terbakar. Etanol memiliki rumus molekul C2H6O dan bobot molekul 46,07.
Penggunaannya sebagai pelarut dalam sediaan topikal sebanyak
60-90% sedangkan sebagai pengawet penggunaannya ≥ 10%. Etanol 96%
UIN Syarif Hidayatullah Jakarta
BAB 3
METODE PENELITIAN
3.1 Waktu dan Tempat Penelitian
Penelitian dilaksanakan di Laboratorium Penelitian 2 dan Laboratorium Teknologi Sediaan Padat Program Studi Farmasi, Fakultas Kedokteran dan Ilmu Kesehatan Universitas Islam Negeri Syarif Hidayatullah Jakarta. Waktu penelitian dimulai pada bulan Februari 2015 hingga Juli 2015.
3.2 Alat dan Bahan
3.2.1 Alat
Alat yang digunakan dalam penelitian ini antara lain : hot plate
(Cimarec Thermo Scientific, Amerika Serikat), alat gelas (Schoot Duran, Jerman), thermometer, spatula, lumpang dan alu, pipet, timbangan analitik (KERN KB, Jerman), stopwatch, viskotester 6R (Haake, Spanyol), pH meter (Horiba F-52, Jepang), refrigerator (SANYO Medicool, Jepang), dan oven (France Etuves C3000, Perancis).
3.2.2 Bahan
Bahan yang digunakan adalah serbuk getah buah pepaya (Carica papaya L.) (MM Natures, Indonesia), Polivinil Alkohol, Hidroksipropil Metilselulosa (ASHLAND, Amerika Serikat), propilen glikol, metil paraben, propil paraben, etanol 96%, dan aquadest.
3.3 Prosedur Kerja
UIN Syarif Hidayatullah Jakarta
Tabel 3.1 Formulasi Sediaan Gel Masker Peel off Serbuk Getah Pepaya
Bahan Konsentrasi (%) Fungsi
F1 F2 F3
Serbuk getah pepaya PVA HPMC Propilen Glikol Metil Paraben Propil Paraben Etanol 96% Aquadest 3 8 2 15 0,2 0,1 15 Ad 100 3 8 3 15 0,2 0,1 15 Ad 100 3 8 4 15 0,2 0,1 15 Ad 100 Zat Aktif Basis gel Basis gel Humektan Pengawet Pengawet Pelarut Pelarut
3.3.2 Pembuatan Masker Peel off Serbuk Getah Pepaya
1. Pembuatan sediaan masker wajah peel off diawali dengan menghaluskan PVA, kemudian dikembangkan menggunakan aquadest suhu 90oC di dalam lumpang panas, diaduk hingga mengembang sempurna dan terbentuk basis gel PVA yang homogen (wadah A) 2. Kemudian di dalam tempat terpisah, HPMC dikembangkan
menggunakan aquadest suhu 90oC di dalam lumpang panas yang hingga mengembang dan terbentuk massa yang homogen (wadah B). 3. Setelah PVA dan HPMC mengembang sempurna, HPMC
dicampurkan dengan pengadukan yang konstan ke dalam wadah A yang berisi PVA hingga keduanya bercampur dengan sempurna. 4. Propilen glikol dimasukkan ke dalam wadah A lalu diaduk hingga
tercampur sempurna.
5. Pada wadah lainnya, serbuk getah pepaya dilarutkan terlebih dahulu dalam sebagian aquadest, kemudian dicampurkan ke dalam wadah A hingga tercampur sempurna
6. Pada wadah terpisah lainnya, nipagin dan nipasol dilarutkan terlebih dahulu dalam etanol 96%, kemudian dimasukkan ke dalam wadah A dan diaduk hingga tercampur sempurna.
UIN Syarif Hidayatullah Jakarta
3.4 Evaluasi
3.4.1 Uji Stabilitas
1. Uji Stabilitas pada Suhu Ruang (27±2oC)
Masing-masing formula sediaan sebanyak 100 gram ditempatkan pada suhu ruang (27±2oC) selama 28 hari, serta diamati parameter fisika dan kimia pada hari ke 1, 7, 14, 21, dan 28 (Chandira et al., 2010)
2. Uji Stabilitas pada Suhu Tinggi (40±2oC)
Masing-masing formula sediaan sebanyak 100 gram ditempatkan pada suhu tinggi (40±2oC) yakni dalam oven selama 28 hari, serta diamati parameter fisika dan kimia pada hari ke 1, 7, 14, 21, dan 28 (Chandira et al., 2010).
3. Uji Cycling Test
Uji dilakukan dengan cara menyimpan sediaan dari masing-masing formula yang ditempatkan dalam wadah gelas transparan. Sediaan disimpan pada suhu 4±2oC selama 24 jam, kemudian dipindahkan ke dalam oven yang bersuhu 40±2oC selama 24 jam. Perlakuan ini adalah satu siklus. Pengujian dilakukan sebanyak 6 siklus atau 12 hari dan diamati ada atau tidaknya perubahan yang terjadi pada masing-masing sediaan. Kondisi sediaan dibandingkan selama percobaan dengan kondisi sediaan sebelumnya (Anonim, 2004).
3.4.2 Paramater Uji Stabilitas 1. Pengujian Organoleptis
UIN Syarif Hidayatullah Jakarta
2. Pengujian pH
Pengukuran pH dilakukan dengan menggunakan pH meter. Masing-masing formula harus memenuhi rentang pH dengan kisaran sesuai dengan pH kulit yaitu 4,5 – 6,5 (Tranggono, 2007).
3. Pengujian Homogenitas
Pemeriksaan homogenitas dilakukan dengan cara meletakkan sediaan diantara dua kaca objek dan diamati ada atau tidaknya partikel kasar yang terdapat dalam sediaan (Kuncari et al., 2014).
4. Pengujian Waktu Kering
Pengujian dilakukan dengan cara mengoleskan 1 gram dari masing-masing formula sediaan ke punggung tangan dengan ukuran 7 cm x 7 cm, kemudian dilihat menggunakan stopwatch waktu yang diperlukan oleh sediaan untuk mengering, yaitu waktu hingga sediaan membentuk lapisan film (Pertiwi, 2012)
5. Pengujian Daya Sebar
Sebanyak 1 gram dari masing-masing formula sediaan diletakkan di atas kertas grafik yang sudah dilapisi dengan plastik akrilik transparan, kemudian ditutup dengan plastik akrilik transparan lain dan diukur diameternya. Beban 19 gram diletakkan di atas sediaan, didiamkan selama 1 menit dan dicatat diameter gel yang menyebar. Beban 20 gram selanjutnya ditambahkan di atas sediaan sehingga beban maksimum yang digunakan adalah seberat 99 gram, dan setiap kali beban ditambahkan, maka sediaan harus didiamkan selama 1 menit dan dicatat diameter sediaan yang menyebar (Izzati, 2014) 6. Pengujian Viskositas
UIN Syarif Hidayatullah Jakarta
BAB 4
HASIL DAN PEMBAHASAN
4.1 Hasil Evaluasi Stabilitas Sediaan Masker Peel off
Uji stabilitas sediaan masker peel off dilakukan dengan cara membandingkan keadaan ketiga formula sediaan saat sebelum dan sesudah dilakukan pengujian.
Evaluasi sediaan masker peel off meliputi pemeriksaaan organoleptis, pH, homogenitas, waktu kering, daya sebar, dan viskositas. Ketiga formula sediaan masker peel off serbuk getah buah pepaya di uji pada kondisi suhu kamar (27±2oC) dan suhu tinggi (40±2oC) selama 4 minggu. Pengujan sediaan juga meliputi cycling test yang dilakukan selama 6 siklus atau 12 hari (Anonim, 2004). Pemeriksaan ini dilakukan sebagai simulasi adanya perubahan suhu setiap hari untuk mendapatkan kestabilan sediaan dalam waktu sesingkat mungkin.
4.1.1 Hasil Evaluasi Awal Sediaan
[image:38.595.94.535.234.654.2]Sediaan masker peel off berturut-turut yakni konsentrasi HPMC 2%, 3%, dan 4% memiliki karakter sebagai berikut :
Tabel 4.1 Karakteristik Awal Sediaan
Paramater Formula 1 Formula 2 Formula 3
Organoleptis
pH Homogenitas Waktu Kering
Viskositas
Sedikit keruh, berbau etanol, ada gelembung udara
6,5 Homogen
30 menit 3070 cps
Sedikit keruh, berbau etanol,
ada gelembung
udara 6,7 Homogen
30 menit 10.610 cps
Sedikit keruh, berbau etanol,
ada gelembung
udara 7 Homogen
UIN Syarif Hidayatullah Jakarta
Gambar 4.1 Pengujian Daya Sebar
Keadaan awal pada seluruh sediaan sebelum dilakukan pengujian adalah berwarna sedikit keruh, berbau etanol, dan terdapat gelembung udara. Formula 1 memiliki nilai pH sebesar 6,5 dengan nilai viskositas sebesar 3070 cps. Formula 2 memiliki pH 6,7 dengan nilai viskositas sebesar 10.610 cps. Formula 3 memiliki pH 7 dengan nilai viskositas sebesar 39.900 cps. Berdasarkan hasil tersebut dapat dilihat bahwa semakin tinggi konsentasi HPMC, maka akan mengakibatkan meningkatnya nilai viskositas. Hasi pengujian daya sebar menunjukkan bahwa semakin besar konsentrasi HPMC, maka daya sebar sediaan akan menurun.
0 5 10 15 20 25 30 35
34 54 74 94 114
L
uas
(cm
2)
Beban (gram)
Formula 1
Formula 2
UIN Syarif Hidayatullah Jakarta
[image:40.595.90.540.115.611.2]4.1.2 Hasil Organoleptis Sediaan
Tabel 4.2 Hasil Uji Organoleptis Sediaan pada Suhu Ruang (27±2oC)
Waktu Formula 1 Formula 2 Formula 3
UIN Syarif Hidayatullah Jakarta
Tabel 4.3 Uji Organoleptis Sediaan pada Suhu Tinggi (40±2oC)
Waktu Formula 1 Formula 2 Formula 3
Minggu 1 Minggu 2 Minggu 3 Minggu 4 Jernih, berbau etanol, homogen, terdapat sedikit gelembung udara Jernih, berbau etanol, homogen, tidak ada gelembung udara Jernih, berbau etanol, homogen, tidak ada gelembung udara Jernih, berbau etanol, homogen, tidak ada gelembung udara Jernih, berbau etanol, homogen, cukup banyak gelembung udara Jernih, berbau etanol, homogen, gelembung udara berkurang Jernih, berbau etanol, homogen, gelembung udara terus berkurang dari sebelumnya Jernih, berbau etanol, homogen, gelembung udara sangat sedikit Jernih, berbau etanol, homogen, terdapat banyak gelembung udara Jernih, berbau etanol, homogen, gelembung udara terus berkurang dari sebelumnya Jernih, berbau etanol, homogen, gelembung udara terus berkurang dari sebelumnya Jernih ,berbau etanol,homogen, gelembung udara terus berkurang dari sebelumnya
Secara organoleptis, keseluruhan sediaan masker peel off pada evaluasi awal masih berwarna sedikit keruh, lalu perlahan setelah dilakukan pengujian baik pada suhu ruang maupun pada suhu tinggi terjadi perubahan warna sediaan menjadi jernih (tidak berwarna). Perubahan warna sediaan menjadi jernih diakibatkan karena berkurangnya jumlah gelembung. Ketiga formula masker pada kondisi suhu ruang maupun suhu tinggi berbau etanol dan tidak menunjukkan adanya perubahan hingga akhir penyimpanan yakni pada minggu keempat.
UIN Syarif Hidayatullah Jakarta
yang sangat banyak ini dimungkinkan karena proses pengadukan selama pembuatan sediaan yang dapat merangkap udara disekitar sediaan yang bergerak melingkar. Tetapi gelembung tersebut perlahan berkurang selama penyimpanan baik pada suhu ruang maupun suhu tinggi. Hal ini disebabkan karena seiring dengan lamanya penyimpanan dan perubahan suhu maka udara didalam gelembung yang membentuk buih menekan dinding gelembung dengan kuat sehingga gelembung tersebut pecah dan perlahan berkurang (Padmadisastra et al., 2003).
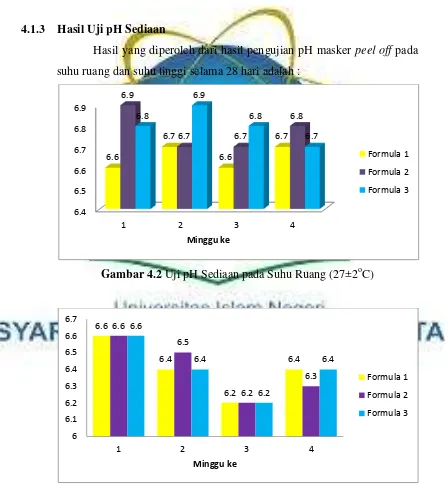
4.1.3 Hasil Uji pH Sediaan
[image:42.595.92.540.249.737.2]Hasil yang diperoleh dari hasil pengujian pH masker peel off pada suhu ruang dan suhu tinggi selama 28 hari adalah :
Gambar 4.2 Uji pH Sediaan pada Suhu Ruang (27±2oC)
Gambar 4.3 Uji pH Sediaan pada Suhu Tinggi (40±2oC) 6.4 6.5 6.6 6.7 6.8 6.9
1 2 3 4
6.6
6.7
6.6
6.7 6.9
6.7 6.7
6.8 6.8 6.9 6.8 6.7 Minggu ke Formula 1 Formula 2 Formula 3 6.6 6.4 6.2 6.4 6.6 6.5 6.2 6.3 6.6 6.4 6.2 6.4 6 6.1 6.2 6.3 6.4 6.5 6.6 6.7
1 2 3 4
Minggu ke
Formula 1
Formula 2
UIN Syarif Hidayatullah Jakarta
Pada pengamatan stabilitas terhadap nilai pH sediaan terlihat bahwa ketiga formula pada suhu ruang dan suhu tinggi cenderung berubah-ubah, yakni terjadi penurunan dan kenaikan pH yang bervariasi selama pengujian. Perubahan nilai pH pada sediaan tidak signifikan, sehingga semua formula dapat dikatakan stabil.
Kestabilan pH merupakan salah satu parameter penting yang menentukan stabil atau tidaknya suatu sediaan. Nilai pH awal dari masing-masing formula hingga setelah pengujian baik dalam kondisi suhu ruang maupun suhu tinggi berada sedikit diluar kisaran pH kulit yaitu 4,5 – 6,5 akan tetapi pH yang dimiliki oleh ketiga formulasi tersebut tidak ada yang melebihi pH netral sehingga tidak bersifat basa. Nilai pH sediaan sebaiknya sesuai dengan pH kulit wajah yaitu 4,5 – 6,5 (Noor dan Desy, 2009). Jika sediaan memiliki pH yang terlalu basa maka dapat menyebabkan kulit menjadi kering, sedangkan jika pH terlalu asam akan menimbulkan iritasi kulit (Djajadisastra, 2004 dalam Izzati, 2014).
4.1.4 Hasil Uji Waktu Kering
Hasil yang diperoleh dari hasil pengujian waktu kering masker
[image:43.595.89.535.209.651.2]peel off pada suhu ruang dan suhu tinggi selama 28 hari adalah :
Gambar 4.4 Uji Waktu Kering pada Suhu Ruang (27±2oC) 0
10 20 30 40 50 60 70
1 2 3 4
M
e
n
it
Minggu ke
Formula 1
Formula 2
UIN Syarif Hidayatullah Jakarta
Gambar 4.5 Uji Waktu Kering pada Suhu Tinggi (40±2oC)
Pengujian waktu kering sediaan dilakukan dengan mengamati waktu yang diperlukan sediaan untuk mengering, yaitu waktu dari saat sediaan mulai dioleskan pada kulit hingga benar-benar terbentuk lapisan yang kering (Pertiwi, 2012).
Setelah sediaan mengering, lalu sediaan diangkat dari permukaan kulit dengan cara dikelupas. Dari hasil penelitian pada 5 orang responden menunjukkan bahwa seiring dengan meningkatnya konsentrasi HPMC, maka sediaan menjadi lebih mudah diangkat. Hal itu sesuai dengan teori dimana PVA memiliki kelemahan yaitu bersifat kaku, maka dengan penambahan HPMC akan meningkatkan fleksibilitas sediaan.
Faktor yang paling berpengaruh signifikan terhadap waktu kering adalah konsentrasi etanol dalam formulasi. Peningkatan konsentrasi etanol akan mempersingkat waktu kering sediaan, hal tersebut dikarenakan etanol memiliki tingkat volatilitas yang lebih tinggi dibandingkan dengan air murni (Beringhs et al 2013). Pada formulasi sediaan masker peel off ini digunakan konsentrasi etanol sebesar 15%, hal tersebut didasarkan pada
formulasi yang terdapat dalam buku Hary’s Cosmeticology yang
menyebutkan bahwa konsentrasi etanol dapat digunakan hingga 30% dalam sediaan masker peel off.
Dari data pengujian waktu kering, diperoleh hasil bahwa masing – masing formula memenuhi persyaratan waktu kering yang baik. Pada Formula 1 dan Formula 2 baik pada kondisi suhu ruang maupun kondisi
0 10 20 30 40 50 60 70 80
1 2 3 4
M
e
n
it
Minggu ke
Formula 1
Formula 2
UIN Syarif Hidayatullah Jakarta
suhu tinggi mulai menunjukkan adanya perubahan waktu kering sediaan, tetapi formula 3 masih berada dalam ketentuan kriteria waktu kering yang baik. Formula 3 memiliki waktu kering yang lebih cepat dibandingkan dengan formula 1 dan Formula 2. Hal tersebut mungkin disebabkan karena seiring meningkatnya konsentrasi HPMC pada formula 3, maka akan lebih banyak etanol yang terikat pada polimer, sehingga memperlama waktu penguapan etanol.
Setelah 4 minggu pengujian pada kondisi suhu ruang terjadi perubahan yang signifikan, dimana waktu kering masing-masing formula menjadi lebih lama, terutama pada formula 1 dan 2. Hal yang sama juga terjadi pada pengujian di suhu tinggi, dan perubahan lama waktu kering yang sangat derastis terjadi pada ketiga formula. Sediaan pada suhu tinggi cenderung memiliki waktu kering yang sangat lama, hal tersebut terjadi karena seiring dengan peningkatan suhu, maka etanol menjadi lebih mudah menguap. Etanol dalam sediaan gel masker peel off berfungsi untuk mempercepat waktu pengeringan sediaan. Saat etanol menguap, maka akan memberikan pengaruh pada sediaan berupa peningkatan waktu kering atau waktu sediaan untuk mengering menjadi lebih lama (Beringhs et al, 2013)
UIN Syarif Hidayatullah Jakarta
4.1.5 Hasil Uji Viskositas
Hasil yang diperoleh dari hasil pengujian viskositas masker peel off
pada suhu ruang dan suhu tinggi selama 28 hari adalah :
[image:46.595.96.529.166.617.2]Gambar 4.6 Uji Viskositas pada Suhu Ruang (27±2oC)
Gambar 4.7 Uji Viskositas pada Suhu Tinggi (40±2oC)
Viskositas adalah suatu ungkapan dari resistensi zat cair untuk mengalir. Semakin tinggi viskositas aliran, maka akan semakin besar resistensinya. Viskositas sediaan dipengaruhi oleh beberapa faktor diantaranya adalah faktor pencampuran atau pengadukan saat proses pembuatan sediaan, pemilihan basis gel dan humektan, serta ukuran partikel (Ansel, 1989 dalam Angela, 2012). Pengukuran viskositas
3270 3930
7210 3590 33600 13550 0 5000 10000 15000 20000 25000 30000 35000 40000
Minggu Awal Minggu Akhir
Vi sko si tas (c p s) Formula 1 Formula 2 Formula 3
2870 3640 3290 3660
21400 17100 0 5000 10000 15000 20000 25000
Minggu Awal Minggu Akhir
UIN Syarif Hidayatullah Jakarta
dilakukan pada minggu awal (minggu ke-1) dan minggu terakhir (minggu ke-4) yang diuji pada suhu ruang dan suhu tinggi.
Pemeriksaan viskositas dilakukan dengan menggunakan Haake Visco tester 6R dengan nomer spindel yang berbeda untuk setiap formula, namun dengan kecepatan yang sama yaitu Rpm 20. Dari hasil uji viskositas dilihat dari parameter perbedaan konsentrasi HPMC dalam formula sangat terlihat jelas bahwa semakin tinggi penggunaan HPMC maka viskositasnya akan semakin meningkat. Peningkatan konsentrasi HPMC dapat meningkatkan jumlah serat polimer sehingga semakin banyak juga cairan yang tertahan dan terikat oleh agen pembentuk gel sehingga viskositas menjadi meningkat (Martin et al., 1993 dalam Sukmawati, 2013).
Hasil pengamatan sediaan pada suhu ruang menunjukkan bahwa pada minggu ke empat, formula 1 mengalami peningkatan, sedangkan formula 2 dan 3 mengalami penurunan nilai viskositas dibandingkan dengan minggu pertama.
Hasil pengamatan sediaan pada suhu tinggi menunjukkan hasil yang berbeda dengan sediaan yang disimpan pada suhu ruang, dimana pada minggu ke-empat formula 1 dan 2 mengalami peningkatan nilai viskositas, sedangkan formula 3 mengalami penurunan dibandingkan dengan minggu pertama.
Pada minggu pertama seluruh formula yang disimpan pada suhu tinggi memiliki nilai viskositas yang lebih rendah dibandingkan dengan sediaan yang disimpan pada suhu ruang. Namun pada minggu ke empat terjadi perubahan dimana formula 2 dan 3 yang disimpan pada suhu tinggi memiliki nilai viskositas yang lebih besar dibandingkan dengan formula 2 dan 3 yang disimpan pada suhu ruang. Adapun hasil pengukuran viskositas dapat dilihat dalam lampiran 6.
UIN Syarif Hidayatullah Jakarta
dimana semakin banyak jumlah gelembung maka akan meningkatkan nilai viskositas (Black and White, 1977). Kondisi temperatur juga ikut berpengaruh terhadap nilai viskositas. Seiring meningkatnya temperatur, maka ukuran gelembung menjadi lebih besar, sehingga lebih mudah pecah dan mengakibatkan viskositasnya menurun (Rust and Manga, 2002).
Solusi yang dapat digunakan agar data hasil pengukuran viskositas sediaan tidak bias adalah dengan cara menghilangkan gelembung terlebih dahulu dari sediaan. Gelembung dapat dihilangkan dengan cara penggunaan mesin agitasi yang akan mengaduk sediaan dari bawah, atau dengan cara menggunakan penutup pada saat pengadukan agar tidak terdapat udara yang terjerap. Cara lain yang dapat digunakan yakni dengan memanaskan sediaan dalam waktu singkat menggunakan vakum, atau penambahan agen anti busa (Black and White, 1977).
4.1.6 Hasil Uji Daya Sebar
[image:48.595.97.535.206.616.2]Hasil yang diperoleh dari hasil pengujian daya sebar masker peel off pada suhu ruang dan suhu tinggi selama 28 hari adalah :
Gambar 4.8 Uji Daya Sebar pada Suhu Ruang (27±2o) Minggu ke 1
0
10 20 30 40 50 60 70
34 54 74 94 114
L
u
as
(c
m
2 )
Beban (gram)
Formula 1
Formula 2
UIN Syarif Hidayatullah Jakarta
Gambar 4.9 Uji Daya Sebar pada Suhu Ruang (27±2o) Minggu ke 2
[image:49.595.80.540.122.648.2]Gambar 4.10 Uji Daya Sebar pada Suhu Ruang (27±2o) Minggu ke 3
Gambar 4.11 Uji Daya Sebar pada Suhu Ruang (27±2o) Minggu ke 4 0 10 20 30 40 50 60
34 54 74 94 114
L u as (c m 2) Beban (gram) Formula 1 Formula 2 Formula 3 0 10 20 30 40 50 60 70
34 54 74 94 114
L u as (c m 2 ) Beban (gram) Formula 1 Formula 2 Formula 3 0 10 20 30 40 50 60 70
34 54 74 94 114
UIN Syarif Hidayatullah Jakarta
Gambar 4.12 Uji Daya Sebar pada Suhu Tinggi (40±2o) Minggu ke 1
Gambar 4.13 Uji Daya Sebar pada Suhu Tinggi (40±2o) Minggu ke 2
Gambar 4.14 Uji Daya Sebar pada Suhu Tinggi (40±2o) Minggu ke 3 0 10 20 30 40 50 60 70
34 54 74 94 114
L uas ( cm 2) Beban (gram) Formula 1 Formula 2 Formula 3 0 10 20 30 40 50 60
34 54 74 94 114
L u as (c m 2 ) Beban (gram) Formula 1 Formula 2 Formula 3 0 10 20 30 40 50
34 54 74 94 114
UIN Syarif Hidayatullah Jakarta
Gambar 4.15 Uji Daya Sebar pada Suhu Tinggi (40±2o) Minggu ke 4
Pengujian daya sebar dilakukan untuk mengetahui kecepatan penyebaran sediaan saat dioleskan pada kulit. Gel yang baik membutuhkan waktu yang lebih sedikit untuk tersebar dan akan memiliki nilai daya sebar yang tinggi (Madan dan Singh, 2010 dalam Sukmawati,2013). Pengujian daya sebar dilakukan dengan menggunakan beban sebesar 19 gram hingga 99 gram. Berat kaca akrilik yang digunakan adalah sebesar 15 gram, jadi berat akhir keseluruhan setelah ditambahkan kaca akrilik menjadi 114 gram. Sebanyak 1 gram sediaan diletakkan di atas kertas grafik yang dilapisi oleh kaca akrilik transparan kemudian ditutup dengan kaca akrilik transparan lain kemudian diberi beban, diukur diameternya dan kemudian ditentukan luasnya. Berdasarkan hasil pengujian daya sebar sediaan yang diperoleh baik pada suhu ruang maupun suhu tinggi dapat disimpulkan bahwa semakin meningkatnya penggunaan HPMC dalam formula, maka daya menyebar gel akan semakin berkurang. Penurunan daya sebar terjadi melalui peningkatan ukuran unit molekul karena telah mengabsorbsi pelarut sehingga cairan tersebut tertahan dan meningkatkan tahanan untuk mengalir dan menyebar (Martin et al., 1993 dalam Sukmawati, 2013). Formula 3 dengan konsentrasi HPMC paling tinggi yakni 4% memilki kemampuan penyebaran yang paling rendah.
Pada minggu pertama hingga minggu ke tiga, sediaan yang diuji dalam suhu tinggi menunjukkan data daya sebar yang lebih kecil bila dibandingkan dengan sediaan yang diuji dalam suhu ruang. Sediaan dalam
0 10 20 30 40 50 60 70 80
34 54 74 94 114
Lu
as
(c
m
2)
Beban (gram)
Formula 1
Formula 2
UIN Syarif Hidayatullah Jakarta
suhu tinggi cenderung memiliki nilai daya sebar yang lebih kecil, hal tersebut dikarenakan akibat pengaruh suhu tinggi, maka etanol akan lebih mudah menguap sehingga konsistensi sediaan menjadi lebih padat dan lebih rigid yang mengakibatkan kemampuannya untuk menyebar menjadi berkurang.
Secara umum, seiring dengan lamanya waktu pengujian maka daya sebar sediaan baik pada suhu ruang maupun suhu tinggi terus mengalami penurunan. Namun pada minggu ke empat masing-masing formula pada seluruh kondisi penyimpanan mengalami peningkatan daya sebar dan daya sebar sediaan pada suhu tinggi lebih besar dari sediaan yang disimpan pada suhu ruang padahal pada penyimpanan minggu awal sampai minggu ketiga sediaan yang disimpan pada suhu tinggi daya sebarnya selalu lebih rendah dari sediaan pada suhu kamar. Adanya perubahan tersebut pada minggu ke empat mengindikasikan bahwa sediaan mulai menunjukkan tanda ketidakstabilan.
4.1.7 Hasil Uji Cycling Test
UIN Syarif Hidayatullah Jakarta
Tabel 4.4 Uji Organoleptis dan Homogenitas pada Cycling Test
Waktu Formula 1 Formula 2 Formula 3
Siklus 1 Siklus 2 Silkus 3 Siklus 4 Siklus 5 Siklus 6
Jernih, berbau etanol, homogen, cukup banyak gelembung
udara
Jernih, berbau etanol, homogen, gelembung
udara berkurang
Jernih, berbau etanol, homogen, gelembung
udara terus berkurang
Jernih, berbau etanol, homogen, gelembung
udara semakin berkurang
Jernih, berbau etanol, homogen, gelembung
udara hilang
Jernih, berbau etanol, homogen, tidak ada
gelembung udara
Jernih, berbau etanol, homogen, banyak
gelembung udara
Jernih, berbau etanol, homogen, gelembung
udara berkurang
Jernih, berbau etanol, homogen, gelembung
udara berkurang
Jernih, berbau etanol, homogen, gelembung
udara terus berkurang
Jernih, berbau etanol, homogen, gelembung
udara semakin berkurang
Jernih, berbau etanol, homogen, gelembung
udara hilang
Jernih, berbau etanol, homogen, sangat banyak gelembung
udara
Jernih, berbau etanol, homogen, gelembung
udara berkurang
Jernih, berbau etanol, homogen, gelembung udara
berkurang
Jernih, berbau etanol, homogen, gelembung udara
berkurang
Jernih, berbau etanol, homogen, gelembung udara
berkurang
Jernih, berbau etanol, homogen, sedikit gelembung udara
Cycling test dilakukan dengan tujuan untuk memperoleh gambaran terjadinya sineresis pada gel yang dapat terjadi karena sebagian cairan antarsel keluar yang menyebabkan gel menjadi mengkerut dan juga untuk mengamati terjadinya perubahan yang mengindikasikan adanya ketidakstabilan sediaan.
Pengujian cycling test dilakukan dengan cara mengkondisikan sediaan pada perubahan kondisi ekstrim selama 6 siklus. Masing – masing formula sediaan akan diuji setiap satu siklus. Sebelum dilakukan pengujian, setiap sediaan didiamkan terlebih dahulu hingga sediaan berada pada suhu normal, yakni pada suhu ruang.
UIN Syarif Hidayatullah Jakarta
berwarna (jernih), berbau etanol dan terlihat homogen secara fisik. Perbedaan yang terlihat adalah berupa semakin berkurangnya gelembung udara seiring dengan lamanya waktu pengujian. Formula 3 dengan konsentrasi HPMC paling tinggi yaitu sebesar 4% memiliki jumlah gelembung yang paling banyak dan sulit menghilang. Hal tersebut dikarenakan pada saat proses pengadukan, gaya yang diberikan cukup besar sehingga semakin banyak udara yang terjerap di dalam sediaan dan untuk menghilangkannya juga diperlukan tekanan yang lebih besar untuk menekan dinding gelembung dengan kuat sehingga gelembung tersebut pecah dan akhirnya menghilang. Selain itu, ketiga formula sediaan juga tidak menunjukkan adanya sineresis hingga akhir siklus.
Hasil yang diperoleh dari hasil pengujian pH masker peel off pada cycling test adalah :
Gambar 4.16 Uji pH pada Cycling Test
Pemeriksaan nilai pH pada masing-masing formula menunjukkan perubahan yang bervariasi yang terjadi pada siklus yang berbeda. Formula 1 menunjukkan nilai pH yang sama dari awal siklus hingga siklus ke empat, namun pada siklus ke 5 mulai terjadi perubahan yaitu berupa penurunan pH hingga akhir siklus. Formula 2 mulai menunjukkan penurunan pada siklus ke dua dan nilai pH yang dihasilkan tetap sama
6.35 6.4 6.45 6.5 6.55 6.6 6.65 6.7 6.75 6.8 6.85
1 2 3 4 5 6
Siklus ke
Formula 1
Formula 2
UIN Syarif Hidayatullah Jakarta
hingga siklus ke empat, kemudian pH sediaan kembali turun pada siklus ke lima dan nilai pH tetap stabil hingga siklus ke enam. Formula 3 menunjukkan hasil nilai pH yang bervariasi, namun nilai pH mulai stabil pada siklus ke lima hingga siklus ke enam.
Variasi nilai pH yang terjadi pada sediaan tidak memberikan hasil yang berbeda secara signifikan, sehingga sediaan dapat dikatakan sediaan tersebut stabil dalam pengujian cycling test selama 6 siklus.
Tabel 4.6
Waktu Formula 1
(menit) Formula 2 (menit) Formula 3 (menit) Siklus 1 Siklus 2 Siklus 3 Siklus 4 Siklus 5 Siklus 6 30 30 30 30 30 30 30 30 30 30 30 30 30 30 30 30 30 30
[image:55.595.90.538.254.685.2]Dari hasil pengujian waktu kering selama 6 siklus menunjukkan bahwa waktu kering dari masing-masing formula tidak mengalami perubahan dan ketiga formula gel masker peel off masih memenuhi kriteria waktu kering yang baik yaitu antara 15 – 30 menit (Vieira, 2009).
Gambar 4.17 Uji Viskositas selama Cycling Test
Dari hasil pengujian viskositas pada siklus awal (siklus ke-1) hingga siklus akhir (siklus ke-6) diperoleh data yang bervariasi dimana
2370 2970
11160 4250 28100 22700 0 5000 10000 15000 20000 25000 30000
Siklus Awal Siklus Akhir
UIN Syarif Hidayatullah Jakarta
pada formula 1 terjadi peningkatan nilai viskositas, sedangkan pada formula 2 dan formula 3 terjadi penurunan viskositas. Hal tersebut menunjukkan bahwa setiap formula menunjukkan respon yang berbeda setelah dikondisikan selama proses cycling test. Gelembung yang terdapat dalam sediaan juga sangat mengganggu dalam pengujian viskositas, sehingga data yang dihasilkan menjadi bias.
[image:56.595.87.536.255.661.2]