Tinjauan Pustaka
Penatalaksanaan terkini Artritis Reumatoid dengan paradigma baruTreat-to-Target (T2T)
Putu Gede Surya Wibawa, Gede Kambayana. Program Studi Pendidikan Dokter Spesialis Ilmu Penyakit Dalam FK Unud/RSUP Sanglah Denpasar Bali
Pendahuluan
Artritis Reumatoid (AR) adalah penyakit yang tersebar luas serta melibatkan semua kelompok ras dan etnik di dunia. Penyakit ini merupakan suatu penyakit autoimun yang etiologinya belum diketahui dan ditandai oleh sinovitis erosif simetris yang walaupun terutama mengenai jaringan persendian, disertai keterlibatan jaringan ektraartikular (1).
Dalam banyak bidang medis, target terapi telah terbukti meningkatkan keluaran dan menurunkan risiko kerusakan organ. Dalam perawatan pasien diabetes, hiperlipidemia, hipertensi, aspek ini telah diadopsi secara luas dalam praktek klinis, dokter melakukan pemeriksaan laboratorium untuk kolesterol dan trigleserida, gula darah, dan nilai HbA1c, memeriksa tekanan darah dan menyesuaikan terapi yang tepat, dan pasien mengetahui nilai dari hal ini dan lebih peduli akan target terapi. Pengobatan AR telah mengalami perubahan dramatis dalam 20 tahun terakhir, salah satunya melalui perubahan paradigma yang disebut rekomendasi ’treat to target’ (T2T). T2T bertujuan meningkatkan keluaran dan pengurangan risiko kerusakan organ. Dalam RA, kerusakan sendi dan cacat fisik adalah keluaran utama yang merugikan terkait dengan penurunan kualitas hidup dan kematian dini (2).
Batasan
Artritis Reumatoid (AR) adalah merupakan suatu penyakit autoimun melibatkan semua kelompok ras dan etnik di dunia yang etiologinya belum diketahui. Ditandai oleh sinovitis erosif simetris yang walaupun terutama mengenai jaringan persendian, disertai keterlibatan jaringan ektraartikular. Perjalanan penyakit AR ada 3 macam yaitu monosiklik, polisiklik dan progresif. Sebagian besar kasus perjalanannya kronik fluktuaktif yang mengakibatkan keruskan sendi yang progresif, kecacatan dan bahkan kematian dini (1,3-5).
Epidemiologi
Prevalensi dan insiden penyakit ini bervariasi antara populasi satu dengan lainya, di Amerika Serikat dan beberapa daerah di Eropa prevalensi AR sekitar 1% pada kaukasia dewasa; Perancis sekitar 0,3%, Inggris dan Finlandia sekitar 0,8% dan Amerika Serikat 1,1% sedangkan di Cina sekitar 0,28%. Jepang sekitar 1,7% dan India 0,75%. Insiden di Amerika dan Eropa Utara mencapai 20-50/100000 dan Eropa Selatan hanya 9-24/100000. Di Indonesia dari hasil survey epidemiologi di Bandungan Jawa Tengah didapatkan prevalensi AR 0,3 %, sedang di Malang pada penduduk berusia diatas 40 tahun didapatkan prevalensi AR 0,5 % di daerah Kotamadya dan 0,6% di daerah Kabupaten, sementara di Poliklinik Reumatologi RSUPN Cipto Mangunkusumo Jakarta, pada tahun 2000 kasus baru AR merupakan 4,1% dari seluruh kasus baru. Di poliklinik reumatologi RS Hasan Sadikin didapatkan 9% dari seluruh kasus reumatik baru pada tahun 2000-2002. Wanita 3 kali lebih sering terkena dibandingkan pria. Dapat mengenai semua usia namun prevalensi muncul seiring waktu dan lebih tinggi pada perempuan berusia diatas 65 tahun, dikaitkan faktor hormonal sex yang ikut berperan. (1,5-6)
Etiologi
diperkirakan sebagai faktor pencetus AR. Faktor lingkungan yang utama adalah merokok, faktor lain adalah minum alkohol, kopi, status vitamin D, dan status sosial ekonomi rendah. Faktor genetik adalah 50% risiko terjadinya AR, faktor genetik seperti produk komplek histokompatibilitas utama kelas II (HLA-DR4) telah lama diduga berperanan dalam timbulnya penyakit ini, dimana risiko relatif 4:1 untuk menderita penyakit ini pada mereka dengan HLA-DR4. (3-6)
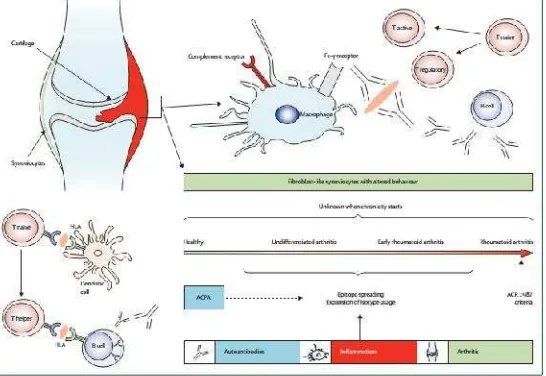
Patogenesis
Radikal oksigen menyebabkan terjadinya depolimerisasi hyaluronate sehingga viskositas cairan sendi menurun, merusak kolagen dan proteoglikan rawan sendi. Leukotrien LTB4 menyebabkan migrasi dan agregasi kuat neftrofil. Prostaglandin E2 memiliki efek vasodilator kuat dan merangsang resorpsi tulang osteoklastik, juga memiliki efek anti inflamasi dengan menghambat sekresi IL-2, A-interferon.
Pengendapan kompleks imun juga menyebabkan masuknya sel T kedalam membran sinovial dan akan merangsang terbentuknya pannus yang merupakan elemen paling bersifat destruktif pada patogenesis AR. Pannus adalah jaringan granulasi yang terdiri dari makrofag yang teraktivasi, sel fibroblast yang berproliferasi dan jaringan mikrovaskular. Sitokin IL-1 dan TNF memainkan peran penting untuk memicu sel pannus menghasilkan kolagen dan enzim proteolitik yang merusak tulang rawan secara lokal dan menghambat pembentukan molekul matrik baru. Dua sitokin tersebut bersama IL-6 juga berperan dalam dimineralization dari tulang yang berperan dalam aktivasi osteoklast yang berakumulasi pada daerah lokal resorpsi tulang. Pannus akan menginvasi jaringan kolagen dan proteoglikan rawan sendi serta tulang sehingga mengancurkan struktur persendian. Bila proses pembentukan pannus ini tidak terhenti baik oleh karena pengobatan atau remisi spontan, maka akan terjadi ankilosis dan juga peningkatan ekspresi intracellular adhesion molecule-1 (ICAM-1) yang merupakan tempat perlekatan sel mononukleus pada endotel mikrovaskular, yang mengakibatkan peningkatan adhesi sel mononukleus pada endotel kapiler.
Rantai peristiwa imunologis ini umumnya akan terhenti bila antigen penyebab dapat dihilangkan dari lingkungan tersebut. Akan tetapi pada AR, antigen atau komponennya umumnya akan menetap pada struktur persendian sehingga proses dekstruksi sendi akan terus berlangsung. Hal ini terjadi juga karena terbentuknya faktor reumatoid, Faktor reumatoid adalah autoantibodi klasik dalam radang sendi. IgM dan IgA faktor reumatoid adalah penanda patogen kunci yang ditunjukan terhadap fragmen Fc IgG. Jenis antibodi tambahan (dan semakin penting) yang ditujukanagainst citrullinated peptides (ACPA).Meskipun sebagian besar, tapi tidak semua, pasien dengan ACPA positif juga positif untuk faktor reumatoid, ACPA tampak lebih spesifik dan sensitif untuk diagnosis AR dan tampak menjadi prediktor yang lebih baik terhadap prognosis yang buruk seperti kerusakan sendi yang progresif. 50-80% dari individu dengan AR memiliki faktor reumatoid, ACPA, atau keduanya. Bagaimanapun suatu imunoglobulin dapat berubah sifatnya menjadi antigen, hal ini belum dapatditerangkan dengan jelas. Faktor reumatoid juga dapat berikatan dengan komplemen atau mengalami agregasi sendiri, sehingga proses peradangan akan terus berlanjut. Terbentuknya autoantibodi terhadap colagen type II baik yang bersifat native ataupun yang telah mengalami denaturasi dapat pula mengekalkan terjadinya peradangan dengan mekanisme yang sama. Pentingnya peran sel limfosit B pada proses inflamasi kronik telah dibuktikan melalui observasi terapi dengan antibodi monoklonal terhadap marker sel B, CD 20, menyebabkan deplesi yang cepat dari limfosit B, penurunan titer serum faktor reumatoid, dan perbaikan parsial tanda dan gejala peradangan. (3,5,6)
Manifestasi klinis
Manifestasi umum. Sebagian besar pasien dengan keluhan konstitusional berupa perasaan badan lemah, mudah lelah, nafsu makan menurun, penurunan berat badan. Meskipun demam bisa sampai 40 oC, namun demam > 38OC jarang dan kemungkinan ada infeksi.
Manifestasi Artikuler. Meskipun inflamasi dapat mengenai setiap sendi diartrosis. Namun, paling sering mengenai sendi kecil dan simetris yaitu sendi pergelangan tangan, lutut dan kaki. Sendi lainnya juga dapat terkena seperti sendi siku, bahu sterno-klavikula, panggul, pergelangan kaki. Kelainan pada tulang belakang terbatas pada leher. Keluhan sering berupa kaku sendi pagi hari, pembengkakan dan nyeri sendi. Lamanya kaku sendi pagi hari mencerminkan beratnya penyakit. Keluhan nyeri dan kekakuan akan meningkat sejalan dengan beratnya keadaan dan diikuti dengan hambatan untuk jalan, naik tangga, membuka pintu dan lainnya. Kelainan fisik awal khas terlihat jari berbentuk fusiform akibat pembengkakan sendi interphalangeal proksimal yang simetris. Jarang mengenai interphalangeal distal. Juga bersama pembengkakan simetris metakarpophalangeal. Akibat kelemahan jaringan lunak terjadi deformitas bentuk leher angsa (swan neck deformity) atau “boutonniere deformity”. Keadaan ini
menyebabkan kemampuan memegang dan menggenggam berkurang. Pada pergelangan tangan, kelainan bervariasi dapat berupa pembengkakan sinovium,
hambatan gerakan, sindrom “carpal tunnel” atau atropi otot tenar. Kelainan pada kaki mirip pada tangan.
lain berupa episkleritis yang ringan dan akan sembuh spontan. Dapat pula terjadi skleritis yang dapat menimbulkan gejala skleromalasia perforans yang dapat menyebabkan kebutaan; 3)Sistem Kardiovaskular. Kelainan jantung asimptomatis perikarditis ditemukan sekitar 50% pada autopsi. Meskipun perikarditis biasanya asimptomatik, namun kasus jarang bisa terjadi kematian karena tamponade. Kelainan jantung yang simptomatis sering berupa perikarditis konstriktif yang berat. Kelainan jantung lain dapat berupa nodul rematoid pada miokardium dan katub jantung. Lesi ini dapat menyebabkan disfungsi katub, embolisasi, ganguan konduksi, aortitis dan kardiomiopati; 4)Sistem respiratorik. Manifestasi paling sering pada pria, penyakit pleura, fibrosis interstitial, nodul pleuropulmonary, pneumonitis, dan arteritis. Manifestasi jarang adalah hipertensi pulmoner sekunder. ; 5)Sistem Saraf.Manifestasi AR pada sistem neuro sering tidak jelas. Umumnya berhubungan dengan mielopati akibat instabilitas vertebra, servikal, neuropati jepitan atau neuropati iskemik akibat vaskulitis; 6) Sistem Hematologis. Anemia akibat penyakit kronik dengan gambaran eritrosit normositik normokromik atau hipomikromik ringan disertai kadar besi serum rendah dan TIBC yang normal atau rendah adalah gambaran umum pada AR. Sindrom Felty adalah AR dengan splenomegali, neutropenia, anemia dan ulkus pada tungkai. Sindrom Felty juga sering dengan limpadenopati, trombositopeni. Sering terjadi pada AR yang sangat berat dan HLA-DR4 positif; 7)Osteoporosis Sekunder, adalah umum dan dikaitkan dengan terapi glukokortikoid dan AR itu sendiri. (1,3-6)
Diagnosis
Selama ini diagnosis AR memakai kriteria ACR tahun 1987 dengan sensitivitas 77-95% dan spesifitas 85-98%. Tapi kriteria ini mulai dipertanyakan kesahihannya dalam mendiagnosis AR dini sehingga dipandang perlu untuk menyusun kriteria baru yang tingkat kesahihannya lebih baik
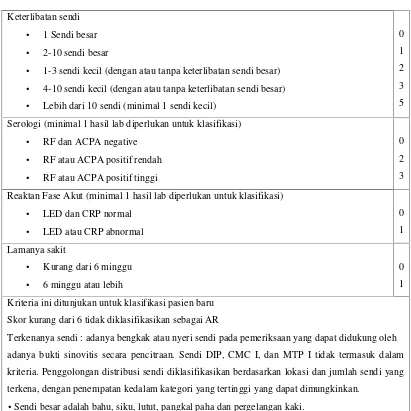
[image:8.595.106.517.301.712.2]Saat ini diagnosis AR di Indonesia mengacu pada kriteria diagnosis menurut American College of Rheumatology/European League Against Rheumatism 2010 yaitu: (1,6-7)
Tabel 1. Kriteria klasifikasi AR ACR/EULAR 2010 (1)
Keterlibatan sendi
• 1 Sendi besar
• 2-10 sendi besar
• 1-3 sendi kecil (dengan atau tanpa keterlibatan sendi besar)
• 4-10 sendi kecil (dengan atau tanpa keterlibatan sendi besar)
• Lebih dari 10 sendi (minimal 1 sendi kecil)
0
1
2
3
5
Serologi (minimal 1 hasil lab diperlukan untuk klasifikasi)
• RF dan ACPA negative
• RF atau ACPA positif rendah
• RF atau ACPA positif tinggi
0
2
3
Reaktan Fase Akut (minimal 1 hasil lab diperlukan untuk klasifikasi)
• LED dan CRP normal
• LED atau CRP abnormal
0
1
Lamanya sakit
• Kurang dari 6 minggu
• 6 minggu atau lebih
0
1
Kriteria ini ditunjukan untuk klasifikasi pasien baru
Skor kurang dari 6 tidak diklasifikasikan sebagai AR
Terkenanya sendi : adanya bengkak atau nyeri sendi pada pemeriksaan yang dapat didukung oleh
adanya bukti sinovitis secara pencitraan. Sendi DIP, CMC I, dan MTP I tidak termasuk dalam
kriteria. Penggolongan distribusi sendi diklasifikasikan berdasarkan lokasi dan jumlah sendi yang
terkena, dengan penempatan kedalam kategori yang tertinggi yang dapat dimungkinkan.
•Sendi besar adalah bahu, siku, lutut, pangkal paha dan pergelangan kaki.
•Sendi kecil adalah MCP, PIP, MTP II-V, IP ibu jari dan pergelangan tangan.
normal;
positif rendah adalah nilai yang lebih tinggi dari batas atas normal tapi sama atau kurang dari 3
kali nilai tersebut; positif tinggi adalah nilai yang lebih tinggi dari 3 kali batas atas. Jika RF hanya
diketahui positif atau negatif, maka positif harus dianggap sebagai positif rendah
Lamanya sakit adalah keluhan pasien tentang lamanya keluhan atau tanda sinovitis (nyeri, bengkak
atau nyeri pada perabaaan)
Diagnosis banding
Pada kasus dengan poliartritis inflamasi selain AR perlu dipertimbangkan diagnosis banding seperti spondiloartropati seronegatif, misalnya artritis psoriatik, artritis gout poliartikuler, lupus eritematosus sistemik, dan artritis reaktif. (1,3-6)
Penatalaksanaan Evaluasi Awal Pasien
Apabila diagnosis AR telah ditegakan maka:
1). Tentukan aktivitas penyakit (LED, CRP, sinovitis), status fungsional, masalah mekanik sendi, gejala ekstraartikular serta adanya kerusakan radiologis pada sendi yang terlibat.
2). Apabila pasien AR akan mendapatkan DMARD, a). Lakukan pemeriksaan laboratorium awal yaitu darah perifer lengkap, LED, CRP, RF atau ACPA, fungsi hati dan ginjal karena beberapa obat DMARD bersifat toksik terhadap hati dan ginjal. Sebaiknya pasien diperiksa serologi untuk hepatitis B dan C terutama yang direncanakan untuk penggunaan MTX; b). Foto toraks diperlukan untuk mendeteksi ada tidaknya infeksi (misalnya tuberkulosis paru), karena beberapa jenis DMARD dapat berpotensi meningkatkan kerentanan untuk mendapat infeksi, dan manifestasi ekstra artikular pada paru; c).Pastikan wanita penderita AR yang akan memakai DMARD tidak dalam keadaan hamil.
Tabel 2. Pilar penatalaksanaan (1)
Pilar Penatalaksanaan Artritis Reumatoid
1) Edukasi
2) Latihan / Program Rehabilitasi
3) Pilihan Pengobatan: 1. DMARD 2. Agen Biologik 3. Kortikosteroid 4. Obat Anti Inflamasi Non Steroid (NSAID).
4) Pembedahan
Penatalaksanaan AR dengan rekomendasi ‘treat to target’ (T2T) perbaikan tahun 2014.
Berbagai studi telah menunjukan bahwa penatalaksanaan AR dengan rekomendasi T2T lebih superior dibandingkan penatalaksanaan konvensional. Dalam Penatalaksanaan AR dengan rekomendasi ‘treat to target’(T2T) perbaikan tahun 2014 secara umum ada 2, yaitu prinsip umum penatalaksanaan dan sasaran penatalaksanaan.
Prinsip Umum Penatalaksanaan
1. Pengobatan AR harus didasarkan pada keputusan bersama antara pasien dengan reumatologis. Pasien tak hanya diberikan penjelasan tentang pilihan terapi yang dapat dipergunakan dan alasan-alasan dipergunakan suatu pendekatan terapi tertentu dengan menimbang keuntungan dan kerugian, tetapi pasien hendaknya juga diberikan peran dalam menetapkan pilihan terapi mana yang akan dipilih. Perbaikan 2014 juga merekomendasikan keterlibatan petugas kesehatan profesional, khususnya spesialis nurse.
2. Sasaran utama pengobatan pasien-pasien AR adalah memperpanjang selama mungkin kualitas hidup yang baik dengan mengatasi keluhan, mencegah kerusakan struktural, menormalkan fungsi dan kehidupan sosialnya dan aktivitas terkait pekerjaan
4. Pengobatan diarahkan melalui penilaian aktivitas penyakit dan disesuaikan berdasarkan hal tersebut untuk mencapai keberhasilan pengobatan yang
optimal
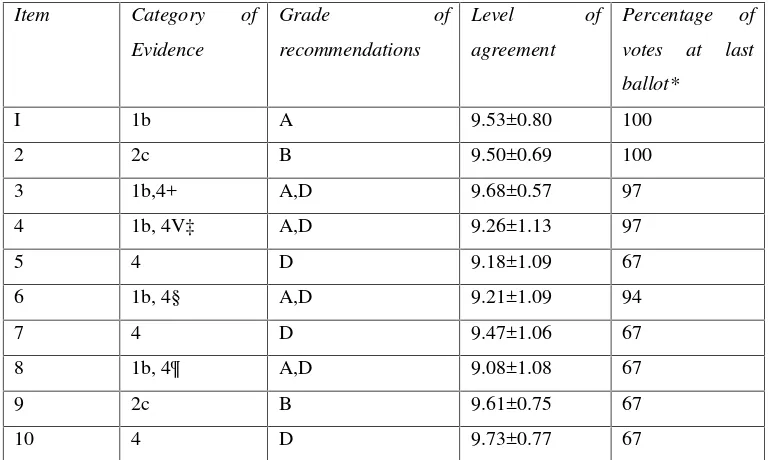
[image:11.595.133.519.270.500.2]Selanjutnya ada 10 rekomendasi dari T2T dengan perbaikan 2014 terkait target penatalaksanaan. Dimana sebelumnya akan dijelaskan bukti, rekomendasi, persetujuan dan pengambilan suara terhadap 10 item tersebut melalui tabel berikut.
Tabel 3.Evidence, grade of recommendation, agreement and votes for each of the recommendations (as pertinent)(9)
Item Category of
Evidence
Grade of
recommendations
Level of
agreement
Percentage of
votes at last
ballot*
I 1b A 9.53±0.80 100
2 2c B 9.50±0.69 100
3 1b,4+ A,D 9.68±0.57 97
4 1b, 4V‡ A,D 9.26±1.13 97
5 4 D 9.18±1.09 67
6 1b, 4§ A,D 9.21±1.09 94
7 4 D 9.47±1.06 67
8 1b, 4¶ A,D 9.08±1.08 67
9 2c B 9.61±0.75 67
10 4 D 9.73±0.77 67
Sebagian besar item membutuhkan hanya satu suara dan tidak menjalani lebih dari dua
votings.
† 1b untuk bukti bahwaaktivitas rendah-penyakit adalah target pengobatan yang baik, tapi 4
karena pendapat ahli bahwa itu adalah tujuan alternatif untuk remisi.
‡ 1b untuk bukti bahwa penggunaan penilaian penting dibandingkan dengan
perawatan rutin, tetapi tidak ada penelitian besar telah membandingkan penilaian yang
termasuk jumlah sendi
dengan beberapa yang tidak; Oleh karena itu 4 untuk menghitung bagian sendi.
§1b untuk kebutuhan untuk menggunakan penilaian , 4 untuk beberapa komponen waktu
disebutkan.
¶1b untuk penyesuaian biasa yang sebagian besar dilakukan setiap tiga bulan, tapi 4 untuk
jadwal disebutkan, karena tidak ada perbandingan antara penyesuaian pada titik waktu yang
Sasaran Penatalaksanaan
1. Sasaran utama pengobatan AR adalah suatu kondisi remisi klinis. Remisi klinis secara konsisten telah menunjukkan hasil yang lebih baik daripada kondisi aktivitas penyakit lainnya, bahkan aktivitas low disease. Sementara itu juga, dua studi menargetkan DAS28 <2.6 dibandingkan dengan konvensional bukan DAS28, satu pihak dengan AR dini dan satu pihak AR yang telah berlangsung, menunjukkan keuntungan yang signifikan menargetkan kondisi ini. Meskipun hal ini sulit dicapai. Beberapa ahli menilai hal ini dengan frekuensi remisi yang diperoleh melalui suatu pengobatan.
2. Remisi klinis adalah tidak adanya keluhan dan tanda dari aktivitas keradangan penyakit. Meskipun hilangnya keradangan tidak dapat ditemukan pada seluruh sendi yang terkena, tetapi bengkaknya sendi pada 1 jari saja dapat merupakan remisi. Kadar CRP juga perlu diperhitungkan dalam menentukan adanya remisi.
3. Jika remisi total tidak dapat dicapai, aktivitas penyakit yang rendah dapat diterima sebagai sasaran terapi terutama pada pasien yang sudah lama menderita
4. Penggunaan cara penilaian aktivitas penyakit yang valid yang termasuk penilaian pada sendi diperlukan dalam praktek sehari-hari untuk mengarahkan cara pengobatan. Rekomendasi ini bergeser ke atas dari posisi
5. Pemilihan penilaian aktivitas penyakit dan nilai target harus dipengaruhi oleh komorbiditas, faktor pasien dan risiko terkait obat. Rekomendasi itu bergeser
dari posisi no. 9 tahun 2010 ke no.5. Sekali lagi, keputusan ini muncul atas dasar pemikiran dan keinginan untuk memberikan sesuatu yang lebih menonjol dan perhatian terhadap rekomendasi ini. Sejak kehadiran beberapa penyakit penyerta, seperti penyakit jantung berat, diabetes yang tidak terkontrol, atau gangguan fungsi ginjal atau hati, mungkin menghalangi upaya untuk mengubah arah pengobatan untuk mencapai target pengobatan utama, tujuan pengobatan mungkin harus berbeda pada pasien tersebut. Pengalaman serupa berkaitan dengan kontraindikasi atau aspek keselamatan; jika pasien menderita infeksi berulang, salah satu kemungkinan akan menahan diri dari intensifikasi terapi untuk menghindari risiko terapi berlebihan. Dengan demikian, secara keseluruhan, rekomendasi ini berkaitan terhadap pendekatan personal dari strategi pengobatan, mengingat semua faktor yang berhubungan dengan individu pasien.
6. Harus diperoleh data tentang aktivitas penyakit yang dicatat secara regular, mungkin setiap bulan pada pasien yang mempunyai aktivitas tinggi/sedang atau lebih jarang ( misal setiap 6 bulan) pada pasien dengan aktivitas penyakit rendah atau remisi. Perubahan terhadap rekomendasi ini hanya terkait perpindahan ke no.6 dari no.5 tahun 2010. Perubahan lain terkait
pernyataan “3-6 bulan” untuk kontrol pada pasien dengan aktivitas penyakit
berkelanjutan belum jelas, 3 atau 6 bulan mungkin dianggap sebagai persyaratan mutlak minimum.
7. Perubahan struktural dan gangguan fungsional serta komorbiditas harus dipertimbangkan ketika membuat keputusan klinis, selain menilai aktivitas penyakit. Penambahan kata “komorbiditas” kedalam rekomendasi T2T 2014
dengan perbaikan, adalah untuk memberi penegasan pentingnya mempertimbangkan komorbiditas didalam membuat keputusan klinis. Harus diingat bahwa gangguan fungsional pada pasien dengan AR mungkin tidak hanya disebabkan karena penyakit sendi tetapi juga konsekuensi dari penyakit penyerta; memang, bahkan pada pasien dengan remisi ketat mungkin mengalami skor cacat yang tinggi sebagai akibat dari komplikasi penyakit lain.
8. Sampai sasaran pengobatan yang diinginkan tercapai, obat-obatan hendaknya disesuaikan minimal setiap 3 bulan. Berbagai uji klinik menunjukkan bahwa manfaat klinik maksimal suatu pengobatan biasanya diperoleh setelah 3 bulan. Dengan demikian jika pasien tidak memperoleh minimal aktivitas penyakit rendah dalam 3 bulan sejak awal terapi, maka terapi perlu ditinjau ulang.
9. Sasaran pengobatan yang diinginkan harus dipertahankan sepanjang perjalanan sisa penyakit. Rekomendasi ini didasarkan pada pengamatan bahwa berhentinya kerusakan sendi dan perbaikan dari fungsi fisik tergantung dari pemeliharaan kondisi remisi klinis. Aspek kepatuhan terhadap terapi juga harus dipertimbangkan karena ketidakpatuhan akan membuat pasien mengalami flare hingga empat kali lebih sering daripada pasien yang patuh. 10.Ahli rematologi harus melibatkan pasien dalam menetapkan target
pengobatan dan strategi untuk mencapai target tersebut. Rekomendasi tidak hanya telah disederhanakan, tetapi peran proaktif sekarang ditugaskan ke ahli
rematologi (sebelumnya: ’di bawah pengawasan ahli rematologi’). Tidak
dengan pasien, di sejalan dengan informasi masing-masing pada penyakit dan manfaat dan risiko dari berbagai terapi. Memang, pasien memiliki berbagai keyakinan yang berkaitan dengan terapi DMARD dan komunikasi yang tepat memungkinkan pasien untuk membuat keputusan. Selain itu, kepatuhan terhadap pengobatan telah jelas terbukti tergantung pada tingkat informasi dan interaksi yang baik dengan rheumatologist tersebut. Dalam konteks ini, juga harus menegaskan bahwa pasien dengan AR memerlukan perawatan multidisiplin dan bahwa di banyak negara perawat praktisi /spesialis atau profesional kesehatan lainnya mengambil peran yang sangat penting dalam memberikan informasi dan pengelolaan pasien. Menawarkan perawatan yang tersedia, atau mencoba untuk membangun itu, juga merupakan bagian dari peran keseluruhan ahli rematologi tersebut. Item ini inheren terdiri dari semua aspek rekomendasi saat ini, seperti pengaturan target terapi, sarana evaluasi penyakit, obat yang dipilih dan terapi non-medis termasuk risiko mereka, fokus pada komorbiditas dan faktor pasien lainnya, tindak lanjut semua proses ini harus dipertimbangkan ketika ahli rematologi 'melibatkan' pasien. Memang, suatu tantangan untuk menjelaskan kepada pasien yang aktivitas penyakitnya telah meningkat secara signifikan dan bahwa terapi harus diintensifkan-dan rekomendasi ini dan terutama mereka versi pasien mungkin akan membantu untuk tujuan ini. Program edukasi yang mendukung proses ini perlu disebarluaskan. (2,9-14)
Penatalaksanaan
Edukasi
Latihan/Program Rehabilitasi
Pada saat diagnosis AR ditegakan maka program latihan fisik aerobik bisa direkomendasikan. Latihan fisik harus disesuaikan secara individual berdasarkan kondisi penyakit dan komorbiditas yang. Latihan aerobik dapat dikombinasikan dengan latihan penguatan otot (regio terbatas atau menyeluruh), dan latihan untuk kelenturan, koordinasi dan kecekatan tangan serta kebugaran tubuh
Mengurangi nyeri dalam jangka pendek yaitu terapi fisik TENS (transcutaneous electrical nerve stimulation) dan laser kekuatan rendah. Terapi lain adalah kombinasi parafin (termoterapi) dan latihan aktif. Penggunaan ultrasound, muscular electro stimulation danmagnetotherapymasih belum cukup bukti untuk bisa digunakan secara rutin, tetapi bisa dipertimbangkan pada kasus-kasus tertentu yang tidak respon dengan terapi lainnya
Pada penderita AR stadium lanjut perlu diberi penjelasan tentang cara-cara proteksi sendi. Penggunaan alat bantu perlu dipertimbangkan pada penderita yang memiliki keterbatasan dalam melakukan aktivitas sehari-hari. Pada periode inflamasi aktif maka ortotik statis dapat digunakan (pertama selama sehari penuh dan sesudahnya hanya pada malam hari. Kegunaannya seharusnya dievaluasi secara periodik, dan ortotik yang tidak memberi manfaat sebaiknya tidak digunakan. Upaya terapi psikologis (misalnya relaksasi, mengatasi stress dan memperbaiki pandangan hidup yang positif) dapat membantu pasien AR menyesuaikan hidup dengan kondisi mereka.(1,3-6,16)
Pilihan Pengobatan
Disease Modifying Anti Rheumatic Drugs(DMARDs)
Obat-obatan yang mempengaruhi proses perjalanan AR disebut sebagai “Slow Acting Anti Rheumatic Drugs” (SAARD) atau dikenal DMARDs. memiliki
bulan pengobatan kecuali agen biologik yang efeknya lebih awal. Ada dua cara pendekatan pemberian DMARDs pada pasien AR. Pertama, DMARDs tunggal yang dimulai dari saat yang sangat dini. Pendekatan ini didasarkan pada pemikiran bahwa destruksi sendi pada AR terjadi pada masa dini penyakit. Kedua, DMARDs kombinasi dua atau lebih secara simultan seperti penggunaan obat-obatan imunosupresif pada penyakit keganasan.
Prinsip penggunaan DMARDs :
1. Semua AR yang diagnosisnya sudah tegak harus mendapatkan DMARDs sedini mungkin kecuali ada kontra indikasi. Idealnya dalam waktu 3 bulan sejak timbulnya gejala.
2. Penggunaan DMARD pada pasien yang hamil. Sebagian besar pasien AR akan membaik selama kehamilan. Tetapi kemudian terdapat risiko terjadi kekambuhan pada saat postpartum. Tidak didapatkan peningkatan kejadian abortus atau kematian ibu hamil dengan AR. Sebagian besar obat-obat yang digunakan pada pengobatan AR (DMARDs) belum terbukti keamananya sehingga tidak bisa diberikan pada kehamilan. Studi pada pasien SLE, klorokuin dan azatioprin dapat diberikan pasien yang hamil sehingga obat tersebut dapat dipertimbangkan untuk diberikan pada pasien AR yang hamil. Kortikosteroid merupakan obat yang dapat dipertimbangkan untuk digunakan pada wanita hamil dengan AR, tetapi perlu penilaian lebih cermat mengenai manfaat dan risikonya sebelum memberikan obat ini.
3. Pemilihan jenis DMARDs ditentukan oleh 3 faktor
a. Faktor obat: efektivitasnya, kemudahan pemberian, sistem monitoring, waktu yang diperlukan sampai obat memberikan khasiat, kemungkinan efek samping dan yang tidak kalah penting adalah biaya pengobatan. b. Faktor pasien: kepatuhan pasien, komorbiditas, beratnya penyakit dan
kemungkinan prognosisnya.
Memulai dan menghentikan DMARDs
• Sebelum memulai pengobatan dengan DMARDs harus dilakukan pemeriksaan untuk menyingkirkan adanya TB. (tes tuberculin dan foto toraks; jika ada keraguan dapat dikonsulkan dengan bagian paru).
• Pertimbangkan pengobatan jangka pendek dengan glukortikoid (oral, intramuskular atau intra-artikular) untuk memperbaiki gejala secara cepat pada pasien AR baru terdiagnosa jika mereka belum menerima glukokortikoid sebagai bagian dari terapi kombinasi DMARD.
• Pada pasien dengan recent onset RA yang menerima terapi kombinasi DMARD dan yang bertahan dengan hasil yang memuaskan, kurangi dosis obat dengan hati-hati ke tingkat yang masih dapat mempertahankan kontrol penyakit.
• Pada pasien AR yang baru terdiagnosis dimana terapi kombinasi DMARDs tidak dapat diberikan (misalnya karena penyakit penyerta atau kehamilan), mulai monoterapi DMARD dengan penekanan pada peningkatan yang cepat hingga dosis klinis efektif.
• Pada pasien AR yang kondisi penyakitnya stabil, kurangi dosis obat DMARD atau agen biologik dengan hati-hati. Segera kembali ke dosis penuh pada tanda pertama timbulnya kekambuhan.
• Ketika memulai obat baru untuk memperbaiki pengendalian penyakit pada rejimen pengobatan pasien AR, pertimbangkan mengurangi atau menghentikan obat DMARD yang sudah ada saat penyakit telah dapat dikendalikan.
• Pada setiap pasien AR dimana dosis obat DMARDs non biologik atau biologik sedang diturunkan atau dihentikan, harus disiapkan review dini.
• Mengingat banyaknya pertimbangan dalam pemberian DMARDs ini, maka konsultasi dengan konsultan reumatologi sangat penting pada saat akan memulai pemberian DMARDs (1,3,8,16-18)
agen biologik adalah: 1) Anti TNF-∂ (Etanercept, Infliximab, Golimumab).
TNF-∂adalah sitokin pro inflamasi yang diproduksi oleh makrofag dan limfosit dalam jumlah besar dalam sendi pasien AR yang diproduksi secara lokal oleh sel makrofag dan limfosit yang menginfiltrasi ruang sinovial. Sehingga hambatan TNF-∂ sangat berguna secara klinis dalam pengobatan AR; 2) Anti CD20 (Rituximab). Pentingnya peran sel limfosit B pada proses inflamasi kronik telah dibuktikan melalui observasi terapi dengan antibodi monoklonal terhadap marker sel B, CD 20, menyebabkan deplesi yang cepat dari limfosit B, penurunan titer serum faktor reumatoid, dan perbaikan parsial tanda dan gejala peradangan; 3) Anti IL-6R (Tocilizumab). Sitokin IL-1 dan TNF memainkan peran penting untuk memicu sel pannus menghasilkan kolagen dan enzim proteolitik yang merusak tulang rawan secara lokal dan menghambat pembentukan molekul matrik baru. Dua sitokin tersebut bersama IL-6 juga berperan dalam dimineralization dari tulang yang berperan dalam aktivasi osteoklast yang berakumulasi pada daerah lokal resorpsi tulang, sehingga hambatan terhadap IL-6 ini dapat memberikan hasil yang baik dalam pengelolaan AR. Dan beberapa yang belum beredar di Indonesia yaitu, anti CTLA-4 (abatacept), anti TNF-∂ (adalimumab, certolizumab), anti IL-1(anakinra) dan tofacitinib (1,3-6,8)
Kortikosteroid. Kortikosteroid oral dosis rendah/sedang ( dosis rendah <7,5 mg/hari dan sedang 7,5-30 mg/hari) bisa menjadi bagian dari pengobatan AR. Hindari pemberian bersama OAINS sambil menunggu efek terapi dari DMARDS. Kortikosteroid diberikan dalam jangka waktu sesingkat mungkin dan dosis serendah mungkin yang dapat mencapai efek klinis. Pemberian kortikosteroid bersama DMARDs dapat menurunkan LED dan CRP lebih cepat, meningkatkan fungsi mobilisasi serta mengurangi progresi erosi sendi (1,3-6,19)
Tabel 4. DMARDs yang dipergunakan pada AR (1,3,8)
DMARDs Mekanisme Dosis Efektiv
itas
Efek
samping
Persiapan
monitoring
Kloroquin Menghambat lisosom
dan pelepasan IL-1 6,5
mg/kgbb/h
ari
(200-400 mg)
+ Jarang,
kerusakan
makula
Pemeriksaan mata
pada awal
pengobatan,
selanjutnya setiap 1
tahun
Sulfazalasin Menghambat
angiogenesis dan
migrasi PMN
2x500
mg/hari
ditingkatka
n sampai
3x1000 mg
++ Supresi
sumsum
tulang
Awal pengobatan:
G6PD, darah perifer
tiap 4 minngu
selama 3 bulan
selanjutnya tiap 1
bulan, fungsi hati di
cek 1 bulan
selanjutnya tiap 3
bln
Metotreksat Menurunkan
kemotaksis PMN dan
pengaruhi sintesa
DNA
7,5–25
mg/mingg u +++ Fibrosis hati, pneumonia interstisiel dan supresi sumsum tulang
Awal: rontgen
thorak, fungsi hati,
darah tepi lengkap,
kreatinin.
Selanjutnya darah
tepi dan fungsi hati
tiap bulan
Leflunomide Menghambat enzim
dihidroorotat
dehidrogenase,
sehingga pembelahan
sel limfosit T auto
reaktif menjadi
terhambat
Loading
dose 100
mg/hari
selama 3
hari, selanjutnya 20 mg/hari +++ Diare,alop ecia,rash, sakit kepala, secara teoritisberi siko infeksi karena imunosupr esi
Darah tepi lengkap,
fungsi hati dan
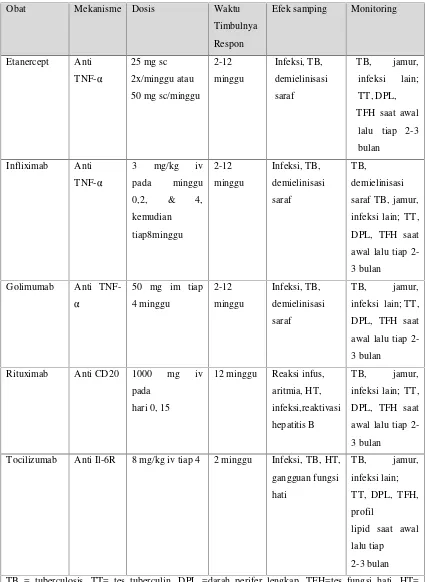
Tabel 4. DMARD Biologik untuk pengobatan Artritis Reumatoid (1,3,8)
Obat Mekanisme Dosis Waktu
Timbulnya
Respon
Efek samping Monitoring
Etanercept Anti
TNF-α
25 mg sc
2x/minggu atau
50 mg sc/minggu 2-12
minggu
Infeksi, TB,
demielinisasi
saraf
TB, jamur,
infeksi lain;
TT, DPL,
TFH saat awal
lalu tiap 2-3
bulan
Infliximab Anti
TNF-α
3 mg/kg iv
pada minggu
0,2, & 4,
kemudian tiap8minggu 2-12 minggu Infeksi, TB, demielinisasi saraf TB, demielinisasi
saraf TB, jamur,
infeksi lain; TT,
DPL, TFH saat
awal lalu tiap
2-3 bulan
Golimumab Anti
TNF-α
50 mg im tiap
4 minggu 2-12 minggu Infeksi, TB, demielinisasi saraf
TB, jamur,
infeksi lain; TT,
DPL, TFH saat
awal lalu tiap
2-3 bulan
Rituximab Anti CD20 1000 mg iv
pada
hari 0, 15
12 minggu Reaksi infus,
aritmia, HT,
infeksi,reaktivasi
hepatitis B
TB, jamur,
infeksi lain; TT,
DPL, TFH saat
awal lalu tiap
2-3 bulan
Tocilizumab Anti Il-6R 8 mg/kg iv tiap 4 2 minggu Infeksi, TB, HT,
gangguan fungsi
hati
TB, jamur,
infeksi lain;
TT, DPL, TFH,
profil
lipid saat awal
lalu tiap
2-3 bulan
TB = tuberculosis, TT= tes tuberculin, DPL =darah perifer lengkap, TFH=tes fungsi hati, HT=
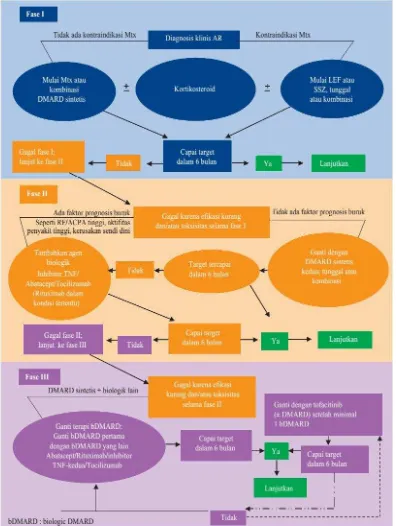
Gambar 2. Rekomendasi penggunaan DMARD sintetis dan biologik pada pasien AR (bDMARD = biologic DMARD) (1,3,8).
dirujuk juga jika didapatkan ruptur tendon, kompresi saraf dan stress fracture. (1,3-6,20).
Pemantauan Pengobatan
Pengobatan pasien AR memerlukan pemantuan aktivitas penyakit yang baik melalui evaluasi klinis maupun laboratorium dengan menggunakan skor sepertiDisease Aktivity Score28 (DAS28) atau kriteria remisi dari ACR 1987. Pengukuran LED atau CRP merupakan kunci untuk pemantauan penyakit. (1,2,9,20)
Tabel 6. Nilai ambang batas aktivitas penyakit Artritis Reumatoid berdasarkan nilaiDisease Aktivity Score(DAS28) (1)
Aktivitas penyakit Nilai DAS28-LED Nilai DAS28-CRP
Remisi ≤ 2,6 ≤ 2,3
Rendah ≤ 3,2 ≤ 2,7
Sedang > > 3,2 s/d≤ 5,1 >2,7 s/d≤ 4,1
Tinggi > 5,1 > 4,1
Kriteria AR menurut ACR 1987 dikatakan dalam remisi klinis apabila : 1. Lama keluhan kaku sendi tidak lebih dari 15 menit
2. Tanpa keluhan kelelahan 3. Tanpa keluhan nyeri sendi
4. Tanpa adanyatenderness atau nyeri gerak sendi 5. Tanpa ada pembengkakan jaringan sekitar sendi
6. LED (cara Westergren) kurang dari 20 mm pada pria dan kurang dari 30 mm pada wanita
Disebut remisi bila memenuhi 5 atau lebih kriteria diatas dan berlangsung selama 2 bulan atau lebih secara terus-menerus (1,20).
Daftar pustaka
[image:23.595.113.520.332.438.2]2. Smolen Josef S, Aletaha Daniel, Bijlsma Johannes W J, Breedveld Ferdinand C, Boumpas Dimitrios, Burmester Gerd et al. Treating rheumatoid arthritis to target: recommendations of an international task force. Ann Rheum Dis 2010;69:631–637
3. Daud Rizasyah. Artritis Reumatoid. Dalam: Sudoyo AW, Setiyohadi B, Alwi I, Simadibrata MK, Setiati S, eds. Buku Ajar Ilmu Penyakit Dalam. Edisi 5. Jakarta: Internal Publishing 2010;pp.1184-1191
4. Hellmann David B., Imboden John B. Rheumatoid Arthritis In Current Medical Diagnosis and Treatment 52nd Edition. New York:The McGraw-Hill Companies, Inc 2013;pp.826-831
5. Longo Dan L, Kasper Dennis L, Jameson J. Larry, et al. Rheumatoid Arthritis in Harrison’s Principles of Internal Medicine 18th edition. New York:The McGraw-Hill Companies, Inc 2012; pp.314
6. Scott David L, Wolfe Frederick, Huizinga Tom W J. Rheumatoid arthritis. Lancet 2010; 376: 1094–1108
7. Barnabe Cheryl, Xiong Juan, Pope Janet E., Boire Gilles, Hitchon Carol, Haraoui Boulos, Thorne J. Carter, et al. Factors associated with time to diagnosis in early rheumatoid arthritis.Rheumatol Int2014;34:85–92
8. Smolen Josef S, Landewé Robert, Breedveld Ferdinand C, Buch Maya, Burmester Gerd, Dougados Maxime, et al. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2013 update.Ann Rheum Dis2013;0:1–18 9. Smolen Josef S, Breedveld Ferdinand C, Burmester Gerd R, Bykerk Vivian,
Dougados Maxime, Emery Paul et al. Treating rheumatoid arthritis to target: 2014 update of the recommendations of an international task force. Ann Rheum Dis2015;0:1–13
10. Schoels Monika, Knevel Rachel, Aletaha Daniel, Bijlsma Johannes W J, Breedveld Ferdinand C, Boumpas Dimitrios T, Gerd Burmeste, et al. Evidence for treating rheumatoid arthritis to target: results of a systematic literature search.Ann Rheum Dis2010;69:638–643
international recommendations. Ann Rheum Dis 2011 doi: 10.1136/ard.2010.146662
12. Haraoui Boulos, Smolen Josef S, Aletaha Daniel, Breedveld Ferdinand C, Burmester Gerd, Codreanu Catalin , et al. Treating Rheumatoid Arthritis to Target: multinational recommendations assessment questionnaire.Ann Rheum Dis 2011. doi:10.1136/ard.2011.154179
13. Ruderman Eric M., Nola Kamala M., Ferrell Stanley, Sapir Tamar, Cameron Davecia R .Incorporating the Treat-to-Target concept in Rheumatoid Arthritis. JMCP2012; 18(9): 1-17
14. Harrold Leslie R, Reed George W, Harrington J Timothy, Barr Christine J, Saunders Katherine C, Gibofsk Allan. The rheumatoid arthritis treat-to-target trial: a cluster randomized trial within the Corrona rheumatology network. BMC Musculoskeletal Disorders2014,15:389
15. Marloes Vermeer, Hillechiena H Kuper, Hein J Bernelot Moens, Monique Hoekstra, Marcel D Posthumus, Piet LCM van Rie. Adherence to a treat-to-target strategy in early rheumatoid arthritis: results of the DREAM remission induction cohort.Arthritis Research & Therapy2012,14:R254
16. Bingham Clifton, Ruffing Victoria. Rheumatoid Arthritis Treatment. 2014. site by:www.hopkins-arthritis.org
17. Harrold Leslie R, Reed George W, Barr Christine J, Saunders Katherine C, Gibofsky Allan, Jeffrey Greenberg D, et al. The rheumatoid arthritis treat-to-target trial: a cluster randomized trial within the Corrona rheumatology network. BMC Musculoskeletal Disorders 2014, 15:389 doi:10.1186/1471-2474-15-389
18. Saeki Yukihiko, Matsui Toshihiro, Saisho Koichiro, Tohma Shigeto. Current
treatments of rheumatoid arthritis: from the ‘NinJa’ registry.Expert Rev. Clin.
Immunol2012;8(5):455–465
20. Lipsky Peter E. Rheumatoid Arthritis in Harrison’s Rheumatology second