Cocoa’s Shell(Theobroma cacao Linn.) as Natural Colorant of Cotton and Silk (The Effect of Fixative on the Depth of Shade and Fadeless as Revealed by
RGB Digital Image Processing Method)
Tirza Thea Lewita Sumasa*, A. Ign Kristijanto**, Hartati Soetjipto** *) Mahasiswa Program Studi Kimia Fakultas Sains dan Matematika
**) Dosen Program Studi Kimia Fakultas Sains dan Matematika Universitas Kristen Satya Wacana
Jalan Diponegoro 52-60 Salatiga – 50711 [email protected]
ABSTRACT
The objectives of this study are : firstly, to determine the effect of fixative types on the depth of shade color of cotton and silk which stained using extract of cocoa’s shell. Secondly, to determine the effect of fixative type on the fade proof color of cotton and silk toward washing. Thirdly, to determine the effect of fixative types on the fade proof color of cotton and silk toward washing and ironing. And all three were revealed by RGB digital image processing methode.
The result of this study showed that : 1) The use of “tunjung” as fixative on cotton produce the darkest color for all hue in comparison to verdigris and alum, respectively. While on silk, “tunjung” showed the darkest color for all hue, prusi and alum had the same depth of shade of color in red and grey hue, but brighter to alum in green and blue hue 2) Cotton and silk material showed fadeless of color toward washing treated for all hue with “tunjung” as fixative, on the contrary, verdigris showed fade of color in all hue exception in green hue on silk, and alum showed fade of color in red and grey hue on cotton, blue and grey hue on silk, 3) Cotton material showed fadeless of color toward washing and ironing for all hue with prusi as fixative, on the contrary “tunjung” and alum showed fadeless of color in red hue, while on silk didn’t showed fade of color exception in blue hue with alum as fixative.
Key words : cacao’s shell, natural colorant, cotton, silk, RGB
PENDAHULUAN
Warna menjadi daya tarik tersendiri yang berperan penting dalam industri tekstil karena warna memiliki kekuatan dalam menciptakan keindahan dan suasana tertentu. Bahan pewarna yang banyak digunakan selama ini adalah bahan pewarna sintetis/buatan yang bersifat karsinogenik dan beresiko tinggi terhadap kesehatan. Pewarna sintetis memang memiliki keunggulan dibandingkan pewarna alami yaitu komposisinya tetap, pilihan warnanya lebih bervariasi, penggunaannya jauh lebih
mudah, hasil pewarnaan lebih cerah, tersedia untuk semua jenis serat dan pada umumnya tahan luntur. Menghadapi abad yang berorientasi lingkungan ini, kekhawatiran akan dampak lingkungan dari zat warna sintetik non degradable yang merusak dan menganggu kesehatan membangkitkan kembali pemakaian zat warna alami. Zat warna alami diyakini lebih aman dari pada zat warna sintetis karena sifatnya yang non karsinogen dan teknologi pembuatan serta penggunaannya yang relatif sederhana menjadikannya sangat cocok untuk industri kecil dan menengah yang pada saat ini sedang digalakkan pemerintah untuk menunjang komoditi ekspor.
Salah satu cara pengelolaan limbah yaitu dengan menggunakan kembali limbah hasil industri sebagai bahan baku produk baru yang memiliki nilai tambah. Salah satu jenis industri yang dapat berkontribusi terhadap pencemaran lingkungan adalah industri coklat. Dalam pengolahan biji coklat, kulit biji coklat yang dipisahkan dari nibnya, memiliki porsi 11-13% kulit biji dari berat biji kering (Jurniati, 2013). Menurut pengamatan, sampai saat ini umumnya kulit biji coklat hanya digunakan sebagai kompos untuk pupuk tanaman, sebagai pakan ternak atau dibiarkan saja sehingga menyebabkan cemaran lingkungan. Menurut Sartini dkk (2007), biji kakao kaya akan komponen-komponen senyawa fenolik, antara lain: katekin, epikatekin, proantosianidin, asam fenolat, tanin dan flavonoid lainnya.
Pada umumnya zat pewarna atau colouring matter dalam jumlah besar berupa tanin. Tanin mengandung gugus-gugus hidroksil yang mempunyai pasangan elektron bebas sehingga dimungkinkan dapat membentuk kompleks dengan logam yang menyediakan orbital kosong (Dalzell dan Kerven, 1998 dalam Rosyda dan Ersam, 2010). Mahro et al. 2007 dalam Soetjipto dkk., 2012 melaporkan bahwa ekstrak biji coklat dapat mewarnai wool menjadi berwarna coklat.
Pemakai pewarna alam cenderung untuk menggunakan serat alami dan serat alami berasal dari 2 sumber yaitu tumbuhan dan hewan. Serat tumbuhan terdiri dari kapas, flax atau linen, rami (serat dari Boehmeria nivea), jute (serat dai Carchorus capsularis), hem (serat dari Cannabis sativa) dan lain-lain. Serat tumbuhan yaitu serat kapas (selulosa) dengan tenunan rapat, anyaman polos, lembut dan diberi sedikit kanji disebut mori. Sedangkan, serat hewan terdiri dari wol (bulu domba), sutera (fibroin ulat sutera), mohair (bulu kambing angora), dan alpaca (bulu ilama).
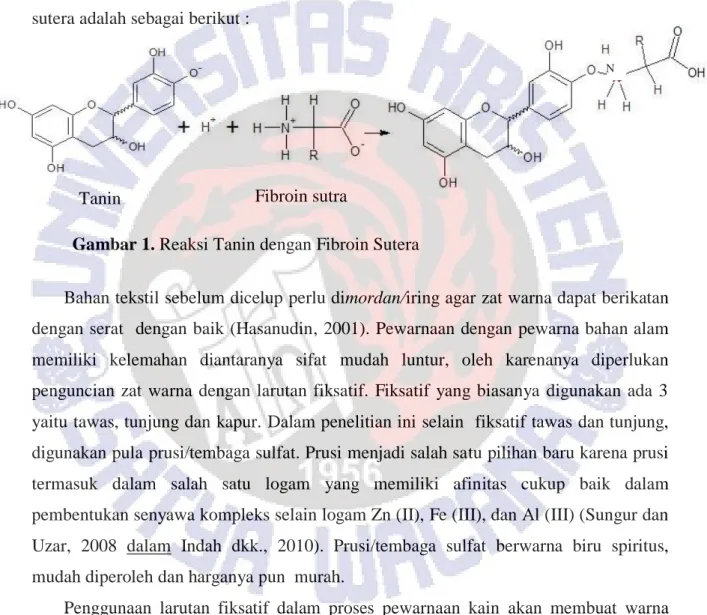
Serat selulosa dan sutra mempunyai sifat yang hampir sama diantaranya yaitu sangat higroskopis sehingga memungkinkan dapat menyerap zat warna dengan baik (Sewan, 1978 dalam Suheryanto, 2010). Semua serat hewan berbasiskan protein dan komposisi penyusun serat protein yang terbesar dari serat sutera adalah fibroin (76%) dan serisin sebagai perekat (22%) (Noerati dkk, 2013), sehingga yang berperan penting dalam reaksi pewarnaan adalah fibroin. Mekanisme reaksi antara tanin dengan fibroin sutera adalah sebagai berikut :
Bahan tekstil sebelum dicelup perlu dimordan/iring agar zat warna dapat berikatan dengan serat dengan baik (Hasanudin, 2001). Pewarnaan dengan pewarna bahan alam memiliki kelemahan diantaranya sifat mudah luntur, oleh karenanya diperlukan penguncian zat warna dengan larutan fiksatif. Fiksatif yang biasanya digunakan ada 3 yaitu tawas, tunjung dan kapur. Dalam penelitian ini selain fiksatif tawas dan tunjung, digunakan pula prusi/tembaga sulfat. Prusi menjadi salah satu pilihan baru karena prusi termasuk dalam salah satu logam yang memiliki afinitas cukup baik dalam pembentukan senyawa kompleks selain logam Zn (II), Fe (III), dan Al (III) (Sungur dan Uzar, 2008 dalam Indah dkk., 2010). Prusi/tembaga sulfat berwarna biru spiritus, mudah diperoleh dan harganya pun murah.
Penggunaan larutan fiksatif dalam proses pewarnaan kain akan membuat warna tidak mudah pudar (Ruwana, 2008). Oleh karena itu, perlu diketahui sejauh mana pengaruh fiksatif terhadap ketuaan dan ketahanan luntur warna limbah kulit coklat pada kain batik mori dan sutra dengan menggunakan metode pengolahan citra digital RGB (Red Green Blue), di mana nilai gelap terang ditentukan berdasarkan skala yang ditetapkan (0-1), yaitu semakin kecil nilainya (0) menandakan semakin gelap warnanya dan semakin besar menjadi semakin terang (1).
Gambar 1. Reaksi Tanin dengan Fibroin Sutera
Tanin Fibroin sutra
Berdasarkan latar belakang di atas, maka tujuan penelitian ini adalah :
1. Menentukan ketuaan warna alami ekstrak tanin kulit biji coklat yang difiksasi dengan fiksatif tunjung, tawas, dan prusi terhadap kain batik mori dan sutra. 2. Menentukan ketahanan luntur warna kain mori dan sutra yang telah difiksasi
terhadap pencucian.
3. Menentukan ketahanan luntur warna kain mori dan sutra yang telah difiksasi terhadap pencucian dan penyeterikaan.
METODE PENELITIAN Waktu dan Tempat
Penelitian dilaksanakan di Laboratorium Kimia Lingkungan, Program Studi Kimia, Fakultas Sains dan Matematika, Universitas Kristen Satya Wacana dari bulan Juli-November 2013.
Bahan
Sampel berupa limbah kulit biji coklat diperoleh dari PT. Ceres Bandung, kain mori, dan kain sutra. Sedang bahan kimiawi yang digunakan adalah soda abu Na2CO3,
tunjung FeSO4.7H2O, tawas KAl(SO4)2. 12 H2O, prusi CuSO4.5H2O, asam asetat
CH3COOH, dan detergen biasa (bukan detergen penghilang noda). Semua bahan
kimiawi yang digunakan adalah bahan dengan grade teknis. Piranti
Piranti yang digunakan antara lain neraca analitis, panci stainless steel, kompor, termometer, setrika listrik, kipas angin, pemindai (scanner) HP F2235, dan program MatLab 65.
Metode
Persiapan kain (mordanting) (Kusriniati, 2007)
Proses mordanting kain mori dilakukan dengan perendaman kain selama 12 jam dalam larutan detergen 2% (b/v) dilanjutkan dengan pembilasan. Setelah itu mori dicelup dalam larutan mendidih (campuran 8 g tawas dan 2 g soda abu/L air) selama 1 jam, kemudian didiamkan semalam, dibilas dan dikeringanginkan. Sementara untuk kain sutra dilakukan dengan larutan soda abu 1 gram/l yang dipanaskan hingga suhu 60°C. Kain sutra direndam dalam larutan dan dibolak-balik selama 5 menit. Selanjutnya kain diangkat dan dibilas dengan air dingin hingga bersih, kemudian dikeringanginkan
Ekstraksi kulit biji coklat
Kulit biji coklat dibungkus dengan kertas saring dan direbus dalam air dengan perbandingan 1:40 (gr/ml) hingga volumenya menjadi setengahnya. Kemudian ekstrak dipekatkan lagi hingga ½ volume awal, lalu didinginkan.
Pembuatan larutan fiksatif
Disiapkan 3 larutan fiksatif, yaitu tunjung 2%, tawas 5% dan prusi 2,5%. Masing-masing fiksator dilarutkan sampai homogen, didiamkan semalam kemudian disaring dan diambil filtratnya.
Pencelupan dalam larutan pewarna dan fiksatif
Kain dicelupkan ke dalam larutan pewarna selama 10 menit, lalu dikering anginkan hingga setengah kering. Pencelupan diulangi hingga 5 kali kemudian dikeringkan. Kain yang sudah diwarnai kemudian direndam dalam larutan fiksatif selama 10 menit, lalu dibilas dengan air kemudian dikeringkan.
Pengujian ketuaan warna dengan RGB (Padmasari, 2012)
Kain yang telah direndam dalam larutan fiksatif dan dikeringkan, dipindai dengan scanner HP F2235. Selanjutnya data hasil pindaian diproses dengan program MatLab 65 sehingga diperoleh data RGB.
Pengujian ketahanan luntur terhadap pencucian (Atikasari, 2005)
Kain hasil fiksasi dicuci sebanyak 5 kali dengan larutan detergen 1% dan dibilas dengan air panas (±60ºC) sebanyak 2 kali. Kain dicelup dalam larutan asam asetat 0,014% selama 1 menit dan dibilas ulang dengan air dingin, lalu dikeringkan. Dilakukan pemindaian data gambar yang diperoleh diberi kode sesuai perlakuan yang diberikan untuk kemudian dianalisa dengan program MatLab 65.
Pengujian terhadap penyeterikaan (Atikasari, 2007)
Kain dilapisi kain putih diatasnya, lalu diseterika selama 10 detik. Selanjutnya dilakukan pemindaian dan diproses dengan program MatLab 65.
ANALISA DATA
Data ketuaan warna kain dianalisa dengan menggunakan RAK (Rancangan Acak Kelompok) dengan 3 perlakuan dan 9 kali ulangan. Sebagai perlakuan adalah 3 jenis fiksatif, yaitu tunjung (2%), tawas (5%), dan prusi (2,5%), sedangkan sebagai kelompok adalah waktu proses kain.
Data ketahanan luntur warna kain (pencucian dan setrika) dianalisa dengan analisa Dwi Ragam dengan rancangan dasar RAK, 3 perlakuan dan 9 ulangan. Data hasil percobaan dianalisis menggunakan analisa sidik ragam dan uji F pada taraf nyata 5%. Untuk menguji beda antar perlakuan dilakukan uji beda nyata jujur (BNJ) dengan tingkat kebermaknaan 5% (Steel dan Torrie, 1980).
HASIL DAN PEMBAHASAN
Pengaruh berbagai jenis fiksatif terhadap ketuaan warna kain mori dengan pewarna limbah kulit biji coklat
Rataan ketuaan warna (±SE) kain mori dengan pewarnaan limbah kulit biji coklat antar berbagai fiksatif yang diekspresikan dengan nilai RGB dan Grey berkisar antara 0,3828 ± 0,0119 sampai dengan 0,9371 ± 0,0419 (Tabel 1).
Tabel 1. Rataan Ketuaan Warna (±SE) Kain Mori Hasil Pewarnaan Limbah Kulit Biji Coklat antar Berbagai Jenis Fiksatif
Jenis Fiksatif Tu 2% Pr 2,5% Tw 5% Red (R) w = 0,098 0,5412 ± 0,011 (a) 0,7105 ± 0,0375 (b) 0,9371 ± 0,0419 (c) Green (G) w = 0,017 0,4679 ± 0,0116 (a) 0,5495 ± 0,0110 (b) 0,6345 ± 0,017 (c) Blue (B) w = 0,017 0,3828 ± 0,0119 (a) 0,4601 ± 0,0109 (b) 0,5451 ± 0,017 (c) Grey (Gr) w = 0,042 0,4822 ± 0,0105 (a) 0,5511 ± 0,0267 (b) 0,6503 ± 0,0253 (c) Keterangan : *w = BNJ 5 %
*Tu = Tunjung; Pr = Prusi; Tw= Tawas;
*Angka-angka yang diikuti oleh huruf yang sama menunjukkan ketuaan warna yang sama, sedangkan angka yang diikuti oleh huruf yang berbeda menunjukkan antarperlakuan berbeda secara bermakna. Keterangan ini juga berlaku untuk Tabel 2-6
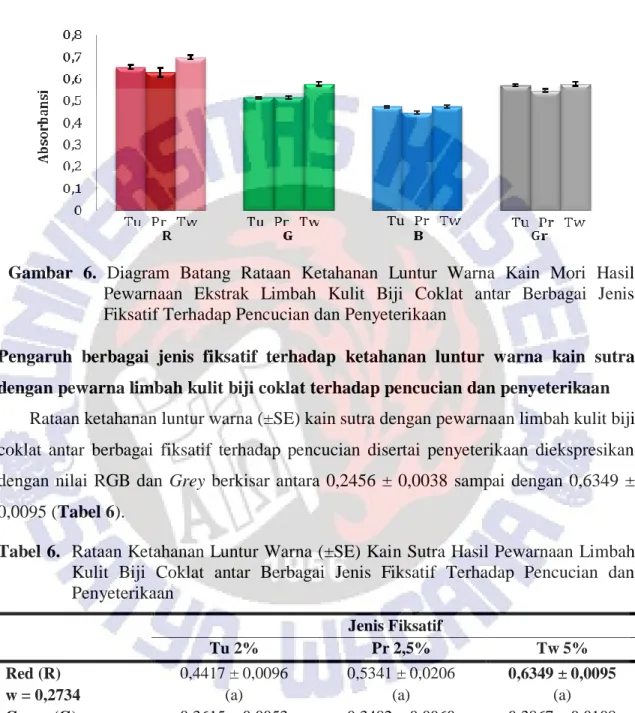
Tabel 1 menunjukkan kain mori dengan ketuaan warna yang paling gelap berturut-turut adalah dengan fiksatif tunjung, prusi dan selanjutnya tawas. Kain mori hasil pewarnaan ekstrak tanin dari limbah kulit biji coklat menunjukkan hasil serupa dengan penelitian Padmasari (2012) yang menggunakan limbah teh hijau dengan penambahan fiksatif, yaitu: tunjung > kapur > tawas (Gambar 2).
Gambar 2. Diagram Batang Rataan Ketuaan Warna Kain Mori Hasil Pewarnaan Limbah Kulit Biji Coklat antar Berbagai Jenis Fiksatif
Keterangan : R = Red/merah, G = Green /hijau, B = Blue/biru dan Gr = Grey/abu- abu. Keterangan ini berlaku juga untuk Gambar 4 – 8
Pengaruh berbagai jenis fiksatif terhadap ketuaan warna kain sutra dengan pewarna limbah kulit biji coklat
Rataan ketuaan warna (±SE) kain sutra dengan pewarnaan limbah kulit biji coklat antar berbagai fiksatif yang diekspresikan dengan nilai RGB dan Grey berkisar antara 0,2270 ± 0,0427 sampai dengan 1,0000 ± 0,0000 (Tabel 2).
Tabel 2. Rataan Ketuaan Warna (±SE) Kain Sutra Hasil Pewarnaan Limbah Kulit Biji Coklat antar Berbagai Jenis Fiksatif
Jenis Fiksatif Tu 2% Pr 2,5% Tw 5% Red (R) w = 0,013 0,4371 ± 0,0065 (a) 1,0000 ± 0,0000 (b) 0,9955 ± 0,0020 (b) Green (G) w = 0,021 0,3906 ± 0,0091 (a) 0,4661 ± 0,0063 (b) 0,6089 ± 0,0121 (c) Blue (B) w = 0,138 0,2270 ± 0,0427 (a) 0,3151 ± 0,0392 (b) 0,4805 ± 0,0086 (c) Grey (Gr) w = 0,103 0,4097 ± 0,0085 (a) 0,5521 ± 0,0525 (b) 0,6450 ± 0,0105 (b)
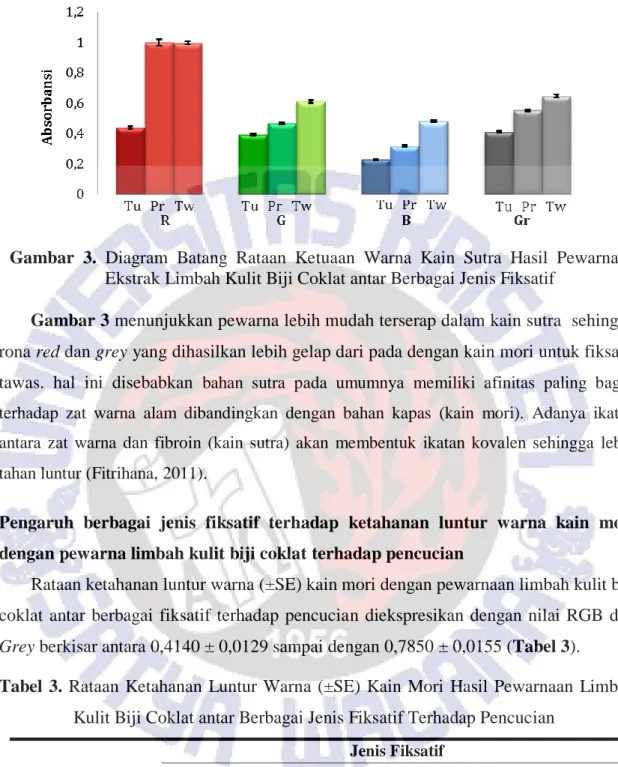
Dari Tabel 2, terlihat bahwa kain sutra dengan fiksatif tunjung mempunyai ketuaan warna paling gelap untuk semua rona (red, green, blue, dan grey), sedangkan prusi dan tawas memiliki ketuaan warna yang sama untuk rona red dan grey, sebaliknya berbeda (lebih terang) pada tawas untuk rona green dan blue (Gambar 3).
Gambar 3. Diagram Batang Rataan Ketuaan Warna Kain Sutra Hasil Pewarnaan Ekstrak Limbah Kulit Biji Coklat antar Berbagai Jenis Fiksatif
Gambar 3 menunjukkan pewarna lebih mudah terserap dalam kain sutra sehingga rona red dan grey yang dihasilkan lebih gelap dari pada dengan kain mori untuk fiksatif tawas. hal ini disebabkan bahan sutra pada umumnya memiliki afinitas paling bagus terhadap zat warna alam dibandingkan dengan bahan kapas (kain mori). Adanya ikatan antara zat warna dan fibroin (kain sutra) akan membentuk ikatan kovalen sehingga lebih tahan luntur (Fitrihana, 2011).
Pengaruh berbagai jenis fiksatif terhadap ketahanan luntur warna kain mori dengan pewarna limbah kulit biji coklat terhadap pencucian
Rataan ketahanan luntur warna (±SE) kain mori dengan pewarnaan limbah kulit biji coklat antar berbagai fiksatif terhadap pencucian diekspresikan dengan nilai RGB dan Grey berkisar antara 0,4140 ± 0,0129 sampai dengan 0,7850 ± 0,0155 (Tabel 3).
Tabel 3. Rataan Ketahanan Luntur Warna (±SE) Kain Mori Hasil Pewarnaan Limbah Kulit Biji Coklat antar Berbagai Jenis Fiksatif Terhadap Pencucian
Jenis Fiksatif Tu 2% Pr 2,5% Tw 5% Red (R) w = 0,0498 0,5939 ± 0,0085 (a) 0,6744 ± 0,0065 (b) 0,7850 ± 0,0155 (c) Green (G) w = 0,1158 0,4854 ± 0,0093 (a) 0,5509 ± 0,0118 (ab) 0,6211 ± 0,0182 (b) Blue (B) w = 0,0803 0,4140 ± 0,0129 (a) 0,4923 ± 0,0131 (b) 0,5599 ± 0,0183 (b) Grey (Gr) w = 0,0574 0,5100 ± 0,0103 (a) 0,5800 ± 0,0102 (b) 0,6661 ± 0,0187 (c)
Dari Tabel 3 terlihat bahwa fiksatif tunjung tidak mengalami kelunturan terhadap pencucian untuk semua rona pada kain mori, sedangkan pada prusi semua rona mengalami kelunturan dan tawas paling luntur untuk rona merah dan abu-abu. (Gambar 4).
Gambar 4. Diagram Batang Rataan Ketahanan Luntur Warna Kain Mori Hasil Pewarnaan Ekstrak Limbah Kulit Biji Coklat antar Berbagai Jenis Fiksatif Terhadap Pencucian
Pengaruh berbagai jenis fiksatif terhadap ketahanan luntur warna kain sutra dengan pewarna limbah kulit biji coklat terhadap pencucian
Rataan ketahanan luntur warna (±SE) kain sutra dengan pewarnaan limbah kulit biji coklat antar berbagai fiksatif terhadap pencucian diekspresikan dengan nilai RGB dan Grey berkisar antara 0,2053 ± 0,0065 sampai dengan 0,9000 ± 0,0068 (Tabel 4).
Tabel 4. Rataan Ketahanan Luntur Warna (±SE) Kain Sutra Hasil Pewarnaan Limbah Kulit Biji Coklat antar Berbagai Jenis Fiksatif Terhadap Pencucian
Jenis Fiksatif Tu 2% Pr 2,5% Tw 5% Red (R) w = 0,648 0,4730 ± 0,0134 (a) 0,7101 ± 0,0057 (b) 0,9000 ± 0,0068 (b) Green (G) w = 0,1058 0,3021 ± 0,0046 (a) 0,3644 ± 0,0049 (a) 0,5017 ± 0,0091 (b) Blue (B) w = 0,033 0,2053 ± 0,0065 (a) 0,2613 ± 0,0066 (b) 0,4415 ± 0,0069 (c) Grey (Gr) w = 0,037 0,2997 ± 0,0045 (a) 0,4006 ± 0,0054 (b) 0,5820 ± 0,0079 (c)
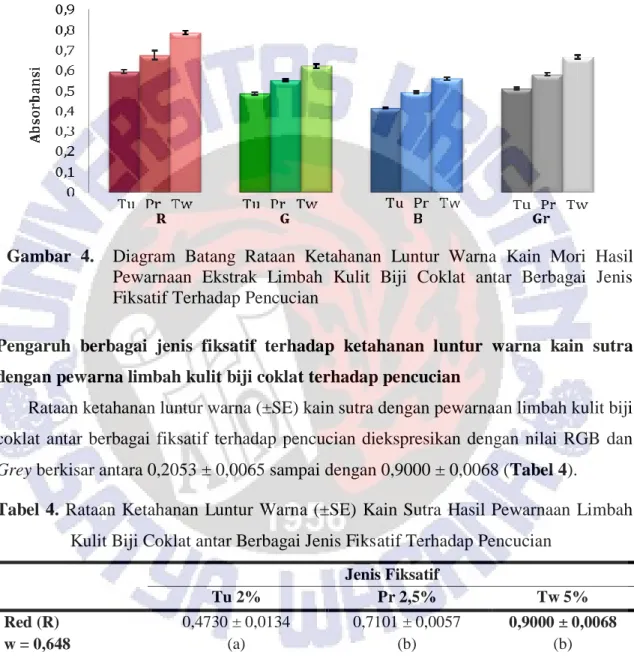
Tabel 4 menunjukkan warna kain sutra dengan fiksatif tunjung tidak mengalami kelunturan untuk semua rona. Sementara kain sutra dengan fiksatif prusi mengalami
kelunturan pada rona red, blue dan grey, dan kain sutra dengan fiksatif tawas paling luntur untuk rona blue dan grey (Gambar 5).
Gambar 5. Diagram Batang Rataan Ketahanan Luntur Warna Kain Sutra Hasil Pewarnaan Ekstrak Limbah Kulit Biji Coklat antar Berbagai Jenis Fiksatif Terhadap Pencucian
Pengaruh berbagai jenis fiksatif terhadap ketahanan luntur warna kain mori dengan pewarna limbah kulit biji coklat terhadap pencucian dan penyeterikaan
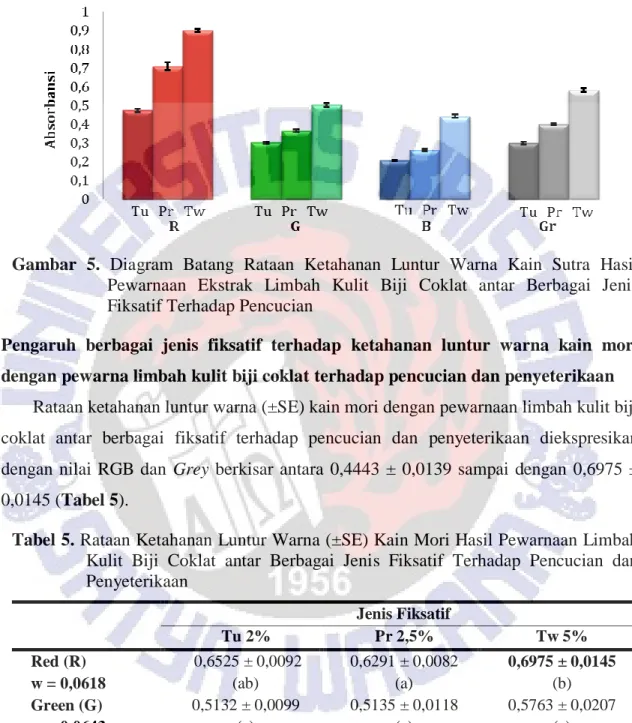
Rataan ketahanan luntur warna (±SE) kain mori dengan pewarnaan limbah kulit biji coklat antar berbagai fiksatif terhadap pencucian dan penyeterikaan diekspresikan dengan nilai RGB dan Grey berkisar antara 0,4443 ± 0,0139 sampai dengan 0,6975 ± 0,0145 (Tabel 5).
Tabel 5. Rataan Ketahanan Luntur Warna (±SE) Kain Mori Hasil Pewarnaan Limbah Kulit Biji Coklat antar Berbagai Jenis Fiksatif Terhadap Pencucian dan Penyeterikaan Jenis Fiksatif Tu 2% Pr 2,5% Tw 5% Red (R) w = 0,0618 0,6525 ± 0,0092 (ab) 0,6291 ± 0,0082 (a) 0,6975 ± 0,0145 (b) Green (G) w = 0,0643 0,5132 ± 0,0099 (a) 0,5135 ± 0,0118 (a) 0,5763 ± 0,0207 (a) Blue (B) w = 0,067 0,4720 ± 0,0127 (a) 0,4443 ± 0,0139 (a) 0,4721 ± 0,0202 (a) Grey (Gr) w = 0,0411 0,5700 ± 0,0105 (a) 0,5460 ± 0,0113 (a) 0,5760 ± 0,0195 (a)
Dari Tabel 5 terlihat bahwa warna kain mori dalam fiksatif prusi tidak mengalami kelunturan terhadap pencucian dan panas penyeterikaan untuk semua rona, sedangkan
fiksatif tunjung dan tawas mengalami kelunturan untuk rona merah (Gambar 6). Hal ini dikarenakan kain mori tahan terhadap suhu tinggi dan merupakan kain tahan panas setrika (Khayati (1997) dalam Padmasari, 2012).
Gambar 6. Diagram Batang Rataan Ketahanan Luntur Warna Kain Mori Hasil Pewarnaan Ekstrak Limbah Kulit Biji Coklat antar Berbagai Jenis Fiksatif Terhadap Pencucian dan Penyeterikaan
Pengaruh berbagai jenis fiksatif terhadap ketahanan luntur warna kain sutra dengan pewarna limbah kulit biji coklat terhadap pencucian dan penyeterikaan
Rataan ketahanan luntur warna (±SE) kain sutra dengan pewarnaan limbah kulit biji coklat antar berbagai fiksatif terhadap pencucian disertai penyeterikaan diekspresikan dengan nilai RGB dan Grey berkisar antara 0,2456 ± 0,0038 sampai dengan 0,6349 ± 0,0095 (Tabel 6).
Tabel 6. Rataan Ketahanan Luntur Warna (±SE) Kain Sutra Hasil Pewarnaan Limbah Kulit Biji Coklat antar Berbagai Jenis Fiksatif Terhadap Pencucian dan Penyeterikaan Jenis Fiksatif Tu 2% Pr 2,5% Tw 5% Red (R) w = 0,2734 0,4417 ± 0,0096 (a) 0,5341 ± 0,0206 (a) 0,6349 ± 0,0095 (a) Green (G) w = 0,0999 0,3615 ± 0,0053 (a) 0,3482 ± 0,0060 (a) 0,3867 ± 0,0108 (a) Blue (B) w = 0,055 0,2456 ± 0,0038 (a) 0,2535 ± 0,0061 (a) 0,3395 ± 0,0079 (b) Grey (Gr) w = 0,1121 0,4062 ± 0,0061 (a) 0,3803 ± 0,0066 (a) 0,4166 ± 0,0098 (a)
Tabel 6 menunjukkan kain sutra dalam berbagai fiksatif tidak mengalami kelunturan terhadap pencucian dan penyeterikaan untuk semua rona kecuali rona blue untuk fiksatif tawas (Gambar 7). Ramainas (1989), dalam Derisa (2012), menyatakan selain sifat afinitas, kain sutra dapat menyesuaikan diri terhadap suhu.
Gambar 7. Diagram Batang Rataan Ketahanan Luntur Warna Kain Sutra Hasil Pewarnaan Ekstrak Limbah Kulit Biji Coklat antar Berbagai Jenis Fiksatif Terhadap Pencucian dan Penyeterikaan
Ketahanan luntur warna kain mori maupun sutra terhadap pencucian maupun pencucian dan penyeterikaan tidak lepas dari peran fiksatif. Penggunaan larutan fiksatif dalam proses pewarnaan kain akan membuat warna tidak mudah pudar (Ruwana, 2008). Dalam penelitian ini, telah dilakukan pengukuran panjang gelombang maksimum masing-masing fiksatif, serta fiksatif yang diberi ekstrak tanin untuk menentukan pengaruhnya terhadap intensitas serapan UV-cahaya tampak dengan spektrofotometri UV-VIS (Tabel 7).
Tabel 7. Data Panjang Gelombang Maksimum Serapan UV-Cahaya Tampak Ekstrak Tanin dengan Penambahan Berbagai Fiksatif
Panjang
Gelombang (nm) Ekstrak (E) Tawas (Tw) E + Tw Prusi (Pr) E + Pr Tunjung (Tu) E + Tu 370 1,8182 0,1117 1,3307 0,0109 0,8286 1,8861 1,9957 385 1,5735 0,1120 1,1124 0,0146 0,6238 2,2007 2,3188 400 1,2976 0,1089 0,9333 0,0135 0,4605 1,4622 2,4685 600 0,3099 0,0918 0,2513 0,0933 0,1242 0,0345 0,2946 Tabel 7 menunjukkan fiksatif tunjung dengan penambahan ekstrak tanin mengalami kenaikan panjang gelombang maksimum (dari 385-400 nm), sementara fiksatif prusi mengalami penurunan panjang gelombang maksimum (600-370 nm), dan fiksatif tawas tidak mengalami perubahan panjang gelombang maksimum. Menurut
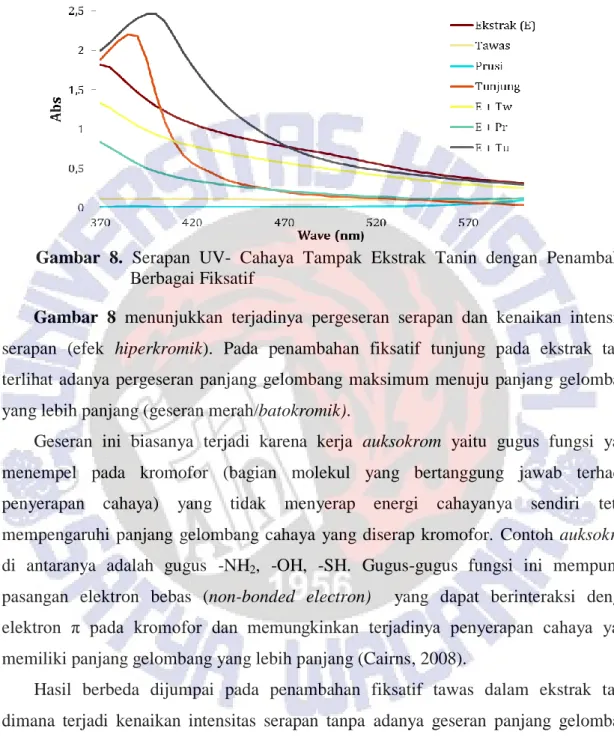
Cairns (2008), panjang gelombang maksimum dapat berubah ketika suatu senyawa mengalami ionisasi (Gambar 8).
Gambar 8. Serapan UV- Cahaya Tampak Ekstrak Tanin dengan Penambahan Berbagai Fiksatif
Gambar 8 menunjukkan terjadinya pergeseran serapan dan kenaikan intensitas serapan (efek hiperkromik). Pada penambahan fiksatif tunjung pada ekstrak tanin terlihat adanya pergeseran panjang gelombang maksimum menuju panjang gelombang yang lebih panjang (geseran merah/batokromik).
Geseran ini biasanya terjadi karena kerja auksokrom yaitu gugus fungsi yang menempel pada kromofor (bagian molekul yang bertanggung jawab terhadap penyerapan cahaya) yang tidak menyerap energi cahayanya sendiri tetapi mempengaruhi panjang gelombang cahaya yang diserap kromofor. Contoh auksokrom di antaranya adalah gugus -NH2, -OH, -SH. Gugus-gugus fungsi ini mempunyai
pasangan elektron bebas (non-bonded electron) yang dapat berinteraksi dengan elektron π pada kromofor dan memungkinkan terjadinya penyerapan cahaya yang memiliki panjang gelombang yang lebih panjang (Cairns, 2008).
Hasil berbeda dijumpai pada penambahan fiksatif tawas dalam ekstrak tanin dimana terjadi kenaikan intensitas serapan tanpa adanya geseran panjang gelombang maksimum. Dalam hal ini dapat diduga tidak adanya kerja auksokrom. Kenaikan intensitas serapan dipengaruhi oleh intensitas serapan ekstrak tanin tinggi. Selanjutnya pada penambahan fiksatif prusi dalam ekstrak tanin, intensitas serapan mengalami kenaikan disertai pergeseran panjang gelombang maksimum menuju panjang gelombang yang lebih pendek atau geseran biru (efek hipsokromik). Geseran biru biasanya terjadi jika senyawa dengan ausokrom basa terion, dan pasangan elektron
bebas tidak lagi dapat berinteraksi dengan elektron-elektron kromofor. Kenaikan intensitas serapan menunjukkan kenaikan terhadap fotosensitivitas. Semakin kuat fotosensitivitas maka semakin gelap warna yang dihasilkan, sebaliknya semakin rendah fotosensitivitas maka semakin cerah warna yang dihasilkan (Kombado, 2013).
Tanin mengandung gugus-gugus fenol, sehingga memiliki banyak pasangan elektron bebas yang dapat berikatan membentuk senyawa kompleks dengan logam seperti Fe(III), Cu (II), dan logam-logam transisi lainnya. Jika dilihat gugus OH -termasuk dalam ligan medan lemah dan Fe (III) memiliki bilangan koordinasi 6 sehingga menghasilkan ion kompleks [Fe(OH)6]3- dengan spin tinggi akibatnya
elektron-elektron akan mengisi kelima orbital d tanpa berpasangan terlebih dahulu. Ion logam Cu(II) mempunyai elektron terluar lebih banyak dari Fe(III), sehingga orbital kosong yang disediakan ion logam Fe(III) lebih banyak, akibatnya pasangan elektron bebas dari gugus OH pada tanin akan lebih mudah terikat. Rosyda dan Ersam (2010) menyatakan, ion logam yang paling banyak terkompleks dengan senyawa tanin adalah Fe(III) > Cu(II) > Zn(II).
KESIMPULAN DAN SARAN Kesimpulan
1. Kain mori dengan fiksatif tunjung menunjukkan warna yang paling gelap diikuti fiksatif prusi dan tawas. Sementara kain sutra dengan fiksatif tunjung menunjukkan ketuaan warna yang paling gelap untuk semua rona, sedangkan fiksatif prusi dan tawas memiliki ketuaan warna yang sama untuk rona merah dan abu-abu, namun lebih terang pada tawas untuk rona hijau dan biru.
2. Kain mori dan sutra dengan fiksatif tunjung tidak mengalami kelunturan terhadap pencucian untuk semua rona. Kain Mori pada fiksatif prusi mengalami kelunturan untuk semua rona, namun pada kain sutra rona hijau tidak luntur. Fiksatif tawas pada mori mengalami kelunturan pada rona merah dan abu-abu, sedangkan pada sutra luntur pada rona biru dan abu-abu.
3. Kain mori dengan fiksatif prusi tidak mengalami kelunturan terhadap pencucian dan panas penyeterikaan untuk semua rona, sebaliknya fiksatif tunjung dan tawas mengalami kelunturan untuk rona merah. Sedangkan kain sutra hanya mengalami kelunturan untuk rona biru dengan fiksatif tawas.
UCAPAN TERIMA KASIH
Terimakasih kepada segenap dosen, laboran dan staff Fakultas Sains dan Matematika, teristimewa kedua pembimbing untuk setiap bantuan dan perhatian yang diterima penulis. Ibunda dan adikku terkasih untuk doa dan kasih sayangnya, teman seperjuangan Maria, juga Stevan untuk bantuannya, dan semua pihak yang telah membantu penulis menyelesaikan penelitian ini, yang terakhir namun tidak akan terlupa, untuk Steven Santosa, terima kasih atas kesetiannya dan semangat yang ditularkan kepada penulis.
DAFTAR PUSTAKA
Atikasari, A., 2005. Kualitas Tahan Luntur Warna Batik Cap Di Griya Baik Larissa Pekalongan. Semarang : Universitas Negeri Semarang
Bogoriani, N.W., 2010. Ekstraksi Zat Warna Alami Campuran Biji Pinang, Daun Sirih, Gambir dan Pengaruh Penambahan KMnO4 terhadap Pewarnaan Kayu Jenis
Albasia. Jurnal Kimia 4(2) 125-134 ISSN 1907-9850. Bukit Jimbaran : Jurusan Kimia FMIPA Universitas Udayana
Cairns, Donald., 2008. Intisari Kimia Farmacy, Ed. 2. Jakarta : Penerbit Buku Kedokteran EGC
Derisa, 2012. Pengaruh Garam Terhadap Hasil Pencelupan Bahan Sutra. Skripsi. Padang: Universitas Negeri Padang.
Fessenden R. J. dan J. S. Fessenden. 1982. Kimia Organik Edisi Ketiga Jilid 1. Terjemahan Aloysius Handyana Pudjatmaka. Jakarta : Erlangga
Fitrihana, N., 2011. Teknik Eksplorasi Zat Pewarna Alam dari Tanaman di Sekitar Kita
Untuk Pencelupan Bahan Tekstil. Skripsi. Yogyakarta: Universitas Negeri
Yogyakarta.
Hamid, Tilani., D. Muhlis, 2005. Perubahan Sifat Fisika dan Kimia Kain Sutera Akibat Pewarna Alami Kulit Akar Pohon Mengkudu (Morinda citrifolia). Jurnal Teknologi : Edisi No. 2. Tahun XIX, 163-170 ISSN 0215-1685. Jakarta : Program Studi Teknik Kimia, Departemen Teknik Gas dan Petrokimia Fakultas Teknik Universitas Indonesia
Harborne, J.B. 1987. Metode Fitokimia Penuntun Cara Modern Menganalisis Tumbuhan. Bandung : Institut Teknologi Bandung
Hasanudin, 2001. Penelitian Penerapan Zat Warna Alam Dan Kombinasinya Pada Produk Batik Dan Tekstil Kerajinan (Contoh-contoh Warna). Yogyakarta : Balai Besar Litbang Industri Kerajinan dan Batik
Indah, U. R., I. Kris Murwani, dan D. Presetyoko, 2009/2010. Optimalisasi Ekstraksi Zat Warna pada Kayu Intsia bijuga dengan Metode Pelarutan. Prosiding Tugas Akhir semester Jurusan Kimia, Fakultas Matematika dan Ilmu Pengetahuan Alam. Surabaya : Institut Teknologi Sepuluh Nopember
Jurniati, 2013. Pola Sebaran Karakteristik Fisik Biji Kakao ( Theobroma Cacao L.) Berdasarkan Posisi Buah Pada Pohon. Makasar : Universitas Hasanudin
Kombado, A. R., 2013. Limbah Kerabang Telur Puyuh (Cortunix cortunix japonica) sebagai Pewarna Alami Kain Batik. (Pengaruh Jenis Fiksatif terhadap Ketuaan
dan Ketahanan Luntur Ditelaah dengan Metode Pengolahan Citra Digital RGB). Skripsi. Salatiga : Universitas Kristen Satya Wacana
Kusriniati, D., 2007. Pemanfaatan Daun Sengon (Albizia falcataria) sebagai Pewarna Kain Sutera menggunakan Mordan Tawas dengan Konsentrasi yang Berbeda pada Busana Camisol. Semarang : Universitas Negeri Semarang
Noerati, Gunawan, M. Iwan dan Atin S., 2013. Bahan Ajar Pendidikan dan latihan Profesi Guru (PLPG): Teknologi Tekstil Sekolah Tinggi. Teknologi Tekstil
Padmasari, A. Kumala., 2012. Limbah Teh Hijau sebagai Pewarna Alami Batik Tulis (Pengaruh Jenis Fiksatif terhadap Ketuaan dan Ketahanan Luntur Ditelaah dengan Metode Pengolahan Citra Digital RGB). Skripsi. Salatiga : Universitas Kristen Satya Wacana
Periskiana, R., 2011. Limbah Gergaji Kayu Suren (Toona sureni Merr.) Sebagai Pewarna Alami Batik Tulis (Pengaruh Jenis Fiksatif Terhadap Ketuaan Dan Ketahanan Luntur Ditelaah Dengan Metode Pengolahan Citra Digital RGB). Skripsi. Salatiga : Universitas Kristen Satya Wacana
Rosyda, A. Ika, dan T. Ersam, 2010. Peningkatan Kualitas Kayu (Instia bijuga) : Kompleksasi Logam Cu(II), Fe(III) Dan Zn(II) Oleh Senyawa Tanin. Surabaya : Jurusan Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam Institut
Teknologi Sepuluh Nopember
Ruwana, Iftitah, 2008. Pengaruh Fiksasi Terhadap Ketahanan Luntur Warna pada Proses Pencelupan Kain Kapas dengan Menggunakan Zat Warna dari Limbah Kayu Jati. Teknologi dan Kejuruan. Vol. 31, No.1
Sa’adah, Lailis, 2010. Isolasi dan identifikasi Senyawa Tanin dari Daun Belimbing (Averrhoa bilimbi L.). Malang : Fakultas Sains dan Teknologi Universitas Islam Negeri (UIN) Maulana Malik Ibrahim
Sartini., M. Natsir Djide., Gemini Alam., 2007. Ekstraksi Komponen Bioaktif ari Limbah Kulit Buah Kakao dan Pengaruhnya terhadap Aktivitas Antioksidan dan Antimikroba. Makasar : Universitas Hasanuddin
Soetjipto, H., A. Ign. Kristijanto, dan Y. Martono, 2012. Pemanfaatan Limbah Kulit Biji Kakao Sebagai Sumber Pewarna Alami Batik. Laporan Penelitian. Salatiga : Progdi Kimia, Fakultas Sains dan Matematika Universitas Kristen Satya Wacana Steel, R.G.D. and J.H.Torie, 1981. Principle and Procedures of Statistic A Biometrical
Approach, 2nd ed. Mc Graw-Hill International. Book Co, Kugakusha, Japan
Suheryanto, Dwi., 2010. Optimalisasi Celupan Ekstrak Daun Mangga pada Kain Batik Katun dengan Iring Kapur. Balai Besar Kerajinan Batik
Sutara, P. K., 2009. Jenis Tumbuhan sebagai Pewarna pada Beberapa Perusahaan Tenun di Gianyar. Jurnal Bumi Lestari, Volume 9 No. 2 hlm. 217 – 223.