POTENSI KULIT KACANG TANAH SEBAGAI ADSORBEN
ZAT WARNA REAKTIF CIBACRON RED
APRILIA SUSANTI
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
ABSTRAK
APRILIA SUSANTI. Potensi Kulit Kacang Tanah Sebagai Adsorben Zat Warna Reaktif Cibacron Red. Dibimbing oleh BETTY MARITA SOEBRATA dan MOHAMMAD KHOTIB.
Limbah industri merupakan masalah utama dalam pengendalian dampak lingkungan. Pengolahan limbah secara fisika dan kimia yang sudah ada sangatlah mahal dan dihasilkannya lumpur dalam jumlah yang besar. Penghilangan zat warna juga tidak dapat berlangsung secara optimum, zat warna tetap tinggal dalam kadar cukup tinggi di dalam air hasil olahannya. Oleh karena itu, metode adsorpsi dapat menjadi metode alternatif untuk mengatasi pencemaran zat warna yang ekonomis dan sederhana. Beberapa produk samping pertanian berpotensi sebagai adsorben, salah satunya adalah kulit kacang tanah.
Pada penelitian ini, kulit kacang tanah yang digunakan sebagai adsorben cibacron red yang telah dimodifikasi dengan asam sulfat 97%. Parameter yang diujikan adalah waktu adsorpsi, bobot adsorben, dan konsentrasi awal zat warna. Kondisi optimum yang diperoleh untuk adsorben tanpa modifikasi pada parameter adalah 45 menit, 1.0 g, dan 100 ppm. Kondisi optimum untuk adsorben modifikasi asam ialah 60 menit, 1.5 g, dan 150 ppm. Arang aktif yang digunakan sebagai pembanding kapasitas adsorpsi memiliki kondisi optimum sebagai berikut 60 menit, 3.0 g, dan 150 ppm. Pada pengujian larutan tunggal, kapasitas adsorpsi cibacron red oleh adsorben tanpa modifikasi, dengan modifikasi, dan arang aktif, berturut-turut sebesar 476.34, 8837.00, dan 3827.50 µg/g adsorben. Efisiensi penjerapan pada larutan tunggal berturut-turut sebesar 4.69, 87.14, dan 72.56%. Persen penurunan warna oleh ketiga jenis adsorben pada limbah industri tekstil, berturut-turut sebesar 2.03, 97.08, dan 51.65%. Hal ini menunjukkan bahwa adsorben modifikasi asam lebih efektif menjerap warna. Tipe isoterm yang dianut oleh ketiga jenis adsorben adalah isoterm Freundlich dengan linearitas >90%.
ABSTRACT
APRILIA SUSANTI. Potency of Peanut hulls as an Adsorbent Reactive Dyes Cibacron Red. Supervised by BETTY MARITA SOEBRATA and MOHAMMAD KHOTIB.
Industrial waste water is an important problem in the environment impact control. Physical and chemical waste processing are very expensive and produce sludge in the huge amount. The dyes removal also could not be going optimum, the dyes still in high content on the product processing water. Therefore, adsorption method could be an economical and simple alternative to solve caused by pollution. Some agriculture waste biomass can be used as adsorbent, such as peanut hull.
POTENSI KULIT KACANG TANAH SEBAGAI ADSORBEN
ZAT WARNA REAKTIF CIBACRON RED
APRILIA SUSANTI
Skripsi
sebagai salah satu syarat untuk memperoleh gelar Sarjana Sains pada
Departemen Kimia
DEPARTEMEN KIMIA
FAKULTAS MATEMATIKA DAN ILMU PENGETAHUAN ALAM
INSTITUT PERTANIAN BOGOR
Judul : Potensi Kulit Kacang Tanah sebagai Adsorben Zat Warna Reaktif Cibacron Red
Nama : Aprilia Susanti
NIM : G44204055
Menyetujui:
Pembimbing I, Pembimbing II,
Betty Marita Soebrata, S.Si, M.Si. Mohammad Khotib, S.Si. NIP 131 694 523 NIP 132 324 223
Mengetahui:
Dekan Fakultas Matematika dan Ilmu Pengetahuan Alam Institut Pertanian Bogor
Dr. drh. Hasim, DEA NIP 131 578 806
PRAKATA
Bismillahirrahmanirrahim…
Alhamdulillah, segala puji bagi Allah SWT karena atas rahmat dan karunia-Nya
penulis dapat menyelesaikan karya ilmiah ini. Karya ilmiah ini berjudul Potensi Kulit Kacang Tanah sebagai Adsorben Zat Warna Reaktif Cibacron Red, yang dilaksanakan pada bulan Mei sampai dengan Oktober 2008 bertempat di Laboratorium Kimia Fisik dan Lingkungan, IPB.
Penulis mengucapkan terima kasih kepada Ibu Betty Marita Soebrata, S.Si, M.Si. dan Bapak Mohammad Khotib, S.Si selaku pembimbing yang telah memberikan masukan dan pengarahan kepada penulis. Ungkapan terima kasih dihaturkan kepada Bapak, Mamah, Kak Irwan, Kak Shinta, Deky, dan Ria atas doa dan dukungannya. Ucapan terima kasih juga disampaikan kepada staf Departemen Kimia IPB, Ibu Ai, Bapak Nano, Bapak Mail, Bapak Eman, dan Bapak Didi atas bantuannya. Saya haturkan banyak terima kasih kepada Egih, Maipa, Ai, Kak Sari, Mba Lia, dan Kak Fahrizal atas kerja samanya selama ini. Penulis juga mengucapkan terima kasih kepada Ikhsan atas kebersamaan dan semangat selama menjalankan penelitian.
Akhir kata, penulis menyampaikan semoga karya ilmiah ini bermanfaat bagi pembaca. Amin.
Bogor, Januari 2009
Aprilia Susanti
RIWAYAT HIDUP
Penulis dilahirkan di Jakarta pada tanggal 12 April 1986 sebagai anak kedua dari empat bersaudara, putri dari pasangan Muhammad Husein dan Ratna Komala.
Tahun 2004 penulis lulus dari SMU Negeri 44 Jakarta dan memperoleh kesempatan melanjutkan studi di Departemen Kimia Fakultas Matematika dan Ilmu Pengetahuan Alam IPB melalui jalur Undangan Saringan Masuk IPB (USMI).
DAFTAR ISI
Halaman
DAFTAR TABEL ... vii
DAFTAR GAMBAR ... vii
DAFTAR LAMPIRAN ... vii
PENDAHULUAN ... 1
TINJAUAN PUSTAKA Kacang Tanah ... 1
Adsorpsi... 2
Isoterm Adsorpsi ... 2
Isoterm Adsorpsi Freundlich... 2
Isoterm Adsorpsi Langmuir... 3
Arang Aktif... 3
Modifikasi Adsorben ... 3
Zat Warna Reaktif ... 4
Cibacron Red ... ... 4
BAHAN DAN METODE Bahan dan Alat ... 4
Metode Penelitian ... 4
HASIL DAN PEMBAHASAN Panjang Gelombang Maksimum dan Pembuatan Kurva Standar ... 5
Kondisi Optimum Waktu Adsorpsi, Bobot Adsorben, dan Konsentrasi ... 6
Kondisi Optimum Adsorben Tanpa Modifikasi ... 6
Kondisi Optimum Adsorben Modifikasi Asam ... 6
Kondisi Optimum Arang Aktif ... 7
Adsorpsi Larutan Tunggal ... 8
Isoterm Adsorpsi ... 8
Adsorpsi Limbah Industri ... 9
SIMPULAN DAN SARAN Simpulan ... 10
Saran ... 10
DAFTAR PUSTAKA ... 10
DAFTAR TABEL
Halaman
1 Komposisi kimia kulit kacang tanah... 2
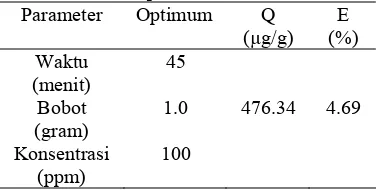
2 Kondisi optimum ATM... 6
3 Kondisi optimum AMA... 7
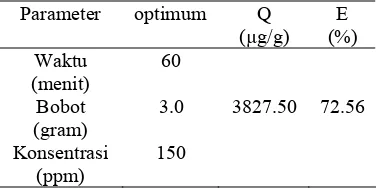
4 Kondisi optimum arang aktif... 7
DAFTAR GAMBAR
Halaman 1 Struktur cibacron red... 42 Kurva standar cibacron red ... 5
3 Perbandingan kapasitas adsorpsi cibacron red oleh adsorben tanpa modifikasi, modifikasi asam, dan arang aktif... 8
4 Perbandingan efisiensi penjerapan cibacron red oleh adsorben tanpa modifikasi, modifikasi asam, dan arang aktif... 8
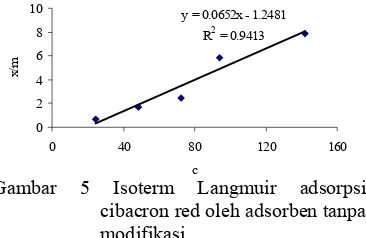
5 Isoterm Langmuir adsorpsi cibacron red oleh adsorben tanpa modifikasi... 8
6 Isoterm Freundlich adsorpsi cibacron red oleh adsorben tanpa modifikasi ... 9
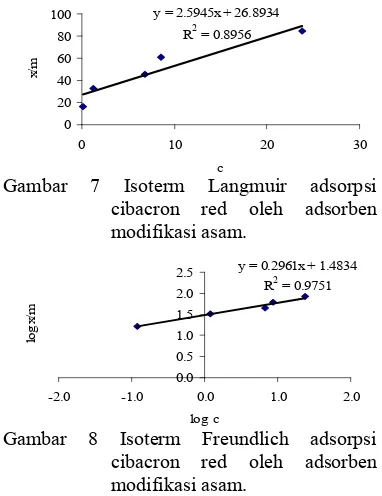
7 Isoterm Langmuir adsorpsi cibacron red oleh adsorben modifikasi asam ... 9
8 Isoterm Freundlich adsorpsi cibacron red oleh adsorben modifikasi asam ... 9
9 Isoterm Langmuir adsorpsi cibacron red oleh arang aktif ... 9
10 Isoterm Freundlich adsorpsi cibacron red oleh arang aktif ... 9
11 Konsentrasi warna limbah tekstil setelah dijerap masing-masing adsorben ... 10
12 Persen penurunan warna limbah tekstil setelah dijerap masing-masing adsorben. 10
DAFTAR LAMPIRAN
Halaman 1 Bagan alir penelitian ... 132 Penentuan panjang gelombang maksimum zat warna cibacron red ... 14
3 Kurva standar cibacron red pada panjang gelombang maksimum 517 nm... 14
4 Penentuan kondisi optimum adsorben tanpa modifikasi... 15
5 Analisis statistik kondisi optimum adsorben tanpa modifikasi…………... 16
7 Analisis statistik kondisi optimum adsorben modifikasi asam ………... 18 8 Penentuan kondisi optimum arang aktif... 19 9 Analisis statistik kondisi optimum arang aktif ... 20 10 Isoterm Langmuir dan Freundlich untuk adsorpsi cibacron red oleh adsorben tanpa modifikasi ... 21 11 Isoterm Langmuir dan Freundlich untuk adsorpsi cibacron red oleh adsorben
modifikasi asam... 22 12 Isoterm Langmuir dan Freundlich untuk adsorpsi cibacron red oleh arang aktif... 23 13 Penentuan konsentrasi warna dan persen penurunan warna untuk adsorpsi limbah
PENDAHULUAN
Limbah merupakan masalah utama dalam pengendalian dampak lingkungan. Zat warna adalah salah satu jenis polutan yang mengandung bahan beracun sehingga limbah yang dihasilkannya berbahaya bagi kesehatan manusia, baik yang terlibat langsung dengan kegiatan industri maupun yang berada di lingkungan sekitar perusahaan. Permenkes No. 173/Men.Kes/Per./VIII/1977 menunjuk-kan bahwa hanya 8 parameter yang digunamenunjuk-kan untuk evaluasi kualitas badan air, yaitu BOD, pH, klorida, amonia, detergen, fenol, besi, serta lemak dan minyak. Di antara kedelapan parameter tersebut, warna tidak diikutsertakan, padahal warna merupakan salah satu parameter yang penting sebagai indikator pencemaran.
Zat warna reaktif cibacron red sering dipakaiuntuk mewarnai serat kapas atau serat selulosa karena kualitas pencelupannya yang baik dan penggunaannya mudah. Zat warna ini termasuk dalam kelas azo (Manurung et al. 2004). Zat warna azo merupakan zat warna yang mempunyai sifat karsinogenik, membahayakan hewan air, tidak mudah terurai secara biologi, dan mencemari lingkungan melalui buangan limbah cairnya.
Pengolahan limbah secara fisika dan kimia yang sudah ada sangatlah mahal dan dapat memberi masalah lingkungan yang baru, yaitu dihasilkannya lumpur dalam jumlah yang besar. Terlebih lagi, penghilangan zat warna tidak dapat berlangsung secara optimum, zat warna tetap tinggal dalam kadar cukup tinggi di dalam air hasil olahannya. Oleh karena itu, metode adsorpsi dapat menjadi metode alternatif untuk mengatasi pencemaran zat warna yang ekonomis dan sederhana.
Adsorben adalah zat penjerap yang dapat digunakan untuk memurnikan udara dan gas, memurnikan pelarut, menghilangkan bau dalam pemurnian minyak nabati dan gula, menghilangkan warna produk-produk alam dan larutan, serta sebagai penjerap zat warna dalam pengolahan limbah. Menurut Gufta (1998) adsorben dapat menjerap berbagai polutan baik senyawa organik (zat warna) maupun anorganik (logam berat), dengan mekanisme adsorpsi, filtrasi, penukar ion, dan endapan. Arus utama dalam penelitian adsorben ialah pemanfaatan produk samping pertanian sebagai adsorben zat warna. Marshall dan Mitchell (1996) juga telah melaporkan beberapa produk samping pertanian yang berpotensi sebagai adsorben,
yaitu tongkol jagung, gabah padi, gabah kedelai, biji kapas, jerami, ampas tebu, serta kacang tanah. Hasil penelitian Alamsyah (2007) menggunakan kulit buah kakao sebagai adsorben untuk zat warna biru metilena dari limbah tekstil dengan kapasitas adsorpsi 1605.99 µg/g adsorben. Fahrizal (2008) menunjukkan bahwa modifikasi selulosa pada tongkol jagung mampu menjerap biru metilena dari limbah tekstil dengan kapasitas adsorpsi 518.07 µg/g adsorben. Raghuvanshi et al. (2004) memperlihatkan bahwa ampas tebu dapat mengadsorpsi zat warna biru metilena dengan efisiensi penjerapan mencapai 90%. Hasil-hasil penelitian tersebut menunjukkan bahwa limbah pertanian yang mengandung selulosa dapat diolah lebih lanjut sebagai adsorben dan diharapkan mampu meningkatkan nilai tambahnya.
Kacang tanah merupakan salah satu sumber protein nabati yang cukup penting dalam pola menu makanan di masyarakat Indonesia. Produksi tanaman kacang tanah di Indonesia pada tahun 2005 sebesar 785.526 ton, tahun 2006 meningkat menjadi 837.495 ton, dan tahun 2007 diharapkan mencapai 1 juta ton (BPS 2007). Kulit kacang tanah mempunyai potensi menjadi adsorben karena mengandung selulosa yang cukup tinggi sehingga dapat dijadikan adsorben untuk menjerap zat warna.
Penelitian ini bertujuan mengukur pengaruh waktu optimum adsorpsi, bobot optimum adsorben, dan konsentrasi awal zat warna terhadap efisiensi dan kapasitas adsorpsi serta menentukan isoterm adsorpsi dari adsorben yang berasal dari kulit kacang tanah.
TINJAUAN PUSTAKA
Kacang TanahTanaman kacang tanah (Arachis hypogaea L.), yang ditanam di Indonesia sebetulnya bukanlah tanaman asli, melainkan tanaman yang berasal dari benua Amerika, tepatnya dari daerah Brazilia (Amerika Selatan). Kacang tanah adalah tanaman palawija yang berumur pendek. Di Indonesia kacang tanah ditanam di daerah dataran rendah dengan ketinggian maksimal 1000 meter di atas permukaan air laut. Daerah yang paling cocok untuk tanaman kacang sebenarnya adalah daerah dataran dengan ketinggian 0-500 meter di atas permukaan laut.
2
lembaga (germ) 3.10-3.60% (Ketaren 1986). Kulit kacang tanah dapat digunakan sebagai bahan bakar, bahan pembenah tanah, bahan campuran pembuatan papan hardboard, dan masih cukup baik dipakai sebagai campuran pakan ternak. Berikut dapat dilihat komposisi kimia kulit kacang tanah pada Tabel 1.
Tabel 1 Komposisi kimia kulit kacang tanah Komponen %
Adsorpsi merupakan peristiwa terakumulasinya partikel pada permukaan (Atkins 1999). Zat yang menjerap disebut adsorben, sedangkan zat yang terjerap disebut adsorbat. Adsorben dapat berupa zat padat maupun zat cair. Adsorben padat diantaranya adalah silika gel, alumina, platina halus, selulosa, dan arang aktif. Adsorbat dapat berupa zat padat, zat cair, dan gas.
Faktor-faktor yang mempengaruhi proses adsorpsi antara lain sifat fisik dan kimia adsorben misalnya luas permukaan, ukuran partikel, komposisi kimia, sifat fisik, dan kimia adsorbat, misalnya ukuran molekul dan komposisi kimia, serta konsentrasi adsorbat dalam fase cairan. Semakin kecil ukuran partikel, maka semakin besar luas permukaan padatan persatuan volume tertentu sehingga akan semakin banyak zat yang diadsorpsi (Atkins 1999).
Teori adsorpsi menjelaskan pengikatan atau penggabungan molekul terlarut pada permukaan adsorben oleh gaya elektrik lemah yang dikenal dengan ikatan van der Waals. Adsorpsi akan terkonsentrasi pada sisi permukaan yang memiliki energi yang lebih tinggi. Aktivasi adsorben akan menaikan energi pada permukaannya sehingga dapat meningkatkan tarikan terhadap molekul terlarut (Jason 2004). Koefisien adsorpsi menjadi nilai yang penting dalam proses penghilangan kontaminan dalam air. Jason (2004) mendefinisikan koefisien adsorpsi sebagai nilai saat kontaminan terhilangkan dari fase cair (adsorbat) menuju fase padat (adsorben).
Ukuran pori dan luas permukaan adsorben merupakan hal yang sangat penting dalam adsorpsi. Perbesaran luas permukaan
adsorben dapat dilakukan dengan memperkecil ukuran partikelnya. Adsorben polar cenderung mengadsorpsi adsorbat polar secara kuat, dan mengadsorpsi adsorbat nonpolar secara lemah. Sebaliknya adsorben nonpolar cenderung untuk mengadsorpsi secara kuat adsorbat nonpolar dan mengadsorpsi adsorbat polar secara lemah (Bird 1993).
Proses adsorpsi berlangsung melalui tiga tahapan, yaitu makrotransport, mikrotransport, dan sorpsi. Makrotransport meliputi perpindahan adsorbat melalui air menuju interfase cair-padat dengan proses pemanasan dan difusi. Mikrotransport meliputi difusi adsorbat melalui sistem makropori dan submikropori. Sorpsi adalah istilah untuk menjelaskan kontak adsorbat terhadap adsorben. Istilah ini digunakan karena sulitnya membedakan proses yang berlangsung¸ apakah fisika atau kimia. Kapasitas adsorpsi suatu adsorben untuk sebuah kontaminan dapat ditentukan dengan menghitung isoterm adsorpsi (Tchobanogglous dan Franklin 1991).
Isoterm Adsorpsi
Adsorpsi sering dirangkaikan dengan istilah isoterm yang menunjukkan hubungan antara aktivitas (konsentrasi) fase cair dari adsorbat dan jumlah adsorbat pada suhu konstan. Isoterm adsorpsi menunjukkan hubungan kesetimbangan antara konsentrasi adsorbat dalam fluida dan dalam permukaan adsorben pada suhu tetap. Kesetimbangan terjadi pada saat laju pengikatan adsorben terhadap adsorbat sama dengan laju pelepasannya. Persamaan yang dapat digunakan untuk menjelaskan data percobaan isoterm dikaji oleh Freundlich dan Langmuir.
Isoterm Adsorpsi Freundlich
3
Apabila dilogaritmakan, persamaan akan menjadi: C = konsentrasi kesetimbangan adsorbat
dalam larutan setelah adsorpsi (ppm) k, n = konstanta empiris
Isoterm Freundlich menganggap bahwa pada semua sisi permukaan adsorben akan terjadi proses adsorpsi di bawah kondisi yang diberikan. Isoterm Freundlich tidak mampu memperkirakan adanya sisi-sisi pada permukaan yang mampu mencegah adsorpsi pada saat kesetimbangan tercapai, dan hanya ada beberapa sisi aktif saja yang mampu mengadsorpsi molekul terlarut (Jason 2004).
Isoterm Adsorpsi Langmuir
Isoterm Langmuir dibuat untuk menggambarkan pembatasan sisi adsorpsi dengan asumsi bahwa sejumlah tertentu sisi sentuh adsorben yang membentuk ikatan kovalen dan ion. Isoterm Langmuir disebut juga adsorpsi kimia karena adanya reaksi antara molekul-molekul adsorbat dengan adsorben yang membentuk ikatan kovalen dan ion. Isoterm Langmuir diturunkan berdasarkan persamaan berikut ini:
Isoterm langmuir dipelajari untuk mengambarkan pembatasan sisi adsorpsi dengan asumsi bahwa sejumlah tertentu sisi sentuh adsorben ada pada permukaannya dan semuanya memiliki energi yang sama, serta bahwa adsorpsi bersifat dapat balik (Atkins 1999).
Arang adalah padatan berpori hasil pembakaran bahan yang mengandung karbon. Arang tersusun dari atom-atom karbon yang berikatan secara kovalen membentuk struktur heksagonal datar dengan sebuah atom pada setiap sudutnya. Susunan kisi-kisi heksagonal
datar ini tampak seolah-olah seperti pelat-pelat datar yang saling bertumpuk dengan sela-sela diantaranya.
Arang aktif merupakan padatan amorf yang mempunyai luas permukaan dan jumlah pori sangat banyak (Baker et al. 1997). Manes (1998) menyatakan bahwa arang aktif adalah bentuk umum dari berbagai macam produk yang mengandung karbon yang telah teraktifkan untuk meningkatkan luas permukaannya. Arang aktif berbentuk kristal mikro karbon grafit yang pori-porinya telah mengalami pengembangan kemampuan untuk mengadsorpsi gas dan uap dari campuran gas dan zat-zat yang tidak larut atau yang terdispersi dalam cairan (Roy 1985).
Luas permukaan, dimensi, dan distribusi arang aktif bergantung pada bahan baku, pengarangan, dan proses aktivasi. Berdasarkan pada ukuran porinya, ukuran pori arang aktif diklasifikasikan menjadi tiga, yaitu mikropori (diameter <2 nm), mesopori (diameter 2-50 nm), dan makropori (diameter >50 nm) (Baker et al. 1997).
Keistimewaan dari arang aktif adalah gugus fungsional pada permukaannya. Gugus kompleks oksigen yang terletak di permukaan membuat permukaan arang aktif menjadi reaktif secara kimiawi dan menentukan sifat adsorpsinya seperti hidrofilik, keasaman, dan potensial negatif (Setiadi dan Sugiharso 1999).
Modifikasi Adsorben
4
Zat Warna Reaktif
Zat warna merupakan senyawa organik yang keberadaannya dalam perairan dapat mengganggu ekosistem didalamnya sebelum dibuang ke perairan. Zat warna dapat digolongkan menurut cara diperolehnya, yaitu zat warna alam dan zat warna sintetis. Penggolongan zat warna berdasarkan pemakaiannya, misalnya zat warna yang langsung dapat mewarnai serat disebut sebagai zat warna substantif dan zat warna yang memerlukan zat-zat pembantu supaya dapat mewarnai serat disebut zat reaktif (Manurung et al. 2004).
Penggolongan lainnya berdasarkan susunan kimia atau inti zat warna tersebut, yaitu zat warna nitroso, nitroazo, poliazo, indigoido, antrakuinon, ptalosianin. Selain itu, penggolongan yang lebih umum dikenal adalah berdasarkan aplikasi (cara pewarnaan), yaitu zat warna direk, asam, basa, mordan, belerang, bejana, naftol, dispersi, dan reaktif.
Zat warna reaktif termasuk zat warna yang larut dalam air, reaktif terhadap serat selulosa, dan sering dipakai dalam industri tekstil, yaitu procion, cibacron, remazol, levafix, drimarine, dan primazine. Zat warna reaktif adalah kromofor yang mengandung gugus yang aktif dan reaktif terhadap permukaan pada bahan tertentu. Zat warna ini memiliki gugus reaktif monoklorotriazina dan vinil sulfon yang juga dapat diaplikasikan untuk serat protein, yaitu wool dan nilon. Zat warna reaktif seperti zat warna azo umumnya mempunyai sifat sulit terbiodegradasi.
Kromofor zat warna reaktif biasanya merupakan sistem azo dan antrakuinon dengan berat molekul relatif kecil. Daya serap terhadap serat tidak besar sehingga zat warna yang tidak bereaksi dengan serat mudah dihilangkan. Gugus-gugus penghubung dapat mempengaruhi daya serap dan ketahanan terhadap asam atau basa. Pada umumnya agar reaksi dapat berjalan dengan baik maka diperlukan penambahan alkali atau asam sehingga mencapai pH tertentu (Manurung et al. 2004).
Cibacron red
Zat warna cibacron briliant red 3B-A (C32H19ClN8Na4O14S4) termasuk zat warna
bifungsional yang mengandung dua gugus reaktif, yaitu monoklorotriazin dan vinil sulfon. Cibacron red merupakan bubuk yang berwarna merah, memilki pH 6-7, dan kelarutan dalam air 100 g/l (Ciba 2002). Cibacron red merupakan zat warna reaktif
dalam kelas azo. Zat warna azo merupakan jenis zat warna mempunyai sistem kromofor dari gugus azo (-N=N-) yang berikatan dengan gugus aromatik. Zat warna ini mempunyai bobot molekul sebesar 1000.25 g/mol dan umumnya analisisnya menggunakan spektroskopi sinar tampak dengan panjang gelombang maksimum 517 nm (Aldrich 2007). Struktur cibacron red dapat dilihat pada Gambar 1.
Gambar 1 Struktur cibacron red.
BAHAN DAN METODE
Bahan dan Alat
Bahan-bahan yang digunakan adalah kulit kacang tanah, serbuk zat warna cibacron red, arang aktif, dan limbah cair industri tekstil. Alat-alat yang digunakan adalah spektrofotometer spektronik 20D+ Thermo Electron Corporation, spektrofotometer spektronik DR/2000 Hach, neraca analitik Kern ALJ 220-4, oven, shaker Heidolph Titramax 101, dan ayakan ukuran 100 mesh.
Metode Penelitian Adsorben
Adsorben yang digunakan adalah kulit kacang tanah. Kulit kacang tanah diperoleh dari kebun bibit University Farm, Dramaga-Bogor. Kulit kacang tanah yang digunakan adalah varietas gajah berumur 100 hari. Adsorben dibuat menjadi ukuran kurang dari 100 mesh. Adsorben kulit kacang tanah kemudian dibandingkan dengan adsorben komersil, yaitu arang aktif yang terbuat dari tempurung kelapa.
Preparasi Kulit Kacang Tanah (Raghuvanshi et al. 2004)
5
Kulit kacang tanah yang telah dihaluskan ditambahkan asam sulfat pekat 97%, lalu dipanaskan pada suhu 160°C selama 36 jam. Setelah itu, dibilas dengan air destilata untuk menghilangkan kelebihan asam. Kemudian bahan dikeringkan pada suhu 110°C. Serbuk kulit kacang tanah ini selanjutnya disebut adsorben modifikasi asam (AMA).
Pembuatan Larutan Zat Warna
Larutan stok zat warna konsentrasi 1000 ppm dibuat dengan cara melarutkan 1.00 g serbuk cibacron red dalam air destilata dan diencerkan hingga satu liter. Kemudian larutan tersebut dibuat dengan konsentrasi 0.5, 1.0, 5.0, 10.0, 15.0, 20.0, dan 25.0 ppm untuk pembuatan kurva standar.
Penentuan Kondisi Optimum Waktu Adsorpsi, Bobot, dan Konsentrasi Awal Zat Warna
ATM, AMA, dan arang aktif dengan variasi bobot adsorben 1.0, 2.0, dan 3.0 gram dimasukkan ke dalam 100 ml larutan zat warna cibacron red dengan konsentrasi awal 50, 100, dan 150 ppm, kemudian larutan dikocok dengan shaker. Adsorpsi dilakukan dengan variasi waktu adsorpsi 30, 45, dan 60 menit (Raghuvanshi et al. 2004), dilihat perubahan warna yang terjadi. Campuran disaring dan dibaca absorbansi filtratnya dengan spektronik 20D+ pada panjang gelombang maksimum. Desain penentuan kondisi optimum adsorpsi dilakukan menggunakan desain rancangan acak lengkap faktorial dengan program statistika ver.6 metode respon surface. Kondisi yang digunakan sebagai faktor adalah waktu adsorpsi, bobot adsorben, dan konsentrasi awal zat warna sedangkan responnya kapasitas adsorpsi (Q) dan efisiensi penjerapan (E).
Kapasitas adsorpsi dan efisiensi penjerapan dapat dihitung dengan persamaan:
(
)
Q = kapasitas adsorpsi per bobot adsorben (µg/g adsorben) V = volume larutan (ml)
Co = konsentrasi awal larutan (ppm)
Ca = konsentrasi akhir larutan (ppm)
m = bobot adsorben (g)
Penentuan Isoterm Adsorpsi
Erlenmeyer yang berisi bobot optimum ATM dan AMA dilarutkan dalam 100 ml larutan zat warna cibacron red dengan variasi konsentrasi 0.0, 25.0, 50.0, 75.0, 100.0, dan 150.0 ppm pada kondisi waktu optimum untuk masing-masing adsorben kemudian disaring dan diukur adsorbansinya pada panjang gelombang maksimum. Arang aktif sebagai pembanding diperlakukan sama seperti halnya kulit kacang tanah. Kemudian diukur kapasitas adsorpsi (Q) dan konstanta afinitas dihitung dengan model isoterm Langmuir dan Freundlich (Atkins 1999).
Penentuan Kapasitas Adsorpsi Limbah Industri Tekstil
ATM, AMA, dan arang aktif yang didapat pada perlakuan kondisi optimum dimasukan pada limbah industri tekstil yang terlebih dahulu diketahui intensitas warnanya dilarutkan dalam 100 ml limbah cair. Campuran disaring dan filtrat yang diperoleh diukur intensitas warnanya (unit Pt-Co) pada panjang gelombang 455 nm dengan spektronik DR/2000.
HASIL DAN PEMBAHASAN
Panjang Gelombang Maksimum danPembuatan Kurva Standar
Pemilihan panjang gelombang yang tepat untuk pengukuran sampel ialah yang paling banyak diserap oleh sampel tersebut. Pengukuran pada panjang gelombang tersebut akan memberikan kepekaan dan ketelitian pengukuran yang paling tinggi dengan spektrofotometer. Panjang gelombang maksimum cibacron red yang diperoleh adalah 517 nm (Lampiran 2). Menurut Aldrich (2007) panjang gelombang maksimum cibacron red adalah 517 nm.
Kurva standar ialah gambaran yang menunjukkan hubungan antara serapan suatu sinar tertentu dengan konsentrasi zat yang menyerap sinar dapat dilihat pada Lampiran 3. Persamaan kurva standar cibacron red yang dihasilkan adalah y = 0.0130x + 0.0037 dengan R2= 0.9998 (Gambar 2).
6
Kondisi Optimum Waktu adsorpsi, Bobot Adsorben, dan Konsentrasi
Adsorben dari kulit kacang tanah digunakan untuk menjerap zat warna reaktif cibacron red dan limbah cair industri tekstil. Penentuan kondisi optimum dilakukan dengan mengukur tiga parameter, yaitu waktu adsorpsi, bobot adsorben, dan konsentrasi awal zat warna. Setiap adsorben memiliki karakteristik yang berbeda dalam proses adsorpsi, sehingga kondisi yang dibutuhkan untuk adsorpsi juga berbeda.
Penentuan kondisi optimum dilakukan menggunakan metode respon surface sebagai suatu kumpulan teknik penyelesaian masalah dengan menggunakan matematika dan statistik dalam bentuk model matematika atau fungsi dalam menganalisis masalah tersebut. Respon yang ingin dicapai dipengaruhi oleh beberapa peubah sehingga respon tersebut berada pada titik optimumnya. Penentuan kondisi optimum ini melibatkan dua respon, yaitu kapasitas adsorpsi dan efisiensi penjerapan. Dari dua respon tersebut dengan analisis statistik didapatkan titik temu kedua respon tersebut sehingga didapatkan suatu kondisi optimum masing-masing adsorben.
Kondisi Optimum Adsorben Tanpa Modifikasi
Data pada Lampiran 4 dan 5 untuk adsorben tanpa modifikasi (ATM) menunjukkan bahwa penjerapan zat warna (adsorbat) mencapai kesetimbangan (optimum) pada waktu 45 menit, bobot 1.0 gram, dan konsentrasi 100 ppm. Kapasitas adsorpsi dan efisiensi penjerapan adsorben tanpa modifikasi mengalami kenaikan sampai mencapai maksimum dengan nilai ketepatan percobaan yang dilakukan menggunakan program statistik sebesar 80.30%, maka dihasilkan nilai kapasitas adsorpsi dan efisiensi penjerapan sebesar 476.34 µg/g (artinya sebanyak 476.34 µg adsorbat yang terjerap dalam 1.0 g adsorben) dan 4.69% (Tabel 2).
Tabel 2 Kondisi optimum ATM Parameter Optimum Q
(µg/g)
Kapasitas adsorpsi dan efisiensi penjerapan meningkat seiring dengan meningkatnya waktu adsorpsi. Waktu optimum yang diperoleh adsorben tanpa modifikasi adalah 45 menit. Setelah melewati 45 menit, kapasitas adsorpsi dan efisiensi penjerapan menurun (Lampiran 5). Hal ini sesuai dengan hasil penelitian Raghuvanshi et al. (2004) yang menyatakan bahwa efisiensi penjerapan berbanding lurus dengan waktu sampai pada titik tertentu, kemudian mengalami penurunan setelah melewati titik tersebut.
Bobot ATM menunjukkan adanya penurunan kapasitas adsorpsi dan efisiensi penjerapan seiring meningkatnya bobot adsorben. Pada saat bobot adsorben dinaikkan sedangkan konsentrasi cibacron red tetap, terjadi penurunan kapasitas adsorpsi. Peningkatan sisi aktif akan meningkatkan penyebaran adsorbat, sehingga kapasitas adsorpsi lebih rendah dibandingkan dengan jumlah sisi aktif yang lebih sedikit. Pada bobot 1.0 gram hampir seluruh permukaan adsorben telah terikat dengan adsorbat, sedangkan pada bobot 2.0 dan 3.0 gram masih banyak sisi aktif yang belum berikatan dengan adsorbat sehingga kapasitas adsorpsi 1.0 gram lebih besar dibandingkan dengan kapasitas adsopsi pada bobot 2.0 dan 3.0 gram (Lampiran 5).
Kapasitas adsorpsi dan efisiensi penjerapan meningkat seiring dengan kenaikan konsentrasi awal cibacron red hingga konsentrasi 100 ppm kemudian kapasitas adsorpsi dan efisiensi penjerapannya menurun pada konsentrasi 150 ppm, hal ini menunjukkan bahwa ATM mengalami kejenuhan pada konsentrasi yang lebih tinggi (Lampiran 5). Penurunan kapasitas adsorpsi disebabkan adanya penurunan molekul cibacron red yang terikat pada sisi aktif permukaan adsorben. Pencirian adsorpsi cibacron red menunjukkan bahwa kejenuhan permukaan adsorben bergantung pada konsentrasi cibacron red tersebut. Pada konsentrasi yang rendah adsorben mampu menjerap lebih banyak molekul cibacron red yang tersedia dengan cepat. Sementara itu, pada konsentrasi yang tinggi molekul cibacron red tersebar pada seluruh permukaan adsorben melalui difusi intrapartikel secara besar-besaran dengan kecepatan yang lebih rendah. Kondisi Optimum Adsorben Modifikasi
Asam
7
penjerapan yang lebih besar dibandingkan adsorben tanpa modifikasi. Hal ini sesuai dengan hasil penelitian Raghuvanshi et al. (2004) yang menunjukkan bahwa modifikasi asam oleh asam sulfat dapat meningkatkan efisiensi penjerapan.
Pengaruh waktu adsorpsi, bobot, dan konsentrasi terhadap kapasitas adsorpsi dan efisiensi penjerapan oleh adsorben modifikasi asam (AMA) dapat dilihat pada Lampiran 6 dan 7. Kapasitas adsorpsi dan efisiensi penjerapan terus mengalami kenaikan dan mencapai kondisi optimum pada waktu 60 menit, bobot 1.5 gram, dan konsentrasi 150 ppm, dari analisis statistiknya didapat nilai kapasitas adsorpsi dan efisiensi penjerapan dengan nilai ketepatan percobaan 77.06% sebesar 8837.00 µg/g (artinya sebanyak 8837.00 µg adsorbat yang terjerap dalam 1.5 g adsorben) dan 87.14% (Tabel 3). Hasil ini membuktikan bahwa modifikasi asam pada adsorben dapat meningkatkan kapasitas adsorpsi dan efisiensi penjerapan. Modifikasi adsorben dengan asam paling umum dilakukan dan terbukti sangat efektif dalam meningkatkan kapasitas dan efisiensi adsorben (Gufta 1998).
Tabel 3 Kondisi optimum AMA Parameter optimum Q
(µg/g)
Waktu adsorpsi adsorben modifikasi asam sebesar 60 menit belum dikatakan optimum karena adsorben membutuhkan waktu yang lebih lama agar terjadi kesetimbangan antara adsorben dan adsorbat. Ketersediaan tapak aktif diperbesar dengan penambahan bobot AMA, tetapi peningkatan tapak aktif berbanding terbalik dengan kapasitas adsorpsi (Lampiran 6 dan 7). Hal ini dikarenakan tapak aktif dalam jumlah besar membutuhkan waktu kesetimbangan yang lebih lama. Pada Lampiran 7 terlihat bahwa bobot optimum adsorben modifikasi sebesar 1.5 gram dan setelah melewati titik tersebut, kapasitas adsorpsi menurun dan efisiensi penjerapan meningkat. Penurunan kapasitas adsorpsi setelah mencapai nilai optimum dimungkinkan adanya sisi aktif yang belum berikatan dengan adsorbat sehingga kapasitas adsorpsi 1.5 gram lebih besar dibandingkan
3.0 gram. Barros et al. (2003) menyatakan bahwa peningkatan bobot adsorben akan menyediakan tapak aktif yang lebih besar, sehingga meningkatkan efisiensi penjerapan.
Konsentrasi cibacron red optimum yang diperoleh oleh AMA adalah 150 ppm (Lampiran 6 dan 7). Melalui Lampiran 7 dapat dilihat bahwa pada selang konsentrasi yang diberikan, kapasitas adsorpsi berbanding lurus dengan konsentrasi awal cibacron red. Kenaikan kapasitas adsorpsi mengindikasikan jumlah molekul cibacron red yang terjerap pada tapak aktif semakin besar. Konsentrasi yang tinggi akan meningkatkan jumlah molekul cibacron red dalam larutan, sehingga semakin besar kemungkinannya akan terjerap. Semakin besar konsentrasi, semakin tinggi jumlah molekul dalam larutan, sehingga meningkatkan laju reaksi antara molekul adsorbat dan adsorben (Barros et al. 2003). Pada penelitian ini, konsentrasi 150 ppm belum dapat dikatakan sebagai konsentrasi optimum, karena kapasitas adsorpsi yang lebih besar masih mungkin diperoleh pada konsentrasi yang lebih tinggi.
Kondisi Optimum Arang Aktif
Arang aktif merupakan adsorben komersial yang memiliki kemampuan menjerap berbagai jenis senyawa dan zat warna. Proses adsorpsi pada arang aktif dianggap sebagai proses fisikokimia: molekul atau ion-ion adsorbat terikat oleh permukaan partikel yang reaktif. Selain itu, materi ini memiliki pori-pori sehingga molekul adsorbat dapat terperangkap dalam pori tersebut.
Lampiran 8 dan 9 menunjukkan pengaruh waktu adsorpsi, bobot, dan konsentrasi terhadap kapasitas adsorpsi dan efisiensi penjerapanoleh arang aktif. Kondisi optimum yang diperoleh adalah waktu 60 menit, bobot 3.0 gram, dan konsentrasi 150 ppm (Tabel 4), dari analisis statistiknya dengan ketepatan percobaan 73.97% didapat nilai kapasitas adsorpsi dan efisiensi sebesar 3827.50 µg/g (artinya sebanyak 3827.50 µg adsorbat yang terjerap dalam 3.0 g adsorben) dan 75.56%. Tabel 4 Kondisi optimum arang aktif
8
ATM AMA Arang aktif
Jenis adsorben
ATM AMA Arang aktif
Jenis adsorben
Gambar 3 Perbandingan kapasitas adsorpsi cibacron red oleh adsorben tanpa modifikasi, adsorben modifikasi asam, dan arang aktif.
Q
Arang aktif yang digunakan berasal dari tempurung kelapa memiliki ukuran 300 mesh. Luas permukaan akan semakin besar jika ukuran adsorben semakin kecil. Luas permukaan yang besar meningkatkan ketersediaan tapakaktif, sehingga waktu yang dibutuhkan untuk mencapai waktu kesetimbangan lebih lama. Hal ini menjadi salah satu faktor yang menyebabkan kapasitas adsorpsi arang aktif terus mengalami peningkatan pada selang waktu yang diberikan.
Bobot 3.0 gram merupakan bobot optimum arang aktif. Semakin besar bobot menyebabkan kapasitas adsorpsi menurun dan efisiensi penjerapan meningkat (Lampiran 9). Semakin besar bobot adsorben menyebabkan luas permukaan aktifnya juga meningkat. Peningkatan jumlah luas permukaan aktif akan meningkatkan efisiensi penjerapan. Kenaikan kapasitas adsorpsi terus meningkat sampai pada selang konsentrasi 150 ppm, ini dikarenakan jumlah molekul cibacron red yang terjerap pada tapak aktif dari arang aktif semakin besar (Lampiran 9). Hal ini menunjukkan bahwa kondisi optimum arang aktif pada ketiga parameter belum dikatakan optimum, karena kapasitas adsorpsi dan efisiensi penjerapan yang lebih besar masih mungkin diperoleh pada waktu, bobot, dan konsentrasi yang lebih tinggi.
Adsorpsi Larutan Tunggal
Kulit kacang tanah sebagai adsorben yang potensial perlu diuji kemampuannya dalam menjerap zat warna dengan cara membandingkan dengan adsorben komersial (dalam penelitian ini digunakan arang aktif). Kapasitas adsorpsi dan efisiensi penjerapan digunakan sebagai faktor pembanding. Perbandingan antara ATM, AMA, dan adsorben komersial terhadap kapasitas adsorpsi dan efisiensi penjerapan menggunakan kulit kacang tanah dapat dilihat pada Gambar 3 dan 4.
Gambar 4 Perbandingan efisiensi penjerapan cibacron red oleh adsorben tanpa modifikasi, adsorben modifikasi asam, dan arang aktif.
Kapasitas adsorpsi AMA lebih tinggi dibandingkan ATM dan arang aktif berturut-turut sebesar 8837.00, 476.34, dan 3827.50 µg/g adsorben (Gambar 3). Efisiensi penjerapan AMA juga menunjukkan hal yang sama, lebih tinggi jika dibandingkan ATM dan arang aktif berturut-turut sebesar 87.14, 4.69, dan 72.56% (Gambar 4). Hasil ini membuktikan bahwa modifikasi asam pada adsorben dapat meningkatkan kapasitas adsorpsi dan efisiensi penjerapan.
Isoterm Adsorpsi
Tipe isoterm adsorpsi dapat digunakan untuk mempelajari mekanisme adsorpsi zat warna. Kapasitas adsorpsi dipelajari melalui tipe isotermnya. Telah banyak isoterm adsorpsi yang dikembangkan untuk mendeskripsikan interaksi antara adsorben dan adsorbat. Isoterm Freundlich dan Langmuir pada umumnya dianut oleh adsorpsi padat-cair (Atkins 1999).
Kurva regresi linier untuk tipe isoterm Freundlich dan Langmuir menggunakan data konsentrasi awal cibacron red, konsentrasi terjerap, dan bobot adsorben (Lampiran 10, 11, dan 12). Isoterm adsorpsi cibacron red oleh ATM tipe Langmuir dan Freundlich diperlihatkan pada Gambar 5 dan 6. Hasil penelitian menunjukkan bahwa semua kurva adalah linier. Hal ini disebabkan oleh banyaknya gugus kimia yang reaktif pada permukaan adsorben dan dapat mendukung terjadinya proses adsorpsi.
9
Gambar 6 Isoterm Freundlich adsorpsi cibacron red oleh adsorben tanpa modifikasi.
Linieritas kedua tipe isoterm pada adsorpsi cibacron red menunjukkan linieritas yang tinggi, yaitu 94.13% untuk isoterm Langmuir dan 96.50% untuk isoterm Freundlich. Fakta ini menunjukkan bahwa kedua tipe isoterm terjadi pada proses adsorpsi untuk cibacron red. Jika dibandingkan linieritas kedua tipe isoterm tersebut, dapat dilihat ternyata linieritas isoterm adsorpsi tipe Freundlich lebih tinggi dibandingkan isoterm Langmuir. Hasil penelitian ini dikuatkan oleh Hussein et al. (2004) yang menyatakan bahwa dengan linieritas 90%, dapat dinyatakan bahwa kedua tipe isoterm adsorpsi terjadi pada proses adsorpsi zat warna.
y = 1.5220x - 0.5878
Gambar 7 Isoterm Langmuir adsorpsi cibacron red oleh adsorben modifikasi asam.
Gambar 8 Isoterm Freundlich adsorpsi cibacron red oleh adsorben modifikasi asam.
Isoterm adsorpsi cibacron red oleh AMA menunjukkan linieritas yang tinggi, yaitu 89.56% untuk isoterm Langmuir dan 97.51% untuk isoterm Freundlich. Dengan melihat linieritas kedua tipe isoterm adsorpsi tersebut, ternyata linieritas isoterm Freundlich lebih tinggi dibandingkan dengan isoterm Langmuir
(Gambar 7 dan 8). Oleh karena itu, isoterm adsorpsi cibacron red tipe Freundlich lebih baik digunakan untuk mencirikan mekanisme adsorpsi cibacron red (Lampiran 11).
Gambar 9 Isoterm Langmuir adsorpsi cibacron red oleh arang aktif.
Gambar 10 Isoterm Freundlich adsorpsi cibacron red oleh arang aktif. Isoterm adsorpsi oleh arang aktif juga mengikuti isoterm Freundlich berdasarkan linieritasnya, yaitu 96.09% untuk isoterm freundlich dan 94.33% untuk isoterm Langmuir (Gambar 9 dan 10). Berdasarkan hasil tersebut, diduga adsorpsi ATM, AMA, dan arang aktif mengikuti tipe isoterm Freundlich. Pendekatan Freundlich mengasumsikan bahwa permukaannya bersifat heterogen, membentuk banyak lapisan, terdapat sisi aktif adsorpsi yang memiliki afinitas tinggi, dan bagian lainnya memiliki afinitas yang rendah.
Adsorpsi Limbah Industri
10
didapat. Panjang gelombang yang digunakan adalah panjang gelombang yang terbaik untuk pengukuran warna dalam limbah, yaitu 455 nm.
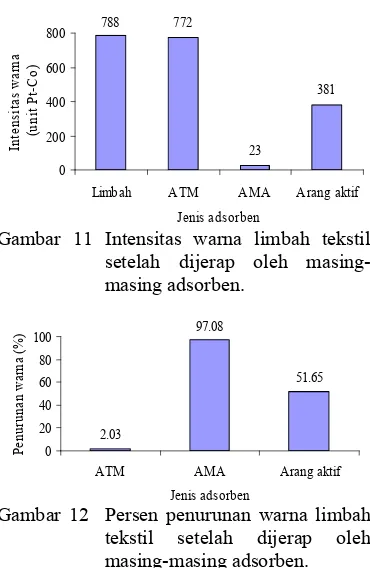
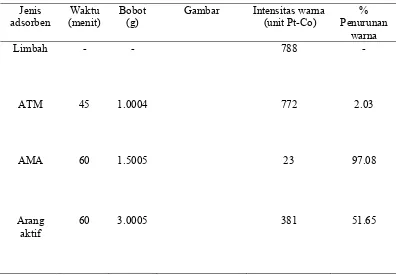
Intensitas warna limbah awal yang diukur adalah 788 unit Pt-Co. Setelah dijerap dengan masing-masing adsorben ATM, AMA, dan arang aktif ternyata didapat intensitas warnanya berkurang berturut-turut sebesar 772, 23, dan 381 unit Pt-Co terlihat pada Gambar 11. Persen penurunan warna dari intensitas awal limbah setelah dijerap masing-masing adsorben adalah 2.03, 97.08, dan 51.65% (Gambar 12). Persen penurunan warna AMA, yaitu sebesar 97.08% ini jauh lebih besar dibandingkan dengan ATM dan arang aktif. Terbukti bahwa AMA lebih efektif menjerap warna limbah industri dibandingkan ATM dan arang aktif.
788 772
Limbah ATM AMA Arang aktif Jenis adsorben
Gambar 11 Intensitas warna limbah tekstil setelah dijerap oleh masing-masing adsorben.
2.03
ATM AMA Arang aktif
Jenis adsorben
Gambar 12 Persen penurunan warna limbah tekstil setelah dijerap oleh masing-masing adsorben.
Berdasarkan standar baku mutu air bersih Permenkes No. 416/Men.Kes/Per./IX/1990 untuk intensitas warna yang dapat diterima pada umumnya sebesar 50 unit Pt-Co. Setelah limbah industri dijerap oleh masing-masing adsorben terbukti hanya intensitas warna AMA yang dapat diterima umumnya untuk air bersih karena lebih kecil intensitasnya jika dibandingkan dengan standar baku mutu air bersih untuk warna. Intensitas warna setelah dijerap ATM dan arang aktif masih jauh dari nilai standar baku mutu air bersih sehingga
dapat dikatakan adsorpsi terhadap limbah industri kurang baik.
SIMPULAN DAN SARAN
SimpulanModifikasi asam terhadap kulit kacang tanah terbukti mampu meningkatkan kapasitas adsorpsi dan efisiensi penjerapan cibacron red. Kapasitas adsorpsi dan efisiensi penjerapan cibacron red oleh adsorben modifikasi asam lebih besar dibandingkan dengan adsorben tanpa modifikasi dan arang aktif. Persen penurunan warna limbah industri oleh adsorben modifikasi asam juga lebih besar dibandingkan adsorben tanpa modifikasi dan arang aktif. Proses adsorpsi cibacron red dan limbah industri tekstil menggunakan adsorben modifikasi asam lebih efektif dibandingkan adsorben tanpa modifikasi dan arang aktif. Hal ini membuktikan bahwa adsorben modifikasi asam dapat menggantikan arang aktif sebagai adsorben komersial.
Tipe isoterm yang dianut oleh ketiga jenis adsorben adalah isoterm Freundlich. Isoterm ini mengasumsikan bahwa permukaannya bersifat heterogen, membentuk banyak lapisan, terdapat sisi aktif adsorpsi memiliki afinitas yang tinggi, dan bagian lainnya memiliki afinitas yang rendah.
Saran
Berdasarkan hasil penelitian ini, maka tahapan selanjutnya yang perlu dilakukan adalah memperluas kisaran taraf yang digunakan sebagai faktor kondisi optimum karena masih teramati pada ujung-ujung taraf. Pencirian lebih lanjut adsorben modifikasi asam dari kulit kacang tanah, yaitu dengan Scanning electron microscopy (SEM) dan spektrofotometri inframerah. Adsorpsi terhadap limbah sendiri perlu dilakukan uji lanjut untuk mengukur parameter selain warna, yaitu COD dan BOD.
DAFTAR PUSTAKA
Alamsyah Z. 2007. Biosorpsi Biru Metilena Oleh Kulit Buah Kakao [skripsi]. Bogor: Fakultas Matematika dan IPA, Institut Pertanian Bogor.
Aldrich S. 2007. Cibacron brilliant red 3G-A. [terhubung berkala]. http: //www.sigma-aldrich.com [20 Apr 2008].
11
Rohhadyan T, editor. Oxford: Oxford University Press. Terjemahan dari: Physical Chemistry.
Baker FS, Miller CE, Repik AJ, Tollens ED. 1997. Activated Carbon. New York: J Wiley.
Barros JLM, Macedo GR, Duarte MML, Silva EP, Lobato AKCL. 2003. Biosorption of cadmium using the fungus aspergillus niger. Braz J Chem Eng 20: 3.
Bird T. 1993. Kimia Fisik untuk Universitas. Jakarta: Gramedia Pustaka Utama. BPS. 2007. Statistik Pertanian Indonesia.
Jakarta: Biro Pusat Statistik.
[Ciba] Specialty Chemicals Indonesia. 2002. Cibacron red B-E. [terhubung berkala]. http://agrippina.bcs.deakin.edu.au/bcs_ad min/msds/msds_docs/Cibacron%20Red% 20B-E.pdf [15 Mei 2008].
[Depkes]. 1977. Peraturan Menteri Kesehatan RI No. 173/Men.Kes/Per./VIII/1977 ten-tang syarat-syarat evaluasi kualitas badan air. Jakarta: Depkes.
[Depkes]. 1990. Peraturan Menteri Kesehatan RI No. 416/Menkes/Per./IX/1990 tentang syarat-syarat dan pengawasan kualitas air bersih. Jakarta: Depkes.
[Deptan]. 2008. Pemanfaatan limbah sebagai bahan pakan ternak. [terhubung berkala]. http://jajo 66.files.wordpress.com [16 Feb 2008].
Fahrizal. 2008. Pemanfaatan tongkol jagung sebagai biosorben zat warna biru metilena [skripsi]. Bogor: Fakultas Matematika dan Ilmu Pengetahuan Alam, Institut Pertanian Bogor.
Fessenden RJ dan Fessenden JS. 1986. Kimia Organik jilid 1. Edisi ke-3. penerjemah; Pudjaatmaka AH. Jakarta: Erlangga. Terjemahan dari: Organic Chemistry. Gufta FK. 1998. Utilization of bagasse fly ash
generated in the sugar industry for removal and recovery of phenol and p-Nitrophenol from wastewater. J Chem Tech Biotechnology 70: 180-186.
Hussein H, Ibrahim SF, Kandeel K, Moawad H. 2004. Biosorption heavy metal from waste water using Pseudomonas sp. Elec J Biotechnol 7: 1.
Jason PP. 2004. Activated carbon and some applications for the remediation soil and
ground water pollution. [terhubung berkala]. http://www.ce.edu/program areas [16 Feb 2008].
Ketaren S. 1986. Pengantar Teknologi Minyak dan Lemak Pangan. Jakarta: UI Pr. Manes M. 1998. Activated Carbon Adsorption
Fundamental. Di dalam: R.A. Meyers (penyunting). Encyclopedia of Environ-mental Analysis and Remediation. Volume 1. New York: J Wiley.
Manurung R, Hasibuan R, Irvan. 2004. Perombakan zat warna azo reaktif secara aerob-anaerob. [terhubung berkala]. http://library.usu.ac.id/download/ft/tkimia -renita2. [16 Feb 2008].
Marshall WE, Mitchell M J. 1996. Agriculture by-product as metal adsorbent: Sorption properties and resistance to Mechanical abrasion. J Chem Tech Biotechnology 66: 192-198.
Mulyatna L, Pradiko H, Nasution UK. 2003. Pemilihan persamaan adsorpsi isoterm pada penentuan kapasitas adsorpsi kulit kacang tanah terhadap zat warna remazol golden yellow 6. www.unpas.ac.id/pmb/home/images/ar ticles/infomatek/jurnal_V_3_3.html [2 Feb 2008].
Notodarmojo S. 2004. Pencemaran Tanah danAir Tanah. Bandung: ITB Pr.
Raghuvanshi SP, Singh R, Kaushik CP. 2004. Kinetics study of methylene blue dye bioadsorption on bagasse. App Ecol Environ Research 2: 35-43.
Roy GM. 1985. Activated Carbon Application in The Food and Pharmaceutical Industries. Lancaster: Tanchnomic.
Setiadi, Sugiharso E. 1999. Pengaruh impregnan NaOH terhadap luasan permukaan karbon aktif dan kemampuan adsorpsi terhadap CO2. Di dalam
Fundamental dan Aplikasi Teknik Kimia. Prosiding Seminar Nasional; Surabaya, 24-25 Nov 1994. Depok: Universitas Indonesia A17: 1-7.
13
Lampiran 1 Bagan alir penelitian
Kulit kacang
tanah
Preparasi Sampel
Arang
aktif
Penghancuran 100 mesh
Pencucian dengan air destilata dan NaOH
Modifikasi asam
Tanpa modifikasi
Penentuan isoterm adsorpsi
Aplikasi terhadap limbah industri
14
Lampiran 2 Penentuan panjang gelombang maksimum zat warna cibacron red
Panjang gelombang (nm)
%
Transmitan Absorban
515 54.8 0.2612
516 54.4 0.2644
517 54.2 0.2660
518 54.6 0.2628
519 54.8 0.2612
520 54.6 0.2628
521 55.0 0.2596
522 55.2 0.2581
523 55.4 0.2565
524 55.4 0.2565
525 55.6 0.2549
0.2540 0.2560 0.2580 0.2600 0.2620 0.2640 0.2660 0.2680
514 515 516 517 518 519 520 521 522 523 524 525 526 Panjang gelombang (nm)
A
b
s
o
rb
a
n
s
Lampiran 3 Kurva standar cibacron red pada panjang gelombang maksimum 517 nm
[Cibacron Red]
(ppm) %T A
0.5 98.0 0.0088
1 96.6 0.0150
5 85.2 0.0696
10 73.2 0.1355
15 63.0 0.2007
20 54.6 0.2628
15
Lampiran 4 Penentuan kondisi optimum adsorben tanpa modifikasi
16
Lampiran 5 Analisis statistik kondisi optimum adsorben tanpa modifikasi
Profiles for Predicted Values and Desirability
Bobot
Kondisi optimum yang dihasilkan: waktu = 45 menit
17
Lampiran 6 Penentuan kondisi optimum adsorben modifikasi asam
Bobot (g)
Waktu (menit)
Konsentrasi awal (ppm)
Konsentrasi
akhir (ppm) Q (µg/g) E (%)
1.0004 30 50 0.4244 4955.8227 99.15
2.0004 30 50 0.4244 2478.3450 99.15
3.0003 30 50 0.2882 1656.8941 99.42
1.0002 45 50 2.0322 4795.8205 95.94
2.0001 45 50 0.6298 2468.3866 98.74
3.0002 45 50 0.3564 1654.7044 99.29
1.0004 60 50 0.3562 4962.6382 99.29
2.0000 60 50 0.2882 2485.5896 99.42
3.0001 60 50 0.2882 1657.0045 99.42
1.0001 30 100 49.8461 5014.8885 50.15
2.0003 30 100 7.0450 4647.1700 92.96
3.0003 30 100 1.1837 3293.5468 98.82
1.0001 45 100 34.6919 6530.1574 65.31
2.0003 45 100 4.8707 4755.8690 95.13
3.0002 45 100 0.4244 3319.0199 99.58
1.0002 60 100 30.2428 6974.6698 69.76
2.0003 60 100 4.0240 4798.0826 95.98
3.0002 60 100 0.3562 3321.2370 99.64
1.0002 30 150 58.3278 9165.3931 61.11
2.0003 30 150 13.0445 6846.9213 91.30
3.0003 30 150 1.5699 4947.1749 98.95
1.0001 45 150 47.8120 10218.2921 68.13
2.0001 45 150 6.6315 7168.0656 95.58
3.0003 45 150 0.4927 4991.1058 99.67
1.0002 60 150 43.0877 10689.0938 71.27
2.0004 60 150 2.9764 7349.7109 98.02
18
Lampiran 7 Analisis statistik kondisi optimum adsorben modifikasi asam
Profiles for Predicted Values and Desirability
Bobot
Kondisi optimum yang dihasilkan: waktu = 60 menit
19
Lampiran 8 Penentuan kondisi optimum arang aktif
Bobot (g)
Waktu (menit)
Konsentrasi awal (ppm)
Konsentrasi
akhir (ppm) Q (µg/g) E (%)
1.0003 30 50 17.1147 3287.5448 65.77
2.0001 30 50 9.7492 2012.4906 80.50
3.0002 30 50 6.2980 1456.6373 87.40
1.0003 45 50 24.6466 2534.6974 50.71
2.0002 45 50 6.9854 2150.5708 86.03
3.0002 45 50 5.9546 1468.0805 88.09
1.0002 60 50 13.5870 3640.5756 72.83
2.0000 60 50 9.4023 2029.8859 81.20
3.0003 60 50 13.9382 1201.9580 72.12
1.0000 30 100 58.9995 4100.0546 41.00
2.0000 30 100 31.6112 3419.4412 68.39
3.0001 30 100 19.2493 2691.5987 80.75
1.0003 45 100 55.0033 4498.5379 45.00
2.0001 45 100 26.4650 3676.5652 73.53
3.0002 45 100 14.2895 2856.8727 85.71
1.0002 60 100 53.8135 4617.9571 46.19
2.0001 60 100 31.6104 3419.3112 68.39
3.0002 60 100 19.2493 2691.5539 80.75
1.0003 30 150 107.8274 4216.0002 28.12
2.0003 30 150 67.5500 4121.8825 54.97
3.0005 30 150 39.4803 3683.4378 73.68
1.0002 45 150 100.0100 4998.2387 33.33
2.0001 45 150 82.7377 3362.9457 44.84
3.0004 45 150 45.2170 3492.3008 69.86
1.0002 60 150 106.8981 4309.3302 28.73
2.0002 60 150 70.4498 3977.2082 53.03
20
Lampiran 9 Analisis statistik kondisi optimum arang aktif
Profiles for Predicted Values and Desirability
Bobot
0.0000 3827.5 6500.0
waktu konsentrasi Desirability
#1 #2 #3 #4 #5 #6 #7 #8 #9 #10 #11 #12 #13 #14 #15 #16 #17
#18#20#210.#22#23#24#25#26#27#28#29#30#31#32#33#34#35#36#37#38#39#40#41#42#43#44#45#46#47#49#50.5#51#52#53#54#55#56#57#58#59#60#61#62#63#64#65#66#67#68#69#70#71#72#73#74#75#76#96#88#95#94#93#92#91#90#89#78#87#86#85#84#83#82#81#80#79#971. 1202.0 3100.1 4998.2
QA
A
10.000 75.562 110.00
#1 #2 #3 #4 #5 #6 #7 #8 #9 #10 #11 #12 #13 #14 #15 #16 #170.
#19#20#21#22#23#24#25#26#27#28#29#30#31#32#33#34#35#36#37#38#39#40#41#42#43#44#45#46#47#49#50.5#51#52#53#54#55#56#57#58#59#60#61#62#63#64#65#66#67#68#69#70#71#72#73#74#75#76#77#95#88#94#93#92#91#90#89#87#79#86#85#84#83#82#81#801. 28.115 58.103 88.091
%A
A
1. 3.
.73968
30. 60. 50. 150.
D
e
sira
b
ilit
y
Kondisi optimum yang dihasilkan: waktu = 60 menit
21
Lampiran 10 Isoterm Langmuir dan Freundlich untuk adsorpsi cibacron red oleh
adsorben tanpa modifikasi
C0 *Ca
(ppm) (ppm) Isoterm Langmuir
Isoterm Freundlich
No m (g) c x* x/m log c log x/m
1 0
2 25 24.2839 1.0001 24.2839 0.7161 0.7160 1.3853 -0.1451
3 50 48.3175 1.0000 48.3175 1.6825 1.6825 1.6841 0.2260
4 75 72.5362 1.0002 72.5362 2.4638 2.4633 1.8606 0.3915
5 100 94.1526 1.0000 94.1526 5.8474 5.8474 1.9738 0.7670
6 150 142.2038 1.0003 145.2038 7.9039 7.9015 2.1526 0.8977 * Ca digunakan sebagai variabel c pada rumus Isoterm Langmuir dan Freundlich
Bobot biosorben digunakan sebagai variabel m pada rumus Isoterm Langmuir dan
Freundlich
Nilai x = C0−Ca
Persamaan garis isoterm Langmuir yang diperoleh y = 0.0652x – 1.2481 dengan r =
94.13%, maka dari persamaan
1
1
C
m
/
x
C
α
+
αβ
=
, diperoleh nilai α = 15.3374 dan β = –0.0052
Persamaan garis isoterm Freundlich yang diperoleh y = 1.4096x − 2.1257 dengan r=
96.50%, maka dari persamaan Log (
m
x
) =
n
1
Log C + Log k, diperoleh nilai n = 0.7094
22
Lampiran 11 Isoterm Langmuir dan Freundlich untuk adsorpsi cibacron red oleh adsorben
modifikasi asam
C0 *Ca
(ppm) (ppm) Isoterm Langmuir
Isoterm Freundlich
No m (g) c x* x/m log c log x/m
1 0
2 25 0.1187 1.5000 0.1187 24.8813 16.5875 -0.9256 1.2198
3 50 1.2186 1.5002 1.2186 48.7814 32.5166 0.0859 1.5121
4 75 6.8376 1.5002 6.8376 68.1624 45.4356 0.8349 1.6574
5 100 8.5338 1.5004 8.5338 91.4662 60.9612 0.9311 1.7851
6 150 23.8203 1.5000 23.8203 126.1797 84.1198 1.3769 1.9249 * Ca digunakan sebagai variabel c pada rumus Isoterm Langmuir dan Freundlich
Bobot biosorben digunakan sebagai variabel m pada rumus Isoterm Langmuir dan
Freundlich
Nilai x = C0−Ca
Persamaan garis isoterm Langmuir yang diperoleh y = 2.5945x + 26.8934 dengan r =
89.56%, maka dari persamaan
1
1
C
m
/
x
C
α
+
αβ
=
, diperoleh nilai α = 0.3854 dan β =0.0965
Persamaan garis isoterm Freundlich yang diperoleh y = 0.2961x + 1.4834 dengan r=
97.51%, maka dari persamaan Log (
m
x
) =
n
1
Log C + Log k, diperoleh nilai n = 3.3772
23
Lampiran 12 Isoterm Langmuir dan Freundlich untuk adsorpsi cibacron red oleh arang
aktif
C0 *Ca
(ppm) (ppm) Isoterm Langmuir
Isoterm Freundlich
No m (g) c x* x/m log c log x/m
1 0
2 25 7.3294 3.0001 7.3294 17.6706 5.8900 0.8651 0.7701
3 50 14.2895 3.0003 14.2895 35.7105 11.9025 1.1550 1.0756
4 75 17.8247 3.0002 17.8247 57.1753 19.0572 1.2510 1.2801
5 100 19.2493 3.0002 19.2493 80.7507 26.9155 1.2844 1.4300
6 150 26.8301 3.0004 26.8301 123.1699 41.0512 1.4286 1.6133 * Ca digunakan sebagai variabel c pada rumus Isoterm Langmuir dan Freundlich
Bobot biosorben digunakan sebagai variabel m pada rumus Isoterm Langmuir dan
Freundlich
Nilai x = C0−Ca
Persamaan garis isoterm Langmuir yang diperoleh y = 1.8683x – 10.9935 dengan r =
94.33%, maka dari persamaan
1
1
C
m
/
x
C
α
+
αβ
=
, diperoleh nilai α = 0.5352 dan β = –0.1699
Persamaan garis isoterm Freundlich yang diperoleh y = 1.5220x – 0.5878 dengan r=
96.09%, maka dari persamaan Log (
m
x
) =
n
1
Log C + Log k, diperoleh nilai n = 0.6570
24
Lampiran 13 Penentuan intensitas warna dan persen penurunan warna untuk adsorpsi
limbah industri tekstil
Jenis adsorben
Waktu (menit)
Bobot (g)
Gambar Intensitas warna (unit Pt-Co)
% Penurunan
warna
Limbah - - 788 -
ATM 45 1.0004 772 2.03
AMA 60 1.5005 23 97.08
Arang aktif