BAB II
TINJAUAN PUSTAKA
2.1 Definisi Gastritis
Gastritis adalah proses inflamasi pada mukosa dan submukosa lambung sebagai respon terhadap jejas (injury) yang dapat bersifat akut maupun kronik.1
Gastritis adalah inflamasi mikroskopis yang merupakan diagnosis histologis, bukan klinis. Sejak tahun 1761, Morgagni menggunakan istilah erosi untuk mendeskripsikan gastritis. Gastritis (erosi gaster) didefinikan adanya kerusakan mukosa yang tidak menembus mukosa muskularis. Perbedaan antara gastritis dan ulkus gaster berdasarkan kedalaman rusaknya mukosa, sementara ulkus gaster menembus sampai mukosa muskularis. Dari endoskopi, kedalaman rusaknya mukosa hanya bisa diperkirakan. Durasi gastritis bisa akut, kronik, maupun rekuren. Gastritis sering ditemukan pada 3-12% subjek penelitian yang asimtomatik dan 4-49% pada pasien klinis.17
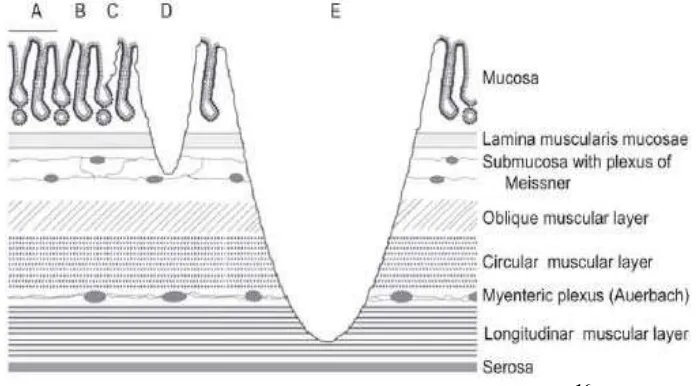
Gambar 2.1. Struktur potong lintang dinding gaster.16
Pada sebagian besar kasus inflamasi mukosa gaster tidak berkorelasi dengan keluhan dan gejala klinis pasien. Sebaliknya keluhan dan gejala klinis pasien berkorelasi dengan komplikasi gastritis.18
2.2 Epidemiologi Gastritis
Gastritis merupakan salah satu masalah kesehatan yang umum terjadi, hampir 10% dari orang-orang yang dirawat dibagian unit gawat darurat rumah sakit datang dengan kasus gastritis. Berdasarkan penelitian WHO ( World Health Organization ) dilaporkan prevalensi gastritis dibeberapa negara sebagai berikut: Inggris 22%, China 31%, Kanada 3%, dan Perancis 29,5%. Sekitar 1,8-2,1 juta penduduk mengalami gastritis setiap tahunnya.19
Angka kejadian gastritis menurut WHO adalah 40,8%, dan merupakan salah satu dari sepuluh penyakit terbanyak pada passien rawat inap di rumah sakit.19
2.3. Klasifikasi Gastritis
Terdapat beberapa klasifikasi dari gastritis antara lain klasifikasi berdasarkan infiltrat inflamasi yang membagi menjadi akut dan kronik; klasifikasi secara makroskopis yang membagi menjadi gastritis erosiva dan non erosiva; klasifikasi berdasarkan endoskopi yang membagi menjadi gastritis komplit, inkomplit, dan erosif hemoragik; serta klasifikasi menurut ICD-10.
2.3.1 Klasifikasi Berdasarkan Infiltrat Inflamasi
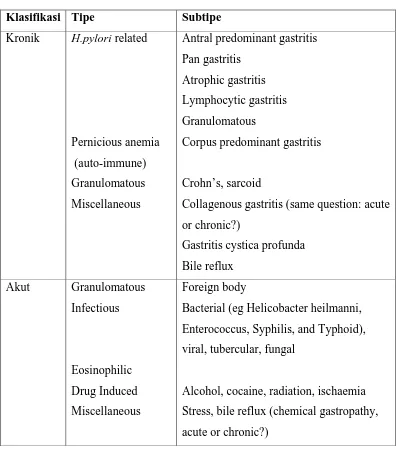
Tabel 2.1. Klasifikasi Gastritis Akut dan Kronik. 1
Klasifikasi Tipe Subtipe
Kronik H.pylori related
Pernicious anemia (auto-immune) Granulomatous Miscellaneous
Antral predominant gastritis Pan gastritis
Atrophic gastritis Lymphocytic gastritis Granulomatous
Corpus predominant gastritis
Crohn’s, sarcoid
Collagenous gastritis (same question: acute or chronic?)
Gastritis cystica profunda Bile reflux
Akut Granulomatous
Infectious
Eosinophilic Drug Induced Miscellaneous
Foreign body
Bacterial (eg Helicobacter heilmanni, Enterococcus, Syphilis, and Typhoid), viral, tubercular, fungal
Alcohol, cocaine, radiation, ischaemia Stress, bile reflux (chemical gastropathy, acute or chronic?)
2.3.2 Klasifikasi secara Makroskopis
trauma langsung. Erosi superfisial dan lesi mukosa punktata bisa terjadi. Erosi dalam, ulkus, bahkan perforasi terjadi pada kasus berat atau yang tidak ditangani. Lesi khas muncul di korpus, tetapi antrum juga bisa terlibat. Ciri khas dari gastritis erosiva adalah lesi mukosa tidak menembus lapisan mukosa muskularis. Sementara gastritis non-erosiva mengacu pada kelainan histologis yang terutama akibat infeksi H.pylori. Kebanyakan pasien gastritis non-erosiva asimtomatis.21
2.3.3 Klasifikasi Gastritis Berdasarkan Endoskopi
Klasifikasi ini membagi gastritis menjadi gastritis komplit dengan tipe matur dan imatur, gastritis inkomplit, serta gastritis erosif hemoragik.
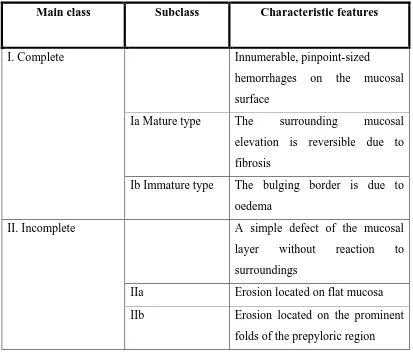
Tabel 2.2. Klasifikasi gastritis berdasarkan endoskopi 17
Main class Subclass Characteristic features
I. Complete Innumerable, pinpoint-sized
hemorrhages on the mucosal surface
Ia Mature type The surrounding mucosal
elevation is reversible due to fibrosis
Ib Immature type The bulging border is due to
oedema
II. Incomplete A simple defect of the mucosal
layer without reaction to surroundings
IIa Erosion located on flat mucosa
IIb Erosion located on the prominent
III.Hemorrhagic-erosive gastritis
Innumerable, pinpoint-sized
hemorrhages on the mucosal surface with erythrodiapedesis and engorged blood vessels within mucosa and submucosa
2.4 Etiologi Gastritis
Berikut akan dijelaskan etiologi gastritis. Rugge M membagi etiologi gastritis berdasarkan agen yang ditransmisikan, kimiawi, fisik, faktor imun, dan idiopatik. Rugge M juga membagi etiologi gastritis berdasarkan 3 bentuk utama antara lain gastritis Helicobacter pylori, gastritis kimiawi, dan gastritis autoimun. Lalu Toljamo K mengelompokkan berbagai etiologi gastritis menjadi 3 kelompok yaitu agen kimiawi, penyakit, dan faktor fisik/ mekanik. Adapun Adibi P menuliskan etiologi gastritis menjadi 2 bagian besar yaitu gastritis Helicobacter
pylori dan gastritis non Helicobacter pylori.
Sedangkan gastritis kronik didefenisikan secara histology berupa peningkatan jumlah limfosit dan sel plasma pada mukosa lambung. Berdasarkan etiologi gastritis kronik dikelompokkan menjadi tipe A, yaitu berasal dari autoimun, tipe B yaitu berasal dari infeksi H. pylori dan beberapa kasus lain dengan etiologi yang belum jelas. Secara endoskopi mukos menunjukkan gambaran atropi.Sedangkan secara histology ditemukan infiltrasi sel limfosit-plasma pada daerah mukosa sel-sel parietal. Neutrofil jarang ditemukan. Mukosa dapat menunjukkan perubahan kea rah metaplasia intestinal.Pada stsdium akhir mukosa atropi dan sel-sel parietal tidak ditemukan namun H. pylori dapat ditemukan. Gejala gastritis kronik dapat asimtomatik, beberapa gejala yang dapat ditemukan berupa nyeri epigastrium ringan, mual, tidak nafsu makan. Pemeriksaan endoskopi perlu dilakukan oleh karena gastritis kronik beresiko terhadap terjadinya ca gaster. Pasien gastritis tipe A memiliki kelainan autoimun pada organ lain khususnya penyakit tiroid.22
2.4.1 Etiologi Gastritis Berdasarkan Agen yang Ditransmisikan, Kimiawi, Fisik, Imun dan Idiopatik
Berikut ditampilkan tabel etiologi gastritis yang ditulis oleh Rugge M.
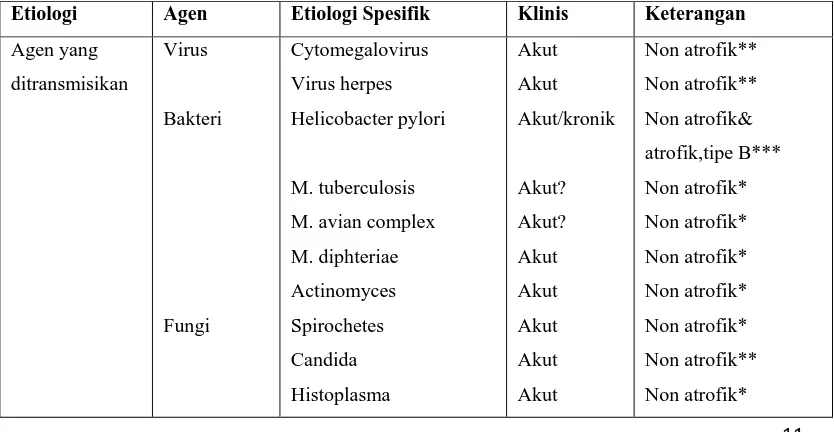
Tabel 2.3. Etiologi Gastritis Berdasarkan Agen yang Ditransmisikan, Kimiawi, Fisik, Imun, dan Idiopatik 2
Etiologi Agen Etiologi Spesifik Klinis Keterangan
Agen yang
M. avian complex
Parasit Phycomycosis
Non atrofik &
atrofik ***
Non atrofik,tipe C***
Non atrofik,tipe C**
Non atrofik,tipe C*
Non atrofik,tipe C***
Agen Fisik Radiasi Akut/kronik Non atrofik &
atrofik*
Immuno-mediated
Autoimun
Obat : Ticlopidine
?Gluten
Non atrofik & atrofik
Non atrofik &
atrofik*
Idiopatik Crohn’s disease
Sarkoidosis
2.4.2. Etiologi Utama menurut Adibi P
Adibi P menulis ada 2 etiologi utama dari gastritis yaitu gastritis
H.pylori dan gastritis non H.pylori.20
Berbagai macam penyebab terjadinya gastritis non H.pylori antara lain: 1. Gastritis kimiawi
i. Gastritis alkoholik
ii. Gastritis yang diinduksi obat
Obat yang berhubungan dengan gastritis antara lain acarbose, alkohol, antibiotik (eritromisin oral), bifosfonat, herbal (garlic, ginkgo, saw palmetto, feverfew, chaste tree
berry, white willow), zat besi, metformin, miglitol, NSAID
(termasuk COX-2), opiat, orlistat, potasium klorida (KCl), teofilin.
iii. Gastritis refluks (empedu atau duodenal juice) iv. Gastritis kimiawi lainnya
2. Gastritis radiasi 3. Gastritis alergi 4. Gastritis autoimun
5. Bentuk khusus gastritis, gastritis NOS/ unspecified 6. Duodenitis
2.5 Patofisiologi
2.5.1 Patofisiologi Gastritis secara Umum
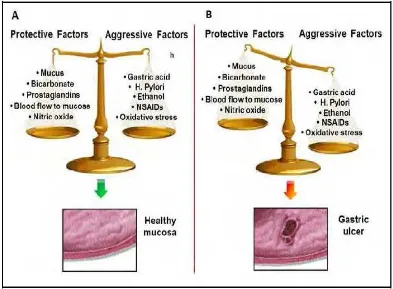
Gambar 2.2. Patofisiologi Gastritis 24
Keterangan : (A) mukosa gaster normal akibat adanya keseimbangan antara faktor agresif dan pertahanan mukosa. (B) pembentukan ulkus gaster karena ketidakseimbangan faktor agresif dan faktor pertahanan mukosa.
2.5.2 Patofisiologi Gastritis akibat NSAID
menjaga integritas mukosa dan aliran darah mukosa. NSAID dapat menekan aktivitas COX-1, yang berakibat pada lesi mukosa gaster.25
Aspirin, salah satu NSAID yang digunakan secara luas di klinis bisa menyebabkan stres ulcer dan mengeksaserbasi ulkus gaster sebelumnya. Interaksi NSAID dan stres dapat menyebabkan lesi pada gaster dengan salah satu mekanismenya adalah dengan meningkatkan sitokin inflamasi salah satunya TNF-α.26
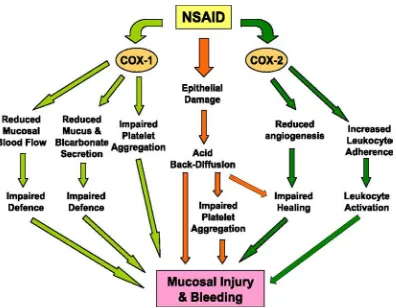
Gambar 2.3. Pembentukan lesi gaster akibat NSAID 27
mengganggu mikrosirkulasi lokal, yang berdampak terjadinya nekrosis iskemik. Penggunaan NSAID jangka panjang pada pasien H.pylori secara signifikan menyebabkan erosi yang lebih berat dibandingkan pada pada pasien yang tidak terinfeksi H.pylori, namun hal ini masih kontroversi.17
2.5.3 Patofisologi Gastritis Helicobacter pylori
H.pylori tinggal di lapisan mukus yang melapisi epitel gaster. H.pylori
mensekresikan faktor-faktor, peptida, dan lipopolisakarida yang bersifat kemotaktik terhadap neutrofil dan monosit. In vivo, infeksi H.pylori di mukosa gaster menginduksi produksi sitokin-sitokin IL-1β, IL-6, IL-8 dan TNF-α. IL-1 atau TNF-α saja, maupun TNF-α bersinergis dengan IFN-γ menginduksi produksi IL-8 di sel gaster. Peningkatan produksi IL-8 bisa disebabkan infeksi H.pylori maupun sekunder dari peningkatan kadar IL-1 atau TNF-α. Produksi IL-8 oleh sel epitel gaster berkepanjangan dapat menyebabkan rekruitmen neutrofil dan limfosit ke jaringan yang terinfeksi.21
H.pylori menginduksi sitokin-sitokin proinflamasimelalui aktivasi NF-κB. Aktivasi NF-κB oleh infeksi H. pylori menginduksi ekspresi berbagai gen, termasuk pengkodean sitokin interleukin (IL)-1, IL-6. IL-8,TNFα, faktor pertumbuhan endotel vaskular (VEGF), siklooksigenase 2 (COX-2), sintesa diinduksi oksida nitrat (iNOS), regulator siklus sel , matrix metalloproteinase (MMP) -2, MMP-7, MMP-9 dan molekul adhesi.25 Respons inflamasi yang terjadi menyebabkan Treg mensekresikan sitokin imunosupresif, yang mempertahankan kadar H.pylori dalam mukosa gaster. Peran Treg dalam memodulasi respon imun pejamu selama infeksi H.pylori telah beberapa kali dipikirkan. Treg adalah subset dari sel T yang mensupresi respon imun pejamu dan berhubungan dengan kanker.5
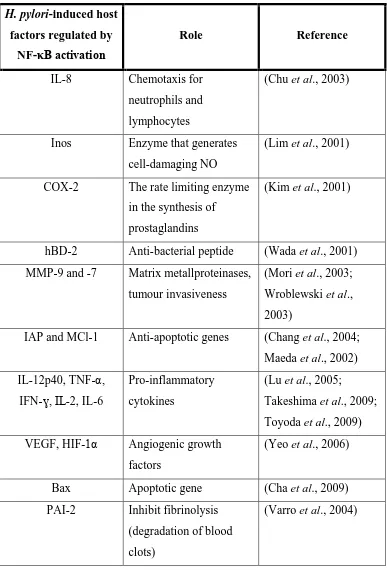
Tabel 2.4. Faktor-faktor pejamu yang diregulasi oleh aktivasi NF-κB sebagai respons terhadap infeksi H.pylori30
H. pylori-induced host
factors regulated by NF-κB activation
Role Reference
IL-8 Chemotaxis for
neutrophils and lymphocytes
(Chu et al., 2003)
Inos Enzyme that generates
cell-damaging NO
(Lim et al., 2001)
COX-2 The rate limiting enzyme
in the synthesis of prostaglandins
(Kim et al., 2001)
hBD-2 Anti-bacterial peptide (Wada et al., 2001)
MMP-9 and -7 Matrix metallproteinases,
tumour invasiveness
(Mori et al., 2003; Wroblewski et al., 2003)
IAP and MCl-1 Anti-apoptotic genes (Chang et al., 2004;
Maeda et al., 2002)
Takeshima et al., 2009; Toyoda et al., 2009)
VEGF, HIF-1α Angiogenic growth
factors
(Yeo et al., 2006)
Bax Apoptotic gene (Cha et al., 2009)
PAI-2 Inhibit fibrinolysis
(degradation of blood clots)
2.6 Diagnostik Gastritis Helicobacter pylori
Metode diagnostik untuk mendeteksi kuman H. pylori dibagi menjadi pemeriksaan invasif dan pemeriksaan non invasif. Beberapa metode telah dikembangkan untuk mendeteksi keberadaan infeksi kuman H pylori, yang dapat dilihat pada tabel di bawah ini.
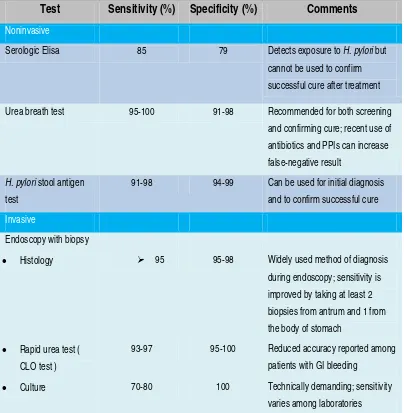
Tabel 2.5. Pemeriksaan diagnostik untuk Helicobacter pylori 31
Test Sensitivity (%) Specificity (%) Comments
Noninvasive
Serologic Elisa 85 79 Detects exposure to H. pylori but cannot be used to confirm successful cure after treatment
Urea breath test 95-100 91-98 Recommended for both screening and confirming cure; recent use of antibiotics and PPIs can increase false-negative result
H. pylori stool antigen test
91-98 94-99 Can be used for initial diagnosis and to confirm successful cure Invasive
Endoscopy with biopsy
• Histology 95 95-98 Widely used method of diagnosis during endoscopy; sensitivity is improved by taking at least 2 biopsies from antrum and 1 from the body of stomach
• Rapid urea test ( CLO test )
93-97 95-100 Reduced accuracy reported among patients with GI bleeding
2.7 Hubungan Sitokin Inflamasi dengan Gastritis 2.7.1 Sitokin Inflamasi terhadap Gastritis non H.pylori
Kadar serum sitokin seperti IL-6, TNF-α, IL-1β, dan IFN-γ pada pasien yang mengalami inflamasi lebih tinggi daripada individu normal. Penurunan kadar IL-6 dan TNF-α merupakan petunjuk terjadinya perbaikan inflamasi. IL-6 disekresikan oleh sel T dan makrofag untuk menstimulasi respons imun terutama selama ada kerusakan jaringan yang menyebabkan terjadinya inflamasi. IL-6 juga berperan dalam melawan infeksi. TNF-α merupakan sitokin yang terlibat dalam inflamasi sistemik dan termasuk kelompok sitokin yang menstimulasi reaksi akut. TNF-α menginduksi apoptosis dan inflamasi. IL-6 dan TNF-α berperan dalam lesi di lambung.32
Cedera pada lambung akibat kimiawi seperti NSAID bisa menyebabkan peningkatan ekspresi mediator inflamasi seperti TNF-α, IL-1β, maupun IL-8. Penelitian Lee et al pada tikus menemukan pemberian indometasin secara signifikan meningkatkan ekspresi TNF-α, IL-1β, IL-8 pada sel epitel gaster. Hal ini mengkorfirmasi mediator inflamasi berperan dalam kerusakan sel epitel gaster akibat indometasin. Menurut Tanigawa T, et al pemberian PPI bisa menurunkan produksi TNF-α dan IL-1β. Jadi PPI memiliki efek anti inflamasi dengan menekan secara langsung induksi TNF-α dan IL-1β melalui inhibisi NF-κB dan aktivasi ERK pada sel-sel inflamasi. Penelitian Tanigawa T, et al dan Lee HJ, et al mengkonfirmasi bahwa pada erosi gaster terjadi peningkatan sitokin-sitokin inflamasi.33,34
Gastritis kimiawi/ gastropati seperti NSAID memiliki berbagai patogenesis/ mekanisme yang menyebabkan cedera seperti inhibisi prostaglandin, efek toksik langsung dari NSAID, dan stimulasi sitokin proinflamasi seperti TNF-α, IL-1β, IL-6, IL-8, IFN-γ dan infiltrasi sel-sel inflamasi di lamina propria yang menyebabkan penurunan aliran darah mukosa, hipoksia, dan penurunan pertahanan mukosa.35
TNF-α. Adanya penurunan sitokin proinflamasi ini setelah mendapatkan gastroprotektor.32
Penelitian Eamlamnam K, et al pada lesi gaster akut yang diinduksi asam asetat terjadi peningkatan leukosit, TNF-α, dan penurunan IL-10. Sehingga saat terjadi proses penyembuhan terjadi penurunan TNF-α dan leukosit serta peningkatan kadar IL-10. Pada inflamasi gaster kronik terjadi peningkatan IL-10 yang secara simultan mengurangi inflamasi jaringan gaster. Peningkatan IL-10 sebagai sitokin antiinflamasi guna menekan inflamasi di gaster.36
Naito Y, et al dan Jainu M, et al melaporkan bahwa inflamasi gaster mukosa akibat aspirin akibat peningkatan produksi TNF-α dan IL-1 yang berdampak pada akumulasi neutrofil.37,38
Iskemiapun menginduksi lesi gaster, kemungkinan akibat banyak pembentukan radikal bebas, tetapi peranan sitokin proinflamasi seperti IL-1β dan TNF-α dalam proses penyembuhan lesi ini belum dipelajari mendalam. Konturek PC, et al melakukan percobaan pada tikus menemukan bahwa lesi gaster dimediasi oleh pembentukan radikal bebas, menyebabkan supresi mikrosirkulasi gaster dan aktivitas sekresi dari gaster. Serta terjadi peningkatan superoksida dismutase dan pelepasan IL-1β dan TNF-α bisa mengaktivasi ekspresi ICAM-1 dan infiltrasi neutrofil, yang berperan penting dalam progresivitas iskemia yang menginduksi erosi gaster akut menjadi ulkus kronis.39
2.7.2 Sitokin Inflamasi terhadap Gastritis H.pylori
H. pylori yang menginfeksi kurang lebih 50% penduduk di seluruh
dunia, yang menyebabkan inflamasi lambung kronis yang akan menjadi atrofi, metaplasia, displasia dan akhirnya kanker lambung.3
inflamasi. Adanya inflamasi karena H. pylori dapat ditunjukkan dengan peningkatan IL-1β, IL-2, IL-6, IL-8 dan TNF-α.39
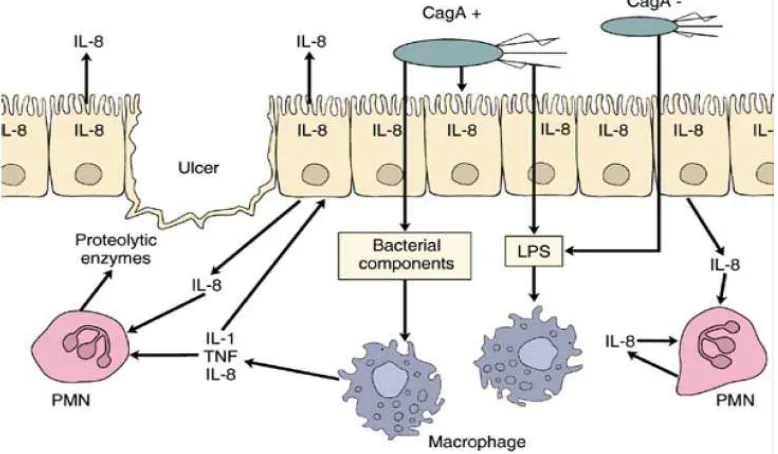
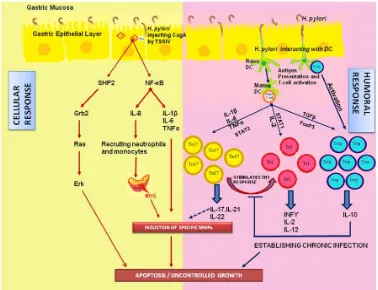
Inflamasi lambung ditemukan bervariasi pada pasien yang terinfeksi dengan H. pylori tergantung dari respon imun pejamu terhadap organisme. Mekanisme inflamasi terhadap infeksi H pylori melibatkan respon imun spesifik dan imun non spesifik, seperti terlihat pada gambar di bawah ini. Proses tersebut juga akan menimbulkan keluarnya mediator sitokin, pada gastritis karena H. pylori, seperti pada tabel di bawah.41
Tabel 2.6. Sitokin yang dihasilkan sebagai implikasi dari gastritis
H. pylori 41
Mediator Usual actions
Cytokines
TNF-α Pro-inflammatory (activation of leukocytes)
IL-1α/β Pro-inflammatory (activation of leukocytes)
IL-6 Pro-inflammatory, B-and T-cell
activation/differentiation
IL-7 T- and B- cell regulation
IL-10 Immune down-regulation
IL-12 Stimulation of Th1 response
IFN-ɣ Pro-inflammatory, especially cellular immunity
GM-CSF Pro-inflammatory, maturation factor
Chemokines
IL-8 Neutrophil recruitment and activation
GRO-α Neutrophil recruitment and activation
RANTES Mononuclear cell recruitment and activation
MIP-1α Mononuclear cell recruitment and activation
TNF-α berperan untuk meningkatkan reaksi inflamasi dan diyakini berperan penting dalam kerusakan mukosa gaster akibat H.pylori. TNF-α menyebabkan kaskade inflamasi terhadap infeksi, respons inflamasi berlebihan di mukosa gaster yang berhubungan dengan inhibisi sekresi asam lambung dan kerentanan yang lebih tinggi terhadap Ca gaster.42
Infeksi H.pylori berkontribusi terhadap rekrutmen neutrofil dan limfosit yang menyebabkan kerusakan epitel melalui pelepasan sitokin, salah satunya TNF-α. Bodger K, et al melaporkan bahwa ada hubungan signifikan antara IL-6, IL-8, TNF-α pada pasien yang terinfeksi H.pylori. Sitokin ini
berkorelasi dengan derajat inflamasi dan aktivitas neutrofil, di mana makin tinggi kadar sitokin sebanding dengan peningkatan derajat inflamasi dan aktivitas neutrofil.41
menekan inflamasi dan mendukung kolonisasi H.pylori yang lebih lama pada mukosa gaster.43,44,30
2.8 Matrix metalloproteinase pada Infeksi H. pylori
Proteinase adalah satu kelas enzim yang mampu menghidrolisa ikatan peptida. Biokatalis ini secara garis besar dibagi menjadi dua kelompok utama: eksopeptidase dan endopeptidase. Mereka dibagi lagi menjadi protease serin, protease Treonin, protease Sistein, protease Aspartat, metalloprotease, protease asam glutamat berdasarkan sifat katalitik mereka. Sumber protease dibatasi terutama untuk perut, pankreas dan usus kecil, dimana mereka dimanfaatkan untuk pencernaan protein. Matrix metalloprotein (MMP) adalah Zn yang membutuhkan endopeptidases, pemain penting untuk remodeling jaringan ECM (Extra cellular matrix). Bakteri virulen yang mendiami usus kadang-kadang mengeluarkan protease yang dapat langsung mengaktifkan MMP tuan rumah, sehingga meningkatkan efisiensi biokimia mereka untuk mendegradasi ECM penjamu.5
Degradasi ECM merupakan langkah penting dalam terjadinya ulkus mukosa lambung. Matrix metalloproteinase (MMP) mampu meluruhkan ECM dan terlibat dalam respon immunologi pada infeksi H. Pylori. Dengan demikian gen pengkodean protein ini merupakan kandidat fungsional yang ideal untuk investigasi profil genetik individual yang beresiko untuk terjadinya ulkus lambung pada infeksi H. Pylori.15
faktor larut, perubahan dalam bentuk sel, mekanik dan stres oksidatif juga dapat mengakibatkan induksi MMP.45
Selama infeksi H. pylori, sel-sel epitel gaster menghasilkan MMP dalam menanggapi berbagai rangsangan inflamasi. Oleh karena itu, IL-21 dapat mengatur produksi MMP melalui sel-sel epitel gaster.13
Sesuai dengan preferensi substrat, MMPs dapat dibagi menjadi enam
kelompok: kolagenase (MMP-1, -8, -13), gelatinase (MMP-2-9),
stromelysin(MMP-3,-10, 11,-19), matrilysin (MMP-7,-26), MTMMPs (MMP-14,-15,-16,-17,-23,-24,-25), dan kelompok heterogen (MMP-12,-20,-21,-27,-28).45
2.9 Matrix metalloprotein (MMP)-7
MMP-7, yang juga disebut matrilysin, memiliki aktivitas proteolitik luas dan mampu mengaktifkan MMPs lainnya, sehingga mungkin memainkan beberapa peran selama remodeling jaringan.11
MMP-7 dinyatakan dalam jaringan normal seperti paru-paru, monosit, endometrium, sel-sel mesangial, dan dalam epitel duktal dan kelenjar. Berbeda dengan MMPs lainnya, yang biasanya diekspresikan dalam stroma jaringan, MMP-7 dinyatakan terutama dalam sel-sel tumor. Selain degradasi matriks ekstraseluler, MMP-7 meningkatkan perkembangan tumor dengan menghambat apoptosis pada sel-sel kanker, dengan mengurangi adhesi sel dan dengan merangsang angiogenesis.11
Respon awal untuk infeksi H. pylori melibatkan peningkatan MMP-7, yang pada gilirannya akan meningkatkan IGF-II ekstraseluler fungsional, dengan demikian merangsang proliferasi sel epitel dan myofibroblast. Induksi awal sistem ini dapat dianggap sebagai bagian dari respon kerusakan epitel. 46
stimulan myofibroblast. MMP-7 dilepaskan dari kultur kelenjar lambung manusia dengan cara H. pylori mengatur proliferasi myofibroblasts utama lambung manusia, diduga, substrat MMP-7 yang relevan dapat diidentifikasi dalam media myofibroblasts lambung, dan MMP-7 mempengaruhi aksi myofibroblasts dalam mengendalikan proliferasi sel epitel.46
MMP-7 meningkat pada mukosa lambung subjek yang terinfeksi H.
Pylori. Dibanding MMP lainnya, MMP-7 relatif tidak biasa dan diproduksi
terutama di sel-sel epitel. Substratnya termasuk protein matriks ekstraseluler, selain itu sekarang sudah jelas bahwa MMP-7 dapat melepaskan berbagai macam sitokin dan faktor pertumbuhan, termasuk Fas ligan, tumor necrosis factor, HB-epidermal growth factor(HB-EGF) dan kemokin. 46
H. pylori dapat meningkatkan sekresi MMP-1 dan MMP-3 dalam sel
lambung manusia, dan peningkatan kadar MMP-7 dan MMP-9 ditemukan di mukosa lambung yang terinfeksi H. pylori. MMPs tidak hanya terlibat dalam respons peradangan mukosa tetapi juga dalam patogenesis H. pylori-terkait ulkus lambung, dan dengan demikian menggambarkan calon gen yang ideal untuk studi genetik.15
MMP-7 terlokalisasi pada pinggir koloni epitel sel lambung. Tingkat penyebaran sel kelenjar lambung lebih tinggi pada kultur yang teinfeksi H.
pylori dibandingkan dengan kontrol, dan ini dihambat oleh antisense oligo
nukleotida MMP-7. Ada bukti lebih lanjut bahwa induksi MMP-7 dalam Mukosa lambung oleh strain kuman H. pylori tertentu. MMP-7 dinyatakan dalam sel-sel epitel gaster dari 80% spesimen penderita yang terkolonisasi H.
pylori cag(+), tetapi tidak pada cag(−) atau subjek yang tidak terinfeksi.
Strain H. pylori cag (+) meningkatkan ekspresi MMP-7 di AGS sel 5-7 kali lipat, sedangkan cag(-) tidak berpengaruh. Inaktivasi cagE, tapi tidak cagA atau vacA, benar-benar melemahkan induksi MMP-7.15
Induksi MMP-7 berlangsung selama ada respon dari sel epitel terhadap infeksi bakteri.47
Aktivasi NF-κB oleh infeksi H. pylori menginduksi ekspresi berbagai gen, termasuk pengkodean sitokin interleukin (IL)-1, IL-6. IL-8,TNFα, faktor pertumbuhan endotel vaskular (VEGF), siklooksigenase-2 (COX-2), sintesa diinduksi oksida nitrat (iNOS), regulator siklus sel , matrix metalloproteinase (MMP) -2, MMP-7, MMP-9 dan molekul adhesi.28
Ekspresi berlebihan MMP-7 telah ditunjukkan dalam berbagai jenis kanker. Dalam kanker lambung, ekspresi MMP-7 telah dikaitkan dengan perkembangan kanker dan kelangsungan hidup.48
Korelasi antara ekspresi MMP-7 dan virulensi bakteri, faktor cag+ pada subjek yang terinfeksi H.pylori telah banyak diobservasi.5
2.10 Kerangka Teori
Gambar 2.8. Kerangka Teori
Pasien Abdominal Discomfort
Dispepsia
Gastritis
Endoskopi: mukosa mengalami edema, eritema ( spotted, patchy, linear ) / eksudat / perdarahan / erosif.
Biopsi
CLO test: gel tetap kuning (negatif)/ berubah warna menjadi merah (positif)
MMP-7 ↑ MMP-7
Wawancara PADYQ: kuesioner dengan 11 pertanyaan yang mengevaluasi gejala nyeri epigastrium, mual, muntah, perut kembung, dan
early satiation. Gejala nyeri epigastrium, mual,
perut kembung bagian atas dinilai intensitas, durasi, dan frekuensi; sementara muntah dan
early satiationdinilai frekuensi. Skor > 6 :
dispepsia
Biopsi dilakukan pada 2 tempat kurvatura mayor dan minor antrum anterior