Yohana. J Syiah Kuala Dent Soc, 2017, 2 (2):97-101
[JDS]
JOURNAL OF SYIAH KUALA
DENTISTRY SOCIETY
Journal Homepage : http://jurnal.unsyiah.ac.id/JDS/97 PERBANDINGAN CAIRAN FIKSASI BOUIN DENGAN BUFFER FORMALIN TERHADAP HEPAR TIKUS PUTIH
Winny Yohana 1
1
Staf Biologi Oral Fakultas Kedokteran Gigi Universitas Padjadjaran
Abstract
Histopathological examination plays an important role in assisting the diagnosis of disease. One indispensable ingredient is a liquid fixation. fixation is a critical step in the preparation of histological section by which body tissue immersed in fixation liquid and preserved from decay thereby preventing autolysis and putrefaction. The aim of this study is to determine the better fixation in between bouin liquid and buffer formalin. The study was an experimental laboratory of two rats. A rat is injected fluids Bouin, others injected buffer formalin. The rat’s liver is taken and immersed into a fluid according to the injection of a liquid fixation. The rat’s liver was histologically prepared with hematoxylin eosin staining. The assessment by microscopically examination at 450X magnification. As an indicator seen from the changes in the nucleus of the cell, if there is a cell necrosis (bad) and normal cells (good). The study result shows that Bouin liquid got more normal cells (84.61%), while buffer formalin (38.46%). In conclusion, bouin liquid better than buffer formalin
Keywords: fixation, liquid bouin, buffer formalin
PENDAHULUAN
Pemeriksaan histopatologi berperan
penting dalam membantu menegakkan
diagnosa penyakit. Adapun tahapan dalam pembuatan sediaan adalah pengambilan jaringan, fiksasi, dehidrasi, clearing, embedding, blocking, pemotongan dan pewarnaan jaringan.1-4 Salah satu bahan yang diperlukan dalam pembuatan sediaan adalah cairan fiksasi. Tujuan fiksasi jaringan antara lain untuk mencegah terjadinya autolysis dan pembusukan, memelihara atau mengawetkan
Corresponding author
Email address : winnyspkga@yahoo.com
keadaan sel dan elemen jaringan agar identik dengan keadaan yang masih hidup, serta menggumpalkan jaringan yang cair agar memudahkan pemotongan sediaan.1-7
Cairan fiksasi yang biasa digunakan adalah cairan formalin dan buffer formalin yang hasilnya cukup memuaskan. Selain itu dapat pula dipergunakan cairan bouin yang mempunyai daya penetrasi yang lebih cepat dan merata.3-4, 7-10
Adapun tujuan penelitian ini adalah untuk mengetahui cairan fiksasi manakah yang daya penetrasinya lebih baik antara cairan buffer formalin dan cairan bouin. Untuk mengetahui baik tidaknya cairan fiksasi tersebut dapat dilihat dibawah mikroskop.
Yohana. J Syiah Kuala Dent Soc, 2017, 2 (2):97-101
98 BAHAN DAN METODE
Metode penelitian yang dipergunakan adalah metode eksperimental laboratorium, dengan tehnik pengumpulan secara sampling acak sederhana. Objek penelitian adalah tikus
dengan berat kurang lebih 200gram,
sedangkan yang menjadi subyek penelitian/ sampel adalah sel hepar tikus tersebut. Tujuan penelitian ini adalah untuk mengetahui cairan fiksasi manakah yang lebih baik diantara cairan formalin dan cairan buffer formalin. Salah satu cara untuk mengetahui baik tidaknya cairan fiksasi adalah dengan pemeriksaan di bawah mikroskop pada sediaan tersebut. secara matematis dapat dirumuskan sebagai berikut: Hasil sediaan merupakan fungsi dari fiksasi, artinya apabila fiksasi jaringan baik maka hasil sediaannya akan baik pula. Sebaliknya apabila fiksasi jaringan jelek maka hasil sediaannya akan jelek pula.
Indikator baik tidaknya sediaan adalah nekrosis sel dan detil sel yang terdapat pada sediaan. Untuk mengetahui indikan ini, maka diperlukan adanya suatu pengukuran dimana hal ini jenis ukuran yang dipergunakan adalah ukuran nominal. Ukuran nominal adalah suatu ukuran yang diberikan kepada indikan dengan menggunakan angka dengan tujuan untuk memberikan label dan tidak menunjukkan tingkatan apa-apa. Adapun label yang
dipergunakan adalah angka 1 untuk
menunjukkan hasil sediaan yang baik, dan angka 0 untuk menunjukkan hasil sediaan yang jelek. Berdasarkan uraian di atas dapat ditarik suatu hipotesis sebagai berikut:
Hipotesis nol: cairan bouin tidak lebih baik atau sama dengan cairan buffer formalin Hipotesis alternatif: cairan bouin lebih baik daripada cairan buffer formalin.
Bahan dan Alat-alat Penelitian
Bahan-bahan yang dipergunakan
adalah 2 ekor tikus dengan berat kurang lebih 200gram, chloretyl dan pentotal, cairan buffer formalin dan cairan bouin, alkohol, zat warna hematoksilin eosin. Sedangkan alat yang dipergunakan adalah: kapas, spuit, becker glass, scalpel, objek glass dan cover glass.
Cara Kerja
Mula-mula tikus dianestasi dengan chloretyl, lalu diteruskan dengan penyuntikan pentotal secara intraperitoneal, kemudian disectio di daerah rongga dada sampai bagian abdomen. Lalu disuntikkan cairan bouin.
Tikus yang satu lagi diberikan perlakuan yang sama namun disuntikkan buffer formalin lalu ditunggu 5 menit. Kemudian masing-masing hepar tikus diambil secukupnya dan direndam dalam becker glass yang telah diisi cairan fiksasi yang sesuai dengan keadaan sewaktu cairan fiksasi disuntikkan. Waktu yang dibutuhkan untuk
memfiksasi hepar disesuaikan menurut
kebutuhan.
Tahap selanjutnya sama seperti
pembuatan sediaan pada umumnya sampai pada pewarnaan hematoksilin eosin dan penyelesaiannya. Penilaian: dilakukan secara mikroskopis pembesaran 450 kali, dengan kriteria untuk nekrosis sel: Baik; apabila tidak terdapat nekrosis sel, Jelek: terdapat nekrosis sel untuk detil sel: baik; apabila tidak terjadi perubahan detil sel. Jelek; terjadi perubahan detil sel.
Data yang diperoleh melalui
pemeriksaan secara mikroskopis kemudian ditabulasikan kedalam bentuk tabel untuk dibandingkan kedua cairan buffer formalin dan cairan bouin.
HASIL
Hasil pengamatan secara mikroskopis dengan pembesaran 450 kali terhadap hepar tikus yang terdapat dalam tabel 1 dengan jumlah sampel 26 , di bawah ini pengujian hipotesis:
1 n1 = 26 p1 = 22/26 = 0,8461 = 84,6% 2 n2 = 26 p2 = 10/26 = 0,3846 = 38,46% Ho = p1 ≤ p2
H1 = p1≥ p2
Uji statistic , t hitung = 3,4193 t tabel = 1,7080
Oleh karena t hitung > t tabel maka Ho ditolak sehingga dapat disimpulkan bahwa cairan lebih baik daripada buffer formalin (detil sel).
Yohana. J Syiah Kuala Dent Soc, 2017, 2 (2):97-101
99
Tabel 1. Sel Hepar Difiksasi oleh Cairan Bouin dan Buffer Formalin (Detil sel)
Nomor sampel
Bouin Bufer Formalin
Baik jelek Baik Jelek
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X Jumlah 22 4 10 16
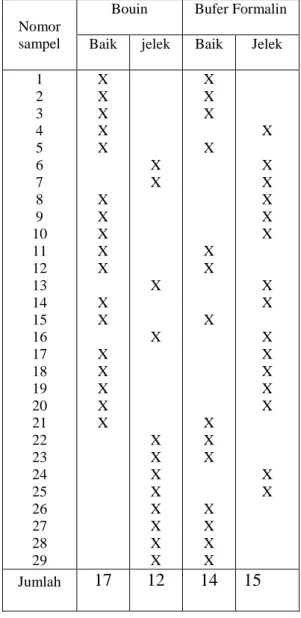
Hasil pengamatan secara mikroskopis dengan pembesaran 450 kali terhadap hepar tikus yang terdapat dalam tabel 2 dengan jumlah sampel 29 , dibawah ini pengujian hipotesis
1 n3 = 29 p3 = 17/29 = 0,5682 2 n4 = 29 p4 = 14/29 = 0,4827 Ho = p3 ≤ p4
H1 = p3≥ p4
Uji statistik, t hitung = 5,9482, t tabel = 1,7010
Oleh karena t hitung > t tabel maka Ho ditolak sehingga dapat disimpulkan bahwa cairan lebih baik daripada buffer formalin (nekrosis sel).
Tabel 2. Sel Hepar yang telah Difiksasi oleh Cairan Bouin dan Buffer Formalin (Nekrosis sel)
Nomor sampel
Bouin Bufer Formalin
Baik jelek Baik Jelek
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X X Jumlah 17 12 14 15
Gambar 1. Gambaran Mikroskopis 450
kali pada Sel Hepar Tikus Difiksasi Cairan Bouin.
Yohana. J Syiah Kuala Dent Soc, 2017, 2 (2):97-101
100
Gambar 2. Gambaran Mikroskopis 450
kali pada Sel Hepar Tikus Difiksasi Buffer Formalin.
PEMBAHASAN
Formalin merupakan cairan fiksasi yang dapat digunakan secara luas, baik sebagai cairan tunggal maupun sebagai campuran. Tetapi cairan ini tidak dapat
disimpan lama, karena akan terjadi
pengendapan paraformaldehid sehingga
terjadi penurunan konsentrasi formalin.1-3,10 Cairan formalin bersifat asam yang dapat dinetralisir sebelum dipakai dengan menambahkan Natrium karbonat. Efek utama formalin terhadap jaringan tubuh adalah
pengikatan protein tanpa menimbulkan
penggumpalan, serta mengikat lemak dengan tidak mempengaruhi lemak netral.1-6 Fiksasi dengan formalin membutuhkan waktu sekitar 3 sampai 7 hari.3-4
Cairan bouin dapat memfiksasi
jaringan lebih cepat daripada buffer formalin yaitu 6 sampai 24 jam. Cairan ini mengadakan pengikatan terhadap protein membentuk asam pikrat. Warna kuning pada specimen dapat dihilangkan dengan cara merendamnya pada alkohol 70%. Penggunaan cairan bouin ditujukan untuk mendapatkan gambaran mikroskopis yang baik.2-4,8,9
Berdasarkan hasil penelitian dapat
diterangkan bahwa cairan bouin lebih baik
dibandingkan cairan formalin dalam
keperluan fiksasi jaringan (khusus untuk sediaan kecil).
Pengamatan secara mikroskopis
menunjukkan bahwa pada pada jaringan yang difiksasi oleh cairan bouin, ternyata
menunjukkan sangat sedikit nekrosis sel serta menunjukkan detil sel yang baik. Cairan
formalin memfiksasi jaringan yaitu
menunjukkan adanya nekrosis sel dan ditemukan detil sel yang baik.
Perbandingan antara hasil penelitian dan studi kepustakaan ternyata baik cairan bouin maupun formalin dapat digunakan sebagai cairan fiksasi yang menghasikan detil sel yang baik. adapun nekrosis sel yang terjadi pada jaringan yang difiksasi oleh formalin kemungkinan diakibatkan oleh penurunan konsentrasi formalin tersebut.
KESIMPULAN
Hasil penelitian menunjukkan bahwa sediaan dengan menggunakan cairan fiksasi bouin lebih banyak sel yang normal (84,61%), sedangkan buffer formalin (38,46%). Cairan Bouin lebih baik daripada cairan buffer formalin.
DAFTAR PUSTAKA
1. Howat J William, Wilson A Beverley. Tissue fixation and the effect of molecular
fixatives on downstream staining
procedures. ScienceDirect. November 2014. vol. 70(1): 12-9.
2. Thavarajah R, Mudimbaimannar K. V, Elizabeth J, Rao K U, Ranganathan K. Chemical and Physical basic of Routine
Formaldehyde Fixation. J. Oral
Maxillofac Pathol Sep-Dec; 2012. 16(3): 400-5.
3. Bruce A. Johnson, Alexander, Lewis, Julian, Raff, Martin, Robert, Keith, Walter. Peter. Molecular Biology of the Cell: Histology Fixatives. New York and London: Garland Science. 2002.p.30-2. Available in https://cellbiology.med.unsw. 4. Mercer University School of Medicine
Savannah. Histotechniques. 2017.
Available in https://library.med.utah.edu/ 5. Gatta L Benerini, Cadel M, Balzarani P,
Castriciano S. Application of alternative fixatives to formalin in diagnostic
pathology. Eur J Histochem.
Yohana. J Syiah Kuala Dent Soc, 2017, 2 (2):97-101
101 6. Carson, Freida L; Christa Hladik.
Histotechnology: A Self Instructional Text. Hongkong: American Society for clinical Pathology Press. 2009. 3rd ed p2.
7. Bancroft,John D, Gamble, Marilyn.
Theory and practice of histology
techniques 6thed. China: Churchill Livingstone Elsevier 2008.p72.
8. Jensen K., Theory and Practice of Histological Techniques. Journal
of Neuropathology and
Experimental Neurology. Medical,
2008. p.433-8. Available in
https://books.google.co.id>books
9. Eltoum I, Fredenburgh J, Myers RB, Grizzle WE. Introduction to the theory and practice of fixation of tissues. J Histotechnol . 2001:24;173-4.
10.Rolls G. Fixation and Fixative: Factor
influencing chemical fixation,
formaldehyde and Glutaraldehyde.