SKRIPSI
PENGARUH KADAR ASAM OLEAT PADA SISTEM
NLC DENGAN LIPID SETIL ALKOHOL : ASAM
OLEAT DIBANDINGKAN DENGAN SLN TERHADAP
LAJU PELEPASAN APMS
AFINA F A
051111074
FAKULTAS FARMASI UNIVERSITAS AIRLANGGA DEPARTEMEN FARMASETIKA
SKRIPSI
PENGARUH KADAR ASAM OLEAT PADA SISTEM
NLC DENGAN LIPID SETIL ALKOHOL : ASAM
OLEAT DIBANDINGKAN DENGAN SLN TERHADAP
LAJU PELEPASAN APMS
AFINA F A
051111074
FAKULTAS FARMASI UNIVERSITAS AIRLANGGA DEPARTEMEN FARMASETIKA
LEMBAR PERSETUJUAN PUBLIKASI ILMIAH
Demi perkembangan ilmu pengetahuan, saya menyetujui skripsi saya dengan judul “Pengaruh Kadar Asam Oleat Pada Sistem NLC Dengan Lipid Setil Alkohol : Asam Oleat Dibandingkan dengan SLN Terhadap Laju Pelepasan APMS” untuk dipublikasikan atau ditampilkan di internet, digital library Perpustakaan Universitas Airlangga atau media lain untuk kepentingan akademik sebatas dengan Undang- Undang Hak Cipta.
Demikian pernyataan persetujuan publikasi skripsi ini saya buat dengan sebenarnya.
Surabaya, September 2015
LEMBAR PERNYATAAN
Saya yang bertanda tangan dibawah ini : Nama : Afina F. A
Nim : 05111074
Fakultas : FARMASI
Menyatakan dengan sesungguhnya bahwa hasil tugas akhir yang saya tulis dengan judul :
Pengaruh Kadar Asam Oleat Pada Sistem NLC Dengan Lipid Setil Alkohol : Asam Oleat Dibandingkan dengan SLN Terhadap Laju Pelepasan APMS
Adalah benar-benar merupakan hasil karya saya sendiri. Apabila dikemudian hari diketahui bahwa skripsi ini menggunakan data fiktif atau hasil plagiarisme, maka saya bersedia menerima sanksi berupa pembatalan kelulusan dan atau pencabutan gelar yang saya peroleh.
Demikian surat pernyataan ini saya buat untuk dipergunakan sebagaimana mestinya.
Surabaya, September 2015
Lembar Pengesahan
PENGARUH KADAR ASAM OLEAT PADA SISTEM
NLC DENGAN LIPID SETIL ALKOHOL: ASAM
OLEAT DIBANDINGKAN DENGAN SLN TERHADAP
LAJU PELEPASAN APMS
SKRIPSI
Dibuat untuk memenuhi syarat mencapai gelar Sarjana Farmasi pada
Fakultas Farmasi Universitas Airlangga 2015
Oleh :
AFINA F A NIM : 051111074
Skripsi ini telah disetujui oleh:
Pembimbing Utama Pembimbing Serta
KATA PENGANTAR
Puji syukur kepada Allah SWT atas segala nikmat dan karunia-Nya sehingga diselesaikannya penulisan skripsi dengan judul “Pengaruh Kadar Asam Oleat Pada Sistem NLC Dengan Lipid Setil Alkohol: Asam Oleat Dibandingkan dengan SLN Terhadap Laju Pelepasan APMS” untuk memenuhi syarat memperoleh gelar Sarjana Farmasi pada Fakultas Farmasi Universitas Airlangga.
Selama penyelesaian skripsi ini dukungan dan dorongan yang diberikan sangat membantu dalam menghadapi masalah dan hambatan yang ada. Pada kesempatan ini ucapan terima kasih penulis sampaikan kepada :
1. Prof. Dr. Widji Soeratri, DEA, Apt. selaku pembimbing utama yang telah meluangkan waktu untuk membimbing
2. Dr. Noorma Rosita, M.Si selaku pembimbing serta yang telah memberikan mencurahkan waktu dan ilmu yang sangat bermanfaat selama proses pengerjaan skripsi
3. Dr. Tristiana Erawati, M.Si. dan Dr. Dwi Setyawan, M. Si.,selaku dosen penguji yang memberikan banyak masukan 4. Prof Dr. Tutuk Budiati M.S. Apt. selaku dosen wali yang telah
banyak membimbing saya selama empat tahun ini
5. Seluruh dosen dan staff Departemen Farmasetika Fakultas Farmasi Universitas Airlangga
7. Teman- teman Lab Farmasetika beserta kakak-kakak S2 (Mbak Ushie, Mbak Nurul, Mbak Karin, dan Mas Teguh)
8. Teman- teman kelas C 2011 (CTM) yang teristimewa Natasha Era, Meida Ayu, Alfiah Rizqi, Naili Uswatun, dan Anggita Dian. Terima kasih atas semangat yang diberikan
9. Oktavia Indah Ambarsari sebagai sejawat terkasih, atas dukungan, bantuan, dan kebersamaan selama masa kuliah 10. Dewi, Nubila, Najmah, Glaveria, Riska, Shafitri, dan Imroatus
sebagai sahabat terkasih dan penopang dibalik layar
11. Andre Maulana, kakak dan sahabat terbaik yang selalu berbagi dan menasihati.
12. Kedua orang tua tercinta, Moh Rumli dan Lutfiyah, atas pengertian, pengorbanan dan kasih sayang dalam mendidik saya 13. Seluruh pihak yang terlibat dalam penyelesaian skripsi ini.
Semoga skripsi ini dapat bermanfaat untuk perkembangan ilmu pengetahuan dibidang farmasi. Terima kasih atas segala kritik dan saran yang diberikan dalam penyusunan skripsi ini.
Surabaya, September 2015
RINGKASAN
PENGARUH KADAR ASAM OLEAT PADA SISTEM NLC DENGAN LIPID SETIL ALKOHOL : ASAM OLEAT DIBANDINGKAN DENGAN SLN TERHADAP LAJU
PELEPASAN APMS
AFINA F. A.
Nanostructured Lipid Carrier (NLC) merupakan sistem penghantaran obat baru hasil pengembangan dari Solid Lipid Nanoparticle (SLN) dimana keduanya memiliki banyak keistimewaan. Konsep NLC dikembangkan untuk memperbaiki beberapa permasalahan yang timbul pada sistem SLN yaitu jumlah penjerapan obat yang terlalu rendah, keluarnya obat dari sistem selama penyimpanan, dan kandungan air yang terlalu tinggi pada dispersi SLN (Müller et al., 2002).
Pada penelitian ini dibuat sistem SLN dan NLC dengan kadar lipid 10% yang terdiri dari lipid setil alkohol dan asam oleat. APMS digunakan sebagai model obat yang dijerap dalam sistem SLN dan NLC. Tujuan dari penelitian ini adalah untuk membandingkan efektivitas sistem SLN dan NLC dalam hal ini laju pelepasan APMS dari sistem SLN dan NLC pada setiap formula. Sistem SLN tidak mengandung asam oleat dan sistem NLC dibuat dengan perbedaan rasio setil alkohol : asam oleat 9,5:0,5; 9:1; dan 8,5;1,5. Penggunaan asam oleat sebagai minyak dalam NLC berperan penting dalam menurunkan proses kristalisasi dan meningkatkan penurunan modifikasi keteraturan kristal asam stearat, serta merupakan faktor utama yang mempengaruhi kecepatan pelepasan bahan aktif dalam sistem NLC (Woo et al., 2014).
pada formula base dan 2336,4 ± 1118,203 nm pada formula dengan APMS. pH seluruh formula berada pada rentang 3,96-4,13. Adapun nilai viskositas seluruh formula berada pada rentang 800-1200 cps. Efisiensi penjebakan terbesar terdapat pada formula NLC-APMS dengan kadar asam oleat terbesar (1,5%) yaitu 27.60± 0.4229 % dan terkecil adalah SLN-APMS 13.463 ± 0.2953.
Pada penelitian ini dilakukan pengukuran laju pelepasan (flux) APMS dari sistem SLN dan NLC menggunakan perangkat uji disolusi
ABSTRACT
EFFECTS OF OLEIC ACID IN NLC SYSTEM WITH CETYL ALCOHOL : OLEIC ACID AS LIPID COMPARED WITH SLN
SYSTEM ON RELEASE PROFILE OF PMCA
AFINA F A
Nanostructured lipid carriers (NLC) was the second generation of Solid Lipid Nanoparticles (SLN) that was developed by mixing solid lipid and liquid lipids. This concept has some advanteges such as giving more modulation of drug release, increasing drug loading and prevent its leakage. In this study, p-methoxycinnamic (PMCA), cetyl alcohol (CA) and oleic acid (OA) was used as lipids that aimed to investigate the influence of increasing OA ratio on release of PMCA from SLN and NLCs system. Tween 80 was used as surfactant and propylene glycol as co-surfactant. SLN and NLC were prepared by hot High Shearing Homogenization (HSH) technique. SLN and NLC were evaluated on particle size, pH, viscosity, and entrapment efficiency (EE). NLC with highest OA (1,5%) hs the smallest particle size 1347,03 ± 196,01 nm for NLC base 276,8 ± 49,43 nm for NLC-PMCA. EE was significantly influenced by OA content. NLC-PMCA with 1,5% OA has the highest EE (27.60± 0.4229 %). The release study of SLN-PMCA and NLC-PMCA were evaluated using USP dissolution Aparatus 5-Paddle Over Disk. Based on statistical analysis using ANOVA One Way, it showed there were no significant differences between flux of SLN-PMCA and NLCs-PMCA with different content of OA.
DAFTAR ISI
BAB II TINJAUAN PUSTAKA ... 6
2.1 Nanostructured Lipid Carriers (NLC) ... 6
2.1.1 Kelebihan dan kekurangan ... 6
2.1.2 Komponen penyusun ... 7
2.1.3 Teknik pembuatan ... 8
2.1.4 Karakterisasi NLC ... 11
2.2 Pelepasan ... 14
2.2.1 Faktor-faktor yang mempengaruhi pelepasan ... 17
2.2.2 Uji pelepasan ... 18
2.3 Asam p-Metoksisinamat ... 19
2.4 Setil alkohol ... 20
2.5 Asam oleat ... 21
2.6 Tween 80... 21
2.7 Propilenglikol ... 23
BAB III KERANGKA KONSEPTUAL ... 25
3.1 Uraian Kerangka Konseptual ... 25
3.2 Kerangka Konseptual ... 28
BAB IV METODE PENELITIAN ... 29
4.1 Bahan Penelitian ... 29
4.2 Alat Penelitian ... 29
4.3 Prosedur Penelitian ... 30
4.3.1 Analisis kualitatif bahan penelitian ... 32
4.3.2 Pembuatan kurva baku APMS dalam larutan dapar asetat pH 4,2 ± 0,2 ... 33
4.3.3 Pembuatan kurva baku APMS dalam larutan dapar fosfat .... 34
4.3.4 Pembuatan NLC ... 36
4.3.6 Uji karakteristik NLC ... 39
4.3.7 Uji pelepasan APMS dari sistem NLC ... 41
4.4 Analisis Data ... 44
4.4.1 Perhitungan parameter pelapasan APMS dari sistem NLC ... 44
4.4.2 Analisis statistika ... 45
BAB V HASIL PENELITIAN ... 46
5.1 Pemeriksaan Kualitatif Bahan Penelitian ... 46
5.1.1 Pemeriksaan kualitatif APMS... 46
5.1.2 Pemeriksaan kualitatif setil alkohol ... 48
5.1.3 Pemeriksaan kualitatif asam oleat ... 49
5.2 Penentuan kurva baku APMS ... 51
5.2.1 Kurva baku dalam larutan dapar asetat pH 4,2 ± 0,2 ... 51
5.2.2 Kurva baku dalam larutan dapar fosfat pH 7.4 ± 0.05 ... 53
5.3 Pemeriksaan pengaruh bahan tambahan terhadap serapan APMS 55 5.4 Hasil uji homogenitas dan peroleh kembali APMS dalam sistem SLN maupun NLC ... 56
5.5 Penentuan Karakteristik Sistem SLN-NLC APMS ... 56
5.5.1 Hasil pemeriksaan organoleptis sistem SLN-NLC APMS .... 56
5.5.2 Hasil pengukuran ukuran partikel sistem SLN-NLC APMS . 57 5.5.3 Hasil pengukuran polydispersity index (pi) ukuran partikel sistem SLN-NLC APMS ... 58
5.5.4 Hasil pengukuran pH sistem SLN-NLC ... 60
5.5.5 Hasil penentuan viskositas sistem SLN-NLC ... 60
5.5.6 Hasil penentuan efisiensi penjebakan sistem SLN-NLC APMS 61 5.6 Hasil Uji Pelepasan APMS dari Sistem SLN-NLC ... 62
5.6.1 Penentuan profil pelepasan ... 62
5.6.2 Hasil perhitungan laju pelepasan (fluks) apms dari sistem SLN-NLC ... 62
BAB VI PEMBAHASAN ... 65
BAB VII KESIMPULAN DAN SARAN ... 70
7.1 Kesimpulan ... 70
7.2 Saran ... 70
DAFTAR GAMBAR
Gambar 2. 1 Tipe struktur NLC (Mäder, 2006) ... 14
Gambar 2. 2 Struktur Asam p-Metoksisinamat ... 19
Gambar 2. 3 Struktur Setil Alkohol ... 20
Gambar 2. 4 Struktur Asam Oleat ... 21
Gambar 2. 5 Struktur Tween 80 ... 22
Gambar 2. 6 Struktur Propilenglikol ... 23
Gambar 3. 1 Skema Kerangka Konseptual ... 28
Gambar 4. 1 Skema Kerja Penelitian ... 31
Gambar 5. 1 Hasil pemeriksaan spektra IR APMS ... 46
Gambar 5. 2 Spektra IR APMS berdasarkan pustaka... 47
Gambar 5. 3 Termogram DTA APMS ... 47
Gambar 5. 4 Hasil pemeriksaan spektra IR setil alkohol ... 48
Gambar 5. 5 Spektra IR setil alkohol berdasarkan pustaka ... 49
Gambar 5. 6 Termogram DTA setil alkohol ... 49
Gambar 5. 7 Hasil pemeriksaan spektra IR asam oleat ... 50
Gambar 5. 8 Spektra IR asam oleat berdasarkan pustaka ... 50
Gambar 5. 9 Profil serapan larutan baku kerja APMS pada larutan dapar asetat pH 4,2 ± 0,2 ... 52
Gambar 5. 10 Kurva baku serapan APMS dalam larutan dapar asetat pH 4.2 ± 0.2 ... 52
Gambar 5. 11 Profil serapan larutan baku kerja APMS dalam larutan dapar fosfat pH 7.4 ± 0.05 ... 53
Gambar 5. 12 Kurva baku serapan APMS dalam larutan dapar fosfat pH 7.4 ± 0.05 ... 54
Gambar 5. 13 Serapan larutan dapar asetat pH 4,2 ± 0,2, APMS, SLN base, NLC base, SLN APMS, dan NLC APMS dalam larutan dapar asetat pH 4,2 ± 0,2 ... 55
Gambar 5. 15 Diagram ukuran partikel sistem SLN dan NLC APMS dengan lipid 10% (setil alkohol:asam oleat) ... 58 Gambar 5. 16 Diagram homogenitas ukuran partikel sistem SLN-NLC
APMS dengan lipid 10% (setil alkohol:asam oleat) ... 59 Gambar 5. 17 Diagram efisiensi penjebakan sistem SLN dan NLC APMS
... 61 Gambar 5. 18 Kurva hubungan antara waktu (menit) dan jumlah
kumulatif APMS yang lepas dari sistem SLN maupun NLC ... 63 Gambar 5. 19 Histogram laju pelepasan APMS dari sistem SLN maupun
DAFTAR TABEL
Tabel IV. 1 Larutan Baku Kerja APMS dalam dapar asetat pH 4,2 ± 0,2 34 Tabel IV. 2 Larutan Baku Kerja APMS dalam Dapar Fosfat pH 7,2 ± 0,05
... 35
Tabel IV. 3 Formulasi Sistem NLC ... 36
Tabel V. 1 Hasil pemeriksaan kualitatif sampel APMS ... 47
Tabel V. 2 Hasil pemeriksaan kualitatif sampel setil alkohol ... 48
Tabel V. 3 Hasil pemeriksaan kualitatif sampel asam oleat ... 50
Tabel V. 4 Nilai serapan APMS pada berbagai kadar dalam larutan dapar asetat pH 4.2 ± 0.2 pada panjang gelombang maksimum 304,0 nm 52 Tabel V. 5 Nilai serapan APMS pada berbagai kadar dalam larutan dapar fosfat pH 7.4 ± 0.05 pada panjang gelombang maksimum 285,0 nm ... 54
Tabel V. 6 Hasil perolehan kembali APMS dalam sistem SLN-NLC dengan lipid setil alkohol:asam oleat ... 56
Tabel V. 7 Hasil pemeriksaan organoleptis sistem SLN-NLC APMS dengan lipid setil alkohol:asam oleat ... 57
Tabel V. 8 Ukuran partikel sistem SLN-NLC APMS ... 58
Tabel V. 9 Homogenitas ukuran partikel sistem SLN-NLC APMS ... 59
Tabel V. 10 pH sistem SLN-NLC APMS ... 60
Tabel V. 11 Viskositas sistem SLN-NLC APMS ... 60
Tabel V. 12 Efisiensi Penjebakan Sistem SLN-NLC APMS ... 61
Tabel V. 13 Hasil Uji HSD Efisiensi Penjerapan ... 62
Tabel V. 14 Laju pelepasan APMS dalam sistem SLN-NLC ... 63
DAFTAR LAMPIRAN
LAMPIRAN 1 Sertifikat Analisis APMS ... 74
LAMPIRAN 2 Sertifikat analisis Asam Oleat ... 75
LAMPIRAN 3 Sertifikat Analisis Setil Alkohol ... 76
LAMPIRAN 4 Sertifikat Analisis Tween 80 ... 77
LAMPIRAN 5 Sertifikat Analisis Propilenglikol ... 78
LAMPIRAN 6 Sertifikat Analisis Natrium Asetat ... 79
LAMPIRAN 7 Sertifikat Analisis Asam Asetat Glasial ... 80
LAMPIRAN 8 Sertifikat Hasil Uji Viskositas Sistem SLN-NLC APMS 81 LAMPIRAN 9 Tabel Efisiensi Penjebakan ... 82
LAMPIRAN 10 Hasil Uji pelepasan APMS dari Sistem SLN dan NLC . 83 LAMPIRAN 11 Data Hasil Pengolahan Statistik ANOVA Satu Arah .... 97
LAMPIRAN 12 Tabel Hasil Pengukuran Ukuran Partikel Rata-Rata Sistem SLN-NLC APMS ... 100
BAB I PENDAHULUAN
1.1 Latar Belakang
Nanostructured Lipid Carrier (NLC) merupakan sistem penghantaran obat baru hasil pengembangan dari Solid Lipid Nanoparticle (SLN) dimana keduanya memiliki banyak keistimewaan. Kedua sistem ini memberikan sifat adesif yang sangat berperan penting dalam menimbulkan sifat oklusifitas, efek hidrasi pada kulit, peningkatan absorbsi dan penetrasi aktif, serta efek pelepasan terkendali. Konsep NLC dikembangkan untuk memperbaiki beberapa permasalahan yang timbul pada sistem SLN yaitu jumlah penjerapan obat yang terlalu rendah, keluarnya obat dari sistem selama penyimpanan, dan kandungan air yang terlalu tinggi pada dispersi SLN (Müller et al., 2002). NLC memberikan fleksibilitas yang lebih baik dalam memodulasi pelepasan obat, meningkatkan jumlah penjerapan obat, dan menghindari kebocoran penjerapan. Pada NLC, campuran lipid padat dan lipid cair menghasilkan bentuk padat pada suhu kamar hingga suhu 40ºC. (Souto and Müller, 2007). Selain itu, sistem nanopartikel dengan ukuran partikelnya yang sangat kecil terbukti memiliki kemampuan dalam mempertahankan stabilitas fisika dan kimia dari bahan aktif dan menjamin kontak antara bahan aktif dan kulit dan penetrasi bahan aktif ke dalam kulit. (Li and Ge, 2012).
pemilihan fase lipid yang akan digunakan, diantaranya jarak titik lebur, morfologi kristal, viskositas, dan polaritas (Qian et al., 2011).
Pada penelitian sebelumnya, telah dilakukan karakterisasi sistem SLN-APMS dimana SLN dengan lipid setil alkohol dapat menghasilkan efektifitas penjerapan 68,54% dan ukuran partikel 119,25 nm, sementara SLN yang dibuat dari lipid asam stearat memiliki efektifitas penjerapan 58,8% dan ukuran partikel dalam rentang 575-2107 nm (Rahmawan et al.,
2012).
APMS merupakan salah satu konstituen yang terkandung dalam minyak atsiri dalam rimpang kering tanaman kencur (Kaempferia galanga)yang dilaporkan memiliki aktivitas analgesik dan antiinflamasi (Vittalrao et al., 2011). Mekanisme kerja APMS sebagai antiinflamasi adalah melalui hambatan enzim sikolooksigense (COX) 1 dan 2 (Ekowati dan Diyah, 2010). Sebagai antiinflamasi, profil pelepasan prolonged release diharapkan dapat meningkatkan efektivitas APMS. Pada penelitian ini, dilakukan penjerapan APMS dalam sistem penghantaran SLN dan NLC yang keduanya memiliki perbedaan pada ada tidaknya lipid cair. Danya lipid cair/minyak dalam sistem NLC diharapkan dapat meningkatkan efektivitas penjerapan APMS di dalam matriks lipid sehingga dapat memberikan profil pelepasan prolonged release yang lebih optimal.
padat terjadi lebih awal dan menyebabkan lipid cair berada pada bagian luar matriks bersama bahan obat dan membentuk drug-enrich shell yang dapat memicu profil pelepasan segera (Hu et al., 2005). Selain itu, berdasarkan penelitian yang dilakukan oleh Woo et al., (2014), hasil analisis Differential Scanning Calorimetry (DSC) menunjukkan keberadaan asam oleat pada matriks asam stearat dapat mengacak susunan kisi kristal yang mengakibatkan penurunan derajat keteraturan kristal dan hal tersebut berakibat pada peningkatan efisiensi penjerapan.
Selain lipid padat dan lipid cair, komponen penyusun sistem NLC adalah emulgator. Dalam memilih emulgator harus memperhatikan tegangan antarmuka, kinetika adsorbsi, kemampuan dalam menginterfensi pertumbuhan kristal dan nukleasi, serta kemampuan dalam mencegah agregasi partikel (Qian et al., 2011). Seluruh jenis surfaktan non ionik memiliki potensi kecil dalam menimbulkan sensitivitas kulit oleh karena itu jenis surfaktan ini sangat direkomendasikan untuk penggunaan dermal (Kovacevic et al., 2011). Salah satu contoh surfaktan non ionik yang aman dan sering digunakan dalam sediaan farmasi adalah tween 80.
Untuk meningkatkan stabilitas droplet yang dihasilkan, penggunaan kosurfaktan sangat bermanfaat. Propilenglikol merupakan salah satu bahan yang dapat digunakan sebagai kosurfaktan. Berdasarkan penelitian yang dilakukan oleh Loo et al., (2012), NLC dengan propilenglikol menghasilkan ukuran partikel lebih kecil, memiliki persentase peningkatan hidrasi kulit lebih besar, dan menurunkan
sebagai kosurfaktan, propilenglikol juga dapat berfungsi sebagai
enhancer. Kombinasi antara sistem NLC yang memiliki sifat oklusif dengan enhancer yang dapat memodifikasi stratum korneum sebagai barier kulit yang utama, merupakan cara yang menjanjikan dalam penghantaran obat melalui kulit (Vitorino et al., 2013).
Profil pelepasan obat merupakan suatu parameter penting untuk desain dan evaluasi suatu sistem penghantaran obat (Mühlen et al., 1997). Modifikasi profil pelepasan obat sebagai fungsi dari matriks lipid, kadar surfaktan, dan parameter produksi dapat mungkin dilakukan untuk mendapatkan profil pelepasan yang diinginkan. Dengan mengetahui pengaruh faktor-faktor tersebut profil pelepasan obat dari NLC dapat dibuat menjadi pelepasan tertunda, pelepasan dipercepat, atau keduanya jika diinginkan terdapat dosis inisial pada penggunaan obat (Müller et al.,
2000). Berdasarkan penelitian yang dilakukan oleh Hu et al. (2005), konsentrasi asam oleat di bawah 15% dalam kombinasi bersama asam stearat pada sistem NLC merupakan faktor utama yang mempengaruhi profil pelepasan obat pada tahap awal pelepasan, sementara konsentrasi asam oleat 30% merupakan konsentrasi optimal yang dapat memberikan efisiensi penjerapan 69,95% dengan kapasitas muatan 3,5%.
(Müller et al., 2002) sehingga efektifitas APMS sebagai analgesik anti-inflamasi dapat ditingkatkan.
1.2 Rumusan Masalah
Bagaimana pengaruh kadar asam oleat pada pelepasan APMS dari sistem SLN maupun NLC dengan kadar lipid 10% yang terdiri dari setil alkohol : asam oleat (10:0; 9,5:0,5; 9:1; dan 8,5:1,5), tween 80, dan propilenglikol?
1.3 Tujuan Penelitian
Menentukan parameter pelepasan APMS dari sistem SLN maupun NLC dengan kadar lipid 10% yang terdiri dari setil alkohol : asam oleat (10:0; 9,5:0,5; 9:1; dan 8,5:1,5), tween 80, dan propilenglikol.
1.4 Manfaat Penelitian
BAB II
TINJAUAN PUSTAKA
2.1 Nanostructured Lipid Carriers (NLC)
Nanostructured Lipid Carriers (NLC) adalah sistem penghantaran dimana partikel lipid parsial-kristal berjari-jari ≤100 nm tersebar dalam fase air yang mengandung pengemulsi, sebagai sistem penghantaran yang potensial dan memiliki beberapa keuntungan dalam keadaan tertentu bila dibandingkan dengan sistem koloid lainnya (Tamjidi et al., 2013).
Matriks NLC merupakan campuran molekul lipid spasial yang berbeda, biasanya campuran lipid padat dan cair, yang membuat susunan kristal matriks yang lebih tidak sempurna untuk mengakomodasi molekul obat lebih dari SLN dan tetap dalam wujud padat pada suhu kamar meski mengandung lipid cair/minyak (Chen et al., 2010). Sistem NLC membentuk sebuah platelet padat dengan minyak yang nampak diantara platelet padat dan lapisan surfaktan (Mäder, 2006).
2.1.1Kelebihan dan kekurangan
Sebagai sistem penghantaran obat, NLC memiliki beberapa kelebihan diantaranya :
1. Struktur NLC (tipe imperfection, amorf, dan multiple) dapat mengakomodasi lebih banyak obat dan menurunkan resiko kebocoran selama penyimpanan dibandingkan dengan SLN (Zhuang et al., 2010).
2. Memberikan perlindungan terhadap bahan-bahan yang labil secara kimia dengan mencegah degradasi kimia.
4. NLC dengan ukuran partikelnya yang kecil menjamin kontak antara bahan aktif dan menjamin penetrasi obat kedalam kulit (Li and Ge, 2012).
5. Membentuk lapisan tipis pada permukaan kulit sehingga memiliki efek controlled ucclusion dan skin hidration.
6. Meningkatkan biovailabilitas bahan aktif di kulit dan dapat membentuk skin targeting sistem.
7. Memberikan stabilitas fisika untuk formulasi topikal (Müller et al.,
2007).
2.1.2 Komponen penyusun a. Lipid Padat dan Lipid Cair
b. Emulgator
Beberapa jenis emulgator yang telah banyak digunakan untuk membentuk sistem NLC adalah jenis poloxamer, polisorbat, lesitin, dan asam empedu. Diketahui bahwa kombinasi emulgator dapat menurunkan aglomerasi partikel secara signifikan (Mäder, 2006). Jenis emulgator dapat mempengaruhi kecepatan pelepasan obat dalam sistem NLC. Pada penelitian yang dilakukan oleh Chen et al.,
(2010) menunjukkan bahwa sistem NLC yang menggunakan emulgator soybean phosphatidylcholine (SPC) memberikan pelepasan yang lebih lambat dibanding dengan Myverol, sementara untuk efektivitas penjebakan, Myverol memberikan penjebakan yang lebih besar dibanding SPC. Penggunaan Polyhidroxy surfactant
sebagai emulgator pada konsentrasi 1% (b/b) dapat menghasilkan diameter partikel rata-rata 200 nm dan kecenderungan kristalisasi partikel meningkat sejalan dengan peningkatan panjang rantai hidrofilik jenuh dari surfaktan. (Kovacevic et al., 2011).
2.1.3 Teknik pembuatan
a. High Shear Homogenization and Ultrasound
kualitas dispersi masih kurang baik karena masih dijumpai mikropartikel dan untuk penggunaan metode ultrasound, terdapat kemungkinan kontaminasi logam (Mäder, 2006).
b. High Pressure Homogenization
Metode High Pressure Homogenization menggunakan tekanan tinggi (100-2000 bar) untuk mendorong lipid cair melalui celah sempit. Pada umumnya konsentrasi lipid yang digunakan 5 sampai 10%. Pada metode ini digunakan shear stress dan cavitation
sebagai gaya yang dapat merubah pertikel menjadi ukuran submikron. Terdapat dua pendekatan dalam proses pembentukan sistem NLC menggunakan metode HPH, yaitu Hot Homegenization Technique
dan Cold Homegenization Technique. Pada kedua teknik ini, pertama obat dilarutkan atau didispersikan pada lipid yang dileburan pada suhu 5-10º C diatas titik leburnya.
Pada Hot Homegenization Technique, bahan aktif yang telah didispersikan pada lelelah lipid didispersikan pada larutan surfaktan encer pada suhu yang sama dengan pengadukan menggunakan high shear device seperti Ultra-Turrax sehingga membentuk pre-emulsi lalu dihomogenkan menggunakan piston gap homogenizer untuk membentuk nanoemulsi o/w panas dan didinginkan pada suhu kamar. Pada suhu kamar, lipid akan mengalamai rekristalisasi dan membentuk nanopartikel. Pada Cold Homegenization Technique
selama proses homogenisasi, dan mengurangi paparan panas terhadap sampel (Singhal et al., 2011).
c. Microemulsion Technique
Pada metode ini campuran lipid dileburkan terlebih dahulu kemudian bahan aktif dimasukkan kedalam leburan lipid. Pada suhu yang sama, siapkan campuran air, surfaktan, dan kosurfaktan untuk membentuk fase air dan kemudain fase air dimasukkan ke dalam leburan lipid dengan pengadukan sedang. Untuk menghasilkan mikroemulsi dibutuhkan perbandingan yang tepat dari setiap bahan yang digunakan. Mikroemulsi yang telah terbentuk kemudian didispersikan ke dalam fase air dengan perbanding mikroemulsi panas dan fase air (1:25 – 1:50) dengan kecepatan pengadukan sedang (Singhal et al., 2011).
d. Solvent Emulsification-Evaporation Technique
Pada metode ini, bahan-bahan lipofilik dan bahan aktif yang hidrofob dilarutkan dalam pelarut organik yang tidak campur dengan air (contoh : sikloheksana, diklorometana, toluena, dan kloroform) kemudian larutan tersebut diemulsifikasikan ke dalam fase air menggunakan High Speed Homogenizer untuk meningkatkan efisiensi emulsifikasi, emulsi yang terbentuk dilewatkan pada
microfluidizer. Tahap akhir adalah penguapan pelarut organik dengan pengadukan mekanik pada suhu kamar sehingga diperoleh presipitasi lipid nanopartikel (Singhal et al., 2011).
e. Solvent Emulsification-Diffusion Technique
kedua cairan. Leburan lipid kemudian dilarutkan dalam air jenuh pelarut organik (fase organik/ fase internal) dan kemudian diemulsifikasi ke dalam pelarut organik jenuh air yang mengandung emulgator dengan diaduk menggunakan magnetic stirrer sehingga membentuk sistem emulsi o/w, emulsi ini kemudian diencerkan dengan air (1:5-1:10) agar pelarut berdifusi ke dalam fase air dan kemudian terjadi agregasi lipid nanopartikel. Kondisi ini dilakukan pada suhu kamar atau suhu dibawah kelarutan lipid dengan kecepatan pengadukan yang dipertahankan konstan. Tahap akhir adalah proses penghilangan pelarut dengan vacuum distillation atau lyophilization
(Singhal et al., 2011).
2.1.4 Karakterisasi NLC
Karakterisasi lipid dalam sistem NLC sangat penting dilakukan untuk mengetahui adanya perubahan sifat lipid yang dipengaruhi oleh parameter pembuatan atau adanya interaksi dengan bahan-bahan pembentuk sistem dan bahan aktif. Parameter penting dalam karakterisasi NLC adalah ukuran partikel, bentuk partikel, jenis modifikasi lipid, dan derajat kristalisasi Modifikasi lipid dan derajat kristalisasi sangat berhubungan dengan penjebakan obat dan kecepatan pelepasan (Mäder, 2006).
2.1.4.1 Ukuran partikel NLC
Ukuran partikel NLC dapat diamati dengan menggunakan beberapa alat seperti Photon correlation spectroscopy (PCS), Laser Diffraction (LD), Atomic force microscopy (AFM), dan Transmission Electron Microscopy (TEM), Scanning Electron Microscopy (SEM),
Microscopy (FFEM). PCS dan LD menggunakan prinsip efek hamburan cahaya yang digunakan untuk menghitung ukuran partikel. Perhitungan yang tidak pasti dapat terjadi pada partikel yang berbentuk nonspheric. Kedua metode ini memiliki keterbatasan dalam pengkuran partikel dengan populasi ukuran partikel yang berbeda. Sementara TEM dapat mengukur ukuran partikel secara langsung. (Mäder, 2006).
2.1.4.2 Morfologi partikel NLC
Untuk mengetahui morfologi partikel NLC, dapat digunakan
Transmission Electron Microscopy (TEM) yang mampu memenunjukkan mikrostruktur seperti misel, kristalin, emulsi, dan nanopartikel (Hou et al.,
2003). Selain TEM, dapat digunakan Scanning Electron Microscopy
(SEM). Metode SEM dilakukan dengan cara mengencerkan sampel dengan aqua destilata kemudian diletakkan pada plat alumunium yang telah dilapisi pita karbon pada kedua sisinya dan dikeringkan dalam desikator. Sampel kemudian dilapisi emas agar terkonduksi dan diamati pada tegangan 25kV (Vitorino et al., 2011). Pada penelitian sebelumnya, diketahui morfologi partikel SLN-APMS dengan lipid setil alkohol berbentuk spheric sementara lipid asam stearat berbentuk oval (Rahmawan et al., 2012).
2.1.4.3 Efisiensi penjebakan
Efesiensi penjebakan atau entrapment efficiency (Ee) adalah presentase bahan aktif yang terjebak di dalam partikel lipid. Untuk bahan aktif yang bersifat lipofilik biasanya memiliki nilai Ee antara 90-98%. Pada penelitian sebelumnya, diketahui efisiensi penjebakan APMS dalam sistem SLN dengan lipid setil alkohol adalah 68,54% (Rahmawan et al.,
entrapment efficiency (Ee) dan Drug Loading Capacity (L) dapat dihitung dengan persamaan berikut :
= − 100%
= − 100%
Keterangan :
Wa : Jumlah obat yang ditambahkan ke dalam sistem
Ws : Jumlah bahan obat bebas dalam supernatan
Wl : Jumlah lipid yang digunakan dalam sistem
2.1.4.4 Tipe NLC (Muller et al., 2002)
Terdapat tiga tipe NLC yang dipengaruhi oleh proses pembuatan dan komposisi campuran matriks lipid yang terbentuk. Tiga tipe tersebut yaitu :
a. The Imperfect Type
Tipe ini dapat mengakomodasi lebih banyak bahan aktif karena susunan matriksnya yang tidak sempurna. Tipe ini dapat diperoleh dengan cara mencampur lipid padat dengan sejumlah kecil minyak. Disebabkan oleh perbedaan panjang rantai antara asam lemak dan campuran mono-, di-, dan triasilgliserol tipe NLC ini tidak dapat membentuk struktur kristal yang teratur (Souto and Müller, 2007).
b. The Amorphous Type
c. The multiple type
Tipe ini hampir sama dengan emulsi w/o/w yang pada tipe ini terdiri dari minyak dalam lipid padat dalam dispersi air dimana matriks lipid padat mengandung nanokompartemen tipis dari minyak. Tipe ini dapat diperoleh dengan cara mencampur lipid padat dengan jumlah minyak yang tinggi. Tipe NLC dapat dilihat pada gambar 2.1
Gambar 2. 1 Tipe struktur NLC (Mäder, 2006)
2.2 Pelepasan
Profil pelepasan obat merupakan suatu parameter penting untuk desain dan evaluasi suatu sistem penghantaran obat (Mühlen
Berdasarkan penelitian yang dilakukan oleh Mühlen et al.
(1997) profil pelepasan bahan obat dari matriks lipid dapat diatur berdasarkan sifat dasar lipid, suhu produksi, dan konsentrasi surfaktan yang digunakan. Suhu yang tinggi dan konsentrasi surfaktan yang tinggi dapat menghasilkan profil pelepasan segera (brust release). Kelarutan bahan obat dalam fase air pada suhu kamar juga mempengaruhi profil pelepasan obat. Saat kelarutan obat pada fase air menurun selama proses pendinginan, obat akan mengalami re-partisi ke dalam fase lipid yang juga mengalami penurunan suhu, inti partikel lipid yang mengalami kristalisasi selama pendinginan tidak dapat menampung obat, sehingga obat akan berada pada permukaan partikel lipid dan akan menghasilkan pelepasan segera (brust release).
Pada sistem NLC dimana terdapat penambahan lipid cair pada sistem, memiliki kelebihan dalam hal penjebakan akibat penurunan modifikasi keteraturan kisi kristal dan karena bahan obat pada umumnya memiliki kelarutan yang lebih besar pada lipid cair/minyak dibandingkan lipid padat. Kapasitas penjebakan yang tinggi lebih baik ini juga dapat menghasilkan profil pelepasan
prolonged release (Chen et al., 2010).
= . ( − )……….(1) Dimana dC/dt adalah jumlah obat yang terlepas per satuan waktu, K adalah konstanta pelepasan orde satu, C adalah kadar obat yang terlarut, dan Cs adalah kelarutan bahan obat.
Pelepasan bahan aktif dari matriks menggunakan persamaan yang dikembangkan oleh Higuchi berdasarkan hukum Fick pertama dan kemudian diterapkan untuk difusi obat padat yang terdispersi dalam bentuk matriks yang homogen.
Persamaan dari Hukum Higuchi :
= [ (2 − ) . ] / ………(2)
= . . / ………...(3)
2.2.1Faktor-faktor yang mempengaruhi pelepasan
Terdapat beberapa faktor yang dapat mempengaruhi profil pelepasan obat dalam sistem NLC, yaitu:
1. Jenis lipid dan afinitas bahan aktif terhadap pembawa
Komposisi matriks lipid yang berbeda akan menghasilkan profil pelepasan yang berbeda. Setiap jenis lipid memiliki susunan kristal dan modifikasi kristal, titik lebur, nilai hydrophilic lypophilic balance (HLB) yang berbeda. Hal tersebut menyebabkan afinitas bahan aktif yang akan dijebak menjadi berbeda untuk setiap jenis lipid yang berbeda (Dubey, 2012). Semakin besar afinitas pembawa terhadap bahan obat maka semakin kecil pelepasan dari pembawa. Sebaliknya, obat yang memiliki afinitas kecil terhadap pembawa maka jumlah obat yang dilepaskan juga semakin besar (Sinko and Singh, 2011).
2. Kelarutan bahan aktif dalam lipid
Kelarutan bahan obat merupakan penentu pelepasannya dari sediaan, dan ketika kelarutan obat bergantung pada pH, maka adanya perubahan pH lingkungan menyebabkan perubahan kelarutan obat dan merubah pula mekanisme pelepasannya (Badaway and Hussain, 2007).
3. Ukuran partikel sistem koloid
Ukuran partikel suatu sistem koloid merupakan faktor krusial pada pelepasan bahan obat selain faktor di dalam partikelnya (Dubey, 2012). Semakin besar ukuran partikel sistem, maka jarak difusi yang perlu ditempuh molekul bahan aktif terlepas dari sistem semakin besar, sehingga pelepasan dapat diperlambat.
Viskositas mempengaruhi mobilitas atau kemudahan pergerakan bahan aktif untuk terlepas dari pembawa. Semakin viskus sediaan, akan semakin besar hambatan pelepasan yang berakibat semakin lama waktu difusi bahan aktif, begitu pula sebaliknya (Anggraeni et al., 2012).
2.2.2Uji pelepasan (Waghmare, 2012)
Terdapat dua metode uji pelepasan obat secara in vitro, yaitu : a. Tabung Dialisis
NLC ditempatkan dalam tabung dialysis prewashed yang dapat ditutup kedap udara. Tabung didialisis dalam media disolusi yang sesuai pada suhu kamar , sampel dikeluarkan dari media disolusi pada interval waktu yang sesuai, disentrifugasi dan dilakukan analisis kadar obat menggunakan metode analisis yang sesuai (spektrofotometri UV-VIS, HPLC, dll). Kondisi sink perlu dijaga dalam media disolusi. Kekurangan metode ini adalah kurangnya pengenceran langsung sistem SLN atau NLC oleh media disolusi.
b. Franz Diffusion Cell
Sistem SLN atau NLC ditempatkan dalam chamber donor dari
2.3 Asam p-Metoksisinamat
Asam p-Metoksisinamat (APMS) merupakan senyawa aktif hasil hidrolisis dari etil p-Metoksisinamat (EPMS) yang berasal dari ekstrak tanaman Kampferia galanga atau kencur
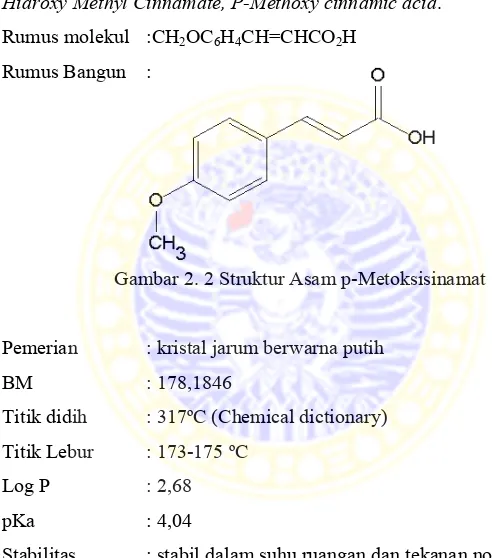
Nama Kimia : 4-Methoxy cinnamic acid, 4-Methoxycinnamate, P-Hidroxy Methyl Cinnamate, P-Methoxy cinnamic acid.
Rumus molekul :CH2OC6H4CH=CHCO2H Rumus Bangun :
Gambar 2. 2 Struktur Asam p-Metoksisinamat
Pemerian : kristal jarum berwarna putih
BM : 178,1846
Titik didih : 317ºC (Chemical dictionary) Titik Lebur : 173-175 ºC
Log P : 2,68
pKa : 4,04
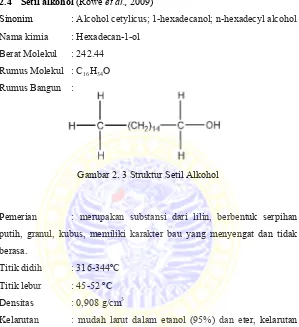
2.4 Setil alkohol (Rowe et al., 2009)
Sinonim : Alcohol cetylicus; 1-hexadecanol; n-hexadecyl alcohol Nama kimia : Hexadecan-1-ol
Berat Molekul : 242.44 Rumus Molekul : C16H34O Rumus Bangun :
Gambar 2. 3 Struktur Setil Alkohol
Pemerian : merupakan substansi dari lilin, berbentuk serpihan putih, granul, kubus, memiliki karakter bau yang menyengat dan tidak berasa.
Titik didih : 316-344ºC Titik lebur : 45-52 ºC Densitas : 0,908 g/cm3
Kelarutan : mudah larut dalam etanol (95%) dan eter, kelarutan meningkat dengan peningkatan suhu, praktis tidak larut dalam air, pada saat melebur dapat campur dengan lemak, parafin padat atau cair dan isoporpil miristat.
Viskositas : ≈ 7 mPa s (7 cP) pada 50 ºC
2.5 Asam oleat (Rowe et al., 2009)
Sinonim : 9,10-octadecenoic acid; asam cis-9-octadecenoat; Acidum oleicum; Crodolene; Crossential 094; Emersol; Glycon. Nama kimia : (Z)-9-Octadecenoic acid
Berat Molekul : 282.47 Rumus Molekul : C18H34O2 Rumus Bangun :
Gambar 2. 4 Struktur Asam Oleat
Pemerian : minyak dengan warna kekuningan hingga coklat pucat, minyak lipid dengan bau dan rasa menyerupai lemak.
Titik didih : 286 ºC pada 13.3 kPa (100 mmHg) (mengalami dekomposisi pada 80–100 ºC)
Titik lebur : 13-14 ºC Densitas : 0,895 g/cm3
Kelarutan : campur dengan benzene, kloroform, etanol (95%), eter, heksana, minyak atsiri, dan fixed oil, praktis tidak larut dalam air. Viskositas : 26 mPa s (26 cP) pada 25 ºC
Stabilitas dan penyimpanan : dengan adanya paparan udara, asam oleat secara bertahap mengabsorbsi oksigen, warna semakin gelap, dan bau semakin menyengat, pada tekanan atmosfer, akan mengalami dekomposisi jika dipanaskan pada suhu 80–100 ºC.
Nama kimia : Polyoxyethilene 20 sorbitan mono oleate Berat Molekul : 1310
Rumus Molekul : C64H124O26 Rumus Bangun :
Gambar 2. 5 Struktur Tween 80
Pemerian : mempunyai bau khas dan rasa pahit yang hangat, pada suhu 25 ºC berwarna kuning.
Titik didih 149 ºC
Kelarutan : mudah larut dalam air, larut dalam etanol dan etil asetat, tidak larut dalam paraffin cair dan minyak lemak.
Viskositas : 425 mPa s pada 25 ºC
Stabilitas dan penyimpanan : stabil terhadap elektrolit, asam, dan basa lemah, terjadi saponifikasi dengan adanya asam atau basa kuat. Merupakan ester asam oleat yang sensitiv terhadap oksidasi. Bersifat higroskopis dan apabila akan digunakan, harus diukur kandungan airnya dan dikeringkan bila perlu. Dapat membentuk peroksida bersama surfaktan polioksietilen lainnya. Disimpan dalam wadah tertutup rapat dan ditempat yang kering dan sejuk.
135 secara signifikan memiliki viskositas yang lebih rendah dibandingkan dengan sistem NLC dengan tween 60.
2.7 Propilenglikol (Rowe et al., 2009)
Sinonim :1,2-Dihydroxypropane; E1520; 2-hydroxypropanol; methyl ethylene glycol; methyl glycol; propane-1,2-diol; propylenglycolum
Nama kimia : 1,2-Propanediol Berat Molekul : 76,09
Rumus Molekul : C3H8O2 Rumus Bangun :
Gambar 2. 6 Struktur Propilenglikol
Pemerian : Cairan jernih, tidak berwarna, tidak berbau, berasa manis, sedikit berasa pahit menyerupai gliserin
Titik didih : 188ºC Titik lebur : -59 ºC
Densitas : 1.038 g/cm3 pada 20ºC
Stabilitas dan penyimpanan : pada suhu dingin, propilenglikol stabil pada wadah yang tertutup rapat, namun pada suhu tinggi dan keadaan terbuka, dapat menyebabkan oksidasi menghasilkan propionaldehid, asam laktat, asam piruvat, dan asam asetat. Secara kimia stabil ketika dicampur dengan etanol (95%), gliserin, atau air; larutan dalam air dapat disterilisasi dengan autoklaf.
BAB III
KERANGKA KONSEPTUAL
3.1 Uraian Kerangka Konseptual
NLC sebagai generasi baru dari SLN merupakan sistem lipid nanopartikel yang menggabungkan lipid padat dan lipid cair sebagai pembawa. Adanya lipid cair pada sistem NLC dapat menurunkan keteraturan kisi kristal dari matriks lipid yang terbentuk sehingga NLC memiliki kelebihan dalam hal mengakomodasi lebih banyak obat dan menurunkan resiko kebocoran selama penyimpanan (Souto and Müller, 2007; Zhuang et al., 2010). Efektifitas penjerapan yang baik pada NLC dapat menghasilkan profil pelepasan prolonged release dan meningkatkan stabilitas bahan obat, selain itu penggunaan lipid sebagai sistem pembawa dapat ditoleransi dengan baik oleh kulit sehingga dapat menurunkan resiko iritasi selama penggunaan (Souto and Müller, 2007).
Berdasarkan hasil penelitian yang dilakukan oleh Hu et al. (2005) dan Woo et al. (2014), Penggunaan asam oleat sebagai minyak dalam NLC berperan penting dalam menurunkan proses kristalisasi dan meningkatkan penurunan modifikasi keteraturan kristal asam stearat, serta merupakan faktor utama yang mempengaruhi kecepatan pelepasan bahan aktif dalam sistem NLC. Perbedaan titik lebur antara lipid padat dan lipid cair menyebabkan proses kristalisasi lipid padat terjadi lebih awal dan menyebabkan lipid cair berada pada bagian luar matriks bersama bahan obat dan membentuk drug-enrich shell yang dapat memicu profil pelepasan segera. Konsentrasi asam oleat di bawah 15% dalam kombinasi bersama asam stearat pada sistem NLC merupakan faktor utama yang mempengaruhi profil pelepasan obat pada tahap awal pelepasan, sementara konsentrasi asam oleat 30% merupakan konsentrasi optimal yang dapat memberikan efisiensi penjerapan 69,95% dengan kapasitas muatan 3,5%.
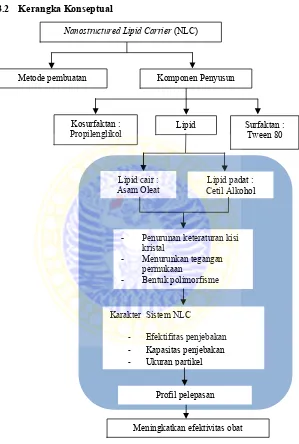
3.2 Kerangka Konseptual
Gambar 3. 1 Skema Kerangka Konseptual
Nanostructured Lipid Carrier (NLC)
Lipid Kosurfaktan :
Propilenglikol
Metode pembuatan Komponen Penyusun
Surfaktan : Tween 80
Lipid cair : Asam Oleat
- Penurunan keteraturan kisi kristal
- Menurunkan tegangan permukaan
- Bentuk polimorfisme
Lipid padat : Cetil Alkohol
Karakter Sistem NLC
- Efektifitas penjebakan - Kapasitas penjebakan - Ukuran partikel
Profil pelepasan
BAB IV
METODE PENELITIAN
4.1 Bahan Penelitian
Bahan-bahan yang digunakan dalam penlitian ini bila tidak dinyatakan lain, memiliki kemurnian pharmaceutical grade, antara lain asm p-metoksisinamat, setil alkohol, asam oleat, tween 80, propilenglikol, etanol pro analisis, dan aquadest. Dapar asetat pH 4,2 ± 0,2 dibuat dari C2H4O2 (asam asetat glasial) dan C2H3NaO2 (Natrium asetat anhidrat) pro analisis. Dapar fosfat pH 7,4 ± 0,05 dibuat dari Na2HPO4 (Narium fosfat dibasa) dan NaH2PO4 (natrium fosfat monobasa) pro analisis.
4.2 Alat Penelitian
Alat-alat yang digunakan dalam penelitian ini antara lain
Ultra-Turax High Shear Homogenizer, One Fourier Transform Infrared (FTIR), Spektrometer Perkin Elmer Instrument, Differential Thermal Analysis (DTA), DelsaTM Nano Submicron Particle Size
4.3 Prosedur Penelitian
Penelitian ini merupakan penelitian eksperimental laboratoris dengan tujuan menentukan pengaruh kadar asam oleat (0%; 0,5%; 1%; 1,5%) pada pelepasan APMS dari sistem NLC.
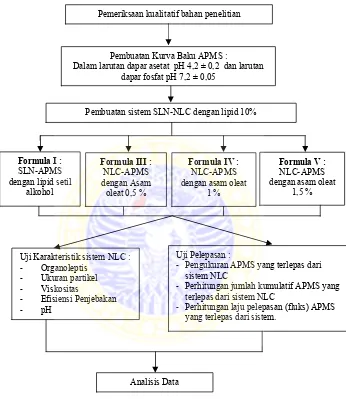
Tahap pertama dalam penelitian ini adalah melakukan analisis kualitatif bahan penelitian, yaitu APMS, setil alkohol, dan asam oleat. Kemudian dilakukan pembuatan kurva baku APMS dalam larutan dapar asetat 4,2 ± 0,2 dan dalam larutan dapar fosfat 7,4 ± 0,05. Tahap selanjutnya adalah pembuatan sistem NLC, yang kemudian diuji karakteristiknya dan uji pelepasan APMS dari sistem NLC. Penentuan uji pelepasan dilakukan dengan mengamati nilai serapan APMS pada panjang gelombang maksimum menggunakan spektrofotometri UV-Vis, sehingga diperoleh nilai serapan yang kemudian digunakan untuk mengetahui profil dan laju pelepasan (fluks) APMS dari sistem NLC. Dilakukan replikasi sebanyak tiga kali. Tahap akhir merupakan analisis data menggunakan one way ANNOVA.
Gambar 4. 1 Skema Kerja Penelitian Analisis Data
Uji Pelepasan :
- Pengukuran APMS yang terlepas dari sistem NLC
- Perhitungan jumlah kumulatif APMS yang terlepas dari sistem NLC
- Perhitungan laju pelepasan (fluks) APMS yang terlepas dari sistem.
Uji Karakteristik sistem NLC : - Organoleptis
Pembuatan sistem SLN-NLC dengan lipid 10% Pembuatan Kurva Baku APMS :
Dalam larutan dapar asetat pH 4,2 ± 0,2 dan larutan dapar fosfat pH 7,2 ± 0,05
4.3.1Analisis kualitatif bahan penelitian
Pemeriksaan kualitatif bahan penelitian meliputi APMS, setil alkohol, dan asam oleat. Pemeriksaan dilakukan berdasarkan sertifikat analisis srta pemeriksaan berikut:
1. Organoleptis
Pemeriksaan organoleptis dilakukan secara visual meliputi pemeriksaan bentuk, warna, dan bau. Hasil yang diperoleh kemudian dibandingkan dengan sertifikat analisis.
2. Spektra serapan inframerah
Pemeriksaan ini dilakukan dengan menggunakan teknik pellet KBr pada panjang gelombang (λ) 400-4000 cm-1. Sebanyak 1 mg zat digerus dengan 100 mg serbuk KBr kering kemudian ditekan/dikompresi dengan penekan hidrolik yang dilengkapi dengan alat penarik uap air agar diperoleh lempeng tipis yang ditembus cahaya. Lempeng dipindai pada panjang gelombang 400-4000 cm-1. Spektra inframerah yang diperoleh dari sampel dibandingkan dengan spektra inframerah dari pustaka (Depkes RI, 1995).
3. Pemeriksaan suhu lebur
Penentuan suhu lebur dilakukan dengan alat Differetial Thermal Analysis (DTA). Bahan ditimbang 3-5 mg dan dimasukkan ke dalam sample pan, kemudian ditutup. Sample pan kemudian dimasukkan dalam sample holder. Sebagai sample pan digunakan
4.3.2 Pembuatan kurva baku APMS dalam larutan dapar asetat pH 4,2 ± 0,2
a. Pembuatan larutan dapar asetat pH 4,2 ± 0,2
Untuk penentuan efisiensi penjebakan digunakan larutan dapar asetat pH 4,2 ± 0,2 yang dibuat dengan menambahkan 368 mL asam asetat 0,2 M (diperoleh dengan mengencerkan 11,5 mL asam asetat glasial dalam 1 L aqua bebas CO2) ke dalam 132 mL Na asetat 0,2 M (diperoleh dengan melarutkan 16,4 gram Na asetat anhidrat dalam 1 L aqua bebas CO2) kemudian ditambahkan 5,8 gram NaCl dan selanjutnya ditambahkan aquadest hingga volum 1 L.
b. Pembuatan larutan baku induk APMS 100 ppm
Ditimbang dengan seksama 10,0 mg APMS, dilarutkan dalam 10,0 mL etanol kemudian ditambahkan larutan dapar asetat pH 4,2 ± 0,2 sampai volume 100,0 mL pada labu ukur dan dikocok sampai homogen.
c. Pembuatan larutan baku kerja APMS
Tabel IV. 1 Larutan Baku Kerja APMS dalam dapar asetat pH 4,2 ± 0,2 dengan Dapar Asetat pH 4,2 ±
0,2
d. Penentuan panjang gelombang maksimal
Panjang gelombang maksimum ditentukan dengan menggunakan larutan baku kerja APMS konsentrasi 2,0 dan 12,0 μg/mL. nilai absorbsi tiap-tiap konsentrasi diamati dengan spektrofotomtri UV-VIS pada rentang panjang gelombang 200-400 nm. Sebagai blanko digunakan dapar asetat pH 4,2 ± 0,2. Panjang gelombang maksimum adalah panjang gelombang dengan serapan maksimum.
e. Penentuan persamaan kurva baku
Kurva baku dibuat dengan melakukan pengukuran larutan baku kerja pada panjang gelombang maksimum terhadap blanko yang berisi media solusi. Dari hasil pengamatan dibuat kurva serapan vs kadar, kemudian dibuat perssamaan regresi y= bx + a (kadar sebagai aksis dan serapan sebagai ordinat). Linieritas ditunjukkan dengan harga r, dikatakan linier bila harga r yang diperolah lebih besar dari nilai r tabel.
4.3.3Pembuatan kurva baku APMS dalam larutan dapar fosfat a. Pembuatan larutan dapar fosfat pH 7,4 ± 0,05
(diperoleh dengan melarutkan 27,589 gram NaH2PO4 dalam 1 L aqua bebas CO2) ke dalam 450,0 mL NaH2PO4 0,1 M (diperoleh dengan melarutkan 14,196 NaH2PO4 dalam 1 L aqua bebas CO2) dan ditambahkan aquadest hingga volume 1 L.
b. Pembuatan larutan baku induk APMS 100 ppm
Ditimbang dengan seksama 10,0 mg APMS, dilarutkan dalam 10,0 mL etanol kemudian ditambahkan larutan dapar fosfat pH 7,2 ± 0,05 sampai volume 100,0 mL pada labu ukur dan dikocok sampai homogen.
c. Pembuatan larutan baku kerja APMS
Dibuat larutan baku kerja APMS melalui pengenceran larutan baku induk APMS dengan larutan dapat fosfat pH 7,2 ± 0,05 sehingga diperoleh larutan baku kerja dengan konsentrasi 0,5; 1,0; 2,0; 4,0; 6,0; 8,0; 10; 12,0; 15,0; 20,0 dn 30,0 μg/mL. Larutan ini kemudian digunakan untuk menentukan panjang gelombang maksimal APMS dan membuat kurva baku. Digunakan larutan blanko dapar fosfat pH 7,2 ± 0,05.
Tabel IV. 2 Larutan Baku Kerja APMS dalam Dapar Fosfat pH 7,2 ± 0,05 Kadar APMS dengan Dapar Asetat pH 4,2 ±
d. Penetuan panjang gelombang maksimum
Panjang gelombang maksimum ditentukan dengan menggunakan larutan baku kerja APMS konsentrasi 2,0 dan 12,0 μg/mL. nilai absorbsi tiap-tiap konsentrasi diamati dengan spektrofotomtri UV-VIS pada rentang panjang gelombang 200-400 nm. Sebagai blanko digunakan dapar fosfat pH 7,2 ± 0,05. Panjang gelombang maksimum adalah panjang gelombang dengan serapan maksimum.
e. Penentuan persamaan kurva baku
Kurva baku dibuat dengan melakukan pengukuran larutan baku kerja pada panjang gelombang maksimum terhadap blanko yang berisi media solusi. Dari hasil pengamatan dibuat kurva serapan vs kadar, kemudian dibuat perssamaan regresi y= bx + a (kadar sebagai aksis dan serapan sebagai ordinat). Linieritas ditunjukkan dengan harga r, dikatakan linier bila harga r yang diperolah lebih besar dari nilai r tabel.
4.3.4Pembuatan NLC
a. Formulasi sistem NLC
Tabel IV. 3 Formulasi Sistem NLC
b. Cara pembuatan NLC
NLC-APMS dibuat dengan melebur lipid pada suhu 60ºC menggunakan hot plate dalam gelas beker, kemudian ditambahkan APMS sambil diaduk perlahan dengan menggoyang-goyangkan beker hingga APMS larut. Lalu ditambahkan tween 80 panas, kemudian diaduk dengan Ultra-Turax High Shear Homogenizer dengan kecepatan 3200 rpm selama 2 menit pada suhu 60 ± 0,5ºC. Setelah ditambahkan propilenglikol panas dan diaduk lagi dengan kecepatan dan waktu yang sama, lalu ditambahkan dapar asetat pH 4,2 ± 0,2 panas hingga volum 20,0 mL. setelah itu dilakukan High Shear Homogenization selama 8 menit dengan kecepatan 24000 rpm. Tahap selanjutnya adalah tahap pendinginan yang dilakukan dengan cara memindahkan emulsi tersebut dari High Shear Homogenizer ke aats hot plate, kemudian diaduk menggunakan
Gambar 4. 2 Skema Pembuatan NLC dengan Metode High Shear Homogenization
Setil Alkohol + Asam Oleat
Lelehkan pada suhu 60ºC di atas
hot plate
+ APMS (asam p-Metoksi sinamat)
Aduk dengan Ultra-Turax Homogenizer 3400 rpm selama 2’
dengan suhu 90 ± 0,5 ºC)
+ Propilenglikol panas (70 ± 0,5 ºC)
Aduk dengan Ultra-Turax Homogenizer 3400 rpm selama 2’
dengan suhu 70 ± 0,5 ºC)
Fase lipid + Dapar asetat panas pH 4,2 ± 0,2 ad 40,0 mL
High Shear Homogenization selama 8’ dengan kecepatan 24000 rpm
Aduk menggunakan magnetic stirrer 500 rpm hingga
mencapai suhu kamar
Panaskan pada suhu 70 ºC di atas hot plate
Dapar asetat pH 4,2 ± 0,2
+ Tween 80 panas (70 ± 0,5 ºC)
Pre-emulsi
4.3.5 Uji homogenitas dan perolehan kembali APMS dalam sistem SLN dan NLC
Uji homogenitas dan perolehan kembali dilakukan dengan menimbang 50,0 mg sediaan SLN atau NLC APMS pada gelas beker, kemudian ditambahkan 1 mL etanol dan ±5 mL dapar asetat. Campuran tersebut kemudian disonikasi selama 30 menit untuk merusak sistem SLN dan NLC sehingga baik APMS yang terjebak dalam matrik maupun yang berada pada fase air dapat terlarut. Setelah disonikasi, ditambahkan dapar asetat pH 4,2 ± 0,2 ad tepat tanda dalam labu ukur 25,0 mL. larutan disaring menggunakan kertas saring, kemudian dpipet 5,0 mL dan diencerkan kembali ad 25,0 mL dalam labu ukur 25,0 mL. hasil pengenceran disaring menggunakan milipore. Larutan yang telah disaring kemudian diukur serapannya dengan spektrofotometer pada panjang gelombang 200-400 nm. Serapan yang diperoleh dikonversikan menjadi kadar dengan memasukkan ke dalam persamaan garis regresi yang telah diperoleh dalam larutan dapar asetat pH 4,2 ± 0,2. Dilakukan tiga kali repliasi untuk setiap sediaan kemudian dihitung nilai simpangan baku dan % KV nya.
4.3.6 Uji karakteristik NLC
1. Pemeriksaan organoleptis NLC
Pemeriksaan organoleptis dilakukan secara visual meliputi pemeriksaan warna, bau, dan konsistensi SLN. 2. Pemeriksaan ukuran NLC
dilakukan pengamatan pada sudut 165º dan suhu 25ºC. Data yang dihasilkan merupakan ukuran partikel yang dihitung dari fluktuasi rata-rata intensitas hamburan cahaya.
3. Penentuan pH menggunakan magnetic stirrer sampai homogen. Kemudian elektroda dimasukkan ke dalam NLC yang telah diencerkan, terakhir amati dan catat angka yang ditunjukkan oleh pH meter.
4. Penentuan viskositas
Penentuan viskositas dilakukan untuk melihat kekentalan NLC yang dihasilkan akibat pengaruh penambahan bahan lain seperti surfaktan dan akibat pengaruh metode pembuatan. Pengukuran viskositas dilakukan menggunakan alat viscometer Brookfiled Cone and Plate
dengan kecepatan putar 20 rpm. sejumlah sampel dimasukkan ke dalam gelas kemudian dicelupi rotor yang sesuai. Alat dijalankan dan amati angka yang tertera pada skala.
5. Uji efisiensi penjebakan
1000 rpm. Supernatant diambil dan dianalisis dengan spektrofotometer untuk mengetahui APMS yang tidak terjebak. Selanjutnya kadar APMS yang tidak terjebak dalam sistem NLC (Cf) dihitung dengan persamaan kurva baku. Jumlah bahan aktif yang terjebak dalam NLC (DE = Drug Entrapment) dihitung dengan rumus :
(%) = − 100%
Ct adalah konsentrasi awal APMS yang digunakan dalam membuat suspensi. Selanjutnya dihitung rata-rata dan harga simpangan baku efisiensi penjebakan APMS dalam sistem NLC.
4.3.7 Uji pelepasan APMS dari sistem NLC a. Pembuatan media disolusi
Media disolusi yang digunakan adalah dapar fosfat pH 7,4 ± 0,05. Cara pembuatan dapar fosfat adalah dengan menambahkan 50,0 mL NaH2PO4 0,2 M (diperoleh dengan melarutkan 27,589 gram NaH2PO4 dalam 1 L aqua bebas CO2) ke dalam 450,0 mL NaH2PO4 0,1 M (diperoleh dengan melarutkan 14,196 NaH2PO4 dalam 1 L aqua bebas CO2) dan ditambahkan aquadest hingga volume 1 L.
b. Penyiapan membran difusi
dengan aquadest satu malam (± 12 jam). Sesaat sebelum digunakan, membran ditiriskan sampai tidak ada air yang menempel.
c. Perangkat alat uji pelepasan
Alat dan perlengkapan yang digunakan dalam laju pelepasan APMS dari sistem NLC adalah rangkaian alat uji disolusi Hanson-Research SR-6 yang dilengkapi dengan sel difusi serta pengaduk berbentuk paddle.
Sel difusi terbuat dari bahan stailess steel berbentuk silinder pipih. Tempat penampung sampel mempunyai garis tengah 2,9 cm dengan tebal 0,4 cm. sebagai pengaman untuk mencegah kebocoran, sel difusi dilengkapi dengan karet penyekat berbentuk ring sebagai penghubung antara tempat sampel dengan penghubungnya.
d. Penyiapan sel difusi
Gelas arloji dan sudip ditimbang dalam kondisi kosong kemudian NLC-APMS ditimbang ± 2 gram. Selanjutnya sel difusi diisi dengan NLC-APMS dan permukaannya diratakan dengan sudip. Menimbang kembali gelas arloji dan sudip beserta sisa NLC-APMS, kemudian dihitung jumlah NLC-APMS yang masuk pada sel difusi. Diatasnya dipasang ring penyekat dari karet unutk mencegah kebocoran, lalu diklem dengan lempengan sel yang lain dnegan rapat.
pengambilan sampel diganti dengan larutan dapar fosfat pH 7,4 ± 0,05 dengan jumlah dan suhu yang sama. Cuplikan diamati serapannya menggunakan spektrofotometer UV-VIS pada panjang gelombang maksimum APMS sesuai penentuan panjang gelombang maksimum APMS dalam dapar fosfat. Konsentrasi APMS dalam cuplikan dihitung dengan menggunakan persamaan regresi kurva baku APMS dalam dapar fosfat pH 7,4 ± 0,05. Untuk memperhitungkan pengenceran 5,0 mL media pelepasan, kadar terukur dikoreksi dengan persamaan Wurster :
= ′ + ( )
Keterangan :
Cn : Kadar sebenarnya setelah dikoreksi
C’n : Kadar terbaca (hasil perhitungan dari nilai serapan sample yang tebaca pada spektrofotometer dalam ppm)
Cs : kadar terbaca dari sampel sebelumnya Vs : Volume sampel
Vm : Volume media
f. Penentuan jumlah kumulatif APMS yang terlepas dari sistem SLN dan NLC
Penentuan jumlah kumulatif APMS yang terlepas dari sistem NLC per satuan luas membran (μg/cm2) tiap waktu diperoleh dari konsentrasi (μg/mL) yang diperoleh setiap waktu ditambah koreksi Wurster kemudian dikalikan dengan jumlah media (500 mL) dan selanjutnya dibagi luas permukaan membran.
h. Penentuan kecepatan pelepasan (fluks) APMS dari sistem SLN dan NLC
Dari gambar profil pelepasan APMS yang dihasilkan, ditentukan keadaan steady state terlebih dahulu, selanjutnya dibuat persamaan regresi pada daerah steady state tersebut. Berdasarkan hukum difusi Higuchi,
slope dari persamaan regresi tersebut merupakan kecepatan pelepasan (fluks) APMS dari sistem NLC. Kondisi steady state adalah kondisi dimana membran berada dalam keadaan jenuh atau proses difusi sudah berjalan konstan.
4.4 Analisis Data
4.4.1 Perhitungan parameter pelapasan APMS dari sistem NLC a. Penentuan Jumlah Kumulatif APMS yang Terlepas dari Sistem
NLC
Penentuan jumlah kumulatif APMS yang terlepas per satuan luas membran tiap waktu (μg/cm2), dihitung dari konsentrasi yang diperoleh setiap waktu (μg/mL) ditambah faktor koreksi Wurster kemudian dikalikan dengan jumlah media (500 mL) dan selanjutnya dibagi luas permukaan membran. Langkah berikutnya dibuat kurva hubungan antara jumlah kumulatif APMS yang terlepas (μg/cm2) terhadap akar waktu (menit1/2).
b. Penentuan profil pelepasan APMS dari sistem NLC
Profil pelepasan APMS pada suhu 32ºC ± 0,5 ºC merupakan rerata hubungan antara jumlah APMS yang terlepas (μg/cm2) vs akar waktu (menit1/2). Data diperoleh dari replikasi tiga kali pengamatan.
Dari kurva yang dihasilkan antara jumlah kumulatif APMS yang terlepas (μg/cm2) vs akar waktu (menit1/2) jika mengikuti persamaan linier maka fluks ditentukan dengan menghitung slope dari persamaan garis linier. Namun, jika kurva yang dihasilkan mengikuti persamaan non linier, maka fluks ditentukan dengan menghitung area dibawah kurva pelepasan APMS. Area dibawah kurva dihitung menggunakan rumus trapesium.
4.4.2 Analisis statistika
Harga laju pelepasan (Fluks) APMS dianalisis dengan statistika menggunakanmetode analisis varian (ANOVA) satu arah untuk mengetahui apakah ada perbedaan fluks yang bermakna antara sistem SLN dan NLC. Dari hasil analisis tersebut diperoleh nilai harga F hitung yang kemudian dibandingkan dengan F table dan dilakukan uji HSD
BAB V HASIL PENELITIAN
5.1 Pemeriksaan Kualitatif Bahan Penelitian
Untuk memastikan bahwa bahan-bahan pembentuk sistem SLN maupun NLC memiliki kemurnian yang sesuai dengan pustaka, maka dilakukan pemeriksaan kualitatif APMS, setil alkohol, dan asam oleat untuk kemudian dibandingkan dengan pustaka. Uji kualitatif tersebut terdiri dari organoleptis, profil spektra inframerah, dan termogram DTA.
5.1.1 Pemeriksaan kualitatif APMS
Hasil pemeriksaan spektra IR dan suhu lebur APMS dapat dilihat pada gambar 5.1, gambar 5.2 dan 5.3. Berdasarkan hasil pemeriksaan kualitatif APMS yang dapat dilihat pada table V.1, spektra APMS dibandingkan dengan spektra IR APMS dari pustaka, terlihat bahwa APMS yang digunakan dalam penelitian memberikan serapan beberapa gugus pada bilangan gelombang yang sesuai dengan rentang dalam pustaka, begitu juga hasil pemeriksaan suhu lebur menggunakan DTA yang sesuai dengan suhu lebur dalam pustaka.
Gambar 5. 2 Spektra IR APMS berdasarkan pustaka (www.sigmaaldrich.com)
Gambar 5. 3 Termogram DTA APMS
Tabel V. 1 Hasil pemeriksaan kualitatif sampel APMS
Pemeriksaan Pengamatan Pustaka
Organoleptis Serbuk berwarna putih Serbuk berwarna putiha)
Suhu Lebur 174,1oC 173 – 175oCb)
Bilangan gelombang (cm-1)
:
a) Pustaka berdasarkan sertifikat analisis yang didapatkan b) Chemicalland21.com
5.1.2 Pemeriksaan kualitatif setil alkohol
Hasil pemeriksaan spektra IR setil alkohol dan spektra IR berdasarkan pustaka dapat dilihat pada gambar 5.4, gambar 5.5, dan gambar 5.6. Berdasarkan kualitatif setil alkohol yang dapat dilihat pada table V.2, terlihat bahwa setil alkohol yang digunakan dalam penelitian memberikan serapan beberapa gugus pada bilangan gelombang yang sesuai dengan rentang dalam pustaka, namun suhu lebur setil alkohol berbeda 0,8 oC dari rentang yang terdapat dalam pustaka.
Tabel V. 2 Hasil pemeriksaan kualitatif sampel setil alkohol Pemeriksaan Pengamatan Pustaka (Rowe et al., 2009) Organoleptis Butiran berwarna putih Butiran berwarna putih Suhu Lebur 53,8oC 47-53 oC
Bilangan gelombang (cm-1):
1640-1820
Gambar 5. 5 Spektra IR setil alkohol berdasarkan pustaka (sdbs.db.aist.go.jp)
Gambar 5. 6 Termogram DTA setil alkohol
5.1.3 Pemeriksaan kualitatif asam oleat
Tabel V. 3 Hasil pemeriksaan kualitatif sampel asam oleat
Pemeriksaan Pengamatan Pustaka
Organoleptis Cairan kental berwarna kuning kecoklatan Cair berwarna kekuningan coklat. Identifikasi spektra IR
Gugus : -C=O -C-O -C=C alkena -C=C aromatik O-H karboksilat
Bilangan gelombang (cm-1) :
1737,18 1171,32 1640,30 1473,18 2917,20
Bilangan gelombang (cm-1)a):
1640-1820 1110-1300 1600-1650 1475-1600 2400 – 3400 Keterangan :
a) Fessenden & Fessenden, 1999
Gambar 5. 7 Hasil pemeriksaan spektra IR asam oleat
5.2 Penentuan kurva baku APMS
Penentuan kurva baku APMS dilakukan dalam dua larutan yaitu larutan dapar asetat pH 4,2 ± 0,2 sebagai fase air pada sistem SLN mapun NLC dan larutan dapar fosfat pH 7,4 ± 0,05 sebagai media uji pelepasan.
5.2.1 Kurva baku dalam larutan dapar asetat pH 4,2 ± 0,2
Kurva baku APMS dalam larutan dapar asetat pH 4,2 ± 0,2 ini digunakan untuk perhitungan kadar dalam uji homogenitas dan efisiensi penjebakan sistem SLN dan NLC. Tahapan penentuan kurva baku APMS dalam dapar asetat pH 4,2 ± 0,2 µ= 0,998 adalah dengan menentukan panjang gelombang maksimum APMS dan kemudian penentuan kurva baku APMS.
5.2.1.1 Hasil penentuan panjang gelombang maksimum dalam dapar asetat pH 4,2 ± 0,2
Panjang gelombang maksimum APMS dalam dapar asetat pH 4,2 ± 0,2 ditentukan dengan melakukan scanning seperti pada gambar 5.9 terhadap larutan baku kerja APMS pada kadar 1 ppm dan 12 ppm. Berdasarkan hasil penentuan panjang gelombang maksimum APMS diperoleh panjang gelombang maksimum APMS dalam dapar asetat 304,0 nm.
5.2.1.2 Hasil Penentuan kurva baku APMS dalam larutan dapar asetat pH 4.2 ± 0.2
tiga kali replikasi diperoleh persamaan regresi y= 0.1348x - 8.429 x10-3 dengan koefisien korelasi 0.9998.
Gambar 5. 9 Profil serapan larutan baku kerja APMS pada larutan dapar asetat pH 4,2 ± 0,2
Tabel V. 4 Nilai serapan APMS pada berbagai kadar dalam larutan dapar asetat pH 4.2 ± 0.2 pada panjang gelombang maksimum 304,0 nm
Kadar (ppm) Serapan
Gambar 5. 10 Kurva baku serapan APMS dalam larutan dapar asetat pH 4.2 ± 0.2
0.000 2.000 4.000 6.000 8.000 10.000 12.000 14.000
se
ra
pa
n
5.2.2 Kurva baku dalam larutan dapar fosfat pH 7.4 ± 0.05 Tahapan penentuan kurva baku APMS dalam dapar fosfat pH 7,4 ± 0,05 adalah dengan menentukan panjang gelombang maksimum APMS dan kemudian penentuan kurva baku APMS.
5.1 Hasil penentuan panjang gelombang maksimum
Panjang gelombang maksimum APMS dalam dapar asetat ditentukan dengan melakukan scanning terhadap larutan baku kerja APMS pada kadar 0,5 ppm dan 15 ppm yang berbeda pada panjang gelombang 200-400 nm menggunakan spektrofotometer UV-Vis.
Berdasarkan hasil penentuan panjang gelombang maksimum APMS diperoleh panjang gelombang maksimum APMS dalam dapar fosfat 285,0 nm seperti yang terlihat pada gambar 5.11
Gambar 5. 11 Profil serapan larutan baku kerja APMS dalam larutan dapar fosfat pH 7.4 ± 0.05
APMS 15ppm
5.2 Hasil penentuan kurva baku APMS dalam larutan dapar fosfat pH 7.4 ± 0.05
Kurva baku APMS diperoleh dari hasil pengukuran serapan larutan baku kerja APMS dalam larutan dapar fosfat pH 7.4 ± 0.05 dengan kadar 0,5; 1,0; 2,0; 4,0; 6,0; 8,0; 10,0; 12,0; 5,0; 20,0; 30,0 ppm pada panjang gelombang maksimum APMS dalam larutan dapar fosfat (285,0 nm). Berdasarkan hasil perhitungan gabungan dari tiga kali replikasi diperoleh persamaan regresi y = 0.11610x + 0.0285 dengan koefisien korelasi 0.99895.
Tabel V. 5 Nilai serapan APMS pada berbagai kadar dalam larutan dapar fosfat pH 7.4 ± 0.05 pada panjang gelombang maksimum 285,0 nm
Kadar (ppm) Serapan
5.3 Pemeriksaan pengaruh bahan tambahan terhadap serapan APMS
Pemeriksaan pengaruh bahan tambahan terhadap serapan APMS dilakukan dengan scanning panjang gelombang dapar asetat pH 4,2 ± 0,2, larutan dapar fosfat pH 7,4 ± 0,05, APMS dalam dapar asetat pH 4,2 ± 0,2, APMS dalam larutan dapar fosfat pH 7,4 ± 0,05, SLN base, NLC base, SLN APMS, serta NLC APMS.
Gambar 5. 13 Serapan larutan dapar asetat pH 4,2 ± 0,2, APMS, SLN base, NLC base, SLN APMS, dan NLC APMS dalam larutan dapar asetat
pH 4,2 ± 0,2
Gambar 5. 14 Serapan larutan dapar fosfat pH 7,4 ± 0,05, APMS, SLN base, NLC base, SLN APMS, dan NLC APMS dalam larutan dapar fosfat
Berdasarkan hasil scanning panjang gelombang, diketahui bahwa bahan-bahan yang digunakan pada sistem SLN maupun NLC tidak mempengaruhi serapan APMS pada panjang gelombang maksimalnya.
5.4 Hasil uji homogenitas dan peroleh kembali APMS dalam sistem SLN maupun NLC
Tabel V. 6 Hasil perolehan kembali APMS dalam sistem SLN-NLC dengan lipid setil alkohol:asam oleat
Formula Rata-rata Perolehan
kembali± SB (%) % KV
(10:0)-APMS 114,48 ± 1,16 1,02
(9,5:5)-APMS 105,94 ± 1,48 1,40
(9:1)-APMS 104, 38 ± 0,18 0,17
(8,5:1,5)-APMS 102,46 ± 1,25 1,22
Dari keempat formula, berdasarkan table V.6 diatas uji homogenitas APMS berada pada rentang 102,46-114,48% kadar yang memenuhi persyaratan penetapan kadar bahan aktif dalam sediaan jadi yaitu 80-120% (ICH Harmonised Tripartite Guidline, 2005) dan memiliki nilai %KV 0,18-1,48% yang menunjukkan proses pembuatan sistem SLN maupun NLC memiliki presisi yang baik.
5.5 Penentuan Karakteristik Sistem SLN-NLC APMS
Dilakukan penentuan karakteristik SLN-APMS maupun NLC-APMS berupa orgnaoleptis, ukuran partikel, pH, viskositas, serta efisiensi penjebakan.