6 BAB II
TINJAUAN PUSTAKA
2.1 Betametason
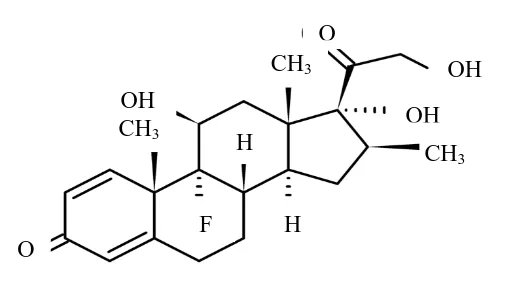
Betametason mengandung tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket. Menurut Ditjen POM, (1995) betametason mempunyai struktur dengan rumus bangun dan rumus molekul seperti yang tersebut dibawah ini :
Gambar 2.1 Rumus struktur betametason (Ditjen POM, 1995).
Rumus molekul dalam kloroform; larut dalam etanol; sukar larut dalam eter dan benzen. (Ditjen POM, 1995)
: C22H29FO5
: 392,47
: 9-Fluoro-11 β, 17, 21- trihidroksi -16 β-metilpregna-1,4-diena 3,20-dion
: Serbuk, putih sampai praktis putih; tidak berbau
: Praktis tidak larut dalam air, mudah larut dalam aceton dan dalam kloroform; larut dalam etanol; sukar larut dalam eter dan benzen
7
Indikasi : Alergi dan peradangan lokal
Efek samping : Atropi lokal, gatal-gatal, hipopigmentasi, dermatitis perioral dan alergi, serta infeksi sekunder (Sartono,1996).
Semua kortikosteroid secara oral di absorpsi dengan langsung efeknya baru tampak setelah 4 - 6 jam, maka untuk efek cepat hendaknya digunakan injeksi dari derivat yang mudah larut. Masa paruhnya berkisar antara 1,5 dan 5 jam, tetapi bertahan jauh lebih lama. Misalnya: deksametason dan betametason (Tan dan Rahardja, 2007).
2.2 Deksklorfeniramin maleat
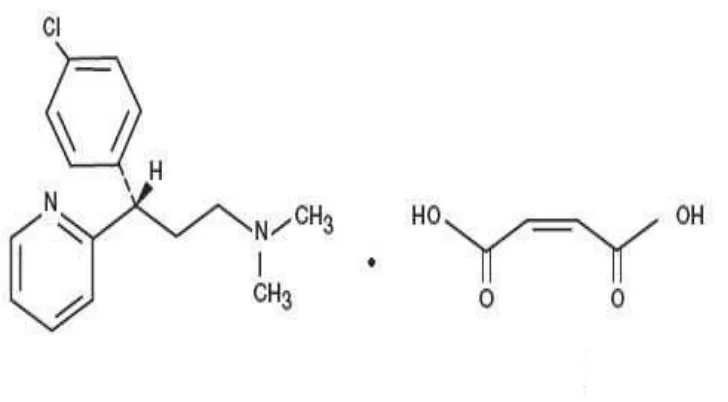
Deksklorfeniramin maleat mengandung tidak kurang dari 90,0% dan tidak lebih dari 110,0% dari jumlah yang tertera pada etiket. Menurut Ditjen POM, 1995 deksklorfeniramin maleat mempunyai struktur dengan rumus bangun dan rumus molekul seperti yang tersebut dibawah ini :
8 Rumus molekul : C16H19ClN2. C4H4O6
Berat molekul : 390,87
Nama kimia : (+)-2-[p-Kloro α-[(Dimetilamino)etil]benzil] piridina maleat
Pemerian : Serbuk hablur putih tidak berbau
Susut pengeringan : Lakukan pengeringan pada suhu 65oC selama 4 jam sebelum digunakan.
Kelarutan : Mudah larut dalam air, larut dalam etanol dan dalam kloroform, sukar larut dalam benzen dan dalam eter Indikasi : Antihistamin
Efek samping : Vertigo, tinitus, lelah, penat, inkoordinasi, kabur, diplopia, euforia, gelisah, tremor, mulut kering, disuria, palpitasi, hipotensi, sakit kepala, rasa berat dan lemah pada tangan (Tan dan Rahardja, 2007).
Deksklorfeniramin maleat setelah pemberian oral atau parenteral, AH1 diabsorpsi secara baik. Efeknya timbul 15-30 menit setelah pemberian oral dan maksimal 1-2 jam. Lama kerja AH1 setelah pemberian dosis tunggal kira-kira 4-6 jam. Kadar tertinggi terdapat pada paru-paru, sedangkan pada limpa, ginjal, otak, otot dan kulit kadarnya lebih rendah (Tan dan Rahardja, 2007).
2.3 Spektrofotometri Ultraviolet-Visibel (UV-Vis)
9
menghasilkan sinar dari spektrum dengan panjang gelombang tertentu dan fotometer sebagai alat pengukur intensitas cahaya yang ditransmisikan atau yang diabsorpsi (Gandjar dan Rohman, 2007). Pada spektrofotometer, panjang gelombang yang benar-benar terseleksi dapat diperoleh dengan bantuan alat pengurai cahaya seperti prima. Suatu spektrofotometer tersusun dari spektrum tampak yang kontinu, monokromator, sel pengabsorpsi untuk larutan sampel atau blangko dan suatu alat untuk mengukur perbedaan absorpsi antara sampel dan pembanding (Khopkar, 1985).
2.3.1 Penyerapan Radiasi
Jika suatu molekul sederhana dikenakan radiasi ultraviolet maka molekul tersebut akan menyerap radiasi ultraviolet. Interaksi antara molekul dengan radiasi ultraviolet ini akan meningkatkan energi dari tingkat dasar ke tingkat tereksitasi. Apabila pada molekul yang sederhana tadi hanya terjadi transisi elektronik pada satu macam gugus yang terdapat pada molekul, maka hanya akan terjadi satu absorpsi yang merupakan garis spektrum. Terjadinya dua atau lebih pita spektrum diberikan oleh molekul dengan struktur yang lebih kompleks karena terjadi beberapa transisi sehingga mempunyai lebih dari satu panjang gelombang (Gandjar dan Rohman, 2007).
Sebagai contoh, molekul organik sederhana yang mempunyai dua jenis ikatan karbon-karbon seperti pada etilen. Ikatan π lebih lemah dari ikatan σ dan akibatnya elektron π lebih tinggi energinya dari elektron σ (Munson, 1984).
10
merupakan kromofor yang dapat menyerap radiasi ultraviolet. Salah satu kromofor yang paling sederhana adalah benzen (Watson, 2005).
Gugus fungsi seperti –OH, -O, -NH2, dan –OCH3 yang memberikan
transisi n → π* disebut gugus auksokrom. Gugus ini adalah gugus yang tidak dapat menyerap radiasi ultraviolet-sinar tampak, tetapi apabila gugus ini terikat pada gugus kromofor mengakibatkan pergeseran panjang gelombang ke arah yang lebih besar (efek batokromik atau pergeseran merah) dan disertai peningkatan intensitas (efek hiperkromik) (Gandjar dan Rohman, 2007).
2.3.2 Hukum Lambert-Beer
Menurut Gandjar dan Rohman (2007) Hukum Lambert, serapan berbanding lurus terhadap ketebalan sel yang disinari. Sedangkan menurut Beer, serapan berbanding lurus dengan konsentrasi. Kedua pernyataan ini dapat dijadikan satu dalam Hukum Lambert-Beer, sehingga diperoleh bahwa serapan berbanding lurus terhadap konsentrasi dan ketebalan sel, yang dapat ditulis dengan persamaan :
A = a.b.c (g/liter) atau A = ε. b. c (mol/liter) atau A = A1
1.b.c (g/100 ml)
Dimana: A = serapan a = absorptivitas b = ketebalan sel c = konsentrasi
11
Menurut Denney dan Sinclair (1991) hukum Lambert-Beer terdapat beberapa pembatasan yaitu:
1. Larutan yang menyerap cahaya adalah campuran yang homogen. 2. Menggunakan sinar monokromatis.
3. Rendahnya konsentrasi dari senyawa yang menyerap cahaya.
Absorbansi yang terbaca pada spektrofotometer hendaknya antara 0,2 sampai 0,6. Anjuran ini berdasarkan anggapan bahwa pada kisaran nilai absorbansi tersebut kesalahan fotometrik yang terjadi adalah paling minimal (Gandjar dan Rohman, 2007).
Parameter kekuatan energi radiasi yang diabsorpsi oleh molekul adalah absorbansi (A) yang dalam batas konsentrasi tertentu nilainya sebanding dengan banyaknya molekul yang mengabsorpsi radiasi. Senyawa yang tidak mengabsorpsi radiasi ultraviolet - sinar tampak dapat juga ditentukan dengan spektrofotometri ultraviolet - sinar tampak, apabila ada reaksi kimia yang dapat mengubahnya menjadi kromofor atau dapat disambungkan dengan suatu pereaksi kromofor (Gandjar dan Rohman, 2007).
2.3.3 Kegunaan Spektrofotometri Ultraviolet - Visibel (UV-Vis)
Kegunaan spektrofotometri ultraviolet dalam analisis kualitatif sangat terbatas karena rentang daerah radiasi yang relatif sempit hanya dapat mengakomodasi sedikit sekali puncak absorpsi maksimum dan minimum, karena itu identifikasi senyawa yang tidak diketahui tidak memungkinkan untuk dilakukan (Satiadarma, dkk., 2004).
12
(Cairns, 2008), dimana menurut Holme dan Peck (1983) konsentrasi sampel dalam senyawa dihitung dengan rumus sebagai berikut:
Ct
Cs At
As =
Keterangan: As = Absorbansi baku pembanding At = Absorbansi zat dalam sampel Cs = Konsentrasi baku pembanding Ct = Konsentrasi zat dalam sampel
Metode spektrofotometri memiliki beberapa keuntungan antara lain kepekaan yang tinggi, ketelitian yang baik, mudah dilakukan, cepat pengerjaannya dan dapat digunakan untuk menentukan senyawa campuran (Munson, 1984).
Penentuan kadar senyawa organik yang mempunyai struktur kromofor atau mengandung gugus kromofor, serta mengabsorpsi radiasi ultraviolet penggunaanya cukup luas (Satiadarma, dkk., 2004).
2.3.4 Komponen Spektrofotometer Derivatif
Komponen-komponen pada spektrofotometer UV-Vis biasa sama dengan komponen pada spektrofotometer derivatif. Alat spektrofotometer harus dilengkapi dengan peralatan sedemikian rupa untuk dapat menghasilkan spektrum derivatif (Ditjen POM, 1995). Biasanya spektrofotometer telah mempunyai
software untuk mengolah data yang dapat dioperasikan melalui komputer yang
13
Menurut Day dan Underwood (1998), unsur -unsur terpenting suatu spektrofotometer adalah sebagai berikut:
1. Sumber-sumber lampu: lampu deuterium digunakan untuk daerah Ultraviolet pada panjang gelombang dari 190-350 nm, sementara lampu halogen kuarsa atau lampu tungsten digunakan untuk daerah visibel pada panjang gelombang antara 350- 900 nm.
2. Monokromotor: digunakan untuk memperoleh sumber sinar yang monokromatis. Alatnya berupa prisma untuk mengarahkan sinar monokromatis yang diinginkan dari hasil penguraian.
3. Kuvet (sel): digunakan sebagai wadah sampel untuk menaruh cairan ke dalam berkas cahaya spektrofotometer. Kuvet itu haruslah meneruskan energi radiasi dalam daerah spektrum yang diinginkan. Pada pengukuran di daerah sinar tampak, kuvet dapat digunakan, tetapi untuk pengukuran pada daerah ultraviolet kita harus menggunakan sel kuarsa karena gelas tidak tembus cahaya pada daerah ini. Kuvet tampak dan ultraviolet yang khas mempunyai ketebalan 1 cm, namun tersedia kuvet dengan ketebalan yang sangat beraneka, mulai dari ketebalan kurang dari 1 mm sampai 10 cm bahkan lebih.
14 2.4 Spektrofotometri Derivatif
2.4.1 Pengertian Spektrofotometri Derivatif
Spektofotometri derivatif adalah metode spektrofotometri ultraviolet yang mentransformasikan spektrum serapan biasa menjadi spektrum derivatif pertama, kedua atau spektrum derivatif dengan order yang lebih tinggi (Ditjen POM, 1995). Pada spektrofotometri konvensional, spektrum serapan merupakan plot serapan (A) terhadap panjang gelombang (λ). Pada spektrofotometri derivatif, plot serapan terhadap panjang gelombang dimana:
A = f (λ), order nol
dA / dλ = f ′ (λ), order pertama d2A / dλ2 = f ″ (λ), order kedua dan seterusnya (Owen, 1995).
Menurut Talsky (1994) sesuai dengan hukum Lambert-Beer, maka ada hubungan linier antara konsentrasi dengan absorbansi untuk semua orde pada spektrofotometri derivatif adalah:
dA / dλ = �� ( 1%,1��) d� x bc
d²A / dλ² = �²� ( 1%,1��) d�² x bc d A / dλ = �˟� ( 1%,1��)
15
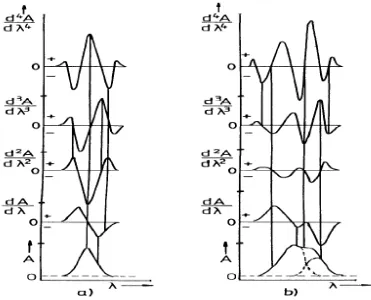
Gambar 3. Spektrum serapan normal (derivat ke-nol) sampai derivat ke-empat (Talsky, 1994). Gambar (a) menunjukkan spektrum serapan normal (satu peak) yang diderivatisasi sampai spektrum derivat ke-empatnya, sedangkan Gambar (b) menunjukkan spektrum yang saling overlapping yang diderivatisasi mulai dari spektrum serapan normal hingga spektrum derivat ke empat (Talsky, 1994).
Konsep derivatif telah diperkenalkan pertama kali pada tahun 1950, dimana terlihat memberikan banyak keuntungan. Aplikasi utama spektrofotometri derivatif ultraviolet - cahaya tampak adalah untuk identifikasi kualitatif dan analisis sampel. Metode spektrofotometri derivatif sangat cocok untuk analisis pita absorpsi yang tumpang tindih (Owen, 1995).
16
Spektrofotometri derivatif yang dikombinasikan dengan teknik zero
crossing atau transformasi Fourier untuk teknik pemrosesan data telah banyak
dikembangkan untuk analisis kuantitatif senyawa aktif pada formulasi obat (Batubara, dkk., 2005).
2.4.2 Metode Spektrofotometri Derivatif
Ada tiga metode spektrofotometri derivatif yang sering digunakan dalam analisa kuantitatif antara lain metode zero crossing, metode peak to peak dan metode multivariate spectrophotometric calibration (Talsky, 1994). Metode
zero-crossing memisahkan campuran biner dari spektrum derivatifnya di panjang
gelombang pada saat satu komponen tidak ada sinyal. Pengukuran zero crossing tiap komponen dalam campuran merupakan fungsi tunggal konsentrasi dari yang lainnya (Nurhidayati, 2007).
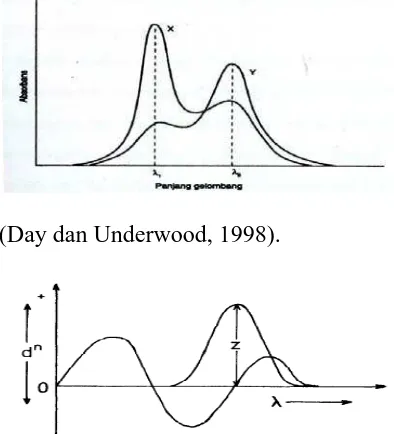
Kurva sederhana aplikasi zero crossing dapat dilihat pada Gambar 2.3.
(Day dan Underwood, 1998).
(Talsky, 1994).
17
Bila campuran analit memiliki panjang gelombang zero-crossing lebih dari satu, maka yang dipilih untuk dijadikan panjang gelombang analisis adalah panjang gelombang zero crossing yang serapan pasangannya dan campurannya persis sama, karena pada panjang gelombang tersebut dapat secara selektif mengukur serapan senyawa pasangannya dan memiliki serapan yang paling besar. Pada serapan yang paling besar, serapannya lebih stabil sehingga kesalahan analisis dapat diperkecil (Nurhidayati, 2007).
Panjang gelombang serapan maksimum suatu senyawa pada spektrum normal akan menjadi panjang gelombang zero crossing pada spektrum derivat
pertama, panjang gelombang tersebut tidak mempunyai serapan atau dA/dλ = 0
(Munson,1984).
Prinsip utama derivatisasi adalah menghilangkan dasar pita-pita serapan luas yang terjadi terhadap perubahan bertahap panjang gelombang. Spektrum derivatif pertama di peroleh dengan memplot misalnya kemiringan sekmen spektrum sebesar 2 nm, dalam spektrum yang kemiringannya 0 pada puncak maksimum dan kemiringannya maksimum pada sekitar separuh dari tinggi puncak (Watson, 2005).
2.4.3 Penggunaan Spektrofotometri Derivatif
18
Spektrofotometri derivatif banyak digunakan untuk zat-zat dalam suatu campuran yang spektrumnya saling mengganggu atau tumpang tindih (overlapping) dan dimana zat-zat tersebut dapat larut dalam pelarut yang sama serta memiliki serapan maksimum pada panjang gelombang yang berdekatan (Mulja dan Suharman, 1995).
2.5 Validasi Metode Analisis
Validasi metode adalah suatu proses yang menunjukkan bahwa prosedur analitik telah sesuai dengan penggunaan yang dikehendaki. Validasi merupakan persyaratan mendasar yang diperlukan untuk menjamin kualitas dan hasil dari semua aplikasi analitik (Ermer dan McB. Miller, 2005). Parameter analisis yang ditentukan pada validasi adalah akurasi, presisi, limit deteksi, limit kuantitasi, kelinieran, dan rentang (Gandjar dan Rohman, 2007).
2.5.1 Akurasi (Kecermatan)
Akurasi adalah kedekatan antara nilai hasil uji yang diperoleh melalui metode analitik dengan nilai sebenarnya. Akurasi dinyatakan dalam persen perolehan kembali (% recovery). Akurasi dapat ditentukan dengan dua metode, yakni spiked – placebo recovery dan standard addition method. Pada spiked –
placebo recovery atau metode simulasi, analit murni ditambahkan (spiked) ke
dalam campuran bahan pembawa sediaan farmasi, lalu campuran tersebut dianalisis dan jumlah analit hasil analisis dibandingkan dengan jumlah analit teoritis yang diharapkan. Jika plasebo tidak memungkinkan untuk disiapkan, maka sejumlah analit yang telah diketahui konsentrasinya dapat ditambahkan langsung ke dalam sediaan farmasi. Metode ini dinamakan standard addition
19 2.5.2 Presisi (Keseksamaan)
Presisi adalah ukuran keterulangan metode analitik, termasuk di antaranya kemampuan instrumen dalam memberikan hasil analitik yang reprodusibel. Berdasarkan rekomendasi ICH (the International Conference on the
Harmonisation), karakteristik presisi dilakukan pada 3 tingkatan, yakni
keterulangan (repeatability), presisi antara (intermediate precision) dan reprodusibilitas (reproducibility). Keterulangan dilakukan dengan cara menganalisis sampel yang sama oleh analis yang sama menggunakan instrumen yang sama dalam periode waktu singkat. Presisi antara dikerjakan oleh analis yang berbeda. Sedangkan reprodusibilitas dikerjakan oleh analis yang berbeda dan di laboratorium yang berbeda (USP 30 NF 25, 2007).
2.5.3 Batas Deteksi dan Batas Kuantitasi
Batas deteksi adalah konsentrasi analit terendah dalam sampel yang masih dapat dideteksi, meskipun tidak selalu dapat dikuantifikasi. Sedangkan batas kuantitasi adalah konsentrasi analit terendah dalam sampel yang dapat ditentukan dengan presisi dan akurasi yang dapat diterima pada kondisi operasional metode yang digunakan (Harmita, 2004).
2.5.4 Linearitas
20
Linieritas dapat diukur dengan melakukan pengukuran tunggal pada konsentrasi yang berbeda-beda. Data yang diperoleh selanjutnya diproses untuk selanjutnya dapat ditentukan nilai kemiringan (slope), intersep dan koefisien korelasinya (Gandjar dan Rohman, 2007).
2.5.6 Rentang